文档内容
(15)晶体结构与性质—高二化学人教版暑假作业本
1.下面有关晶体的叙述中,不正确的是( )
A.氯化钠晶体中,每个 周围距离相等的 共有6个
B.金刚石为空间网状结构,由共价键形成的碳原子环中,最小的环上有6个碳原子
C.氯化铯晶体中,每个 周围紧邻8个
D.干冰晶体中,每个 分子周围紧邻12个 分子
2.下列说法错误的是( )
A.冰中,一个水分子周围有4个紧邻分子
B. 晶体中,一个 周围有6个 紧邻
C.干冰中,一个 分子周围有12个分子紧邻
D. 晶体( )中,一个Fe原子周围有8个Fe原子紧邻
阅读下列材料,完成 题:
苯甲酸乙酯可用于配制香水和食用香精。实验室可以苯甲酸与乙醇为原料制备苯甲酸乙酯:
已知:
物质 乙醇 苯甲酸 乙醚 苯甲酸乙酯
密度/( ) 0.789 1.2659 0.7318 1.0500
沸点/℃ 78.5 249.0 34.5 212.0
相对分子质量 46 122 74 150
3.根据晶体中的晶胞结构,判断下列晶体的化学式中不正确的是( )
A B C EF D XYZ
3
A.A B.B C.C D.D
4.下列说法正确的是( )
A.石墨晶体是一种混合型晶体,兼有共价晶体、分子晶体和金属晶体的特征B.价层电子排布为 的元素位于第四周期第ⅧB族
C.基态Cr原子的价层电子排布式:
D. 晶体中存在离子键,共价键,配位键和氢键等化学键
5.下列关于分子晶体的说法不正确的是( )
A.分子晶体中含有分子 B.固态或熔融态时均能导电
C.分子间以分子间作用力相结合 D.熔、沸点一般比较低
6.下列关于共价晶体和分子晶体的说法中不正确的是( )
A.金刚石、水晶和干冰都属于共价晶体
B.共价晶体中存在共价键,分子晶体中可能存在共价键
C.共价晶体的硬度通常比分子晶体的大
D.有的分子晶体的水溶液能导电
7.金晶体的晶胞为面心立方堆积,如图所示。设金原子的直径为d,设N 为阿伏加德罗常数
A
的值,在立方体的各个面的对角线上,3个金原子彼此两两相切,M表示金的摩尔质量。下
列说法错误的是( )
A.每个金晶胞中含有4个金原子
B.金属键无方向性,金属原子尽可能地采取密堆积
C.一个晶胞的体积是
2M
D.金晶体的密度是
d3N
A
8.氟化钾镁是一种具有优良光学性能的材料,主要应用于激光领域,其立方晶胞结构如图。
表示阿伏加德罗常数的值。下列说法错误的是( )A. 的配位数为12
B.若 位于晶胞的体心,则 位于晶胞的面心
C.每个 位于距其最近且等距的 构成的正四面体空隙中
D.若晶胞参数为anm,则晶体的密度是
9.下列关于晶体的说法正确的组合是( )
①在晶体中只要有阴离子就一定有阳离子
②CaTiO 晶体中(晶胞结构如上图所示)每个Ti4+
3
和12个O2-相紧邻
③金刚石、SiC、NaF、NaCl、H O、H S晶体的熔点依次降低
2 2
④分子晶体中分子间作用力越大,分子越稳定
⑤SiO 晶体中每个硅原子与两个氧原子以共价键相结合
2
⑥离子晶体熔化时晶格能越大,熔点越高
⑦晶体状态能导电的一定是金属晶体
A.①②③④ B.①②⑥⑦ C.②③④⑤ D.
①②③⑥
10.下列说法中,正确的是( )
A.冰融化时,分子中 发生断裂
B.共价晶体中,共价键越强,熔点越高
C.分子晶体中,共价键键能越大,该分子晶体的熔沸点一定越高
D.分子晶体中,分子间作用力越大,对应的物质越稳定
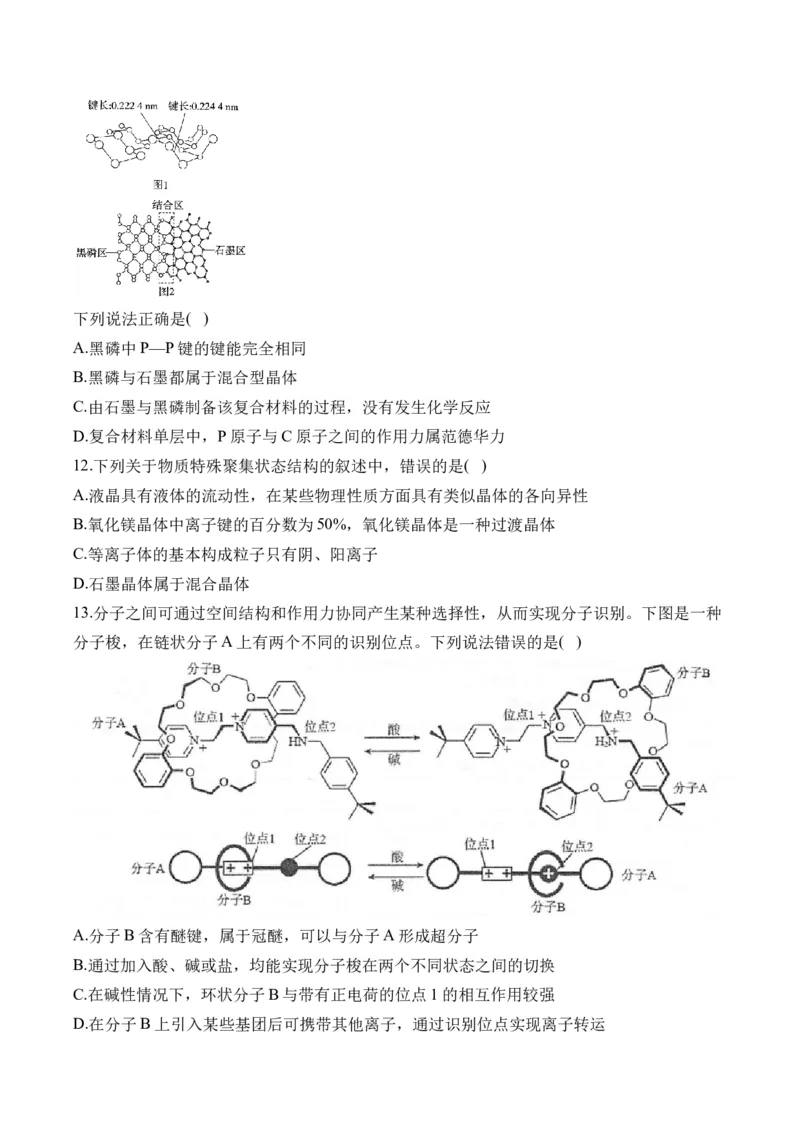
11.磷及其化合物在电池、催化等领域有重要应用。黑磷与石墨类似,也具有层状结构(如图
1)。为大幅度提高锂电池的充电速率,科学家最近研发了黑磷—石墨复合材料,其单层结构
俯视图如图2所示。下列说法正确是( )
A.黑磷中P—P键的键能完全相同
B.黑磷与石墨都属于混合型晶体
C.由石墨与黑磷制备该复合材料的过程,没有发生化学反应
D.复合材料单层中,P原子与C原子之间的作用力属范德华力
12.下列关于物质特殊聚集状态结构的叙述中,错误的是( )
A.液晶具有液体的流动性,在某些物理性质方面具有类似晶体的各向异性
B.氧化镁晶体中离子键的百分数为50%,氧化镁晶体是一种过渡晶体
C.等离子体的基本构成粒子只有阴、阳离子
D.石墨晶体属于混合晶体
13.分子之间可通过空间结构和作用力协同产生某种选择性,从而实现分子识别。下图是一种
分子梭,在链状分子A上有两个不同的识别位点。下列说法错误的是( )
A.分子B含有醚键,属于冠醚,可以与分子A形成超分子
B.通过加入酸、碱或盐,均能实现分子梭在两个不同状态之间的切换
C.在碱性情况下,环状分子B与带有正电荷的位点1的相互作用较强
D.在分子B上引入某些基团后可携带其他离子,通过识别位点实现离子转运14.氮族元素可以形成多种多样的化合物,回答下列问题:
(1)基态As原子的价电子的轨道表示式是_________。
(2)叠氮酸( )常用于引爆剂,可用联氨( )制取。比较联氨与双氧水分子
中键角大小: _________ (填“>”、“=”或“<”,下同)。叠氮酸结构
如图所示: , 为 杂化,已知参与形成π键的电子越多,键长越短,则键
长;①_________②。
(3)乙胺( )和2-羟基乙胺( )都可用于染料的合成,乙胺碱
性更强,原因是_________。
(4)磷酸一氢盐受热易脱水聚合,生成环状的偏磷酸根。环状三偏磷酸根的结构如图所示,
则由n个磷氧四面体连接形成的环状偏磷酸根的通式是_________。
(5)砷与金属钠、铁、铜可形成一种绝缘体材料,其晶胞结构图钠原子沿z轴投影如图所
示,已知m原子的分数坐标为 ,晶胞参数为 , 。铜周
围距离最近的砷原子的个数是_________,n原子的分数坐标是_________,若阿伏加德罗常
数值为 ,该晶体密度是_________ (用含 的代数式表示)。
15.W、X、Y、Z为原子序数依次增大的四种元素, 和 具有相同的电子层结构;Y的原
子核外电子总数是最外层电子数的3倍;Z元素的原子M层电子全排满,3d轨道电子数比s
轨道电子总数多3。回答下列问题:
(1)四种元素中电负性最大的是________(填元素符号),其中Y原子的核外电子排布式为________。
(2)单质 和 互为同素异形体,其中沸点较高的是________(填分子式),原因是
________________。W和X的氢化物所属的晶体类型分别为________和________。
(3)W和Z形成的一种化合物的晶体结构如图1,该化合物中Z元素的化合价为________。
(4)W和X能够形成化合物F,其晶胞结构如图2所示,晶胞参数a=0.566nm,F的化学式
为____________;晶胞中W离子的配位数为____________;晶体F的密度为___________
( 表示阿伏加德罗常数的值,列出表达式)。
答案以及解析
1.答案:A
解析:A.氯化钠晶体中 和 间隔排列,所以每个 周围有上下左右前后6个 ,同
样每个 周围也是前后左右上下6个 ,根据晶体结构分析,与 最近且等距的 有
12个,A项错误;
B.金刚石网状结构中,每个碳原子含有4个共价键,由共价键形成的碳原子环中,最小的环
上有6个碳原子,B项正确;
C.氯化铯晶体中,铯离子的配位数是8,每个 周围等距且最近的是晶胞顶点的8个Cl,C
项正确;
D.二氧化碳晶体属于面心立方,每个二氧化碳分子周围紧邻二氧化碳分子个数为12,D项正
确;
故选A。
2.答案:D
解析:一个 原子周围有6个 原子紧邻,D项错误。
3.答案:A解析:A.根据晶胞结构图可知,A原子个数为1,B原子个数为 ,所以A和B的原子
个数比为1:1,化学式为AB,故A错误;
B.根据晶胞结构图可知,C原子个数为1,D原子个数 ,所以C和D的原子个数比为
2:1,化学式为 ,故B正确;
C.根据晶胞结构图可知,E原子个数为 ,F原子个数为 ,所以E和F的原子
个数比为1:1,化学式为EF,故正确;
D.根据晶胞结构图可知,X原子个数为1,Y原子个数为 ,Z原子个数为 ,所
以X、Y、Z的原子个数比为1:3:1,化学式为 ,故D正确;
故选A。
4.答案:A
解析:A.石墨晶体层与层之间是分子间作用力,层内碳原子之间形成共价键,有自由移动电
子,含有金属键,所以石墨为混合型晶体,故A正确。
5.答案:B
解析:A项,分子晶体是由分子构成的;
B项,固态或熔融态时,分子晶体既不电离也没有自由移动的电子,均不能导电;
C项,分子间以分子间作用力相结合;
D项,分子晶体的熔、 沸点一般比较低。
6.答案:A
解析:A.金刚石和水晶是共价晶体,干冰是分子晶体,A错误;
B.共价晶体中存在共价键,故金刚石中存在共价键,分子晶体中可能存在共价键,如水中存
在共价键,也可能不存在共价键,如稀有气体中不存在共价键,B正确;
C.共价晶体中共价键的强度强于分子间作用力,故共价晶体的硬度通常比分子晶体的大,C
正确;
D.HCl为分子晶体,溶于水后的溶液盐酸可以导电,D正确;
故选A。
7.答案:C
解析:由金晶体的晶胞图可知,Au原子处于顶点与面心位置,由均摊法可知,晶胞中含有的A山原子数目 ,A正确:金属晶体中,金属键无方向性,金属原子尽可能地
采取紧密堆积,B正确;在立方体的各个面的对角线上3个金原子彼此两两相切,金原子的
直径为d,故面对角线的长度为2d,立方体的棱长为 ,故晶胞的体积为 ,C错
误;由A项分析知,金晶胞中含有4个Au原子,故晶胞的质量为 ,晶胞的体积为
,故晶胞密度 ,D正确。
8.答案:C
解析:A.由图可知,与 等距且最近的 位于棱心,共12个,即 的配位数为
12,故A正确;B.每个 位于距其最近且等距的 构成的正八面体体心中,故B错误;C.若
位于晶胞的体心,则 位于晶胞的顶点处, 位于面心,故C正确;D.由均摊法可知.1个晶
胞中含有 的数目为 , 的数目为 , 的数目为1,晶胞的质量为:
,密度为: ,故D正确:故选B。
9.答案:D
解析:①晶体呈中性,晶体中阴离子所带电荷总数与阳离子所带电荷总数相等,晶体中只要
有阴离子,必定是离子晶体,所以一定有阳离子,故①正确;
②在题目所给晶体结构模型中每个 周围有3个 与之相邻,用均摊法求得晶体中每个
离子周围共有: 个 ,故②正确;
③金刚石、SiC属于原子晶体,原子半径:CNaCl, 都属于分子晶体,分子间作用力
和氢键主要决定分子晶体的熔沸点等,金刚石、 晶体的熔点依次降
低,故③正确;
④分子晶体中分子间作用力越大,熔沸点越高,分子稳定性取决于分子中形成的化学键,故
④错误
⑤ 晶体中每个硅原子与四个氧原子以共价键相结合,每个氧原子和两个硅原子相结合形
成共价键,故⑤错误;⑥离子晶体熔沸点与晶格能成正比,所以离子晶体中晶格能越大其熔点越高,故⑥正确;
⑦石墨是非金属晶体,能导电,故⑦错误;故选:D。
10.答案:B
解析:A.冰融化时,水分子没有改变,改变的是分子间的距离,所以分子中 键没有发
生断裂,A错误;
B.共价晶体中,共价键的键能越大,破坏共价键所需的能量越大,该晶体的熔点越高,B正
确;
C.分子晶体熔化或沸腾时,只改变分子间的距离,不需要破坏分子内的共价键,所以该晶体
的熔沸点高低与键能无关,C错误;
D.分子晶体中,物质的稳定性与分子内原子间的共价键有关,与分子间作用力无关,D错
误;
故选:B。
11.答案:B
解析:黑磷中P—P键的键长不完全相等,则黑磷中P—P键的键能不完全相同,A错误;黑
磷与石墨都属于混合型晶体,B正确;由石墨与黑磷制备该复合材料的过程,有P—P键和C
—C键的断裂及P—C键的形成,则发生了化学反应,C错误;复合材料单层中,P原子与C
原子之间的作用力属共价键,D错误。
12.答案:C
解析:A.液晶像液体一样具有流动性,也具有晶体的各向异性,故A正确;
B.氧化镁晶体中离子键、共价键的成分各占50%,所以氧化镁晶体是一种过渡晶体,故B正
确;
C.等离子体主要是由电子和正离子及中性粒子组成,故C错误;
D.石墨晶体结构是层状的,每一层原子之间由共价键组成正六边形结构,层与层之间由范德
华力互相吸引,石墨晶体属于混合晶体,故D正确;
选C。
13.答案:B
14.答案:(1)
(2)>;<
(3)2-羟基乙胺上羟基氧电负性大,有吸电子作用,使氨基氮电子云密度减小,碱性减弱
(4)(5)4; ; .
解析:(1)基态As原子的价电子排布式为 ,轨道表示式为 。
(2)H-N-N中孤电子对数小于H-O-O中的孤电子对数,孤电子对对成键电子排斥作用较
大,孤电子对数量越多,键角则相对越小,因此键角H-N-N>H-O-O。①中N-N两个氮原子均
为两个p轨道的电子参与形成两个Π键,剩下一个p轨道和s轨道形成sp杂化,②中右边的
N,只形成1个Π键,两个p轨道和一个s轨道形成 杂化,因此键长①<②。
(3)2-羟基乙胺中羟基氧的电负性较大,具有吸附电子的作用,使氨基氮电子云密度减小,
碱性较弱。
(4)根据图示可知,P原子与O原子的个数比为1:3,每个P化合价为+5价,每个O化合
价为-2价,则每一个 这样的结构带一个负电荷,则n个磷氧四面体连接形成的环状偏磷
酸根的通式为 。
(5)以上顶面中心的Cu为例,与其距离最近的砷原子位于其下方的两个和上方晶胞底部的
两个,因此铜周围距离最近的砷原子的个数为4。已知m原子的坐标为(0.75,0.25,
0.20),N原子位于晶胞上方靠前的位置,坐标为(0.75,0.75,0.8)。该晶胞中含有Cu个
数为 =4,Fe个数为 =4,As个数为8,Na个数为8,则其密度
为
15.答案:(1)O; (或 )
(2) ; 相对分子质量较大且为极性分子,范德华力大;分子晶体;离子晶体
(3)+1
(4) ;8;
解析:Z元素的原子M层电子全部排满,3d轨道电子数比s轨道电子总数多3,Z价电子排布
为 ,Z是Cu元素;W、X、Y、Z为原子序数依次增大的四种元素,Y的原子核外电子
总数是最外层电子数的3倍,则Y是P元素; 、 具有相同的电子层结构,W是O元
素.X是Na元素。
(1)元素的非金属性越强,电负性越大,四种元素中电负性最大的是O;Y是P元素,P原子的核外电子排布式为 。
(2) 和 互为同素异形体, 相对分子质量较大且为极性分子,范德华力大,所以沸点较
高的是 , 由分子构成,属于分子晶体,NaH由离子构成,属于离子晶体。
(3)根据均摊原则,晶胞中Cu原子数为4、O原子数为 ,化学式为 ,该化合物中
Cu元素的化合价为+1,
(4) 的半径小于 ,所以黑球表示 、白球表示 ,根据均推原则, 数为8、
数 ,F的化学式为 ;晶管中 离子的配位数为8;晶体F的密度为
.