文档内容
关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
模块一 知识主题
热点突破 金属与酸、盐溶液反应的图像问题
01考情透视·目标导航
02知识导图·思维引航
03核心精讲·题型突破
考点一 金属与酸反应的图像问题 ►知识点二 等量酸与足量金属的反应
【真题研析】 【命题探究】
►考法01 产生氢气的质量随反应时间变化 考点二 金属与盐溶液反应的图像问题
的图像(等质量金属与足量酸) 【真题研析】
►考法02 产生氢气的质量随加入酸质量的 ►考法01 金属质量的变化
变化图像(等质量金属与足量酸) ►考法02 溶液(或溶质)的质量变化
►考法03 产生氢气的质量随反应时间变化 【核心精讲】
的图像(足量金属与等质量酸) ►知识点一 溶解度与溶解性
►考法04 产生氢气的质量随加入酸质量的 ►知识点二 溶解度与溶质质量分数
变化图像(足量金属与等质量酸) 【命题探究】
【核心精讲】
►知识点一 等量金属与足量酸的反应
考点要求 课标要求 命题预测
了解饱和溶液和溶解度的含义;查阅溶 本专题的内容是中考常考的考点。常以选
解度数据,绘制溶解度曲线;认识结晶现 择题和填空与简答题的形式进行考查,考查的
象。 命题点有:饱和与不饱和溶液的转化方法、溶
解度随温度的变化情况、某温度下,溶解度大
认识溶质质量分数的含义,学习计算溶
小的判断及比较、溶解度曲线上的点的含义、
质质量分数。
判断物质提纯的方法、计算或比较溶液中溶质
1关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
质量分数的大小等。
考点一 金属与酸反应的图像分析
考法 01 产生氢气的质量随反应时间变化的图像(等质量金属与足量酸)
1.(2024·山东济宁·中考真题)下列图像能正确反映对应变化关系的是
A.图Ⅰ表示向一定量的盐酸和硫酸混合溶液中不断加入 溶液
B.图Ⅱ表示向一定量的稀盐酸中不断滴加水
C.图Ⅲ表示向等质量不同金属粉末中分别加入足量等浓度的稀硫酸
D.图Ⅳ表示在恒温条件下,将饱和氯化钠溶液蒸发适量的水
【答案】C
【解析】A、向一定量的盐酸和硫酸混合溶液中不断加入 Ba ( OH ) 溶液,氢氧根离子与氢离子会结合
2
成水,钡离子与硫酸根会结合成不溶于酸的沉淀硫酸钡,沉淀一开始就会出现,图像错误;
B、稀盐酸溶液显酸性,pH<7,向一定量的稀盐酸中不断滴加水,溶液的pH逐渐增大,但不会大于7,
图像错误;
C、向等质量不同金属粉末中分别加入足量等浓度的稀硫酸,由于三种金属的活动性:镁>锌>铁,所以
相同时间,镁反应速度最快,铁最慢,相同时间镁产生气体最多,曲线最陡,铁产生气体最少,曲线最缓;
镁与硫酸反应生成硫酸镁和氢气,铁与硫酸反应生成硫酸亚铁和氢气,锌与硫酸反应生成硫酸锌和氢气,
方程式及相关质量关系如下: 、 、
,由于酸足量,所以金属完全反应,消耗等量的三种金属,镁产生气体
2关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
最多,锌产生气体最少,图像正确;
D、恒温条件下,将饱和氯化钠溶液蒸发适量的水,有氯化钠析出,析出晶体后的溶液仍为该温度下的饱
和溶液,溶质质量分数不变,图像错误;
故选C。
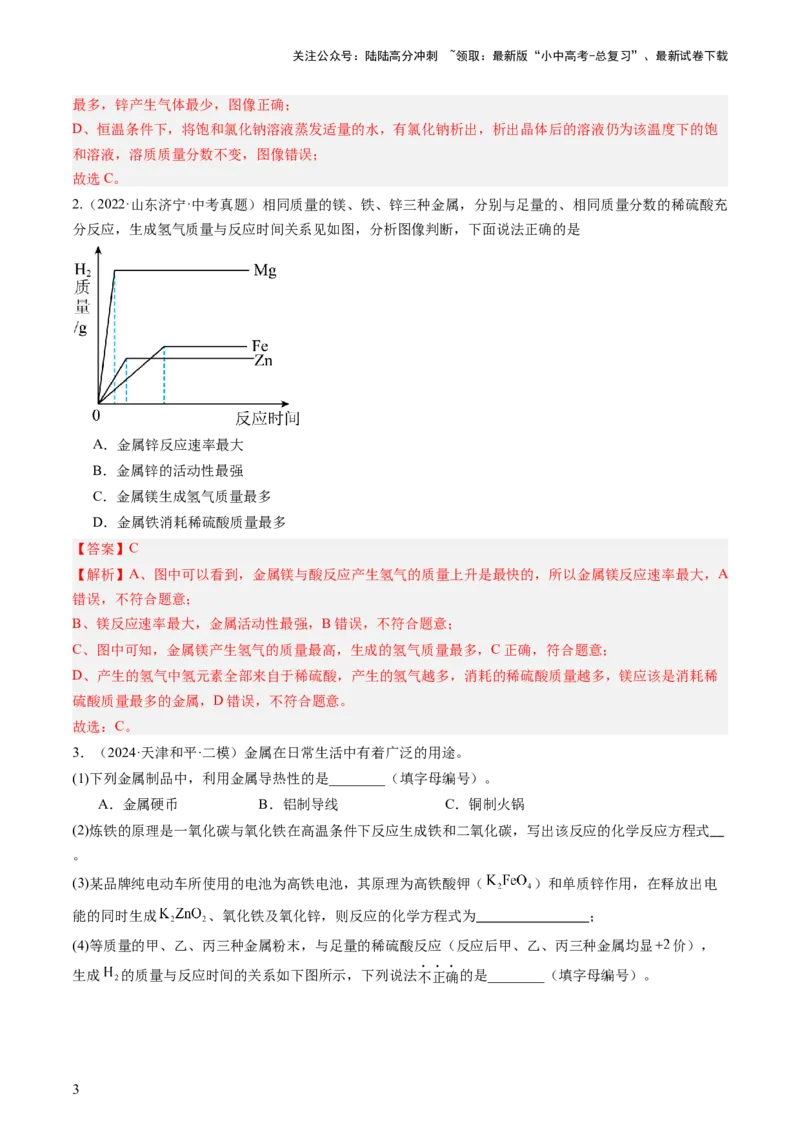
2.(2022·山东济宁·中考真题)相同质量的镁、铁、锌三种金属,分别与足量的、相同质量分数的稀硫酸充
分反应,生成氢气质量与反应时间关系见如图,分析图像判断,下面说法正确的是
A.金属锌反应速率最大
B.金属锌的活动性最强
C.金属镁生成氢气质量最多
D.金属铁消耗稀硫酸质量最多
【答案】C
【解析】A、图中可以看到,金属镁与酸反应产生氢气的质量上升是最快的,所以金属镁反应速率最大,A
错误,不符合题意;
B、镁反应速率最大,金属活动性最强,B错误,不符合题意;
C、图中可知,金属镁产生氢气的质量最高,生成的氢气质量最多,C正确,符合题意;
D、产生的氢气中氢元素全部来自于稀硫酸,产生的氢气越多,消耗的稀硫酸质量越多,镁应该是消耗稀
硫酸质量最多的金属,D错误,不符合题意。
故选:C。
3.(2024·天津和平·二模)金属在日常生活中有着广泛的用途。
(1)下列金属制品中,利用金属导热性的是________(填字母编号)。
A.金属硬币 B.铝制导线 C.铜制火锅
(2)炼铁的原理是一氧化碳与氧化铁在高温条件下反应生成铁和二氧化碳,写出该反应的化学反应方程式
。
(3)某品牌纯电动车所使用的电池为高铁电池,其原理为高铁酸钾( )和单质锌作用,在释放出电
能的同时生成 、氧化铁及氧化锌,则反应的化学方程式为 ;
(4)等质量的甲、乙、丙三种金属粉末,与足量的稀硫酸反应(反应后甲、乙、丙三种金属均显 价),
生成 的质量与反应时间的关系如下图所示,下列说法不正确的是________(填字母编号)。
3关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
A.三种金属的活动性:乙>甲>丙 B.生成氢气的质量:甲>乙>丙
C.相对原子质量:甲>乙>丙 D.消耗硫酸的质量:甲>乙>丙
(5)某同学用称量法测定铁在氧气中燃烧的产物。将 铁在一定量的氧气中燃烧得到 固体。则得
到的固体产物可能是_________(填字母)。
A. B. 和 的混合物
C. 和 的混合物 D. 、 和 的混合物
【答案】(1)C
(2)
(3)
(4)C
(5)C
【解析】(1)A、用作金属硬币,是利用了金属硬度大、有金属光泽的性质,不符合题意;
B、铝制导线,是利用了铝的导电性和延展性,不符合题意;
C、铜制火锅,是利用了铜的导热性,符合题意;
故选:C;
(2)高温条件下,氧化铁和一氧化碳反应生成铁和二氧化碳,该反应的化学方程式:
;
(3)高铁酸钾(KFeO)和单质锌作用,在释放出电能的同时生成KZnO、氧化铁及氧化锌,则反应的
2 4 2 2
化学方程式为: ;
(4)A、根据图示,等质量甲、乙、丙三种金属,至完全反应,乙用的时间最少,丙用的时间最多,金属
的活动性越强,与酸反应的速率越快,则反应需要时间越短,因此三种金属的活动性是乙>甲>丙,该选
项说法正确;
B、根据图示,则生成氢气的质量是甲>乙>丙,该选项说法正确;
C、由于化合价相同,产生的氢气质量与金属的相对原子质量成反比,产生氢气质量越多,说明该金属的
相对原子质量越小,因此相对原子质量是甲<乙<丙,该选项说法不正确;
D、由质量守恒定律可知,生成氢气的质量等于参加反应的硫酸中氢元素的质量,生成氢气的质量越多,
消耗硫酸的质量越多,则消耗硫酸的质量:甲>乙>丙,该选项说法正确;
4关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
故选:C;
(5)设11.2g铁完全燃烧生成四氧化三铁的质量是x,则有 ,
,解得x≈15.47g;而实际生成的固体质量15.8g>15.47g,说明生成的另一种固体中含氧量比
四氧化三铁中的含氧量高,Fe O、Fe O、FeO中含氧量的比较可根据铁原子相等将化学式变形,得到
3 4 2 3
Fe O、Fe O、Fe O,由此可见三氧化二铁中氧元素的含量高,所以固体可能是Fe O 和 Fe O 的混合物,
6 8 6 9 6 6 3 4 2 3
故选:C。
考法 02 产生氢气的质量随加入酸质量的变化图像(等质量金属与足量酸)
4.(2023·山东潍坊·中考真题)向两个盛有相同质量铝粉和铁粉的烧杯中,分别滴加相同浓度的稀硫酸,
产生氢气的质量与加入稀硫酸的质量关系如图所示。下列说法正确的是
A.a点时,两个烧杯中的酸都恰好完全反应
B.b点时,两个烧杯中产生氢气的质量相同
C.c点时,两个烧杯中都有金属剩余
D.右侧曲线不能反映铁和铝的金属活动性强弱
【答案】CD
【解析】A、由图可知,a点时,Al与稀硫酸恰好完全反应,盛铁的烧杯中的酸有剩余,故选项说法错误;
B、由图可知,b点时,两个烧杯中消耗硫酸不相等,产生氢气的质量不相同,故选项说法错误;
C、由图可知,c点之后,两个烧杯都能继续产生氢气,则c点时,两个烧杯中都有金属剩余,故选项说法
正确;
D、由图可知,该曲线是氢气与酸的曲线,不是氢气与时间的曲线,故右侧曲线不能反映反应的速率,不
能反映铁和铝的金属活动性强弱,故选项说法正确。
故选CD。
5.(2024·山东泰安·中考真题)下列图像与对应实验相符的是
5关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
A.用等质量、等溶质质量分数的过氧化氢溶液分别制取氧气
B.向等质量的Mg、Fe中分别滴加溶质质量分数相同的足量稀硫酸
C.向一定质量接近饱和的硝酸钠溶液中加入硝酸钠固体
D.向稀硫酸中加入蒸馏水
【答案】C
【解析】A、用等质量、等溶质质量分数的过氧化氢溶液分别制取氧气,催化剂只能影响反应速率,不影
响产生氧气的质量,有催化剂的反应速率快,至完全反应所需时间短,故选项图像错误;
B、由反应的质量关系 、 可知,向等质
量的镁和铁中分别滴加足量且溶质质量分数相等的稀硫酸,若消耗硫酸相同,则生成氢气质量相同,故开
始两斜线重合,后因硫酸过量,镁消耗硫酸多,生成氢气多,拐点高些,故选项图像错误;
C、向一定质量接近饱和的硝酸钠溶液中加入硝酸钠固体,硝酸钠能继续溶解,当达到饱和状态后不再继
续溶解,则溶质质量分数先增大,后不变,故选项图像正确;
D、稀硫酸显酸性,溶液的pH小于7,加水稀释,溶液的酸性减弱,溶液的pH逐渐增大,溶液始终显酸
性,pH不可能大于或等于7,故选项图像错误。
故选C。
考法 0 3 产生氢气的质量随反应时间变化的图像(足量金属与等质量酸)
6.(2024·河南周口·二模)现有等质量的铁和锌两种金属,分别与等质量同浓度的稀盐酸充分反应,产生
氢气的质量与反应时间的关系如图所示。根据图中所提供的信息,得出的结论不正确的是
A.充分反应后消耗的稀盐酸一样多
B.图线 A 表示锌的反应情况
C.反应结束后至少有一种金属剩余,则剩余金属一定是为锌
D.金属B反应过程中可观察到金属溶解、有气泡产生、溶液变为浅绿色
【答案】C
【详解】A、由图可知,最终生成氢气的质量相同,根据氢元素守恒,则消耗的盐酸的质量相同,该选项
6关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
结论正确;
B、由于锌比铁活泼,则锌和盐酸反应比铁和盐酸反应的速率快,则A表示锌的反应情况,该选项结论正
确;
C、由于 、 ,则生成等质量氢气时,
消耗的锌的质量更多,若有一种金属剩余,则剩余金属一定为铁,该选项结论不正确;
D、结合前面分析可知,B表示铁,铁和盐酸反应生成氯化亚铁和氢气,则可观察到金属溶解、有气泡产
生、溶液变为浅绿色,该选项结论正确。
故选C。
7.(2024·山东济宁·二模)在相同质量、相同质量分数的稀硫酸中,分别加入足量的Mg、Fe、Zn三种金
属,其发生反应的质量关系如下图,不正确的是
A. B.
C. D.
【答案】D
【解析】A、在相同质量、相同质量分数的稀硫酸中,分别加入足量的Mg、Fe、Zn三种金属,Mg、Fe、
Zn与稀硫酸反应均生成氢气,由于金属是过量的,因此生成氢气的质量与稀硫酸的质量有关,所以最终生
成氢气的质量是相等的,由化学方程式 、 、
可知,相同质量、相同质量分数的稀硫酸分别与足量的Mg、Fe、Zn反应生成的
硫酸镁、硫酸亚铁、硫酸锌质量大小关系为硫酸锌>硫酸亚铁>硫酸镁,则反应后溶液质量大小关系为锌
>铁>镁,故该图像表示正确,不符合题意;
B、在相同质量、相同质量分数的稀硫酸中,分别加入足量的Mg、Fe、Zn三种金属,Mg、Fe、Zn与稀硫
酸反应均生成氢气,由于金属是过量的,因此生成氢气的质量与稀硫酸的质量有关,所以最终生成氢气的
7关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
质量是相等的,由化学方程式 、 、
可知,生成等质量的氢气消耗的金属质量大小关系为锌>铁>镁,故该图像表
示正确,不符合题意;
C、在相同质量、相同质量分数的稀硫酸中,分别加入足量的Mg、Fe、Zn三种金属,Mg、Fe、Zn与稀硫
酸反应均生成氢气,由于金属是过量的,因此生成氢气的质量与稀硫酸的质量有关,所以最终生成氢气的
质量是相等的,根据金属活动性Mg>Zn >Fe可知,Mg、Fe、Zn三种金属与稀硫酸反应的反应速率Mg
>Zn>Fe,故该图像表示正确,不符合题意;
D、在相同质量、相同质量分数的稀硫酸中,分别加入足量的Mg、Fe、Zn三种金属,Mg、Fe、Zn与稀硫
酸反应均生成氢气,则随着反应的进行,硫酸的质量逐渐减少直至完全反应,故该图像表示不正确,符合
题意。
故选:D。
考法 0 4 产生氢气的质量随加入酸质量的变化图像(足量金属与等质量酸)
8.下列图像能正确表示对应叙述的有___________(填序号)。
A.表示足量的Zn粉、Fe粉与等质量、等浓度的稀盐酸反应时,反应时间与生成氢气质量的关系
B.表示等质量的Zn粉、Fe粉与足量的相同浓度的稀盐酸反应时,反应时间与生成氢气质量的关系
C.表示等质量的Zn粉、Fe粉与足量的相同浓度的稀盐酸反应时,加入酸的质量与生成氢气质量的关系
D.表示向盛有等质量、等浓度的稀盐酸中分别加入足量的Zn粉、Fe粉的质量与生成氢气质量的关系
【答案】ABCD
【解析】(5)A、足量的Zn粉、Fe粉与等质量、等浓度的稀盐酸反应,由于锌的金属活动性比铁强,所
以锌的反应速率比铁快,由于金属是过量的,所以生成氢气的质量与稀盐酸有关,则最终生成氢气的质量
相等,故该图像能表示足量的Zn粉、Fe粉与等质量、等浓度的稀盐酸反应时,反应时间与生成氢气质量
的关系,符合题意;
B、等质量的Zn粉、Fe粉与足量的相同浓度的稀盐酸反应,由于锌的金属活动性比铁强,所以锌的反应速
率比铁快,根据化学方程式 、 可知,等质量的锌、铁与足量
相同浓度的稀盐酸反应生成氢气的质量铁>锌,故该图像能表示等质量的Zn粉、Fe粉与足量的相同浓度
的稀盐酸反应时,反应时间与生成氢气质量的关系,符合题意;
8关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
C、等质量的Zn粉、Fe粉与足量的相同浓度的稀盐酸反应,根据化学方程式 、
可知,等质量、等浓度的稀盐酸与锌、铁反应生成的氢气质量相等,等质量的锌、
铁与足量相同浓度的稀盐酸反应生成氢气的质量铁>锌,故该图像能表示等质量的Zn粉、Fe粉与足量的
相同浓度的稀盐酸反应时,加入酸的质量与生成氢气质量的关系,符合题意;
D、向盛有等质量、等浓度的稀盐酸中分别加入足量的Zn粉、Fe粉,根据化学方程式
、 可知,等质量的锌、铁与相同浓度的稀盐酸反应生成氢气
的质量铁>锌,由于金属是过量的,则生成氢气的质量与稀盐酸有关,则最终生成氢气的质量相等,故该
图像能表示向盛有等质量、等浓度的稀盐酸中分别加入足量的Zn粉、Fe粉,加入金属的质量与生成氢气
质量的关系,符合题意。
故选:ABCD。
解题思路
1.确定过量的物质
明确金属与酸谁过量,一种物质过量,计算时以另一种物质为准。
2.“五看”图像:
一看坐标:明确纵横坐标,找准自变量与因变量的关系;
二看起点:图像的起点,在原点还是在坐标轴上;
三看转折点:图像的转折点和终点;
四看比例:看图像中的纵坐标和横坐标的比例关系;
五看图像的特征:斜线的坡度、水平线对应的纵坐标的数值;
3.找出图中化学反应量的关系
将图像表示的意义与化学反应联系起来,找出图像与化学反应中量的具体关系,再进行分析,进而解决相
关问题。
知识点一 等量金属与足量酸的反应
1.产生氢气的质量随反应时间变化的图像
9关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
(1)比较斜线的坡度:
图像中斜线的坡度表示产生氢气的速率,斜线坡度越陡,产生氢气越快,金属越活泼。
(生成H 的速率由金属活动性决定,金属越活泼,产生氢气的速率越快。)
2
(2)比较水平线对应的纵坐标
图像中的水平线对应的纵坐标表示反应结束产生氢气的质量,水平线越高,生成的氢气越多。
金 属 的 化合 价
(3)产生氢气的质量=金属的质量× (金属的化合价指生成的盐中金属元素的化
金 属 的 质 量
合价)。
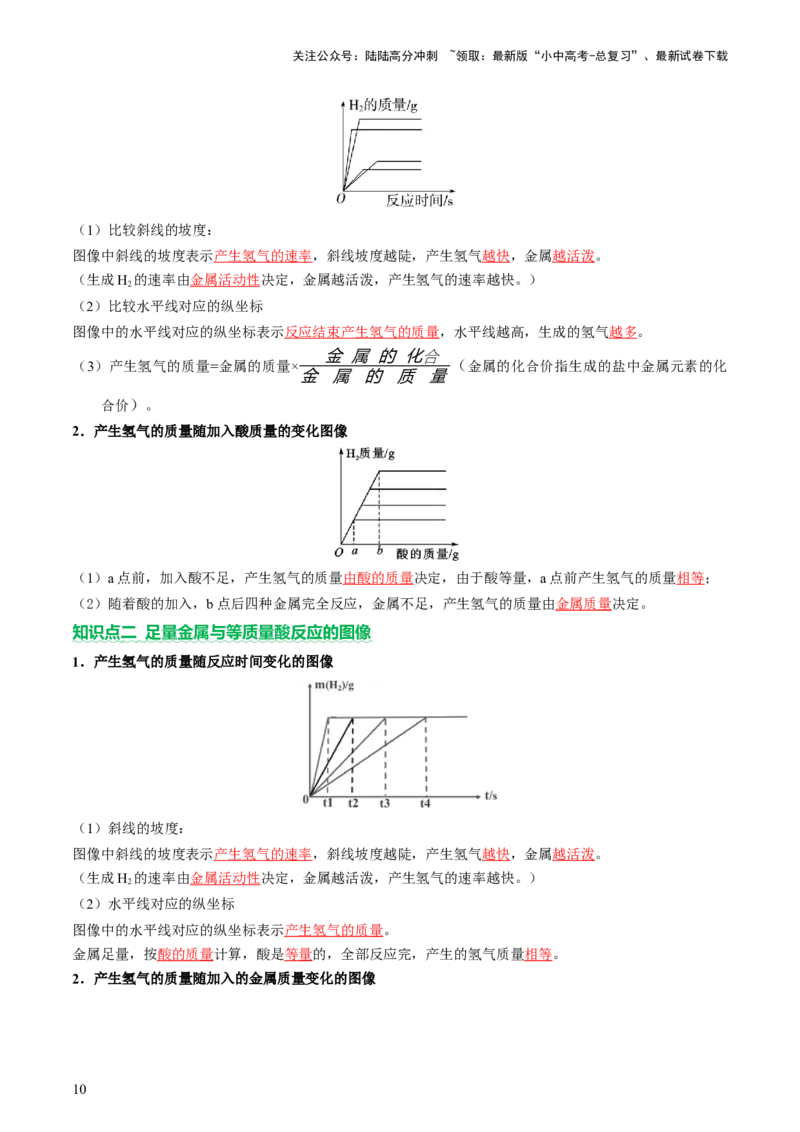
2.产生氢气的质量随加入酸质量的变化图像
(1)a点前,加入酸不足,产生氢气的质量由酸的质量决定,由于酸等量,a点前产生氢气的质量相等;
(2)随着酸的加入,b点后四种金属完全反应,金属不足,产生氢气的质量由金属质量决定。
知识点 二 足量金属与等质量酸反应的图像
1.产生氢气的质量随反应时间变化的图像
(1)斜线的坡度:
图像中斜线的坡度表示产生氢气的速率,斜线坡度越陡,产生氢气越快,金属越活泼。
(生成H 的速率由金属活动性决定,金属越活泼,产生氢气的速率越快。)
2
(2)水平线对应的纵坐标
图像中的水平线对应的纵坐标表示产生氢气的质量。
金属足量,按 酸 的 质量 计算,酸是等量的,全部反应完,产生的氢气质量相等。
2.产生氢气的质量随加入的金属质量变化的图像
10关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
(1)a点之前,酸足量,产生氢气的质量由 金属 的质量 决定,图像斜线越陡,产生氢气的质量越多。
(2)最终生成氢气的质量由 酸 的质量 决定,酸的质量相等,则最终产生氢气的质量相等。
1.现有质量相等的X、Y、Z三种金属,分别放入三份溶质质量分数相等的足量稀硫酸中,X不发生反应,
Y、Z在生成物中均显+2价,Y、Z反应生成氢气的质量与反应时间的关系如图所示,则下列说法正确的是
A.X、Y、Z的金属活动性顺序为:Y>Z>X
B.相对原子质量:Y>Z
C.完全反应生成氢气的质量:Y Y >X,错误;
B. 一定量金属与足量酸完全反应时,产生氢气质量= ;Y、Z在生成物中
均显+2价,且Y生成氢气质量大,则相对原子质量:YZ,错误;
D. Y、Z在生成物中均显+2价,则Y与HSO 反应的化学方程式为: ,正确;
2 4
故选D。
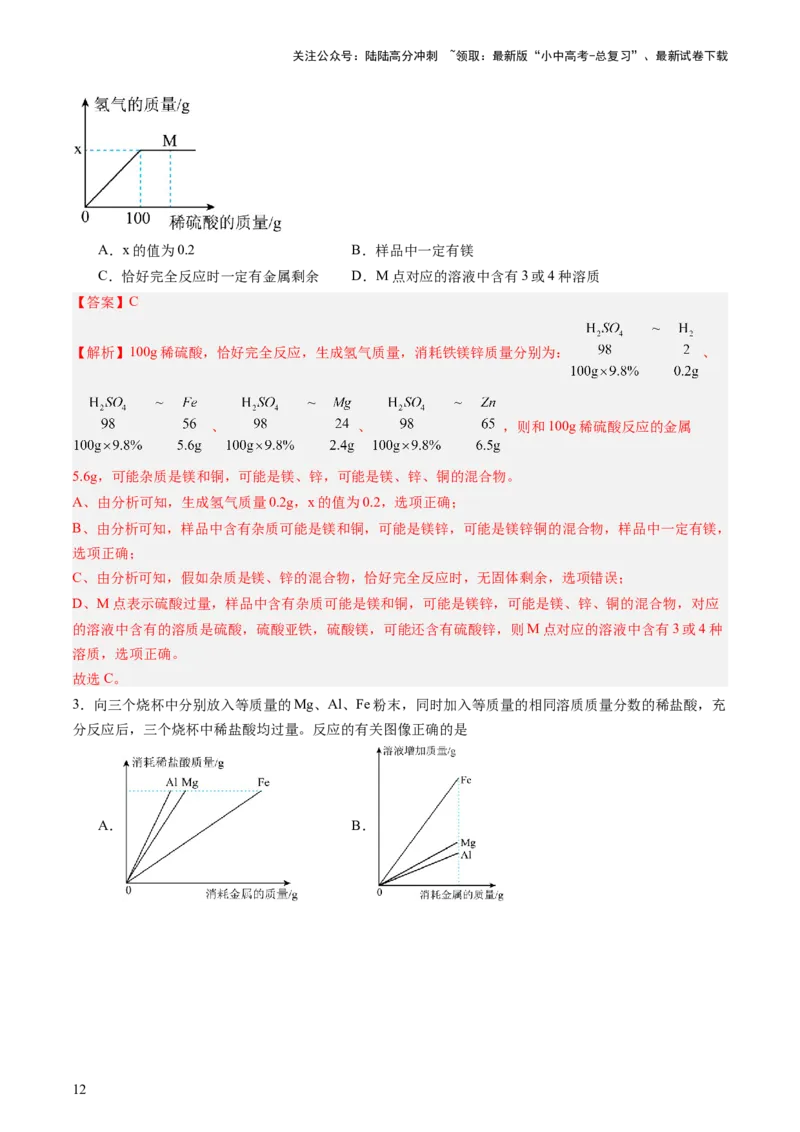
2.现有某铁样品5.6g,含有的杂质为镁、锌、铜中的两种或三种,向样品中逐渐加入溶质质量分数为
9.8%的稀硫酸,产生氢气的质量与加入稀硫酸的质量的关系如图所示。下列说法错误的是
11关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
A.x的值为0.2 B.样品中一定有镁
C.恰好完全反应时一定有金属剩余 D.M点对应的溶液中含有3或4种溶质
【答案】C
【解析】100g稀硫酸,恰好完全反应,生成氢气质量,消耗铁镁锌质量分别为: 、
、 、 ,则和100g稀硫酸反应的金属
5.6g,可能杂质是镁和铜,可能是镁、锌,可能是镁、锌、铜的混合物。
A、由分析可知,生成氢气质量0.2g,x的值为0.2,选项正确;
B、由分析可知,样品中含有杂质可能是镁和铜,可能是镁锌,可能是镁锌铜的混合物,样品中一定有镁,
选项正确;
C、由分析可知,假如杂质是镁、锌的混合物,恰好完全反应时,无固体剩余,选项错误;
D、M点表示硫酸过量,样品中含有杂质可能是镁和铜,可能是镁锌,可能是镁、锌、铜的混合物,对应
的溶液中含有的溶质是硫酸,硫酸亚铁,硫酸镁,可能还含有硫酸锌,则M点对应的溶液中含有3或4种
溶质,选项正确。
故选C。
3.向三个烧杯中分别放入等质量的Mg、Al、Fe粉末,同时加入等质量的相同溶质质量分数的稀盐酸,充
分反应后,三个烧杯中稀盐酸均过量。反应的有关图像正确的是
A. B.
12关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
C. D.
【答案】B
【解析】等质量的Mg、Al、Fe与足量等质量的相同溶质质量分数的稀盐酸反应,参加反应的物质及生成
的物质的质量关系如下:
为方便比较,Al与盐酸反应可看成: 。
A、根据以上质量关系可知,参与反应的三种金属质量相同时,Al、Mg、Fe消耗稀盐酸的质量关系为 :
: ,所以等质量的三种金属消耗稀盐酸的质量关系为Al>Mg>Fe,最终Al消耗的稀盐酸最多,Fe最
少。故A错误;
B、等质量的三种金属产生氢气的质量关系是Al>Mg>Fe(Al是18g可生成2gH, Mg是24g可生成
2
2gH, Fe是56g可生成2gH,故等质量的Al、Mg、Fe与足量盐酸反应生成H 的质量是Al最多,Fe最
2 2 2
少), 因溶液增加的质量是加入金属的质量和生成H 的质量差,加入金属的质量都相等,产生H 越多,
2 2
溶液质量增加的越少,故溶液增加的质量关系是Fe>Mg>Al。故B正确;
C、等质量的Mg、Al、Fe与足量稀盐酸反应生成H 的质量关系为Al>Mg>Fe(因每24gMg可生成2gH,
2 2
每56gFe可生成2gH,每18gAl可生成2gH),故Mg、Al、Fe与足量稀盐酸反应生成H 的质量关系为
2 2 2
Al>Mg>Fe,而图中生成H 的质量相等。故C错误;
2
D、因酸过量,最终三种金属完全反应,而三种金属的质量相等,图中消耗的三种金属的质量不相等。故
D错误。
故选B。
4.现有等质量的铁和锌两种金属,分别与等质量同浓度的稀盐酸充分反应,产生氢气的质量与反应时间
的关系如图所示。根据图中所提供的信息,得出的结论不正确的是
13关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
A.充分反应后消耗的稀盐酸一样多
B.图线 A 表示锌的反应情况
C.反应结束后至少有一种金属剩余,则剩余金属一定是为锌
D.金属B反应过程中可观察到金属溶解、有气泡产生、溶液变为浅绿色
【答案】C
【解析】A、由图可知,最终生成氢气的质量相同,根据氢元素守恒,则消耗的盐酸的质量相同,该选项
结论正确;
B、由于锌比铁活泼,则锌和盐酸反应比铁和盐酸反应的速率快,则A表示锌的反应情况,该选项结论正
确;
C、由于 、 ,则生成等质量氢气时,
消耗的锌的质量更多,若有一种金属剩余,则剩余金属一定为铁,该选项结论不正确;
D、结合前面分析可知,B表示铁,铁和盐酸反应生成氯化亚铁和氢气,则可观察到金属溶解、有气泡产
生、溶液变为浅绿色,该选项结论正确。
故选C。
5.分别向同质量、同质量分数的稀盐酸中加入X、Y两种金属粉末,反应时的质量关系如图所示。下列说
法正确的是
A.加入金属的质量: B.金属的活动性:
C.参加反应的酸的质量: D.最终所得溶液的质量:
【答案】C
【解析】A、由图可知,加入的金属的质量:X>Y,该选项说法不正确;
B、由于该图横坐标不是时间,则无法比较金属活动性顺序,该选项说法不正确;
C、由图可知,最终生成的氢气的质量相同,根据氢元素守恒,则说明参加反应的酸的质量相同,该选项
说法正确;
D、根据质量守恒定律,由于消耗的金属质量X>Y,生成的氢气的质量相同,消耗的酸的质量相同,则最
终所带溶液的质量:X>Y,该选项说法不正确。
14关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
故选C。
6.把相同质量的甲、乙两种金属分别加入相同质量、相同质量分数的足量稀盐酸中,产生氢气的质量随
时间变化的曲线如图所示,下列说法不正确的是
A.完全反应后甲生成的气体比乙多
B.乙的金属活动性比甲强
C.在盐酸盐中甲的化合价一定比乙高
D.甲的相对原子质量可能比乙小
【答案】C
【解析】A、由图可知,完全反应后甲生成的气体比乙多,该选项说法正确;
B、由图可知,乙完全反应需要时间短,说明乙的金属活动性比甲强,该选项说法正确;
C、根据图示,无法确定甲、乙的化合价,该选项说法不正确;
D、由图可知,完全反应后甲生成的气体比乙多,如果甲、乙反应后在化合物中最大化合价相同时,则甲
的相对原子质量比乙小,该选项说法正确;
故选:C。
7.等质量的甲、乙、丙三种金属分别与三份等质量且足量的稀硫酸充分反应(反应后甲、乙、丙三种金属
元素均显+2价),生成氢气的质量与反应时间的变化关系如图所示。下列说法正确的是
A.反应消耗硫酸的质量相同 B.化学反应速率:甲>乙>丙
C.所得溶液的质量:甲<乙<丙 D.相对原子质量:甲>乙>丙
【答案】C
【解析】A、由纵坐标可知,生成氢气的质量:甲>乙>丙,根据质量守恒定律可知化学反应前后氢元素
的质量不变,因此反应消耗硫酸的质量:甲>乙>丙,说法错误,不符合题意;
B、金属的活动性越强,化学反应速率越快,根据完全反应所消耗的时间可知三种金属的活泼性:甲>丙
>乙,说明化学反应速率:甲>丙>乙,说法错误,不符合题意;
C、由纵坐标可知,生成氢气的质量:甲>乙>丙,根据质量守恒定律可知化学反应前后物质总质量不变,
由于是等质量的甲、乙、丙三种金属与等质量且足量的稀硫酸反应,生成的氢气是气体所以会逸出,则反
应后所得溶液质量:甲<乙<丙,说法正确,符合题意;
15关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
D、等质量的金属和等质量且足量的稀硫酸完全反应产生氢气的质量为
,由于反应后甲、乙、丙三种金属元素均显+2价,而生成氢
气的质量:甲>乙>丙,则相对原子质量:甲<乙<丙,说法错误,不符合题意。
故选:C。
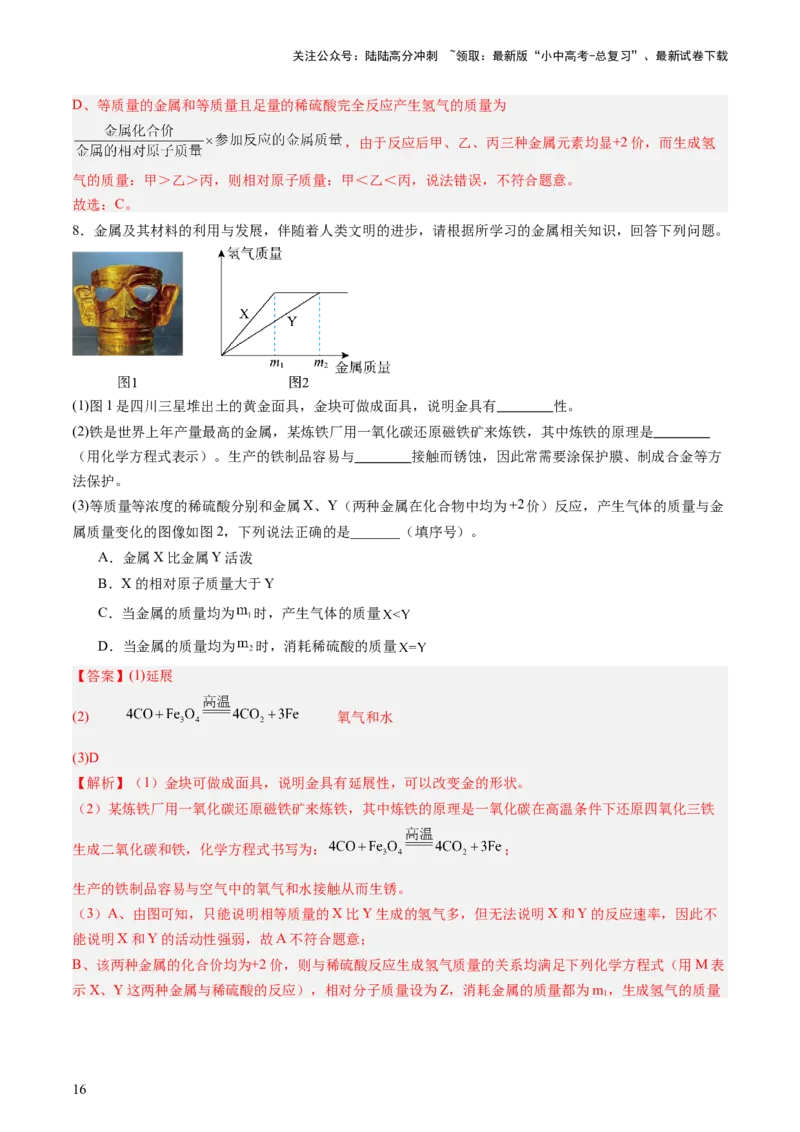
8.金属及其材料的利用与发展,伴随着人类文明的进步,请根据所学习的金属相关知识,回答下列问题。
(1)图1是四川三星堆出土的黄金面具,金块可做成面具,说明金具有 性。
(2)铁是世界上年产量最高的金属,某炼铁厂用一氧化碳还原磁铁矿来炼铁,其中炼铁的原理是
(用化学方程式表示)。生产的铁制品容易与 接触而锈蚀,因此常需要涂保护膜、制成合金等方
法保护。
(3)等质量等浓度的稀硫酸分别和金属X、Y(两种金属在化合物中均为 价)反应,产生气体的质量与金
属质量变化的图像如图2,下列说法正确的是_______(填序号)。
A.金属X比金属Y活泼
B.X的相对原子质量大于Y
C.当金属的质量均为 时,产生气体的质量
D.当金属的质量均为 时,消耗稀硫酸的质量
【答案】(1)延展
(2) 氧气和水
(3)D
【解析】(1)金块可做成面具,说明金具有延展性,可以改变金的形状。
(2)某炼铁厂用一氧化碳还原磁铁矿来炼铁,其中炼铁的原理是一氧化碳在高温条件下还原四氧化三铁
生成二氧化碳和铁,化学方程式书写为: ;
生产的铁制品容易与空气中的氧气和水接触从而生锈。
(3)A、由图可知,只能说明相等质量的X比Y生成的氢气多,但无法说明X和Y的反应速率,因此不
能说明X和Y的活动性强弱,故A不符合题意;
B、该两种金属的化合价均为+2价,则与稀硫酸反应生成氢气质量的关系均满足下列化学方程式(用M表
示X、Y这两种金属与稀硫酸的反应),相对分子质量设为Z,消耗金属的质量都为m,生成氢气的质量
1
16关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
为m,则有: ,可得 ,根据图可知,当消耗金属的质量都为m 时,
1
X产生氢气的质量大于Y产生氢气的质量,由此可知X的相对原子质量小于Y,故B不符合题意;
C、由图可知,当金属的质量均为m 时,产生气体的质量X大于Y,故C不符合题意;
1
D、由图可知,当金属的质量均为m 时,X、Y生成相等质量的氢气,根据氢元素来源于反应的酸中,故
2
此时消耗的稀硫酸的质量相等,故D符合题意;
故选D。
考点二 金属与盐溶液反应的图像问题
考法 0 1 金属质量的变化
1.(2024·河北邯郸·三模)向盛有一定质量FeCl 、MgCl 和CuCl 混合溶液的烧杯中,加入锌粉至过量使
2 2 2
其充分反应(溶液始终未饱和),烧杯中不溶性固体的质量随锌粉质量的变化情况如图所示。下列说法正
确的是
A.过滤出M点时溶液中的固体,干燥后加入稀盐酸,有气泡产生
B.M到P过程中溶液的质量一直在增大
C.P点溶液中的溶质为ZnCl
2
D.溶液质量:Q>P
【答案】B
【解析】A、M点时发生的反应为锌和氯化铜反应生成铜和氯化锌,过滤后所得的固体中只含有铜,铜不
能和盐酸反应,则加入稀盐酸,不会有气泡产生,该选项说法不正确;
B、由于 、 ,锌和氯化铜、氯化亚铁反
应时,固体质量均减小,根据质量守恒定律可知,溶液质量增大,该选项说法正确;
C、P点表示锌和氯化亚铁恰好反应,此时溶液中的溶质有氯化锌和氯化镁,该选项说法不正确;
D、P点时反应结束,则溶液质量:Q=P,该选项说法不正确。
故选B。
2.(2022·四川遂宁·统考中考真题)向AgNO 和Cu(NO) 的混合溶液中缓慢连续加入m克锌粉,析出固
3 3 2
体的质量与加入锌粉的质量关系如图所示,下列分析不正确的是
17关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
A.向N点对应溶液中加入氯化钠溶液,有白色沉淀产生
B.P点对应的固体一定有Cu,可能有Ag
C.Q点对应的溶液为无色,此时溶液的溶质无Cu(NO),只有Zn(NO)
3 2 3 2
D.加入m克锌粉后,过滤,向滤渣中加入稀盐酸,有气泡产生
【答案】B
【解析】向AgNO 和Cu(NO) 的混合溶液中缓慢连续加入m克锌粉,锌先和硝酸银反应生成硝酸锌和银,
3 3 2
再和硝酸铜反应生成硝酸锌和铜,第一个拐点表示硝酸银恰好完全反应,第二个拐点表示硝酸铜恰好完全
反应。
A、N点位于第一个拐点之前,表示硝酸银没有完全反应,加入氯化钠溶液,氯化钠和硝酸银生成氯化银沉
淀和硝酸钠,分析正确。
B、P点为与两个拐点之间,表示硝酸银恰好完全反应,硝酸铜有剩余,对应的固体一定有Cu,Ag,分析错
误。
C、Q点位于第二个拐点之后,表示硝酸银、硝酸铜完全反应,且锌粉过量,对应的溶液为无色,分析正确。
D、m克锌粉对应点在两拐点之后,表示硝酸银、硝酸铜完全反应,且锌粉过量,向滤渣中加入稀盐酸,盐
酸和锌生成氯化锌和氢气,有气泡产生,分析正确。
故选:B。
考法 0 2 溶液(或溶质)的质量变化
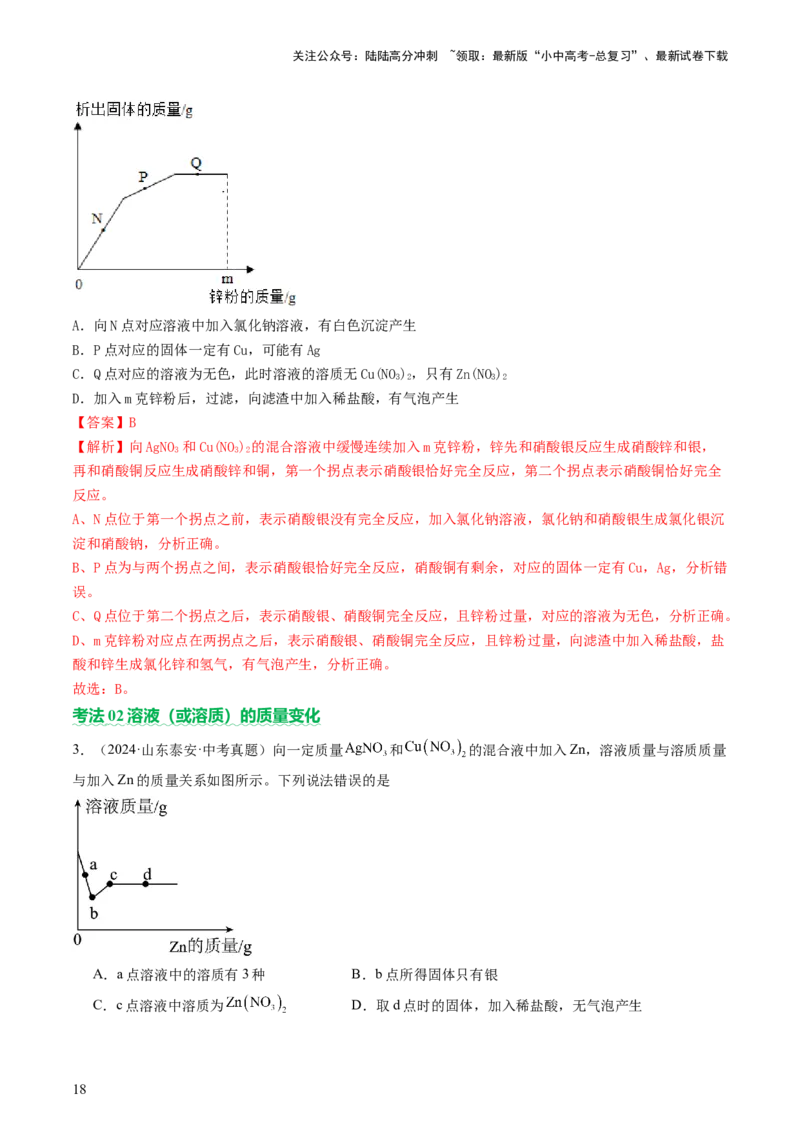
3.(2024·山东泰安·中考真题)向一定质量 和 的混合液中加入Zn,溶液质量与溶质质量
与加入Zn的质量关系如图所示。下列说法错误的是
A.a点溶液中的溶质有3种 B.b点所得固体只有银
C.c点溶液中溶质为 D.取d点时的固体,加入稀盐酸,无气泡产生
18关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
【答案】D
【解析】根据金属活动性Zn>H>Cu>Ag,向一定质量AgNO 和Cu(NO ) 混合溶液中加入Zn,锌先
3 3 2
与AgNO 反应生成硝酸锌和银,待AgNO 反应完,若还有锌粉,锌才能与Cu(NO ) 反应生成硝酸锌和
3 3 3 2
铜。
A、a点时发生的是Zn与AgNO 溶液反应生成硝酸锌溶液和银,硝酸银还没反应完,a点溶液中的溶质有
3
硝酸银、硝酸锌、硝酸铜三种,故选项说法正确;
B、b点锌和硝酸银恰好完全反应,则得到的固体为Ag,故选项说法正确;
C、c点时,硝酸银和硝酸铜恰好完全反应,此时的溶质只有反应产物硝酸锌,故选项说法正确;
D、d点时,加入的锌过量,此时固体为锌、铜和银,加入稀盐酸后,锌会和稀盐酸反应生成氢气,会产生
气泡,故选项说法错误;
故选:D。
4.(2024·广西梧州·一模)向一定质量的Cu(NO ) 和AgNO 的混合溶液中逐渐加入锌粉。反应过程中
3 2 3
溶质Cu(NO ) 的质量随加入锌粉质量的变化关系如图所示。下列说法错误的是
3 2
A.a点时,溶液的总质量与反应前相比减小
B.b点时,溶液为Cu(NO )、AgNO 和Zn(NO ) 的混合溶液
3 2 3 3 2
C.c点时,溶液呈蓝色
D.d点时,过滤所得滤渣为Cu和Ag的混合物
【答案】B
【解析】根据金属活动性:Zn>H>Cu>Ag,向一定质量的Cu(NO ) 和AgNO 的混合溶液中逐渐加入锌
3 2 3
粉,锌先与硝酸银反应生成银和硝酸锌,化学方程式为: ;待硝酸银完全反
应后,锌再与硝酸铜反应生成铜和硝酸锌,化学方程式为: 。
A、a点时,硝酸铜的质量没有改变,表示硝酸银没有完全反应,根据化学方程式
可知,每65份质量的锌能置换出216份质量的银,反应后固体质量增加,
根据质量守恒定律,反应后溶液质量减小,选项说法正确;
B、b点表示硝酸银完全反应,硝酸铜没有参加反应,此时溶液为硝酸铜、硝酸锌的混合溶液,选项说法错
误;
C、c点时,硝酸铜的质量还在继续减小,此时硝酸银完全反应,硝酸铜部分参加反应,溶液为Zn(NO )
3
和Cu(NO ) 的混合溶液,溶液呈蓝色,选项说法正确;
2 3 2
D、d点时,锌和硝酸铜恰好完全反应,过滤所得滤渣为Cu和Ag的混合物,选项说法正确;
19关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
故选:B。
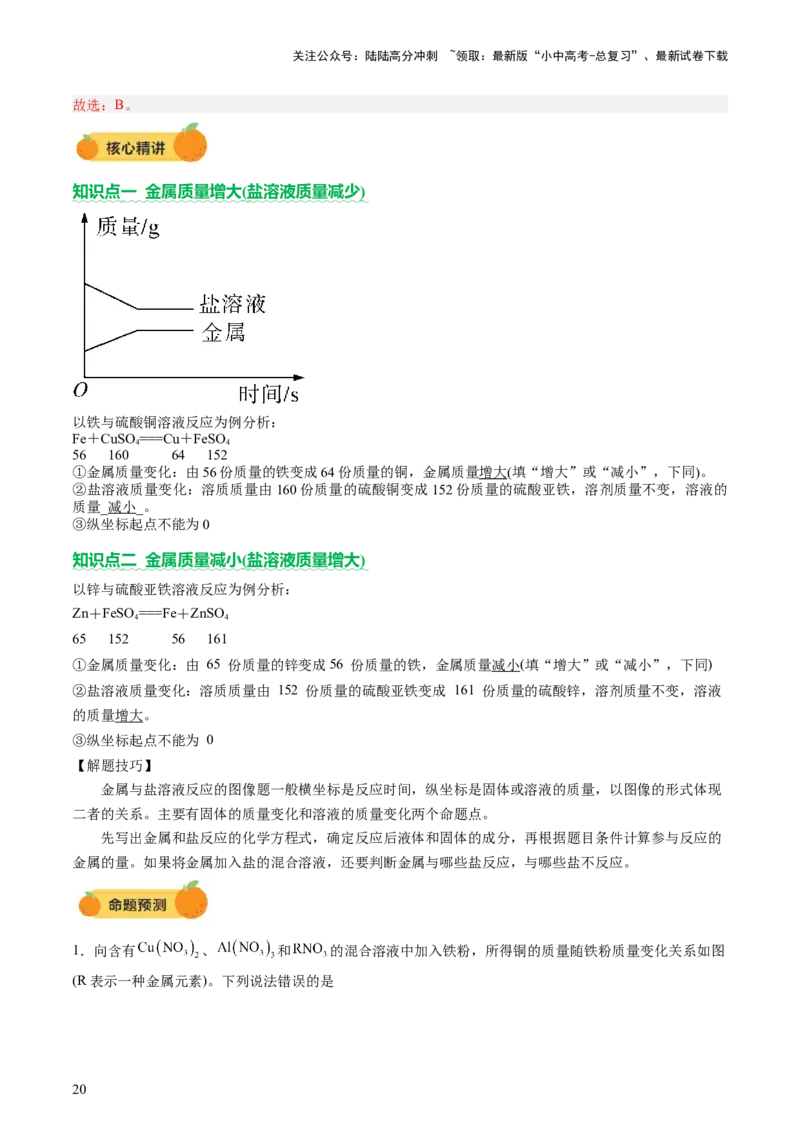
知识点 一 金属质量增大 ( 盐溶液质量减少 )
以铁与硫酸铜溶液反应为例分析:
Fe+CuSO ===Cu+FeSO
4 4
56 160 64 152
①金属质量变化:由56份质量的铁变成64份质量的铜,金属质量增大(填“增大”或“减小”,下同)。
②盐溶液质量变化:溶质质量由160份质量的硫酸铜变成152份质量的硫酸亚铁,溶剂质量不变,溶液的
质量_减小_。
③纵坐标起点不能为0
知识点 二 金属质量减小 ( 盐溶液质量增大 )
以锌与硫酸亚铁溶液反应为例分析:
Zn+FeSO ===Fe+ZnSO
4 4
65 152 56 161
①金属质量变化:由 65 份质量的锌变成56 份质量的铁,金属质量减小(填“增大”或“减小”,下同)
②盐溶液质量变化:溶质质量由 152 份质量的硫酸亚铁变成 161 份质量的硫酸锌,溶剂质量不变,溶液
的质量增大。
③纵坐标起点不能为 0
【解题技巧】
金属与盐溶液反应的图像题一般横坐标是反应时间,纵坐标是固体或溶液的质量,以图像的形式体现
二者的关系。主要有固体的质量变化和溶液的质量变化两个命题点。
先写出金属和盐反应的化学方程式,确定反应后液体和固体的成分,再根据题目条件计算参与反应的
金属的量。如果将金属加入盐的混合溶液,还要判断金属与哪些盐反应,与哪些盐不反应。
1.向含有 、 和 的混合溶液中加入铁粉,所得铜的质量随铁粉质量变化关系如图
(R表示一种金属元素)。下列说法错误的是
20关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
A.金属R的活动性比铜弱
B.b点所得溶液中一定含有 、
C.b点所得铜的质量为6.4g
D.a点时,所得溶液中含有3种溶质
【答案】C
【解析】A、由于金属活动性顺序:Al>Fe>Cu,则铁能和硝酸铜反应生成铜和硝酸亚铁,不能和硝酸铝反
应,但由图可知,刚开始时没有铜生成,说明开始时铁和RNO 反应,则说明金属R的活动性比铜弱,该
3
选项说法正确;
B、b点表示铁和硝酸铜恰好完全反应,则此时溶液中的溶质为硝酸铝和硝酸亚铁,该选项说法正确;
C、由于 ,则5.6g铁完全和硫酸铜反应时,生成铜的质量为6.4g,但由
图可知,刚开始时,铁和RNO 反应,则生成的铜的质量小于6.4g,该选项说法不正确;
3
D、a点时,表示铁和硝酸铜反应,但此时硝酸铜还未完全反应,则所得溶液中的溶质有硝酸铜、硝酸铝和
硝酸亚铁,共三种,该选项说法正确。
故选C。
2.烧杯中现有质量为11.2g的铁,先逐滴向烧杯中加入一定量的Cu(NO) 溶液,充分反应后再逐滴加入
3 2
AgNO 溶液,剩余固体质量与所加溶液总质量的关系如图所示。下列说法正确的是
3
A.A点剩余固体中Cu的质量为mg B.AB段发生的是Cu和AgNO 溶液的反应
1 3
C.C点溶液中的溶质为Fe(NO) 和AgNO D.m 对应的数值为43.2
3 2 3 2
【答案】D
【解析】先向烧杯中加入一定量的硝酸铜溶液,铁和硝酸铜反应生成硝酸亚铁和铜,充分反应后,逐滴加
入硝酸银溶液,由图可知,加入硝酸银溶液后,出现两个拐点,说明铁和硝酸铜反应后,铁剩余,金属活
动性:Fe>Cu>Ag,加入硝酸银溶液,铁先与硝酸银反应生成硝酸亚铁和银,待铁完全反应后,铜和硝酸
21关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
银反应生成硝酸铜和银。
A、由分析可知,A点剩余固体为反应生成的铜和剩余的铁,故A点剩余固体中铜的质量小于mg,不符合
1
题意;
B、由分析可知,AB段发生的反应为铁和硝酸银反应生成硝酸亚铁和银,不符合题意;
C、C点时,铜和硝酸银恰好完全反应,铁和硝酸银反应生成了硝酸亚铁和银,铜和硝酸银反应生成了硝酸
铜和银,故此时溶液中的溶质为硝酸亚铁和硝酸铜,不符合题意;
D、烧杯中现有质量为11.2g的铁,先逐滴向烧杯中加入一定量的硝酸铜,铁和硝酸铜反应:
,待完全反应后,加入硝酸银,铁和硝酸银反应:
,铜和硝酸银反应: ,由此可知,m 对应的剩余
2
固体的质量相当于11.2g铁和硝酸银完全反应生成银的质量,则m 对应的数值为:
2
,符合题意。
故选D。
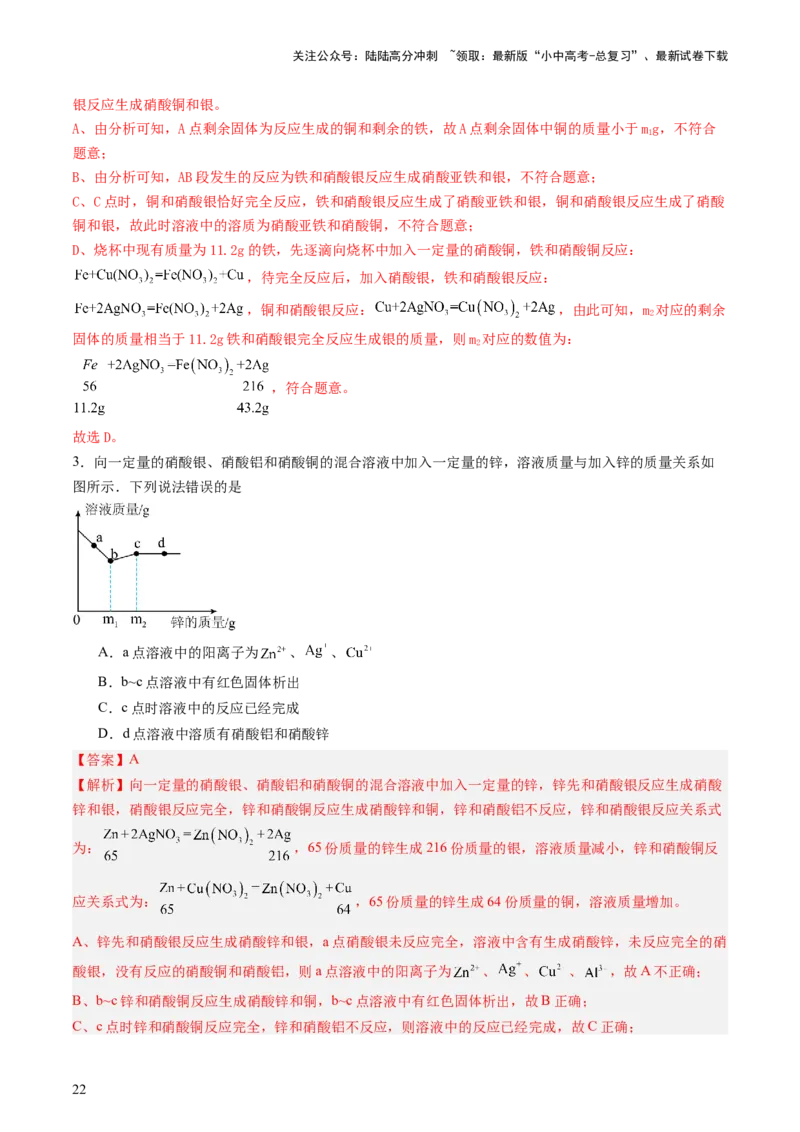
3.向一定量的硝酸银、硝酸铝和硝酸铜的混合溶液中加入一定量的锌,溶液质量与加入锌的质量关系如
图所示.下列说法错误的是
A.a点溶液中的阳离子为 、 、
B.b~c点溶液中有红色固体析出
C.c点时溶液中的反应已经完成
D.d点溶液中溶质有硝酸铝和硝酸锌
【答案】A
【解析】向一定量的硝酸银、硝酸铝和硝酸铜的混合溶液中加入一定量的锌,锌先和硝酸银反应生成硝酸
锌和银,硝酸银反应完全,锌和硝酸铜反应生成硝酸锌和铜,锌和硝酸铝不反应,锌和硝酸银反应关系式
为: ,65份质量的锌生成216份质量的银,溶液质量减小,锌和硝酸铜反
应关系式为: ,65份质量的锌生成64份质量的铜,溶液质量增加。
A、锌先和硝酸银反应生成硝酸锌和银,a点硝酸银未反应完全,溶液中含有生成硝酸锌,未反应完全的硝
酸银,没有反应的硝酸铜和硝酸铝,则a点溶液中的阳离子为 、 、 、 ,故A不正确;
B、b~c锌和硝酸铜反应生成硝酸锌和铜,b~c点溶液中有红色固体析出,故B正确;
C、c点时锌和硝酸铜反应完全,锌和硝酸铝不反应,则溶液中的反应已经完成,故C正确;
22关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
D、d点硝酸银和硝酸铜已反应完全均生成硝酸锌,锌和硝酸铝不反应,则d点溶液中溶质有硝酸铝和硝酸
锌,故D正确;
故选A。
4.向一定质量AgNO 和Cu(NO ) 的混合溶液中加入锌粉,溶液质量与加入锌粉的质量关系如图所示。下
3 3 2
列说法错误的是
A.a点溶液中的溶质有3种 B.取c点的固体,加入稀盐酸,有气泡产生
C.若取b~c段溶液,滴加稀盐酸,无白色沉淀产生 D.d点溶液中溶质为Zn(NO )
3 2
【答案】B
【解析】在金属活动性顺序中,Zn>Cu>Ag,所以向一定质量AgNO 和Cu(NO ) 的混合溶液中加入Zn粉,
3 3 2
锌粉先与AgNO 发生置换反应 ,每65份质量的Zn置换出216份质量的Ag,
3
固体质量增大,则溶液质量减小。锌粉将Ag置换完之后,若锌粉充足,则锌粉与Cu(NO ) 发生置换反应
3 2
,每65份质量的Zn置换出64份质量的Cu,固体质量减小,则溶液质量增大。
A、根据图象,从反应开始直到b点,溶液质量减小,说明是锌粉与AgNO 发生置换反应,在a点时,
3
AgNO 没有全部参加反应,溶液中含有AgNO、Cu(NO ) 和生成的Zn(NO ),溶质是3种,A正确;
3 3 3 2 3 2
B、b~c段溶液质量增加,说明是锌粉与Cu(NO ) 发生置换反应,c点是锌粉刚好将Cu(NO ) 置换完,则溶
3 2 3 2
质只有Zn(NO ),固体有Ag、Cu,这三种物质无法与稀盐酸反应,所以没有气泡产生,B错误;
3 2
C、b~c段溶液质量增加,说明是锌粉与Cu(NO ) 发生置换反应,而此时AgNO 已在a~b段被置换完,溶
3 2 3
液中没有AgNO,滴加稀盐酸,无白色沉淀产生,C正确;
3
D、d点时锌过量,溶液中的溶质只有Zn(NO ),D正确。
3 2
故选:B。
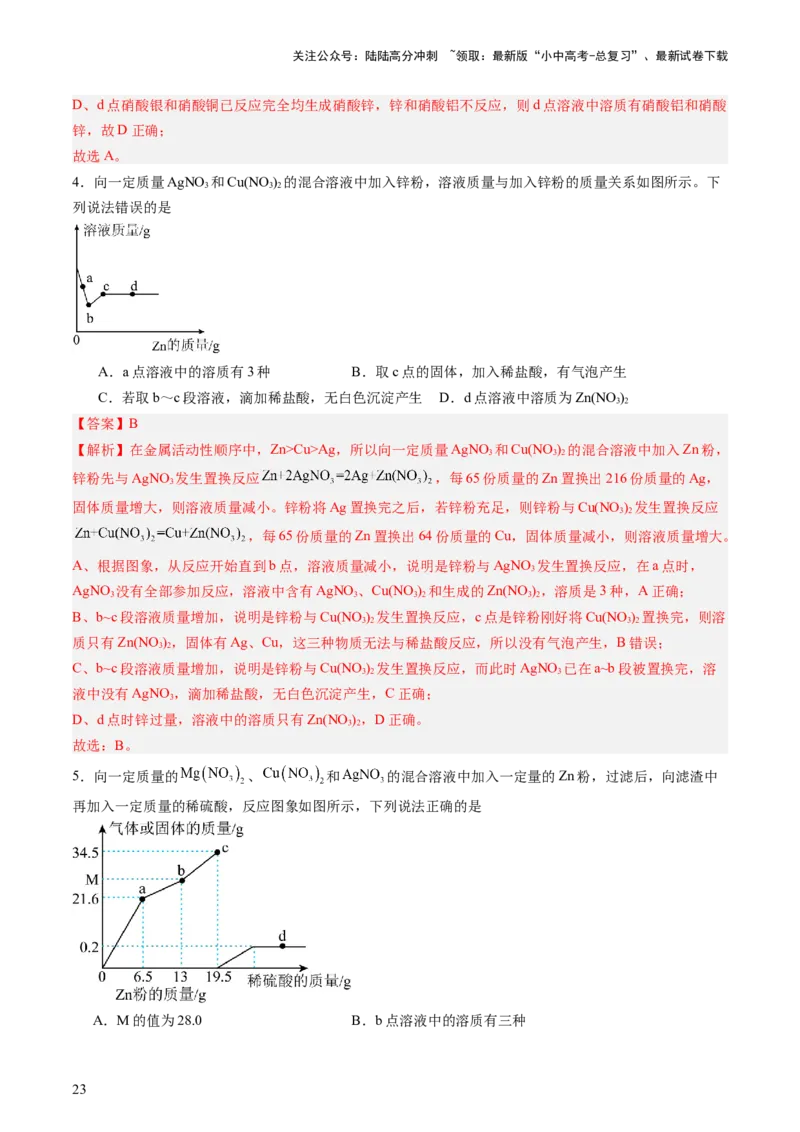
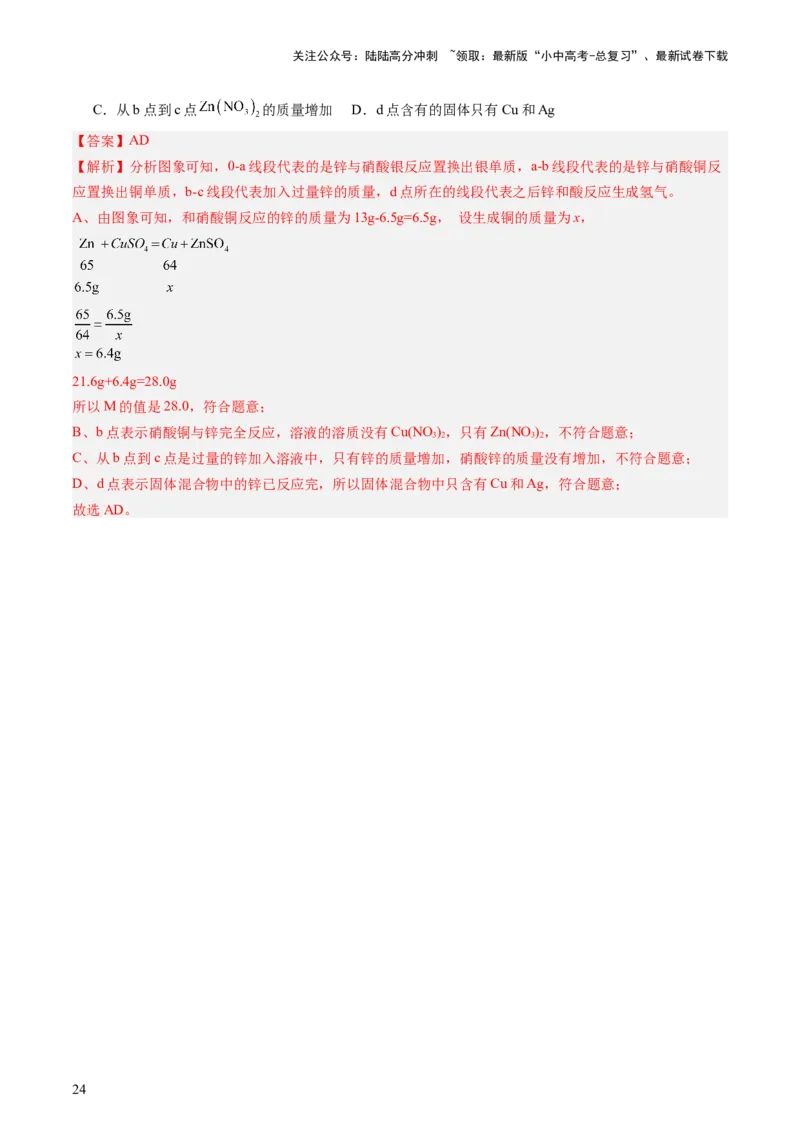
5.向一定质量的 、 和 的混合溶液中加入一定量的Zn粉,过滤后,向滤渣中
再加入一定质量的稀硫酸,反应图象如图所示,下列说法正确的是
A.M的值为28.0 B.b点溶液中的溶质有三种
23关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
C.从b点到c点 的质量增加 D.d点含有的固体只有Cu和Ag
【答案】AD
【解析】分析图象可知,0-a线段代表的是锌与硝酸银反应置换出银单质,a-b线段代表的是锌与硝酸铜反
应置换出铜单质,b-c线段代表加入过量锌的质量,d点所在的线段代表之后锌和酸反应生成氢气。
A、由图象可知,和硝酸铜反应的锌的质量为13g-6.5g=6.5g, 设生成铜的质量为x,
21.6g+6.4g=28.0g
所以M的值是28.0,符合题意;
B、b点表示硝酸铜与锌完全反应,溶液的溶质没有Cu(NO ),只有Zn(NO ),不符合题意;
3 2 3 2
C、从b点到c点是过量的锌加入溶液中,只有锌的质量增加,硝酸锌的质量没有增加,不符合题意;
D、d点表示固体混合物中的锌已反应完,所以固体混合物中只含有Cu和Ag,符合题意;
故选AD。
24