文档内容
氮及其化合物
【教学目标】
(1)掌握氮的重要性质,了解氮在我们生活中的重要用途。
(2)掌握氮的氧化物的性质,氮的重要化合物的用途及硝酸的相关注意事
项。
(3)掌握氮族元素的性质,理解氮族元素原子结构与性质递变规律。
【教学重点】
氮及其重要化合物的性质及转化
【教学难点】
氮及其重要化合物的性质及相关实验
【教学过程】
一、导入
我们上节课学习了硫的相关性质,掌握非金属元素的学习方法,那我们又
知道空气中含量最多的元素为氮气,这节课我们就带着已有的学习方法,对氮
及其化合物知识展开学习!
二、知识讲解
使用建议说明:《氮及其化合物》知识内容丰富,涉及面广,是高考命题
的热点内容之一。试题常以氮元素及其化合物知识为载体,考查基本概念、基
本理论、实验、计算等,具有较强的综合性。
考点1 氮气、氮的氧化物、硝酸
使用建议说明:考纲要求了解氮及其化合物的主要性质;了解氮的氧化物
及其对环境的影响;了解硝酸的主要性质;通过浓硫酸、硝酸分别与不活泼金
属、非金属的反应,认识浓硫酸、硝酸的强氧化性;通过比较浓硫酸与稀硫酸,
浓硝酸与稀硝酸性质的差异,认识浓度、反应条件对反应产物的影响。
一、氮气( )
(1)分子结构:电子式为 ,结构式为 ,氮氮叁键键能大,
分子结构稳定,化学性质不活泼。(2)物理性质:纯净的氮气是无色无味的气体,难溶于水,空气中约占总
体积的78%。
(3)化学性质:常温下性质稳定,可作保护气;但在高温、放电、点燃等
条件下能与 、 、IIA族的Mg、Ca等发生化学反应,即发生氮的固定(将
空气中的氮气转变为含氮化合物的过程,有自然固氮和人工固氮两种形式)。
中N元素0价,为N的中间价态,既有氧化性又有还原性。
①与 反应:
②与 反应:
③与活泼金属反应:
(4)氮气的用途:化工原料;液氮是火箭燃烧的推进剂;还可用作医疗、
保护气等。
二、氮的氧化物
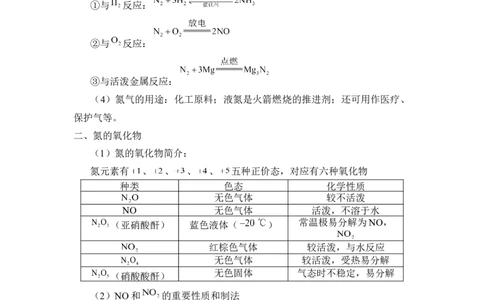
(1)氮的氧化物简介:
氮元素有 、 、 、 、 五种正价态,对应有六种氧化物
种类 色态 化学性质
无色气体 较不活泼
NO 无色气体 活泼,不溶于水
(亚硝酸酐) 蓝色液体( )
常温极易分解为NO,
红棕色气体 较活泼,与水反应
无色气体 较活泼,受热易分解
无色固体 气态时不稳定,易分解
(硝酸酸酐)
(2)NO和 的重要性质和制法
①性质: (易被氧气氧化,无色气体转化为红棕色);
(平衡体系);
(工业制硝酸);(尾气吸收);
有较强的氧化性,能使湿润的KI淀粉试纸变蓝。
②制法:NO: (必须________
法收集NO);
: (必须___________法收
集 )
(3)氮的氧化物溶于水的计算
① 或 与 ( 非 ) 的 混 合 气 体 溶 于 水 可 依 据
利用气体体积变化差值进行计算。
② 和O 的混合气体溶于水时由 进行计算,
2
当体积比 时,恰好反应; 时, 过量,剩余NO;
时, 过量,剩余 。
③NO和 同时通入水中时,由 进行计算,原
理同②。
④NO、 、 的混合气体通入水中,先按①求出NO的体积,再加上
混合气体中NO的体积再按③方法进行计算。
三、硝酸( )
(1)物理性质:
无色、刺激性气味、易挥发液体,能与水以任意比例互溶,常用浓硝酸的
质量分数大约为69%。
(2)化学性质
硝酸为强酸,具有以下性质:
①具有酸的通性;②不稳定性: ;
③强氧化性:无论浓、稀硝酸均具有强氧化性,与金属反应时不放出氢气。
A、与金属反应: ;
3;
;
常温下浓硝酸与铁、铝发生钝化。
B.与非金属反应: 。
C.与其他还原剂反应,如H S、SO 、Fe2+等。
2 2
D.与有机物反应:硝化反应、酯化反应、与蛋白质发生颜色反应等。
(3)制法
①实验室制法:硝酸盐与浓硫酸微热,
(不能用强热和稀硫酸);
②工业制法:氨的催化氧化法, ;
; ;
尾气处理:
(4)用途:制硝酸盐、氮肥、炸药、染料等。
考点2 氨气和铵盐
使用建议说明:氨气与铵盐部分是常考内容,考纲要求了解氨气的主要性
质及其应用,了解氨气的实验室制法,了解铵盐的主要性质及其应用。所以此
处内容大家再授课时务必要注重学生基础知识掌握的把控。
1、氨气( )
(1)分子结构:由极性键形成的三角锥形的极性分子,N原子有一孤对电子;N为 价,为N元素的最低价态;
(2)物理性质:无色、刺激性气味的气体,密度比空气小,极易溶于水,
常温常压下1体积水能溶解700体积的氨气,易液化(可作致冷剂);
(3)化学性质:
①与 反应: ,
溶液呈弱碱性,氨水的成份为: 、 、 、 、 、
,氨水易挥发;
②与酸反应: , (有白烟生成);
③还原性(催化氧化):
(N为 价,最低价态,具有还原性);
(4)实验室制法 ;
工业上采取 与 在高温高压催化剂条件下合成氨气;
(5):化工原料,制硝酸、氮肥等,作致冷剂。
2、铵盐
(1)物理性质:白色晶体,易溶于水;
(2)化学性质:
①受热分解: ( 以上可分解),
;
②与碱反应: ,
铵盐与碱溶液反应的离子方程式: (该性质可用
于氨气的制取和铵根离子的检验)。
三、例题精析使用建议说明:此处内容主要用于教师课堂的精讲,每个题目结合试题本
身、答案和解析部分,教师有的放矢的进行讲授或与学生互动练习。
例题1只用一种试剂就能将 、 、 、 四种溶液
区分开,这种试剂是( )
A. 溶液 B. 溶液
C. 溶液 D. 溶液
【答案】C
【解析】分析四种盐溶液,两种铵盐,可以用碱液区分,两种硫酸盐都可
用 区分,故选用 即可区分。
例题2下列关系图中,A是一种正盐,B是气态氢化物,C是单质,F是强
酸。当X无论是强酸还是强碱时都有如下转化关系(其他反应产物及反应所需
条件均已略去),当X是强碱时,过量的B跟 反应除生成C外,另一产物是
盐酸盐。
――→――→――→――→――→
下列说法中不正确的是( )
A.当 X 是强酸时,A、B、C、D、E、F 中均含同一种元素,F 可能是
B.当X是强碱时,A、B、C、D、E、F中均含同一种元素,F是
C.B和 的反应是氧化还原反应
D.当X是强酸时,C在常温下是气态单质
【答案】D
【解析】A是正盐,既可以与强酸反应又可以与强碱反应,并且生成产物 B
都是氢化物,A必须是铵盐,B如果是酸根离子形成的氢化物能与 反应,说
明其有还原性,有还原性的氢化物常见的是 ,故A是 ,A项,当X
是强酸时,B就是 ,那么C是S,D是 ,E是 ,F就是 ,A对;
B项,当X是强碱时,B就是 ,C就是 ,D就是NO,E就是 、F就
是 ,故B对;C项,不管B是 还是 ,与氯气发生的都是氧化还原
反应,C对;D项,当X是强酸时C是S,是固态单质,D错。
例题3物质的量之比为 的锌与稀硝酸反应,若硝酸被还原的产物为 ,
反应结束后锌没有剩余,则该反应中被还原的硝酸与未被还原的硝酸的物质的
量之比是( )A. B.
C. D.
【答案】A
【解析】设 参与反应,因Zn无剩余,则最终生成了 ,
显然含有 ,这部分是没有参与氧化还原反应的 ; 过
程 中 N 元 素 的 化 合 价 价 → 价 , 根 据 得 失 电 子 守 恒 有 :
,则 ,即有1MOLHNO 被还原。
3
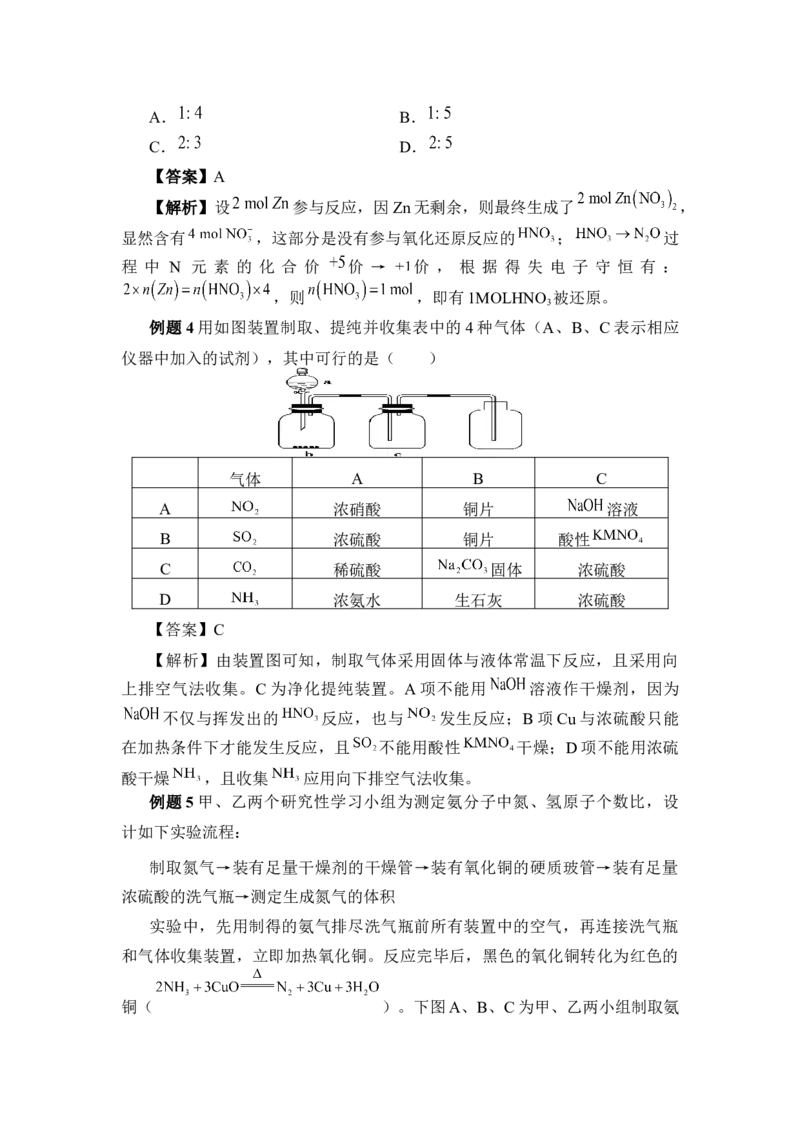
例题4用如图装置制取、提纯并收集表中的4种气体(A、B、C表示相应
仪器中加入的试剂),其中可行的是( )
气体 A B C
A 浓硝酸 铜片 溶液
B 浓硫酸 铜片 酸性
C 稀硫酸 固体 浓硫酸
D 浓氨水 生石灰 浓硫酸
【答案】C
【解析】由装置图可知,制取气体采用固体与液体常温下反应,且采用向
上排空气法收集。C为净化提纯装置。A项不能用 溶液作干燥剂,因为
不仅与挥发出的 反应,也与 发生反应;B项Cu与浓硫酸只能
在加热条件下才能发生反应,且 不能用酸性 干燥;D项不能用浓硫
酸干燥 ,且收集 应用向下排空气法收集。
例题5甲、乙两个研究性学习小组为测定氨分子中氮、氢原子个数比,设
计如下实验流程:
制取氮气→装有足量干燥剂的干燥管→装有氧化铜的硬质玻管→装有足量
浓硫酸的洗气瓶→测定生成氮气的体积
实验中,先用制得的氨气排尽洗气瓶前所有装置中的空气,再连接洗气瓶
和气体收集装置,立即加热氧化铜。反应完毕后,黑色的氧化铜转化为红色的
铜( )。下图A、B、C为甲、乙两小组制取氨气时可能用到的装置,D为盛有浓硫酸的洗气瓶。
甲小组测得:反应前氧化铜的质量 、氧化铜反应后剩余固体的质量 、
生成氮气在标准状况下的体积 。乙小组测得:洗气前装置D的质量 、洗
气后装置D的质量 、生成氮气在标准状况下的体积 。
请回答下列问题:
(1)写出仪器A的名称:________。
(2)甲、乙两小组选择了不同的方法制取氨气,请将实验装置的字母编号
和制备原理填写在下表的空格中。
实验装置 实验药品 制备原理
反应的化学方程式
氢氧化钙、硫酸 为
甲小组 A
铵 ①______________
________________
氢氧化钠溶于氨水
②______________ 浓氨水、氢氧化 后放热,增加氢氧
乙小组
________________ 钠 根浓度,加快氨气
逸出
(3)甲小组用所测得数据计算出氨分子中氮、氢的原子个数之比为
________。
(4)乙小组用所测得数据计算出氨分子中氮、氢的原子个数比明显小于理
论 值 , 其 原 因 是
________________________________________________________
_____________________________________________________________________
。
【答案】(1)圆底烧瓶
(2)①
②B(3)
(4)浓硫酸吸收了未反应的氨气,从而使计算的氢的含量偏高
【解析】(1)仪器A的名称为圆底烧瓶。(2)①氢氧化钙与硫酸铵反应生
成 硫 酸 钙 、 氨 气 和 水 , 反 应 的 化 学 方 程 式 为
;②浓氨水是液体,氢氧化钠是
固体,为使氨气逸出,把氨水滴入固体氢氧化钠中,随着氢氧化钠溶解放热,
氨气挥发放出气体,故选B装置。(3)反应前氧化铜的质量为 、氧化铜反
应后转化成的铜的质量为 ,则氧化铜中氧元素的质量为 ,生成的
水中氧元素的质量等于参加反应氧化铜中氧元素的质量,则生成的水中氧原子
的个数为 ;水中氢原子个数是氧原子个数的两倍,因此氢原子个
数为 ,生成的氮气在标准状况下的体积为 ,则氮气中氮原
子 的 个 数 为 ; 因 此 氮 、 氢 原 子 个 数 比 为
。(4)乙小组用所测数据计算出氨
分子中氮、氢的原子个数比小于理论值,其原因是洗气瓶 D中的浓硫酸不但吸
收了反应生成的水,还吸收了未反应的氨气,从而使计算的氢的量偏高。
四、课堂运用使用建议说明:在对课堂知识讲解完,把握了重点突破了难
点以及练习精讲了之后,再用练习马上进行课堂检测,根据学生情况建议分 3
个难度层次:易,中,难。
基础
1.氨水显弱碱性的主要原因是( )
A.通常状况下,氨的溶解度不大
B.氨水中的 少量电离
C.溶于水的氨分子只有少量发生电离
D.氨本身的碱性弱
2.物质氧化性、还原性的强弱,不仅与物质的结构有关,还与物质的浓度
和反应温度有关。下列各组物质在反应中的产物与物质的浓度有关的是(
)
①Cu与 溶液②Cu与 溶液③Zn与 溶液④Fe与HCl溶液A.①③ B.③④
C.①② D.①③④
3.下列关于浓硝酸和浓硫酸的叙述中正确的是( )
①常温下都可用铝制容器贮存
②露置在空气中,容器内酸液的质量都减轻
③常温下都能与铜较快反应
④露置在空气中,容器内酸液的浓度都降低
A.①② B.③④
C.②③ D.①④
【答案】
1.B
2.A
3.D
【解析】
1、氨气极易溶于水,溶于水的氨气大部分与水结合成一水合氨(
), 少部分电离成 和 ,因此氨水呈弱碱性。氨气本身不能电
离,也不显碱性。
2、本题考查物质氧化性和还原性的影响因素。铜与浓硝酸反应生成 ,
与稀硝酸反应生成NO,硝酸氧化性的强弱与浓度有关;铜与氯化铁溶液反应,
与浓度和温度无关,产物唯一;锌与硫酸反应:稀硫酸生成氢气,浓硫酸则生
成二氧化硫,硫酸氧化性的强弱与其浓度有关;铁与盐酸反应只生成氯化亚铁
和氢气。
3、常温下,二者均能使铝钝化,①正确;露置在空气中,浓硫酸吸水质量
增加,②错误;浓硫酸在常温下与铜没有明显的反应,③错误;在空气中,浓
硝酸挥发、浓硫酸吸水,二者浓度都降低,④正确。
巩固
4、在下列反应中, 既表现出氧化性,又表现出酸性的是( )
A.
B.C.
D.
5、下列关于氨水的叙述正确的是( )
A.氨水显碱性,是因为氨水是一种弱碱
B.氨水和液氨成分相同
C.氨水中物质的量浓度最大的粒子是 (除水外)
D.1MOL·L-1的氨水指在1L溶液中含 、 、 物质的量之
和为1MOL
6、下列有关实验操作、现象和解释或结论都正确的是( )
选 现
实验操作 解释或结论
项 象
过量的 Fe 粉中加入稀 溶
稀 将 Fe 氧化
A ,充分反应后,滴入 液呈红
为
KSCN溶液 色
无
常温下,Fe、Al 放入浓 Fe、Al 与浓
B 明显现
或浓 中 或浓 发生钝化
象
Al 箔表面被
无
C Al箔插入稀 中 氧化,形成致密的氧化
现象
膜
试
用玻璃棒蘸取浓 点
D 纸变蓝 浓 具有酸性
到红色石蕊试纸上
色
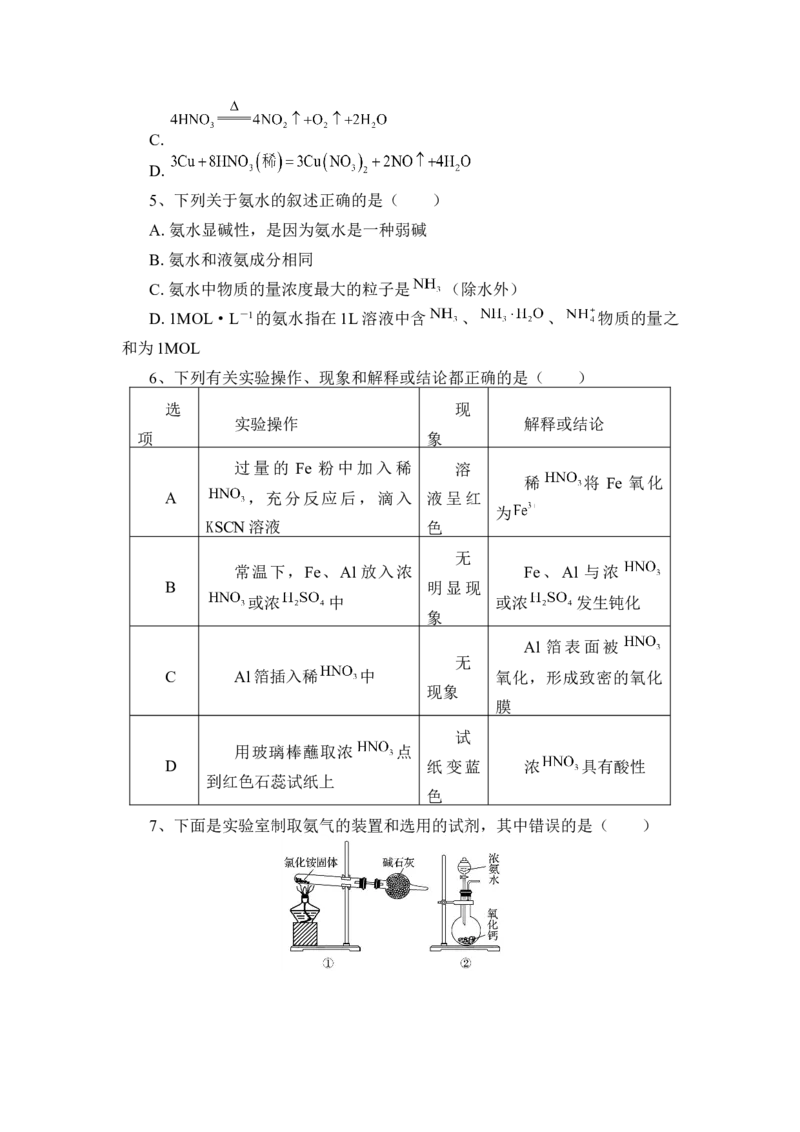
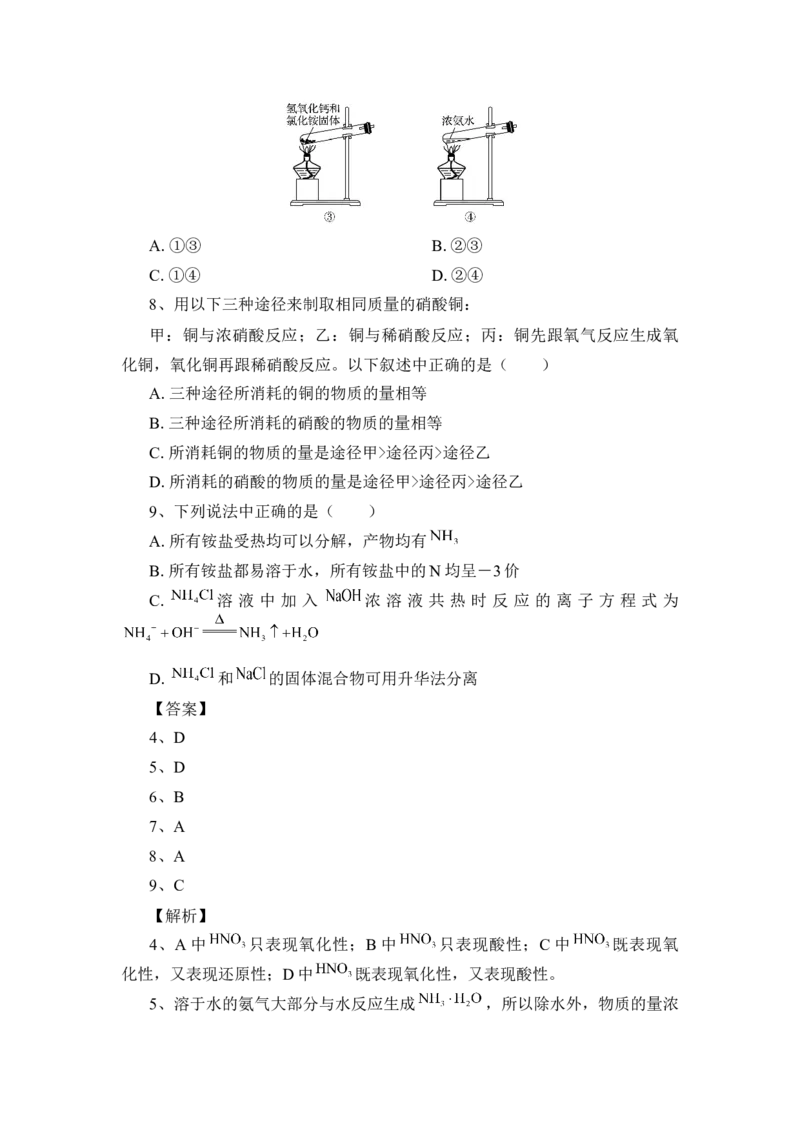
7、下面是实验室制取氨气的装置和选用的试剂,其中错误的是( )A.①③ B.②③
C.①④ D.②④
8、用以下三种途径来制取相同质量的硝酸铜:
甲:铜与浓硝酸反应;乙:铜与稀硝酸反应;丙:铜先跟氧气反应生成氧
化铜,氧化铜再跟稀硝酸反应。以下叙述中正确的是( )
A.三种途径所消耗的铜的物质的量相等
B.三种途径所消耗的硝酸的物质的量相等
C.所消耗铜的物质的量是途径甲>途径丙>途径乙
D.所消耗的硝酸的物质的量是途径甲>途径丙>途径乙
9、下列说法中正确的是( )
A.所有铵盐受热均可以分解,产物均有
B.所有铵盐都易溶于水,所有铵盐中的N均呈-3价
C. 溶 液 中 加 入 浓 溶 液 共 热 时 反 应 的 离 子 方 程 式 为
D. 和 的固体混合物可用升华法分离
【答案】
4、D
5、D
6、B
7、A
8、A
9、C
【解析】
4、A中 只表现氧化性;B中 只表现酸性;C中 既表现氧
化性,又表现还原性;D中 既表现氧化性,又表现酸性。
5、溶于水的氨气大部分与水反应生成 ,所以除水外,物质的量浓度最大的粒子是 ; 是一种弱碱,在水中发生部分电离使溶液
呈碱性;氨水中共含有六种粒子,分别是 、 、 、 、
和少量的H+,是一种混合物,液氨是纯净物。
6、稀硝酸与铁粉反应,铁首先被氧化成 ,过量铁粉将 还原,最终
得到 ,滴入 溶液不显红色,A错误;常温下,Fe、Al在浓 或浓
中发生钝化,生成致密的保护膜阻止了反应进行,B正确;Al箔能与稀
反应放出气体,C错误;浓硝酸具有氧化性,能使红色石蕊试纸先变红后
褪色,D错误。
7、实验室制取氨气的方法有:铵盐与碱加热制取氨气,常用 与
反应,固体与固体反应,因为有水生成,试管口应略向下倾斜,
③错误;在浓氨水中加入CaO,CaO与水反应使溶液中 增大,消耗了水,
并且放出大量的热,使 分解放出氨气,②正确;加热浓氨水,加快氨
气挥发,④正确;①是错误的,因为氯化铵分解生成的 与HCl冷却后又生
成 ,不能得到 。
8、由于制取的 的量相同,据铜原子守恒可知A正确。
9、A项,有的铵盐受热分解产生氨气(如 ),有的铵盐受热分解不
产生氨气(如硝酸铵);D项,可用加热法分离 和某些固体(不分解、
不升华的固体)的混合物,但其过程为先受热分解,再降温化合,而不是升华。
拔高
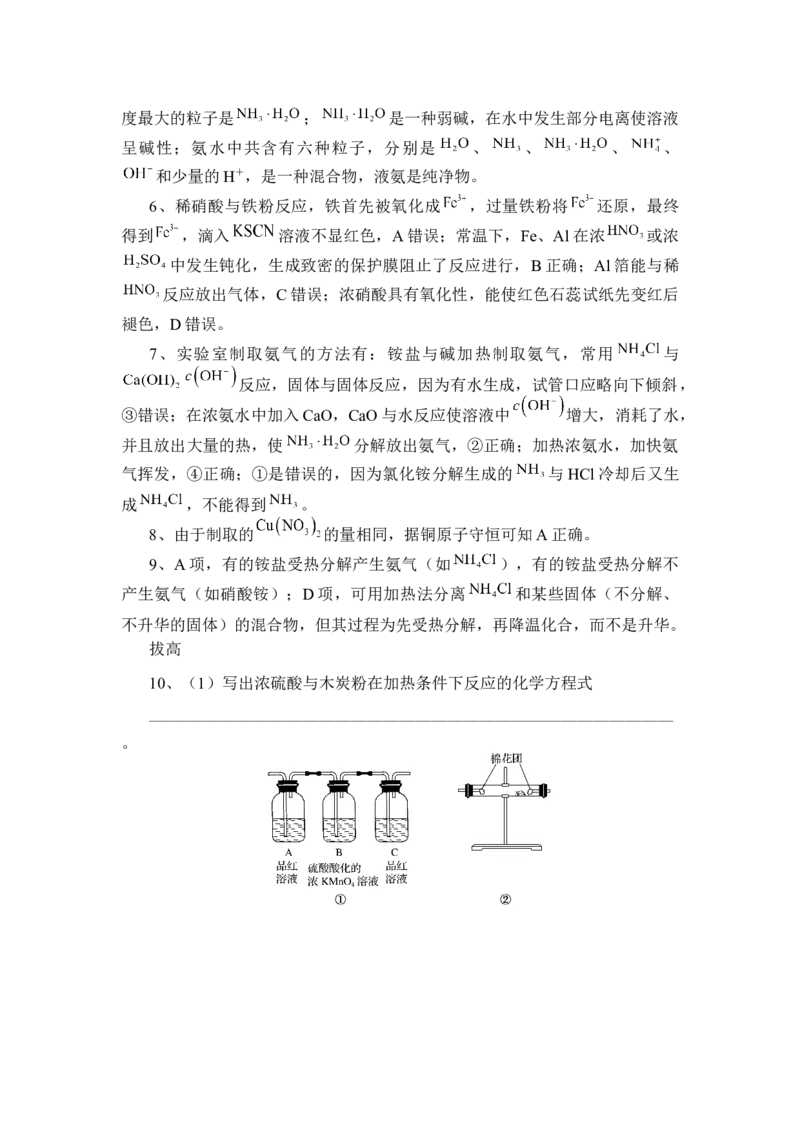
10、(1)写出浓硫酸与木炭粉在加热条件下反应的化学方程式
_________________________________________________________________
。(2)试用上图所示各装置设计一个实验,验证上述反应所产生的各种产物。
这 些 装 置 的 连 接 顺 序 ( 按 产 物 气 体 从 左 至 右 的 流 向 ) 是
________→________→________→________(填装置的编号)。
(3)实验室可观察到装置①中A瓶的溶液褪色,C瓶的溶液不褪色,A瓶
溶液的作用是________,B 瓶溶液的作用是________,C 瓶溶液的作用是
________。
(4)装置②中所加的固体药品是________,可验证的产物是________,确
定 装 置 ② 在 整 套 装 置 中 的 位 置 的 理 由 是
_____________________________________________________________________。
(5)装置③中所盛溶液是________,可验证的产物是________。
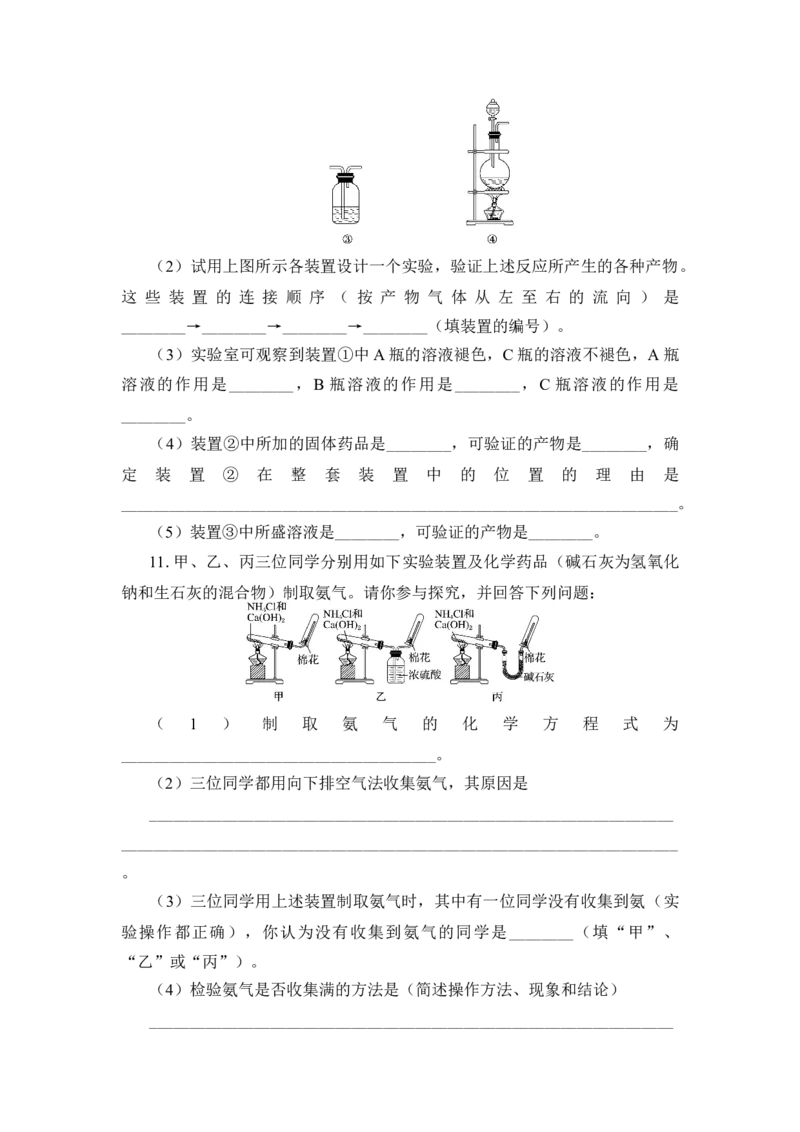
11.甲、乙、丙三位同学分别用如下实验装置及化学药品(碱石灰为氢氧化
钠和生石灰的混合物)制取氨气。请你参与探究,并回答下列问题:
( 1 ) 制 取 氨 气 的 化 学 方 程 式 为
_______________________________________。
(2)三位同学都用向下排空气法收集氨气,其原因是
_________________________________________________________________
_____________________________________________________________________
。
(3)三位同学用上述装置制取氨气时,其中有一位同学没有收集到氨(实
验操作都正确),你认为没有收集到氨气的同学是________(填“甲”、
“乙”或“丙”)。
(4)检验氨气是否收集满的方法是(简述操作方法、现象和结论)
_________________________________________________________________。
(5)三位同学都认为,采用上述各自的装置,还可用于加热碳酸氢铵固体
的方法来制取纯净的氨气,你认为哪位同学能够达到实验目的________(填
“甲”、“乙”或“丙”)。他们还认为,装置中的 固体可用
固体代替,你认为________(填“能”或“不能”)。
12.将 铜置于一定量的浓硝酸中并微热。当铜片完全消失时,共收集到
和NO的混合气体 (标准状况)。
(1)写出上述过程中,有关反应的离子方程式
_________________________________________________________________
、
_________________________________________________________________
、
_________________________________________________________________
。
(2)完成该反应至少需要量取 的浓硝酸________mL。
(3)混合气体中 的体积为
_________________________________________________________________
_______L,NO的体积________L(均为标准状况下)。
(4)将收集上述气体的容器倒扣在盛有水的水槽中,并向其中缓慢通入
使其充分反应,若要使溶液恰好充满容器,则理论上需要参加反应的 的物质
的量为________mol。
【答案】
10.(1)
(2)④
②
①
③
(3)验证 的存在
充分吸收
验证 是否已被吸收完全(4)无水硫酸铜
水
由于产物通过①、③时会带出水蒸气,所以②必须放在①、③之前
(5)澄清的石灰水
11.(1)
(2)氨气的密度比空气小,氨气极易溶于水
(3)乙
(4)用湿润的红色石蕊试纸靠近试管口,如果试纸变蓝,则氨气已满(或
用蘸有浓盐酸的玻璃棒靠近试管口,如果产生白烟,则氨气已满)
(5)丙
不能
12.(1)
(2)600
(3)22.4
22.4
(4)1
【解析】
10.C与浓硫酸发生反应: 。反应中的
生成物有三种: 、 、 。在检验这三种产物时要避免相互干扰,如检
验 时一般用澄清石灰水,而 也会使澄清的石灰水变浑浊,所以在检验
之前必须先除去 ;同时,在气体通过水溶液后,水蒸气会随之带出,所
以必须在通过水溶液之前检验水的存在,由上分析可知装置的连接顺序是
④→②→①→③。
11.(1)实验室用氢氧化钙和氯化铵在加热条件下制备氨气,反应方程式
为 。(2)氨气易溶于水,不能用排
水法收集,氨气密度比空气小,应用向下排空气法收集。(3)氨气为碱性气体,通过盛有浓硫酸的洗气瓶时,与硫酸反应而被吸收,故答案为乙。(4)氨气为
碱性气体,与水反应生成 ,电离出 ,溶液呈碱性,检验时可用湿
润的红色石蕊试纸靠近试管口,如果试纸变蓝,则氨气已满,或用蘸有浓盐酸
的玻璃棒靠近试管口,如果产生白烟,则氨气已满。(5)碳酸氢铵加热分解生
成氨气、二氧化碳和水,其中可用碱石灰吸收二氧化碳和水,只有丙能做到,
氯化铵加热分解生成氨气和氯化氢,在温度较低时又重新生成氯化铵,不能只
用氯化铵制备氨气。
12.(1)首先是浓硝酸与铜发生反应产生硝酸铜、二氧化氮和水,然后当
反应进行到一定程度,硝酸变稀后,稀硝酸与铜发生反应,产生硝酸铜、一氧
化氮和水,反应的离子方程式是 ;
。(2)反应中被还原的 生成
NO、 混合气体,混合气体的物质的量为 ,未被
还原的硝酸生成 , ,由氮原子守恒可知,
,故需要硝酸的
体积 。(3)设混合气体中 、NO的物质
的量分别为 、 ,根据电子转移守恒及二者体积列方程计算,再根据
计算各自的体积;根据电子得失守恒及二者体积,可得:
,解得 、 ,故二氧化氮的体积 ,
NO的体积 。(4)反应又生成 ,分析整个过
程可知,铜提供的电子等于氧气获得的电子,由电子守恒可知,故需要氧气的
物质的量为 。
五、课堂小结
使用建议说明:此处内容主要用于教师对本节课重点内容进行总结,一方
面是对本节课的重点难点内容的回顾,更重要的是针对这节课学生出现的问题
再次进行复习提问等,以达到让学生课上掌握的目的,同时可以对下节课内容
进行简单的铺垫,以体现出本节课内容与下节课内容之间的关系。
学习目标定位:知道 的物理性质特点以及氨水显碱性的原因;学会氨
气的实验室制取、收集和检验方法;学会铵盐的性质及 的检验方法;通过
浓硫酸、硝酸分别与不活泼金属、非金属的反应,认识浓硫酸、硝酸的强氧化性;通过比较浓硫酸与稀硫酸,浓硝酸与稀硝酸性质的差异,认识浓度、反应
条件对反应产物的影响。
1、氮气的性质及用途
2、氮氧化合物的性质
3、氨气的物理性质
4、氨与水的可逆反应
5、氨的催化氧化
6、氨气的制取
7、铵盐的性质
8、硝酸的强氧化性
六、课后作业
使用建议说明:此处内容主要用于教师根据学生掌握情况有针对性的进行
课后作业的布置,掌握好的同学可以适当的布置难度大一些的作业,成绩一般
的同学可以以基础题和巩固题目为主,但是一定要控制作业的数量,给学生布
置的作业一般不要超过5题,这样学生才能保证做题的质量。
基础
1.下列对于硝酸的认识,不正确的是( )
A.浓硝酸和稀硝酸都具有氧化性
B.铜与硝酸的反应属于置换反应
C.金属与硝酸反应不能制取氢气
D.可用铁或铝制容器盛装冷的浓硝酸
2.各取 分别投入足量的下列酸中(必要时可加热):①浓硫酸、
②浓硝酸、③稀硫酸、④稀硝酸,充分反应后在相同条件下得到的气体体积由
大到小的顺序是( )
A.②>④>①>③ B.②>①>④>③
C.①>②>④>③ D.③>④>①>②
3.某同学在实验室中发现了一瓶无色而有刺激性气味的气体,根据气味判
断可能是氨气,但不能确定是氨气。下列提供的方法中,能帮他检验该气体是
否为氨气的是( )
A.将湿润的红色石蕊试纸放在打开的瓶口
B.将湿润的蓝色石蕊试纸放在打开的瓶口C.用蘸有浓硫酸的玻璃棒靠近打开的瓶口
D.将干燥的红色石蕊试纸放在打开的瓶口
【答案】
1.B
2.B
3.A
巩固
4.关于氨的喷泉实验形成的原理解释正确的是( )
A.氨水呈碱性
B.氨气极易溶于水,烧瓶内外形成压强差
C.氨气易液化
D. 溶于水后形成的溶液易挥发
5.下列反应中,说明氨有还原性和碱性的是( )
A.
B.
C.
D.
6.(1)在浓硝酸中放入铜片:
①开始时反应的化学方程式为_______________________________________,
实验现象为_______________________________________________________。
② 若 铜 有 剩 余 , 则 反 应 将 要 结 束 时 反 应 的 化 学 方 程 式 为
________________________________________________________________。
③待反应停止后,再加入少量 25%的稀硫酸,这时铜片上又有气泡产生,
其 原 因 是
______________________________________________________________。
(2)若 粉与一定量浓 反应,当Cu完全反应时,收集到标准
状况下 气体,则消耗硝酸______mol,生成 ______mol。
(3)若向Cu中加入硫酸和硝酸的混酸溶液制取 溶液,则混酸中硫
酸与硝酸的最佳物质的量之比为________。7.如下图所示,图中每一方格表示有关的一种反应物或生成物,其中A、C
为无色气体。请填写下列空白:
(1)物质 X 可以是_____________,C 是______________________,F 是
______________________,G是______________________。
( 2 ) 反 应 ① 的 化 学 方 程 式 是
_________________________________________。
反应②的化学方程式是___________________________________________。
【答案】
4.B
5.B
6.(1)①
铜片逐渐消失,溶液逐渐变绿,有红棕色气体逸出
②
③加入稀硫酸后, 与原溶液中的 构成强氧化性的条件,又能与过量
的Cu反应
(2)0.11
0.015
(3)
7.(1) 或
(2)
拔高8. 铜跟适量的浓硝酸反应,铜全部作用后,共收集到气体
(标准状况),反应消耗的 的物质的量可能是( )
A. B.
C. D.
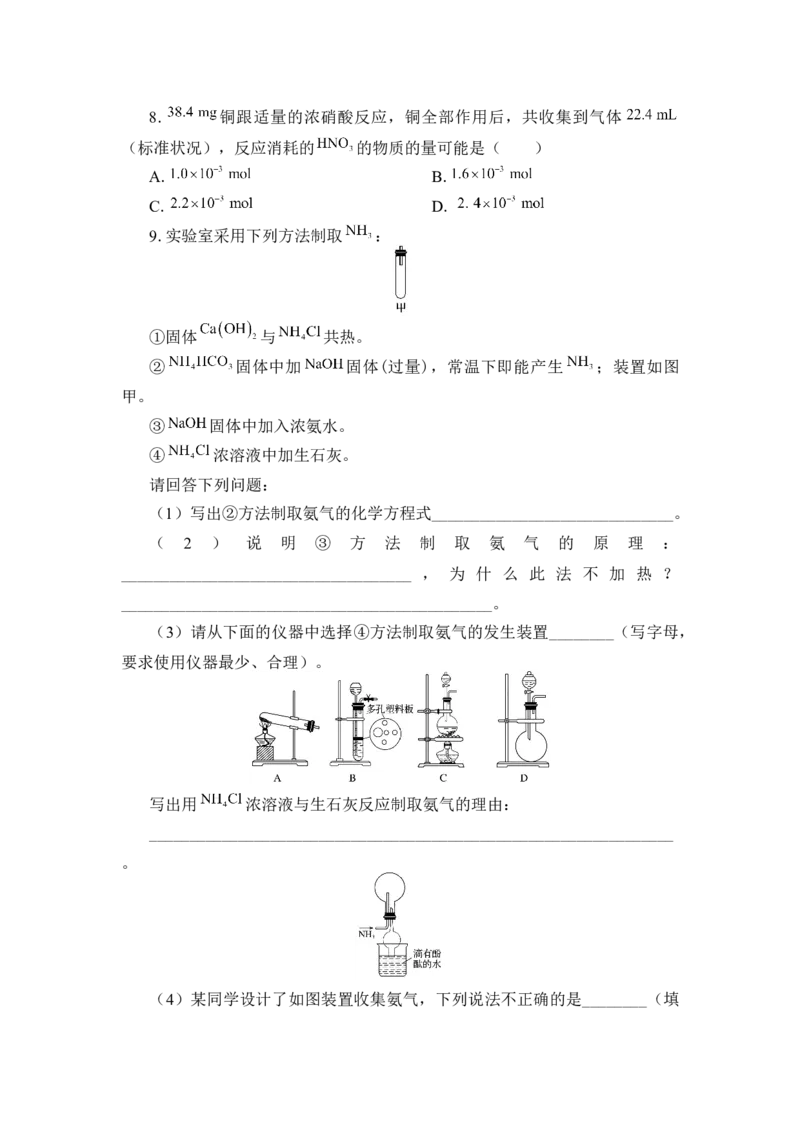
9.实验室采用下列方法制取 :
①固体 与 共热。
② 固体中加 固体(过量),常温下即能产生 ;装置如图
甲。
③ 固体中加入浓氨水。
④ 浓溶液中加生石灰。
请回答下列问题:
(1)写出②方法制取氨气的化学方程式______________________________。
( 2 ) 说 明 ③ 方 法 制 取 氨 气 的 原 理 :
____________________________________ , 为 什 么 此 法 不 加 热 ?
______________________________________________。
(3)请从下面的仪器中选择④方法制取氨气的发生装置________(写字母,
要求使用仪器最少、合理)。
写出用 浓溶液与生石灰反应制取氨气的理由:
_________________________________________________________________
。
(4)某同学设计了如图装置收集氨气,下列说法不正确的是________(填字母)。
A.收集氨气的原理是向下排空气法
B.干燥管的作用是防止倒吸
C.当烧杯中的水变红时证明氨气已收集满
D.该装置会形成红色喷泉
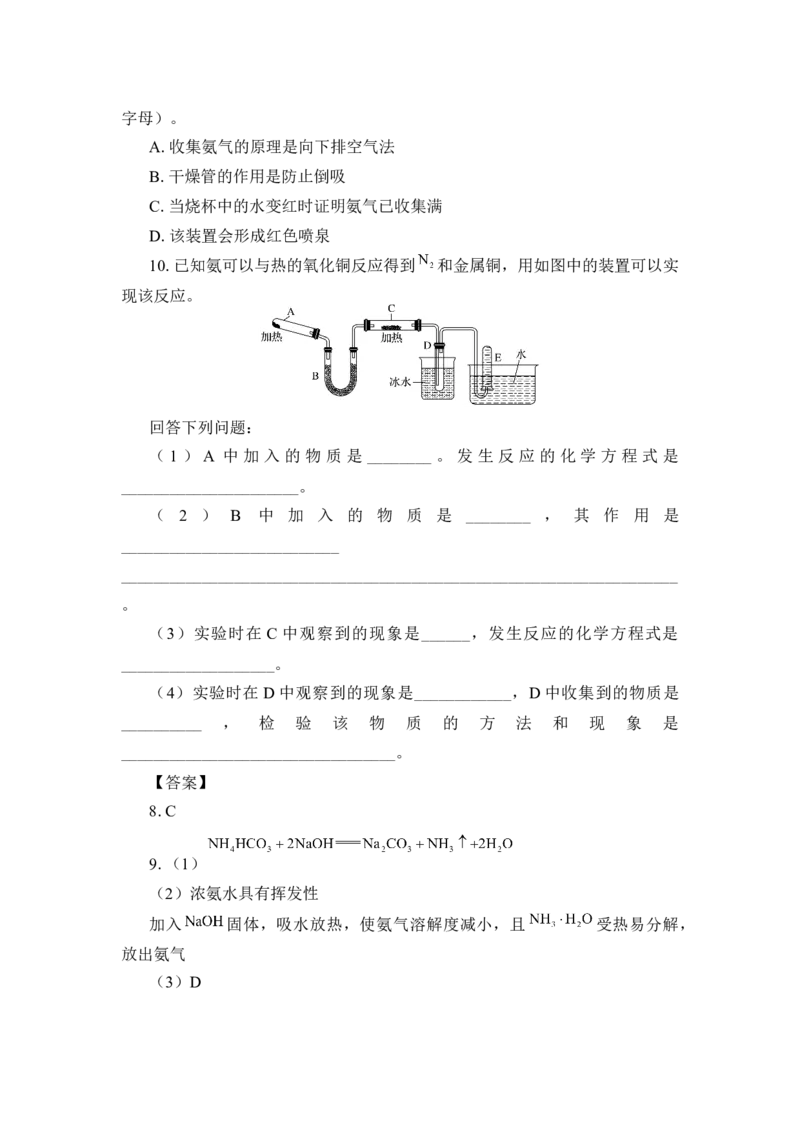
10.已知氨可以与热的氧化铜反应得到 和金属铜,用如图中的装置可以实
现该反应。
回答下列问题:
( 1 ) A 中 加 入 的 物 质 是 ________ 。 发 生 反 应 的 化 学 方 程 式 是
______________________。
( 2 ) B 中 加 入 的 物 质 是 ________ , 其 作 用 是
___________________________
_____________________________________________________________________
。
(3)实验时在 C 中观察到的现象是______,发生反应的化学方程式是
___________________。
(4)实验时在 D中观察到的现象是____________,D中收集到的物质是
__________ , 检 验 该 物 质 的 方 法 和 现 象 是
__________________________________。
【答案】
8.C
9.(1)
(2)浓氨水具有挥发性
加入 固体,吸水放热,使氨气溶解度减小,且 受热易分解,
放出氨气
(3)D,消耗水并放热, 和 受热发生反应:
(4)D
10.(1)固体 和
(其他合理答案也可)
(2)碱石灰(或CaO)
除去 中的水蒸气
(3)黑色粉末变为红色且右管口有水珠出现
(4)出现无色液体
氨水
用湿润的红色石蕊试纸,若变蓝则说明有 存在(也可以用蘸有浓盐酸
的玻璃棒放在容器口,若有白烟出现,也说明有 存在;用无水 ,若
变蓝则说明有水存在)