文档内容
2019-2020学年高一化学期末复习专项提升卷(人教版2019必修第二册)
专项 07 自然资源的开发利用
1.氧化还原反应广泛应用于金属的冶炼。下列说法不正确的是
A.电解熔融NaCl制取金属钠的反应中,钠离子被还原,氯离子被氧化
B.湿法炼铜与火法炼铜的反应中,铜元素都发生还原反应
C.用磁铁矿炼铁的反应中,1 mol Fe O 被CO还原成Fe,转移9 mol e−
3 4
D.铝热法还原铁的反应中,放出的热量能使铁熔化
2.下列关于物质制备原理错误的是
A.工业制备金属钠:2NaCl 2Na+Cl ↑
2
B.工业生产铁:Fe O+3CO Fe+3CO
2 3 2
C.湿法炼铜:Fe+CuSO===Cu+FeSO
4 4
D.以S为原料,工业生产硫酸在沸腾炉中的反应:2S+3O 2SO
2 3
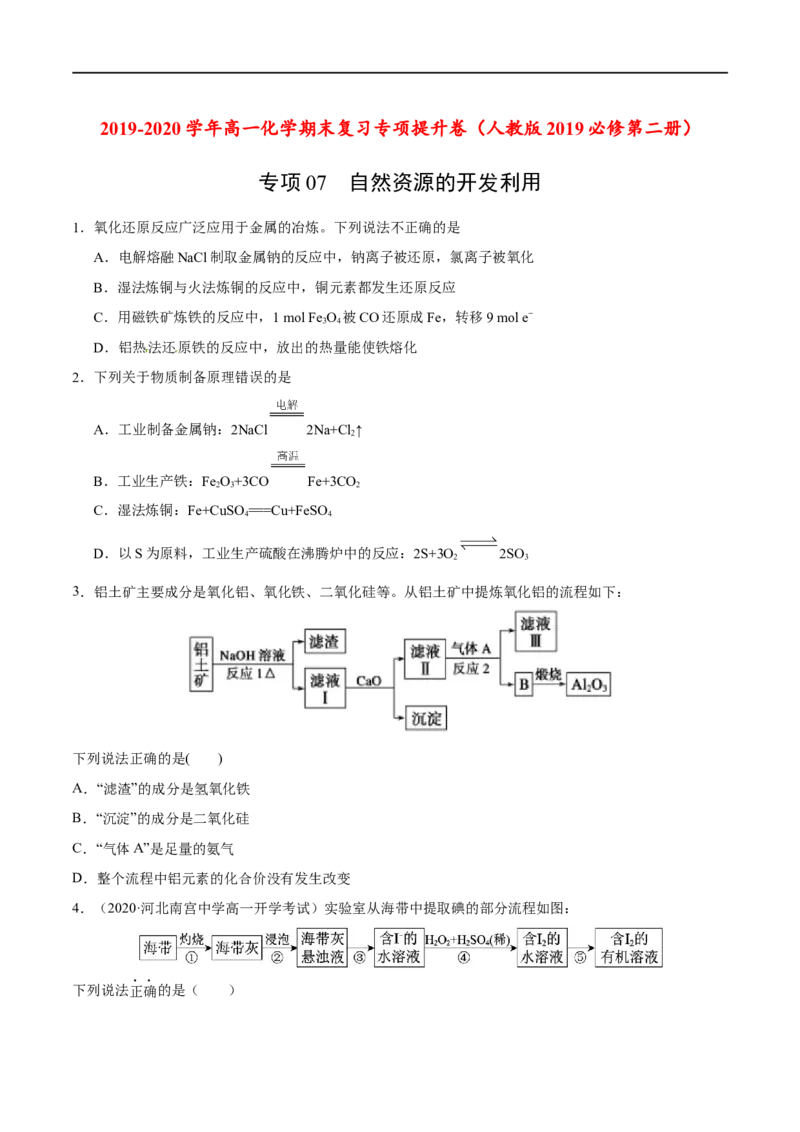
3.铝土矿主要成分是氧化铝、氧化铁、二氧化硅等。从铝土矿中提炼氧化铝的流程如下:
下列说法正确的是( )
A.“滤渣”的成分是氢氧化铁
B.“沉淀”的成分是二氧化硅
C.“气体A”是足量的氨气
D.整个流程中铝元素的化合价没有发生改变
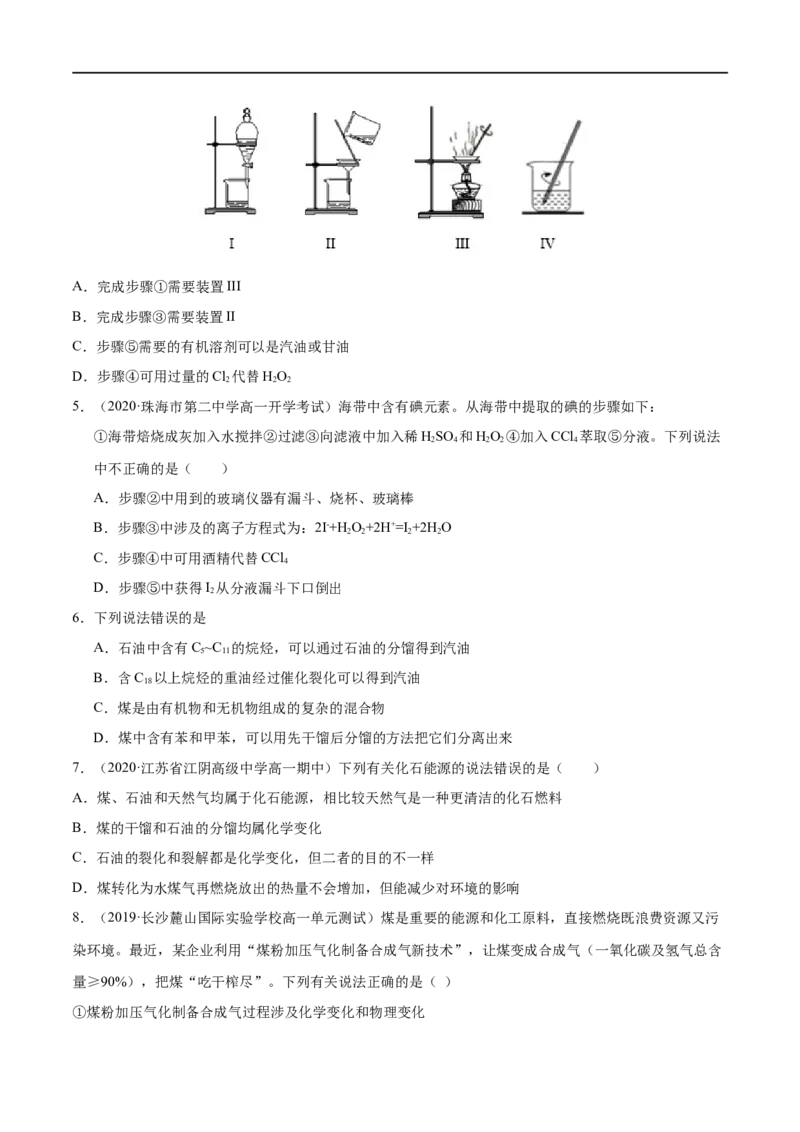
4.(2020·河北南宫中学高一开学考试)实验室从海带中提取碘的部分流程如图:
下列说法正确的是( )A.完成步骤①需要装置III
B.完成步骤③需要装置II
C.步骤⑤需要的有机溶剂可以是汽油或甘油
D.步骤④可用过量的Cl 代替HO
2 2 2
5.(2020·珠海市第二中学高一开学考试)海带中含有碘元素。从海带中提取的碘的步骤如下:
①海带焙烧成灰加入水搅拌②过滤③向滤液中加入稀HSO 和HO ④加入CCl 萃取⑤分液。下列说法
2 4 2 2 4
中不正确的是( )
A.步骤②中用到的玻璃仪器有漏斗、烧杯、玻璃棒
B.步骤③中涉及的离子方程式为:2I-+H O+2H+=I +2H O
2 2 2 2
C.步骤④中可用酒精代替CCl
4
D.步骤⑤中获得I 从分液漏斗下口倒出
2
6.下列说法错误的是
A.石油中含有C ~C 的烷烃,可以通过石油的分馏得到汽油
5 11
B.含C 以上烷烃的重油经过催化裂化可以得到汽油
18
C.煤是由有机物和无机物组成的复杂的混合物
D.煤中含有苯和甲苯,可以用先干馏后分馏的方法把它们分离出来
7.(2020·江苏省江阴高级中学高一期中)下列有关化石能源的说法错误的是( )
A.煤、石油和天然气均属于化石能源,相比较天然气是一种更清洁的化石燃料
B.煤的干馏和石油的分馏均属化学变化
C.石油的裂化和裂解都是化学变化,但二者的目的不一样
D.煤转化为水煤气再燃烧放出的热量不会增加,但能减少对环境的影响
8.(2019·长沙麓山国际实验学校高一单元测试)煤是重要的能源和化工原料,直接燃烧既浪费资源又污
染环境。最近,某企业利用“煤粉加压气化制备合成气新技术”,让煤变成合成气(一氧化碳及氢气总含
量≥90%),把煤“吃干榨尽”。下列有关说法正确的是( )
①煤粉加压气化制备合成气过程涉及化学变化和物理变化②煤粉加压气化制备合成气过程涉及化学变化但没有物理变化
③该技术实现了煤的清洁利用
④该技术实现了煤的高效利用
A.①②③ B.①②④
C.①③④ D.②③④
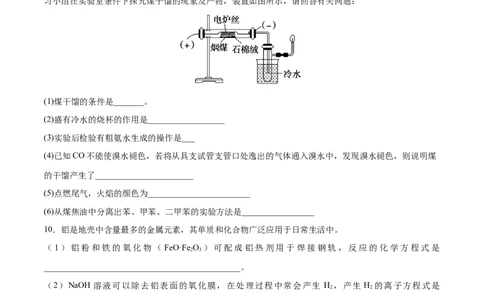
9.将煤直接作为燃料燃烧,不但热效率较低,且产生烟尘、二氧化硫、氮氧化物等物质,造成严重的环
境污染。煤的干馏是提高煤的利用率、生产重要化工原料、降低污染物排放量的有效措施之一。某化学学
习小组在实验室条件下探究煤干馏的现象及产物,装置如图所示,请回答有关问题:
(1)煤干馏的条件是_______。
(2)盛有冷水的烧杯的作用是__________________
(3)实验后检验有粗氨水生成的操作是___
(4)已知CO不能使溴水褪色,若将从具支试管支管口处逸出的气体通入溴水中,发现溴水褪色,则说明煤
的干馏产生了_______________________
(5)点燃尾气,火焰的颜色为________________________
(6)从煤焦油中分离出苯、甲苯、二甲苯的实验方法是_________________
10.铝是地壳中含量最多的金属元素,其单质和化合物广泛应用于日常生活中。
(1)铝粉和铁的氧化物(FeO·Fe O )可配成铝热剂用于焊接钢轨,反应的化学方程式是
2 3
______________________________________________。
(2)NaOH 溶液可以除去铝表面的氧化膜,在处理过程中常会产生 H ,产生 H 的离子方程式是
2 2
__________________________________________。
(3)工业上以铝土矿(AlO·H O)为原料生产铝,主要包括下列过程:
2 3 2
i.将粉粹、筛选后的铝土矿溶解在NaOH溶液中;
ii.加入过量的试剂A使所得溶液中析出Al(OH) 固体;
3
iii.使Al(OH) 脱水生成Al O;
3 2 3
iv.电解熔融Al O 生成Al。
2 3
铝土矿粉粹的目的是________________________,电解熔融 Al O 时,加入冰晶石,其作用是
2 3__________________________。写出电解熔融Al O 的化学方程式____________________________。
2 3
(4)明矾化学式为KAl(SO )·12H O,向明矾溶液中加入Ba(OH) 溶液,当溶液中的SO 2-恰好沉淀时,铝
4 2 2 2 4
元素的存在形式是__________。
11.(2020·河北南宫中学高一开学考试)海水资源的利用具有广阔的前景。从海水中提取Br 与
2
MgCl •6H O的流程如图:
2 2
(1)海水淡化的方法有蒸馏法、___(任写一种)等,考虑成本及效益试剂①可选用___。
(2)比较溶液中Br 的浓度:溶液2___溶液4(填“>”或“<”)。
2
(3)鼓入空气与水蒸气将Br 吹出,吹出的气体用SO 吸收,其化学方程式是__。
2 2
(4)从MgCl 溶液获得MgCl •6H O晶体的主要操作包括____。
2 2 2
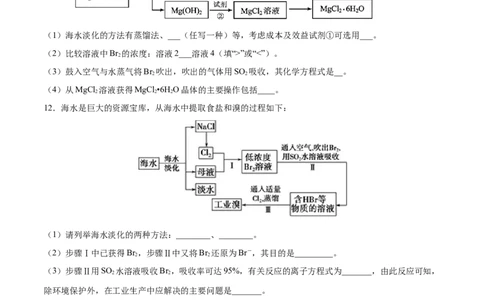
12.海水是巨大的资源宝库,从海水中提取食盐和溴的过程如下:
(1)请列举海水淡化的两种方法:________、________。
(2)步骤Ⅰ中已获得Br ,步骤Ⅱ中又将Br 还原为Br-,其目的是_________。
2 2
(3)步骤Ⅱ用SO 水溶液吸收Br ,吸收率可达95%,有关反应的离子方程式为_______,由此反应可知,
2 2
除环境保护外,在工业生产中应解决的主要问题是_______。
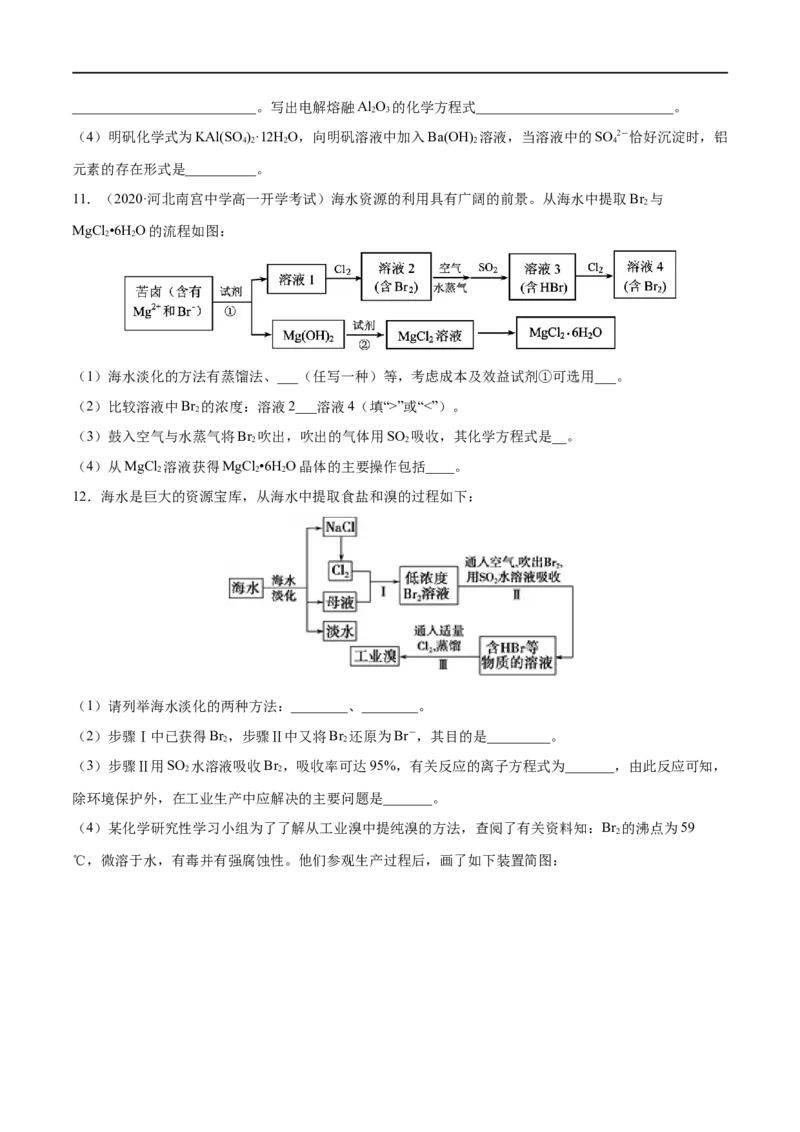
(4)某化学研究性学习小组为了了解从工业溴中提纯溴的方法,查阅了有关资料知:Br 的沸点为59
2
℃,微溶于水,有毒并有强腐蚀性。他们参观生产过程后,画了如下装置简图:请你参与分析讨论:
①图中仪器B的名称是____________。
②整套实验装置中仪器连接均不能用橡胶塞和橡胶管,其原因是__________。
③实验装置气密性良好,要达到提纯溴的目的,操作中如何控制关键条件?___________。
④C中液体颜色为________________。为除去该产物中仍残留的少量Cl,可向其中加入NaBr溶液,充分
2
反应后,再进行的分离操作是________________。
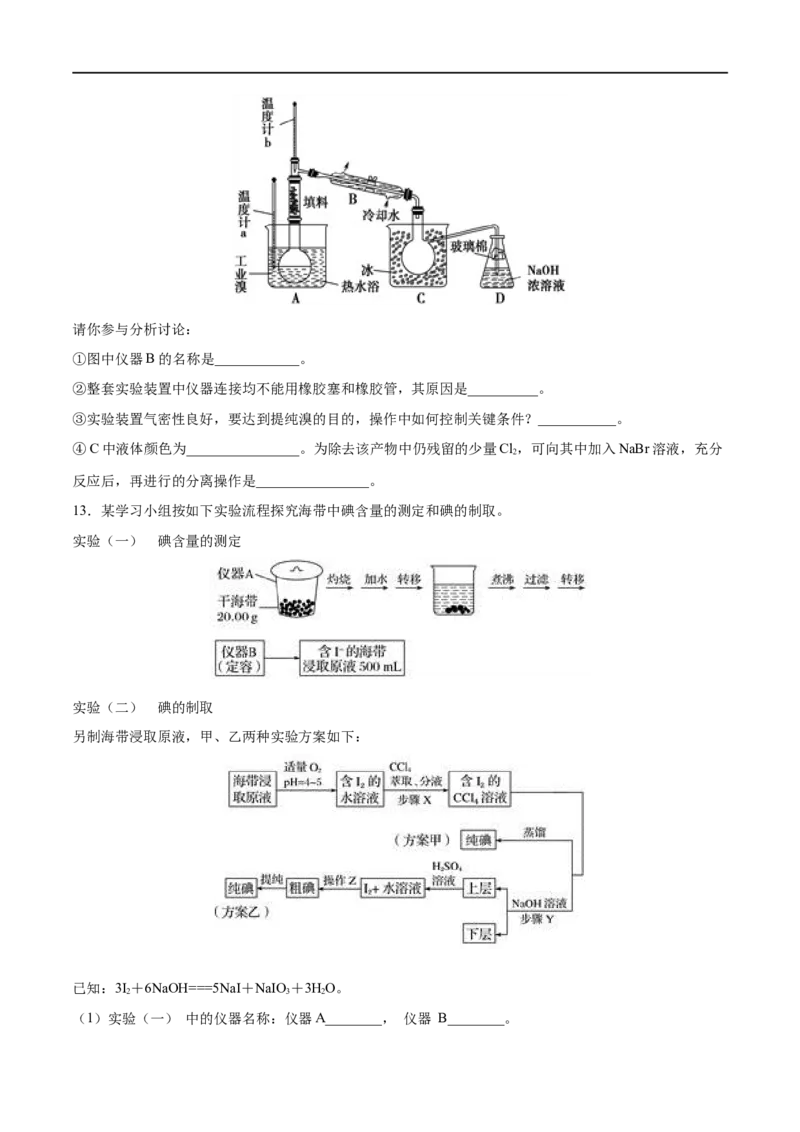
13.某学习小组按如下实验流程探究海带中碘含量的测定和碘的制取。
实验(一) 碘含量的测定
实验(二) 碘的制取
另制海带浸取原液,甲、乙两种实验方案如下:
已知:3I+6NaOH===5NaI+NaIO +3HO。
2 3 2
(1)实验(一) 中的仪器名称:仪器A________, 仪器 B________。(2)①分液漏斗使用前须检漏,检漏方法为__________________。
②步骤X中,萃取后分液漏斗内观察到的现象是___________________。
③下列有关步骤Y的说法,正确的是________。
A 应控制NaOH溶液的浓度和体积
B 将碘转化成离子进入水层
C 主要是除去海带浸取原液中的有机杂质
D NaOH溶液可以由乙醇代替
④实验(二) 中操作Z的名称是________。
(3)方案甲中采用蒸馏不合理,理由是________________________。