文档内容
2019-2020学年高一化学期末复习专项提升卷(人教版2019必修第二册)
专项 08 综合题
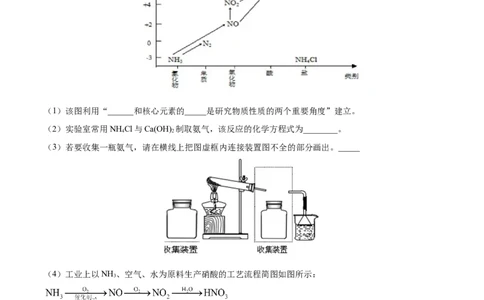
1.(2020·宣威市民族中学高一月考)依据图中氮元素及其化合物的转化关系,回答问题:
(1)该图利用“______和核心元素的_____是研究物质性质的两个重要角度”建立。
(2)实验室常用NH Cl与Ca(OH) 制取氨气,该反应的化学方程式为________。
4 2
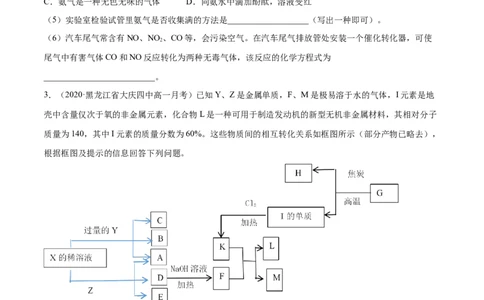
(3)若要收集一瓶氨气,请在横线上把图虚框内连接装置图不全的部分画出。_____
(4)工业上以NH 、空气、水为原料生产硝酸的工艺流程简图如图所示:
3
写出NH →NO的化学方程式__________________________________。
3
(5)图中,X的化学式为_______,将X转化为HNO 属于______________反应(填“氧化还原”或“非氧化
3
还原”)反应。
(6)若要将NH →N,从原理上看,下列试剂可行的是________(填序号)。
3 2
A.O B.Na C.NH Cl D.NO
2 4 2
2.(2020·宣威市民族中学高一月考)硫和氮及其化合物在生产生活中应用广泛。请回答:(1)将SO 通入品红溶液中,现象为品红溶液________,加热后溶液颜色________。
2
(2)已知反应:SO +Cl+2H O ═ 2HCl+H SO ,该反应中的氧化产物是__________。
2 2 2 2 4
(3)木炭与浓硫酸共热的化学反应方程式为:C+2H SO (浓) CO↑+2SO↑+2H O,若生成0.5 mol
2 4 2 2 2
CO,则转移电子的物质的量是_________mol。
2
(4)工业上可以通过氮气和氢气在一定条件下合成氨气。下列关于氨气的性质和用途描述正确的是
____________。
A.氨气易液化,液氨可作制冷剂 B.可用排水法收集氨气
C.氨气是一种无色无味的气体 D.向氨水中滴加酚酞,溶液变红
(5)实验室检验试管里氨气是否收集满的方法是___________________(写出一种即可)。
(6)汽车尾气常含有NO、NO 、CO等,会污染空气。在汽车尾气排放管处安装一个催化转化器,可使
2
尾气中有害气体CO和NO反应转化为两种无毒气体,该反应的化学方程式为
__________________________。
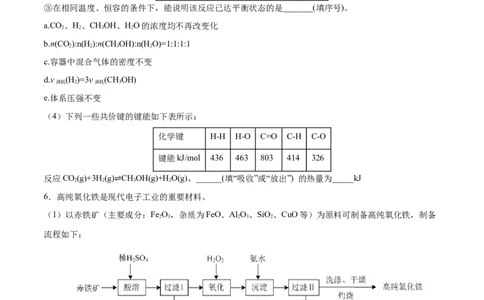
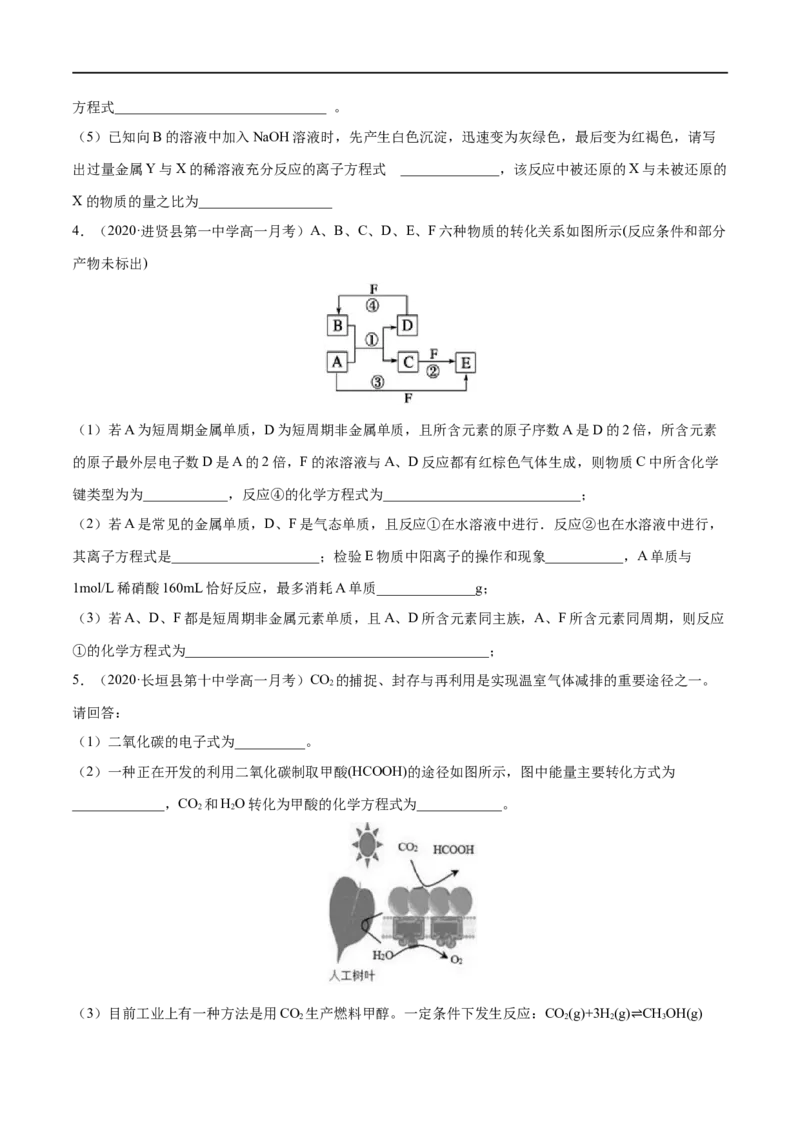
3.(2020·黑龙江省大庆四中高一月考)已知Y、Z是金属单质,F、M是极易溶于水的气体,I元素是地
壳中含量仅次于氧的非金属元素,化合物L是一种可用于制造发动机的新型无机非金属材料,其相对分子
质量为140,其中I元素的质量分数为60%。这些物质间的相互转化关系如框图所示(部分产物已略去),
根据框图及提示的信息回答下列问题。
(1)写出I元素在元素周期表中的位置_________________________________。
(2)K和F反应生成L和M的化学方程式_________________________________________。
(3)将5.2 g 金属Z与足量的X的稀溶液充分反应无气体放出,再向溶液中加入过量的NaOH溶液并加热,
收集到0.448L气体F(标准状况),则整个过程中转移的电子数为_________。
(4)C是空气质量报告中的一种气体污染物,易形成酸雨;P气体是形成另一类型酸雨的主要污染物。实
验室中若想用酸性高锰酸钾溶液除尽P气体,观察到的现象应是____________________,写出相应的离子方程式______________________________ 。
(5)已知向B的溶液中加入NaOH溶液时,先产生白色沉淀,迅速变为灰绿色,最后变为红褐色,请写
出过量金属Y与X的稀溶液充分反应的离子方程式 ______________,该反应中被还原的X与未被还原的
X的物质的量之比为___________________
4.(2020·进贤县第一中学高一月考)A、B、C、D、E、F六种物质的转化关系如图所示(反应条件和部分
产物未标出)
(1)若A为短周期金属单质,D为短周期非金属单质,且所含元素的原子序数A是D的2倍,所含元素
的原子最外层电子数D是A的2倍,F的浓溶液与A、D反应都有红棕色气体生成,则物质C中所含化学
键类型为为____________,反应④的化学方程式为____________________________;
(2)若A是常见的金属单质,D、F是气态单质,且反应①在水溶液中进行.反应②也在水溶液中进行,
其离子方程式是_____________________;检验E物质中阳离子的操作和现象___________,A单质与
1mol/L稀硝酸160mL恰好反应,最多消耗A单质______________g;
(3)若A、D、F都是短周期非金属元素单质,且A、D所含元素同主族,A、F所含元素同周期,则反应
①的化学方程式为___________________________________________;
5.(2020·长垣县第十中学高一月考)CO 的捕捉、封存与再利用是实现温室气体减排的重要途径之一。
2
请回答:
(1)二氧化碳的电子式为__________。
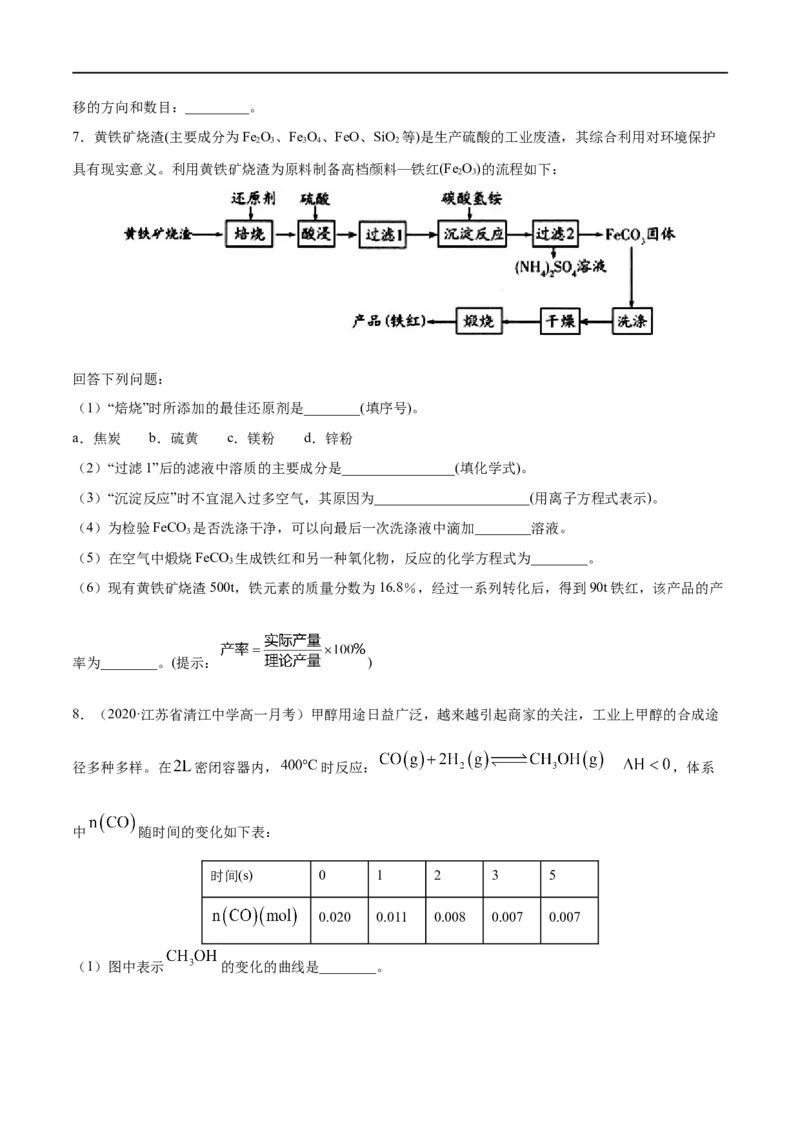
(2)一种正在开发的利用二氧化碳制取甲酸(HCOOH)的途径如图所示,图中能量主要转化方式为
_____________,CO 和HO转化为甲酸的化学方程式为____________。
2 2
(3)目前工业上有一种方法是用CO 生产燃料甲醇。一定条件下发生反应:CO(g)+3H(g) CHOH(g)
2 2 2 3
⇌+H O(g)。
2
①恒容容器中,能加快该反应速率的是_______。
a.升高温度 b.从体系中分离出CHOH c.加入高效催化剂 d.降低压强
3
②在体积为2L的密闭容器中,充入1molCO 和3molH ,测得CO 的物质的量随时间变化如图所示。从反
2 2 2
应开始到5min末,用H 浓度变化表示的平均反应速率________________。
2
t/min 0 2 5 10 15
n(CO)/mol 1 0.75 0.5 0.25 0.25
2
③在相同温度、恒容的条件下,能说明该反应已达平衡状态的是_______(填序号)。
a.CO 、H、CHOH、HO的浓度均不再改变化
2 2 3 2
b.n(CO):n(H):n(CHOH):n(H O)=1:1:1:1
2 2 3 2
c.容器中混合气体的密度不变
d.v (H )=3v (CHOH)
消耗 2 消耗 3
e.体系压强不变
(4)下列一些共价键的键能如下表所示:
化学键 H-H H-O C=O C-H C-O
键能kJ/mol 436 463 803 414 326
反应CO(g)+3H(g) CHOH(g)+H O(g),______(填“吸收”或“放出”) 的热量为_____kJ
2 2 3 2
6.高纯氧化铁是现⇌代电子工业的重要材料。
(1)以赤铁矿(主要成分:Fe O,杂质为FeO、Al O、SiO、CuO等)为原料可制备高纯氧化铁,制备
2 3 2 3 2
流程如下:
①“酸溶”时Al O 发生反应的化学方程式为_________________________________。
2 3
②“氧化”时发生反应的离子方程式为____________________________。
③“灼烧”时发生反应的化学方程式为______________________________。
④滤渣Ⅰ的主要成分与NaOH溶液反应的离子方程式为_______________________________。
(2)FeCO 在空气中高温灼烧也可以制备高纯氧化铁,写出该反应的化学方程式,并用单线桥标出电子转
3移的方向和数目:_________。
7.黄铁矿烧渣(主要成分为Fe O、Fe O、FeO、SiO 等)是生产硫酸的工业废渣,其综合利用对环境保护
2 3 3 4 2
具有现实意义。利用黄铁矿烧渣为原料制备高档颜料—铁红(Fe O)的流程如下:
2 3
回答下列问题:
(1)“焙烧”时所添加的最佳还原剂是________(填序号)。
a.焦炭 b.硫黄 c.镁粉 d.锌粉
(2)“过滤1”后的滤液中溶质的主要成分是________________(填化学式)。
(3)“沉淀反应”时不宜混入过多空气,其原因为______________________(用离子方程式表示)。
(4)为检验FeCO 是否洗涤干净,可以向最后一次洗涤液中滴加________溶液。
3
(5)在空气中煅烧FeCO 生成铁红和另一种氧化物,反应的化学方程式为________。
3
(6)现有黄铁矿烧渣500t,铁元素的质量分数为16.8%,经过一系列转化后,得到90t铁红,该产品的产
率为________。(提示: )
8.(2020·江苏省清江中学高一月考)甲醇用途日益广泛,越来越引起商家的关注,工业上甲醇的合成途
径多种多样。在 密闭容器内, 时反应: ,体系
中 随时间的变化如下表:
时间(s) 0 1 2 3 5
0.020 0.011 0.008 0.007 0.007
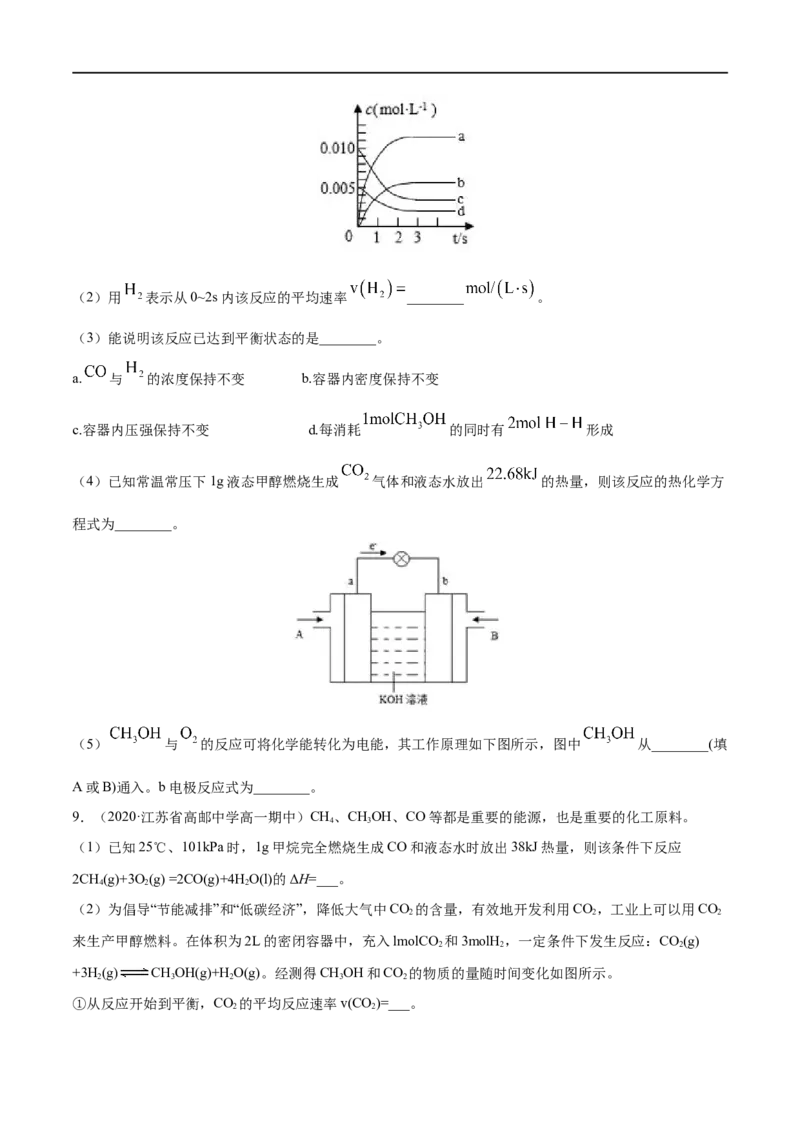
(1)图中表示 的变化的曲线是________。(2)用 表示从0~2s内该反应的平均速率 ________ 。
(3)能说明该反应已达到平衡状态的是________。
a. 与 的浓度保持不变 b.容器内密度保持不变
c.容器内压强保持不变 d.每消耗 的同时有 形成
(4)已知常温常压下1g液态甲醇燃烧生成 气体和液态水放出 的热量,则该反应的热化学方
程式为________。
(5) 与 的反应可将化学能转化为电能,其工作原理如下图所示,图中 从________(填
A或B)通入。b电极反应式为________。
9.(2020·江苏省高邮中学高一期中)CH、CHOH、CO等都是重要的能源,也是重要的化工原料。
4 3
(1)已知25℃、101kPa时,1g甲烷完全燃烧生成CO和液态水时放出38kJ热量,则该条件下反应
2CH(g)+3O(g) =2CO(g)+4H O(l)的ΔH=___。
4 2 2
(2)为倡导“节能减排”和“低碳经济”,降低大气中CO 的含量,有效地开发利用CO,工业上可以用CO
2 2 2
来生产甲醇燃料。在体积为2L的密闭容器中,充入lmolCO 和3molH ,一定条件下发生反应:CO(g)
2 2 2
+3H (g) CHOH(g)+H O(g)。经测得CHOH和CO 的物质的量随时间变化如图所示。
2 3 2 3 2
①从反应开始到平衡,CO 的平均反应速率v(CO)=___。
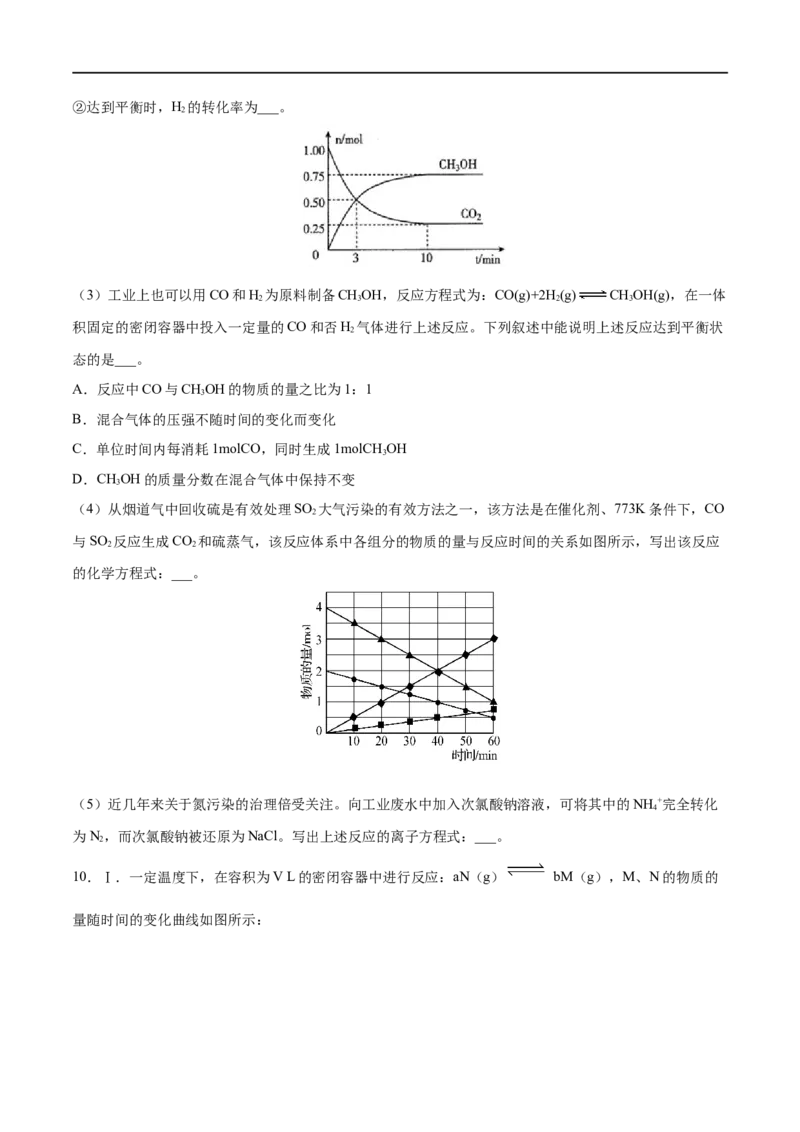
2 2②达到平衡时,H 的转化率为___。
2
(3)工业上也可以用CO和H 为原料制备CHOH,反应方程式为:CO(g)+2H(g) CHOH(g),在一体
2 3 2 3
积固定的密闭容器中投入一定量的CO和否H 气体进行上述反应。下列叙述中能说明上述反应达到平衡状
2
态的是___。
A.反应中CO与CHOH的物质的量之比为1:1
3
B.混合气体的压强不随时间的变化而变化
C.单位时间内每消耗1molCO,同时生成1molCH OH
3
D.CHOH的质量分数在混合气体中保持不变
3
(4)从烟道气中回收硫是有效处理SO 大气污染的有效方法之一,该方法是在催化剂、773K条件下,CO
2
与SO 反应生成CO 和硫蒸气,该反应体系中各组分的物质的量与反应时间的关系如图所示,写出该反应
2 2
的化学方程式:___。
(5)近几年来关于氮污染的治理倍受关注。向工业废水中加入次氯酸钠溶液,可将其中的NH +完全转化
4
为N,而次氯酸钠被还原为NaCl。写出上述反应的离子方程式:___。
2
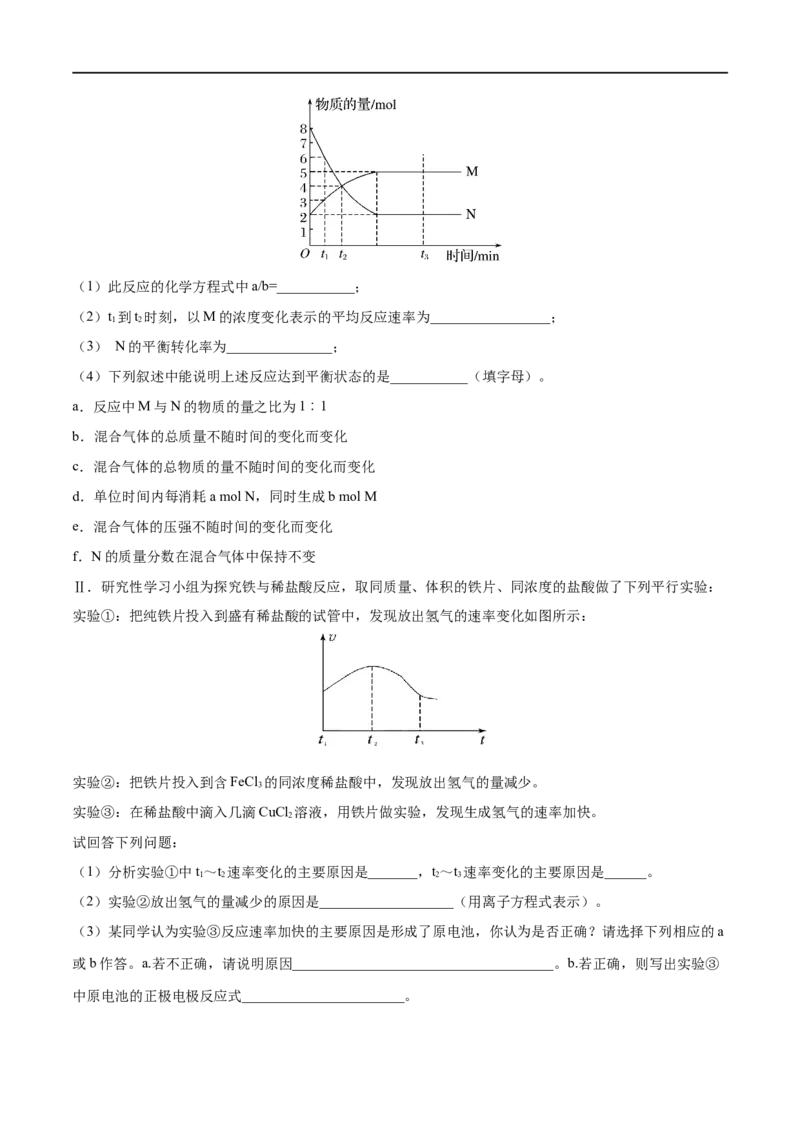
10.Ⅰ.一定温度下,在容积为V L的密闭容器中进行反应:aN(g) bM(g),M、N的物质的
量随时间的变化曲线如图所示:(1)此反应的化学方程式中a/b=___________;
(2)t 到t 时刻,以M的浓度变化表示的平均反应速率为_________________;
1 2
(3) N的平衡转化率为_______________;
(4)下列叙述中能说明上述反应达到平衡状态的是___________(填字母)。
a.反应中M与N的物质的量之比为1︰1
b.混合气体的总质量不随时间的变化而变化
c.混合气体的总物质的量不随时间的变化而变化
d.单位时间内每消耗a mol N,同时生成b mol M
e.混合气体的压强不随时间的变化而变化
f.N的质量分数在混合气体中保持不变
Ⅱ.研究性学习小组为探究铁与稀盐酸反应,取同质量、体积的铁片、同浓度的盐酸做了下列平行实验:
实验①:把纯铁片投入到盛有稀盐酸的试管中,发现放出氢气的速率变化如图所示:
实验②:把铁片投入到含FeCl 的同浓度稀盐酸中,发现放出氢气的量减少。
3
实验③:在稀盐酸中滴入几滴CuCl 溶液,用铁片做实验,发现生成氢气的速率加快。
2
试回答下列问题:
(1)分析实验①中t~t 速率变化的主要原因是_______,t~t 速率变化的主要原因是______。
1 2 2 3
(2)实验②放出氢气的量减少的原因是___________________(用离子方程式表示)。
(3)某同学认为实验③反应速率加快的主要原因是形成了原电池,你认为是否正确?请选择下列相应的a
或b作答。a.若不正确,请说明原因_____________________________________。b.若正确,则写出实验③
中原电池的正极电极反应式_______________________。