文档内容
2019-2020学年高一化学期末复习专项提升卷(人教版2019必修第二册)
专项 04 化学反应速率与平衡的综合判断与计算
1.在 2A(g) + B(g) ===3C(g) + 4D(g)反应中,下面表示的反应速率最快的是
A.v (A)=0.5mol/(L∙s) B.v(B)=1.8 mol/(L∙min) C.v (C)=0.8mol/(L∙s) D.v(D)=1.0
mol/(L∙s)
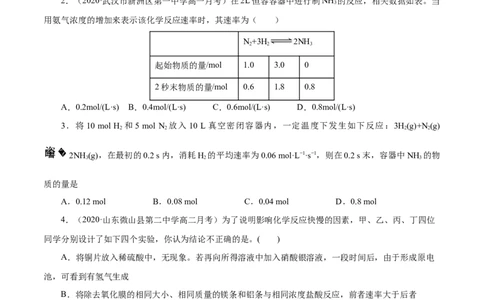
2.(2020·武汉市新洲区第一中学高一月考)在2L恒容容器中进行制NH 的反应,相关数据如表。当
3
用氨气浓度的增加来表示该化学反应速率时,其速率为( )
N+3H 2NH
2 2 3
起始物质的量/mol 1.0 3.0 0
2秒末物质的量/mol 0.6 1.8 0.8
A.0.2mol/(L·s) B.0.4mol/(L·s) C.0.6mol/(L·s) D.0.8mol/(L·s)
3.将10 mol H 和5 mol N 放入 10 L 真空密闭容器内,一定温度下发生如下反应:3H(g)+N(g)
2 2 2 2
2NH (g),在最初的0.2 s内,消耗H 的平均速率为0.06 mol·L−1·s−1,则在0.2 s末,容器中NH 的物
3 2 3
质的量是
A.0.12 mol B.0.08 mol C.0.04 mol D.0.8 mol
4.(2020·山东微山县第二中学高二月考)为了说明影响化学反应快慢的因素,甲、乙、丙、丁四位
同学分别设计了如下四个实验,你认为结论不正确的是。( )
A.将铜片放入稀硫酸中,无现象。若再向所得溶液中加入硝酸银溶液,一段时间后,由于形成原电
池,可看到有氢气生成
B.将除去氧化膜的相同大小、相同质量的镁条和铝条与相同浓度盐酸反应,前者速率大于后者
C.两支试管中分别加入根同质量的氯酸钾,其中一支试管中再加入少量二氧化锰,同时加热,产生
氧气的快慢不同
D.相同条件下等质量的块状和粉末状大理石与相同浓度盐酸反应时,粉末状的反应速率快
5.(2020·瑞安市上海新纪元高级中学高一开学考试)在相同的密闭容器中,用高纯度纳米级Cu O分
2
别进行催化分解水的实验:2HO(g) 2H(g) + O(g) ∆H>0,实验测得反应体系中水蒸气浓度
2 2 2
(mol·L-1)的变化结果如下:
1
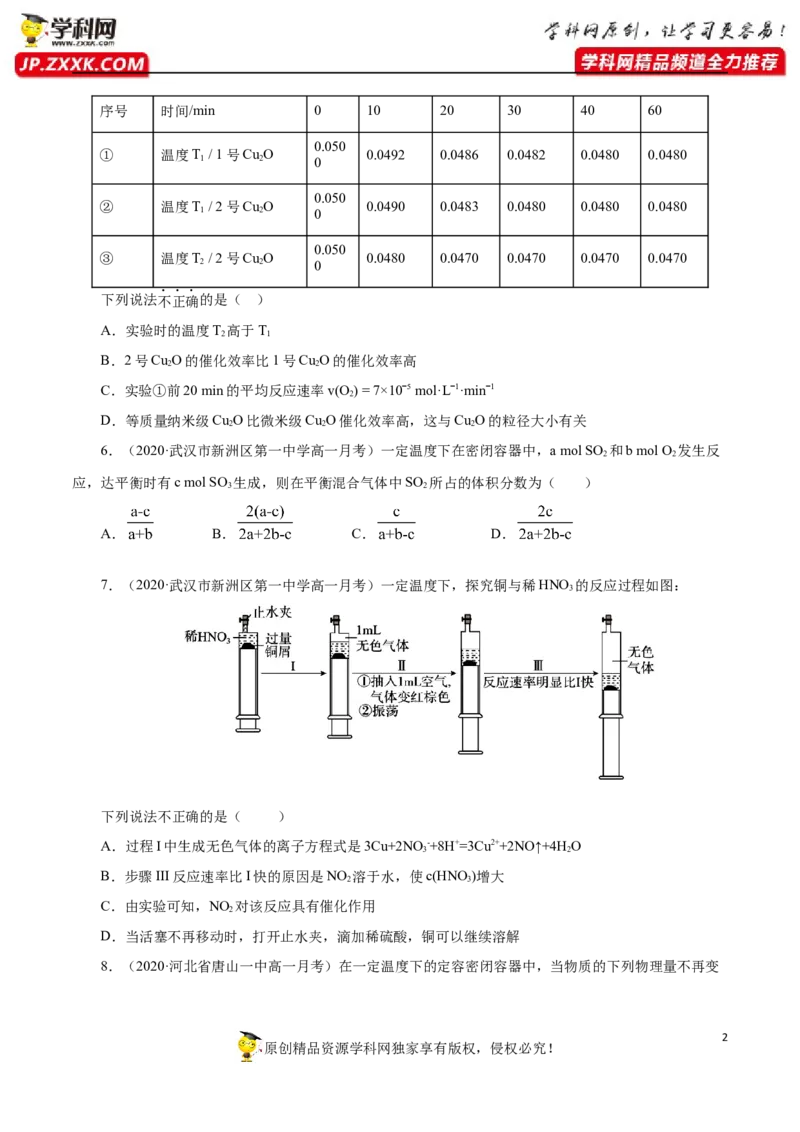
原创精品资源学科网独家享有版权,侵权必究!序号 时间/min 0 10 20 30 40 60
0.050
① 温度T / 1号Cu O 0.0492 0.0486 0.0482 0.0480 0.0480
1 2 0
0.050
② 温度T / 2号Cu O 0.0490 0.0483 0.0480 0.0480 0.0480
1 2 0
0.050
③ 温度T / 2号Cu O 0.0480 0.0470 0.0470 0.0470 0.0470
2 2 0
下列说法不正确的是( )
A.实验时的温度T 高于T
2 1
B.2号Cu O的催化效率比1号Cu O的催化效率高
2 2
C.实验①前20 min的平均反应速率v(O ) = 7×10ˉ5 mol·Lˉ1·minˉ1
2
D.等质量纳米级Cu O比微米级Cu O催化效率高,这与Cu O的粒径大小有关
2 2 2
6.(2020·武汉市新洲区第一中学高一月考)一定温度下在密闭容器中,a mol SO 和b mol O 发生反
2 2
应,达平衡时有c mol SO 生成,则在平衡混合气体中SO 所占的体积分数为( )
3 2
A. B. C. D.
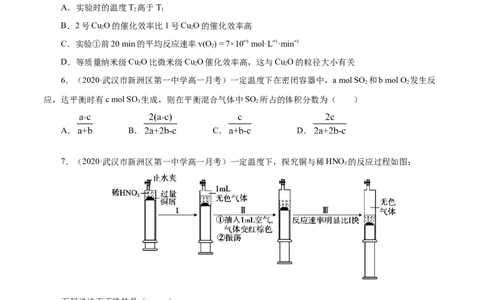
7.(2020·武汉市新洲区第一中学高一月考)一定温度下,探究铜与稀HNO 的反应过程如图:
3
下列说法不正确的是( )
A.过程I中生成无色气体的离子方程式是3Cu+2NO-+8H+=3Cu2++2NO↑+4HO
3 2
B.步骤III反应速率比I快的原因是NO 溶于水,使c(HNO )增大
2 3
C.由实验可知,NO 对该反应具有催化作用
2
D.当活塞不再移动时,打开止水夹,滴加稀硫酸,铜可以继续溶解
8.(2020·河北省唐山一中高一月考)在一定温度下的定容密闭容器中,当物质的下列物理量不再变
2
原创精品资源学科网独家享有版权,侵权必究!化时,不能表明反应: 已达平衡的是( )
A.混合气体的密度
B.混合气体的压强
C. 的物质的量浓度
D.混合气体的平均相对分子质量
9.(2020·河南省登封市实验高级中学高一期中)在两个恒温、恒容的密闭容器中进行下列两个可逆
反应:(甲)2X(g) Y(g)+Z(s) (乙)A(s)+2B(g) C(g)+D(g),当下列物理量不再发生变化时:
①混合气体的密度;②反应容器中生成物的百分含量;③反应物的消耗速率与生成物的消耗速率之比等于
系数之比;④混合气体的压强⑤混合气体的总物质的量。其中能表明(甲)和(乙)都达到化学平衡状态是
( )
A.①②③ B.①②③⑤
C.①②③④ D.①②③④⑤
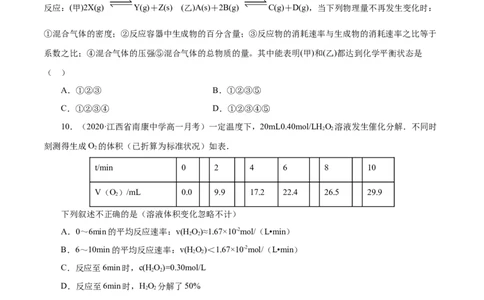
10.(2020·江西省南康中学高一月考)一定温度下,20mL0.40mol/LH O 溶液发生催化分解.不同时
2 2
刻测得生成O 的体积(已折算为标准状况)如表.
2
t/min 0 2 4 6 8 10
V(O)/mL 0.0 9.9 17.2 22.4 26.5 29.9
2
下列叙述不正确的是(溶液体积变化忽略不计)
A.0~6min的平均反应速率:v(HO)≈1.67×10-2mol/(L•min)
2 2
B.6~10min的平均反应速率:v(HO)<1.67×10-2mol/(L•min)
2 2
C.反应至6min时,c(HO)=0.30mol/L
2 2
D.反应至6min时,HO 分解了50%
2 2
11.(2020·河南省登封市实验高级中学高一期中)对于可逆反应4NH +5O 4NO+6H O(g),下列
3 2 2
叙述正确的是( )
A.达到平衡状态,2 v (NH )= 3v (H O)
正 3 逆 2
B.单位时间内生成x mol NO的同时,消耗x mol NH ,则反应达到平衡状态
3
C.达到化学平衡时,若增加容器体积,则正反应速率减小,逆反应速率增大
D.反应达到平衡时,反应物的转化率一定小于100%
3
原创精品资源学科网独家享有版权,侵权必究!12.X、Y、Z为三种气体,把a mol X和b mol Y充入一密闭容器中,发生反应X+2Y 2Z。达
到平衡时,若它们的物质的量满足:n(X)+n(Y)=n(Z),则Y的转化率为
ab 2(ab)
5 5b
A. ×100% B. ×100%
2(ab) ab
5 5a
C. ×100% D. ×100%
13.已知:2A(g)+3B(g) 2C(g)+zD(g),现将2 mol A与2 mol B混合于2 L的密闭容器中,2 s后,
A的转化率为50%,测得v(D)=0.25 mol·L−1·s−1,下列推断正确的是
A.v(C)=0.2 mol·L−1·s−1 B.z=1
C.B的转化率为25% D.C平衡时的浓度为0.5 mol·L−1
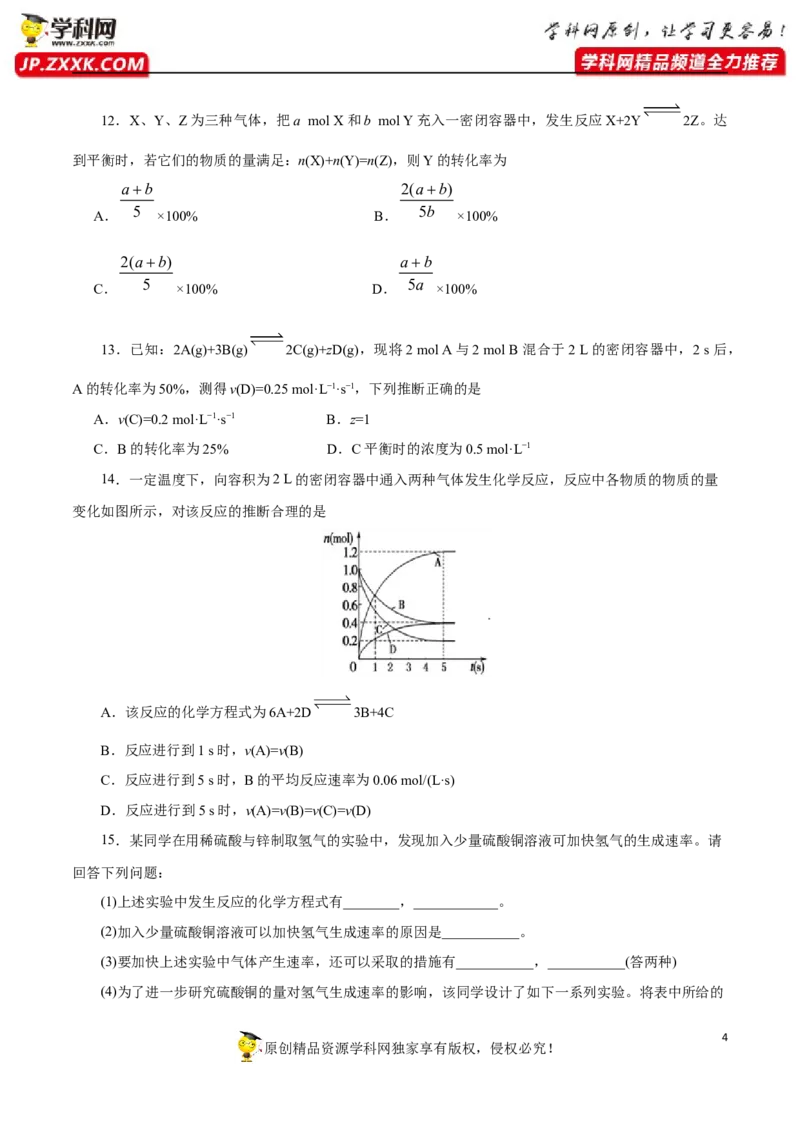
14.一定温度下,向容积为2 L的密闭容器中通入两种气体发生化学反应,反应中各物质的物质的量
变化如图所示,对该反应的推断合理的是
A.该反应的化学方程式为6A+2D 3B+4C
B.反应进行到1 s时,v(A)=v(B)
C.反应进行到5 s时,B的平均反应速率为0.06 mol/(L·s)
D.反应进行到5 s时,v(A)=v(B)=v(C)=v(D)
15.某同学在用稀硫酸与锌制取氢气的实验中,发现加入少量硫酸铜溶液可加快氢气的生成速率。请
回答下列问题:
(1)上述实验中发生反应的化学方程式有________,____________。
(2)加入少量硫酸铜溶液可以加快氢气生成速率的原因是___________。
(3)要加快上述实验中气体产生速率,还可以采取的措施有___________,___________(答两种)
(4)为了进一步研究硫酸铜的量对氢气生成速率的影响,该同学设计了如下一系列实验。将表中所给的
4
原创精品资源学科网独家享有版权,侵权必究!混合溶液分别加入6个盛有过量Zn粒的反应瓶中,收集产生的气体,记录获得相同体积的气体所需时间。
实验混合溶液 A B C D E F
4 mol/L H SO (mL) 50 V V V V V
2 4 1 2 3 4 5
饱和CuSO 溶液(mL) 0 5 15 25 V 50
4 6
HO(mL) V V V V 10 0
2 7 8 9 10
①请完成此实验设计,其中:V=______,V=______,V=_______。
1 6 7
②该同学最后得出的结论为:当加入少量CuSO 溶液时,生成氢气的速率会大大提高,但当加入的
4
CuSO 溶液超过一定量时,生成氢气的速率反而会下降。请分析氢气生成速率下降的主要原因_____。
4
16.(2020·山东省淄博第七中学高一月考)某化学小组为了研究外界条件对化学反应速率的影响,进
行了酸性高锰酸钾与草酸(HC O)的反应,记录如表所示的实验数据:
2 2 4
试管中所加试剂及其用量/mL 溶液褪至无
实验 实验
色所需时间
编号 温度
0.6mol/L H C O 溶液 HO 3mol/L H SO 0.05mol/L KMnO /min
2 2 4 2 2 4 4
① 25 3.0 V 2.0 3.0 1.5
1
② 25 2.0 3.0 2.0 3.0 2.7
③ 50 2.0 V 2.0 3.0 1.0
2
(1)请写出该反应的离子方程式 ______,当该反应以表中数据反应完全时转移电子数为______N 。
A
(2)V=_______mL。
1
(3)根据表中的实验①、②数据,可以得到的结论是 _______。
(4)探究温度对化学反应速率的影响,应选择 _______(填实验编号)
(5)该小组根据经验绘制了n(Mn 2+)随时间变化的趋势如图1所示,但有同学查阅已有实验资料
发现,该实验过程中n(Mn 2+)随时间变化的实际趋势如图2所示。
5
原创精品资源学科网独家享有版权,侵权必究!该小组同学根据图 2 所示信息提出了新的假设,并设计实验方案④继续进行实验探究。
试管中所加试剂及其用量
溶液褪至
实验 实验温 再加入某
无色所需
编号 度/℃ 种固体
时间/min
0.6mol/L 3mol/L 0.05mol/L
HO
HC O 2 HSO KMnO
2 2 4 2 4 4
④ 25 2.0 3.0 2.0 3.0 MnSO t
4
①小组同学提出的假设是________。
②若该小组同学提出的假设成立,应观察到________现象。
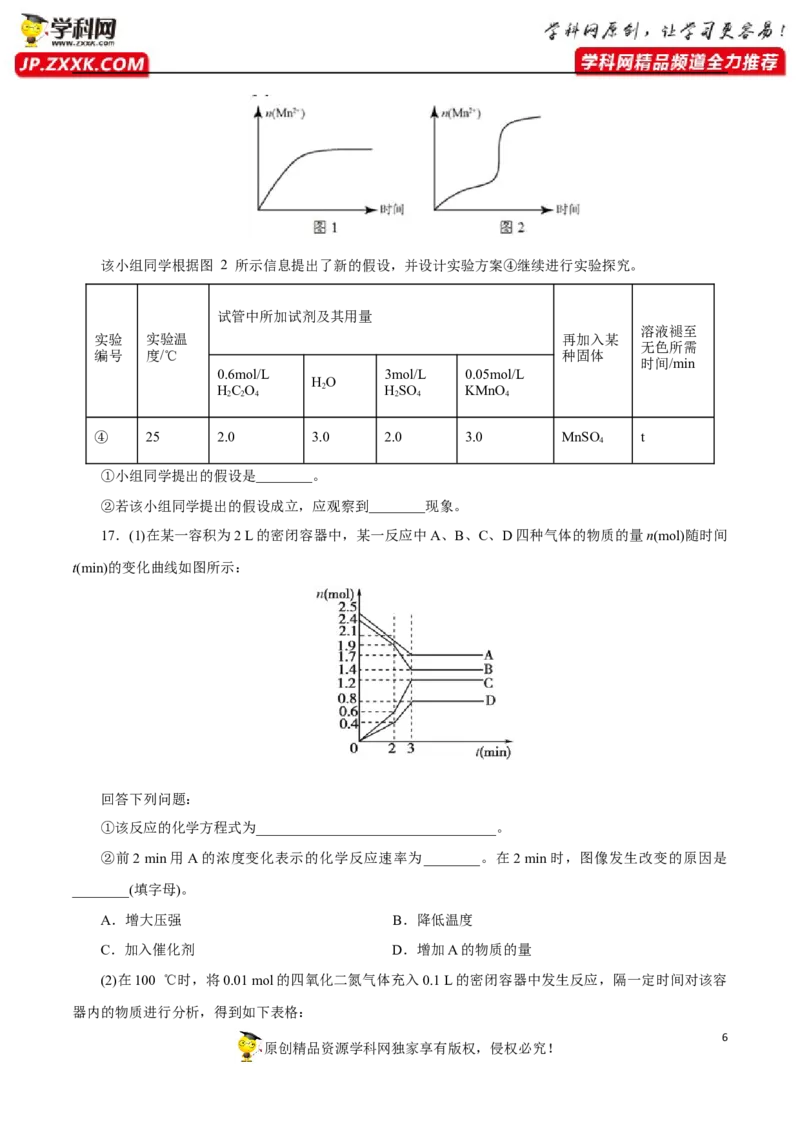
17.(1)在某一容积为2 L的密闭容器中,某一反应中A、B、C、D四种气体的物质的量n(mol)随时间
t(min)的变化曲线如图所示:
回答下列问题:
①该反应的化学方程式为__________________________________。
②前2 min用A的浓度变化表示的化学反应速率为________。在2 min时,图像发生改变的原因是
________(填字母)。
A.增大压强 B.降低温度
C.加入催化剂 D.增加A的物质的量
(2)在100 ℃时,将0.01 mol的四氧化二氮气体充入0.1 L的密闭容器中发生反应,隔一定时间对该容
器内的物质进行分析,得到如下表格:
6
原创精品资源学科网独家享有版权,侵权必究!时间/s
0 20 40 60 80 100
浓度/mol·L−1
c(N O)/mol·L−1 0.100 0.070 0.050 c a b
2 4 3
c(NO )/mol·L−1 0.000 0.060 c 0.120 0.120 0.120
2 2
请填空:
①该反应的化学方程式________________________,达到平衡时四氧化二氮的转化率为_______。
②在0~20 s内,四氧化二氮的平均反应速率为______,哪一时间段______(指0~20、20~40、40~
60、60~80、80~100 s)反应速率最大并解释______。
18.将气体A、B置于固定容积为2 L的密闭容器中,发生如下反应:3A(g)+B(g) 2C(g)+
2D(g),反应进行到10 s末,达到平衡,测得A的物质的量为1.8 mol,B的物质的量为0.6 mol,C的物质
的量为0.8 mol。
(1)用C表示10 s内反应的平均反应速率为____。
(2)反应前A的物质的量浓度是____。
(3)10 s末,生成物D的浓度为__。
(4)A与B的平衡转化率之比为___。
(5)反应过程中容器内气体的平均相对分子质量变化是_(填“增大”、“减小”或“不变”,下
同),气体的密度变化是___。
(6)平衡后,若改变下列条件,生成D的速率如何变化(填“增大”、“减小”或“不变”):
①降低温度____;②增大A的浓度_____;
③恒容下充入氖气________。
(7)下列叙述能说明该反应已达到化学平衡状态的是(填标号)___;
A.v(B)=2v(C)
B.容器内压强不再发生变化
C.A的体积分数不再发生变化
D.器内气体密度不再发生变化
E.相同时间内消耗n mol的B的同时生成2n mol的D
(8)将固体NH I置于密闭容器中,在某温度下发生下列反应:NH I(s) NH (g)+HI(g),2HI(g)
4 4 3
H(g)+I(g)。当反应达到平衡时,c(H)=0.5mol·L-1,c(HI)=4mol·L-1,则NH 的浓度为___。
2 2 2 3
7
原创精品资源学科网独家享有版权,侵权必究!19.(2020·四川省岳池县第一中学高一月考)在800℃2L密闭容器中,反应2NO+O 2NO ,
2 2
n(NO)随时间的变化如下表:
时间(s) 0 1 2 3 4 5
n(NO)/mol 0.020 0.010 0.008 0.007 0.007 0.007
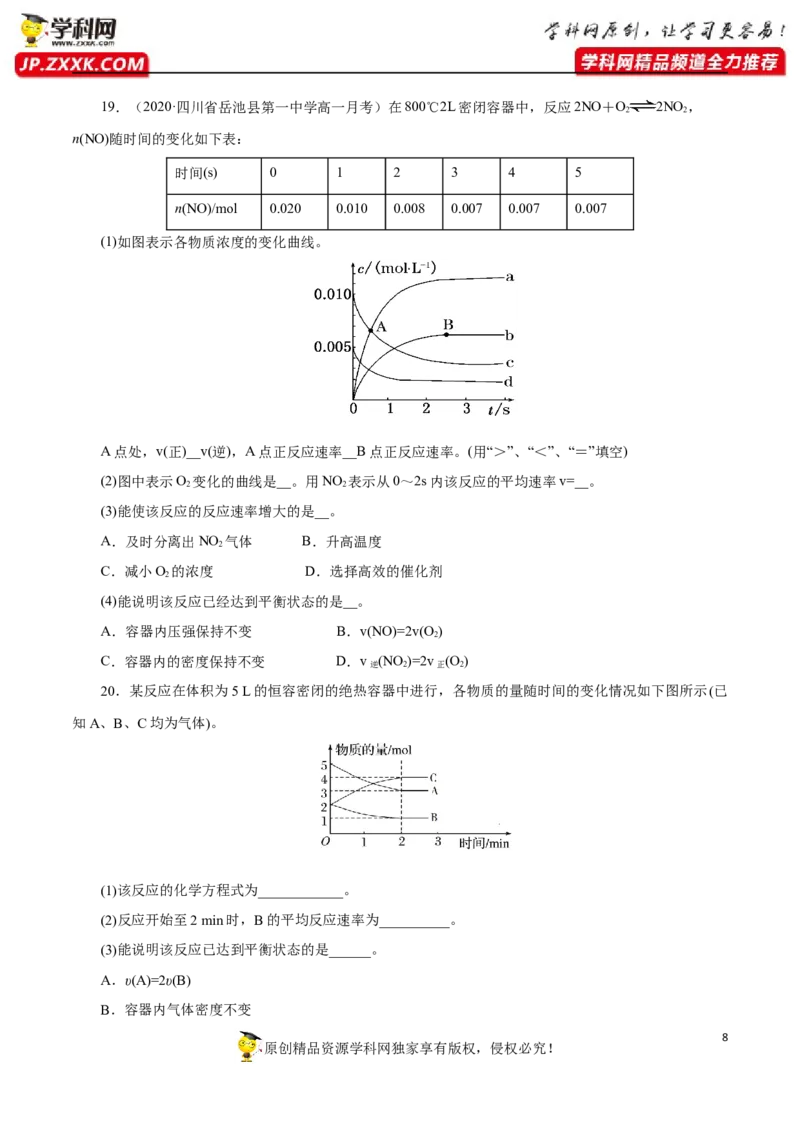
(1)如图表示各物质浓度的变化曲线。
A点处,v(正)__v(逆),A点正反应速率__B点正反应速率。(用“>”、“<”、“=”填空)
(2)图中表示O 变化的曲线是__。用NO 表示从0~2s内该反应的平均速率v=__。
2 2
(3)能使该反应的反应速率增大的是__。
A.及时分离出NO 气体 B.升高温度
2
C.减小O 的浓度 D.选择高效的催化剂
2
(4)能说明该反应已经达到平衡状态的是__。
A.容器内压强保持不变 B.v(NO)=2v(O )
2
C.容器内的密度保持不变 D.v (NO )=2v (O )
逆 2 正 2
20.某反应在体积为5 L的恒容密闭的绝热容器中进行,各物质的量随时间的变化情况如下图所示(已
知A、B、C均为气体)。
(1)该反应的化学方程式为____________。
(2)反应开始至2 min时,B的平均反应速率为__________。
(3)能说明该反应已达到平衡状态的是______。
A.υ(A)=2υ(B)
B.容器内气体密度不变
8
原创精品资源学科网独家享有版权,侵权必究!C.υ (A)=υ (C)
逆 正
D.各组分的物质的量相等
E. 混合气体的平均相对分子质量不再改变的状态
(4)由图求得平衡时A的转化率为_____________。
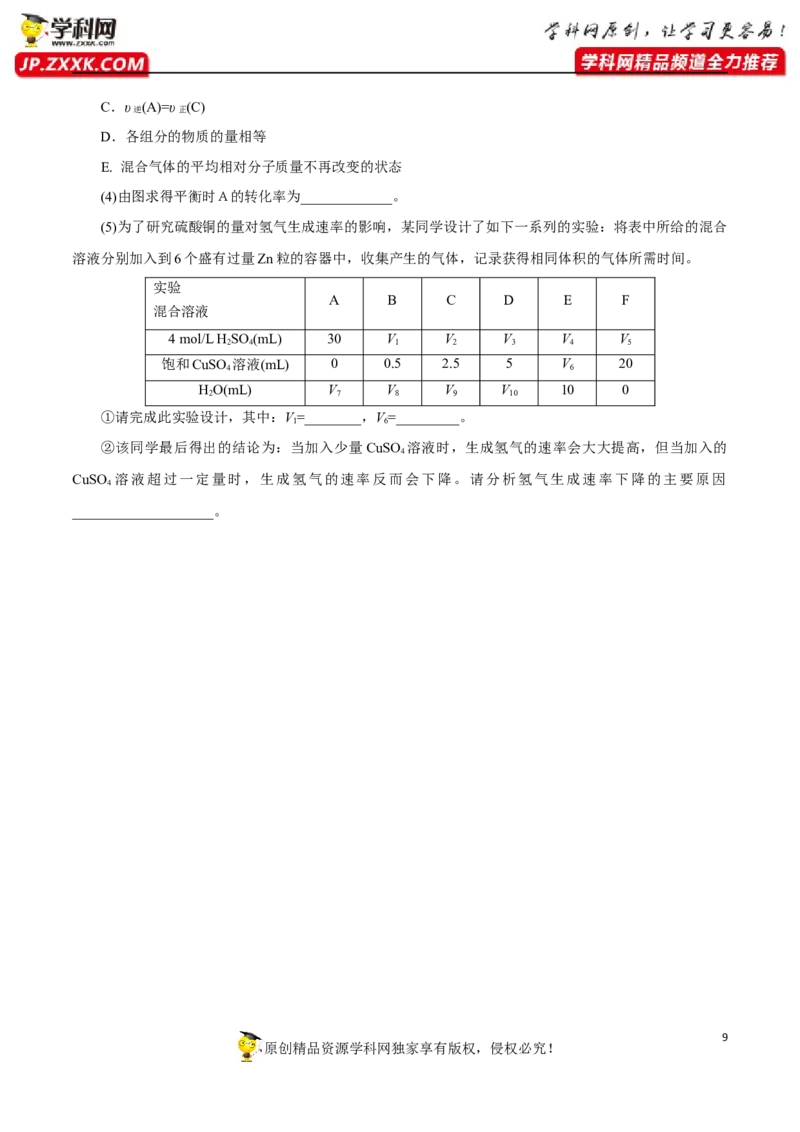
(5)为了研究硫酸铜的量对氢气生成速率的影响,某同学设计了如下一系列的实验:将表中所给的混合
溶液分别加入到6个盛有过量Zn粒的容器中,收集产生的气体,记录获得相同体积的气体所需时间。
实验
A B C D E F
混合溶液
4 mol/L H SO (mL) 30 V V V V V
2 4 1 2 3 4 5
饱和CuSO 溶液(mL) 0 0.5 2.5 5 V 20
4 6
HO(mL) V V V V 10 0
2 7 8 9 10
①请完成此实验设计,其中:V=________,V=_________。
1 6
②该同学最后得出的结论为:当加入少量CuSO 溶液时,生成氢气的速率会大大提高,但当加入的
4
CuSO 溶液超过一定量时,生成氢气的速率反而会下降。请分析氢气生成速率下降的主要原因
4
____________________。
9
原创精品资源学科网独家享有版权,侵权必究!