文档内容
2019-2020学年高一化学期末复习专项提升卷(人教版2019必修第二册)
专项 03 原电池原理的综合判断
1.镍镉(Ni—Cd)可充电电池在现代生活中有广泛应用,它的充放电反应按下式进行:Cd+2NiO(OH)
+2H O Cd(OH) +2Ni(OH) ;由此可知,该电池放电时的负极材料是
2 2 2
A.Cd B.Ni(OH) C.Cd(OH) D.NiO(OH)
2 2
【答案】A
【解析】从总反应式Cd+2NiO(OH)+2H O Cd(OH) +2Ni(OH) 可以看出,放电时,Cd由0价升高到
2 2 2
+2价,Ni由+3价降低到+2价,所以负极材料是Cd,故选A。
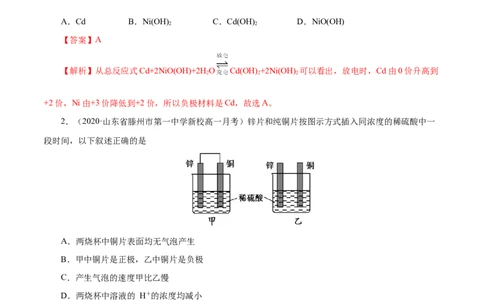
2.(2020·山东省滕州市第一中学新校高一月考)锌片和纯铜片按图示方式插入同浓度的稀硫酸中一
段时间,以下叙述正确的是
A.两烧杯中铜片表面均无气泡产生
B.甲中铜片是正极,乙中铜片是负极
C.产生气泡的速度甲比乙慢
D.两烧杯中溶液的 H+的浓度均减小
【答案】D
【解析】【分析】甲中形成铜锌原电池,锌作负极,失电子,铜作正极,H+在铜极上得电子,生成
H,总反应式为:Zn+H SO =ZnSO +H ↑;乙装置中只是锌片与稀硫酸间发生了置换反应:
2 2 4 4 2
Zn+H SO =ZnSO +H ↑,据此分析解答。
2 4 4 2
【详解】A.甲中形成铜锌原电池,锌作负极,失电子,铜作正极,H+在铜极上得电子,生成H,所
2
以甲中铜片表面有气泡产生,故A错误;
B.甲中铜为正极,乙中不构成原电池,铜片不是电极,故B错误;C.甲能形成原电池,乙不能构成原电池,所以产生气泡的速度甲比乙快,故C错误;
D.甲中铜片上氢离子得电子生成氢气,乙中锌和稀硫酸发生置换反应生成氢气,所以两烧杯的溶液
中氢离子浓度均减小,故D正确;
故选D。
3.(2019·上海交大附中高一月考)LED(Light Emitting Diode)即发光二极管,是一种能够将电能转化
为光能的固态半导体器件。如图是某课外活动小组设计的用化学电源使 LED 灯发光的装置。下列说法不
正确的是( )
A.装置中存在“化学能→电能→光能”的转化
B.溶液中 SO 2-向负极移动
4
C.铜为阳极,锌为阴极
D.如果将锌片换成铁片,则电路中的电流方向不变
【答案】C
【解析】A.装置中通过发生原电池反应,将化学能转化为电能,然后发光二极管发光,将电能转化
为光能,A正确;
B.溶液中Zn为负极,Cu为正极,阴离子(SO 2-)向负极移动,B正确;
4
C.此装置为原电池,电极只讲正、负,不讲阴、阳,C错误;
D.如果将锌片换成铁片,Fe的金属活动性仍大于Cu,则电路中的电流方向不变,D正确;
故选C。
4.在金属活动性顺序中a、b均排在氢前面,a可以从b的硝酸盐溶液中置换出b。将a、b用导线相连
放入CuSO 溶液中,下列叙述不正确的是( )
4
A.导线上有电流,电流方向由a到b
B.a极质量减小,b极质量增大
C.b极上析出氢气
D.a极发生氧化反应,b极发生还原反应
【答案】AC
【解析】【分析】a可以从b的硝酸盐溶液中置换出b,说明金属活泼性:a>b。将a、b用导线相连放入CuSO 溶液中,构成原电池,a是负极、b是正极。
4
【详解】A.导线上有电流,电流方向由b到a,符合题意,A正确;
B.在该原电池中,a极为负极发生失电子的氧化反应,质量减小,b极为正极,发生得电子的还原反
应生成Cu,质量增大,不符合题意,B错误;
C.b极上发生电极反应为:Cu2++2e-=Cu,不会析出氢气,符合题意,C正确;
D.a极为负极发生失电子的氧化反应,b极为正极发生得电子的还原反应,不符合题意,D错误;
答案选AC。
5.(2019·天津芦台二中高一月考)某小组为研究原电池原理,设计如图装置。下列叙述不正确的是
( )
A.无论a和b是否连接均可形成原电池
B.a和b不连接时,铁片上会有金属铜析出
C.a和b用导线连接时,铜片上发生的反应为Cu2++2e-= Cu
D.无论a和b是否连接,铁片均会溶解,溶液从蓝色逐渐变成浅绿色
【答案】A
【解析】A.a和b不连接时,不构成原电池,A错误;
B.a和b不连接时,铁片上会有金属铜析出,B正确;
C.a和b用导线连接时,铜片为正极,所以铜片上发生的反应为 ,C正确;
D.无论a和b是否连接,铁片均会溶解,溶液从蓝色逐渐变成浅绿色,D正确。
答案选A。
6.(2020·福建省福州三中高一期中)由质量均为 10 g 的铁片﹑铜片和足量的 CuSO 溶液组成原电
4
池装置,经过一段时间后,两电极的质量差变为 12 g,则下列说法正确的是( )
A.铁片溶解了 12 g
B.导线中通过了 0.2 mol 电子
C.铜片上析出了 6 g CuD.铜片溶解了 6.4 g
【答案】B
【解析】负极发生:Fe-2e-=Fe2+,正极发生:Cu2++2e-=Cu,设有xmolFe在负极上反应,则正极生成
xmolCu,则(10+64x)-(10g-56x)=12,x=0.1mol,则
A.m(Fe)=0.1mol×56g/mol=5.6g,故A错误;
B.x=0.1mol,则转移的电子的物质的量为0.2mol,故B正确;
C.m(Cu)=0.1mol×64g/mol=6.4g,故C错误;
D.在正极上析出m(Cu)=0.1mol×64g/mol=6.4g,而不是溶解,故D错误;
答案选B。
7.一种新型环保电池是采用低毒的铝合金(丢弃的易拉罐)、家庭常用的漂白水、食盐、氢氧化钠(化
学药品店常见试剂)等原料制作的。电池的总反应方程式为2Al+3ClO-+2OH-=3Cl-+2AlO-+HO。下列
2 2
说法不正确的是( )
A.该电池的优点是电极材料和电解质用完后可以更换
B.该电池发生氧化反应的是金属铝
C.电极的正极反应式为3ClO-+3HO+6e-=3Cl-+6OH-
2
D.当有0.1 mol Al完全溶解时,流经电解液的电子个数为1.806×1023
【答案】D
【解析】A、该电池所用材料都是生活中常见的,电极材料和电解质用完后可以更换,A项正确;
B、金属铝是原电池的负极发生氧化反应,B正确;
C、在正极上,发生还原反应,电极反应为:3ClO-+3HO+6e-=3Cl-+6OH-,C正确;
2
D、电子只能流经导线,不能流经电解液,D不正确;
答案选D。
8.铅蓄电池是最早使用的充电电池。目前汽车上使用的电瓶大多数仍是铅蓄电池,其电池反应为:
Pb+PbO +2HSO 2PbSO +2HO,下列说法正确的是
2 2 4 4 2
A.该电池放电过程中,溶液的pH值增大
B.放电时,电池的负极反应为:Pb-2e-= Pb2+
C.该电池的充、放电过程互为可逆反应
D.放电过程中,电子的流向为:负极→导线→正极→HSO 溶液
2 4
【答案】A【解析】A. 放电时有硫酸消耗,电解质溶液的pH值增大,A项正确;
B. PbSO 是难溶物,正确的电池的负极反应为:Pb-2e-+ SO 2-= PbSO ,B项错误;
4 4 4
C. 该电池的充、放电过程条件不一样,不互为可逆反应,C项错误;
D. 电子不会流过HSO 溶液,D项错误;
2 4
答案选A。
9.(2020·河北省唐山一中高一月考)常温下,将除去表面氧化膜的Al、Cu片插入浓HNO 中组成原
3
电池(图1),测得原电池的电流强度(I)随时间(t)的变化如图2所示,反应过程中有红棕色气体产生。
下列说法错误的是( )
A.0~t 时,原电池的负极是Al片
1
B.0~t 时,正极的电极反应式是 +2H++e−=NO↑+H O
1 2 2
C.t 后,原电池的正、负极发生互变
1
D.t 后,正极上每得到0.3mol电子,则负极质量减少2.7g
1
【答案】D
【解析】【分析】0~t 时,铝为原电池的负极,铜为正极,到t 时,铝在浓硝酸中钝化后不再反应,
1 1
此时铜又成了原电池的负极。
【详解】0~t 时,铝为原电池的负极,铜为正极,到t 时,铝在浓硝酸中钝化后不再反应,此时铜又
1 1
成了原电池的负极。
A、0~t 时,原电池的负极是Al片,故A正确;
1
B、0~t 时,硝酸根离子在正极得电子生成红棕色气体NO ,正极的电极反应式是NO -+2H+
1 2 3
+e−=NO↑+H O,故B正确;
2 2
C、t 后,铝发生钝化,铜作负极,所以,电池的正、负极发生互变,故C正确;
1
D、t 后,铜是负极,每有0.3 mol电子发生转移,就有0.15 mol铜失去电子,负极质量减少9.6 g,故
1
D错误。故选D。
【点睛】本题考查原电池原理,通过图象判断不同时刻原电池的正负极为解答本题的关键,也是易错
点。
10.(2020·河南省林州市林虑中学高一月考)用铜片、银片、Cu(NO ) 溶液、AgNO 溶液、导线和盐
3 2 3
桥(装有琼脂—KNO 的U形管)构成一个原电池(如图)。以下有关该原电池的叙述正确的是( )
3
①在外电路中,电流由铜电极流向银电极;
②正极反应为Ag++e-=Ag;
③实验过程中取出盐桥,原电池仍继续工作;
④将铜片浸入AgNO 溶液中发生的化学反应与该原电池反应相同;
3
A.①② B.③④ C.②④ D.②③
【答案】C
【解析】由于活动性:Cu>Ag,则Cu作负极,电解质溶液为Cu(NO ) 溶液;Ag作正极,电解质溶液
3 2
为AgNO 溶液,盐桥形成闭合回路;
3
①在外电路中,电流由银电极流向铜电极,错误;
②正极为溶液中Ag+得到电子被还原变为Ag,电极反应式为Ag++e-=Ag,正确;
③实验过程中取出盐桥,因为不能形成闭合回路,所以原电池不能继续工作,错误;
④将铜片浸入AgNO 溶液中,发生的化学反应与该原电池反应相同,正确;
3
综上所述②④正确,故选C。
【点睛】原电池中正极得电子发生还原反应,负极失电子发生氧化反应,电子通过导线由负极流向正
极,电解质溶液中阳离子流向正极,阴离子流向负极。
11.(2020·山西省高一月考)已知化学反应:
a.
b.
请回答下列问题:
(1)上述两个化学反应中有一个不可用于设计原电池,它是__________(填写代号),其原因是__________;另一个可用于设计原电池,该原电池中,负极反应式是____________,正极反应式是
___________,电池总反应的离子方程式是_______________。
(2)如果利用化学反应Cu+2Fe3+=Cu2++2Fe2+,设计原电池,请在如图方框中标明电极材料和电解质
溶液的名称(图中“I”表示电流)。______、______、______
【答案】(1)a a是复分解反应,不是自发的氧化原反应 Cu-2e-═Cu2+ 2Ag++2e-═2Ag
Cu+2Ag+=Cu2++2Ag+ Cu
(2)不如铜活泼的金属或石墨 氯化铁或硫酸铁
【解析】(1)上述两个化学反应中有一个不可用于设计原电池,它是a(填写代号),其原因是a是
复分解反应,不是自发的氧化原反应;另一个可用于设计原电池,该原电池中,负极上铜失电子发生氧化
反应,正极上银离子得电子发生还原反应,负极反应式是Cu-2e-═Cu2+;正极反应式是2Ag++2e-
═2Ag;电池总反应的离子方程式是:Cu+2Ag+=Cu2++2Ag+;
故答案为:a;a是复分解反应,不是自发的氧化原反应;Cu-2e-═Cu2+;2Ag++2e-═2Ag;Cu+2Ag
+=Cu2++2Ag+;
(2)根据电池反应式知,负极上铜失电子发生氧化反应,正极上铁离子得电子发生还原反应,所以
负极材料应该是铜,正极材料应该是不如铜活泼的金属或石墨,电解质溶液应该是氯化铁或硫酸铁都可,
故答案为:Cu;不如铜活泼的金属或石墨;氯化铁或硫酸铁。
12.某研究性学习小组对Mg和Al的性质进行了下列的实验及研究。
(1)以镁条、铝片为电极,稀NaOH溶液为电解质构成的原电池(如图1所示)时发现,刚开始时,电流
表指针向右偏转,镁条做负极;但随后很快指针又向左偏转,镁条表面有极少量的气泡产生。
①开始阶段,负极发生的电极反应式是________。
②随后阶段,铝片发生的电极反应式是_______;则镁电极发生的电极反应式是________。(2)经研究测定,镁与不同浓度的硝酸反应,生成气体产物的含量随HNO 浓度变化曲线如图2所示,
3
溶液中的产物有Mg(NO)、NH NO 和HO。96 mg Mg在1 L 4 mol•L−1的HNO 中完全溶解,并可收集到
3 2 4 3 2 3
22.4 mL(标准状况下)气体(忽略反应过程中HNO 浓度的变化),该反应的化学方程式是________。
3
【答案】(1)① Mg+2OH−−2e−===Mg(OH) ↓ ② Al+4OH−−3e−===AlO−+2H O 2H++2e−===H↑(或
2 2 2 2
2HO+2e−===H↑+2OH−)
2 2
(2)40Mg+100HNO===5NO↑+H ↑+NO↑+3N ↑+4NHNO +40Mg(NO )+41H O
3 2 2 2 4 3 3 2 2
【解析】(1)①镁较活泼所以做负极,Mg失电子变成Mg2+,负极反应为Mg+2OH−−2e−===Mg(OH) ↓;
2
②Mg虽比Al活泼,但Mg不能与NaOH溶液反应,而Al可与NaOH溶液反应,故Al作负极,失电子生
成Al3+,Al3+结合OH−生成AlO−,镁做正极,H+在镁电极上得电子生成氢气,电极反应式分别是Al+4OH−
2
−3e−===AlO−+2H O、2H++2e−=H ↑或2HO+2e−===H↑+2OH−;
2 2 2 2 2
(2)金属镁的物质的量是0.004 mol,气体的物质的量是0.001 mol,Mg与总气体物质的量比值为4:
1,由图知:NO :H:N:NO=1:1:3:5,设NO 、H、N、NO系数分别为1,1,3,5,Mg为40。
2 2 2 2 2 2
根据电子转移的数目:产生1 mol NO ,转移1 mol。同理H:2 mol,N:10 mol,NO:3 mol,因此总共
2 2 2
转移电子为(1×1+1×2+3×10+5×3) mol=48 mol,但是40 mol的Mg,转移80 mol电子,还差了32 mol,所以
一定是还有NH NO 生成,生成1 mol NH NO ,转移8 mol电子,现在有32 mol电子,所以是4 mol
4 3 4 3
NH NO ,再根据N守恒,H守恒可知反应为
4 3
40Mg+100HNO ===5NO↑+H ↑+NO↑+3N ↑+4NHNO +40Mg(NO )+41H O。
3 2 2 2 4 3 3 2 2
13.镍镉可充电电池在现代生活中有着广泛的应用,装置如图所示,它的充、放电反应为
Cd+2NiOOH+2H O Cd(OH) +2Ni(OH) 。
2 2 2
请回答下列问题:
(1)放电时,还原反应在 (填“a”或“b”) 极进行,负极的电极反应式为
,在放电过程中,正极附近的电解质溶液碱性会 (填“增强”或“减弱”)。
(2)镍镉废旧电池必须进行回收并集中处理,最主要的原因是
。【答案】(1)b Cd−2e−+2OH− Cd(OH) 增强
2
(2)镍镉废旧电池中残留的Cd2+、Ni2+等重金属离子易对土壤和水源造成污染
【解析】(1)由题给示意图知,镍镉电池中,电流方向是由 b极流向a极,故a极为负极,b极为正极;
放电时,正极发生反应NiOOH+H O+e− Ni(OH) +OH−,是还原反应;镉在负极发生氧化反应,分两步:
2 2
Cd−2e− Cd2+,Cd2++2OH− Cd(OH) ,负极反应式为Cd−2e−+2OH− Cd(OH) ;正极附近电解质溶
2 2
液的碱性增强,负极附近电解质溶液的碱性减弱。
(2)镍镉废旧电池中残留的Cd2+、Ni2+等重金属离子易对土壤和水源造成污染。
14.电子表所用的某种钮扣电池的电极材料为Zn和Ag O,电解质溶液为KOH,其电极反应式为:Zn
2
+2OH--2e-=ZnO+HO、Ag O+HO+2e-=2Ag+2OH-。
2 2 2
(1)原电池是一种__装置。
(2)钮扣电池的负极材料是___。
(3)钮扣电池正极发生的是___反应(填反应类型)。
(4)钮扣电池总反应方程式为___。
【答案】(1)将化学能转化为电能
(2)Zn
(3)还原反应
(4)Zn+Ag O=2Ag+ZnO
2
【解析】(1)根据原电池的概念,原电池是将化学能转化为电能的装置;答案为将化学能转化为电
能。
(2)根据电极反应式知,Zn元素化合价由0价变为+2价,锌失电子发生氧化反应,所以锌作负极;
答案为Zn。
(3)根据电极反应式知,Ag元素化合价由+1价变为0价,氧化银得电子发生还原反应,所以氧化银
作正极;答案为还原反应。
(4)由电极反应式为:Zn+2OH--2e-=ZnO+HO、Ag O+HO+2e-=2Ag+2OH-,两电极反应相加,
2 2 2
得钮扣电池总反应方程式为Zn+Ag O=2Ag+ZnO;答案为Zn+Ag O=2Ag+ZnO。
2 2
15.Ⅰ.氢能是重要的新能源。他的开发、储存和应用,是当前人们关注的热点之一。
(1)开发氢能的方法之一是分解水。开发特殊物质做催化剂,_______(填“能”或“不能”)降低水分解过程中所需能量。
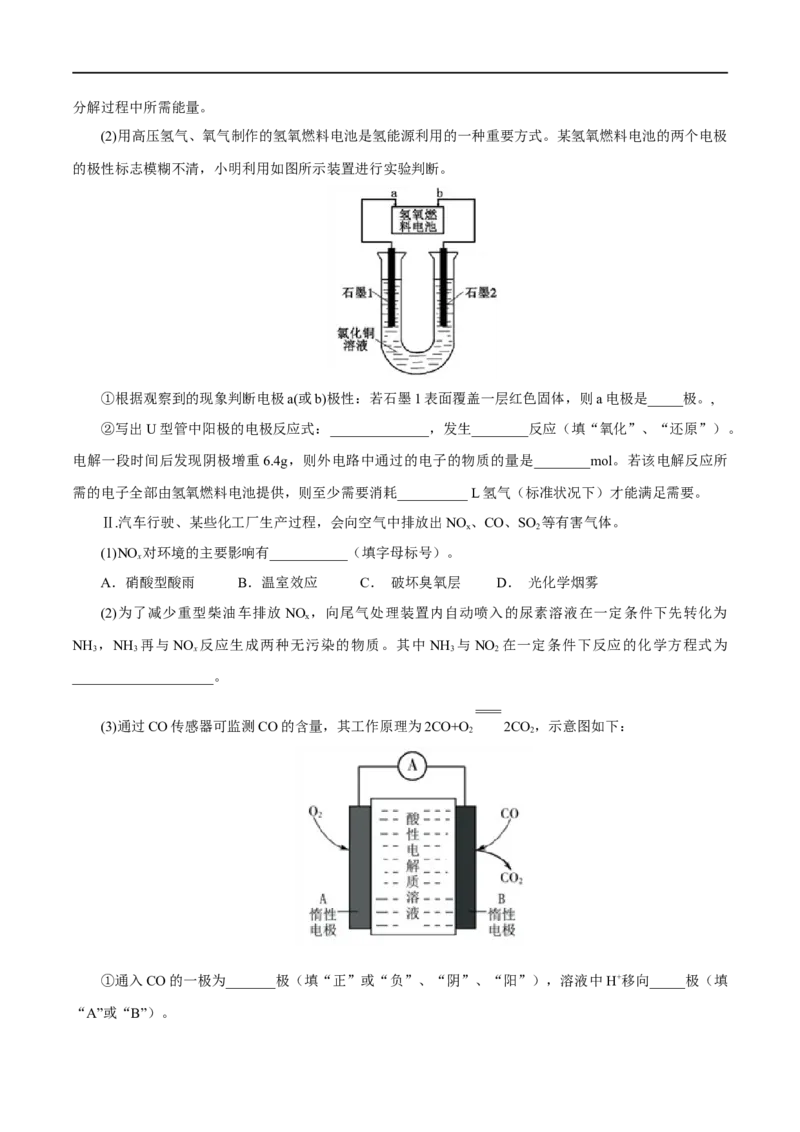
(2)用高压氢气、氧气制作的氢氧燃料电池是氢能源利用的一种重要方式。某氢氧燃料电池的两个电极
的极性标志模糊不清,小明利用如图所示装置进行实验判断。
①根据观察到的现象判断电极a(或b)极性:若石墨1表面覆盖一层红色固体,则a电极是_____极。,
②写出U型管中阳极的电极反应式:______________,发生________反应(填“氧化”、“还原”)。
电解一段时间后发现阴极增重6.4g,则外电路中通过的电子的物质的量是________mol。若该电解反应所
需的电子全部由氢氧燃料电池提供,则至少需要消耗__________ L氢气(标准状况下)才能满足需要。
Ⅱ.汽车行驶、某些化工厂生产过程,会向空气中排放出NO 、CO、SO 等有害气体。
x 2
(1)NO 对环境的主要影响有___________(填字母标号)。
x
A.硝酸型酸雨 B.温室效应 C. 破坏臭氧层 D. 光化学烟雾
(2)为了减少重型柴油车排放NO ,向尾气处理装置内自动喷入的尿素溶液在一定条件下先转化为
x
NH ,NH 再与NO 反应生成两种无污染的物质。其中 NH 与NO 在一定条件下反应的化学方程式为
3 3 x 3 2
____________________。
(3)通过CO传感器可监测CO的含量,其工作原理为2CO+O 2CO,示意图如下:
2 2
①通入CO的一极为_______极(填“正”或“负”、“阴”、“阳”),溶液中H+移向_____极(填
“A”或“B”)。②写出B电极的电极反应式:_____________。
【答案】Ⅰ. (1)不能
(2)①负 ②2C1−−2e− Cl↑ 氧化 0.2 2.24
2
Ⅱ. (1)ACD
(2)8NH +6NO 7N+12H O
3 2 2 2
(3)①负 A ②CO−2e−+H O CO+2H+
2 2
【解析】Ⅰ. (1)催化剂只能降低反应的活化能,不能改变ΔH;开发特殊物质做催化剂,不能降低水分
解过程中所需能量。
(2)①石墨1表面覆盖一层红色固体,石墨1的电极反应式为Cu2++2e− Cu,石墨1为阴极,阴极与
氢氧燃料电池的负极相连,则a电极为负极。
②由于Cl−放电能力大于OH−,U型管中阳极的电极反应式为2Cl−−2e− Cl↑,电解池中阳极发生氧
2
6.4g
化反应。阴极析出n(Cu)= =0.1 mol,阴极电极反应式为Cu2++2e− Cu,外电路中通过电子物
64g/mol
质的量为0.1 mol×2=0.2 mol。H 参与负极反应,1 mol H 失去2 mol电子,若该电解反应所需的电子全部
2 2
由氢氧燃料电池提供,至少消耗 H 物质的量为 0.1 mol,在标准状况下 H 的体积为 0.1 mol×22.4
2 2
L/mol=2.24 L。
II. (1)NO 对环境的影响有:硝酸型酸雨、破坏O 层、光化学烟雾,答案选ACD。
x 3
(2)NH 与NO 反应生成两种无污染的物质,根据原子守恒,生成N 和HO,NH 与NO 在一定条件下
3 x 2 2 3 2
反应的化学方程式为8NH +6NO 7N+12H O。
3 2 2 2
(3)根据工作原理2CO+O 2CO,其中CO发生失电子的氧化反应,O 发生得电子的还原反应。
2 2 2
①原电池中负极发生失电子的氧化反应,阳离子移向正极;通入 CO的一极为负极,B极为负极,通
入O 的一极为正极,A极为正极,溶液中H+移向A极。
2
②B电极为负极,1 mol CO失去2 mol电子生成1 mol CO ,结合酸性电解质溶液以及原子守恒,B电
2
极的电极反应式为CO−2e−+H O CO+2H+。
2 2