文档内容
2021-2022 学年高二化学重难点专题突破
模块一 原子结构与性质
专题 01 基态原子的核外电子排布
一、选择题
1.各电子层排布电子的总数遵循以下规则:①每层最多容纳2n2个电子;②原子最外层电子数≤8;③原子次外
层电子数≤18。决定这3条规律的电子排布规则是( )
A.能量最低原理 B.泡利不相容原理
C.洪特规则 D.能量最低原理和泡利不相容原理
2. 下列各微粒的电子排布式或轨道表示式不符合能量最低原理的是 ( )
A.Fe2+ 1s22s22p63s23p63d6
B.Cu 1s22s22p63s23p63d94s2
C.F
D.Na+
3. 下列判断正确的是 ( )
A.锂原子的核外电子排布式写成1s3违背了能量最低原理
B.电子的吸收光谱和发射光谱总称原子光谱
C.处于基态的氧原子轨道表示式写成 违背了泡利原理
D.某种基态原子中可能存在运动状态完全相同的电子
4.(双选)下列各原子或离子的电子排布式错误的是 ( )
A.C:1s22s12p3 B.O2-:1s22s22p6
C.Si:1s22s22p63s33p1 D.Al3+:1s22s22p6
5.如表中每个选项都有甲、乙两种表述,这两种表述指向的不是同种元素原子的是 ( )
选项 表述甲 表述乙
A 3p能级有1个空原子轨道的基态原子 核外电子排布为1s22s22p63s23p2的原子
2p能级无空原子轨道且有1个未成对电子的基
B 最外层电子排布为2s22p5的原子
态原子
C M层全充满而N层电子排布为4s2的原子 核外电子排布为1s22s22p63s23p64s2的原子D 最外层电子排布为4s24p5的原子
最外层电子数是核外电子总数的 的原子
6.某元素基态原子M层上有一个未成对的单电子,则该基态原子价电子排布不可能是 ( )
A.3d14s2 B.3d94s2 C.3s23p1 D.3s23p5
7.(双选)若某元素原子处于能量最低状态时,电子排布式为1s22s22p63s23p63d104s24p64d15s2,则下列说法正确的
是 ( )
A.该元素原子处于能量最低状态时,原子中共有3个未成对电子
B.该元素原子核外共有5个电子层
C.该元素原子的M层共有8个电子
D.该元素原子最外层有2个电子
8.下列有关核外电子排布的式子不正确的是 ( )
A. Ge的电子排布式:1s22s22p63s23p63d104s24p2
32
B.K的电子排布式:1s22s22p63s23p64s1
C.N原子的轨道表示式为
D.S原子的轨道表示式为
9.短周期Y元素的p轨道上有3个未成对电子,则该元素的最高价氧化物的水化物的化学式可能是( )
A.HYO B.H YO C.HYO D.HYO
3 4 4 4 2 2 4
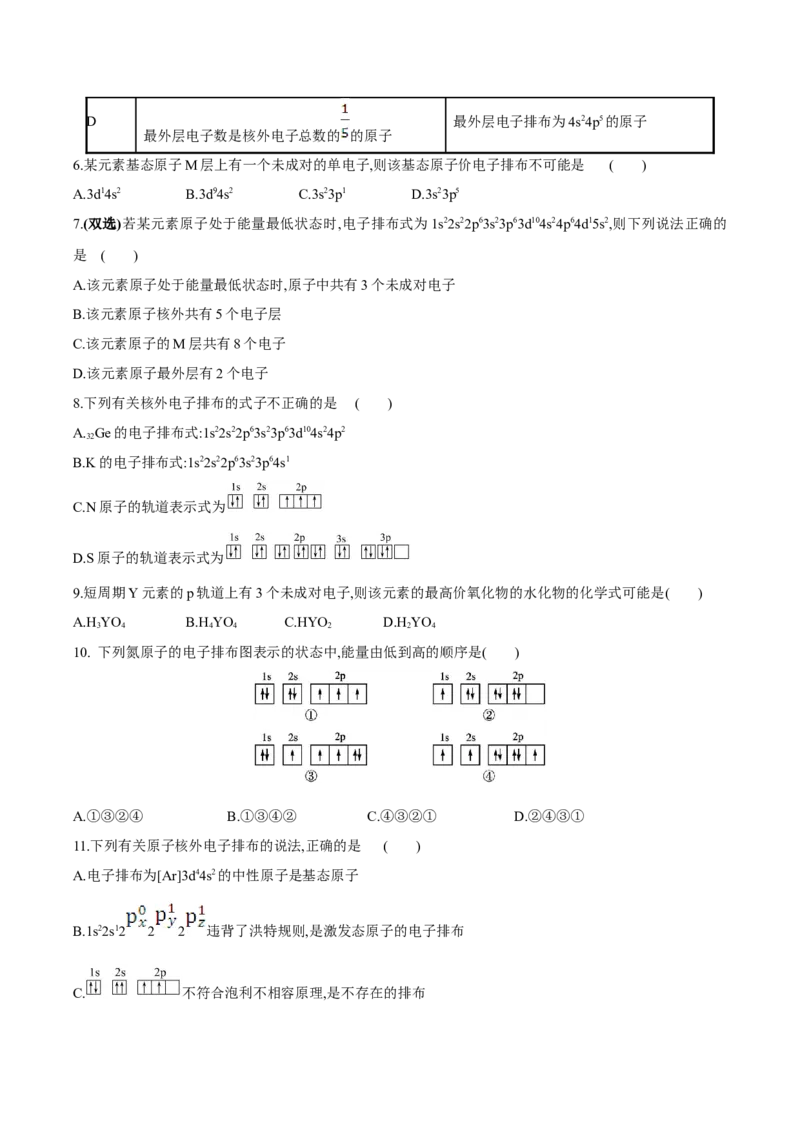
10. 下列氮原子的电子排布图表示的状态中,能量由低到高的顺序是( )
A.①③②④ B.①③④② C.④③②① D.②④③①
11.下列有关原子核外电子排布的说法,正确的是 ( )
A.电子排布为[Ar]3d44s2的中性原子是基态原子
B.1s22s12 2 2 违背了洪特规则,是激发态原子的电子排布
C. 不符合泡利不相容原理,是不存在的排布D.原子结构示意图为 的原子,核外电子云有3种不同形状
12.X、Y、Z为短周期元素,X原子最外层电子排布式为ns1,Y原子最外层电子排布式为(n+1)sn(n+1)p2n,Z原
子的价层电子排布式可以表示为csccp2c。X、Y、Z三种元素形成的化合物的化学式不正确的是 ( )
A.XYZ B.X YZ C.X YZ D.XYZ
2 3 2 4 2 2 3 3
二、非选择题
13.按要求回答下列各小题:
(1)镁元素基态原子核外M层电子的自旋状态 (填“相同”或“相反”)。
(2)Fe成为阳离子时首先失去 轨道电子,Sm的价层电子排布式为4f66s2,Sm3+的价层电子排布式为
。
(3)基态铁原子价层电子的轨道表达式为 。
(4)基态锌原子核外电子排布式为 。
(5)氮原子价层电子的轨道表达式为 。
(6)基态钴原子核外电子排布式为 。
(7)基态Fe3+核外电子排布式为 。
(8)基态锗原子的核外电子排布式为[Ar] ,有 个未成对电子。
(9)镍元素基态原子的电子排布式为 ,3d能级上的未成对电子数为 。
(10)基态砷原子的核外电子排布式为 。
14.(1)基态钛原子的电子排布式为 ;同周期的基态原子与钛原子未成对电子数相同
的元素还有 种。
(2)据媒体报道,法国一家公司日前研发出比当前广泛使用的锂电池成本更低、寿命更长、充电速度更快的钠
离子电池。
Te元素基态原子的价电子排布式为 ;基态钠原子中,核外电子占据的原子轨道总数为
。
(3)镍及其化合物是重要的合金材料和催化剂。基态镍原子的价电子排布式为 ,排布时最高电
子层的电子所占的原子轨道电子云为 形。
15.回答下列问题:
(1)下列叙述中,正确的是________(填字母,下同)。
a.在一个基态多电子的原子中,可以有两个运动状态完全相同的电子
b.在一个基态多电子的原子中,不可能有两个能量完全相同的电子
c.在一个基态多电子的原子中,M层上的电子能量肯定比L层上的电子能量高d.如果某一基态3p能级上仅有2个电子,它们自旋状态必须相反
(2)第2、3、4周期元素原子中p轨道半充满的元素是______________________,前4周期元素中,基态原子未
成对电子数与氮相同的元素有____________种。
(3)镓与硼同主族,写出镓元素原子的电子排布式: ____________________。
(4)写出Ti基态原子的电子排布式___________,基态Co2+的电子排布式____________。
(5)已知X、Y和Z三种元素的原子序数之和等于42。X元素原子的4p轨道上有3个未成对电子,Y元素原
子的最外层2p轨道上有2个未成对电子。X跟Y可形成化合物XY,Z元素可以形成负一价离子。X元素
2 3
的符号是________;Y元素基态原子的轨道表示式为____________,Z元素的名称是______________。
16. 含氟化合物被用于预防龋齿、饮水加氟及其他口腔卫生产品中。起初是用氟化钠(NaF)来为饮用水加氟,
但后来逐渐被氟硅酸(H SiF)及其盐氟硅酸钠(Na SiF)代替。完成下列填空:
2 6 2 6
(1)写出氟原子的电子排布式: ,氟原子有 种能量不同的电子。
(2)镁带能在 CO 中燃烧生成氧化镁和单质碳。氧化镁的电子式为 ,CO 的结构式为
2 2
。与镁同周期、离子半径最小的元素原子的价电子排布式为 ,其1个原子中能量最高的电子有
个。倒卖拉黑不更新,淘宝唯一免费更新店铺: 知二教育