文档内容
高中化学 第一章从实验学化学 第一节化学实验基础知识
物质的分离是将几种物质分开,分别得到几种纯净物 将物质的分 离与提 块状固体用镶子 取用固体
高 抓住 中 物质 化 的特 物 杂 性 学 质 质 寻 的 除 找 提 去第 突 纯 而 破 是 得 口 一 将 到 混 纯 合 净章 物 物 物 中 质 质 从 的 检 少 验 实 量 和实验 验 综合 学 题 化学 纯混 第 淆 二节化学 学 误 计 习 区 量 在实(验瓶中塞倒 较的放 多 , 粉 应液 标 末 体 签用 状 用 向 用 倾 手 药 倒 心 匙 法 ,口挨口)取用液体 取 仪 用 器 药 品的 酒 不 鏡 吹 纺 灯 备 , 精 先 不 灭 热 超 后 源 过 添 , 酒 2/3 温 精 ,不 度 少 可 于 达 1 4 / 0 4 0 ,用 ~ 外 50 0 < P 5 , 不对火 ,
物质的性质误和认仪为器体特积点是紧2密2.4联 L系,物实质验的基量本就操是作1 mol 单位物质的量的吸气 用 取体 , 少所 垂 量占 直 液的 悬 体体 滴 用积 , 滴 不 管 倒 置 ( ) 专概 符 念 号 实 其 世验 符 口 号 压中 仅 强 与 有的 温 关 度 内容 喷灯温度可达100 同 气0 温 体b 同 含 压 有 下 相 , 同 相 数 同 目 体 的 积 分 的 子 任 何
取 力 少 緋 量 >忘 ( 记矗 不 或 分 杂 轟 増 适 由 件 析 质 一 、 量 于 , 物 过 編 不 ) 试 而 质 量 论 减 一 题 学 的 、 物 、 • 中 生 状 过 • 质 易 溶 出 往 态 量 鉴 分 解 现 往 , 杂 别 离 一 多 抓 而 质 题 、 > 种 住 带 必 简 易 限 一 入 答 须 复 制 个 气一 除 原 条 条 体般 尽 件 件 摩步 、 或 而 尔瓣 迷 忽 体 惑 略 积 性 公 其 物 必 式 条 他 质 须 分 遵 高 循 提 纯 学 知 习 能 误 区 22.4 L/mol 化 常 学 见 灼 危 伤 险 防 急 与 火 救 安 与 标 措 全 灭 准 施 措 火 状施况 表 下 达 单 的 式 位 数值 安 外 处理 气 全 事 体摩 及 故体 咨 积 意 的 阿 定 伏 律 加 德罗 适 漏 用 斗 范 水 围 浴 长 lo 颈 o 2 1t . 漏 .: 单 不 斗 以一 存 下纯 在 净 化 的 学 气 平 体 衡 或 的 混 气 合 体 气体
求 一 了 选 解 标 解 条 注 择 策 出 实 件 意 最 略 , 验 从 防 佳 是 综 安 而 火 除 解 合 全 导 、 杂 题 分 常 致 防 途 时 析 识 误 爆 径 应 后 及 选 炸 把 再 意 、 迷 做 外 防 惑 判 事 倒 性 断 故 吸 条 处 理 件 方 一 法 提 知 升 能提升 总 升 结 华 1 mol物危质险所化具学有品的标质志七识一别 符 单 魅 号 位 生 摩 质梳 知尔 量 理 识 分 仪 离 器 概念 公式 冷凝管 表 的 示 集 分 漏 含 体 液 斗 有 的 一 物 定 理 数 量 主 用 目 途 粒 要 用 上 子 p p 分 M V 口 前 = = 液 p n 先 R R 倒 萃 体T 时 T 检 反 出 取 上 应 查 , , 层 分 加 是 下 液 液 液 否 层 , 体 漏 液 从 液 体
通 使 过 用 动 方 阿 结 量 手 法 伏 合 这 实 和 加 质 一 验 操 德 量 核 , 作 罗 守 心 熟 注 定 恒 , 练 意 律 定 它 掌 事 及 律 是 握 项 其 和 其 常推 相 他 用论 关 物 化是 概 理 学进 念 量 仪行 及 之 器气 公 间 的体 式 换 计 进 算 算 行 的 的 换 桥 依 算 梁 据 , , , 但 通 要 一 常 灵 定 模 活 要 式 运 突 是 用 出 : , 物 已 注 质 知 学 意 的 一 法指导 总结 表达式 常 仪 用 器 I 顶号 ” 物匣位 塗 气 摩 瓶 尔(Mi) 注 事 意 项 从放 分 将 口 下 塞 小 出 液 层 孔 , 漏 上 。 放 斗 的 液 上 使 凹 时 玻 槽 漏 应 璃 对 斗 打 准 内 塞 开 上 或 外
操作的个先物后理顺量序,求算物质的量或求算另一个物理量 升华 大气压相等
操作的注意事项 、基本操作 知识 计可算耳公接式加热的仪器蒸发皿、 试 燃 管 烧 、 匙 堪 溶 垠 液 、 中”=c • V
操作I.的状目态的:"气态物质 7 "可以是实纯净京物,全也可以是混合物 梳理 容
应
器
器
和
/
反
隔网可加热或液浴蒸馋烧瓶
烧
、
杯
锥
、
形
烧
瓶
瓶心、(标准状况下)
化学与人2类.如健标康准状态(0巾、101 kPa)同温同压等 不,溶体性摩固尔体与液体的分离 适用范围 过滤 表示“物质的量”的单位 集气瓶、试剂瓶、滴瓶、
是 风 化 否 化 固 旅 学 易 、 态 态 与 潮 吸 环 解 水 4 尔 3 德 境 .、 . . 数 体 定 罗 保 值 积 量 常 护 史 : ( : 数 IJ 任 卩 在 个 状 何 ) 标 分 态 情 , 准 子 况 但 状 ) 下 数 况 的 的 值 下 体 任 不 , 积 何 一 1 为 m 气 定 2 o 2 体 是 l .4 气 均 2 L 2 体 存 .4 ( 在 L 即 / 一 m 阿 o 个 l 伏 气 体 加 摩 2.当大量 分体 固 离 1. 积 体 溶 蒸 四 析 于 发 要 出 溶 过 素 时 液 程 , 中 不 停 的 断 止 固 搅 加 体 拌 学 热 溶 , 质 法 余热 蒸干)5坚 适 竺 用范围 蒸发 实 本 验 操 基 作 量筒 对 子 常 符 象 爬 数 号 用 个 原 m时 组 子 o 不 l需 成 、 能 该 分 7 加 主 刻 物 每 取 子 热 小 要 度 质 座 用 、越 用 由 的 尔 原 离好 途 下 微 物 则 子 , 而 粒 质 : 、 不 上 含 次 原 反 增 粗阿 数 子应 大 启 略伏 越 团, , 普 量加 少 等 无 发 取德 ■微 注 生 液 0 罗 溶 观 刻 意 器 体 注 解 粒 度 事 ,明 , 子 计 线 项 精粒 不 量 , 度子 越 受 所 种 O 读 好 热 有 .l 类 数 , , 微 m . 平 量 不 L 观 嵐 视 筒 配 粒 乂 。 越 不 制
是 是 中 是 是 升 1 态 2 如 . . 否 否 某 否 注 否 华 , 注 1 易 易 些 易 1 意 易 一 S 意 .2 O 燃 體 成 被 标 挥 ’L 气 ,为 、 分 氧 准 足 发体 固 易 作 化 状 的 、体 态 爆 用 况 分 积 ,_ 下 子 是 \碳 物 数 否 原 质 未 在 子 的 必 标 数 聚 是 准 大 集 0 状 . 于 5 状 态 M 依 4 态 下 据 的 , , 蛭 如 类 在 为 标 液 化 试 的 准 态 状 学 剂 保 或 况 固 下 态 水 等 是液态 或固 利 1 球 2 用 . . 蒸 与 3 冷 沸 . 馋 支 要 水 点 烧 管 加 是 不 瓶 口 碎 下 同 加 下 瓷 口 , 热 缘 片 进 除 要 位 , , 去 垫 于 防 上 难 石 同 暴 口 挥 棉 一 沸 出 发 网 水 和指 , 平 不 温 线 挥 7 N F N 导 度 . e 发 a a 注 Q C 分 的 l ? 计 意 别 等 与 杂 的 化 与 溶 H 质 水 学 2 液 S O 适 银 、 反 ; 的 . 用 C C 应 电 U b 范 中 解 的 注 与 围 转 反 意 碱 移 应 事 溶 电 , 项 液 子 C ' 的 u 数 S 反 目 O 应 4 的 . , A 计 g N C 算 O u 。 : 或 玻 、 如 璃仪器 其 作 的 他 洗 基 涤 本 操 计量仪器 阿 常 伏 数 加 滴 德 定 管 罗 注 益 主 意 **工 要 使 商 概 符 用 用 亘 酸 管 溶 刻 念 准 号 途 前 式 盛 液 度 a 旦 要 滴 碱 ; 不 精 丄 洗 定 性 0 在 确 刻 净 管 、 管 表 0 至 . 度 并 0 盛 非 最 示 1 0 在 检 2 M . 酸 氧 下 1 1 k 上I 查 m 性 化 端 m M g L 方 是 o C 、 性 = , l 单 可 , 所 6 任 否 氧 溶 . 位 估 0但 含 何 漏 化 液 2 体 读 x不 的 粒 液 性 , l0 积 到 在 碳 子 2 , 溶 二 3 液 m 0 管 原 所 先 液 者 o . 体 0 l最 子 含 润 - 1 , 不 ' 里 m 上 数 的 洗 碱 能 所 L 端 粒 再 式 互 含 , 子 装 滴 代 最 数 溶 定 ; 事 大
是 腐 便 塑 铁 防 细 滴 防 3 子 4 中 啲 5 . . . 否 蚀 于 料 质 燃 口 瓶 止 注 中 注 的 水 注 具 性 取 瓶 容 、 瓶 变 意 的 意 解 意 C 有 一 用 、 器 防 、 H 质 物 原 弱 , 特 s 毒 - 铅 等 爆 广 C 质 子 电 溶 殊 O 性 皿 等 口 的 个 解 液 物 O 、 、 瓶 组 数 质 中 质 -物 、 成 , 的 摩 F 质 e , N 电 尔 , 的 a 如 离 质 z 啲 量 O 及 量 原 仪 N 物 小 z e 中 某 或 则 器 质 于 、 阴 些 分 的 O 1 阳 离 子 3 量 m 、 离 子 o 中 小 l C ; 子 的 的 于 2 1 方 H 个 溶 中 m 1 2 式 o 数 解 子 m 等 l / F o 比 , 数 放 物 e l 存 C 等 如 目 式 质 I; 3 理: 密 油 存 分 1 — 燥 溶 m 凉 T 封 封 放 器 z o 于 、 : 、 O l 中 C 、 水 避 水 蜡 H 存 | 时 !光 封 封 0 3 C 放 2 , 处 、 O O 由 H 于 , 溶 Fe 2 液 在 , .把 互 1. 分 不 3 体 溶 . 液 相 打 , 液 漏 溶 开 再 总 斗 的 塞 从 量 放 溶 子 上 不 气 ( 在 剂 , 口 超 体 非 ■ ( 铁 里 先 倒 过 的 标 - 标 架 溶 从 出 漏 气 体 准 准 台 解 下 上 斗 体 积 状 状 上 度 口 层 容 的 / 况 况 [ 静 差 放 液 积 体 x ) )2 置 别 出 体 的 积 2. 、 4 较 下 / 3 L L / 分 / 大 4 层 + m 8 F 的 . 2层 e的 o C 注 2 液 l 集 . I溶 4 意 : 合 L 质 分 溶 /m 体 适 散 液 o , — l 用 , 系 转 所 范 , 的 化 以 围 变 为 ' 胶 注 化 F 体 意 e 导 ( 粒 事 致 O 气 子 项 H 微 体 的 ) 观 的 数 : 粒 分 收 目 + 胶 子 液 溶 集 小 体 数 液_ ‘和 于 , X _ 目 体_ 体 原 溶 因 _ 的 积_ 积 溶 液 为 _ 装 变 _Y 的 液 体 胶 _ 置 化 L_ 溶 测 中 积 体 _ 气 。 _ 药 药 液 量/ 粒 _ F 密 L 如 _ 品 e品 的 _ 子 性 数 : _ 的 的 墅 _ 是 检 目 C 取 保 L 分 - 验 溶 用 存 子 的 液 量 的 浓 物 度 质 mol/L 一 度 定 物 溶 质 液 物 量 的 质 浓 的 配 的 度 量 温 制 浓 度计 容量 物 仪 配 瓶 质 器 使的 定 厂 厂 表 制 用量 义 符 单 达 注浓 号 位 式 计 移 意 天 璃 主 \ 度 算 、腐 事 平 棒 要 注 贮 与 、 洗蚀 项 或 、 用 意 存 质 称 涤性 量 胶 途 、 Q 品 量 量 并药 R 亠 o 不 银 筒 头 o 称 不 不 分 或 转品 o 反 球 、 滴 m p 前 溶 标 甄 能量 移放 w 应 o 不 一 管调 解 有 l 缨 取 、 直 在 、 Z 赢 定 零 温 精 L 、 震玻 不 接 质 島 规 点 C度 确 溶 荡璃 加 放 B r 温 § B 格 , 、 配 解 、器 热 在 的 度 壁 的 称 容 制 或 定皿 、 托 物 计 容 时 积 溶 稀 容中 不 质 盘 量 量 “ , 液 释 、称 换 的 程 上 瓶 左 用 、 摇申 塞 量 、 , 物 前 冷 匀 、 烧 右 易 检 却 、 杯 码 事 潮 漏 、 、 装 ” 项 解 , 1 转 瓶 不 、 玻 、
6 不 .注 到 意 2 m 常 o 见 l N 的 H 可 ,( 逆 因 反 其 应 为 , 可 1 逆 m 反 ol 应 N2 ) 和3 mol H2K应实际生产中 得 N-物质所含有的微粒数- 步骤 贴签
”,-物质的质量/g 摩尔质士 g养移液时洒出/洗液未注入, 単四、
X摩尔质量 误差分析 , 濱质减少,浓度下降高中化学第二章化学物质及其变化第一节物质的组成、性质和分类
常见物质的电子式 只讲种类 溶质被溶解物质
酸 式 式 的 盐 状 的 态 电 、 离 鼠 方 袞 程 与 式 化 三 学 \ 计 热 量 化 数 学 的 方 对 程 易 学 写 用 错 语 的 化 不讲个数 元素 宏观角度 物质的组成 组成 能溶解其他 溶剂 的 物 物 质 质
应问‘N 学习误区 分子、原子、离子 微观角度 溶液 一定温度下100g溶剂 形成
溶解度 饱和溶液中所含 溶质的质
石炭酸不是酸,纯碱不是碱 物理变化 ---------根据是否有新物质生成物质的变化 量(单位:g)
酸性氧化物不一定是非金属氧化物, 化学 变匕 丿、
非金属氧化物不一定是酸性氧化物 浊液 悬浊液
碱 属 性 氧 氧 化 化 物 物 不 一 一 定 定 是 是 金 碱 属 性 氧 氧 化 化 物 物 , 金 化学 性區 ) ------------- 讖 - 化 -- 学 ■ 变化物质的性质 乳浊液
金属钝化不是物理变化而是化学变化, 焰 概念 均一、稳定分散剂
色反应不是化学变化而是物理变
总结
I 单 -- 质 ---- 1 同素异形飼 分 作 子 用 间 力 升华 混合物 分类 兰 畐 溶 胶 胶 ( ( 如 如 氢 烟 氧 、 化 雾 铁 ) 胶体)
分子晶体 固溶胶(如烟、水晶)
知识
游离态 梳理 某 沉 些 胶 条 体 件 等 加热、加反电荷 下聚
组成、I I神成 共价键U" U〜 知能提升 学法 ,由安胶粒吸附离子而带电, 性
化合态 ;素~~—物质一原子一—原子胴体 指导 胶体 质/电冰 外加电场作用下定向运动
布朗 胶粒不停地做 运动
化合物 n离子键 无规则运动
离子 〉离子顚体
基本概念 丁达尔一束光通过胶体 效应
宏观角度 微观角度 宏观角度 元素符号 表示构成 物质 化学用语 性 按 质 组 分 成 类 产生“光路”
微粒结构示意图 的微粒 稳定 同种电荷,相互排斥,
知道分子、原子、离子、元素等概念的含义及表示方法 电子式 原因 不易聚沉
知道物理变化、化学变化和物理性质、化学性质 化学式、分子式、最简式、善枣写枣亠 结构式、
正确地对无机物进行分类,尤其能分辨酸、碱、盐、氧化物 结构简式 组成或结构 丿Fe(OH),胶体的制备:向沸水 制备与
物质的 /]中滴加饱和FeCI,溶液,震荡
能从不同的角度区分化学反应类型 化学方程式 分类』 提纯 水解法 | 加热形成透明红褐色体系
区分溶液、浊液、胶体,了解胶体的性质 电离方程式 表 变 示 化 物 质 善析法 常用于分离、提纯胶体
判断同位素、同素异形体、同分异构体、同系物 离子方程式 原理:胶体颗粒不能透过 半
透膜;离子、小分子可 透过
热化学方程式 同种元素 半透膜
熟 正 学 记 确 式 并 书 、 正 写 分 确 常 子 书 见 式 写 的 、 常 电 结 见 子 构 元 式 式 素 、 和 的 结 结 名 构 构 称 示 简 和 意 式 符 图 号 、 化 化 书 学 写 用语 的 电 强 极 碱 反 、 应 大 式 多数盐、活泼金属氧化物 萬子化合物 按化 分 学 类 键 纯净物 ' ) 单质 金属、非金属 氢化
酸、酸酊、非金属氢化物 共价化合物 物
理解化合价的概念和原则,根据化合价 正确
书写化学式或根据化学式求出化合价 强酸、强碱、大多数盐、活泼金属氧化物 强电解质 电解质 按是否 化合物/ —
知道质量守恒定律的含义。正确书写化学方 程式、 弱酸、弱碱、水 弱电解丿 点离分类 、 碱、盐 Y 、酸、
热化学方程式、离子方程式、电极反应式 多数有机化合物、非金属氧化物、氨气 冃5电解质 F同种元棗] 有机化合物高中化学 第二章 化学物质及其变化 第二节离子反应
加强概念的辨析
熟记物质溶解性表,强弱电解质 知 提 能 升 (强酸、强碱、大多数盐)水溶液中完全电离 弓虽电解质 水 下 溶 可 液 导 中 电 或 的 熔 化 融 合 状 物 态
熟记一些重要的离子方程式 电解质
掌握与量有关的离子方程式书写:过量问题处理 原 (弱酸、弱碱、少数盐)水溶液中部分电离 弱电解质 基础 单质与混合物既不是电解质也不是非电解质。]
则是 “以少 定多”原则。一定量要对应成比例 电解质强弱与溶解性及导电性无关。
1.像CO、NH:这些溶于水能导电是因为生成酸或碱 电离 (非金属氧化物、有机物)水溶液中及熔融状态下均不导电的化合物 非电解质
出离子导电,而自身不能电离,故称为非电解质 常见可生成沉淀的离子
2 混 3 但 . . 电 合 像 溶 解 物 一 于 质 既 些 水 和 不 难 的 非 是 溶 全 电 电 性 部 解 解 盐 电 质 质 虽 离 均 也 然 , 为 不 在 所 化 是 水 以 合 非 中 是 物 电 溶 强 , 解 解 电 单 质 度 解 质 不 质 大 和 , 概 辨 念 析 总 升 结 华 C 但 O 未 ?、 身 N 不 H 导 ,等 电 与 , 水 是 反 非 应 电 产 解 物 质 可导电 离 , 子 反应 阳 & 离 + 子 C 「 co O ; 、 ; - P 、 - 0 、 「 S S O 0 ; 阴 「 - 离 、 、 子 SiO
4.电解质溶液的导电性强弱由自由移动的离子 的电荷数和 电解质在溶液中进行的离子间的反应 概念
Ba2+
SiO;-、PO「、
浓度决定,与电解质的强弱无关 丿 学习 SCO「;、-Br-、I-、S2-、
误区 Ag+ OH、
知识缺陷,如:混淆"有色"与“澄清",不 能掌握 COT、sof
物质的溶解性,物质间的化学反应 知识 气体 CO?、改、CNuH2\“ F SeO2+?. 等M/+ S-、OFF、COT、SOT
审题不细,如:忽略了题设的限制条件
梳理
挖隐不力,如:溶液的酸碱性,一些离子 难电离
具有强氧化性 物质 弱酸、弱碱、水
离子共存
思维不全,如:复杂问题需要定性和定量结合 判断
色合物 Fe(SCN),(血红色)
前 液 提 或 是 熔 化 融 合 状 物 态 , 能 其 否 次 导 在 电 水 溶 电解质和非电解质 苴 「 水解 Fe " 、 Al ” 与 CO ; ] HCO ; 、 [ A 1 ( OH ) ,
概念辨析 学法
电离程度是否完全 强电解质和弱电解质
指导 三种特殊情况 MnO;、Cl。-、NO? (H*)与S*、Fe2+J xSOj
导 强 电 弱 的 与 实 电 质 解 : 质 自 的 由 强 移 弱 动 没 的 有 电 必 荷 然 , 联 导 系 丿 电 - 性 电离和溶液的导电性 糸 1 2 . . 符 化 写 合 学 正 客 式 确 观 正 标 事 确 准 实 : 酸性溶 F M e" n 与 0 「 7 「 与 、 S C -、HS cicr 与 cr
强拆弱不拆 离 误 子 判 方 断 程式 的正 溶 大 存 液 量 的 中 共 判 离 断 子 能否 H 可 H + C 将 与 O F ; N e O > 与 ; 、 A 组 「 IO 合 等 ; 具 还 不 有 原 能 强 性 大 氧 离 量 化 子 共 性 氧 存 , 化 3 4 5 、 . . . 符 反 6 电 . 号 应 符 荷 、 无 合 守 条 遗 题 恒 件 漏 设 齐 条 全 件丿 原则 液中 守恒 CIO?与 Cl 原 电 子 荷 守 守 醉 恒 恒 -与sof
易溶拆,难溶不拆 物质拆 符合实际
与不拆 HCO;与Mg”、NH:虽然能水解 但 离子方程式 的书
微溶物清拆浊不拆 总的水解程度不大,能大量存在 写 写:写出正确的化学方程式
浓盐酸、浓硝酸拆,浓硫酸不拆 原子守恒 一色:记住有 步骤 拆:可溶于水的强电解质拆成离子
不平 子 四反应 复分解反应 删:删除等量相同离子,化学计量 数
电荷守恒 二,性:溶液的 氧化还原反应 最简化
反 滴 应 加 物 顺 的 序 用 的 量 不 不 同 同 产物对不对 电子得失守恒 双水解反应 记 强 除 关 忆 拆 同 系 口 弱 离 量 诀 不 子 [ : 拆 保 正 删 证 负 意义 溶液 查 中 : 化 检 学 查 反 是 应 否 的 守 实 恒 质为离子间的反应
电荷平丿 可表示所有同一类型反应高中化学 第二章 化学物质及其变化 第三节氧化还原反应
1 区 .认 分 识 氧 氧 化 化 还 还 原 原 反 反 应 应 与 的 四 本 大 质 基 和 本 特 反 征 应 , 类型的关系 学习 有化合价升降,且升降总值相等 特征 化合价升高, -ne - , 被氧化
2.分析氧化还原反应的四对基本概念 误区 基本概念 氧化剂+还原剂=还原产物+氧化产物
3.氧化性、还原性强弱是电子得失难易而不是多少 丿/ 强氧化性)(强还原性)(弱还原性)(弱氧化
性)
总结 化合价降低,+n€ ,被还原
升华 电子的转移(或 电子 四组基本概念之间的关系
1.运用模型熟记氧化还 对 电 的 子 偏 数 移 相 ) 等 , 且得失 实质
原反应的基本概念 电子转移 表 双线桥法
示方法
2.运用口诀记忆氧化 还原 知能 单线桥法
反应的基本概念
提升
电子得失守恒 歧 核心 写化学式、标化合价、列变 配 化 系 、 数 、 步 查 骤 其 求 他 总 、 数 验 、 证
化型一逆向配平法 归中型 3.掌握氧化还原 反 化原
——正向配平W 应的配平技巧 应配
涉及复杂化学式,无乎 '、) 其元素化合价一零价法 (技厄 缺项型 一 守恒原则确定 缺现欷 ' 知识
為复杂原子团视为一个整体—"丿 进行标价 学法
一整体标址琶一 梳理 指导
四大反应类型 与氧化
还原反 应的关系
氧化性:氧化剂>氧化产物
电子得失守恒
氧 还反 质量守恒 的平 电荷守恒
方法 正向配平
逆向配平
______________ 零价配平
基本方法是化合价的 升 降法,如是缺项一 般为 缺项配平
酸、碱和水
四对基本概 塗的
考查
单质 F2、。2、。2、Brz等
还原性:还原剂=>还原产物 、化合价降低,被还原 常见 氧化 氧化物MnOz、NO?等
氧化性:F2>Cb>Br2:>l2>S 根据物质活动性 氧 得 化 电 剂 子 , , 化 还 合 原发 价降 生 低 还 , 生 被 成 剂 过氧化物H2O2、Na2O2x过氧乙酸等
还原性:K>Ca>Na>Mg Hg>Au 比较判断 氧化性与还 原性 原 还 反 原 应 剂 , , 还 升高 原 , 产 物 被 氧 化 化 合 发 价
强弱的 判断方法A 失电子, 生氧 生成氧化产 盐 KMnO,、K2Cr2O,s FeCh、铜盐等
根据反应条件,贝UB>E 化反应, 物 《论合 价升高,被氧化 常见 还原 J酸 浓硫酸、HNO” HCIO等
一 属 氧 强 性 还 强 般 性 化 ; 越 原 非 越 性 金 强 性 金 强 越 属 , 越 , 根 单 原 据 质 性 原 右 逐 电 上 渐 池 氧 増 、 化 强 电 性 解 逐 池 渐 的 增 电 强 极 ; 反 根 应 据 比 元 较 素 判 周 根 断 期 据 表 元 左 素 下 化 还 / 依 易 据 , : 而 电 非 子 多 得 少 失 难 氧 的 化 规 还 律 原 , 反应 价 转 强 难 态 化 弱 易 规 规 规 规 律 律 律 律 . , 邻价 最 中 萼 强 易 易 高 间 氧 找 失 , 价 价 化 强 电 跳 氧 有 + ( 子 位 强 化 两 强 , 难 还 性 性 弱 失 , 原 ; 同 后 同 一 最 时 难 元 > 低 存 得 素 价 弱 在 , 还 氧 先 不 原 化 与 交 性 + 强 叉 弱 ; 反 还 应 原 ) 既 作 可 还 作 原 剂 氧 剂 化剂 又可 SO J 物 2 化 、 单 合 N 质 a2SOj> N C H O a 2 、 O 、 2 K H 、 、 2 N S A 、 a k 2O H M 2 B x g r S 、 、 等 H H 2 R S C Fe 等 Cb等
一般来说:同一元素,价态越高,氧化性越强 合匕 易得电子,得后难失
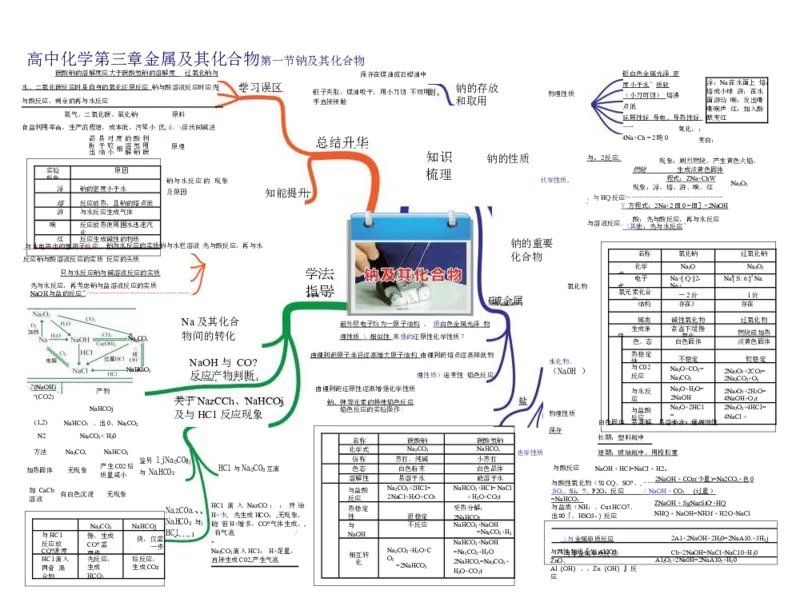
一电子守恒规律高中化学第三章金属及其化合物第一节钠及其化合物
碳酸钠的溶解度应大于碳酸氢钠的溶解度 _ 过氧化钠与
水、二氧化碳反应时是自身的氧化还原反应 钠与酸溶液反应时应先 钠的存放 与酸反应,剩余的再与水反应 和取用
氨气、二氧化碳、氯化钠 原料
食盐利用率高,生产流程短,成本低,污琴小 优,&、\侯氏制碱法
度的酸利 总结升华
溶氢用 原理 解钠碳 钠的性质
实验 原因
现象 代学性质, 浮 钠的密度小于水 知能提升
熔 反应放热,且钠的熔点低
游 与水反应生成气体
响 反应放热使周围水迅速汽
化
红 反应生成碱性的物质 _与__水__电__离__出__的__氫__离__子__反__应___ 钠与水反应的实质钠与水栏溶液 先与酸反应,再与水
反应钠与酸溶液反应的实质 反应的头质
碱金属
Na,CO,
NaHCO3
”(NaOH) 产物 由锂到飽还原性逐渐増强化学性质
"(CO2)
NaHCOj 物理性质 (1,2) NaHCO;、出0、Na2CO3
保存在煤油或石蜡油中 银白色金属光泽 密
学习误区 度小于水~ 质软 浮:Na在水面上 熔: 银 手 子 直 夹 接 取 接 , 触 煤油吸干,用小刀切 不可用 物理性质 (小刀可切) 熔沸 熔 面 成 游 小 动 球 响 游 : : 发 在 出 水 嘶
点低 嘶响声 红:加入酚
延展性好 导电、导热性好 猷变红
一 氣化,:
晶易对 4Na+Ch = 2盹0 变白:
析 出 于 结 较 小相 知识 与。 2 反应 . 现象:剧烈燃烧,产生黄色火焰,
梳理 燃烧 生成淡黄色固体
钠 及原 与 因 水反应的 现象 现象:浮、 程 熔 式 、 : 游 Z 、 N 响 a+ 、 Ch 红 W :Na2O2
、与HQ反应-----------------------------
' V 方程式: 2N a + 2 田 0 = 田] + 2NaOH
与溶液反应. 〈其 酸 他 : : 先 先 与 与 酸 水 反 反 应 应 , ~ 再与水反应
钠的重要
化合物 名称 氧化钠 过氧化钠
只与水反应钠与碱溶液反应的实质 学法 式 化 电 学 子 Na+ N [: a Q 2O :]2- Nat[:S: 6: N ]2 a N 2O a 2 +
先 Na 与 OH 水 与 反 盐 应 的 , 反 再 应 考 " 虑 /- 钠 -- 与 -- 盐 -- 溶 -- 液 -- 反 -- 应 -- 的 -- 实 -- 质 ----------- 指导 氧化物 式 氧元素 价结 化 构 合 Na+ 存 一 在 2价 》 存 1 在 价
N 物 a 间 及 的 其 转 化 化 合 最 理 外 性 层 质 电 \ 子 相 均 似 为 性 一 原 蓦 子 强 结 的 构 还 原 、 性 顶 化 白 学 色 性 金 质 属 7 光泽 物 件 生 色 属 成 、 类 条 态 碱 常 白 性 温 氧 色 氧 下 化 固 化 缓 体 物 慢 燃 淡 过 烧 黄 氧 或 色 化 加 固 物 热 体
NaOH 与 CO? 由锂到飽原子半径逐渐増大原子结构 由锂到飽熔点逐渐降低物 水化物、 热 性 稳定 不稳定 较稳定
反应产物判断 理性质)递变性 焰色反应 (NaOH ) 与 反应 C02 N N a a 2 2 O CO +C 3 O2= 2 2 N N a a2 2 O CO2+ 3 2 + C O O 2 2=
关于NazCCh、NaHCOj 钠、钾等元素的特殊焰色反应
与
应
水反 N
2N
a2
a
O
O
+
H
H2O= 2
4
N
N
a aO2O H2+
+
2
O
H 2t2O=
及与HC1反应现象 焰色反应的实验操作: 保存 白色固体、 与 反易 盐 应潮 酸 解、易溶 N = 2于N a2 水a O C + 、l+ 2 H强 H 2 C O腐 l 蚀性 2 4 2 N N H a a 2O C 2O + l 2 O + + 2 4 t HCI=
N2 Na2CO3< H20 名称 碳酸钠 碳酸氢钠 长期:塑料瓶中
加 加 溶 热 方 液 C 固 法 a 体 Cb 有 N 白 无 a2 色 现 CO 沉 象 , 淀 产 质 N 无 生 量 aH 现 减 C C 0 象 小 O 2 3 后 鉴 与 另 N a l H j C N N O a a 3 2 z C C O O 3 a、 HC H 1 C1 滴 与 入 Na N 2 a C zC O O 3互 : 滴 :开始 与 反 热 化 溶 俗 色 盐 应 稳 学 解 称 态 酸 定 式 性 N 2 T N a 苏 2 a C 白 易 C 打 O l+ 色 溶 3 N 、 + H 粉 于 2 a 2 纯 2 O H C 末 水 + C 碱 O C I 3 = O 2 N 受 a 热 HC + 分 O H 解 3 N 小 白 能 2 + O : H a 苏 色 溶 + H C C C 打 晶 于 l O = O 2 体 水 N , t aCl 也学性质 与 . = 与 与 S N O 酸 盐 酸 a , H 、 性 类 反 C S 氧 ( O 应 i 。 : 化 N ? H 物 、 : ( P 、 N 2 短 如 O a C O 。 期 u C H t Q 反 : H + 、 C 应 玻 H O S C 璃 O 7 l 、 ? = 瓶 、 N 中 a , C - / , _ I - N + - 用 a - Z 2 H O 橡 -N N 2 H -a a 。 胶 -O O + -H 塞 H C + + O : C Sg O ( N z ( a 过 少 zS 量 量 iO ) ) '+ = H N Q a2CO , + 也 0
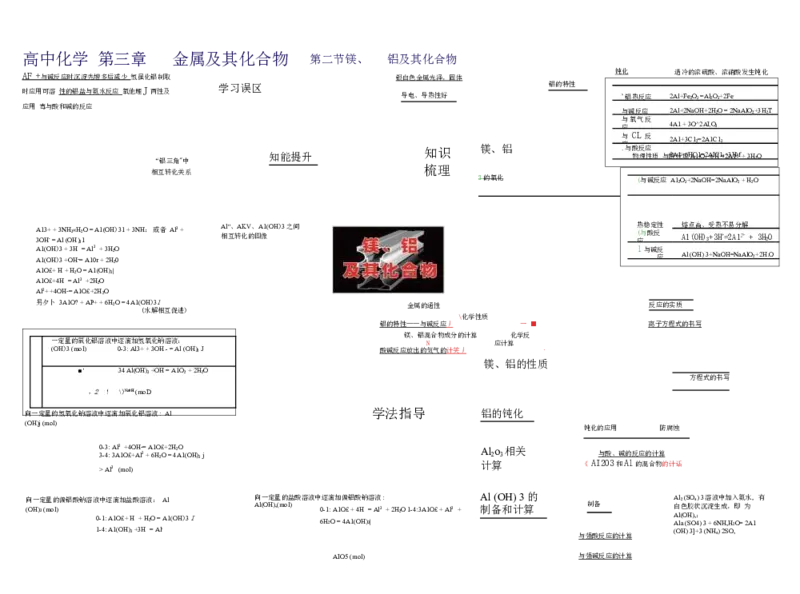
与 反 C H 两 合 O C 应 者 物 H ? 1 速 C 放 滴 混 1 度 入 慢 C 两 先 生 H N O C , 步 反 成 a ? O 2 C 生 应 需 ; O 成 , 3 N 后 生 快 a 反 成 H , C 应 C O 仅 一 O , j z 需 步 N H a C H 1 CO3 与 H 随 N 直 有 + a 接 2 少 气 C 着 生 O , 泡 H 3 成 滴 先 +増 C 入 生 0 多 成 2 H , , 产 C H 1 C 生 C : O O 气 ? H ; 气 泡 + , 足 体 无 量 生 现 , 成 象 / , , , 性 与 N 相 a 互 化 OH 转 N O a 2 2 = C 2 O N 3 很 不 a + H H 稳 反 C 2O O 定 应 + 3 C 2 N ON = 2 H N N N a a 2O H H a a a H H + 2 C C C C C C O O O O O O 3 3 3 = + + 2 + , 3 t = N N N H N a a a 2 2 O O O a C 2 H H C O O 3+ 3 H + 2 与 Z A 应 出 n l 两 ( O # ( - 0 、 性 O 与 「 与 H 物 非 、 ) 金 质金 H 、 属 S [属 、 O 单 如单 3 Z 质 -) n 质A ( 反 I 反 反2 O 应 O 应 应 H 3、 )』反 N A H 12 Q O 3 + 2 C + A 2 b N N + 1 a + 2 a O N 2 0 H N H a = O a = N O 2 H N H H = a 3 + N A f 2 a + H 1 C 0 2 l H 0 2 + + = 2 N H O 2 a N 2 + C 0 a N 1 A 0 a 1 + C 0 H l .+ 20 3H2j高中化学 第三章 金属及其化合物 第二节镁、 铝及其化合物
AF + 与碱反应时沉淀先增多后减少 氢虽化铝制取 银白色金属光泽,固体 钝化 遇冷的浓硫酸、浓硝酸发生钝化
时应用可溶 性的铝盐与氨水反应 氧他鲤J两性及 学习误区 导电、导热性好 铝的特性 '铝热反应 2Al+Fe2O3 =Al2O3+2Fe
应用 毒与酸和碱的反应 与碱反应 2Al+2NaOH+2H2O = 2NaAlO2+3H2T
与氧气反
应 4A1 + 3O^2AI:O3
知识 镁、铝 与 应.与酸 CL 反 反 应 2A1+3C12=2A1C13
“铝三角"中 知能提升 _ 物理性质 与酸2A反1+应6HAC112O=23+A6IHC+1=3+2A3H132+f + 3H2O
梳理
相互转化关系
3 的氧化 (与碱反应 A12O3+2NaOH=2NaAlO2 + H2O
A 3 A A O 1 1 1 3 H ( ( O O + - H H = + ) ) A 3 3 3 N l + + ( H O O 3 3 H H H «H ) _ + = 3 2 1 = O A A = 1 l 0 3 A + r + 1 + ( 3 O 2 H H H 2 2 O ) 0 31 + 3NH: 或者 Al3++ A 相 l" 互 、 转 A 化 KV 的 、 图 A 像 1(OH)3 之间 ( 应 热 1 与 稳 与 酸 定 碱 反 性 反 应 熔 A A 1 l 点 ( ( O O 高 H H 、 ) ) 3 3 受 + + N 3 热 H aO + 不 = H 2 易 = A N 分 1 a J A 解 + lO + 2 + 3 2 H H 2 . O O
A1O£+ H++ H2O = A1(OH)3|
A1O£+4H+ = Al3+ +2H2O
Al3+ +4OH_= A1O£+2H2O
另夕卜 3A1O? + AP+ + 6H2O = 4A1(O (水 H) 解 31 相互促进) 金属的通性 反应的实质
\化学性质
铝的特性——与碱反应 丿 一 ■ 离子方程式的书写
镁、铝混合物成分的计算 化学反
一定量的氯化铝溶液中逐滴加氢氧化钠溶液: N 应计算
(OH)3 (mol) 0-3: Al3+ + 3OH - = Al (OH)3 J 酸碱反应放出的気气的 计笑丿 ・
镁、铝的性质
■ ' 34 Al(OH)3 +OH = A1O2 + 2H2O
方程式的书写
,2 ! \)Na0H (moD
向一定量的氢氧化钠溶液中逐滴加氯化铝溶液: Al 学法指导 铝的钝化
(OH)j (mol) 钝化的应用 防腐蚀
0 3 - - 3 4 : : A 3A l3 1 + O +4 £ O +A H l _ 3 = ++ A 6 1 H O 2 £ O + = 2H 42A O 1(OH)3 j A 计 l2 算 o3 相关 《 AI 与 2 酸 O3 、 和 碱 A 的 l 反 的 应 混 的 合 计 物 算 的计话
> Al3 + (mol)
向 (O 一 H) 定 3 (m 量 o 的 l) 偏铝酸钠溶液 0 1 中 - - 1 4 : : 逐 A A 滴 1 1 O (O 加 £ H + 盐 ) H 3 酸 + + 3 + 溶 H H 液 + 2 = O : A = l ; A A 1 l (OH)3 I 向 Al( 一 O 定 H) 量 ,(m 的 ol 盐 ) 酸溶液中 0 6 逐 - H 1 滴 2 : O A 加 = 1 O 偏 4A £ 铝 1 + ( 酸 O 4H H 钠 + ) 3 = 溶 | A 液 l3 : + + 2H2O 1-4:3A1O£ + Al3+ + A 制 l 备 (O 和 H 计 ) 3 算 的 与强 制 酸 备 反应的计算 A 白 A A (O l l l ( a 2 色 H O ( ( ) S 胶 S H 3 O O ) ] 状 , 4 + 4 : ) 3 ) 3 沉 3 ( 溶 N 淀 + H 液 6 生 4 N ) 中 成 2 H S 加 , , H O 入 2 , 即 O 氨 = 为 2 水 A , 1 有
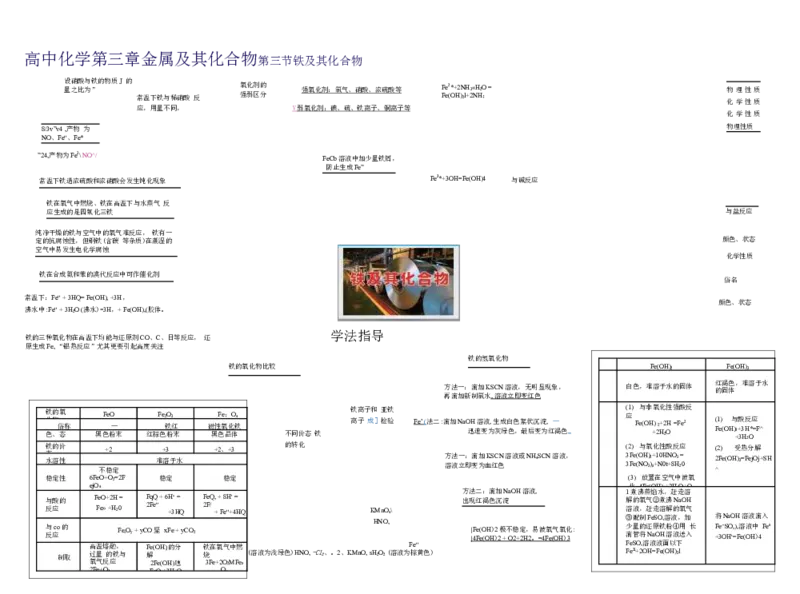
AIO5 (mol) 与强碱反应的计算高中化学第三章金属及其化合物第三节铁及其化合物
设 量 硝 之 酸 比 与 为 铁 ” 的物质J 的 常温下铁与稀硝酸 反 氧 强 化 弱 剂 区 的 分 强氧化剂:氯气、硝酸、浓硫酸等 F F e e( 2* O + H 2 ) N 2l H +2 3« N H H 2O ; = 物 化 理 学 性 性 质 质
应,用量不同, V 弱氧化剂:碘、硫、铁离子、铜离子等
化学性质
8/3v”v4 ,产物 为 物理性质
NO、Fe"、Fe*
”24,产物为Fe3\ NO^/ FeCb溶液中加少量铁屑,
防止生成Fe”
常温下铁遇浓硫酸和浓硝酸会发生钝化现象 FeJ*+3OH=Fe(OH)4 与碱反应
铁在氧气中燃烧、铁在高温下与水蒸气 反
应生成的是四氣化三铁 与盐反应
纯净干燥的铁与空气中的氧气难反应, 铁有一
定的抗腐蚀性,但钢铁(含碳 等杂质)在潮湿的 颜色、状态
空气中易发生电化学腐蚀
化学性质
铁在合成氨和苯的漠代反应中可作催化剂
俗名
常温下:Fe" + 3HQ= Fe(OH), +3H, 颜色、状态
沸水中:Fe" + 3H2O (沸水)=3H,+ Fe(OH),(胶体。
铁的三种氧化物在高温下均能与还原剂CO、C、日等反应, 还 学法指导
原生成Fe, “铝热反应”尤其更要引起高度关注
铁的氢氧化物
铁的氧化物比较 Fe(OH)2 Fe(OH)3
方法一:滴加KSCN溶液,无明显现象, 白色,难溶于水的固体 红 的 褐 固 色 体 ,难溶于水
再滴加新制氯水 , 溶液立即变红色
铁 化 色 的 物 、 俗 氧 态 称 黑色 Fe 粉 O — 末 红棕 F 色 e 铁 2 粉 O 红 3 末 磁 黑 性 色 F 氧 e 晶 ; 化 体 O 铁 4 不同价态 铁 铁 离 离 子 子 成 和 ] 亚 检 铁 验 Fe’ ( 法二:滴加NaO 迅 H 速 溶 变 液 为 ,生 灰 成 绿 白 色 色 , 絮 最 状 后 沉 变 淀 为 , 红 — 褐色„ ( 应 1) Fe 与 (O 非 H + 氧 ) 2 2 化 H +2 2 性 O H+ 强 =F 酸 e2+ 反 ( F 1 e ) (OH 与 ) + 3+ 酸 3 3 H H 反 2O * 应 =F ^
铁 态 水 的 溶 价 性 不 + 稳 2 定 难 + 溶 3 于水 +2、+3 的转化 方 溶 法 液 一 立 : 即 滴 变 加 为血 KS 红 C 色 N溶液或NH4SCN溶液, ( 3 3 2 F F ) e e ( ( O N 与 H O 氧 ) 3) 2+ 5 化 + 1 N 0 性 0 H t 酸 N +8 O 反 H 3 应 2 = 0 ( 2 ^ 2 F ) e(OH 受 )3 热 =F 分 ejO 解 j+ SH
稳 与 反 与 反 定 酸 应 应 co 制 性 的 的 取 6 e 高 过 氧 2 j F F O F 温 量 气 F e e e 4 O + e O 熔 反 » O + + 的 + O 2 2 融 应 H H 2 铁 = , 2 + F 0 2 与 = e F ,Oy + yC F 2 F 解 O F F q e 2 ( Q e e F 坚 O " Q e 稳 + H ( O + x ) 6 定 3 ; H F + 的 H H e 3 ) ‘ 虺 分 2 H + O = Q yCO2 F 2 铁 烧 3 F e F Q 在 / e , + + 氧 + 2 F O O 稳 气 8 e 4 H " 2M + 定 中 ' 4 = F H 燃 e Q 5 (溶液为浅绿色)HNO, -Cl2、。2、KMnO, s K H H M 2 N O n O 2 O ( , 4 溶 \ 液为 F 棕 e" 黄色) 方 出 法 现 | | F 4 二 红 F e( e O : 褐 (O H 滴 色 H ) 2 ) 加 沉 2 极 淀 + N 不 O aO 稳 2+ H 定 2 溶 H , 2 液 。 易 , = 被 4F 氧 e( 气 OH 氧 ) 化 3 : 1 解 溶 ③ 少 滴 F F ( 化 e e 3 煮 S 的 液 配 量 管 2 ) i+ O 沸4 2 氧 , 制 的 将 , 放 F O 溶 蒸e 气 赶 还 F N H 置 ( 液 馅 e O a = ② 走 原 S 在 O F H 液 水 O 煮 溶 铁 e H ) 空 , ( 面 2, 溶 O + 沸 解 粉 溶 气 2 以 H 赶 液 H 的 ④ 液 N ) 中 下 2 2 走 , O l a 氧 用 送 被 O +溶 加 气 入 H O 氧 长 2 将 F + e 3 ^ O N S H a O O '= ,) H F ,溶 e 溶 (O 液 液 H 中 滴 )4 入 Fe 5+高中化学第三章金属及其化合物第四节用途广泛的金属材料
化学腐蚀
不活泼金属组:Cu、
』 g 、 Ag、Pt、Au
Fe"遇苯酚(紫色丄 金 的 属 还 冶 原 炼 剂 中常 用 H2 ( CuO—Cu ) y蚀与防护 / 析氢腐蚀
F ( e3 血 + 遇 红 色 SC ) N- 金属有关的、. — Na C ( ( T Z iC n H O i — ) Zn )
Al ( Cr2O3—Cr) 电化学防护
CO ( FejCh—Fe)
熔点低
红色:Cu、CihO、 je性仁
F 红 e; 褐 。 色 、 :Fe(OH), 总结升华 一硬度大
蓝色:CU(OH)2、CUSOI • 5HzO
黑色:CuO、FeO、FeS、CuS、
AgjS、PbS、FesO」 金属的 开发 金属材料的选用
黄色:AgR AgBr、A&PO,、 S、 利用
NazOz、FeS?
绿色:F C e m SO (O 4 - H 7 ) H 2 2 C O C 、 >3 学法指导
K、Ca、Na、Mg、Al迅速氧化 金属失去电子发生氧化反应 本质 金属的活动性顺序与金属的冶炼 新型材料
金属与
Zn、Fe、Sn、Pb缓慢氧化 。2反应
金属活动顺
Cu、Hg、Ag、Pt、Au很难氧化一
原子失
序
电子
KCaNa Mg Al
由
Zn
大到小,
Fe
还
S
原
n P
性
b
由
|( H
强
)
到
| C
弱
u HgAg | Pt Au
M K g 、 、 C A a l 、 跟 N 水 a 在 跟 加 水 热 反 下 应 缓 剧 慢 烈 反应 金 0反 属 应 与 用 地位:次 能 阳 能 和 力 萬 力 反 子 应 得e 常 化 温被氧 常 气 温能 由 被 小 氧 到 化 大 |常 , 温 氧 干 化 燥 性 空 由弱到强 翼艺能|不能被氧化
(生成氧化膜)|中不易被
损失金属材料、损坏机械设备 与田0反应 常 出 温 氢 置换 加 置 热 换 或 出 与 氢 凡0 ( g )反应 不能置换水中的氢
和酸反应 剧 出酸 烈 中 置 的 换 氢 能 A常l 置 温 换 在 岀 浓 酸 硝 中 酸 的 、 氢 浓 , 硫 F 酸 e、 中 不 与 能 氧 置 化 换 性 稀 酸 酸 反 中 应 的 |只 氢 与王
Mg、Al反应剧烈 阻止金属失去电子被氧化 和碱反应 钝仅化A1和Zn能跟强碱水溶液反应生成H水:反应
改变金属的内部组织结构 和盐反应 先 应 与水反 前面的金属从盐溶液中置换出后面的金属
Sn、Pb反应缓慢
Cu、Hg、Ag、Pt^ Au不能反应 在金属的表面覆盖保护层 碱的热分解 受 解 热不分 受热分解 常温分解
Cu、Hg、Ag可与HNO3反应 硫化物 性 溶解 溶于水 水解 不 水 溶 , 于 溶于 只溶于强氧化性酸
Pt、Au不跟HNO3反应 非氧化性
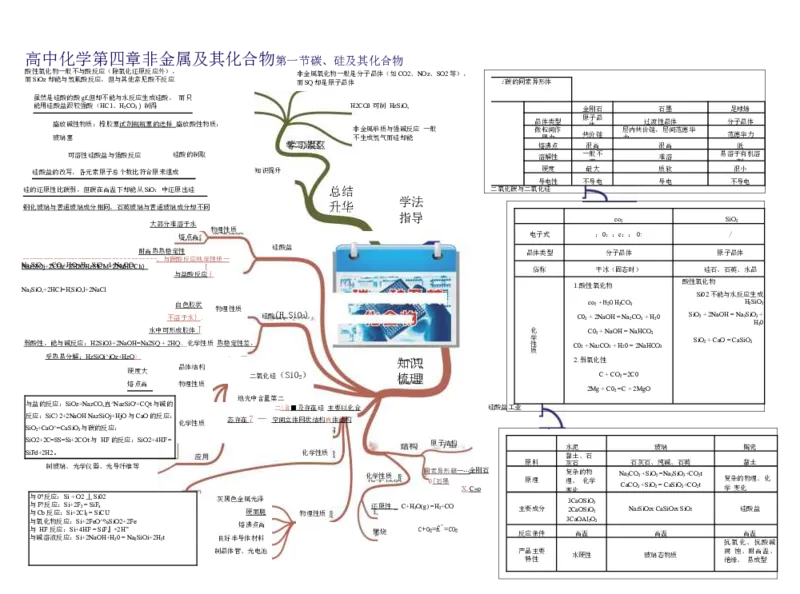
冶炼方法 电解法 热还原法 加热分解法 物理方法高中化学第四章非金属及其化合物第一节碳、硅及其化合物
酸
而
性
Si
氧
Oz
化
却
物
能
一
与
般
氢
不
氟
与
酸
酸
反
反
应
应
,
(
但
除
与
氧
其
化
他
还
常
原
见
反
酸
应
不
外
反
)
应
, 非
而
金
SQ
属
却
氧
是
化
原
物
子
一
晶
般
体
是分子晶体(如CO2、NOz、SO2等),
i碳的同素异形体
虽然是硅酸的酸gf,但却不能与水反应生成硅酸, 而只
能用硅酸盐跟较强酸(HC1、H2CO3)制得 H2CO3 可制 HzSiO, 金刚石 石墨 足球烯
盛 玻 放 璃 碱 塞 性物质:橡胶塞试剂瓶瓶塞的选择 盛放酸性物质: 非 不 金 生 属 成 单 氢 质 气 与 而 强 硅 碱 却 反 能 应 一般 晶 微 体 粒 用 类 间 力 型 作 原 共 子 体 价 晶 键 层 力 内共价 过 键 渡 , 性 层 晶 间 体 范德华 分 范 子 德 晶 华 体 力
学习误区 熔沸点 很高 很高 低
可溶性硅酸盐与强酸反应 硅酸的制取 溶解性 一般 溶 不 难溶 易溶于 剂 有机溶
硅酸盐的改写,各元素原子总个数比符合原来组成 知识提升 硬度 最大 质软 很小
导电性 不导电 导电 不导电
硅的还原性比碳弱,但碳在高温下却能从SiO:中还原出硅 总结 二氧化碳与二氧化硅
钢化玻璃与普通玻璃成分相同,石英玻璃与普通玻璃成分却不同 升华 学法
指导
大部分难溶于水 co2 SiO2
熔点高 物理性质 电子式 :0::c:: 0: /
耐高热热稳定性 硅酸盐 晶体类型 分子晶体 原子晶体
-------------------------------------- 、 与碳酸反应地学性质一
NNaaz3SSiiOO;j+Z+CCOO;z++HZ;OH=zOHH;zSSiiOC;M+l+ZNNaa3CHOC;Ch ) 与盐酸反应 [ 丿 俗称 干冰(固态时) 硅石、石英、水晶
Na2SiO,+2HCl=H;SiO,l+2NaCl 1.酸性氧化物 酸性氧 Si 化 02 物 不能与水反应生成
弱酸性,能与碱反应: H2SiO3+2NaOH=Na2 水 SQ 中 + 可 不 2 形 H 溶 Q 成 白 、 于 胶 色 化 水 体 胶 学 } 状 J 性 . 质 物 热 理 稳 性 定 质 性差 , 硅酸(H,SiO3) 化 学 性 质 C C 02 0 + 2 c C + N o 0 2 2 a 2 N 2 + + C a H O N O 2 3 O a H + O H = H H 2 C N 2 = 0 O a N = 2 3 C a 2 O H N 3 C a + H O H C 3 2 O 0 3 Si S O iO 2 + 2 + 2 N C a a O O H = = C N aS a i 2 H O S 2 i 3 S O H i 3 O 2 + 0 3
受热易分解: HzSiOi^iOz+HzO 〉 ・ — 知识 2.弱氧化性
硬度大 晶体结构 二氧化硅(SiO2) 梳理 C + CO2 =2C0
熔点高 物理性质
2Mg + C02 =C + 2MgO
地壳中含量第二
与盐的反应:SiOz+NazCO,直^NazSiO'+CQt 与碱的 二 \ 含 ■及存在 硅 主要以化合 硅酸盐工业
反 SiO 应 2+ : C S aO iC ^ ) = 2 C + a 2 S N iO aO 3 与 H 碳 Na 的 zS 反 iO 应 j+ : HjO 与CaO的反应: 化学性质 态存在 7 — 空间立体网状结构 直 体结构
S S i i O Fd 2 + + 2 2 H C 2 = 。 8S=Si+2COt 与 HF 的反应:SiO2+4HF = 化学性质 原子结构 水 黏 泥 土、石 玻璃 陶瓷
制玻璃、光学仪器、光导纤维等 化学性质 同 'e 素 [ 石 异 墨 形 籍 — X … . 金 C« 刚 o 石 原 原 料 理 灰 复 理 变 石 杂 、 化 的 化 物 学 N C a a 2 C C 石 O O 灰 3 3 + + 石 S S i i O 、 O 2 2 纯 = = N 碱 C a a 、 2 S S i i O 石 O 3 3 + 英 + C C O O 2 2 t t 复 学 杂 变 的 化 黏 物 土 理、化
与 与 与 与 与 与 氧 碱 0 F C H ? ? b 化 溶 反 反 F 反 物 液 反 应 应 应 反 反 应 : : : 应 应 : S S S i i : : + S i + + i 2 + 2 S S O F 4 C i i 2 2 + + H l = 2 2 2 丄 F F N = S = e i a S S F O O i S i 4 0 C ^ H i 2 % F U + 』 S H i + O 20 2 2 H = + ” 2 N F a e 2SiOi+2H2t 灰 良 黑 好 色 半 金 导 熔 属 体 沸 硬 光 材 点 而 泽 料 高 脆 物理性质 还 燃 原 烧 性 _ C+H2O C ( + g O ) 2 = = H £ 2 ^ + = C C O O2 主 反 要 应 成 条 分 件 3 3 2 C C C a 高 a a O O O 温 A S S l i i 2 O O O 2 2 3 Na2SiO3x 高 Ca 温 SiO3x SiO2 抗氧化 硅 高 、 酸 温 盐 抗酸碱
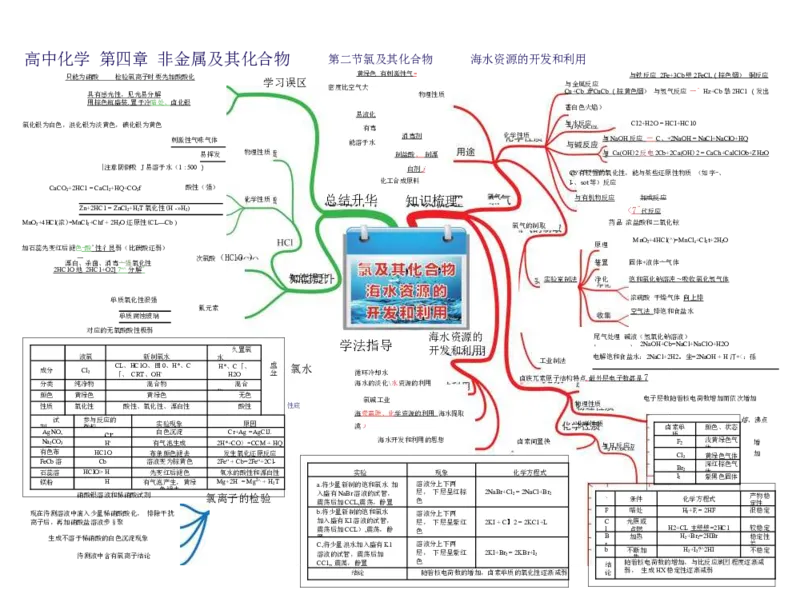
制晶体管、光电池 产品 特 主 性 要 水硬性 玻璃态物质 腐 绝缘 蚀 、 、 易 耐 成 高 型 温、高中化学 第四章 非金属及其化合物 第二节氯及其化合物 海水资源的开发和利用
只能为硝 具 酸 有 感 光 性 检 , 验 见 氯 光 离 易 子 分 时 解 要先加酸酸化 学习误区 密度比空气 黄 大 绿色 有刺激性气 = 物理性质 C 与 u 金 +C 属 b 鸯 反 应 CuCb ( 棕黄 与 色 铁 烟 反 ) 应 与 2 氢 Fe 气 +3 反 C 应 b 壁 一 2 ^ F e H C z l , + ( C 棕 b摯 色 2 烟 H ) C1 铜 ( 反 发 应 出
用棕色瓶盛装 . 置于冷 暗处、 卤化银 苍白色火焰)
易液化
氯化银为白色,浪化银为淡黄色,碘化银为黄色 有毒 与水反应 CI2+H2O = HCI+HC10
刺激性气味气体 能溶于水 消毒剂 化学性质 与 NaOH 反应 一 C 、 + 2NaOH = NaCl+NaClO+HQ
易挥发 物理性质 制盐酸 、 制漂 与 Ca(OH ) 2 反电 2Cb+2Ca(OH ) 2 = CaCh+CalClOb+ZHzO
|注意防倒吸 J易溶于水(1 : 500 ) 白剂 j Cb有较强的氧化性,能与某些还原性物质 (如字-、
CaCO3+2HC1 = CaCl2+HQ+CO2f 酸性(强)
化工合成原料 I-、sot等)反应
化学性质 总结升华 知识梳理 氯气 与有机物反应 加成反应
Zn+2HC1 = ZnCl2+H2T 氧化性(H+-»H2) < 7^ 代反应
MnO2+4HCl(浓)=MnCl2+Chf + 2H2O 还原性(CL—Cb ) 氯气的制取 药品 浓盐酸和二氧化铉
加石蕊先变红后褪色 - 酸 ' 性彳艮 弱(比碳酸还弱) 原理 MnO2+4HCl(^)=MnClz+Cl2t+2H2O
漂白一、杀菌、消毒亠强氧化性 次氯酸(HC1O ) 装置 固体+液体亠气体
2HC1O 地 2HC1+O2] 7"^ 分解 "
知能提升 实验室制法 净化 饱和氯化钠溶沌〜吸收氯化氢气体
单质氧化性很强 浓硫酸 干燥气体 向上排
单质腐蚀玻璃 氟元素 空气法 排饱和食盐水
对应的无氧酸酸性极弱 海水资源的 尾气处理 碱液(氢氧化钠溶液)
久置氯 学法指导 开发和利用 , 、 2NaOH+Cb=NaCl+NaClO+H2O
成分 液 C 氯 l2 C 「 L 、 、 H C C R 1 T O 新 、 、 制 O 田 H 氯 - 0 水 、H*、C 水 H*、 H2 C O 「、 成 分 氯水 循环冷却水 卤族兀 工 素 业 原 制 子 法 结构特点 , 最 电 外 解 层 饱 电 和 子 食 数 盐 都 水 是 : 7 2NaCl+2H2。坐=2NaOH + H汀+<:孫
分类 纯净物 混合物 混合 海水的淡化\水资源的利用
颜 性 色 质 黄 氧 绿 化 色 性 酸性、氧 黄 化 绿 性 色 、漂白性 物 无 酸 色 性 性底 氯碱工业 物理性质 电子层数随着核电荷数增加而依次増加
海 荥赢題 、化 学资源的利用 海水提取
剂AgN 试 O, 参 微 与 粒 反应 cr 的 实 白 验 色 现 沉 象 淀 Cr+A 原 g+= 因 AgClJ. 漠) 化学性质 卤素 质 单 颜色、状态 熔、沸点
有 条F 液石 液镁 N e 溶 固 C 色 蕊 粉 a2 b C液 体布 溶 溶 O3 硝 H 酸 C 银 I H O 溶 C C > b 1 液 H H H O ' + + 和稀硝酸试 有 剂 溶 布 先 气 有 液 条 变 泡 气 变 色 颜 红 产 泡 为 褪 色 后 生 生 棕 去 褪 褪 , 成 黄 去 色 黄 色 绿 氯 2 2 M 离 H F 氣 g 发 e * + " 水 子 + 2 生 + C H 的 O C 氧 + 的 酸 b 〉 = 化 = 性 M = 2 检 还 C F g 和 e C 2 原 " ^ M 漂 验 + + 反 2 白 + C H 应 l H 2 性 - T Q a 入 震 .将 盛 荡 少 有 后 量 加 N 新 a C B 制 C r 实 L 溶 的 ,震 验 液 饱 荡 的 和 , 试 氯 海 静 管 水 水 置 , 开 加 发和利 溶 层 色 用 液 , 的 分 思 下 现 上 想 层 象 下 呈 两 红棕 2NaBr+Cl2 化 = 卤 学 2 素 N 方 a 间 C 程 l 置 + 式 B 换 r2 与 、 H,反应 条件 F C B I2 2 l r 化 2 2 学方程 浅 体 黄 深 体紫 式 黄 绿 红 黑 绿 色 棕 色 色 气 色 固 气 体 气 体 产 定 増 加 物 性 稳
现 离 在 子 待 后 测 , 溶 再 液 加 中 硝 滴 酸 入 盐 少 溶 量 液 稀 步 硝 § 酸 聚 酸化, 排除干扰 b 加 震 .将 入 荡 少 盛 后 量 有 加 新 K C 制 C I溶 L 的 ) 液 饱 ,震 的 和 荡 试 氯 , 管 水 静 , 溶 层 色 液 , 分 下 上 层 下 呈 两 紫红 2KI + C】2 = 2KC1+L F :C l 光 暗 点 照 处 燃 或 H2+C H L 2 + 主 F: 壁 = 壁 2H = F 2HC1 很 较 稳 稳 定 定
生成不溶于 待 稀 测 硝 液 酸 中 的 含 白 有 色 氯 沉 离 淀 子 现 结 象 论 置 C 溶 C , C 将 液 1, 少 的 , 震 量 试 蕩 浪 管 , 水 , 静 加 震 置 入 荡 盛 后 有 加 K1 溶 层 色 液 , 分 下 上 层 下 呈 两 紫红 2KI+Br2 = 2KBr+I2 B r b 结 随 不 加 着 断 热 热 核 加 电荷数的增加 H H , 2+ 2+ B 与 I r 2 2 比 ? = ^ 2 2 反 H H 应 B I r 剧烈程度逐 稳 差 不 渐 定 稳 减 性 定
结论 随着核电荷数的増加,卤素单质的氧化性逐渐减弱 论 弱, 生成HX稳定性逐渐减弱高中化学第四章非金属及其化合物第三节氮及其化合物
不 吸 能 收 用 氨 浓 气 硫 生 酸 成 、 Ca 无 Ch 水 • 氯 8N 化 H 钙 , 作干燥剂, 因CaCb 氨气的干燥 合 填 成 充 氨 灯 、 泡 制 、 硝 作 酸 制 、 冷 作 剂 保护气、 用途 电子式 一 :N"N:
二氧 高 化 温 氮 高 虽 压 然 下 与 发 水 生 反 反 应 应 生 2 成 NO 硝 L 酸,但不是硝酸的酸Bf 竺净的二氧 不 化 肖 氮 酸 卒 的酸酉十 / 学习误区 N2+ 游 O2 离 =^ 态 ^= 氨 2 N t O 氮 、 化 自 合 然 物概念 固定 物理,性质 密度略小于空 无 气 色无味气体、难溶于水、
根瘤菌生物固氮 3 - ,/ ' [类型 / k合成
① ② 当 当 钏 钏 。 。 2 2 ) ) : : K 〃 O 。 2 ) 2 = ) 4 > 4 : : 1 1 时 时 , , 恰 N 好 O2 完 过 全 量 反 , 应 A 剩余 氨工业人工 )' 化学性质 “ 氧化性 *+3田 高 , 温 僵 ' 化 M 剂 S压 '2NH:
气体为NO,消耗O2体积:
汽。2)=![踪一3钏0)] NO2和02混合气体溶于水时, .还原性 N2+O2 2N0
4NO2+O2+2H2O=4HNO3
③当钏0» :汽。2)<4 : 1时,Ch过量, NO2、NO、O2混合 总结升华
剩余气体为。2,消耗NCh体积: K(NO2)= 、气状与水的反应 知识 分子结构
体积差) H-N-H (三角锥形)
① ② ③ 当 当 当 丫 〃 r ( ( N N N O O O ) ) ) : : 汽 汽 : 〃 。 。 0 2 2 2 ) ) ) < = > 4 4 4 : : 3 : 3 时 时 3 , , 时 恰 剰 , 好 余 剰 完 余 Q 全 J N 反 O 应 、 N O 、 和 ^ 4 0 N 2 ° 同 +3 时 O 通 2+ 入 2H 水 2° 中 =4 时 H , NO 3 丿 知能提升 梳理 氨 气 . / J 物理性质 < 云峰 5 无色、有刺激性气味
① 当 ” (N) : "(0)=2 : 5 时,恰好完全反应 、 4NO+3Ch混 -- 合 -- 气 -上 体 述 中 两 N 个 、 反 O 应中,4NO2+O2与 化学性质 \ 极易溶于水 1 : 70 0 Z防倒吸]
②当”(N) : ”(O)>2 : 5时,剰余NO [ 原子个数比均为2 : 5 点水反应 NH3+H2O—NH 技 HQ —NFC+OH-
实验室制法 [ 卢 酸反应 NH,+HC1= NRCK 冒白烟 ) 与氧气
③当”(N) : "(O)V2 : 5时,剩余0?
反应、4NH,+5O2卷您4NO+6HQ
在装有红棕色的两瓶气体中分别加入少量水后振蕩, 水
溶 一 液 瓶 显 气 无 体 色 是 的 澳 一 蒸 瓶 气 气体是NO”水溶液显黄色或 淡黄色的 溶水法 NO?与漠蒸气 的鉴 原理 固态铉盐与碱加热反应
向两瓶红棕色气体中分别加入少量AgNO;溶液后振荡,有 一;,、土 浅 别
黄色沉淀的一瓶气体是漠蒸气,则另一瓶气体是NO? • 渥法 学法指导 、发生装置 固体+固体气体
2 反 N 应 0, =N,OJ无色) L 原因 「 正向为放热 气 气 体 体 颜 颜 色 色 变 变 浅 浅 的 的 为 为 N N O O ? ? 降 加 温 压 J 、 收 干 集 燥 向下排空气法
用装有碱石灰的干燥
硝酸的强氧化性 氮的氧化物 验一满 将湿润的红色石蕊试 管 纸放在瓶口,若变蓝,则满
非金属(如碳、硫等)也 可以和浓硝酸
发生反应」 NO NO2 物 与金属反应无氢气放出 理
性
质
与除钳和金外的其他 金属都可
以反应 .
浓硝酸:二氧化氮 丄/ 二 x 圭 成物丿
稀硝酸:一氧化氮 ] J, 冷的浓硝酸可使 铁、铝发生话在 岁化丿
-
颜色 无色 红棕色
毒性 有毒 有毒
水溶性 不溶于水 易溶于水
- 化
学
性 质
-
将蘸有浓盐酸的玻璃棒接近瓶口,若产生白烟,则满
物理性质 ....r 不稳定性 NHQ—NH 汀 +HC1 ]
铉盐/化学性质
与碱反应 NH,Cl+NaOH=NaCl+NlM+H2O
铉根离子检验
硝酸 与氧气反应 2NO+O2=2NO2 不反应
—物理性质
与水反应 不反应 3N0j+HQ = 2HNO3+NO
与碱反应 不反应 + 2 N N a O N 2 O +2 2 N + a H O 2 H O = ( 吸 Na 收 N 尾 O3 气 ) 竺 % 心林。躍 > - 會。 , 峥。 5 。
3CU+8HNO3 (稀)=3CU(NO)2 Cu+4HNC>3(浓)=CU(NO3)2 +
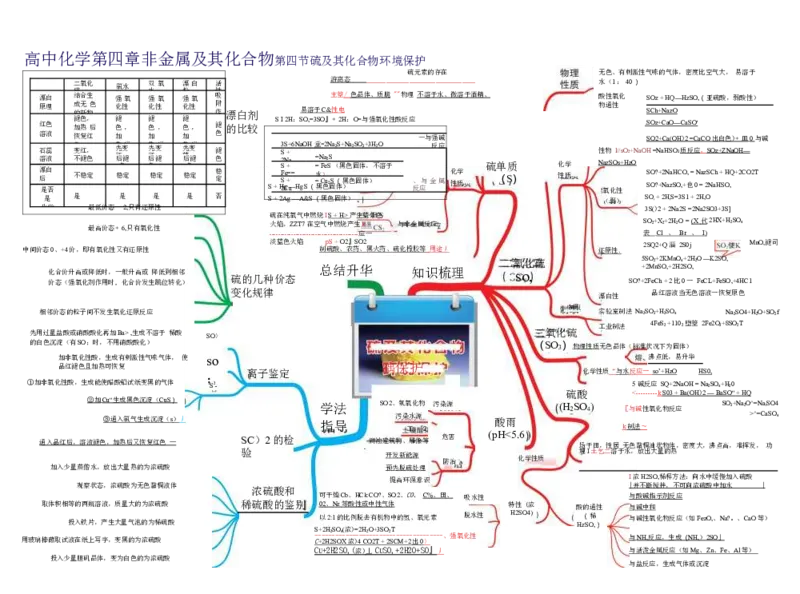
实验室制法 +2NOt+4H2O 2NO2T+2H2O \ 不稳定性 4HNO,坦4NO2f+O2f+2H2O高中化学第四章非金属及其化合物第四节硫及其化合物环境保护
硫元素的存在 无色、有刺激性气味的气体,密度比空气大, 易溶于
漂 原 白 理 二 硫结 成 的 氧 合 无 新 化 生 物 色 强 化 氯 性 水 氧 双 水 强 化性 氧 氧 漂 粉 强 化性 白 氧 活 性吸 附 作 漂白剂 易溶于 C& 游 主 性 离 箜 电 态 / 色 晶 体 __ 、 __ 质 __ 脆 _ _ _ " _ " _ 物 __ 理 __ _ 不 __ 溶 __ 于 __ 水 __ 、 __ 微 __ 溶 __ 于 __ 酒 _ 精 、 酸 物 水 性 通 ( 氧 性 1 : 化 40 ) S S C O h z + + N H az Q O —HzSO,(亚硫酸,弱酸性)
红色 褪 加 色 热 , 后 褪 色, 褪 色, 褪 色, 褪的比较 S I 2H:SO,=3SO』+ 2H:O=与强氧化性酸反应 .SOz+CaO—CaSO'
溶液 恢复红 加 加 加 色 一与强碱 SO2+Ca(OH ) 2 =CaCO 出白色 )+ 皿 0 与碱
石 溶 漂 后 稳是 蕊 液 白 定否 色 变 不 不 红 褪 稳 , 色 定 热先 红后 稳 色 变 ,褪 定 后 热先 红后 色 稳 变 ,褪 定 后 热先 蓝后 稳 色 变 ,褪 定 后 褪 色 稳 定 S + H 3 S 2 S F S 2g S N C e + + + = + u— a = 6 N H a g O S H ( 堂 = = 水 = 黑 N F C = ) 色 a 2 e u 2 S N 2 、 S 固 S a ( 2 ( 体 S 黑 + 黑 ) N 色 色 a2 固 S 固 O 体 体 3+ , 3 ) H 不 2O 溶于 、 反应 与金 反 属 应 化 性 学 质 硫 ( 单 S 质 ) 化 性 学 质 性 N 氧 a 物 zS 化 O l 性 / s / + s O H 2 z + O NaOH S S O O = ? ? N + + a 2 N H N a S z a O S H O 3 C 质 , O +也 反 , = 应 0 N = , a z 2 S S N C O a h z H + + S Z O H N , Q aO +2 H C — O 2T
是 是 是 是 是 否 S + 2Ag —A&S (黑色固体) (弱) SO; + 2H;S=3S1 + 2H,O
化学 最低价态一2,只有还原性 3S()2 + 2Na2S =2Na2SO3+3S]
硫在纯氧气中燃烧I S + H> 产生蓝紫色
最高价态+ 6,只有氧化性 - 火 --- 焰 --- , --- Z -- Z -- T - 7 -- - 在 --- 空 --- 气 --- 中 --- 燃 --- 烧 --- 产 --- 生 --应 k — 、与非金属反应 S 表 O 2+ C X l 2 + 、 2H 2O B r = 、 (X 代 I ) 2HX+H2SO4
中间价态0、+4价,即有氧化性又有还原性 淡蓝色火焰 制 p 硫 S 酸 + 、 O2 农 』 药 SO 、 2 黑火药、硫化橡胶等 _ 用途丿 还原性 . 2SQ2+Q 淄 2S0j MnO,褪司
二氧化硫 5SO2+2KMnO4+2H2O —K2SO,
化 价 合 态 价 ( 升 强 高 氧 或 化 降 剂 低 作 时 用 , 时 一 , 般 化 升 合 高 价 或 发 生 降 跳 低 位 到 转 相 化 邻 ) 硫的几种价态 总结升华 知识梳理 so, SO?+ + 2 2 F M eC nS h O + , + 2 2 比 H2 0 S 一 O, FeCL+FeSO,+4HC1
变化规律 漂白性 品红溶液当无色溶液一恢复原色
相邻价态的粒子间不发生氧化还原反应 制取 实验室制法 Na2SO3+H2SO4 Na2SO4+H2O+SO2f
先用过量盐酸或硝酸酸化再加Ba> ,生成不溶于 稀酸 SO〉 三氧化硫 工业制法 4FeS2 +1102 堕箜 2Fe2O3+8SO2T
的白色沉淀(有SO;时,不用硝酸酸化) (SO3)物理性质无色晶体(标准状况下为固体)
加非氧化性酸,生成有剌激性气味气体, 使 so 沸点低,易升华
品红褪色且加热可恢复 ; 离子鉴定 踽保护 化学性质 “ 与水 反应一 so’+HzO HS0,
①加非氧化性酸,生成能使醋酸铅试纸变黑的气体 S2- 5 碱反应 SQ+2NaOH = Na2SO4+H20
硫酸 <--------- k S03 + Ba(OH ) 2 — BaSO" + HQ
通入品红后,溶液
②
褪
加
色
C
③ ,
u "
通
生
加 入
成
热 氯
黑
后 气
色
又 生
沉
恢 成
淀
复 沉
(
红 淀
C
色 (
u S
— s
)
) 丿 SC)2的检
学
指
法
导 腐蚀
S
建
O2
筑
、
物 污
氣
、 染
氧
工 雕 水
化
: 像 源
物
" 等 2
污染
危
源
害 (p 酸 H< 雨 5.6 )
(H2S
场
O
干
4)
田,性居
[
k 无 制
与
色 法
碱
黏 〜
性
稠
氧
油
化
状
物
物
反
体
应
,密度大,沸点
S
高
O
,
3+
难
Na
挥
2O
发 >
^
^
=
, =
N
C
a
a
!
功
S
S
O
O
4
4
验 开发新能源 防治 化学性质 埋I土乞二溶于水,放出大量的热
加入少量蒸僧水,放出大量热的为浓硫酸 预先脱硫处理
观察状态,浓硫酸为无色黏稠液体 浓硫酸和 提高环保意识 I | 并 浓 不 H2 断 SO 搅 ,稀 拌 释 , 方 不 法 可 : 向 向 浓 水 硫 中 酸 缓 中 慢 加 加 水 入 硫 酸 |
可干燥Cb、HCk CO?、SO2、CO、 C% 、 田 、 吸水性 与酸碱指示剂反应
取体积相等的两瓶溶液,质量大的为浓硫酸 稀硫酸的鉴别 02 、 Nz 等酸性或中性气体 特性 (浓 酸的通性 与碱中和
用玻璃棒蘸取试
投
液
入
在
铁
纸
片
上
,
写
产
字
生
,
大
变
量
黑
气
的
泡
为
的
浓
为
硫
稀
酸
硫酸
C - S - + +
以
- 2 2 - H H
2
- 2 2
:
- S
1
S - O O
的
-4 X - (
比
浓 - 浓 -
例
) — ) =
脱
4 2 — H C
去
-2 O O -
有
2 - + T -
机
3 - S + -
物
O - 2 2- S
中
T - C -
的
M - -
氢
+ - 2 -
、
出 - -
氧
- 0 -
元
〉 - -
素
---、强氧化
脱
性
水 性 H2SO4) Hz ( SO 稀 ,)
与
与 碱
NH
性
, 反
氧
应
化
,
物
生
反
成
应
(
(
N
如
H
F
, )
e z
2
O
S
,、
O 」
N a?。、CaO等)
CU+2H2SO, ( 浓 ) 丄 CUSO,+2H2O+S O 』 丿 与活泼金属反应(如 M g 、 Z n 、 F e 、 A l 等 )
投入少量胆矶晶体,变为白色的为浓硫酸 与盐反应,生成气体或沉淀高中化学 第四章非金属及其化合物 第五节无机推断
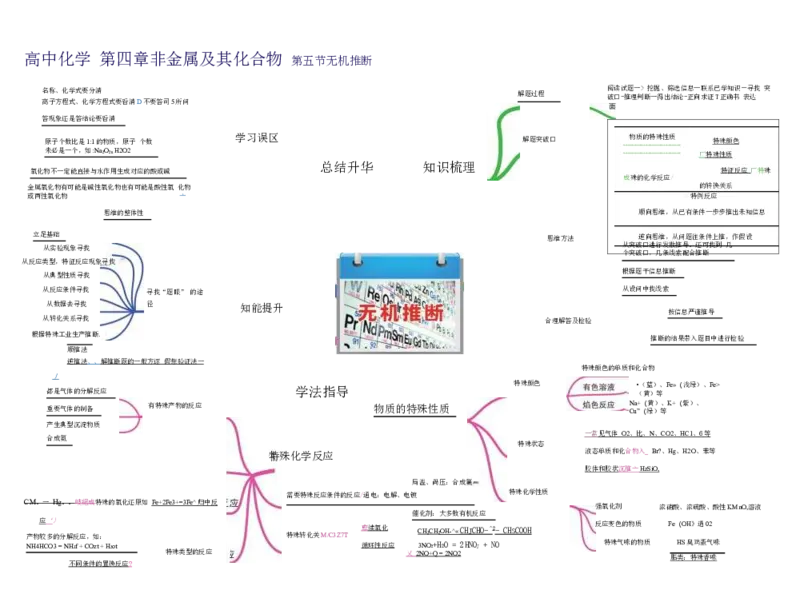
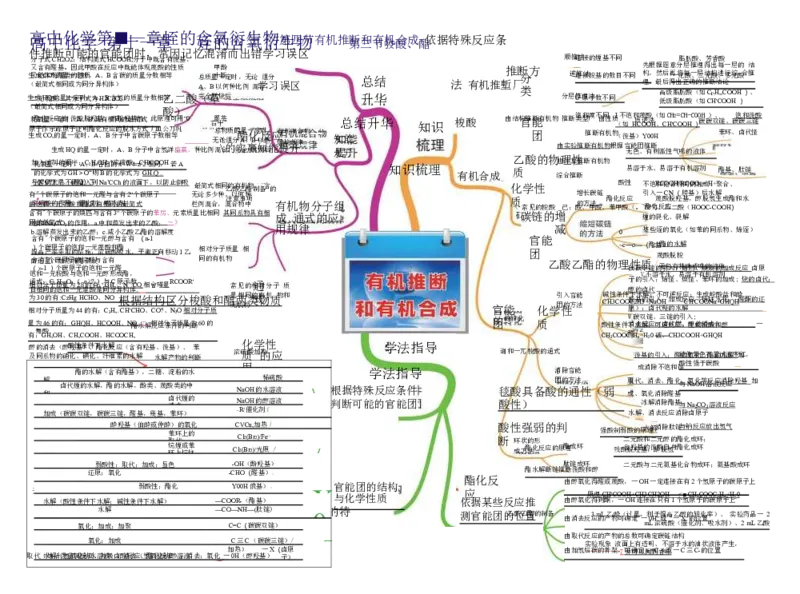
名 离 称 子 、 方 化 程 学 式 式 、 要 化 分 学 清 方程式要看清D 不要答司5所问 解题过程 阅 破 读 口 试 -推 题 理 一 判 > 断 挖 一 掘 得 、 出 筛 结 选 论 信 - 息 正 — 向 联 求 系 证 已 T正 学 确 知 书 识 ― 表 寻 达 找 突
答现象还是答结论要看清
原子个数比是1:1的物质,原子 个数 学习误区 解题突破口 --- 物 --- 质 --- 的 --- 特 --- 殊 --- 性 --- 质 ----- 特殊颜色
未必是一个,如:Na2O2x H2O2 -------------------------- 厂 特殊性质
总结升华 知识梳理
氧化物不一定能直接与水作用生成对应的酸或碱 特征反应 厂特殊
成殊的化学反应/
金属氧化物有可能是碱性氧化物也有可能是酸性氧 化物 的转换关系
或两性氧化物 亠 < 特例反应
思维的整体性 顺向思维,从已有条件一步步推出未知信息
立足基础 思维方法 逆向思维,从问题往条件上推,作假设
从实验现象寻找 从突破口进行发散推导。还可找到 几
个突破口,几条线索配合推断
从反应类型,特征反应现象寻找
从典型性质寻找 根据题干信息推断
从反应条件寻找 寻找“题眼” 的途 从设问中找线索
从数据去寻找 径 知能提升
按信息严谨推导
从转化关系寻找 合理解答及检验
根据特殊工业生产推断. 推断的结果带入题目中进行检验
顺推法
逆推法 、、 解推断题的 一 般方逐 假想验 证法一
特殊颜色的单质和化合物
丿
都是气体的分解反应 学法指导 特殊颜色 • ( ( 黄 蓝 ) ) 等 、Fe»(浅绿)、Fe>
重要气体的制备 有特殊产物的反应 物质的特殊性质 N Cu a+ ”( ( 绿 黄 ) ) 等 、K+(紫)、
产生典型沉淀物质
合成氨 一常 见气体 O 2 、 比、 N 、 CO 2 、 HC 1 、 6 等
特殊状态
特殊化学反应 液态单质和化合物入_ Br?、Hg、H2O、苯等
胶体和胶状 沉推亠 HzSiO ,
局温、咼压:合成氨
需要特殊反应条件的反应/通电:电解、电镀 特殊化学性质
CM。一 Hg。。岐絕成特殊的氧化还原如 Fe+2Fe3+=3Fe^ 归中反 强氧化剂 浓硝酸、浓硫酸、酸性KMnO,溶液
催化剂:大多数有机反应
产物 应 较 ‘ 多 〉 的分解反应,如: 特殊转化关M/C3Z7T 孽 续氧化 CH3CH2 OH-^« CHJCHO- ^ 2 - CHSCOO H 反应变色的物质 Fe(OH》遇02
NH4HCO3 = NH3f + COzt + H2ot 特殊类型的反应 循环性反应 乂 2 3 N N O O + 2 Q +H = 2 O 2 N = O 2 2HNOJ + NO 特殊气味的物质 脂 H 类 S : 臭 特 鸡 殊 蛋 香 气 味 味
不同条件的置换反应 ?高中化学 第五章 物质结构 元素周期律第一节原子结构
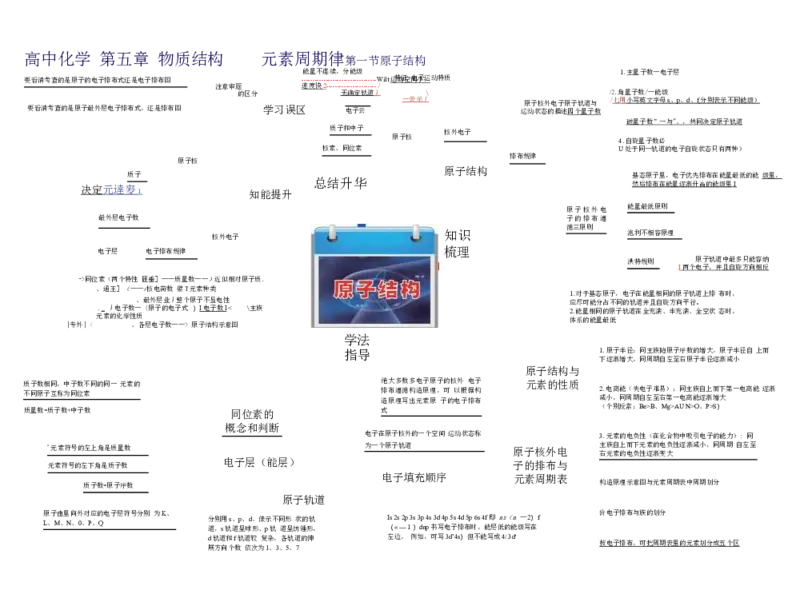
能量不连续,分能级 1.主量子数一电子层
要看清考查的是原子的电子排布式还是电子排布图 ----------------------------------Wilt 运特动征空 间电小子 ,运 动特质
注意审题 速度快 2-----------------------〉
要看清考查的是原子最外层电子排布式,还是排布图 的区分 学习误区 无 电 确 子 定 云 轨道 丿 一 表示丿 \ 运 原 动 子 状 核 态 外 的 电 描 子 述 原 四 子 个 轨 量 道 子 与 数 / / 2 七 .角 用 量 小 子 写 数 英 / 文 — 字 能 母 级 s 、 p 、 d 、 f 分别表示不同能级)
磁量子数”一与 " 、,共同决定原子轨道
质子和中子 原子核 核外电子 4.自旋量子数必
核素、同位素 U处于同一轨道的电子自旋状态只有两种)
原子核 排布规律
原子结构
决定 元達麥 质 子 1 知能提升 总结升华 基 然 态 后 原 排 子 布 里 在 , 能 电 量 子 逐 优 渐 先 升 排 高 布 的 在 能 能 级 量 里 最 I 低的能 级里 ,
原子核外电 能量最低原则
最外层电子数 子的排布遵
核外电子 知识 循三原则 泡利不相容原理
电子层 电子排布规律 梳理
洪特规则 原子轨道中最多只能容纳
I 两个电子,并且自旋方向相反
->同位素(两个特性 匯垂]——质量数——)近似相对原子质.
、通王](——}核电荷数 嬖T元素种类 1.对于基态原子,电子在能量相同的原子轨道上排 布时,
、最外层业丿整个原子不显电性 应尽可能分占不同的轨道并且自旋方向平行。
|专外| < 元 ._ 素 丿 的 电 化 子 学 数 性 、 — 质 各 〈 层 原 电 子 子 的 数 电 — 子 — 式 > ) 原 子 I 电 结 子 构 数 示 I 意 < 图 \主族 2 体 .能 系 量 的 相 能 同 量 的 最 原 低 子轨道在全充满、半充满、全空状 态时,
学法
指导 1.原子半径:同主族随原子序数的増大,原子半径自 上而
下逐渐増大,同周期自左至右原子半径逐渐减小
原子结构与
质 不 子 同 数 原 相 子 同 互 , 称 中 为 子 同 数 位 不 素 同的同一 元素的 绝 排 造 布 大 原理 多 遵循 数 写 多 构 出 电 造 元素 子 原 原 理 原 子 , 子 的 可 的 核 以 电 外 根 子 电 据 排布 子 构 元素的性质 2 减 .电 小 离 , 能 同 ( 周 失 期 电 自 子 左 难 至 易 右 ) 第 : 一 同 电 主 离 族 能 自 逐 上 渐 而 増 下 大 第一电离能 逐渐
质量数=质子数+中子数 同位素的 式 (个别反常:Be>B、Mg>AU N>O、P>S)
概念和判断
电子在原子核外的一个空间 运动状态称 3.元素的电负性(在化合物中吸引电子的能力): 同
'元素符号的左上角是质量数 为一个原子轨道 原子核外电 主 右 族 元 自 素 上 的 而 电 下 负 元 性 素 逐 的 渐 电 变 负 大 性逐渐减小,同周期 自左至
元素符号的左下角是质子数 电子层(能层) 子的排布与
电子填充顺序 元素周期表
质子数=原子序数 构造原理示意图与元素周期表中周期划分
原子轨道
原 L、 子 M 由 、 里 N 向 、 外 0、 对 P 应 、 的 Q 电子层符号分别 为K、 分 道 别 , 用 s轨 s、 道 p 呈 、 球 d、 形 俵 、 示 p轨 不 同 道 形 呈 纺 状 锤 的 形 轨 , I ( s 2 « s — 2p 1 3 ) s 3 d p n 4 p s 书 3d 写 4 电 p 5 子 s 排 4d 布 5p 时 6 , s 4 能 f 即 层 低 ns 的 ( 能 n 级 — 写 2) 在 f 价电子排布与族的划分
d 展 轨 方 道 向 和 个 f 数 轨 道 依 较 次 为 复 1 杂 、 , 3、 各 5 轨 、 道 7 的伸 左边, 例如,可写3d’4s)但不能写成4/ 3d' 按电子排布,可把周期表里的元素划分成五个区咼中化学第五章物质结构元素周期律第二节元素周期表与元素周期律
在周期表中,电负性最大,非金属性最强的元素是F, 第一电离能
最小,金属性最强的元素是Cs
原子结构
电数数 _ 层子子 _ 电 _ 一序数序 一子船 族
元素周期律与元素周期表知识内容丰富,规 律性强。 定义 元素性质随原子序数递増而呈周期性变化的规律
命题多以推断题形式出现,解题时 要以元素及其化合物知识为载体,灵活
运用 物质结构理论,将解释现象、定性判断、归 兴_,、DL 纳总结、定量 实质—核外电子的周期性排布
计算相结合,多方位、多角度、 子习I天区 多层次分析问题,做好知识的
总结、归纳,
质子 使之系统化、规律化 元素周期律 各层最多容纳2/个电子 最 最外层电子数不超过8个 一原 (K层只有2个电子)
周主
一位一 总结升华
表中位置 同主素 元素性质
同周族
同 期 (先 排满 K 层,再排 L 层,再排 !^ 1 层・
第一周期:2种元素
原子半径逐渐减小(稀有气体除外) 3个短周期/ 第二周期: 8 种元素
最外层电子数从 1 ~ 8 第三周期: 8 种元素
主要化合价:正价从+ 1-+7,负价从一4-一1 稀有气体元
素为。价,0、F无正价 第四周期: 1 8 种元素
第五周期:18种元素
得电子能力逐渐增强,失电子能力逐渐减弱 第六周期: 3 2 种元素
(对应单质)还原性逐渐减弱,氧化性逐渐增强 归纳:七主、七副、 一八、
一零;三长、 三短、一不完
生成非金属气态化合物由难到易 学法 全 7个主族 I A~VHA
气态氢化物稳定性由弱到强 指导 7个副族 IB~VHB
最高价氧化物对应水化物的碱性减弱,酸性増强
第一电离能呈增大趋势,电负性变大 元素金属性与
(稀有气体除外,F电负性最大)
非金属性比较 1个VID族 8、9、10三个纵行
一看电子层数,电子层数越多 半
径越大 原子半径比
原子半径逐渐増大 二看核电荷数,电子层数相同 时, 较的一般方法 单质的还原性或离子的氧化性强弱
核电荷数越多半径越小 最高价氧化物对应水化物碱性强弱
单质与盐溶液的置换反应
主要化合价:最高正价=主族序数=最外层电子数 三 核 看 电 核 荷 外 数 电 都 子 相 数 同 , 时 当 , 电 核 子 外 层 电 数 子 和 数 单质与水或非氧化性酸反应置换出氢气的难易
越多半径越大 原电池中的正负极
| 一E繇金属作负极
(对应单质)还原性逐渐増强,氧化性逐渐减弱 以常见元素及其化合物的特殊性质为突破口
解推断题的 非金属性 强
生成非金属气态氢化物由易到难 以元素周期表中某一部分具体结构为突破口 常见突破口 弱判断 单质氧化性或离子还原性强弱
气态氧化物稳定性由强到弱 以元素的原子半径及主要化合价的数据为突破口 最高价氧化物对应水化物的酸性强弱
第一电离能逐渐变小 以元素在周期表中的相对位置及常见元素特殊性为突破口 单质与盐溶液的置换反应
单质与氧气化合生成气态氢化物的 难
电负性逐渐变小 以原子序数数值及大小关系为突破口 易及气态氢化物的稳定性强弱高高中中化化学学 第第五五章章 物物质质结结构构 元素元周素期周律期律第三节化第学四键节分子结构和晶体结构
顶 棱 点 边 : V4\晶胞中 破 粒 坏 子 化 数 学 的 键 计 不 算 一 方 定 法 发 — 生 — 化 均 学 摊 反 法 应 含有共用电子对的单质或范化德合华物力 结构式分的书子写间作用力 分概予念分类 /分 强 非 子 烈 极 或 的 性 晶 相 分 体 互 极 子 内 作性 正 相 用分 负 邻 称子 电 原 为 中 子 化 _ 心 _( 学 _ 重 或 键 _ 合 离_ 。 正 _子 如 负 _)_ 电 c o _间 中 2 _ o 心 = _ c _ 不 =o _ 重 _ 合 _ 。 __ 如 _ H _ , _ 0 - 切
面心 1/2 发生化学反应一定破坏化学键
体心 全由非金属元素 每 C形1 个 成-也 N 的 a 被物 + 个 被 质6也 6 N可 个 a能+ C 所含 l- 包离 包 围子 围 键 着,同 时每个学习误区 学习误区 氢键 表示方法 分子晶 概 体 念 含共价 原 键 子 或 间 不 通过共用电子对形成的相互作用 分子晶体
金 极 一 体 属 性 般 熔 单 元 分 规 沸 质 素 子 律 点 分 与 易 , 差 子 非 溶 原 异 中 金 于 子 较 不 属 极 晶 大 一 元 性 体 定 素 分 〉 含 每 也 化 子 离 化 个 被 合 溶 子 学 正时 剂 8 晶 键 离, 中 个 体 , 子不 ( 正 〉 如 被一 如 离 分 定 H 子 8 H 子 e C 形个 所 等 1 晶 成负 包 稀 体 离离 围 有 。 子子 气 键包 豆 体 围 米 着 曰 , 依 并 同 尖 而 顚 时 金 冲 每 属 个 晶 负离子 总结升华 单质及化合 原 离 物 子 子 的 的 的 总 电 电 电 子 子 子 结 式 式 式 的 的 的 升 书 书 书 写 写 写 华 电 书 子 写 式 的 晶 含 体 化学 类结 键 型构 G 键 极 配 性 键 位 键 化 和 、 学 7 非 键具 1 极 有 性 规 晶 键 则 体 几 类 何 型 单 双 三外 键 键 键形 均 一 — 为 个 个 。 。 0键 键 键 , , 一 两 个 个 原 金 冗 子 属It 键 键 晶 晶 体 体
易 分 自 下离 电 溶 子 由 发子 荷 分 律 质 于 溶 电 生晶 数 子 : 量 水 剂 子 定体 越 晶 気 成 中 中 在 向: 多 体 键 正 ) 外 移阴 , : 〉 比 , 加 动、 即 先 范 ) 非 电 阳 晶 看 德 极 场 离 格 氢 华 性 的 子 能 键 力 分 核 越 , ( 耳 子 间 大 再 范 由 易 距 , 看 德 导 此 溶 越 熔 相 华 电 于 作 小 沸 对 力 圧 非 用 , 点 分 又 极 离 越 子 与 性 子 高 质 相 所 量 对 ]理带 同 。 分 \ 类 解 规 子 晶 冲 体 原 “ 理 f知能 提升>」 、 ' 晶体熔 较 、 规 沸 律 点 丿 高低 V比 用电 提 子 知 升 式 能 表 示 J 物 / 质的形成过程 知识 知识 共价铤 晶体的特点 键能 概 能 各 念 使 向 : 异 X 熔气 性 射 点态 键 线 固基 释 定 产 态 放 原 的 子 最 形 低 成 能量 1 mol化 学
自 撞 由 传 电 递 子 热 与 量 金属离 原 键 子 子 越 碰 晶 稳 体 定 : , 共 熔 价 沸 键 点 键 越 长 高 越短金,属 键y i 梳理 梳理类型 晶体与非晶体 概 意生 念 义衍 : :射 成 键 键 能 两 越 原 大 子 , 的 稳 核 定 间 性 距 越强,反应越困难
晶体中各金原属子晶层体相:对金滑属 原子半径越小,价电子 数 的本质差异 晶体 亠原意子义在:三键维长空越间短里、呈键周能期越性大有,序稳排定列 性越强
动 含 仍 极 保 性共 持 键 越 价 相 的 多 键 互 分 ,作 子 金用 , 属 键 键 的 越 极 强 性 , 不 熔 能 沸 抵 点 消 越高 , 极性分子 种类 漣角 非晶体 概 念 原:子多排原列子相( 对 > 无 2 ) 序 分子中两共价键间夹角
分 只 键 电 子 含 的 子 电 结 非 极 云 子 构 类 极 性 重 云 是 型 性 可 叠 对 否 键 抵 方 称 对 的 消 式 称 分 ( 子 或 S 或 p - 电 S - 含 p 。 o荷 极 轴 头 键 键分 性 对 碰 、 布 键 称 头 s - 是 , p c 否 键 — 均 、 , 匀 -- ) --- 镜 - 肩 p 极 - 像 - - 四 并性 - 对 - 键 肩分 - 称 - 子 ---- 键 与 的 划 区 分 别 分子极性 可能学同时法含 含 共 离 指价 子 键 键 导 蘑 化合物中典型晶体结构 分子晶体 离子键干冰 构 概 成 念 意 由 阴2 3 1 4 . . . , 面义 阴 阳8 6 每 个 个 心: 、 离 个 面 立决 C 阳 子 C O 的 方定 O 离 间? ? 中 分 结分 子 通 周 心 子 构子 构 过 围 各 占 空 成 静 离 占 据 间 电 该 分 据 立 构 作 分 子 方 型 1 用 子 有 个 体 、 形 最 1 的 2 C 极 成 近 O 个 顶 性 且 ?分 点 距 子 离相等的 C02
存在 P N , C 、 h C单 (R N 、键 各 H C、 只 3, C 双 有L,键 一 、 个 三 。 键 键 )正双 三三 四键 键角 面有 有锥 体一 两形 形个 个' 冗 ;t键 键 常 见分子构型 只含共价键化 共 合 价 物 所含键型 1 为 .每 立 个 体网 C 概 构状 与 念 成结 4 亠 由 个 构 金 金 C 属 属 形 阳 阳 成 离 离 正 子 子 四 与 和 面 自 价 体 由 电 结 电 子 构 子 形 , 间 成 空 强 间 烈 发 的 展 相 互作用
BF,、 平面三角形、 反应热与 金刚石 2.C原子数与C-C之比为1 : 2
AW =反应物的S键O,能总和 HQ 一、生成物的键能总和 键能的关系 石墨是原多子电晶子体分、子金,属如晶:体五、氯 分化子磷晶体的 分子中 3.最小C环为六元环却,車每今个C原一子个为原12子个提六供元一环对共电用子,与每个
任、。2、HC1S、ON,O、乙烯气体等直线形 V形」 学法 一种混合晶体- 原子结构 ■原子晶体. 六配元位环相键当于1/2个C慨原,子0 另一个原子空轨道所形成
离子半径越小,离子所带电荷越多, 离 离分子子键构强型弱 指导 缺电子分子,如:BF: 4 . 以 S i 原子代替 C 原子,即为晶体 形 硅 的 成 结 条 构 丄 眾器顓
子键越强 价 , 层 离 电 子 子 晶 对 体 互 的 斥 熔 理 沸 论 点 模 越 型 高 判的 J 判 断断方法 8电子分子,如:C02 离子晶体 SiOz 1 . 在晶体硅结构中每个 Si-Si 键中插入寸竺三
晶格能越大,离子晶 体的熔 金属晶体的 四种堆 .2.1 mo 等 lSiO 电 : 晶 子 体中 体 有 4 mo l Si-0键
① 键 点求 能 越算 越 高价 大 、层 , 硬电 键 度子 越 越 - 对 牢 - 大互 固 - 斥 , - 理 分 - 论 - 子 - " 越 值 - 稳 - 定 ------ 中心原子杂化方式 課 Na'配 繼 位 N 数 子 a+: 6 l , + C 1 l 2 配 x- 位 i-= 数 4个 6,各自配体均构成正八面体 由非极性 Na 键 C 形 l 型 成(如足 积 、 模 。 型 2、Cb、P,等) 3 6 . 每 X 在 ] 个 /6 S = 1 i 1 O 2 个 : 元 晶 环 体 拥 中 有 , Si 最 原 小 子 环 数 为 6X 6 1 个 原 子 /1子 总 2 S = i 总 数 和 1/数2 相 6 个相 同 个 ,同 O 氧, 组 原且 成 子 的 价数电 1 为 2元 环,
------------ 键 -- 长 -- 越 -- 短 -- , -- 键 -- 能 - 越 -- 大 -X , 的 共判价断键方三法参数 cr: 6 — X+ :- + - 8 - x - ^ - = - 4 - 个 -- : 7 ------\每个晶胞实际占有由 ( 极 如 性 C0 键 2、 形 C 成 H , 」 但 等 空 ) 间结构对称 如 NH C 3 O 和 和 电 N 0 2 + ; 等
金晶 阿 体 伏 属结 加金 键构 德属 式 罗键 的的 常越 确 数 键 强 强 定 的 越 , 弱方 求 牢 其 法 算 固 金 与 , 属 分 的 子 硬 越 稳定 / 键角是 晶 的 决定 体 相 金 分 结 关 属 子空 构 计 物 间 算 构 理 型 性 的重 质 要参 的 数 关 丿 系 每个Cs • 每 最 个 近 晶 C C s 胞 + s+ 、 实 6 C 个 际 l ( 配 占 上 位 有 、 数 cs 下 均 -: 、 为 8 左 8 x 极, ^ 配 、 = 性 1 体 右 个 分构 、 ; 子成 前 cr 正 、 : 六 后 1 面 ) 个 体 构成 由 不 正 极 能 八 性 抵 面 键 消 体 形 ( \C成 如 sC, H l C 但 型 1 空 、 间 H2 结 O 构 2、 不 N 对 H, 称 等 , ) 键的极密性 - 置 - 层 --------- < 体 立 面 简 心 方 心 单 立 最 立 立 方 密 方 方 ( 堆 最 ( N 积 密 a 心 、 ( 堆 : 具 似 K M 积 配 、 有 的 g ( 位 F 、相 化 e C 数 Z ) u 似 学 n 、 、 6 : 的 性A T 配 结 质g i 、 ) 位 构 A : 数 , u ) 配表 8 : 位现 配 数出 位 许1 数 2多 12 相
度越大,熔沸点越高高中化学 第六章 化学反应与能量 第一节化学能与热能
化学变化一定伴随能量变化,但能量变化不一定伴随化学变化 在 放 化 出 学 或 反 吸 应 收 过 的 程 热 中 量 概念 Tip 表示参加反应的物质的量与
化学反应是'‘断旧键,建新键"的过程。 将 疋乂 反应热关系的化学方程式
断键吸收能量,成键放出能量记混 学习误区 热化学方程式
忘记是反应物的总能量和生成物的总能量比较 丿 , kj/mol _ 单位 反应热 1 不仅表明了化学反应中的物质变化, 也
书写热化学方程式忘记标物质的聚集状态 在稀溶液中酸碱中和生---------7^— 表明了化学反应中的能量变化
成1 mol水时的反应热中和热 在 101 kPa, 25P时
反应物和生成物要标明其聚集状态, 1 mol 纯物质完全燃烧生成稳定 的氧化物所放出的 定义 放出热量的化学反应,AW<0
压状态 用 下 g 反 、 应 1 、 放 S 出 分 、 别 ^ 代 52 表 25 气 2 或 态 吸 、 收 液 的 态 热 、 量 固 , 态 放 方 热 程 为 式 负 右 、 边 吸 用 热 A 为 R 正 标明恒 能量 ~ 根 J 然 据 烧 盖 热 斯定律求素 分类 放 反 热 应 本 '判 质 断 亠 断键吸收的能量〈成键放出的能量
卩王式注息事项 .方法
热化学方程式中各物质前的化学计量数不表示分子 个数, A0值与热化学方程式化学 计 计算 一 反 中 应 和 物 反 的 应 总 、 能 燃 量 烧 大 反 于 应 生 、 成 金 物 属 的 与 总 酸 能 ( 量 或
只表示物质的量,因此可以是整数或分数丿 量数对应 常见的 水)
放热反 的反应、大多数化合反应
对 即 于 M 相 的 同 值 物 与 质 化 的 学 反 计 应 量 , 数 当 成 化 正 学 比 计 , 量 当 数 化 不 学 同 反 时 应 , 逆 其 向 A 进 //也 行 时 不 , 同 数 , 总结升华 化学反应 应 定义 吸收热量的化学反应,宜>0
值不变,符号相反 丿 中的能量 吸热 [本质
反应 一 断键吸收的能量>成键放出的能量
判 断
标准燃烧热 中和热 方法 反应物的总能量小于生成物的总能量
能 变 量 化 放热反应 燃烧热和中 和热 I I 常 吸 见 热 的 反应 -Ba ( O 大 H 多 ) 数 2 ・ 分 8 解 比 反 0 应 的 、 反 N 应 H .C1和
A//<0,单位 kJ/mol 的区别 化学反应的反应热只与反应的始态(各反应物)和终态
标准 1 mol可燃物 生成1 mol水 若某一个化学反应 可分多 ( 应 各 可 生 以 成 分 物 几 ) 步 有 进 关 行 , , 而 则 与 各 反 分 应 步 的 反 途 应 径 的 无 反 关 应 。 热 即 之 如 和 果 与 一 该 个 反 反 应
1 mol反应物完 生成1 mol水 步进行,则 总反应热为各 一步完成时的反应热是相同的
全 燃烧时放出 时 放出的热
含义 生 反 成 应 物 物 的 的 准分 分 热 反 燃子 子 应 烧成 断 量 物 热键 键 。 , 不时 时 不 同释 吸 同 标 放 收 出 的 的 总 总 能 量 强 约能 量 。 碱 为量 强 中 一 大 和 5 酸 7于 热 .3 和 放热 步 反 反 应 应热之和 吸、放热反应 学 指 法 号 意义 盖 得 ( 果 斯 很 有 应 定 慢 副 用 律 , 反 盖 在 有 应 斯 科 些 发 定 学 反 生 律 研 应 ) , 究 不 , 就 中 容 这 可 具 易 给 以 有 直 测 间 重 接 定 接 要 发 反 地 意 生 应 把 义 , 热 它 。 有 造 们 因 些 成 的 为 反 了 反 有 应 困 应 些 的 难 热 反 产 。 计 应 品 此 算 进 不 时 出 行 纯 如 来
生成物分子成键时释放出的总能量 \微观角度
小于反应物分子断键时吸收的总能量吸热反应)--------------------- 的判断
反 反 应 应 物 物 具 具 有 有 的 的 总 总 能 能 量 量 大 小 于 于 生 生 成 成 物 物 具 具 有 有 的 的 总 总 能 能 量 量 吸 热 反 应 放 〉 热反应 宏观角度 1.组装绝热装置
2 . 准确读取混合液的最高温度
放 吸 热 热 反 反 应 应> 表示方法 中和反应反应热测定的注意事项 3.多次测量取平均值
2H2(g)+O2(g) = 2H2O(g) A//=-483.6 kJ mol 放热反应 盖斯定律的应用
C(s)+H2 的 极 判 ) 断 内 电 电 极 路 反 : 应丿 是 断 电 地 池 进 就 行 连 反 续 应 不 , 断 生 地 成 供 由 物 电 外 不 部 断 供 地 给 被 。 排 在 出 电 , 极 上 I于 不
注意根据电解质 电 溶 极 液 判 的 断 性 方 质 法 确 参 定 照 产 学 物 法指导 电极反应式及电池总反应方程式的书写 知识梳理 金属 卒质 匕 1 化学腐蚀
金属的电化学 的 ・ 腐蚀 < 类型 析氢腐蚀
各种不同用途的电池的广泛应用 腐蚀与防护 电化学腐蚀
金属的防护 一 、 本质 防止金属被氧化'吸氧
金属
例如:铁器损伤用比铁活泼的金属锌修补金属器皿修未卜 的防护 改 在 变 金 金 属 属 表 内 面 部 覆 的 盖 组 保 织 护 结 层 构 或
原电池原理 方法 . 牺牲阳极的阴极保护法
一般负极金属比正极活泼 判 强 断 弱 金属 活动性 的应用 一 KC 般 1 是 溶 装 液 有 的 含 U 琼 形 胶 管 的饱和诚竺■ 外加电流的阴极保护法
锌与稀硫酸反应制取氢气用 粗 加快反应速率 丿 盐桥
锌会加快产生氢气的速率
1.形成闭合回路,使两侧溶液形成通路
学法 作用 /—----
2
-.-平--衡--电--荷----------------------------
负极材料失电子,被氧化 指导 3.提高工作效率,最大程度地降低副反应的发生
负极参加反应 的 原电池电极
酸性溶液 正 电 极 解 反 质 应 溶 考 液 虑) 原电池 反应式的书写 不 作 要 负 形 极 成 "的 "活 思 泼 维 金 定 属 式 一 定
不 属 活 盐 泼 溶 金 液 如鉛蓄电池 两 原 极 电 都 池 参 丿 加反应 的 原电池 正极亠相对不活泼的金属或非金属
原理
两极都不参加
如氢氧燃料电池反应的原电池 负 电子流出(电流流入), 电解
极亠 质溶液阴离子流向的极
〈正
极_ 电子流入(电流流出),
根据原电池的构造,先分析正、负极, 依据电极反应 的 、电解质溶液阳萬子流向的极
再根据反应规律书写电极反应式 现象判断 极一 负 一 极 般是不断溶解,质量减少的
根 简 据 单 电 的 池 电 的 极 总 反 反 应 应 式 , , 找 再 到 用 氧 总 化 反 反 应 应 减 或 去 还 简 原 单 反 的 应 电 , 极 写 反 出 应 一 , 个 从 依据反应 '正 极 有气体生成或质量増加的极
而得到另一个较复杂的电极反应式 类型判断 极_ 负 〜失去电子,发生氧化反应
〈正
书写时,考虑电解质溶液中的离子的参与(尤其是燃料电池) 极 〜得到电子,发生还原反应
考查原电池中电流、电子移动方向高中化学第六章化学反应与能量第三节电解原理及其应用
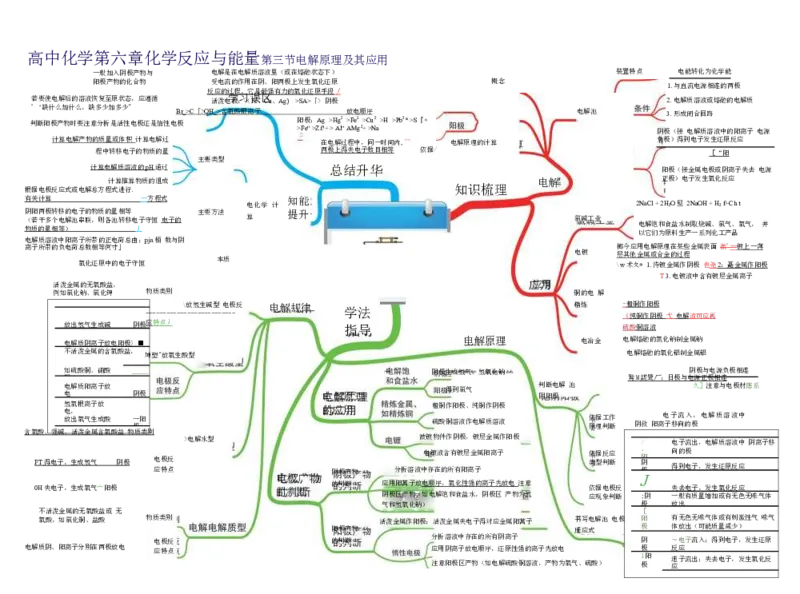
一般加入阴极产物与 电解是在电解质溶液里(或在熔融状态下) 装置特点 电能转化为化学能
若要使电解后的溶液恢
阳
复
极
至
产
原
物
状
的
态
化
,
合
应
物
遵循
反
活
受 应
泼
电 的
电
流 过学
极
的 程
:
作 习,
(
用 它误
F
在 是
e、
阴 区最
C
、 强
u
阳
、
有 两
A
力
g
极
)
的 上 氧
>
发
S
化
A
生
>
还 氧
「
原 化
>
手 还
阴
段 原
极
丿 概念
2
1
.
.
电
与
解
直
质
流
溶
电
液
源
或
相
熔
连
融
的
的
两
电
极
解质
'‘缺什么加什么,缺多少加多少" Br_>C 「 > OH_> 含氧酸根离子 放电顺序 电解池 3.形成闭合回路
判断阳极产物时要注意分析是活性电极还是惰性电极 阳 >F 极 e" : >Z A i? g + + > > H A g l 2 " + A >F M e3 g + 2 + > C > u N 2+ a >H+ >Pb2* >S『+ 阴极(接 电解质溶液中的阳离子 电源
计算电解产物的质量或体积 计算电解过 在电解过程中,同一时间内,~~ 电解原理的计算 负极)得到电子发生还原反应
程中转移电子的物质的量 两极上得失电子数目相等 依据/ [ “阳
主要类型
计算电解质溶液的 pH 通过 总结升华 阳极(接金属电极或阴离子失去 电源
计算推算物质的组成 电解 正极)电子发生氧化反应
根据电极反应式或电解总方程式进行. 知识梳理
有 阴 ( 物 关 阳 若 质 计 两 干 的 算 极 多 量 转 个 相 移 电 等 的 解 ) 电 池 子 串 的 联 物 , 质 则 的 各 量 池 相 转 等 移 电 丿 子 — 守 方 恒 程 式 电 子的 主要方法 电 算 化学 计 知 提 能 升 氯碱工业 2 电 以 Na 解 它 Cl 饱 们 + 和 为 2H 食 原 2O 盐 料 堅 水 生 制 产 2N 取 一 aO 烧 系 H 碱 列 + 、 化 H 氯 工 2 f 气 产 +C 、 品 h t 氧气, 并
电解质溶液中阳离子所带的正电荷总由;pjn栢 数与阴
离子所带的负电荷总数相等何寸」 榔今应用电解原理在某些金属表面 倣' — 镀上一薄
氧化还原中的电子守恒 本质 电镀 层 \ w 其 术 他 夂 金 * 属 1. 或 待 合 镀 金 金 的 属 过 作 程 阴极 也 尧 2 :矗金属作阳极
T 3.电镀液中含有镀层金属离子
活泼金属的无氧酸盐, 应用
例如氯化钠、氯化钾 物质类别 铜的电 解
—--------- \ - 放 -- 氢 -- 生 -- 碱 -- 型 -- - 电 -- 极 - 反 电解规律 学法 精炼 - 《 粗 纯 铜 铜 作 作 阳 阴 极 极 弋 电解 液可应 再
放出氢气生成碱 阴极 应 特点丿 指导 硫酸 铜溶液
电解质阴离子放电阳极〉■ 电解原理 电冶金 电解熔融的氮化钠制金属钠
不活泼金属的含氧酸盐, 坤塑"放氧生酸型 电解熔融的氧化铝制金属铝
0如硫酸铜、硝酸 _____ 一 阴极生成氢气、氢氧化钠 阴极与电源负极相连
银 > 鷲 M 謀鹭 厂 ;日极与电源正极相连
电 电 解质阳离子放 阴极 电解原理 得到氯气 判 阴 断 阳 电 极 解 池 久]注意与电极材應系
氢 电 放 氧 , 出 根 氧 离 气 子 生 放 成酸 一 极 阳 / 的应用 硫 粗 酸 铜 铜 作 溶 阳 液 极 作 、 电 纯 解 铜 质 作 溶 阴 液 极 依 原 据 理 工 判 作 断 阴救 阳离 电 子 子 移向 流 的 入 极 ,电解质溶液中
含氧酸、强碱、活泼金属含氧酸盐 物质类别
>电解水型 被镀物件作阴极,镀层金属作阳极 / 电子流出,电解质溶液中 阴离子移
FT 得电子,生成氢气 阴极 电 应 极 特 反 点 电极广物 阴极产物 分析溶液中 电 存 镀 在 液 的 含 所 有 有 镀 阳 层 离 金 子 属阳离子 依 类 据 型 反 判 应 断 、 阳 阴 极 J 向 得 的 到 极 电子,发生还原反应
0H失电子,生成氧气宀阳极 的判断 的判断 应 阴 用 极 阳 区 萬 产 子 物 放 ( 电 如 顺 电 序 解 , 饱 氧 和 化 食 性 盐 强 水 的 , 离 阴 子 极 先 区 放 产 电 物 注 为 意 氢 依 应 据 现 电 象 极 判 反 断 ~;阴 失 一 去 般 电 有 子 质 , 量 发 増 生 加 氧 或 化 有 反 无 应 色无味气体
气和氢氧化钠) 极 放出
不活泼金属的无氧酸盐或 无 [
氧酸,如氯化铜、盐酸 物质类别 阳极产物 活泼金属作阳极:活泼金属失电子得対应金属阳萬子 书 反 写 应 电 式 解池 电极 阳 极 有 体 无 放 色 出 无 ( 味 可 气 能 体 质 或 量 有 减 刺 少 激 ) 性气 味气
电极反 的判断 分析溶液中存在的所有阴离子 阴 〜电子流入;得到电子,发生还原
电解质阴、阳离子分别在两极放电 应特点 应用阴离子放电顺序,还原性强的离子先放电 极 反应
注意阳极区产物(如电解硫酸铜溶液,产物为氧气、硫酸) 1 极 阳 速 应 子流出;失去电子,发生氧化反
一高中化学第七章化学反应速率和化学平衡 第一节化学反应速率及影响因素
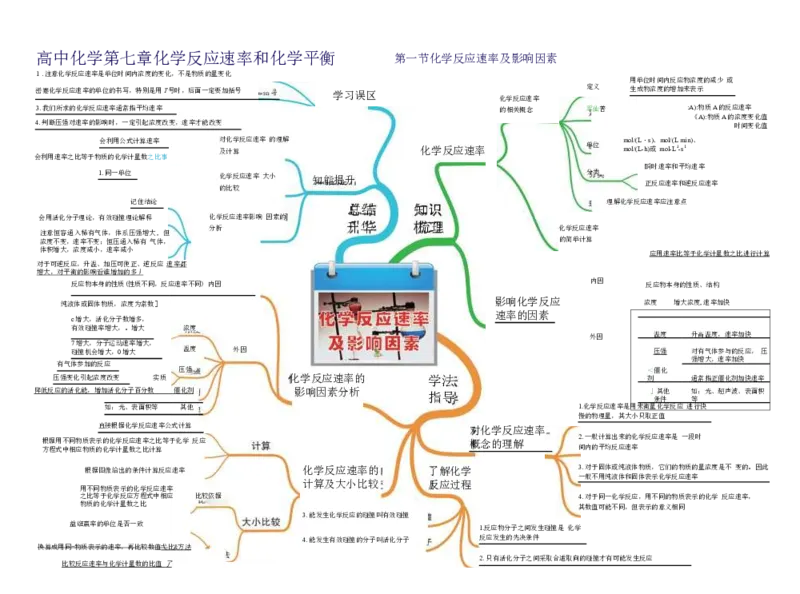
1 .注意化学反应速率是单位时间内浓度的变化,不是物质的量变化
用单位时间内反应物浓度的减少 或
巒蹇化学反应速率的单位的书写,特别是用T号时,后面一定要加括号 学习误区 定义 生成物浓度的增加来表示
化学反应速率
3.我们所求的化学反应速率通常指平均速率 的相关概念 军仙普 :A):物质A的反应速率
《A):物质A的浓度变化值
4.判断压强对速率的影响时,一定引起浓度改变,速率才能改变 时间变化值
会利用公式计算速率 对 及 化 计 学 算 反应速率 的理解 化学反应速率 单位 m m o o l l / / ( ( L L- ・ h) s 或 )、 m m o o l l - /( L L 1 - m s l in)、
会利用速率之比等于物质的化学计量数之比事
瞬时速率和平均速率
1.同一单位 化学反应速率 大小 知能提升 分类
的比较 正反应速率和逆反应速率
记住结论 总结 知识 理解化学反应速率应注意点
会用活化分子理论,有效碰撞理论解释 化学反应速率影响 因素的
分析 升华 梳理 化学反应速率
注意恒容通入稀有气体,体系压强增大, 但
浓度不变,速率不变;恒压通入稀有 气体, 的简单计算
体积増大,浓度减小,速率减小 应用速率比等于化学计量数之比进行计算
对于可逆反应,升温、加压可使正、逆反应 速率都
增大,对平衡的影响看谁増加的多丿
反应物本身的性质(性质不同,反应速率不同) 内因 内因 反应物本身的性质、结构
纯液体或固体物质,浓度为常数] 影响化学反应 浓度 増大浓度,速率加快
速率的因素
c増大,活化分子数増多,
有效碰撞率增大,。増大 浓度
外因 温度 升高温度,速率加快
7增大,分子运动速率増大,
碰撞机会増大,0増大 温度 外因 压强 对有气体参与的反应, 压
有气体参加的反应 强增大,速率加快
压强 <催化
压强变化引起浓度改变 实质 化学反应速率的 学法 剂 通常指正催化剂加快速率
降低反应的活化能,増加活化分子百分数 催化剂 影响因素分析 指导 」 条 其 件 他 如 等 :光、超声波、表面积
如:光、表面积等 其他 1.化学反应速率是用来衡量化学反应 进行快
慢的物理量,其大小只取正值
直接根据化学反应速率公式计算 对化学反应速率
根据用不同物质表示的化学反应速率之比等于化学 反应 概念的理解 2.—般计算出来的化学反应速率是 一段时
方程式中相应物质的化学计量数之比计算 间内的平均反应速率
根据图像给出的条件计算反应速率 化学反应速率的 了解化学 3.对于固体或纯液体物质,它们的物质的量浓度是不 变的。因此
计算及大小比较 反应过程 一般不用纯液体和固体表示化学反应速率
用不同物质表示的化学反应速率
之比等于化学反应方程式中相应 比较依据 4.对于同一化学反应,用不同的物质表示的化学 反应速率,
物质的化学计量数之比 其数值可能不同,但表示的意义相同
3.能发生化学反应的碰撞叫有效碰撞
益诳赢率的单位是否一致 1.反应物分子之间发生碰撞是 化学
4.能发生有效碰撞的分子叫活化分子 反应发生的先决条件
换算成用同-物质表示的速率,再比较数值 弋 比 & 方法
2.只有活化分子之间采取合适取向的碰撞才有可能发生反应
比较反应速率与化学计量数的比值 了高高中中化化学学第 第八七章章水 溶化液学中反的应离速子率平和衡化第学一平节弱衡电 解第质二的节电离 化学平衡及化学反应进行的方向
等
反 比
速
应 等
一
速 于
定
率 化
要
。 学
C一
如 计 如
个
不 量 果弱
表
同 数 是 離 电
示
的 之 恒 碗 解
正
物 比 容 溶 质
反
质 体 液 溶
应
表 系 导 液
速
示 , 电 导
率
还 全 性 电
,
要 部 亲 性
一
注 是 二 气
个
气 意 達
表
体 速 嬰 ,
示
率 /则
逆
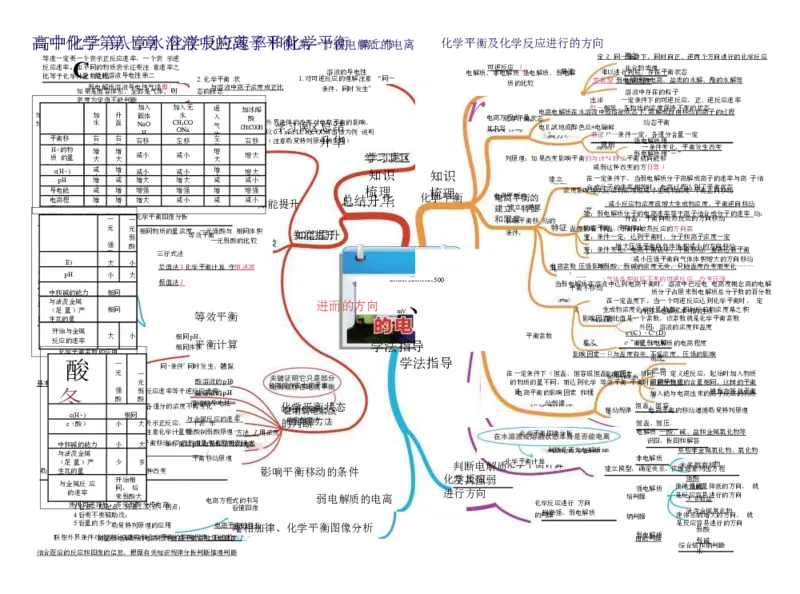
之 2 态 .化 的 学 标与 平 志溶 衡 液 中 状 离子浓度成正比 1.对可逆 条 反 溶 件 应 液 , 的 的 同 理 导 时 解 电 发 注 性 生 意 " “同一 电 r 解质、 可 非 逆 电 反 解 应 质 质 的 丿 比 强 / 较 电解质、弱特电征解 参
定
类 难
义
型 以
同
进 弱
一
行 电
概
化 电 溶
条
到 解
念
合 离 液
件
底 质 物 程 中
下
, 的 类 度 存
,
存 电 理 在
同
在 离 的
时
平 、 粒
向
衡 盐 子
正
状 类
、
态 的
逆
水
两
解
个
、
方
酯
向
的
进
水
行
解
的
等
化学反应
密度为定值不能判断 出泌 一定条件下的可逆反应,正、逆反应速率
如 均 果 相 3 动 是 对 平 动 质 . H 升 看 反 分 衡 + 的 的 温 谁 应 子 移 物 量 , 增 前 质 加 加 后 量 压 得 气 等 , 多 体 为 加 水 右 移 増 大 正 体 定 、 积 值 逆 相 不 反 升 温 右 移 増 大 同 能 应 , 作 速 则 为 率右 减 气 标 加 固 N 均 H 移 小 a 体 志 入 体 O 増 总 大 压 , 、 平 平 C 加 衡左 减 O H 入 水 如 N3 移 小 C a 无 何 O 移 通 入 气 体左 移 增 大 C 加 H 右 增 3 冰 酸 C 移 大 O 醋 OH外 以 ( 界 注 0 学 .1 条 意 m 件 勒 习 ol 的 夏 /L 误改 特 CH 变 列 区 3C 对 原 O 总 升 电 理 OH 离 的 溶 结 华 平 应 液 衡 用 为 的 ) 例 影 响 说 , 学 明 习误区 电 其 离 书 方 写 化 列 程学 原 式平 理 及衡 : 状 如 态 果 电 电 改 离 E 变 試 电 影 地 解 响 或 质 平 醉 在 衡 色 水 的 丝 溶聲 特 与 * 液 电 — 征 计 中 原 鼬 相 尸 * 或 则 4 鲜 等 — 熔 睜 , 条 融 二 各 件 状 平 物 一 态 衡 强 弱 质 定 下 就 电 电 一 的 动 , , 向 解 解 离 条 浓 态 各 能 质 质 解 件 度 平 组 够 用 用 成 变 保 衡 分 " 自 化 持 ― 含 由 , 不 ” 量 移 平 变 一 动 衡 的 定 的 发 状离 生 态子 改 的 变 过程
4(.c平m( p H衡 H o+l)正)向移动减 小増 ,转化率増 大减 不一定减 増 增小 大 大 减 増 小 大 増 大减 增 减 大 小 知识 知识 建立 在 减 一 弱 定 这 条 种 件 改 下 变 , 的 当 方 弱 日 电 婴 解 丿 质分子离解成离子的速率与离 子结
5 仍 导 力电 度 .平 然 电 离 衡 是 能 程 计 定 算 义 往 式 往 和 大减 弱増 大 融 比 合 例 速 式 率小増 强増 大 计算,增 増 强 大 其依据 増 减 强 小 小増 强减 小 增 减 强 小知能提升 总结 梳 升 理 华 化 梳 学平 理 衡 电咼平 建 听 立 的 、特征 浓度影响合增成大分反 . 子 减 应的 小 物速 反 浓率 应 度相 物 或等 浓 减时 度 小, 或 生电 增 成离 大 物过 生 浓程 成 度达 物 '到平 浓 了衡 度 平正 , 衡向 平 状移 衡 态动 逆向移动
看懂图像、联想规律、作—出判断— 化学平衡图像分析 影响平衡移 动的 等:弱电解质分升子温的,电平离衡速向率吸等热于反离应子的结方合向成移分动子的速率 动:
看 运 清 用 条 “ 件 一 , 边 分 倒 析 "的 反 方 应 法 特 元 强 酸 点, 元 弱 酸 相同物 三 质 行 的 式 量 法 浓度等、效一平元衡 一 强 元 酸 弱 与 酸 相 的 同 比 体 较 积 知能提升 条件, 温度影动 定 变 响态 : : /平 条 条 降衡 件 件 温, 一 变 , 増 没 定 化 平 大 有 , , 衡 压 停 达 电 向 强 止 到 离 放 平 平 平 热 衡 衡 衡 反 向 时 破 应 气 , 坏 的 体 分 , 方 体 子 平 向 积 和 衡 赢 减 离 移小 子 动的 浓 ,方 度 重向 一 新移 定 达动新平衡
E) 大 小 差值法 3 化学平衡计算 守 恒法河 电离常数 压 强 影 与响弱)酸/-、--弱-- / 碱- 减 -的- 小 -浓- 压 -度- 强 -无- 平 -关- 衡 -,- 向 -只- 气 -随- 体 -温- 体 -度- 积 -改- 增 -变- 大 -而- 的 -变- 方 -化- 向 -- 移 -- 动 -
看 还
看 反
清 是
清 应与 中
条 恒
反 前活 和
件 温
应 后泼 碱
是 恒
的 气
pH
金 的
恒 压
特 体属 能
温
点 体 力
恒
: 积
容
是 否变
小
相 化 同
大 极值法 丿
进而的方向
--------
、
.-----------500 当弱电 ' 平解 一 衡质不在移溶动液\气
在
中体
一
达体
定
到积
温
电前
度
离后
下
平不
,
衡
质
变
当
时
分
的
一
,
子
可
个
溶
占
逆
可
液
原
反
逆
中
来
应
反
已
弱
,
应
经
电
改
达
电
解
变
到
电
质
压
化
离
总
强
学
度
分
,
平
概
子 衡
念
数 时
离
的 ,
的
百 定
电
分
解
数
用好 ( 生方 足 瓦法 的: 量 量' ) ‘ 产 一边倒" 相同 等效平衡 mV 义 影响因 生 素的 成 比 物 值 浓 是 度 一 化 个 内学 常 因计 数 :量 , 电数 该 解慕 常 质之 数 本积 就 身与 是 的反 化 性应 学 质物 平 浓 衡 度 常 幕 数 之积
开 反物 化 始 应质 学 酸 与 的 平 浓 平 金 速 衡 度 衡 属 率 转 的 常 化 变 数 率 化 的 的 关 应 求 大系 用 解— 小 同-条 相 相 件 同 同 '同 体 pH 时 平积 、 发 衡 生、 计 體鬣 算 学法指 学 导 法指导 平衡常数 影响 意 因 义 素 一只 与温 c c 度 ” "( 有 衡 C (A ) 外 关 量 ) ・ ・ 因 , 弱 C 不浓 c : " 电" ( 受 ( 度 D 溶 旬解 浓 ) 液 质 度 的 的 、 浓 电 压 度 离 强 和 程 的 温 度 影 度 响
元 — 在一定条件下(恒温、恒容或恒温影、响恒因压素),对同一可 定义逆反应,起始时加入物质
基本方法 冬 :三行式和差值法 强 元 弱正 反应速率等于逆反 酸 盐应 溶 溶速 液 液率 的 的 p p H H 包离或存在电离平衡 的 电 物 离 质 平 的 衡 量 的 不 影 同 响 , 因 而 素 达 到 和 化 移 学 等效平衡平衡时,同 加 同离 入 种子 能 物效 与 质应 电 的 离 含 出 量 来 相 的 同 就离 , 称子 这 为反 样 等应 的 效的 平 平物 衡 衡质
c( c(H 酸 + ) ) 用等速: 酸 小注 相 意 同 一 酸 大个表 各 示 组 正 分 反 的 应 浓 , 度 一 不 与 溶 个 再 金 液 表 变 属 的 化 反示 导 应 电 的 性 速率 化 的 证 的 明学 判实 弱 验 电平 断方 解 法 衡质状态 动规律 移动规律恒 恒 温 温 电、 、 离恒 恒 平容 压 衡 . 的移动遵循勒夏特列原理
逆反应,不同物质注意化学计量数强酸制弱酸原理- 方法 J 用浓度 化学平衡图像分析 电解质 —酸、 碱、盐和金属氧化物等
中和碱的能力 不小变,注意大平衡移动稀,释7前 该后物p理H量与变稀化释即倍可数作的标关志系 识图、析图和解答
勒夏特 与 ( 生列 活 足 瓦原 泼 的理 量 金 量的 ) 属 应 产 用,注 意 少 是 减 弱 多 这 种 改 变 平 衡 丿 移 动原理 影响平衡移动的条件 判断电解质化 学平衡计算 判断是否为电解质 建立模型, 非 确 电 定 解 关 质 系,依 某 据 些 题 非 意 金 列 属 出 氧 方物 化 程 物、氧化物
与金 的 使 属 1 2 3 4 速 用 看 看 看 看 反 率 可 面 线 点 要 逆 应 , , , 不 符 即 即 即 要 号 看 线 起 辅 , 坐 的 点 助 多 开 同 来 标 变 、 线 元 始 , 弱 识 化 终 ; 弱 相 酸 某 趋 点 后 酸 大 图 势 、分 ; ; 交步点电、离拐点; 电离方程 看 式 懂 的 图 书 像 写 弱电解质的电离 化 进 及学 行 其反 方 强应 向 弱 化 的 学 判判 反 据断 应 强 进 、 行 弱 电 方 解 向 质 培 炳 判 判 强 据 据 电解质 使 是 使 体 反 体 强 ' 大 活 系 应 强 系 酸 多 泼 能 容 碱 炳 数 金 量 易 増 盐 属 降 进 大氣 低 行 的化 的 的 方物 方 方 向 向 向 , , 就 就
5看量的多少勒夏特列原理的应用 电离平曜衡的相移加动 亠 律、化学平衡图像分析 是反应容 弱 易 酸 进行的方向
联想外界条件对衡化量学弱反电应解速质率的和电化离学程平度衡 电的离影平响衡规常律数 一及联电想离枕 度 俘 J ) - 由弱能电判解据质 弱碱
综合焙和炳判断
结合题给的反应和图像的信息,根据有关知识规律分析判断推理判断 水高中化学 第八章 水溶液中的离子平衡 第二节 水的电离和溶液的酸碱性
応)三匝57^3聪电解质,存在电ggj就,粕誕興*關
1.判断溶液的酸碱性与pH的关系时,如用“pH=7"作标准注意温度一定是常温
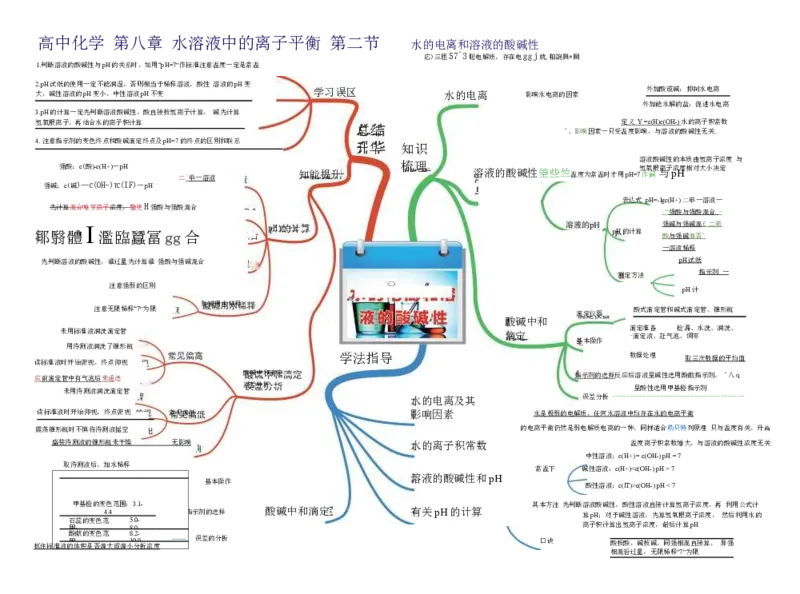
2 大 .p , H 碱 试 性 纸 溶 的 液 使 的 用一 pH 定 变 不 小 能 , 润 中 湿 性 , 溶 否 液 则 p 相 H 当 不 于 变 稀释溶液,酸性 溶液的pH变 学习误区 水的电离 影响水电离的因素 外加酸或碱:抑制水电离
外加能水解的盐:促进水电离
3.pH的计算一定先判断溶液酸碱性,酸直接按氢离子计算, 碱先计算
氢氧根离子,再结合水的离子积计算 总结 '、影响因素一只受 定 温 义 度 影 Y 响 = , c(H 与 )c 溶 (O 液 H 的 -) 水 酸 的 碱 离 性 子 无 积 关 常 . 数
4.注意指示剂的变色终点和酸碱滴定终点及pH=7的终点的区别和联系 升华 知识
强酸:c(酸)-c(H+)一pH 二 ^ 单一溶液 知能提升 梳理 溶液的酸碱性箜些竺温度为常温时才用pH=7 溶 氢 作 液 氧 嗣 酸 根 与 碱 离 性 子p 的 浓H 本 度 质 相 由 对 氢 大 离 小 子 决 浓 定 度 与
强碱:c(碱)—C(OH-)TC(IF)一pH
先计算混合唾穿离子浓度,鑒更H强酸与强酸混合 表达式 pH=-lg
“
c (
强
H+
酸
)
与
二
强
单
酸
一
混
溶
合
液 —
-
鄒翳體 I 濫臨蠶冨gg合 pH的计算 pH的计算 强 酸 碱 与 与 强 强 碱 碱 混 混 否 £ ' 二茧
一溶液稀释
先判断溶液的酸碱性,谁过量先计算谁 强酸与强碱混合 pH 试纸
测定方法 指示剂 一
注意强弱的区别 pH计
駿碱用水稀释
注意无限稀释“7"为限 滴定仪器 酸式滴定管和碱式滴定管、锥形瓶
酸碱中和
未用标准液润洗滴定管 滴定 滴 -滴 定 定 准 液 备 、赶气泡 检 、 漏 调 、 零 水洗、润洗、
基本操作
用待测液润洗了锥形瓶
读标准液时开始俯视,终点仰视 学法指导 数据处理 取三次数据的平均值
应 前滴定管中有气泡后 来通 迭 酸碱中和滴定 指示剂的选择反应后溶液呈碱性选用酚敵指示剂, '八q
未用待测液润洗滴定管 渓差分析 呈酸性选用甲基橙指示剂
水的电离及其 误差分析 ---------------------------------------
读标准液时开始仰视,终点俯视 常见偏低 影响因素 水是极弱的电解质,任何水溶液中均存在水的电离平衡
震荡锥形瓶时不慎将待测液摇空 的电离平衡仍然是弱电解质电离的一种,同样适合勒只特列原理 只与温度有关,升高
盛装待测液的锥形瓶未干燥 无影响 水的离子积常数 温度离子积常数増大,与溶液的酸碱性浓度无关
中性溶液:c(H+) = c(OH-) pH = 7
取待测液后,加水稀释 常温下 碱性溶液:c(H+) 7
基本操作
溶液的酸碱性和pH
酸性溶液:c(lT)>c(OH-) pH < 7
甲基橙的变 4 色 .4 范围:3.1- 指示剂的选择 酸碱中和滴定 有关pH的计算 其本方注 先判断溶 算 液 pH 酸 ; 碱 对 性 于 , 碱 酸 性 性 溶 溶 液 液 , 直 先 接 算 计 氢 算 氣 氢 根 离 离 子 子 浓 浓 度 度 , , 再 然 利 后 用 利 公 用 式 水 计 的
石 围 蕊 : 的变色范 5 8 . . 0 0 - 离子积计算出氢离子浓度,最后计算pH
抓住标准液的 酚 围体 献 :积 的 是 变 否 色 偏 范 大或偏小 8 1 . 0分 2 . - 0析浓度 _____ 误差的分析 口诀 酸按酸,碱按碱,同强相混直接算, 异强
相混看过量,无限稀释"7"为限高中化学 第八章 水溶液中的离子平衡 第三节盐类的水解
电离大于水解显酸性,如: 1 .判断酸式盐的电离和水解的区别 左。 盐电离出来的某一种或多种离子跟水电离出来的H'
HSO ;、 HzPO ; _ _ _ _ _ _ _ _ _ _ _ 学习误区 也乂 或 OH 生成弱电解质的反应叫盐类的水解
水解大于电离显碱性,如: 2 . 弱酸的酸式 盐溶液酸碱性的判断 HCO ;、 HPO 厂 实庾-促进水电离,酸碱中和反应的逆反应~
色 嬰雙弱 碱盐的酸碱性看相对强弱,也有中性的,如:醋酸铉溶液 盐类水解的
条件 . 盐必须溶于水,必须有弱酸阴离子或弱碱阳离子
实质及规律
特征 水解反应为吸热反应
比较同一离子浓度时,要 注 注意一个 水解程度一般较小
意其他离子对它的影响 “影响” 有弱才水解,都弱都水解,越弱越水解,谁强显谁性
弱 离 电 子 解 的 质 水 的 解 电 都 离 是 和 微 盐 弱 溶 的 液 中 紧 “ 抓 微 两 弱 个 ” 规律 多 其 元 盐 弱 碱 酸 性 根 更 , 强 浓 ( 度 如 相 Na 同 zC 时 O 酸 pN 根 aH 比 C 酸 O, 式 ) 酸根水解程度大 得多,
多 解 元 都 弱 以 酸 第 的 一 电 步 离 为 和 主 多 , 元 其 弱 余 酸 各 的 步 酸 为 根 次 离子 水 比 关 较 系 粒子浓度 大小 知能提升 盐 解 中 程 酸 度 根 越 对 大 应 , 的 溶 酸 液 越 的 弱 碱 ( 性 或 ( 阳 或 离 酸 子 性 对 ) 应 越 的 强 碱越弱), 水
注意弱酸酸式根离子有的以水解为主, 电 明 ' 确 主 三 次 个 ” 盐 方 类 程 水 式 解 的 离 书 子 写 盐类水解反应一般是可逆反应,反应方程式中要用可逆符号
离为次;有的以电离为主,水解为次 华升结总 知识梳理 一般盐类水解的程度很小,水解产物的量也很少,通常 不生成
弱酸与弱酸盐以等物质的量浓度组成的 混 沉淀和气体,也不把易分解的产物写成分解的形式
合溶液中,一般来说以弱酸的电离为 主, 多元弱酸的盐水解反应分步写,但以第一步为主; 多
水解为次 原 电 子 荷 守 守 恒 恒 遵 “ 守 守 三 恒 个 " 丿 理原列特夏勒合符 元弱碱盐水解方程式一步到位 组成盐的酸根对应的酸越弱(或阳
质子守恒 影响盐类水解 内 因 -- 盐 -- 本 -- 身 -- 的 -- 性 -- 质 -- - 离 -- 子 、 对 子 应 ( 的 或 碱 弱 越 碱 弱 阳 ) 离 , 子 则 ) 弱 越 酸 易 阴 水 萬 解
平衡的因素 盐的水解是吸热反应,温度越 高水
盐溶液水解生成难挥发性酸时,一般得原物质 度温 解程度越大(越热越水解)
盐溶液水解生成易挥发性酸时,一般得对应的弱诚、 盐 物 溶 判 液 断 蒸干 后产 外因 浓度 浓 (越 度 稀 越 越 小 水 , 解 水 ) 解程度越大
钠盐、钾盐等溶液,一般得原物质 =f 外加酸、碱能促进或抑制盐的 水
■看虑盐受热时是否分解,如:碳酸氢盐 酸、碱 解(H,促进阴离子水解而抑 制
阳离子水解;0H促进阳离 子水解
其他多迎方性面盐考溶虑液,在如空:气次中氯蒸酸干钠注溶意液氧蒸化干得到氯化 趙丿 / 学法指导 盐类水解 而抑制阴离子水解)
加入水解后生成的酸抑制水解和贮存易水解的盐溶液 的应用 在工农业生产 和日 制 制 泡 备 沫 氢 灭 氧 火 化 剂 铁航
由水解规律判断 比较盐溶液的酸碱性 常生活中 ,化肥 的使用
水解呈碱性的离子在 明砚净水
酸 水 性 解 条 呈 件 酸 下 性 不 的 存 萬 在 子在 > 注意溶液的酸碱性 碱性条件 共离判 用应的解水 在化学实验中 热碱液去油污效果好
下不存在 / 存子断
水解互相促进的离子不能共存 - 注意双水解
判断溶液的酸碱性
运用化学平衡移动原理 抓住 只有盐水解, 而酸、碱是电离 判断溶液蒸干时的产物
电荷守恒 电离平衡和水解平衡 比 较 大 小 浓 度 粒 子 水解的类型 强 虽 酸 酸 强 弱 碱 碱 盐 性 不水解,水溶液显中 ' 金 配 属 制 阳 及 离 保 子 存 去 易 杂 水解的盐
原子守恒 遵守三个守恒 盐 Qis碱弱酸盐 水解,水溶液显酸性 判断溶液中离子浓度大小
质子守 盐溶液蒸干后产物判断 水解方程式的书写 \弱酸弱碱盐 水解,水溶液显碱性 判断离子共存
加热、蒸干某些盐溶液时不一定能 得 具体分析
到相应的盐,要考虑盐的水解
(详解见总结升华)
1二般用可逆符号表示,不加气体、沉淀符号高中化学 第八章 水溶液中的离子平衡 第四节 难溶电解质的溶解平衡
氏。只与温度有关,而与沉淀的量和溶液中的离子浓度无关 定义 在一定温度下,某固态物质在100g溶剂里达到饱和状态时所溶解的质量
固体物质 /--------------------------------------------------
一般来说,对同种类型难溶电解质,越小,其溶解度越小,越易 转化为
沉淀。不同类型难溶电解质,不能根据K”比较溶解度的大小 的溶解度,定义式溶解度⑸=|||||xioog
学习误区
绝 数 大 物质 多 的 数 溶 固 解 体的 度 溶 随 解 温度 度随 升高 温 , 度 变 的 化 升 不 高而 明 增 显 大 , , 如 如 : : 氯 硝 化 酸 钠 钾 ; ; 个 少 别 保持不变(或 沉 一 淀 定 在 ) 溶 , 液 其 中 离 达 子 到 浓 沉 度 淀 幕 溶 的 解 乘 平 积 衡 状 玄 态 之 时,各离子 浓 为 度
物质的溶解度随温度升高反而减小,如:氢氧化钙 一个常数,这个常数称之为溶度积常数,简称
疋乂 溶度积,用K“表示
溶解度小于0.01 g的电解质称为难溶电解质。生 成
难溶电解质的反应为完全反应,用生成号 , 总结升华 I A-BKs) 一 力 A"(aq)+g-(a 巩 ■角:_應 、
难溶并非不溶,任何难溶物质在水中均存在溶解平衡 沉淀溶解平衡 常 表达式 K"(A“B“)=[c(A"+)]" • [c(B* ) r
知能提升 数——溶度积
溶解过程常吸热,但氢氧化钙溶解放热,升温其溶解度减小 知识梳理 反映了物质在水中的溶解能力
溶度积是达到溶解平衡时溶液中离子浓度 化 4L, 士 只与难溶电解质的性质和温度
学计量数慕的乘积 溶度积和离 离子 影响因素 有关,与沉淀的量无关
积是任何条件下溶液中离子浓度化学 \ 子积的区别 计量数幕的乘积
离子积 ( Q c ) 溶液中有关萬子浓度幕的乘积
在难溶电解质的溶液中,当离子积大于溶度 、 沉淀反应的应用 沉淀的溶解与生成 沉淀的
积时就 会生成沉淀。如:除 Cu " 、 Hg 2 - 用 S ' 沉
转化
酸碱溶解法 淀 当 的 离 溶 子 解 积 与 小 生 于 成沉 溶 淀 度 反 积 应 、 的应用 溶解平衡的建立
氧化还原法 时,就会使沉淀溶解 溶解平衡
生成络合物 程? 等、定、亙 A '溶解平
衡的特征
用硫酸钥 做钥餐 而不用碳酸銀 _ 误服可
溶性颌盐引起中毒,"X 应尽快服用硫酸 实例探究 符合勒夏特列原理 难溶电解质的本身
钠溶液洗胃 一 >~
影响沉淀溶解 浓度加水冲稀,向溶解方向移动,不变
豊二塑淀转化为更难溶的沉淀 平衡的因素 归* 多数难溶电解质升高温度, 血度
往硫化锌的溶解平衡体系中 加入 沉淀的转化 学法指导 外因 向溶解方向移动,电増大
硫酸铜溶液可生成硫化铜 实例探究 同离子效应一向沉淀方向移动, J 不变
硬水中碳酸氢镁煮沸分解为碳酸镁,7 进一步转化为
更难溶的氢氧化镁 丿 加沉淀剂;调pH -方-法--沉淀的生成 考查溶度积的表达式 在 量 常 数 温 为 下 幕 , 的 溶 乘 液 积 中 是 各 一 离 个 子 常 浓 数 度以它们的 化学计
利用沉淀的生成达到分离或除杂的目的 应用 〉 由溶解度计算溶度积 由溶解度计算出物质的量浓度,再求溶度积
利用平衡移动原理,不断移除平衡体系中的相应离子 由溶度积计算溶解度 由溶度积求出物质的量浓度,再求溶解度
酸碱溶解法,生成配合物用举例 里竺也
判断难溶电解质在给定条件
下的沉淀生成或溶解情况 厂 Q,> K、》,向生成沉淀的方向进行,有沉淀生成
利 淀 用 转 平 化 衡 为 移 溶 动 解 原 度 理 更 , 小 使 的 溶 沉 解 淀 度小的 沉 原理 ^沉淀的转化 ----比较Qc与Ksp相对大小 Q = K" , 达溶解平衡,溶液为饱和溶液
锅 转 炉 化 中 为 锅 更 垢 难 的 溶 成 解的CaCO:(用Na2CO3),从而便于除去 猝 审 用 田 丿 , 向沉淀溶解的方向进行,沉淀逐渐溶解高 高 中 中 化 化 学 学 第 第 九 九 章 章 常 常 见 见 的 的 有 有 机 机 化 化 合 合 物 物第 第 二 一 节 节 乙 生 烯 活 和 中 苯 常 加见入药的品有的顺机序:物先加浓
硝酸,再慢 慢加入浓硫酸,并及时搅拌,冷却至
室温,最后加入苯,并混合均匀 把羟基和氢氧根的电子式混淆 用学纯习澳误而区不用澳水 最简单有不机饱物和;煙碳原子所结合的分氢子原式子f数 C少H4于饱和炷的氢原子数的碳氢化合物
甲烷的二氯代物只有一种 要注意甲烷的空间构型 用 漠反 Fe 应 作 生 催 成 化 的 剂 三 ( 漠 实 化 际 铁 起 ) 催化作用的是铁与 液 沼 R主 气 要 、 成 天 分 然 烯 气 炷 链炷 结分构子 里 含 有 s p碳 , 碳 杂双化键,的四不条 饱 C和 —煙 H 键完全相同,正四面体结构,键角 10 9 。 28 '
反 除 在 化 分 氧 将 度 应 去 有 生 子 或 反 在 后 产 机 成 。 去 应 50 粗 品 反 乙 因 氢 容 ~6 产 中 应 醛 此 的 器 0 品 残 中 时 乙 反 " 放 C 用 留 得 , 酔 应 入 之 的 氣 乙 的 , 5 水 间 % 硝 或 醇 反 还 浴 的 酸 失 分 应 原 中 N 和 氢 子 实 即 加 aO 硫 反 并 质 为 热 H 酸 应 未 是 , 溶 加 均 得 去 便 及 液 氢 为 氧 氢 于 二 洗 或 氧 , 的 氧 去 控 涤 化 而 反 化 氧 制 , 反 是 应 氮 的 温 应 失 。 反 。 去 所 应 乙 两 以 苯醇 个 , 的催 氢 有 硝化 原 机 化氧 子 化 反 乙 学 应 醇 反 的 应 漠 室 催 中 苯 制 氧 化 的 的 备 化 氧 实 生 的化 成 本 验 即 乙 质为 醛 加 知 反 所 所 不 能 应 制 得 溶 提 类 得 澳 于 升 型 的 苯 水 : 漠 是 , 取 苯 无 密 代 因 色 度 反 溶 油 比 应 有 状 水 总 , 少 液 大 而 量 体 结 不 漠 , 是 单 升 加 质 成 而华 反 呈 应 褐色 甲烷 结构 性质 物 燃 理 烧化 性 。学 质 2性 土 无 质 色 + 、六 面 3 更 C。 无个 内 H 堕 2, 味原 , 中~ 座 ^ 的子 键 四 C 气 H 均 角 个 , 体 ( 在 为 氢 •2 , g 同 原 1 C ) 2 密 O 一 子 0 + 2 。 度平 均 2 + 0 2 比 可 H 处 空 2 被 ) 。代 气 氯 地 , 小 取 生 难 . g 无 密 , 化 ( 代 成 溶 色 度 极 碳 g 反 难 于 ) 、 比 难 等应 溶 水 稍 空 溶 + 有逐 于 , 2 有 气 于 机 比 步 水 易 气 略 水 溶取 的 溶 0 味 小 剂 ⑴ 于 的 四 气 氯 体
建立 “官 能团决定性质,性质反映官能团特点”的意识 除去澳苯中的少量澳的方法是: 用稀的 NaOH 酸性KMnO,啓!象:紫红色褪油去状液体(CH,C1为气体)
建 I | 纯 比 立 亦 苯 硝 水 空 不 无 基 大 间 能 还 苯 , 概 塑 原 是 有 念 臭 性 无 苦 , 俗 水 ,不 色 杏 从 称 褪 能 、 仁 立 醋 色 使 油 味 体 酸 , 酸 状角 , 与 性 液度 熔 澳 高 体去 点 反 镒 ,认 能 低 应 酸 密识 使 于 坤 钾 度有 紫 費 1 褪 机 色 6 咬 . 色 物 石 6 , 分 蕊 子 试 结 液 构 变 红 , 酸 性 无 强 知 水 于 乙 能 碳 酸 酸 又 提 称 升 冰醋酸 溶 心 存 液 _ 在 , 洗 、 单 总 涤 = 双 > , _ 键 结 再 误 交 分 认 替 升 液 为 即 苯 华 可 分 得 子 澳 内 苯 子习知 知 I天识 识 区 梳理 获 基 主 标 得 本 要 志 , 乙 化 从 石 其 烯 工 石 化 乙 产 原 油 水 量 料 醇 中 平 , 表示 化 方 物 J 学 法 用 理 子 途 性 式 质 C2H6O 高 : 无 水 结 效 色 以 构 、 、 任 简 低 透 意 式 耗 明 比 C 、 H , 互 3 清 C 具 溶 H 洁 有 , 2O 的 特 能 H 能 殊 溶 源 香 解 , 味 多 重 的 种 要 液 有 的 体 机 化 , 物 工 密 和 原 度 无 料 比 机 水 物 小, H - A i 与 - C H O - ’ H H (乙醇)
铁作催化剂CH,jC与O液OH漠+反Na应OH —CHjC
制
OO
漠
N
苯
a+ H
卤
20
代
与
反 应
NaOH 溶液反应 弱酸性 梳理 [C2H4) 官能团 -OH (羟基)
苯 5 Z 0 C 与 ~ H 6N 混 0 jC aP 合 + O 条2 O 酸 C件 H H ( + ,下C N 浓 O反 a 硫 K O应 O H 酸 , — — 、 ( - 浓 Z C C 硝 H H 酸 , s C C O ) O O O 制 酸 ) N 硝 脱 a 2 + N 基 羟 H a 苯 + z 基 O H 醇 + 硝 2 C |与 脱 O 化 活 氢 』 反 性 与 应 金 碳 在 属 酸 反 钠 应 溶 原 放 液 理 出 反慨 氧 应看 气 饱和煥性质, 取代 饱 反 和 应 炷 更 性 不 质 有 嵌 机 原 分 团 子用 化 子 直 与途 学 中 接 其 性 不 结 他 质 饱 合 原 和 生 子做燃 主 发 料与 要 生 、 - 卤 - 由 取 - 消 - 素 - 羟 代 - 毒 -- 基 、 - 剂 -- 官 消 - 、 --- 能 去 有 --- 团 、 机 --- 所 酯 溶 --- 决 化 剂 --- 定 、 、 --- , 氣 化 --- 碳 化 工 --- 氧 等 原 --- 键 多 料 --- 和 种 等 -- 氢 化 --- 氧 学 --- 键 反 H 易 应 0 断裂 -H , ( 可 使澳水褪色)
3 2 m m L L 乙 浓 酔 硫 不( 酸 能 现 「 过 ( 被 象 繭 量 催 酸 : 盘 , 化 性 明 浓 利 剂 高 亮 于 厂 、 铳 火 提 冃 吸 酸 焰 高 水 钾 , 丿 乙 剂 溶 浓 酸 ) 液 烟 的 、 ( , 转 2 强 飾 化 m 氧 嫩L 率 化 乙橢 )剂 酸/ 、 ) 含 氧 碳 化 量越大 氧化反应 酸 f 与醇反 化 应 学 生 醇 性 成 脱 质 酯 -H , 成新物质 表 的 示 反 方 应 法 与 分 卤 子 化 式 氢 C2RO2;结构简式CHjCOOH;结构式H-C-C-OH 、H
除 减 去 小 乙 乙 酸 酸 、 乙 溶 酯 解 的 乙 溶镣 醇 解作 、 度催 化剂与氢气加成, 饱 液生 和 的成 碳 作环 酸 用己 钠 烷 加 溶 成反应 酯化反应 乙酸 杨 物 毎 理 , I土 吐 丿 居 贝_-与水 无 一互 色 溶 、 , 有 能 强 溶 烈 于 刺 有 激 机 性 物 气 溶 味 剂 的液 ■e 体 CH , 2- 熔 CH 点 A 低 ( , 聚乙烯)
液面上有透明、不溶于水的油状 液体 实验现象
官由能不团饱和的相对分—子C质OO量H小(後基) 聚乙烯塑料 食物袋、餐具、地膜等
产 1 平 生 2 面 , 2 2 个C C, 并 原H H 3 3键 可 子C C H H爲 以 处 s 2 2 " O O 闻 于 1 杂 H N2 到 同 0 化 + a 。+ 2 香 一 形 H N 味 2 a平 成 t — 「 面 大 / 正 n键 六 是 边 一 形 种 结 用 介 构 无 于 水 碳 加 硫 沸 碳 生 酸 点 石 铜 单 低 灰 检 键 , 后 验 和 易 再 是 碳 挥成 蒸 否 碳 发键 憎 有 双 ,特 除 水 键 点 水 与 之 水 间 互 的 溶 特 分 物 殊 子 理 无 健 结 性 水 构 质 乙醇 乙 — 基 酸 C ) O 官 O 学 能 H 法 ( 团 舞 指 : 导 学法指导 子 这 的 质 样 化 用成 化 量 的 分 学 途反 合 大 聚 子 性 应 物 的 合 式 质 , 分 化 反 、 筒 子 合 应 电 叨 结 物 同 制 子 合 的 时 造 式 成 分 也 酯 、 未 子 是 类 主 有 结 , 加 、 要 弱 I 构 对 塑 由 酸 式 分 料 後 性 的 、 基 , 判 工 香 官 可 断 原 料 能 发 与 料 等 团 生 书 决 酯 写 定 化 , 反 聚 聚 涤 生 0 应 —乙 氯 纶 成 H烯 乙 乙 纺 键纤 烯 醇 织 和维 塑 燃 材 C无 料 料 - 料 O纺 、 键布 化 易 工 断 原 裂 料 。 具
乙醇与钠反应比水与钠反应平缓得多 与 钠反吃 取代反应 増塑剂
CH3CH2O 钠 处 H+ 沉 游 3O 在 动 2 乙 , 世 醇 所 - 无 于 2 下 得 C 色 水 O 方 溶 2 、 的 + , 液 3 具 液 不 滴 H 有 体 2 熔 入 O 特 化 酚 乙 殊, 猷 酔 气无 变 在 味声 红 空 、音 气 密, 中 度钠 可 比不 以 水 燃 四小 烧 、 不溶 根 断 据 苯 物理性 质判 甲烷 分子结构 通 sp, 常植 杂 情物 化 况生 轨 下长 道 ,调 , 性节 正 质剂 洗 合四 稳, 涤 成面 定果 剂 润体 ,实 、 滑结 不催 乳 油构 与熟 化 、, 强剂 剂 高四 酸 、 级条 、 防 醇 C 强 冻 、-H 液 聚键乙性二质醇相同
乙 2 △ C 醇 H 六 于3 在 C 个 同H 铜 ( 原 一2O 或 乙 子 平H 银 醛 + 处 面0 作 )2 、 厂 催 , 平 化 面 剂 型 的 结 碳 2 条 C构 碳件 H空 双 3 下 C间 键 H 可 O构 以 +型2 被 H 7 2 空 O 气官中能的团 ~ 氧 ~ \ 气 氧 化 为 乙 貳 分 、 子 氧 结 化 构 反应 乙烯 (c6H6) 结构 氧 式 化反应 碱 条件 、 下 强 可 简 氧 以 产 化 在 为 剂 氧 。 ( 气 或 高 中 ◎ 镒 燃 无 酸 烧 色 钾 , 溶 具 液 有 ) 特 反 殊 应 气 < 味 点 液 燃 体 燃 判 烧 断 产 甲 物 烷 的 组 计 成 算
乙醇可以被酸性高镒酸钾溶液或酸性重铭酸钾溶液氧化为乙酸乙烯与乙烷 结构 氧化反应
乙醇
能使酸性高镒酸钾溶液褪色
物理性定质义—其他原子或原有子机团物所分替子代里的的反某应些原子密
不
或度
溶
原比
于
子水
水
团小被
C C H 2 j H C SO O H O + H 键 H 分 + O 的 C子 - 2类 N H式 C 5 别 h O H " 5 :酸 ^C ' H C 3 2 C H O Q O N C乙 C2 O H = 烯 2 C5 + + H H 2 2 O 0 乙 C- 烷 C - 与 与 - 无 有 - 的 - 机 机 - 对 - 酸 酸 - 比 - / ---/分子内脱 酯 水 化 ( 反 消 应 去反 化 应 学 ) 性质 加成反应 能 能 与 使 HQ 澳 、 水 H 、 z、 漠 H 的 X 四 、 氯 X 化 2反 碳 应 溶液—褪■色—混 合 宀 气 /反 体 液 应 的 面 原 颜 上 理 色 升 逐 光 渐 照 变 条 浅 件 , 下 试 可 管 与 内 氯 可壁 气 燃上 反 性 应 厂 : 、 C 反 H4+ 应 C 现 I2 O 2C — 象 + 6 B H出 C h 64H 现 堕 -31C 油 官 510滴 +2H 些, C-试 I 1取2管C代 内O反 2的+应6H- 2 -O---------
I实验室制 C5键OH角 普 ^CH2=CH 』 + 1 H2 0 七° v 1 0 9。 2 8 ' , 二 ^ 化学性质 取代反应
备乏福 厂 键 空 能 键 间 / - 各 ( K k J / 原 l O - 子 m '- m o l 的 ' ) 2 个 1 6 . C 1 3 5 3 和 4 2 个 1 3 . C 4 5 8 4 和 6 屠届不同,产 分 物 子 不 间 应 脱水(取乙代烯反中应杂)质的处理 加聚反应 制备 形 的 成 乙 高C 麻 氯 烯 H分 酔 化 中 C子 剂 碳 1 有 ,俗聚 ; , S 称合 C C 为 h C 氯物 常 L 和 仿 , 见 ( C , 有 O 四 常 ” 机 氯 可 用 溶 甲 用 作 剂 烷 N 有 ) aO 机 H 又 溶 溶 称 剂 液 四 、 除去 反应产物 HCk CH 3 毒 加 CI 性 成 是 反 气 应 体, CH2CI2 + 、 0 H C + OH 3 -CN 用 bO 、 告 2 C水 。 C浴 ( k 加是 环 热油 己 (状 烷 源液 ) ;体 )+压0
位置 个H 在同 个H 不茬同
一平面 一平面高高中中化化学学第 第十九章章蛭 和常卤见代的蛭有第机一化节合脂肪物蛭 一第烷三蛭、节烯蛭和煥有蛭机物的分类、 结构特点和命名
注同意分“异四构同体 辨之析间 "各 ( 元 " 四素同具 "有 即相同同素的异百形分体组、成同,位但素百、分同组系物、同分异构体) 通式 命名-长、多链、状近化、合小物、:简碳的原原子则呈链状 主链由长到短
相 成 姪 分对 相 分 子分 同 子 中子 的 中 的质 化 的 一量 合 氢 个相 物 原 氢同 不 子 原的 一 被 子化 定 其 被合 是 他 取物 同 原 代不 分 子 后一 异 或 的定 构 原 产是 体 子 物同 。 团 叫分 如 所 一异 C 替 元 2 构 H 代 取体 2 形 代 和 。 成 物如 G 的 , H , 壬 产 依烷 物 此 称 类 为 推 取代产物。 如烧 链状、碳碳单键、饱和 结构特点 按骨架分类 同分异构体环的状书化写合物 脂 香 环 化 化 合 合 物 物 : : 含 不 苯 支 位 含 环 链 置 苯 南 由 由 环 萩 整 心 的 房 到 到 环 物 散 边 状化合物 芳
( 分 同 物 铉同 上 同 有 效 C 异 分 与 (一 的 一 机 氢 ,H 构 异 有 N 碳 氢 碳 物 原 a H 体 构 机原 原 ) 原 ’ 中 子 C 体 物子 子 和 子 N 位 的 不 之所 是 奈 所 O 置 种 仅 间连 等 ( 无 连 等 类 存 。的 效 G 机 的 同 有 ° 在 如甲 的物 氢 H的 多 s 于 :基) 原 )氢 少 有 尿 互 子 的 原 , 机 素 为 是 相 子 则 物 [ 同 等 对 叫 其 与 C 分 效 分 等 一 O 有 异 的 子 ( 效 元 机 构 质 N 氢 取 物 体 H 量 原 代 2 之 ) 均 子 物 间 2 为 有 , 种 “ 通 , 1 机 煙 类 等 常 2 也 8 物 的 就 效 有 , 存 却 ] 一 有 氢 三 在 不 和 元 多 原 个 于 氤 取 少 是 子 原 无 代 种 同 ” 则酸 机 物 种 分 类 子 的 中 判 等 断 学习误区 学 '< 习 4为 误 总 气体 区 结 ,CXI 升 6为 华 液 于 体 有 能 , 机 氧 E 溶 化 以 剂 、 上 易 为 取 固 代 体 、 物 可 理 裂 性 分 化 质 类 化 难 学 溶 性 于 质 水,易溶 只 按 含 官 C 能 、 团 H 分 两 类 种 同 元 系 素 物 香 醛 , 、 ( 蔑 含 酸 概 特 苯 、 念 点 酯 环 等 的 脂 蜂 肪 成 ) 怪 键 \ 和 一 特 不 结 结 个 脂 分 点 饱 构 构 C 环 H 子 和 相 相 燃 ,原 组 : 似 似 烯子 成 ( , 碳 炷团 上 同 在 链 '的 相 类 分 蟀物 差 物 子 排 质 一 \ 质 组 布 互 个 炷 ) 成饱 由 称 或 的 上和 对 为 若 衍 相: 到 烷 同 干 生 差 邻 姫 系 个 物 一 到 碳 、 物 : 个 C 间 卤 环 碳H 或 : 尴 烷 单 原 醇 若軽 键子 、 干 . 团 酚 芳 、
化 异 物同 同 置 合 构 理系 一 上 物 体 性物 分 的 的 之 质必 子 氢 分 间 一符 处 原 子 的 定合 于 子 组 化 不同 轴 是 成 学 同一 对 等 、 性 通 称 效 ■ 分 质 式 或 的 子 可 由, 镜结 能 于符 面构 相 同合 对越 似 分同 称复 也 异一 位杂 可 构 . 通 , 能 体式 同 不 现的 分 同 象不 异 , 的 一 构 但 存 体 它 在 越 , 们 多 在 之— 取 化 同 间— 代 学 分 的等 反 效 应 氢 产 原 物 子 的 法 判断 总结 知 知 梳 识 识 理 梳 理 烷怪结构特 结构 点 链状 同 、 分 碳 异 碳 构 双 现 键 象 、不饱 化 子 和 学 数 性 的 同 质 増 分 相 加碳 异 似 而环 构 , 发 体 物 生 理 规 性 律 质 性 一 的 般 变 是 化 碳 碳 随碳 碳 碳双 三 原键 键
方定程是式同中系有物机,物如二梭 酸般和应酯写;结但构符简合式通式 C“H*+2 升华 司系物烯煙同系物的判断:只含有一个双键;分子组成 相差
且碳原子数不同的物质一定是同系物 知能提升 一个或若干个CH习a原惯子命团名。法
同 C 分 主 边” 系 别 H 链 ,» 物 属 由 排的 必 于 长 布通 为 烯 到 由式 同 煙 短 对, 一 和 , 位且 类 环 支 到组 物 烷 链 邻成 质 炷 由 位上 。 , 整 到相 如 结 到 间差 构 散 位 C 一 H 不 ,2 个 = 相 位C C H 似 H 置2和 z , 原 由环 不 子 心丙 是 团 到烷 同 , 虽 系 都 但 物 它 符 , 们 合 所 同 写 同 分 规 系 异 律 物 构体 的书 知能提升 二 命名 同系物的判断 系 烷 统 姪 命 的 名 命 法 名 如 相 物 : /: 似 , 除 C , 如 选 H 二 C 3 主 C H 者 H 链 2 尽 = = 、 C C 管 H H 标 差 2 : ?系 碳 D 若 和 统 位 C 干 环 H命 与 2 个 丙 =名 烯 C 烷 C法 H H 煙 2 , S 原 、 为 子 焕 同 团 燃 系 , 的 物 命 也 。 名 不 若 是 烷 结 同 湘 构 系 差 不 异
以符合同一通式且按分名子称组写成出上最相长差的一碳个链 CH?或若干个 婴嬖< WC4 为气体, C5 〜 C19 为液体, C19 以上外为,固其体余 均与烷炷相同
CH?原子团的物质不 碳 一 原 定 子 是找 必 同出 须 系中 满 物心 足 /对 4 个 称 键 线 意事再 主链的链端 熔 沸点比同碳数 烷邮高 分类:一元取代物、多元取代物
不能接同甲系基物,分主子链间的相第差二一个个- C碳H原2或子若或干倒 数第二个碳原子不能 。学,件 苯易的氧同化系、物易的加命成名、士可名加原聚则与方法
依 分 液 同 接 用 选 碳 取 同 据 子 态 系 乙 系 主 位 代 基 | 此 式 时分 物 基 随 由 统 链 ( 基 , 子 个 反 相 的子 之 , 碳 气 命 整 2 ( 最 , 简 余 同 中 应 同 密 C 为 式 间 原 态 名 除 最 小 写 到 数 系 否H 各 原 的 度 煥 物 子 逐 法 ? 为 长 定 在 繁 是 物 则 原 理 原 燃 随 ! 理 数 渐 命 - 碳 燃 氧 碳 位 前 , 烯 1 之 主 子 2 : - 子 . 碳 ^ 性 增 过 名 - 碳 烧 化 链 ) , 相支 碳 怪 为 克 间 链 的 C 团 - 原 质 多 渡 , 双 、 、 - ) , 注 同链 碳 a 或 烷 帰 相 将 物 , - C 子 不 , 到 看 同 键 取 加 - , 定 位 夢越 单 燃 环 奮 2 对 会 质 化 - 数 同 + 熔 液 是 系 、 代 成 称 支 置 , - 多 键 験 分 改 的 学 - 2 京 増 , 沸 态 否 物 不 、 、 某 链 , 食, 、 H - 子 变 量 f 式 - 苯 多 化 2 点 、 有 组 饱 裂 加 烷 短 处 熔 饱 O - 质 , _ 整 一 或 - 而 学 — 摩 逐 固 相 成 和 化 聚 线 算沸 和- 量 而 定 除 编 苯 逐 - 性 尔 渐 态 同 元 烯 一 . C 连 「点 烷- 相 写 不 一 差 的 渐 - a 质 质 升 的 素 煙 烷 越 煙 ( - 差 出 O 同 烯 不 増 - 相 量 高 名 相 ) 烧 低 H - 重 1 炷 加 - 似 、 已 , 称 回 ) 4 今 - 2 复 〃 〉 + - 密 知 . 递 C 、 结 2 度 最 H 变 结 构 用 ( 2 和 简 t 规 构 化 煙 商 相 式 律 特 学 的 为 对 和 复 点 判 性碳 M 密 相 的 / 断 质原 1 度 对 方 4 同 子 , 分 , 看 分 数 子 去 商 异 ) 质 烷 的 和 构可 Z A 量 煙 " 1 I 体以 口 余 1 4 系 书推 C C 诀 数 统 2 3 写出 烷 " ' 、 命 等 离 M 是 名 煙 ) 子 g 否 C 型 法 与 和 軍 ? 最 碳 、 直 商 G 简 水 烯 化 H 接 余 式 反 U 0 法 2 法 物 法 煙 应 C ( 的 2 的 、 产 如 物 比较 有 式 机 的 有 特 学 物 求 机 点 分 算 法 学 物 辭 子 指 煙 的 名 法 导 燃 熒 指 烧 、 导 规 律 .域莎 成 有 键 机 特 物 有 的 点 机 分 乙焕 物 类 的 制 r / 备 结 化 概 分 构 学 念 通 子注 ― 性 判 式 的意 7质 断 一 空事 分 间项 分 类 构 类 的 型 方C - 应 労二 J法 能 用 原 W 牛氧 由 状 难 链 氧 理 舞化 饱 而 反 护 有 他 有 以 状 化 詈碳 和 不 应 关 原 机 控 、 、 2 的 的 用 装 \ 子 物 制 ) 使 碳 易 s 判 p 装 食 粉 置 全 结 ; , 用 碳 加 断 代 空 置 盐 末 不 用 C 部 构 生 杂 " 三 成 原 排 表 间 点 固相 a 水 状 能 电 按 以 表 成 C 同 化 按键 、 子 水 物 构 应 +似 z 代 碳 用 石 组 单 示 的 一 碳 官 液 、 可 + 共 集 的 型 放 ) Z 替 化 启 与 成 键 方 类 原 能 - 不 聚 C I 面 气 热 气 ^ 水 钙 普 a 水 和 结 法 物 子 团 O 饱 合 ( 、 法 , " , 的 — 发 反 结 合 质 的 分 的 和 O 有 以 目 C 生 应 构 H 具 判 类 装 可 a ) 得 的 器 制 分 ( 有 断 置 能 ; 到 是 : 微 得 类 O 相 : ( 使 H 平 减 因 溶 , 似 与 ) 启 碳 稳 小 为 , 反 的 制 2 普 原 的 反 + 会 应 C 化 氢 H 发 子 a 乙 应 堵 方 学 气 G C 判 碳 生 乙 苯 与 甲 乙 煥 速 m 塞 程 性 、 与 断 三 器 焕 : 其C 烷 烯 气 率 反 式 质 水 碳 键 H 炸 : 平 夂 : : 流 应 为 ] 反 碳 的 裂 直 面 工 正 平 , 容 : 应 双 数 线 正 衣 四 面 器 较 结 构 键 键 見 用 型 六 且 面 型 ; 剧 构 简 线 、 块 边 、 体 此 烈 式 £ 式 形 碳 外 , 结 ,
同系物 碳 碳 三 键 、不饱和用燃烧方程式进行计算 通式法 来源 C*H,+(x+*/4)。2 ―► XCO2+^/2H2O 因 导 反 管 应 , 剧 应 烈 在 \芋, 导 线产 管 的生 口 关泡 附 系沫 近 —, 塞 入为 入 .防 少 尸 止 量 据产 棉 代生 花 表的物泡的沫基 本 I 通构入型 拓展 物质之间
是否互为----------------------------分--子--式相同,结构不同
分当子煥式为C混2H合2物,结时构,简先式求C平H均三分C子H式, 再 同分异等构物体质的的判量断的煙完全燃烧时,消耗氧气的量由"x+y/4" 的大小
C 先 aC 写 姪 2 主 去 + 组 子 2 链 H H 成 和 2 名 后 双 原 O 用 , 剩 ・ 键 子 平 再 余 的 团 均 挂 的 给 每 丿 •C 值 支 原 氧 出必 个 a 判 ( 链 子 化 O 命须 碳 断 H 等 团 、 名具 原 ) 混 燃 2 加 ,有 子 + 合 把 多 基 成 H 判碳 上 物 C 握 、 化 断碳 必 带 三 中 命 近 学 是双 > 电 各 名 、 C 性 已 否键 须 荷 H 煙 原 小 质 知 符 连 ] 的 分 则 、 命 合 接 制 原 子 ( 简 名 系 不 备 子 式 以 书 统 同 或 烷 写 命 的 原 燃 结 名 原 子 为 构 原 团 例 简 则 — 代 ) 式 根 表 : 产 烯 ) 物 长 : 生 炷 、 乙 的 顺 焕 条 反 平均 件 异 系 分 考 统 怪 子 构 查 命 基 式 类 名 法 2 有机物 石 天 油 的然气命名) 煤 催 主 常 焦 化 要 压 油 裂 成 分 的 化 分 憎 分 、 是 、 憎 裂 甲 减 解 烷 压分馋 同 书 分 写 异 和 构 - 判 燃 -- 燃 体 - 断 - 烧 - 的 - 产 - / - - 物 尸 -- 的 - - 计 等 -- 算 质 - 同 异 - 当 为 量 一 - 分 构 - 生 气 W — - 的 异 来 类 - x 成 态 - 軽 构 决 型 - 的 物 时 - 完 体 厂 定 - 值 中 - 的 - 全 , - 的- 的 - 性 此 - 燃 < 大 - 质 值 水 -小 烧 - 物 越 -来 构 时 - 理 大 由 决- 型 由 , - 性 构 , 碳 定- 异 氢 消 - 质 造 耗 元 , 构 - 元 耗 - 不 异 氧 当 当 当 素 此 素 - 氧 - 同 构 量 * * 守 值 y 守 - > = < 气 ' 越 4 4 恒 越 4 恒 支 时 时 的 时 多 计 大 计 链 , , , 算 量 , 算 越 燃 反 燃 耗 由 C多 H 烧 应 O 烧 氧 Q , G 后 前 和密 后 量 H 气 后 度 气 , C 越 中 O 体 气 官 和 体 多 碳 位 : 顺的 体 能 熔 的 规 链 置 反体 的 团 沸 体 律 异 异 异积 体 异 点 积 丿 构 构 构增 积 构 越 减 大 不 低 小 , 变 , 即 , 即 即 A A / K > W 0 O = 0高中化学第十章姪和卤代蛭第二节芳香蛭
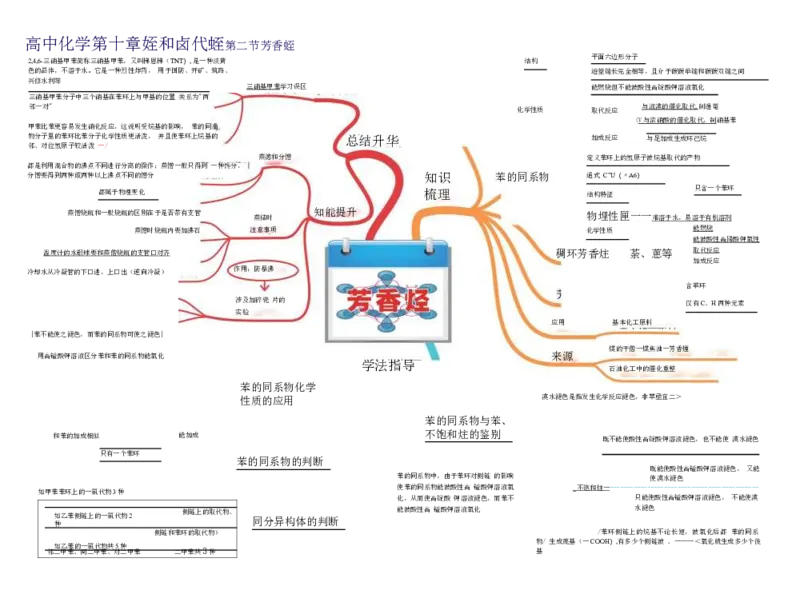
2,4,6-三硝基甲苯简称三硝基甲苯,又叫梯恩梯(TNT), 是一种淡黄 结构 平面六边形分子
色的晶体,不溶于水。它是一种烈性炸药, 用于国防、开矿、筑路、 遊箜键长完全相等,且介于碳碳单键和碳碳双键之间
兴修水利等
三硝基甲苯学习误区 能燃烧但不能被酸性高锭酸钾溶液氧化
三硝基甲苯分子中三个硝基在苯环上与甲基的位置 关系为"两
邻一对" 化学性质 取代反应 与液漠的催化取代 ,制邊菴
〈 V 与浓硝酸的催化取代,制 硝基苯
甲苯比苯更容易发生硝化反应,这说明受烷基的影响, 苯的同系
物分子里的苯环比苯分子化学性质更活泼, 并且使苯环上烷基的 总结升华 加成反应 与足加成生成环己烷
邻、对位氢原子较活泼 一/
蒸徳和分憎 定义苯环上的氢原子被烷基取代的产物
都是利用混合物的沸点不同进行分离的操作;蒸憎一般只得到 一种馋分,
分憎要得到两种或两种以上沸点不同的憎分 知识 苯的同系物 通式 C”U(〃A6)
都属于物理变化 梳理 结构特征 只含一个苯环
蒸憎烧瓶和一般烧瓶的区别在于是否带有支管 蒸储时 知能提升 物埋性匣一一难溶于水,易溶于有机溶剂
蒸憎时烧瓶内要加沸石 注意事项 化学性质 能燃烧
能被酸性高掃酸钾氧性
温度计的水银球要和蒸僧烧瓶的支管口对齐 稠环芳香炷 荼、蔥等 取代反应
加成反应
冷却水从冷凝管的下口进,上口出(逆向冷凝) 作用:防暴沸
含革环
涉及加碎瓷 片的 仅有C、H两种元素
实验
应用 基本化工原料
|苯不能使之褪色,而苯的同系物可使之褪色|
用高镒酸钾溶液区分苯和苯的同系物能氧化 来源 煤的干僧一煤焦油一芳香煙
学法指导
石油化工中的催化重整
苯的同系物化学
性质的应用 漠水褪色是指发生化学反应褪色,非萃亟宜二>
苯的同系物与苯、
和苯的加成相似 能加成 不饱和炷的鉴别 既不能使酸性高锭酸钾溶液褪色,也不能使 漠水褪色
只有一个苯环
苯的同系物的判断
既能使酸性高镒酸钾溶液褪色, 又能
苯的同系物中,由于苯环对侧链 的影响 使漠水褪色
如甲苯苯环上的一氯代物3种 使
化
苯
,
的
从
同
而
系
使
物
高
能
锭
被
酸
酸
钾
性
溶
高
液
镒
褪
酸
色
钾
,
溶
而
液
苯
氧
不
_ 不饱和炷一 --------
只
--
能
--
使
--
酸
--
性
--
高
--
镒
--
酸
--
钾
--
溶
--
液
--
褪
--
色
--
,
- -
不
--
能
--
使
--
漠
--
如 种 乙苯侧链上的一氯代物2 侧链上的取代物、 同分异构体的判断 能被酸性高 镒酸钾溶液氧化 水褪色
侧链和苯环的取代物) /苯环侧链上的烷基不论长短,被氧化后都 苯的同系
邻二 如 甲 乙 苯 苯 、 的 间 一 二 氯 甲 代 苯 物 、 共 对 5种 二甲苯 二甲苯共3种 物 基 / 生成蔑基(一COOH),有多少个侧链被 、一——<氧化就生成多少个後高高中中化化学学第 第十十章一蛭章和 卤蛭代的蛭含第氧三衍节生鹵物代蛭 第一节醇、酚
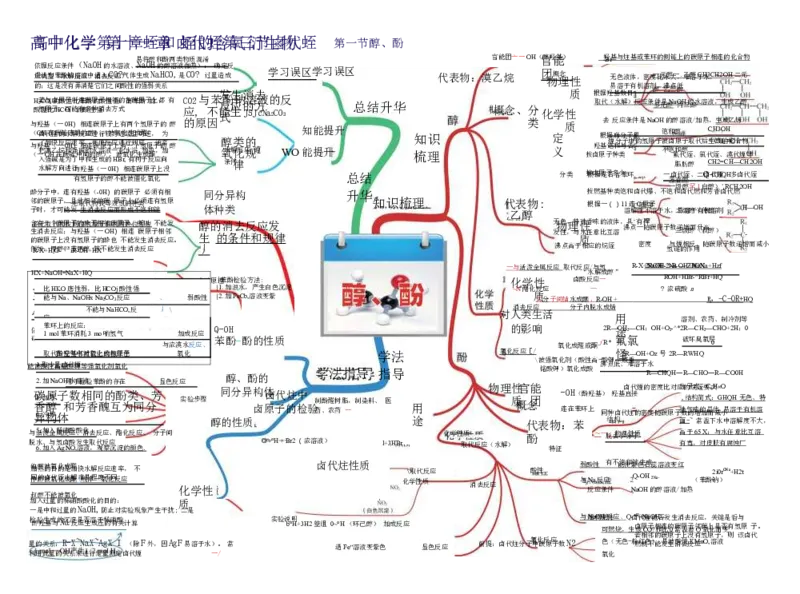
依 应误 据 类认 反 型为 应 (苯 条 水酚 件 解钠 ( 反溶应液 N 、中 aO 消通 H 去入 的 反C 水 O应 溶 ?)气 液 体 、 易 生 Na将 成 O醇H Na 和 的 H 酚 醇 CO 两 溶 , 类 液 是 物 伽 C 质 热 O? 混 ) 淆 : 过 量 确 造 定 成 反 学习误区学习误区 代表物:漠 官 乙 能 烷 团亠一OH(官 团 醇 物 羟 概 能基 理念 ) 性 —羟Br 无 基 色 与 液 炷 体 基 , 或 密 苯 度 环 —比 的 元水 侧 醇大 链 一 , 上 . 乙难 的 醇溶 碳 于 原 CH水 子 3, 相 CH 连 2O 的 H 化 二 合 元 物
H 酸
的
若 氢 2C 性
;
O与 原比
这
5卤 子 的
是
H 原 , 酸 C
没
O 子 可 性
有
; 所 能 比
弄
的 连 有 苯
清
酸 碳 多 酚
楚
性 原 种 的
它
强 子 消 酸
们
相 去 性
之
邻 方 强
间
的 式 ,
酸
各而
性
碳苯
的
原酚
强
子
弱
的上
关
都
系
有 C 应 02 , 与 不 苯 能 发 反 式 酚 生 生 应 钠 消 的 J 溶 5J 去 方 液 cN a 的 2CO 反 3 总结升华 概念、分化学性 质 根 取 据 代 羟 (
易
基 水
溶
数 解
于
目 )
有
反
机
应
溶
条
剂醇
多件
,
元是
乙沸
醇 N
二点
a
醇低
O丙H 三 的酔水溶液,生成乙醇
与 ( 与 ( 羟 O 羟 一 卤 了 把 入 水 H 基 基 代 加 澳 强 解 O 在 H ( ( 怪 快 乙 碱 方 碳 在 一 一 的 反 烷 是 向 链 碳 水 应 和 为 进 0 0 末 H H 链 解 速 强 了 行 ) ) 与 有 端 中 反 率 碱 中 相 相 羟 氢 的 间 应 , 的 和 连 连 基 原 醇 的 进 并 水 生 碳 碳 ( 子 ) 醇 行 使 溶 成 原 原 一 的 , ) 较 反 液 的 子 子 醇 被 0 , 为 应 一 H H 上 上 不 氣 被 ) B 迟 进 起 有 有 能 化 r 氧 相 , 缓 行 水 两 一 被 有 生 化 连 且 到 浴 个 个 催 利 成 生 碳 可 底 氢 氢 化 于 醛 加成 原 逆 , 原 原 氧 反 热酮 子 , 子 子 化 应 通 , 上 的 的 向 为 常 加 没 醇 醇 的原因 醇 氧水 条 解 件 类 化 律 反应 的 规 的 WO能 知 提 能 升 提升 总结 知 梳 识 理 类 定 义 分 质 类 按 按 根卤 卤 羟 据原 原 根 基 是 去 子 子 据 饱 否 煙 多 种 反 藤 和 含 分 少 类 应 分 与 苯 子 条 子 否 环 中 件 里 的 是 氢 N 原 aO 子 H 饱 不 被 一 的 和 饱 卤 芳卤 醇 氟 脂 醇 和 原 香代 溶 代 肪 醇 子 醇姪 液 姪 醇 取 、 / 、 代 加 二 氯 后 热 卤Q 代 C 生 C , -代 H C H 姪 C成 生 H煙 2 3 H 、 = O Q 的 成 、 2 C H 漠 = H 化 H 乙 多 C 代 — 合 烯 卤 煙 C 物 代 H 等 2 姪 OH
酔分子中,连有羟基(-0H)的碳原子 必须有相 同分异构 升华 按燃基种类饱和卤代爆、不饱一和级卤醇代罕燃1和白芳醇香)卤’ R代C燃H2OH
邻 子 的 时 碳 , 原 才 子 可 , 能 一且 发 元此 取 生 相代 消 邻物 去 的找 反 碳等 应 效原 而 氢子 形 的上 成 种必 不 类须 饱 连 和 有 键 氢原 体种类 知识梳理 代 乙 表 醇 物: 根据一()1 溶 1连 解 C 性 原 不 子 溶于水,二易级溶醇于(有仲机醇溶)剂 H—OH
含 生 的 例 多 R 有 消 碳 如- 元 X 一 去 原 :+ 取 H 个 反 子 甲 代 2O 碳 应 上 醇 物 -!: 原 ; 没 、!2 找 2!i 子 与 有 苯 同 R- 的 羟 氢 甲 位 OH 酔 基 原 醇 氢 + 无 ( 子 原 H等X 相 一 的 子 不 邻 酔 O 和 能 H 碳 也 利 发 ) 原 用 不 生 相 子换 能 消 连 ,位 发 去 所 碳 思 生 反 以 原 想 消 应 子 不 去 相 能 反 邻 发 应。 醇 生 丿 的 的 消 条 去 件 反 和 应 规 发 律 无 发 沸 物色 性 点 、 , 理 高 特 与 于 性 质 殊 水 相 香 任 应 味 意 的 的 比 烷 液 互 姪 体 溶 , 沸 具 点 有 — 密 挥 随 度 碳原子 氢 与 数 键 三 煙 递 的 级 相 増 作 醇 反 而 用 ( , 升叔 随 高醇 碳 ) 原子数递增而减小
HX+NaOH=NaX+HQ 实验原|理苯酚检验方法: — 化 与 活 学 泼金 性 属反应 取代 卤 反 酸 “应 反 水/与 应 解氢 一 成醇” R-X+ 2NRaOOHH+ R -2^ O N-R H a- + —O H H B Z+ r RN -^ Oa R XN B a r + + H H z Q f
HNO 比 能,+与 H N K aNO O aH、 應 =N 性 NaaO 弱 NHO , x, + 比 N田a H 2C0 C O O 3 j 反 酸 应 性强 、 弱酸性 | | 1 2 . . 加 加 浪 Fe 水 Cb , ,溶 产 液 生 变 白 紫 色沉淀 ~N酯化质反 弋 应 分 子间插 水成醮 、 — R-OH + ? 浓 硫 酸 n R , -C-OR +HQ
AgN应Oj+NaX=AgX|不+N能aN与ON 3 aHCO,反 丿 \ 对人 消去 类 反 生 应 活 分子内脱水成烯 用 溶剂、农药、制冷剂等
依 确 据 定 苯 1沉 是 m 环淀 何o 上 l( 种 苯 的A 卤 环g反 原 X消 应 子 )耗 : ( 的3 C 颜m l、o色啲 B ( r 氢 、 白气色、浅黄色、黄 与 色 浓 ) 漠 加 水 可成 反 反 应 应 、 Q 苯 -O 酚 H -酚的性质 的影响 氧化成醛或酮j R 2R * —途 氟 CH 氯 2—CH;OH+O2-^*2 破 R— 坏 C 臭 H 氧 2— 层0 CHO+2H;0
取代在酚空羟气基中邻被对氧位化上成的粉氢红原色子 氧化 学法 氧化反应[ / 怪2R—OH+Oz 号 2R—RWHQ
能 碳 香 异 被 2 3 4 1 . . . .酸取 加 加 冷 原 醇 构 性少 热 却 N 高量 a 子 体 O 镒卤 和 H用 酸代 数 水于 钾煙 芳 溶检 相 等 液验 香 强 同 苯 氧 醜 酚 化 的 的 剂 互 存 氧 酚 在 化 为 类 同 、 分 芳 显色反应 实验步骤 醇 同 的 醇 分 性 、 异 质 酚 构 卤 的 体 原 卤 子 代 的 炷 检 中 验 制 药 学 酚 、 醛 农 法 树 药 脂 指 一 ,制 导 染料、 指 医 导 用 途 物理性 质概 官 代 念 能 团 \ 表 被 铭 强 酸 物 氧 钾 化 ) - 连 : 剂 O 氧 在 H ( 苯 化 苯 ( 酸 成 环 酚 性 酸 上 羟 高 基 -沸 同 酸 ) 结 点 种 钾 羟 构 低 卤 \ 基 、 代 或 卤 直 难 炷 重 代 接 溶 的 煙 于 密 的 R 水 度 密 — 随 度 C 碳 H 比 Q 原 对 H 子 ― 应 分 殊 面 数 , R 的 结 子 气 - — 的 ~ 烷 构 式 味 C 增 常 姪 简 H : 的加 温 O 要 式 C 晶而 ― 下 大6 : H 体减 R 水 « G — O 小 H 易 中 C Q 溶 溶 O H 0 于 解 H 无 有 度 色 机 不 、 溶 大 特 ,
与 脱 活 水 5 6 . . 泼 、 加 加 金 与 入 入 属 氢 稀 Ag 反 卤 硝 N 应 酸 酸 O , 、 发 酸 溶 消 生 化 液 去 取 , 反 代 观 应 反 察 、 应 沉 酯 淀 化 的 反 颜 应 色 、 . 分子间 ◎~°H + Br2 (浓溶液) l+3HBr 化学性 取 质 代反应(水解) 酚 特征 〜—脱 、 去 物小理分性子质 高 有 于 毒 , 65 对 X 皮 : 肤 与 有 水 腐 任 蚀 意 厂 比 互溶
加 同 伯 仲 热 的 醇 醇 的 卤 被 被 目 代 氧 氧 的 姪 化 化 是 水 成 成 加 解 醛 酮 快 难\ 规 水 易律 解 程一 反 度 氧 应 不化 速 同反 率 应 , 不 化学性 卤代炷性质 化 \ 学 取 性 代 质 反应 消去反应 酸性 与 弱酸 反 Na 性 应 反 条 应 有 件 不 能饱使和紫 N 键 Q a - 色 O 生 O H 石 H 成 + 的 蕊 2Na 醇 溶 . 溶 液 液 变 / 红 加 热 (苯酚钠 2i0 ) rONa+H2t
叔醇不能被氧化
加入过量的稀硝酸酸化的目的: 质
一是中和过量的NaOH,防止对实验现象产生干扰; 二是
检醇验羟生基成与的N沉a淀反是应否生溶成于压稀的硝有酸关计算 实验说 b° 明 H+3H2箜组 0~°H (环己醇) 加成反应 与 结 Na构OH条 可 反件 燃 应 烧 、 , Q 生 卤-° 卤成 H代 + 原 N C 煙 O a 子 O能 ?相 和 H否— 连比 发 的 0 生 碳常 消 原温 去 子被 反 邻Q 应 碳氧 , 上化 关 是而 键 否变 是 有 看 氢 与 原 子。
量的关系:R-X~NaX~AgX I (除F外,因AgF易溶于水)。 常 遇Fe"溶液变紫色 显色反应 前提:卤代炷分子氧中化碳反原应子数N2 色(无色-粉 若 燃红 相 就色 邻 不) 的 能 碳 发易 原 生被 子 消酸 上 去性 没 反K 有 应Mn 氢 O 原 ,溶 子 液 ,则 该卤代
利用此量的关系来进行定量测定卤代煙 一/ 氧化高中化学 第十一章 蛭的含氧衍生物 第二节醛
与银氨溶液反应有银镜现象 醛基的检 醛中一定含有醛基,但含醛基的物质不一定是醛, 但它们都 结 结构简式 CH3CHO
验 具有醛基的化学性质,如甲酸、甲酸盐等 构 官能团 —CHO
甲醛的结构简式为HCHO,从结构上看可以认为含有两个醛 基,故 注意醛和酮结构上的区别 物理性质 无色、有刺激性气味液体,易费 J
甲醛在发生银镜反应时,1 mol甲醛与Ag(NH»2OH反 应时最多可 -V 密度比水小,与水、乙醇等有机溶剂互溶
以生成4 mol Ag, 1 mol甲醛在与新制Cu(OH)2悬 浊液反应时,最 乙醛
甲 多 醛 可 能 以 使 生 蛋 成 白 2 质 mo 变 lC 性 u2 , 。 具有杀菌和防腐能力。福尔马林(35%~40%\ 甲醛 的甲醛水 学习误区 燃烧 2CH3CHO+502 -^4CO2+4H2O
溶液)可以用来保存动物标本,用作消毒剂等 丿 知能提升 氧化 O2 讐 2CH,
醛类中只有甲醛是气体(常温),推断题中可以作为一个特殊信息 使酸性KMnO,溶液或Br:褪色
化学性质
只有一个醛基 总结 知识梳理 如丄+ H*CH,CHQH
发生银镜反应时,imol 乙 乙醛 升华
醛生成2 mol的银 与新制 Cu(OH》 反应式 Cu2++OH-=Cu(OH ) 2 l 1 反应
有两个醛基 乙醛、甲醛的比较 CH5CHO+2CU(OH)2
4 CH3COOH+C0O]+2凫0
R 炷 发 成 C 基 生 H 4 O 跟 m 银 + o 醛 镜 2 l A 的 基 反 g 银 ( ( 应 N 一 H 时 C 3) , H 2O O I H m )相 亠 ol 连 甲 R 构 醛 CO 成 生 O 的 N 化 FL 合 +3 物 N 叫 H3 做 +2 醛 Agj + H20 反应方 醛 类 程式 醛类物质 银镜反应 2N A H g ‘ N H O Q ; = + A N g( H N ]H H ; 3 O ) [ 沉 — 2 = O 淀 A » H C g 由 + H O 2 蓝 3 H H C l 色 , O O + 一 O N \ N C H > H H JN , 3 + 黄 C O 5 H , A 色 反 O g 一 + l 应 2 + > A 3 5 g N ^ ( 砖 / N H A H 红 3 g + 3 O ) 色 H 2 H O 2 O H +
将稀氨水逐滴加到稀AgNO,溶液中,边滴边 震 生成银镜条件 新制银氨溶液
荡,至最初产生的沉淀恰好溶解为止 银氨溶液
A A g g 水 N O 浴 O H 3 + 加 + 2 N 热 N H H , 3 3 - H H 碱 2 2 O O 性 = = 环 A A 境 g g O ( , N H H 试 l+ 3) N 管 2O H H , 要 N + O 2H 3 2O 实验成功 的 方 的 法 配 条 制 与 液 银 反 氨 应 溶 有毒,使蛋 结 化 构 工原料 H二二 0 H丄相当于含两个酵基)
洁净,不能搅拌和振荡 件 学法指导 白质变性 物理性质 无色、有刺激蠻的气体,易溶于水
银氨溶液不可久置,须现用现配;
试管 内附着的银镜,可用稀硝酸 常见具有醛 甲 燃烧 HCHO + C h CO 2 + H 2O
溶解淆』 基的物质 醛 催化荆 II
2HCHO + O2 «,2H—C—OH
量的关
1 囂 mo 蠶 l — 農 HO 蠶 可生 囂 成 膏 2 m 蠶 ol A 有 g 醛 系 基 , ’甲酸的银 能发生银镜反应或与新制 醛的化 HCHO+O2 箜线 HO—C—OH ―► CO2+H2O
镜 甲 醛 酸 基 反 某 , 酯 故 应 因 能 既 发 丿 含 生 有 银 酯 镜 基 反 又 应 含有 甲 镜 酸 反 某 应 酯 丿 的银 C 有 甲 等 u : 酸 (O 醛 某 H) 类 酯 ,悬 、 、 浊 甲 葡 液 酸 萄 反 、 糖 应 甲 、 的 酸 麦 有 盐 芽 机 、 糖 物 学性质 — — 宀 气 加 反 应 H 生 去 成 O 醇 加成 +田丹CHQH
葡萄糖为五 鼓能发生银镜 常见的能发生加成反应 与新制 Cu(。以反应、国耗银、铜量为 2 倍,生成 银镜反应
羟基醛, 反应/ 0 的官能团或基团 氧 ' 化反应 < 产 被氧 幫 化生成酸 -----------------------*....物..为...H.2.C.O..3. (. C _02和見0 )
-C=C-x-c三c-、 E 有机合成原料 , 遠如奸木 福尔马林:
R R 方 C C 法 H O O ON +2 a+ C C U( 1 有 检 1 O 2 红 验 H O ) 色 醛 I 2 + + 沉 基 3 N H a 淀 的 O 2O 生 一 H 成 种 — 式 应 反 反 用 应 应 /Z 方 现 程 与 应 新制 实验 C 中 U 应 (O 注 H 意 )2 的 反 事项 新 成 的 量 制 功 条 的 件 关 Cu 系 (OHX 配制 I 碱 浊 要 m 性 液 o 点 l 环 ; ― N 境 直 H a 新 接 O OH 制 加 可 要 热 生 CU 过 至 成 ( 量 O 沸 H 1 ) 实 m 2 o 为 验 l C 悬 u 2O 同 同 , 饱 皮 分 分 制 异 制 和 标 构 农 异 本 一 体 药 只 、 构 元 是 化 体 燃 肥 醛 基 由 碳 的 30 于 链 % 醛 通 异 ~4 基 构 0% 式 只 所 的 能 致 甲 连 C 醛 在 ”H 水 碳 2 溶 ” 链 O 液 的 或 | 端 C 点 M , zC 所 H 以 O 醛 ,0高 高 中 中 化 化 学 学 第 第 ■ 十 — 一 章 章 蛭的含 姪 氧 的 衍 含 生 氧 物 衍第生四物节有机推第断三和节有發机酸合、成酯 依据特殊反应条
件推断可能的官能团时,常因记忆混淆而出错学习误区
生 生 ( 分 又 又 二成 成 最 子 含 能 元 简 H C 式 有 体 弱Q O 式 醛 现 酸 C ? 的 相 的 H 基 醛 ,量 2 同 量 。 类 其 O 一 或 一 2 因 的 分 ; 定 为 定 此 性 子 结 时 同 时 甲 质 式 构 , 分 , 酸 为 简 A 异 A 在 、H 式 、 构 2 反 B B C H 体 含 应 2 C 含 ) O O 氢 中 碳 , O 的 既 的 H 质 能 ; 质 分 量 体 量 子 分 现 分 中 数 蔑 数 既 相 酸 相 含 乙等 的 等 有 性 後 二 质 基 酸 , ( 总 A 完 、 质 全草 B 量 燃 十 甲 以 一 烧 斷 酚 何 定 后 种 时 比 , 例 无 论 混学 合 组 , 分 习误区 总 升 结 华 法 有机推塹 推 厂 断 分 类 方 分 顺 层 逆 推 推 连 连 C 推 法 理原 接 接法 法子 的 梭 数 煙 基 不 基 的 同 不 数 同 目不同 先 构 理, 根 , 最 据 然 高 低 后 题 后 级 级 得 意 再— 脂 脂 出 分 将元 脂 肪 肪 正 层 每酸 肪 酸 酸 确 推 一、 酸 ( ( 的 理 层二 、 如 如 推 得 结元 芳 C C 断 出 构酸 H I 香 7H 结 ' 每 进 C 、 酸 „ O 论 C 行 一 多 O O 元 层 综 H O H 酸 的 ) 合 ) 结 推 、
( 生 原 耗酯 最 成 子 氧化 简 作 C 量反 O 式 示 一 生 , 应 的 相 踪 定 成 的 量 同 原 时 H 一 或 子 ,後 Q 定 为 证 的 A酸 时 同 、 明 量 脱 , 分 B 酯 一 羟 A 异 具 化 定 基 、 构 有 反 时 , B 体 相 应 , 醇 分 ) 同 的 A 脱 子 的 、 脱 羟 中 最 B 水 基 含 分 简 方 氢 碳 子 式 式 , 原 中 丿 此 子 含 皿 原 数 氢 公 酸 理 相 詳 刀 可 等 ) 盛 巩 用 赢 " _ 0 、 ___ 种 __ 比 __ 例 右 无 罷 总 混 十 论 、 \ 芸 物 合 " 的 组 质 , 分 的 完实 酯 A 量 全 、 赢 一 化 燃 B 定 知 以 烧 反时 何 后 , 能 应有 燃提 机 烧升 混 规 合 律 物 是 知 总 升 能 结升华 知识 梭酸 由结构官推能 团 断有机物 由 推 实 断 验 类饱 推 型和 断 推 厂度 有 断 不 机 由 有 同 物 性 机 根 质 物 I ( ( 据 不 如 後 官 无 饱 基 能 H 色 和 质 ) C 团 、 蔑 O谱 Y 推 有 酸 O 0 法 0 断 H 刺 ( H 、 激 如 C 性 H CH ' 气 C 2= O 味 C O H 的 H - C 液 ) O O 碳 体 H 碳 ) 双 、 苯 键 环 、 、 碳 饱 卤 碳 和 代 三 後 怪 键 酸
加耗 的 入氧 化 试量 学 剂一 式 的定 为 顺时 G 序 H , > :A O C、 “ 2HB 则 5各O B H自 的 -*的 化 浓x 学 硫+W 式 酸4 为 —-z C/2 G H相 H 'C . 同 Q O O . , H 若A 知识梳理 有机合成 乙 质 酸的物 综 也理 合 计 推 算性 断 推断有机物 易溶于水、易溶于有机溶剂 酯基、肽键
有 的 导 浓 , ( " 饱 管 硫 个 C 和 的O 酸 碳 一 ? 末 的 ) 原 元 端 作 ” 子 發 .不 用 的 ( 酸 能 : 饱 H 和 插 催 Q 和 酯 ) 入 化 一 具 ” 到 剂 元 有 , N 醛 相 a 吸 与 ’ C 同 水 含 C 的 h 剂 有 最 的 2 简 液 " 个 式 面 碳 下 原 , 子 以 防 止 倒吸 无 栏 最 论 例 简 多 混 式 少 合 相 种 , 同 , 混 乙 注 的 以 合 酸 意 有 何 物 乙 事 机 种 中 酯 项 物制,备 含 的 有机物分子组 化 质 ( 常 学 见 性 的梭酸 _己;酸 增 的、 长 方甲 碳 法酸 链 、 酯 苯 化 甲 酸 反 酸 性 应 (。~ 不 引 酯8° 饱 入 勺化 R 蔑 和 一 、反 C 酸 化 C O 乙应 N 脱 O合 二 H ( 羟 物 酸 R 膀 基 间 ( C 基 , O的 H O ) 醇 O 加- O 后 脱 成+ C H 水 氢 、 -C + 解 生 聚 OO 成 合 H 酯 、 ) 和 水
含 同饱 b. 有 的 溶 和 " 最 解 N 个 简 蒸 a 碳 2C式 发 原 O 出3 子 的 来 的 作 的 焕 用 乙 匹 : 醇 与 a ; .中 含 c 和 . 有 减 蒸 3 小 " 发 个 乙 出 碳 酸 来 原 乙 的 子 酯 乙 的 的 酸 苯 溶 ; 房 解 、 度 〜 元 》 素质量比相同 其同系物具有相 成 用 规 通 律 式的应 碳链的增 减 0 煙 某 的 些 裂 姪 化 的 、 氧 裂 化 解 (如苯的同系物、烯姪)
提 醇 含 ) 含 ( 高 过 有 个 有 »-1 产 量 " 碳 " 个 个 ) 率 ; 原 碳 碳 个 采 加 子 原 原 碳 取 热 的 子 子 原 的 将 饱 的 的 子 措 酯 和 饱 烷 的 施 蒸 一 和 軽 饱 : 发 元 一 与 和 浓蔑 元 含 一 硫酸 醇 有 元 酸和 与 醛 吸酯 含 水 有 , 平 ( 衡 n-1 正 向移动1 乙 相 同 对 的 分 有 子 机 质 物 量 相 官 团 能 乙酸乙酯的物理 ~c― 碳 性 o 碳 — 质 单 ( 键 酯 / 一 的 基 蔑 无 酯 引 ) 酸 包 的 入 脱 有 水 : 梭 特 解 烯殊 燃香、味煥的煥液的体加成反应 卤原
相 量 相 为 饱 通 目 对 为 对 和 式 相 3 0 分 分 一 : 同 4 的 6 子 子 元 C 的 的 有 „ 质 质 梭 饱 H 有 : 2 量 C 量 酸 和 „ : z O 为 H 为 与 一 G 2 g ( H 饱 元 4 2 H 4 8 Q 和 建 n C 的 的 H > H 一 酸 2 、 有 有 O ) 元 是 H : 、 :, C 醇 同 与 C N G O 3 O 形 分H H O C , , H 成 异 、原 . 根 C 、 酯 构 N子 H N ” , 体 ' 数 据 C 酯O C H . , O 水 ’ O 二 结 相 解 、 會 相反 C 构 O 瑾 对应 ? 量 分 、 条 区 R 子 N 件 C 2 质 分 O 的 O 量 O 相 判 R 梭 为 对 断 ' 分 6 酸 0 子 的 质 和酯 常 量 无 两 机 见 相 物 同 的 类 相 的 通 式 对 有物 分 机质 子 物 质 和 官 团 能 的转化 化 质 学 引 团性 入 的 官 方 能 法 酸 碱 CH 性 性 3 条 C 条 O 件 件 O 下 子 醇 羟 原 W 消 C 下 碳 2 水 的 的 基 ) 去 水 H 双 V 解 引 卤 的 ; 反 3 解 不 + 键 : 入 代 引 卤 应 N : 溶 、 a 可 : 入 代 ( 不 O 于 三 逆 H 烯 : 軽 卤 可 水 键 反 怪 加 的 代 逆 , 的 应 、 成 水 燃 反 易 引 ; 煥 反 解 、 应 C 溶 入 生 怪 应 醇 H ; 于 ; 'C 成 、 ( 的 生 有 O 梭 苯 烯 消 成 O 机 酸 环 炷 去 N 峻 溶 a 和 的 水 ) 酸 + 剂 G 醇 _ 加 化 盐 _ H _ 成 、 和 Q _ _ H ; 酔 _ 醛 _ 烧 _ 酮 _ 的 _ 的 _ 卤 一 还 代 _ ;
有
醇 及
:舞
的 同
G酸
消 系
H
去 物
,O
( 的
H
醇 硝
、
酸羟 化
CH
性基 、
,C
条) 磺
O
件、 化
OH
下酯 、
、
水化 纤
H
解反 维
CO
应 素
O
( 的
CH
含 水
,
有 解 羟基 水 、 解 後 产 基 物 ) 的 、 判 苯 断 浓硫 化 质酸 学 加的热 性 应 学法指导 询和一兀稜酸的通式
CH3COOC醛2H
後
5+
基
H
的
20
引
破
入
、
:
CH
醛
3
能的
CO
使氧
O
紫化
H
色
+
;
G
石酯
H
蕊
Q
的
H
试水液解变 加红,
酯的水解(含有酯基),二糖、淀粉的水 用 学法指导 消除官能 成消除不饱和键酸性强于碳酸 —
一 解 和 加元成酯( 卤 碳 代 碳 煙 双 的 键 水 , 解 碳 , 碳 酯 三 的 键 水 , 解 醛 根, 基 据酚 , 性类 幾 质、 基 判蔑 , 断酸 卤 消 苯 酯类 代 去 环 的的 煙 ) 结中 的 构 N N -R a a / O O酯 型催 H H 化 的 的的 剂 水 醇 稀 f 类 溶 溶 硫 液 液 酸 \ 根 判 据 断 特 可 殊 能 反 的 应 官 条 能 件 团 毯 酸 酸 性 具 ) 备酸 团 的 的方 通 法 性(弱 取 成 水 代 、 解 、 氧 冰 、 消 化 解 消 去 消 消 去 、 除 除 反 酯 醛 酯 应 化 基 基 消 与 与 、 除 N N 氧 卤 a a 化O 2 原 C H等 O 子 溶 3 反 溶 液应 液 反消 反 应除 应 羟基 加
二 环 元 酯 酯 酔羟基(伯酔或仲酔 苯 取烷 环 ) 环 代煙 上 的 上 或 烷 氧 的 苯 炷 化 有 酯 构 写 C C l关 的 C 2 V ( l B 体 2 C ( r B u 酯 同 2) , r 加 / 2 的 光 )/ 热 F 的 分 照 e书 丿 ‘ 计/ 异 / 酸 断 性 环 成 状 方 强 酯 的 法化 弱 形 反 的 应的 判 原酯理成环 强酸制 残 弱 酸 二 含 酸 脱 元 羟 的 羟 酸 基 原 基 和 的 理 , 二 後酔 消 元 酸脱 除 醇 自氢 肽 的 身 键 酯 酯 与 化 化 钠 成 成 反 环 环 应 ; 放 出氢气
无机 聚 水 酸 酯 解 酯 (酸 与 性 新 条 氧 制 件 化 还 下 C ; 原 u 弱 水 水 加 ( ; 酸 发解 解 成 O 氧 性 生 H ; ; ) 化 ; 银碱 加 , 取 镜 悬 性 聚 代 反 浊 条 ; 应 液 件 弱 加 反 下 酸 成 具 水 性 ; 有 解 ; 显 醛 ) 酯 色 的 化 性质 甲— — 酸C C 算 O O 又 - C C O — - Y = O 称 H R 0 C N H O 0 - 结 ( 蚁 H ( H ( ( — 构 碳 酸酯 俄 酚 醛 ( 碳 基 基 肽 羟 基 双 ) ) 键 基 ) 键 、 ) ) 、 ) 甲 性 X 0酸的 官 与 特 能 化 团 学 的 性 结 质 构 依 测 酯 应 据 官 化 某 能 反 些 团 反 的乙 应 位酸乙 推 置 酯 酯 水 的 解 制 断 备 键推 肽 由 由 由 断 键 醇 消 醇 後 成 氧 去 氧 酸 环 化 反 化 和 原 得 应 得 3 醇 理 m 醛 的 到 . L C 或 产 酮H 乙 蔑 物 ,'C 酔 O 酸 可 一 ( O 二 , 确 O H 过 元 H 一 定 + 量 C连 酸 " O H ,一 接 与 H m 3 利 C L0 一 在 二 H H于 浓 定 只 元 2 "或提 O 硫 连 有 氨 H “高 酸 接 基 1 — 一乙 ( 个 在 化 < 醇 催X ■氢 有 合 " 的 化 C 的 原 物 2 H 转 剂位 个 子 成 3C 化 、置 氢 的O 环 率 吸 O 原 碳 ; C ) 水 子 原 氨 2H 、 剂 的 子 基 5 + ) 碳 上 H 实 酸 、 2 原 0 验 成 2 子 药 环 m 上 品 L 一 乙 酸 2
使酸性 K 氧 M 化 nO ; , 、 加 溟 成 水褪色 C三C 生 (质碳碳三键)/ 刁 由取代反 实 应 验 的 现 产 象 物 液 的 面 总 上 数 有 可 透 确 明 定 、 碳 不 链 溶 结 于 构 水的油状液体产生,
取代(水与解活(泼氢金具氧属有化反後钠应酸水、的溶与通液氣性)卤,;酸能消反发去应生(、酯氢酯化氧化反化反应钠应含醇)蔑溶;基液消,去;氧化 一 加 0 热 H( ) 醇羟基 一 ) X(卤 子 原 ) 由加氢后--碳--的--骨--架--, 7 可 并确可定以>闻=到C香<味或 一C三C-的位置高中化学 第十二章 生命中的基础有机化学物质和有机高分子化合物 第一节油脂
注意油脂和酯的区别和 学习误区 组成 C、H、0三种元
联系 素
油脂是一种特殊的酯 酯和油 总结 来源 植物果 花生、大豆、菜籽等
油脂能发生水解、氢化反应;酯能发生水解反应 脂 系 的关 升华 实动物 脂肪
油脂在碱性条件下的水解反应叫皂化反应 体
矿物油属于多种姪的混合物; 而油脂 Ri—C- -O—CH2
是多种高级脂肪酸的甘油酯 ?! I
矿物油具有燃的性质,不能水解;而油脂具 有 油脂和矿 知能提升 R2—C-K>—CH V脂肪酸甘而备
酯的性质,能水解,并兼有烯煙的性质 物油的比 结构 Ml
油脂中的现象:红色变浅 鉴别:加含酚猷两' 较 知识 R3—c-i-o—CH:
NaOH溶液,加热 梳理 状态 室温下为液态(油)•
矿物油中的现象:无明显变化 固态脂肪
I 软 酸 ( I C 常 亚 脂 I ( 见 油 C , 酸 H „ 脂 酸 H 3 ( 3 3 肪 C ( C5 C C 1 O 5 酸 O “ H O H O H 3 : , “ C H C O ) O ) O O H I H ) ) 油 硬脂 酸 高 甘 级 油 脂 形 肪 成 酸 的 和 酯 组 成 油脂的组成 物理性质 溶 性 密 度 解 比 不 于 水 溶 有 小 于 机 水 溶 剂 I 制高级脂肪酸和甘油 溶
当 酸 结 的 构 燃 中 基 的 , 燃 油 基 酯 R , ,、 不 同 高七 相时 级、 同称 脂R 时 , 为 肪分 称 别 为 代 单 表 甘 结 和结构 C.jHjjCOOCHa CH2—OH
混甘油酯 含有酯基 官 构 能团 7 k 解 酸性条件 CI7H„ C C I7 O H O „C C O H O + C 3 H H ■ 2 2O 、"" i 浓 硫 酸 I C C H H — 2 — O O H H + 3 - C -I7- H -3-3C -- O - O - H -
可能含有碳碳双键 )
化学
CI7H35COOCH2 CH2—OH
区别 油脂和酯的 性质 碱性条件 CnH}5COOCH + 3NaOH--------------CH—OH + SCnH^COONa
形成酯的酔 形成酯 联系 区别和联系 C17H35COOCH2 CH2—OH
或酚 的酸 Z
由 脂 高 酸 酯 油 脂级 、 脂 任 固 油 何 定肪 醇 为 酸 或 甘酸 酚 油 ) ( 和 硬 甘 任 高 肪脂 何 级 酸 油 酸 酸 脂 形 、 成 软 油 类酯 部 脂 ,类 分 属 是中 于 的 酯 一小 学 指 法 导 反应式 C C „ 1 H 7H nC 3 O 3C O O C O H C 2 H + 3H2 -sl^CnH C ^ I7 C H O 35 O CO CH OCH2
无固定的熔沸点 _混合物 C.jHuCOOCHa C„HJ5COOCH2
可发生水解反应 属 于 油脂的判断 一 工业目的 硬化油性质稳定、不易变质.
不饱和油脂可以发酯生、加成
反应 制肥
实验现象 水解产物及皂化 皂 碱性条件下水解生成高级脂肪酸钠
反应 当油脂的皂化反应基本完成后,向 混
用途 盐析 合液中加入食盐细粒,搅拌、静 置,
不
成
饱
,
和
后
性
两
;
者
能
现
与
象为
1 m
褪
ol
色
H
;
2S
关
Br
系
,s 踞
:
加 性质的应用
相关反应参见匕了 生产高级脂肪酸和
高
在水
级
面
脂
,
肪
从
酸
而
钠
跟
将
甘
从
油
混
、
合
食
液
盐
中 析
水 分
出
离
,浮
lmol浦酸甘 油酯能与3 mol H2S Br2 “化学性质”『 甘油
或CL加成 工业生产硬化
肥皂去污原理的
油
应用高 高 中 中 化 化 学 学 第 第 十 十 二 二 章 章 生 生 命 命 中 中 的 的 基 基 础 础 有 有 机 机 化 化 学 学 物 物 质 质 和 和 有 有 机 机 高 高 分 分 子 子 化 化 合 合 物 物 第 第 三 二 节 节 蛋 糖 白 类 质和核酸 定义
酶是一种蛋白质,易变性 组蔑酸成分元子中的炷基上的氣原子被氨基取代的化合物称为氨基酸
条 用 葡 件 具 银 萄 温 有 氨 糖 和 高 溶 结 、 度 液 构 不 的 或 的 需 专 新 推 加 一 制 断 热 性 的 和 , C 淀 ― u 粉 ( -- 水 - O - 解 H -- 程 ) -- 度 , -- 的 、 悬 -- 判 酶 浊 - 断 - 是 液 -- 一 检 - 种 - 验 - 生 - 二 - 物 糖 -- 催 和 -- 化 - 多 - 剂 - 糖 - , - 的 - 具 - 水 - 有 -- 的 -- 特 -- 点 学酶习的特误性学区习误区 总结升华 氨基酸 基 结 通 式 本 构特 概 征 念 亠 定 特 既素 R 义 含 — 征 有 C H 後 — 基 C ( 多 0 4 不 0 足 — 羟 H 一 C 基 定 O 醛 O 有 或 H 甜 多 ) 味 羟 ,又 , 基 含 分 酮 天 有 子 和 然 氨 式 它 氨 基 不 们 基 ( 都 的 酸 — > 符 -脱 都 - N 合 - H 水 是 - 。 J -缩- , a - - ( 合 氨 -- 玦 物 基 - - 0 酸 - ) --- “ -
解 H2 产 SO 物 4, 中 否 有具 则 无有 实 还高 验 原效 将 A 桂性 l 会 、 糖 失 A 产 1 败 2 生 0J 时 . , A 必 l(0 须 H) 用 3 两 N 性 a 物 OH 质 中和作催化剂的 知能提升 总 升 结 华 知识梳理 性 分 质 物 子 理 结 性 构 质 C 两 脱 H 白 2 性 水 色 O 缩 H 晶 ( 合 体 成 C , H 肽 O 有 H 组 键 甜 ) 反 味 成 I 应 C , H 能 元 O 溶 ( 于 分 水 子式为 C 、 C6 H H 、 2 0 6 、 , 属 N、 多 S 羟 、 基 P 醛 等 )
H 与 C 新 O 与 ; 制 C 银 H 、 的 3 氨 N H 氢 C H 溶 P O 氧 遇O , O F 液 ; 化 碘 N x 反 H - 铜 单、 4 应 反 质H 有 S 应 变- 银 ( 等 生 N 蓝 镜 H 成 O 现 红 z 象 S 色 弱 沉 酸 淀 的 、 酸 ° 气 式 酸 葡 根离 萄弱 淀 应 子 酸糖 粉 的铉 盐 的 的 特 特中 既 能 的征 征 与 物 学 反 反 能 质 化 与 碱 学 反 酸 对 的 中 应 又 糖 考 类 查 知 提性 能 升质 梳 知 理 识 葡萄糖 蛋白质 银 燃 与 加 镜 烧 新 成 分 纯 一 制 反 性 应 类 质 C G 离 U 别 H ( 、 反 M O 和 O C 应 ' H H + 式 素 ) Z 提 G C O O H H 2 C Z I 2 H 反 O C 算 Q H H 应 H O ( 、 C 6 H (C C ' H 两 烧 H C 盐 O C O C H 生O 2 H 性 有 H析 H Z + H物 2 O ) 6 2 、 烧 4 O O ) H C H ,体C H H 水 焦 H 2 H ( 内 O ( O C C 解 羽 O + H 的 H + 、 毛 H O O 2 2 蛋A 盐 的 H H 白g ) ) 析 气 , 4 ( C C N质 、 味 O H H, O O 3 变 H ) + 有2 性 2 + O催 C 、 H C U 化 ( - U 颜 O 2 作 色 H C 用 ) H 反 2 + 应 2H 、 2O 灼
蛋白 蔗 质 糖 在 水 麦某 解 芽些 生 糖盐 成 水的 葡 解浓 萄 生溶 糖 成液 和 葡中 果 萄 甘 溶 糖 糖 氨 解 酸、谷氨酸等氨 蛋 基 白 酸 质水 应 解反 分类 用途 反 制 应 镜 特 点业、食 应 品 用 加工、 此 合 CH 反 成 2 应 药 OH 具 具 可 物 (条C 有 有 用 、 H件 高 高 于 医 O温 度 效 H 检 庁 和) 的 催 , 验 等 C, 专 化 O 葡 不O 一 作 萄 N需 性 用 糖 H要< +加2 热 Ag[ + 3NH , + 田 0
二糖或 度 多 降 以 钠糖 碱 低 及 、的 金纤 , 铉 氯水 属维 淀 凝 盐 化解 、素 粉 聚 ( 钠都 镁水 水 可 而 如 )是 、解 解 逆 从 硫 的在 铝生 生 溶 酸 浓无 等成 成 液 铉 溶机 轻葡 葡 中 、 液酸 金萄 萄 析 硫 作 属糖 糖 出 酸 催 盐 化 剂的条 枣 特 征 条 \ 件 念 件 下 1 进 行的 盐 析 物 分 理 子 性 结 质 构 《 ― 可 C 溶 H 无 于 zO 色 乙化 H 分 类 晶 C 醇 H 体 学, O , 难 H 组 易 ) 溶 溶 厂 于 于 ~ 乙 c 水 — 酸 , C 、 H 是 z 脱 O 最 H 氧O 甜 ( 核 的 分 糖 糖 磷 子 核 酸 式 酸 为 ( Q D H N o A O ) ” 不 属 能 多 发 羟 生 基 银 酮 镜 ) 反应 水 溶 的 解 液 氢 产 中 氧溶 物 和 化解 中 作 铜度 都 催 悬减 有 化 浊小 葡 剂 液, 萄 的 进性 糖 稀 行质 。 硫 检不 在 酸 验变 检 ,, 验 然属 其 后物 产 再理 物 加变 前 入化 要 实银 加 质氨 入 溶J) 氧 液 氧 或 化 新 钠 制 原盐析和变性 分 物 子 理 式 性质 无色 成 晶 C1 体 2H , 2 溶 2O 于 11 水 ( , 无 有 醛 甜 基 味 戊 碱 糖 基 与 悬 银 浊 氨 液 溶 不 液 反 、 应 新制CU(OH)3
淀 成 粉 葡 在 萄 稀 糖 硫 , 酸 起 催 始 化 的 作 反 分 用 应 离 下 物 和 发 淀 提 生 粉 纯 水 遇 蛋 解 碘 白 反 变 质 应 蓝 , 色 最 , 终 不 用 生 能 途J 理的区别 氨基 酸 蔗糖 官 及 0 兴 性 能 姓 质 居 团 水 解 : C氨 R 基H N “O H碱 +性 H Q 箜 地 G H n O o 葡 +C 萄 'H 糖 uO s 果 化 糖 于任性、 发生银镜反蛋应白;质而在葡热萄、糖酸遇、碘碱不等变条蓝件色, 但含有 . 来源 甘蔗、甜菜等
醛基,能发下生,银 镜性反质应发。生据改此变可而以凝检聚验 和判断 〜淀 概念 制作甜味食品 粉 否 在 已 水 经 结 溶 进 构 液 行 、 中 完 性 是 全 质 否 改 已 变 经 ; 发 属 生 化 了 学 不水 变 可解 化 逆, 变 以 化 及 实 水 质 解是特征依 据 变 性 淀 解程度 粉 的 水 判断 糖类水解 学 产 法指学导法指导 [ 物 分 理 子 性 式 质 白 两 色 性 晶 G 体 2 , H2 易 2O 溶 ,, 于 ( 水 有 , 醛 有 基 很 ) 小的甜味 麦芽糖 1/化学 加 X射 热 线 、注 葡、 强意 萄重 酸: 糖金 、在 时属 强用 ,盐 碱银 需以 、氨 要及 强溶 先一 氧液 中些 化检 和有 剂验 水机 、水 解物 紫解 液如 外 中 生 甲 线 成 醛 、 的 、 的 无条件 物的检验 氨基酸、蛋白质 性质 与银铉溶液 官 、 能 新 团 制 C U ( O H ) 2 悬浊液发生反应
酒精、机 反 苯 应 酸甲,酸使等溶液呈碱性,才 消 能 毒 发 、 生 杀菌 银镜/------- 现 核酸—— 结构和性质 来两源性 农产品(大米、玉米等)
象 DNA和RNA的比较 用途 制作甜味食品
如果淀粉没有发生水解,则水中只有淀粉, 没 多 羟 羟 基 基 醛 醛 或 或 酮 酮 的 , 物 或 质 能生成 多 蚩白质 分子式 (GHmO。,,,属天然有机高分子化合物
有 现核 葡 象 萄 :酸 糖 加是 。 碘变一蓝;种但不含能磷发生的银镜生反应 y 靱木 ,恤 5 能旳以 牌、 概念彫捋 物理性质 白色粉末,不溶于水
如 只 现 如 物 一 万 对 万 果 有 象 果 淀 葡 : 淀 高 般 个 分 至 粉 萄 加 粉 由 原 子 水 糖 碘 只 分 几 解 。 不 发 几 子 质 完 变 生 子 百 全 蓝 了 千 组 量 , ; 部 化 万 则 能 分 成 可 水 发 水 合 到 , 达 中 生 解 物 几没 银 , 相 十 有 镜 则 , 十淀 反 水 几 粉 应 中 , 既 有 葡 蔗 淀 萄 糖 粉 糖 与 与 与 麦 麦 果 芽 芽 糖 糖 糖 互 互 不 为 为 是 同 同 同 分 分 分 异 异 异 构 构 构 体 体 体 糖 间 系 类 的 之 关 、 构 糖 概 类 念 的 与 、 结 多 糖 纤 淀 维 粉 素 化 分 学 子 性 式 质 盐 变 析 性 体 ( 白 酸 Cs 内 色 催 H 水 i , 化 oO 解 无 水 s) : 臭 解 ”, ( 无 : 味 ( 淀 仁 粉 孔。0,)“+阳 麦 20 芽 變 糖 処 萄 "C 萄 sL 糖 O, 淀 现 粉 象 , : 又 加 有 碘 葡 变 萄 蓝 糖 ; 。 也能发生银镜反应 具有醇、醛的性质 葡萄糖是多羟基醛 灼烧 不 麻 溶 纺 于 织 水 、 及 工 一 业 般 原 溶 料 剂 棉、
S2S 共腺鸟
胞尿胸 梭基 >酸性 既能和酸反应又能和碱反应
在酸或碱存在的条件下加热,通过一 个 氨基酸分子的氨基与另一个氨基酸 分子 的梭基间脱去一分子的水,形成 成肽反应 ----------- 、 含有肽键 - -的化合物 氨基、蔑基、肽键
既能和酸反应又能和碱反应
在酸、碱或酶的作用下,天然蛋白质水解 产物
为多种a-氨基酸。反应断裂肽键,断 0: H II: I
水解反应 键位置:-C+-N-
在轻金属盐溶液中有固体析出 名称 五碳糖 碱基种类 主要存 位 在部 作用 在重金属盐溶液中或加热、强酸、强碱、 强 D N A 脱氧核 酸 糖核 脱氧 糖 核 4 C 种 ) (A、T、G、 细胞核 生物体遗传信息的载体 颜色反应 含 氧 有 化 苯 剂 环 等 的 条 蛋 件 白 下 质 发 遇 生 浓硝酸产生黄色不溶物 R N A 核糖核酸 核糖 4 C 种 ) (A、U、G、 细胞质 根 控 成 据 制 D 体 N 内 A 蛋 提 白 供 质 的 的 信 合 息 产生烧焦羽毛气味-常用此性质鉴别蛋白质高中化学 第十二章 生命中的基础有机化学物质和有机高分子化合物 第四节 有机高分子化合物
不能正确判断热塑性与热固性塑料制品 相对分子质量很大的化合物称为高分子化合物, 其相对 天然高分子
~混滂*箜食公〒=会朮真a平甘*学习误区 分子质量从几万到几百万甚至更高 按来源分有机合成高分子
高分子化合物中重复着的结构单元 链节 热塑性高分子
若链节上都是碳原子,一般是经加聚反应得到 总结升华 高 用 分 " 表 子 示 链节中含有链节的数目称为聚合度,車厶存 采 通 口 常 及 .热固性高分子
的 聚 产 反 物 应 ( 的 甲 产 醛 物 加人聚刿的产断物除聚外)合,若物链节类上型含 手…. 有“酯基、酰胺键”等一般是缩 合成高分子化合物的小分子 单体 按结构分 线型高分子
体型高分子
凡链节的主链上只有两个碳原子(无其他原子) 的 有机高分子 化 合成纤维
高 可 聚物,其合成单体必为一种,将两个半键闭 合即 知能提充 合物的概念 按用途分 合成橡胶
涂料
凡链节的主链上只有四个碳原子(无其他原子), 加聚型的 高分子 知识梳理 有机高分子
且链节无双键的高聚物,其单体必为两种, 在正中 化合物 化合物的分类 黏合剂
划线断开后将四个半键闭合即可 用有机高分子化合物制成的材料
概念
凡链节的主链上只有碳原子,并且存在>C=C< 结构的高 根据高聚物结构简 天然有机高分子材料,如棉花、
聚物,其规律是'‘见双键,四个碳;无双 键,两个 式 羊毛、蚕丝、天然橡胶等
单 碳 、 ” 双 。 键 划 互 线 换 断开,然后将半键闭合,即将 、推断其 達 单 / 体的方 有机局分 分类 合 合 成 成 有 纤 机 维 高 、 分 合 子 成 材 橡 料 胶 , 等 如塑料、
子材料
强度大、电绝缘性好、耐化学腐蚀、不透水等
凡链节是+NH—R—C04r或七O—R—CCH;结构的高聚物, O
链状高分子:热塑性(可反复加工,多次使用)
其合成单体必为一种。在拨基(一C-)上加羟基,在亚氨基 网状高分子:热固性(一经成型,不会受热熔化)
(—NH—)写(—O—)上加氢即得到高聚物的单体。如:
+N
8 士 的单体为 CH3—CH—COOH 常
合
见
成
有
材
机
料
高
及
分
特
子
点 合成
塑 料 如聚乙烯、聚氯乙烯塑料
缩聚型的 高分子 纤维 举例 涤纶、锦纶、腊纶等
化合物 强度高、弹性好、耐磨和耐化
凡链节中间(不在端上)含有一C-O-(酯基)的高聚物, 学法指导 合 橡 成 胶 式^特点 学 差 腐蚀,但吸水性和透气性较
0 举例 丁苯橡胶、顺丁橡胶、氯丁橡胶等
其合成单体必为两种,从酯基一*4o-划虚线处断开, 特点 高弹性、绝缘性、耐油和耐高温等
畿基上加羟基,氧原子上加氢,即可得到高聚物单体
高分子化合物的分类 体型结构的高分子(如橡胶)不容易溶解, 只是有
有机高分子化合物 一定程度的胀大
主链上含有官能团 缩聚物 的基本性质 溶解 线型结构的有机高分子(如有机玻璃) 能溶解
按组成分 天然纤维与 性 在适当的溶剂中,但溶解的 过程比小分子缓慢
类 合成纤维的鉴别
线型结构 按结构分 线 变 型 成 高 固 分 体 子 。 具 例 有 如 热 : 塑 聚 性 氯 , 乙 加 烯 热 塑 时 料 熔化, 冷却后
体型结构 类 煌 呈 ¥壬 底 灰 白 燃 易 色 烧 燃 时 烧 发 , 泡 有 , 烧 有 纸 烧 张 头 的 发 气 的 味 气 , 味 竺 , 竺 千 余 七 烬 —春 热塑性 性 和热固 体 不 型 会 结 受 构 热 的 熔 高 化 分 。 子 例 具 如 有 : 热 酚 固 醛 性 塑 , 料 一经加工 成型就
天然高分子材料 f 按来 源分笠 烬呈灰黑色 强度 高分子材料的强度一般都比较大
合成高分子材料二" 涤纶 一先熔化,后燃烧,燃烧后呈黑色球状
按用途和性质分类 电绝缘 电绝缘性好,这是由于高分子化合物中 只存在
丿 车帛纶一達熔化,后燃烧,有臭味,燃烧后呈黑色球状 性 共价键,没有自由电子的缘故《高频考点透析》考点导图——高中化学(一)
物质的性质
电解质
物质' 的 盐类的水解
分类 化学用语和 化
学常用计量
物质的组成、
性质和分类
水的电离和
溶液的pH
各类物质间
的相互关专
酸碱中
电解质溶液
难溶电解质
^^丼一*5 — E 化学反应 与能
分子结构 量转化
疗一1 物质结构与 元
素周期律 化学反应
脚體•*—*思一*"» 元素周期亀 化学反应速率 和 与热能
化学平衡.
化学反应
与电能.
合成氨工业
化学反应速毛
溶液和胶体 化学平衡
溶液
化学平衡
影响因素
胶体《高频考点透析》考点导图——高中化学(二)
®»K. ites
村 MM .r * t ; —制虫伸茹如e、: 气体的制备 i 例 t iut n cm :" :wM* a MK aM 8nUO u M ( 冲u 如 初險 g C a ; »»u;MntBat> ;
常见无机物 K1HCO,
的
常昆 1■崙5崙 血*—
金属兀素 告g昏**■
常见*
金属元素 物质的分离、
实验设计和
综合实验
有关化学方
程式的计算
化学计算 (2)有关多步
反应的计算
炷的衍生物 燃 衍 和 生 軽 物 的 < 4 « m * 2 i o > » 2 l 童 状 . T 41 f 要 况 l " tg 计 下 标 • 算 气 准 LJ 公 体 状 Tt 式 时 " tf 气 f i ( 次 对 I.) 质 或 g 量 质 质 = 的 2M It L (m . ol) 有 的 关 计 气 算 体 有关混 ( 问 3) 合 题 有 物 的 关 计 过 算 量 初 g 应 判 解 f»f=i 中 B 质 按 答 . g 应p 若 * 祸 反 有 F 反 《 全 咐 H 化 应 关 应 代 W种 « :面 子 学 肉 化 荷 物 入 B■a分 M 反 间 学 个 过 方 单au子 K 应 的 方 或 ・ 程 化 M 按 质 程 , 芮 蜘 个 学 m * ・ 个 林 K十 毗 a - 方 s 6 定 * 以 后 算 、 f W 览 糧 fi 量 上 按 量 物 同 》 式 算 齢 反 ■ 耕 质 , 1 表 应 关 应 质 少 是 成 不 示 湘 系 卻 的 的 絹 量 同 附 以 址 的 反 量 物 i 扯 下 ■ t 行 用 应 ; 等 质 的 = 之 , 点 ・ 的 美 此 同 但 : , 某 备 -
in合气体"»«»«»■'=皿+叫+" 的计算
2> P方程及推广,nV-
nRT iS*W«学方法应用于化学计算中
l 0 . " «» OS t a t G -H '< , I o H-N"OII — P 晌 r- 体 gs ® n I »> 时 iW , « 时 Sf 宁 B. 《 A M tts > t® W 食 Ki • E - t 亲 t> 倨 -竺 3 往 论 往 计 标 算 为 金由 4 或 "H 稼 B 为 itM 瞄 " 法。范牌讨
dSIMBM时.Kft#说与FM姗!的
《«1*>
' —WWB2H s' —
mauMtmutt
S < - - C O - l O i H ** C : — : U C C .C H H O ,C ^ O 0 IK 0 C N > ^ H » M 2 ,* H A 2 g p A < 11 g N t | ^ * H W ( I ) 1 • 0 H H目泯 密t« aH ± a 的时 度 a l t 同 t »t 分压 之» af f £ i t i于下 比 a 8 t » . s * 下 s S 。的 等 Ww T 的 木 于 a S Tm r 司 . 时 相 a ie a * 同 u F w * a , 做 . s n s t W 的 t: i t 同 STWffinait; • — , — «r * « w m «a t ta«MsaK
CH,COOH,C,",OH WT