文档内容
2022 届高三化学二轮复习化学反应中的热效应必刷卷
一、选择题(共17题)
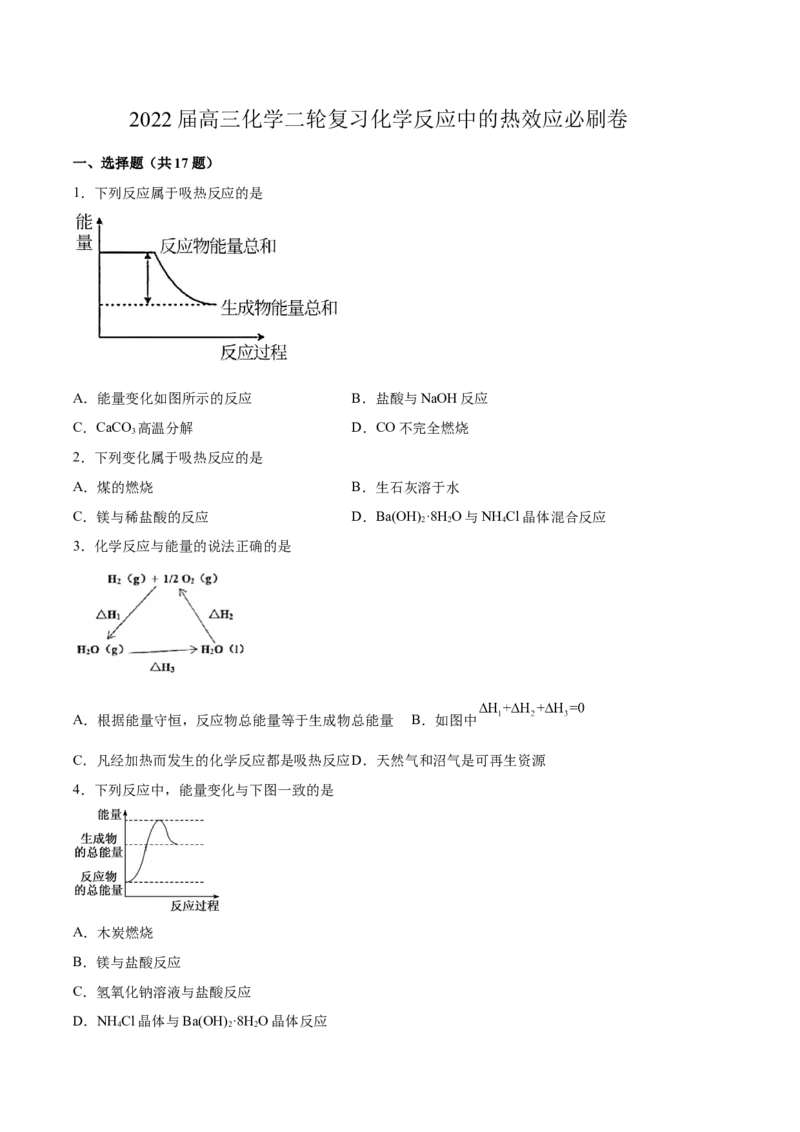
1.下列反应属于吸热反应的是
A.能量变化如图所示的反应 B.盐酸与NaOH反应
C.CaCO 高温分解 D.CO不完全燃烧
3
2.下列变化属于吸热反应的是
A.煤的燃烧 B.生石灰溶于水
C.镁与稀盐酸的反应 D.Ba(OH) ·8H O与NH Cl晶体混合反应
2 2 4
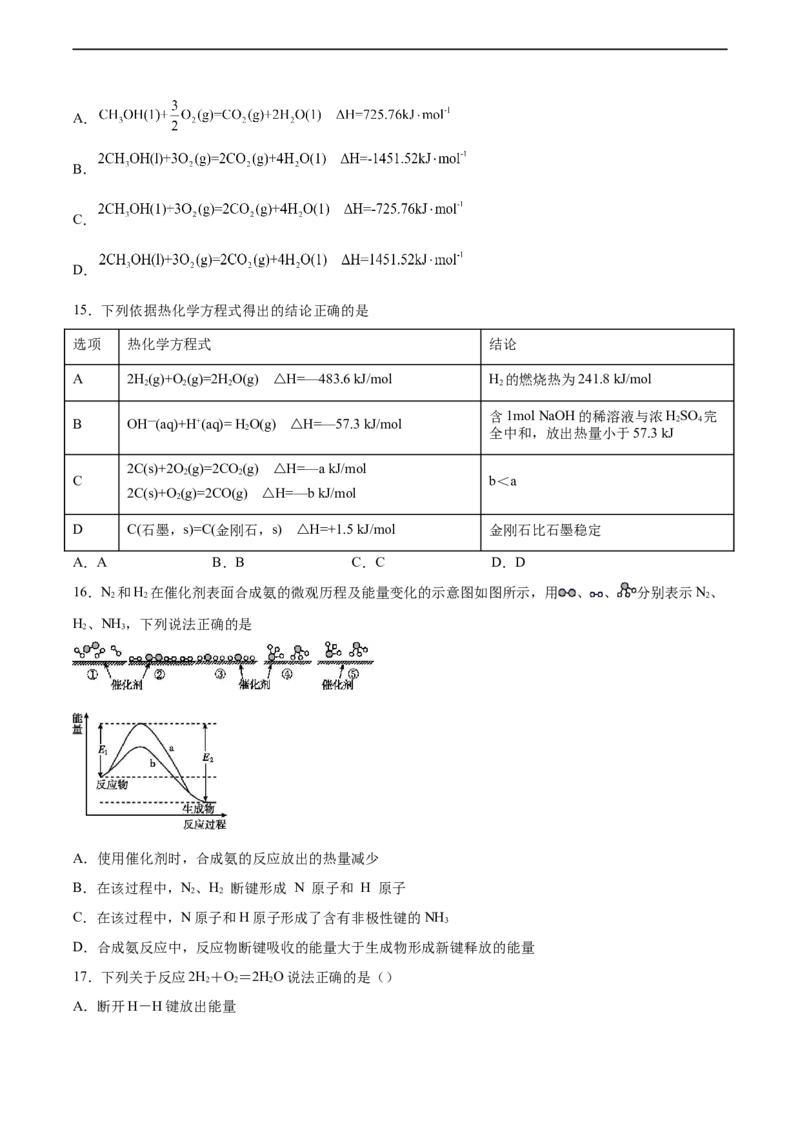
3.化学反应与能量的说法正确的是
A.根据能量守恒,反应物总能量等于生成物总能量 B.如图中
C.凡经加热而发生的化学反应都是吸热反应D.天然气和沼气是可再生资源
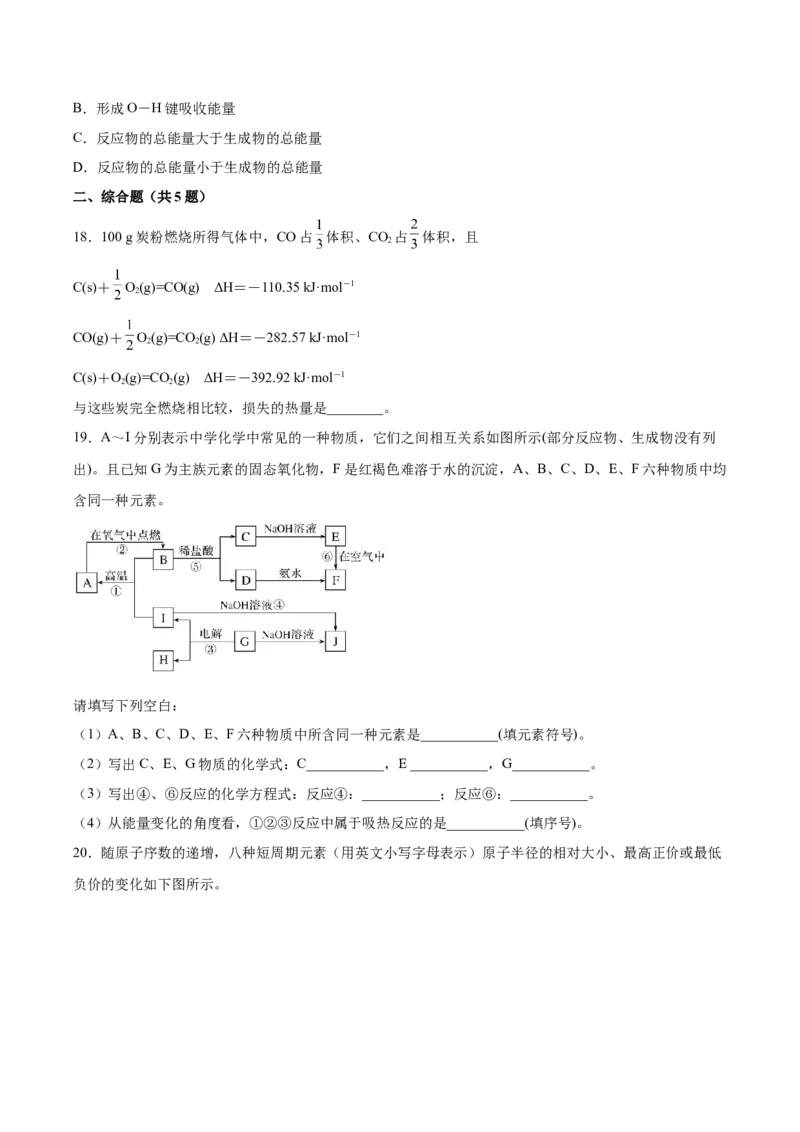
4.下列反应中,能量变化与下图一致的是
A.木炭燃烧
B.镁与盐酸反应
C.氢氧化钠溶液与盐酸反应
D.NH Cl晶体与Ba(OH) ·8H O晶体反应
4 2 25.下列说法正确的是( )
A.所有的放热反应都能在常温常压下自发进行
B.胆矾加热变为白色粉末属放热反应
C.天然气燃烧时,其化学能全部转化为热能
D.反应热只与反应体系的始态和终态有关,而与反应的途径无关
6.未来新能源的特点是资源丰富,在使用时对环境无污染或污染很小,且可以再生。下列属于未来新能
源标准的是
①天然气 ②煤 ③潮汐能 ④石油 ⑤太阳能 ⑥生物质能 ⑦风能 ⑧氢能
A.①②③④ B.①⑤⑥⑦ C.③⑤⑥⑦⑧ D.③④⑤⑥⑦⑧
7.下列属于吸热反应的是
A.
B.破坏反应物中的化学键所需能量大于破坏生成物中的化学键所需能量的反应
C.液态水汽化
D.氢氧化钠溶液与盐酸的中和反应
8.下列说法中正确的是( )
A.已知2CO(g)+O(g)=2CO (g) △H= -566.0kJ•mol﹣1则该反应的反应热为566.0kJ•mol-1
2 2
B.甲烷的燃烧热△H= -890kJ•mol-1,则甲烷燃烧的热化学方程式为CH(g)+O(g)=CO (g)+2HO(g) △H=
4 2 2 2
-890kJ•mol-1
C.在一定条件下将1mol SO 和0.5mol O 置于密闭容器中充分反应,放出热量79.2kJ,则反应的热化学方
2 2
程式为2SO (g)+O(g) 2SO (g) △H= -158.4kJ•mol-1
2 2 3
D.已知稀溶液中,H+(aq)+OH-(aq)=H O(l) △H= -57.3kJ•mol-1,但稀醋酸与稀氢氧化钠溶液反应生成1mol
2
水时放出的热量小于57.3kJ
9.下列热化学方程式正确的是(ΔH的绝对值均正确)( )
A.Hg+1/2O =HgO ΔH=-90.7 kJ·mol-1(反应热)
2
B.P(s)+3/2Cl (g)=PCl (g) ΔH=-306 kJ·mol-1(反应热)
2 3
C.CHOH(l)+3/2O (g)=CO (g)+2HO(g) ΔH=-725.76 kJ·mol-1(燃烧热)
3 2 2 2
D.NaOH(aq)+HNO(aq)=NaNO(aq)+HO(l) ΔH=+57.3 kJ·mol-1(中和热)
3 3 2
10.下表是 、 时一些有机物的摩尔燃烧焓。根据表格分析,下列表述正确的是
化合物 摩尔燃烧焓/( ) 化合物 摩尔燃烧焓/( )甲烷 正丁烷
乙烷 异丁烷
丙烷 乙戊烷
A.丙烷的摩尔燃烧焓为
B.稳定性:正丁烷>异丁烷
C.乙烷燃烧的热化学方程式为
D. 、 下,相同物质的量的气态烷烃 中,n越大,完全氧化生成 和 时
放出的热量越多
11.下列说法不正确的是
A.需要加热才能发生的反应不一定是吸热反应
B.任何放热反应在常温条件下一定能发生
C.反应物和生成物所具有的总能量的相对大小决定了反应是放热还是吸热
D.吸热反应在一定条件下(如常温、加热等)也能发生
12.下列说法或表示法正确的是( )
A.CO(g)的燃烧热是283.0kJ·mol-1,则表示CO(g)的燃烧热的热化学方程式为:2CO(g)+O(g)=2CO(g)
2 2
△H=-283.0kJ·mol-1
B.当反应物的总能量比生成物的总能量高时,为吸热反应;当生成物的总能量比反应物的总能量高时,
则为放热反应
C.在稀溶液中:H+(aq)+OH-(aq)=HO(l) △H=-57.3kJ·mol-1,若将含0.5molHSO 的浓硫酸与含
2 2 4
lmolNaOH的溶液混合,放出的热量等于57.3kJ
D.在101kPa时,2gH 完全燃烧生成液态水,放出285.8kJ热量,氢气燃烧的热化学方程式表示为2H(g)
2 2
+O(g)=2HO(l) △H=-571.6kJ·mol-1
2 2
13.下列反应属于吸热反应的是
A.煅烧石灰石 B.炸药爆炸
C.酸与碱的中和反应 D.生石灰与水反应
14.在25℃、 的条件下, 液态甲醇( )完全燃烧生成 和液态水时放热 ,下
列热化学方程式正确的是A.
B.
C.
D.
15.下列依据热化学方程式得出的结论正确的是
选项 热化学方程式 结论
A 2H(g)+O(g)=2HO(g) △H=—483.6 kJ/mol H 的燃烧热为241.8 kJ/mol
2 2 2 2
含1mol NaOH的稀溶液与浓HSO 完
B OH—(aq)+H+(aq)= HO(g) △H=—57.3 kJ/mol 2 4
2 全中和,放出热量小于57.3 kJ
2C(s)+2O(g)=2CO (g) △H=—a kJ/mol
2 2
C b<a
2C(s)+O(g)=2CO(g) △H=—b kJ/mol
2
D C(石墨,s)=C(金刚石,s) △H=+1.5 kJ/mol 金刚石比石墨稳定
A.A B.B C.C D.D
16.N 和H 在催化剂表面合成氨的微观历程及能量变化的示意图如图所示,用 、 、 分别表示N、
2 2 2
H、NH ,下列说法正确的是
2 3
A.使用催化剂时,合成氨的反应放出的热量减少
B.在该过程中,N、H 断键形成 N 原子和 H 原子
2 2
C.在该过程中,N原子和H原子形成了含有非极性键的NH
3
D.合成氨反应中,反应物断键吸收的能量大于生成物形成新键释放的能量
17.下列关于反应2H+O=2HO说法正确的是()
2 2 2
A.断开H-H键放出能量B.形成O-H键吸收能量
C.反应物的总能量大于生成物的总能量
D.反应物的总能量小于生成物的总能量
二、综合题(共5题)
18.100 g炭粉燃烧所得气体中,CO占 体积、CO 占 体积,且
2
C(s)+ O(g)=CO(g) ΔH=-110.35 kJ·mol-1
2
CO(g)+ O(g)=CO (g) ΔH=-282.57 kJ·mol-1
2 2
C(s)+O(g)=CO (g) ΔH=-392.92 kJ·mol-1
2 2
与这些炭完全燃烧相比较,损失的热量是________。
19.A~I分别表示中学化学中常见的一种物质,它们之间相互关系如图所示(部分反应物、生成物没有列
出)。且已知G为主族元素的固态氧化物,F是红褐色难溶于水的沉淀,A、B、C、D、E、F六种物质中均
含同一种元素。
请填写下列空白:
(1)A、B、C、D、E、F六种物质中所含同一种元素是___________(填元素符号)。
(2)写出C、E、G物质的化学式:C___________,E ___________,G___________。
(3)写出④、⑥反应的化学方程式:反应④:___________;反应⑥:___________。
(4)从能量变化的角度看,①②③反应中属于吸热反应的是___________(填序号)。
20.随原子序数的递增,八种短周期元素(用英文小写字母表示)原子半径的相对大小、最高正价或最低
负价的变化如下图所示。根据判断出的元素回答问题:
(1)f在元素周期表的位置是_________________。
(2)比较d、e简单离子的半径大小(用化学式表示,下同)_____________;比较g、h的最高价氧化物
对应的水化物的酸性强弱是______________。
(3)任选上述元素组成一种四原子共价化合物,写出其电子式________________。
(4)已知1mol e的单质在足量d 中燃烧,恢复至室温,放出255.5kJ热量,写出该反应的热化学方程式:
2
____________________________________________。
(5)由元素f、h形成的物质X与由元素x、z形成的化合物Y可发生以下反应:
①写出X溶液与Y溶液反应的离子方程式____________________________________;
②写出工业上制备f的单质的化学方程式____________________________________。
21.硫酸铵一种优良的氮肥,适用于各种土壤和作物,硫酸铵还可用于纺织、皮革、医药等方面。某化工
厂以硫酸钙为原料制备硫酸铵,其工艺流程如下:
(1)X为_____,操作a名称为_______。
(2)煅烧CaCO 生成生石灰和CO 的反应为_____反应(填“吸热”或“放热”),欲加快该反应速率可采取的
3 2
措施为______(写出一种即可)。(3)上述流程中,可以循环使用的物质有______(写化学式)。
(4)从滤液中获得(NH )SO 晶体,必要的操作步骤是蒸发浓缩,______,过滤等。
4 2 4
(5)写出利用该流程制备(NH )SO 的总化学方程_________。
4 2 4
22.热能是人类论今为止利用的主要能源之一。
(1)下列变化属于放热反应的是______(填序号)。
a.生石灰溶于水 b,浓硫酸稀释 c. 溶于水
d.金属钠溶于水 e.碳酸钠溶于水 f.食物在人体内的缓慢氧化
(2)如图是某一反应的能量变化示意图。
①图中所示反应为___________(填“吸热”或“放热”)反应,逆反应的活化能为_____________。
②图示反应的热化学方程式为__________________________。
(3)已知 ,则反应 的 ____
。参考答案
1.C
【详解】
A.反应物能量总和大于生成物能量总和,当反应发生时,剩余能量以热能形式释放出来,
所以是放热反应,不符题意;
B.酸碱中和反应是放热反应,不符题意;
C.碳酸钙受热分解属于吸热反应,符合题意;
D.所有燃烧均是放热反应,不符题意;
综上,本题选C。
2.D
【分析】
常见的放热反应有:所有的物质燃烧、所有金属与酸或与水、所有中和反应、绝大多数化
合反应、铝热反应;常见的吸热反应有:绝大数分解反应、个别的化合反应(如C和
CO)、工业制水煤气、碳(一氧化碳、氢气)还原金属氧化物、某些复分解(如铵盐和强碱),
2
以此来解答。
【详解】
A. 煤的燃烧,属于放热反应,故A错误;
B. 生石灰溶于水生成氢氧化钙,属于放热反应,故B错误;
C. 镁与稀盐酸的反应生成氯化镁和氢气,属于放热反应,故C错误;
D. Ba(OH) ·8H O与NH Cl晶体混合反应生成氯化钡、氨气和水,是吸热反应,故D正
2 2 4
确;
故选D。
3.B
【详解】
A.化学反应一定有能量变化,根据能量守恒,反应物总能量与生成物总能量一定不等,
故A错误;
B.根据盖斯定理,反应回到原点,热效应为0,故B正确;
C.吸热反应和放热反应,与反应条件无关,故C错误;
D.天然气属于化石能源,不可再生,故D错误;
答案选B。
4.D
【分析】
图中信息显示,反应物的总能量低于生成物的总能量,所以反应为吸热反应。
【详解】
A. 木炭燃烧属于燃烧反应,燃烧反应都是放热反应,A不合题意;
B. 镁与盐酸反应是金属单质与酸的置换反应,属于放热反应,B不合题意;C. 氢氧化钠溶液与盐酸反应是酸碱中和反应,属于放热反应,C不合题意;
D. NHCl晶体与Ba(OH) ·8H O晶体反应,需要吸收热量,为吸热反应,D符合题意;
4 2 2
故选D。
5.D
【详解】
A. △H﹣T△S<0的反应才能自发进行,一个反应放热(△H<0),且△S>0,任何温度下
都自发,如果△H<0,而熵减,低温下才能自发,故A错误;
B. 胆矾加热分解为硫酸铜和水,这是一个分解反应,是吸热的,故B错误;
C. 燃烧除化学能转化为热能外还有光能,故C错误;
D. 反应热等于生成物与反应物能量的差值,反应体系的始态和终态确定,即反应物和生成
物的能量确定,那反应热就确定,与反应的途径与条件没有关系,故D正确。
答案选D。
6.C
【详解】
煤、石油、天然气是化石燃料,能引起严重的空气污染,不是新能源;太阳能、核能、地
热能、潮汐能、风能、氢能、生物质能等都是新能源,综合以上分析,③⑤⑥⑦⑧符合题
意,故选C。
7.B
【详解】
A.葡萄糖被氧化生成 和 的反应为放热反应,不符合题意;
B.破坏反应物中的化学键吸收的能量大于形成生成物中的化学键释放的能量,为吸热反
应,符合题意;
C.液态水汽化不属于化学反应,不符合题意;
D.中和反应为放热反应,不符合题意;
故选B。
8.D
【详解】
A、反应热是有符号的,即该反应的反应热为-566.0kJ·mol-1,故A错误;
B、甲烷的燃烧热,即1mol甲烷燃烧生成CO 和液态水,题中所给反应中的水为气态,即
2
△H>-890kJ·mol-1,故B错误;
C、SO 和氧气反应是可逆反应,本题没有说明有多少SO 或O 消耗,或者是SO 的生成,
2 2 2 3
因此无法计算出该反应的△H,故C错误;
D、醋酸为弱酸,其电离是吸热过程,因此稀醋酸与稀氢氧化钠反应生成1mol水时放出的
热量小于57.3kJ,故D正确;
答案选D。
9.B【详解】
A、选项中的方程式未标注物质聚集状态,不符合热化学方程式书写原则,选项A错误;
B、P(s)+3/2Cl (g)=PCl (g) ΔH=-306 kJ·mol-1(反应热) 符合热化学方程式书写原则,选
2 3
项B正确;
C、燃烧热是1mol纯物质完全燃烧生成稳定的氧化物所放出的热量,水应该为液态水,选
项C错误;
D、酸碱中和反应是放热反应,正确的热化学方程式为NaOH(aq)+HCl(aq)=NaCl(aq)+
HO(l) ΔH=-57.3 kJ·mol-1,选项D错误;
2
答案选B。
10.D
【详解】
A.丙烷的摩尔燃烧焓为 ,A错误;
B.正丁烷和异丁烷互为同分异构体,由表中数据可知,等物质的量的两种物质完全燃烧生
成 和 时,正丁烷放出的热量多,说明正丁烷的能量高,所以稳定性:正丁
烷<异丁烷,B错误;
C.乙烷的摩尔燃烧焓是 ,则乙烷燃烧的热化学方程式可表示为
,C错误;
D.根据表中气态烷烃的摩尔燃烧焓的规律可知, 、 下,相同物质的量的气态烷
烃 中,n越大,分子中含有的C、H原子数越多,物质完全氧化生成 和
时放出的热量越多,D正确;
答案选D。
11.B
【详解】
A.有些放热反应,加热才能发生反应,如铝热反应,需要“高温”条件,A正确;
B.氢气在氧气中燃烧为放热反应;在常温条件下,H 与O 能稳定存在,只有在点燃条件
2 2
下才能发生反应,B不正确;
C.生成物与反应物所具有的总能量的差值为反应的△H,△H<0放热,△H>0吸热,C
正确;
D.氢氧化钡晶体与氯化铵混合,常温下反应生成氯化钡和一水合氨,该反应为吸热反应;
碳与水蒸气制水煤气的反应为吸热反应,在高温条件下也能发生,D正确;
故选B。
12.D
【详解】
A. 燃烧热是1mol可燃物完全燃烧放出的能量,CO(g)的燃烧热是283.0kJ·mol-1,则表示CO(g)的燃烧热的热化学方程式为: CO(g)+ O(g)=CO(g) △H=-283.0kJ·mol-1,
2 2
故A错误;
B. 当反应物的总能量比生成物的总能量高时,为放热反应;当生成物的总能量比反应物的
总能量高时,则为吸热反应,故B错误;
C. 在稀溶液中:H+(aq)+OH-(aq)=HO(l) △H=-57.3kJ·mol-1,浓硫酸稀释放热,
2
所以将含0.5molHSO 的浓硫酸与含lmolNaOH的溶液混合,放出的热量大于57.3kJ,故C
2 4
错误;
D. 2gH 的物质的量是1mol,完全燃烧生成液态水,放出285.8kJ热量,表示氢气燃烧的热
2
化学方程式为2H(g)+O(g)=2HO(l) △H=-571.6kJ·mol-1,故D正确;
2 2 2
13.A
【详解】
A.石灰石的主要成分是碳酸钙,碳酸钙高温下分解生成氧化钙和二氧化碳,是吸热反应,
故A正确;
B.炸药爆炸是放热反应,故B错误;
C.中和反应为放热反应,故C错误;
D.生石灰与水的反应是放热反应,故D错误;
故选:A。
14.B
【详解】
在25℃、 的条件下, 液态甲醇( )完全燃烧生成 和液态水时放热
,则 完全燃烧生成 和液态水时放出的热为
,则 完全燃烧生成 和液态水时放出
的热,该反应是放热反应, 为负值,综上所述B符合题意,故选B;
答案选B。
15.C
【详解】
A. 燃烧热是指1mol可燃物完全燃烧生成稳定的氧化物时放出的热量,H 转化为液态水,
2
H 的燃烧热应为241.8kJ/mol,故A错误;
2
B. 浓硫酸溶解于水的过程放热,则用浓硫酸与NaOH溶液反应生成1mol水,放出的热量
大于57.3kJ,故B错误;
C. 2mol碳单质,完全燃烧时放出热量更多,故有a>b,故C正确;
D. 石墨转化为金刚石吸热,说明石墨的能量低于金刚石,而物质能量越低越稳定,故石墨
比金刚石更稳定,故D错误;
答案选C。
16.B【详解】
A.催化剂不改变反应热,且平衡不移动,不能改变反应放出的热量,故A错误;
B.在②→③过程,存在H-H、N≡N键的断裂,形成 N 原子和 H 原子,故B正确;
C.NH 含有N-H键,为极性键,故C错误;
3
D.合成氨为放热反应。则反应物断键吸收能量小于生成物形成新键释放的能量,故D错
误;
故答案为B。
17.C
【详解】
A.断开H-H键吸收能量,A说法错误;
B.形成O-H键释放能量,B说法错误;
C.该反应为放热反应,则反应物的总能量大于生成物的总能量,C说法正确;
D.该反应为放热反应,反应物的总能量大于生成物的总能量,D说法错误;
答案为C。
18.784.92 kJ
【分析】
碳不完全燃烧损失的热量为生成的一氧化碳燃烧放出的热量,根据碳原子守恒计算出一氧
化碳的物质的量,再根据一氧化碳燃烧的热化学方程式计算。
【详解】
100g碳的物质的量为 = mol,则CO的物质的量为 mol× = mol,由于
CO(g)+ O(g)=CO (g)△H=-282.57kJ/mol,所以 molCO燃烧放出的热量为282.57kJ/
2 2
mol× mol=784.92kJ,即100g碳不完全燃烧生成 molCO损失的热量为784.92kJ。
19.
(1)Fe
(2) FeCl Fe(OH) Al O
2 2 2 3
(3) 2Al+2NaOH+2HO=2NaAlO +3H↑ 4Fe(OH) +O+2HO=4Fe(OH)
2 2 2 2 2 2 3
(4)③
【分析】
G为主族元素的固态氧化物,在电解条件下生成I和H,能与NaOH溶液反应,说明G为
Al O,与NaOH反应生成NaAlO ,而I也能与NaOH反应生成NaAlO ,则I为Al, H为
2 3 2 2
O, C、D分别和碱反应生成E、F,则说明E、F都为氢氧化物、F是红褐色难溶于水的
2
沉淀,E能转化为F,应E为Fe(OH) →Fe(OH) 的转化,所以E为Fe(OH) ,F为
2 3 2
Fe(OH) ,则C为FeCl ,D为FeCl ,B为Fe O,与Al在高温条件下发生铝热反应生成
3 2 3 3 4
A,即Fe,据此解答。(1)
由分析可知,A、B、C、D、E、F六种物质中所含同一种元素是Fe,故答案为:Fe。
(2)
由分析可知,C物质的化学式 为FeCl ,E物质的化学式为 Fe(OH) ,G物质的化学式为
2 2
Al O,故答案为:FeCl 、Fe(OH) 、Al O。
2 3 2 2 2 3
(3)
反应④为Al与NaOH反应生成NaAlO ,化学方程式为:2Al+2NaOH+2HO=2NaAlO +
2 2 2
3H↑,反应⑥为Fe(OH) →Fe(OH) 的转化,反应化学方程式为4Fe(OH) +O+
2 2 3 2 2
2HO=4Fe(OH) ,故答案为:2Al+2NaOH+2HO=2NaAlO +3H↑、4Fe(OH) +O+
2 3 2 2 2 2 2
2HO=4Fe(OH) 。
2 3
(4)
大多数的分解反应属于吸热反应,符合条件的为③,故答案为:③。
20.第三周期第ⅢA族 O2->Na+ HClO >HSO (或
4 2 4
,答案合理即可) 2Na(s)+O (g)=NaO(s) △H=-511kJ·mol-1 Al3++
2 2 2
3NH ·H O=Al(OH) ↓+3NH + (或Al3++3NH +3HO=Al(OH) ↓+3NH +) 2Al O(熔
3 2 3 4 3 2 3 4 2 3
融) 4Al+3O↑
2
【分析】
根据八种元素的最高正价或最低负价分析,x、y、z、d、e、f、g、h依次处于第IA族、第
IVA族、第VA族、第VIA族、第IA族、第IIIA族、第VIA族、第VIIA族,结合原子序
数和原子半径的图像,x、y、z、d、e、f、g、h依次为H、C、N、O、Na、Al、S、Cl元
素。根据元素周期表、元素周期律和相关化学用语作答。
【详解】
根据八种元素的最高正价或最低负价分析,x、y、z、d、e、f、g、h依次处于第IA族、第
IVA族、第VA族、第VIA族、第IA族、第IIIA族、第VIA族、第VIIA族,结合原子序
数和原子半径的图像,x、y、z、d、e、f、g、h依次为H、C、N、O、Na、Al、S、Cl元
素。
(1)f为Al元素,Al在元素周期表的位置是第三周期第IIIA族。
(2)d、e的简单离子依次为O2-、Na+,O2-、Na+具有相同的电子层结构,核电荷数:O2-
r(Na+)。根据“同周期从左到右元素的非金属性逐渐增强,
最高价氧化物对应水化物的酸性逐渐增强”,非金属性:SH SO 。
4 2 4
(3)上述元素组成的常见四原子共价化合物有:C H、NH 、HO 等,它们的电子式依次
2 2 3 2 2
为 、 、 。(4)Na(s)在O(g)中燃烧生成NaO(s),反应的热化学方程式为Na(s)+ O
2 2 2 2
(g)= NaO(s)ΔH=-255.5kJ/mol(或2Na(s)+O (g)=Na O(s)ΔH=-511kJ/
2 2 2 2 2
mol)。
(5)由f、h组成的物质X为AlCl ,由x、z形成的化合物Y为NH ;X与Y在水溶液中
3 3
反应生成M和Z,M是仅含非金属元素的盐,M为NH Cl,Z为Al(OH),Al(OH)
4 3 3
受热分解生成的N为Al O,电解熔融Al O 生成Al和O。
2 3 2 3 2
①X溶液与Y溶液反应的化学方程式为:AlCl +3NH+3H O=Al(OH)↓+3NHCl(或
3 3 2 3 4
AlCl +3NH·H O=Al(OH)↓+3NHCl),反应的离子方程式为:Al3++3NH+3H O=Al
3 3 2 3 4 3 2
(OH)↓+3NH+(或Al3++3NH·H O=Al(OH)↓+3NH+)。
3 4 3 2 3 4
②工业上电解熔融Al O 制备Al,工业上制备Al的化学方程式为:2Al O(熔融)
2 3 2 3
4Al+3O ↑。
2
21.CO 或二氧化碳 过滤 吸热 粉碎石灰石或升高温度 NH ,CO 冷却
2 3 2
结晶或降温结晶 CaSO + 2NH + CO + H O = CaCO + (NH )SO
4 3 2 2 3 4 2 4
【分析】
CaSO 浊液中先通入NH 、后通入X生成CaCO ,根据碳元素守恒,可知X是CO,根据
4 3 3 2
操作a后有滤液和CaCO 沉淀,可知操作a是过滤,此时滤液的主要成分是(NH )SO ,滤
3 4 2 4
液通过提纯操作得到(NH )SO 和母液,碳酸钙灼烧后得到CaO和CO,CO 可以重复利用
4 2 4 2 2
通入A中,CaO与母液反应生成NH ,也可以重复利用通入CaSO 浊液中。
3 4
【详解】
(1)由分析可X为CO,操作a名称为过滤,故答案为:CO 或二氧化碳;过滤;
2 2
(2)煅烧CaCO 生成生石灰和CO 的反应为吸热反应,欲加快该反应速率可采取的措施有:
3 2
粉碎石灰石或者升高温度,故答案为:吸热;粉碎石灰石或者升高温度
(3)由分析可知,上述流程中,可以循环使用的物质有:NH ,CO;
3 2
(4)从滤液中获得(NH )SO 晶体,必要的操作步骤是蒸发浓缩,冷却结晶或降温结晶,过滤、
4 2 4
洗涤等,故答案为:冷却结晶或降温结晶;
(5)根据流程图反应物有CaSO 、NH 、CO ,生成物有CaCO 、(NH )SO ,再根据元素
4 3 2 3 4 2 4
守恒,反应物中有HO,配平即得化学方程式:CaSO + 2NH + CO + H O = CaCO +
2 4 3 2 2 3
(NH )SO ,故答案为:CaSO + 2NH + CO + H O = CaCO + (NH )SO 。
4 2 4 4 3 2 2 3 4 2 4
22.adf 放热
【分析】
(1)放热反应为化学反应, ;
(2)由能量变化示意图可知反应物的能量高于生成物,反应放热,逆反应的活化能指生成
物总能量至能量最高值所需能量;(3)由盖斯定律计算反应热。
【详解】
(1)a.生石灰溶于水, 为放热反应,故a选;
b,浓硫酸稀释,为物理变化,不属于放热反应,故b不选;
c. 溶于水,为物理变化,且变化吸热,故c不选;
d.金属钠溶于水, 为放热反应,故d选;
e.碳酸钠溶于水,为物理变化,不属于放热反应,故e不选;
f.食物在人体内的缓慢氧化,为放热反应,故f选。故答案选:adf;
(2)由能量变化示意图可知反应物的能量高于生成物,反应放热;逆反应的活化能为
;图示反应的热化学方程式为
,故答案为:放热; ;
;
(3)由(2)中 和
根据盖斯定律可知
,故答案为: 。