文档内容
第2讲 氯及其化合物 卤素
[考纲要求]
1.掌握氯单质及其重要化合物的主要性质及应用。2.掌握氯单质及其重要化合物对环
境质量的影响。3.掌握氯气的实验室制法(包括所用试剂、仪器、反应原理和收集方法)。
4.了解卤族元素单质及其重要化合物的主要性质及应用。
考点一 氯及其重要化合物
1 知识梳理
1.氯气的物理性质
2.氯气的化学性质
(1)与金属反应。
① 与 铁 反 应 :
________________________________________________________________________。
② 与 铜 反 应 :
________________________________________________________________________。
(2)与非金属反应。
与 H 反 应 :
2
________________________________________________________________________,(3)与水反应。
离 子 方 程 式 为
________________________________________________________________________。
(4)与碱反应:与NaOH溶液反应。
离 子 方 程 式 为
________________________________________________________________________。
(5)与还原性物质反应。
① 与 碘 化 钾 溶 液 反 应 :
________________________________________________________________________。
② 与 SO 水 溶 液 反 应 :
2
________________________________________________________________________
________________________________________________________________________。
③与FeCl 溶液反应:
2
离 子 方 程 式 为
________________________________________________________________________。
3.氯的重要化合物
(1)次氯酸
(2)漂白粉的成份与性质
[判断] (正确的打“√”,错误的打“×”)
(1)氯气的水溶液可以导电,说明氯气是电解质( )
(2)Cl 通入水中的离子方程式为Cl+HO===2H++Cl-+ClO-( )
2 2 2
(3)Cl 具有很强的氧化性,在化学反应中只能作氧化剂( )
2(4)标准状况下,11.2 L Cl 与水充分反应转移电子数为0.5N( )
2 A
(5)“84”消毒液的消毒原理与HO 的相同,都是利用强氧化性( )
2 2
(6)次氯酸是酸性比碳酸强的弱酸( )
(7)新制取的漂白粉是纯净物( )
(8)漂白粉和明矾都常用于自来水的处理,二者的作用原理是相同的( )
[提醒]
氯水中的微粒与平衡
1.组成微粒——“三分子”“四离子”。
2.三个平衡。
Cl+HO HClO+HCl、HClO H++ClO-、HO H++OH-。
2 2 ⇌ ⇌ 2 ⇌
2 对点速练
练点一 氯气和氯水
1.下列说法错误的是( )
A.氯气做水的杀菌消毒剂
B.氯气能使湿润的淀粉碘化钾试纸变蓝,说明Cl 具有氧化性
2
C.氯气溶于水的离子方程式为Cl+HO 2H++Cl-+ClO-
2 2 ⇌
D.氯气与NaOH溶液反应,Cl 既是氧化剂又是还原剂
2
2.下列关于氯水的说法正确的是( )
A.向氯水中通入少量二氧化硫,氯水的漂白性增强
B.氯水中加入NaCl固体,对溶液的pH无影响
C.常温下,pH=2的氯水中:c(Cl-)+c(ClO-)+c(OH-)=0.01 mol·L-1
D.向氯水中滴加少量NaHCO 溶液的离子反应方程式为Cl +2HCO− ===2CO↑+Cl-
3 2 3 2
+ClO-+HO
2
3.新制饱和氯水具有较强的漂白性,试分析改变下列条件能否增强氯水的漂白性。
( 1 ) 再 通 入 少 量 氯 气 , 原 因 为
________________________________________________________________________________________________________________________________________________。
( 2 ) 通 入 少 量 SO , 原 因 为
2
________________________________________________________________________
________________________________________________________________________。
( 3 ) 加 入 少 量 CaCO 固 体 , 原 因 为
3
________________________________________________________________________
________________________________________________________________________。
( 4 ) 加 入 少 量 NaCO 粉 末 , 原 因 为
2 3
________________________________________________________________________
________________________________________________________________________。
练后归纳
氯水性质的多样性
新制氯水的多种成分决定了它具有多重性质,在不同的化学反应中,氯水中参与反应
的微粒不同。
练点二 氯的常见化合物
4.下列有关NaClO和NaCl混合溶液的叙述正确的是( )
A.该溶液中,NH+ 、Fe2+、SO2− 、Br-可以大量共存
4 4
B.该溶液中,K+、Ag+、Fe3+、NO−
可以大量共存
3
C.向该溶液中加入少量SO 气体,反应的离子方程式为SO+3ClO-+HO===SO2− +Cl-
2 2 2 4
+2HClOD.向该溶液中加入浓盐酸,每产生22.4 L Cl,转移电子数目约为6.02×1023
2
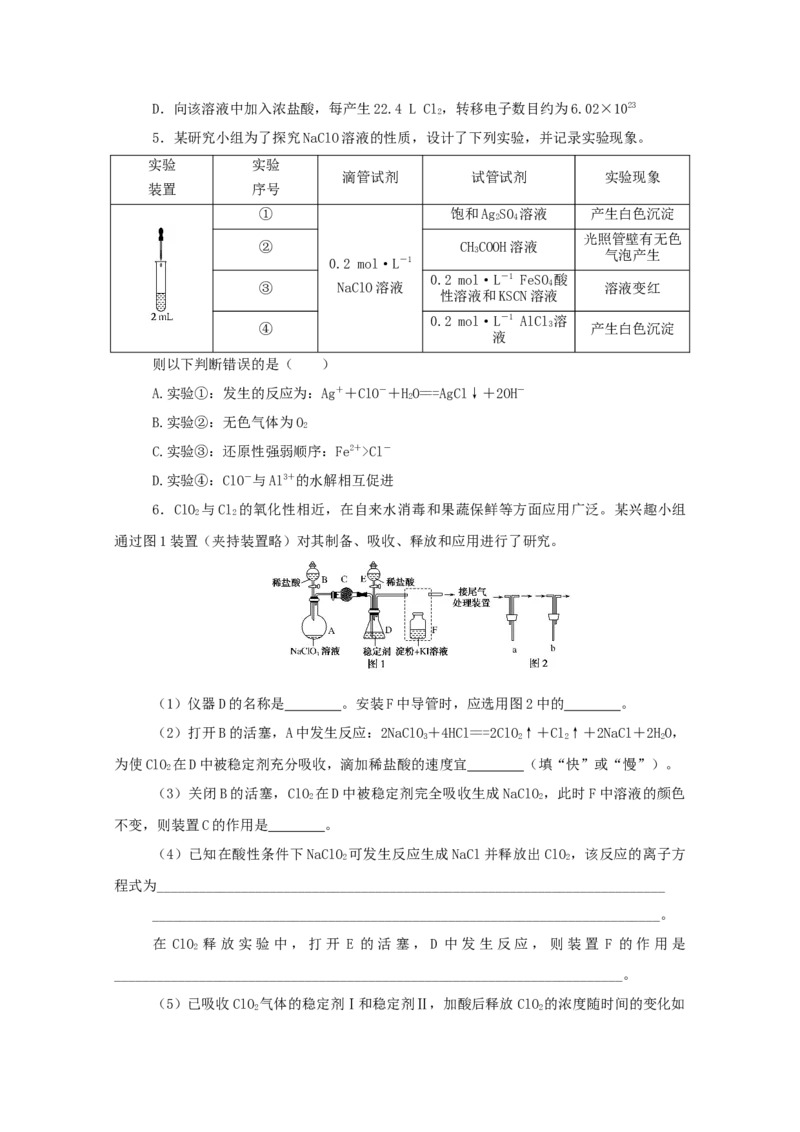
5.某研究小组为了探究NaClO溶液的性质,设计了下列实验,并记录实验现象。
实验 实验
滴管试剂 试管试剂 实验现象
装置 序号
① 饱和AgSO 溶液 产生白色沉淀
2 4
光照管壁有无色
② CHCOOH溶液
3 气泡产生
0.2 mol·L-1
0.2 mol·L-1 FeSO 酸
③ NaClO溶液 4 溶液变红
性溶液和KSCN溶液
0.2 mol·L-1 AlCl 溶
④ 3 产生白色沉淀
液
则以下判断错误的是( )
A.实验①:发生的反应为:Ag++ClO-+HO===AgCl↓+2OH-
2
B.实验②:无色气体为O
2
C.实验③:还原性强弱顺序:Fe2+>Cl-
D.实验④:ClO-与Al3+的水解相互促进
6.ClO 与Cl 的氧化性相近,在自来水消毒和果蔬保鲜等方面应用广泛。某兴趣小组
2 2
通过图1装置(夹持装置略)对其制备、吸收、释放和应用进行了研究。
(1)仪器D的名称是 。安装F中导管时,应选用图2中的 。
(2)打开B的活塞,A中发生反应:2NaClO +4HCl===2ClO↑+Cl↑+2NaCl+2HO,
3 2 2 2
为使ClO 在D中被稳定剂充分吸收,滴加稀盐酸的速度宜 (填“快”或“慢”)。
2
(3)关闭B的活塞,ClO 在D中被稳定剂完全吸收生成NaClO ,此时F中溶液的颜色
2 2
不变,则装置C的作用是 。
(4)已知在酸性条件下NaClO 可发生反应生成NaCl并释放出ClO ,该反应的离子方
2 2
程式为________________________________________________________________________
________________________________________________________________________。
在 ClO 释放实验中,打开 E 的活塞,D 中发生反应,则装置 F 的作用是
2
________________________________________________________________________。
(5)已吸收ClO 气体的稳定剂Ⅰ和稳定剂Ⅱ,加酸后释放ClO 的浓度随时间的变化如
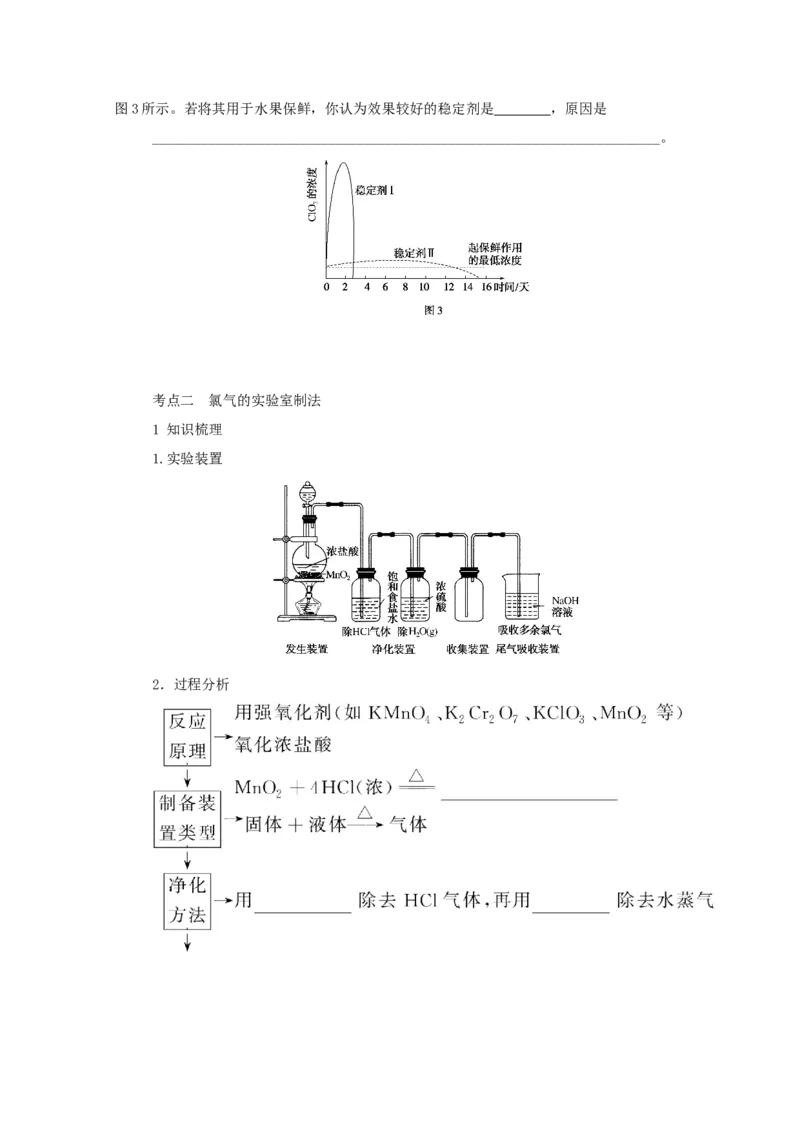
2 2图3所示。若将其用于水果保鲜,你认为效果较好的稳定剂是 ,原因是
________________________________________________________________________。
考点二 氯气的实验室制法
1 知识梳理
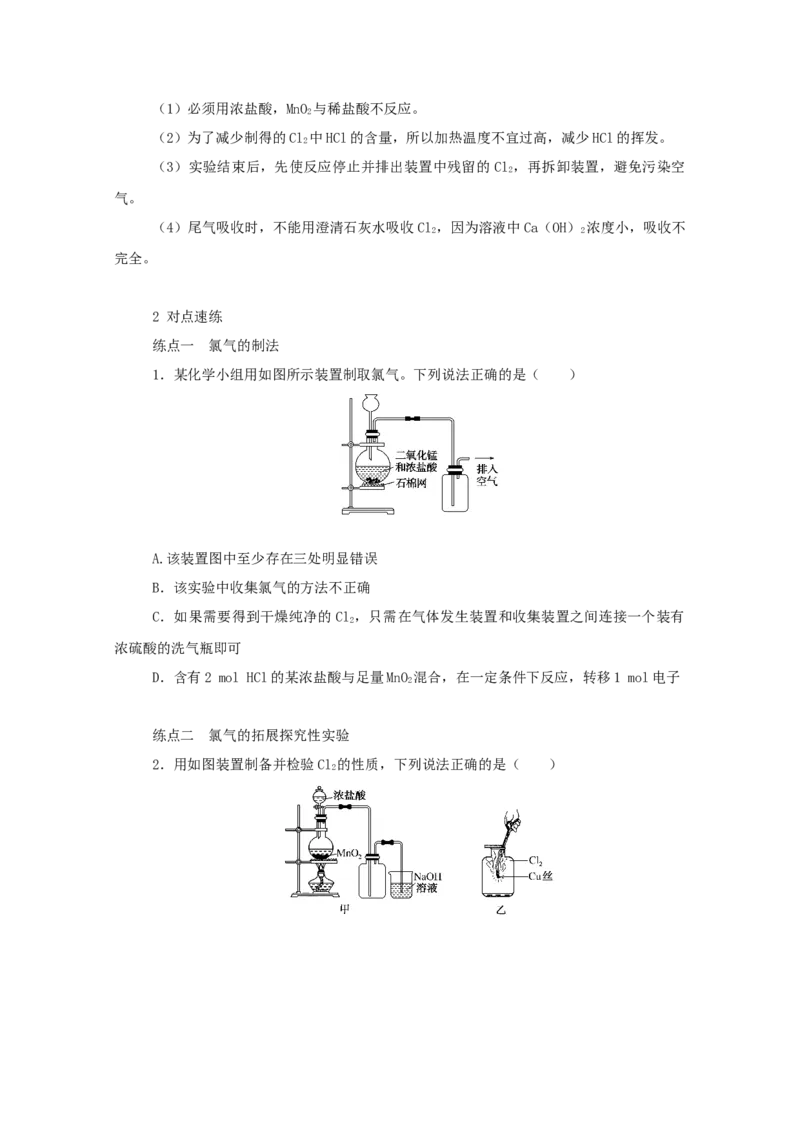
1.实验装置
2.过程分析[思考]
下图是用KMnO 与浓盐酸反应制取适量氯气的简易装置。
4
装置B、C、D的作用分别是:
B________________________________________________________________________;
C________________________________________________________________________;
D________________________________________________________________________。
[判断] (正确的打“√”,错误的打“×”)
(1)实验室用MnO 和稀盐酸共热制取少量氯气( )
2
(2)MnO 与浓盐酸反应制Cl 的离子方程式:MnO +4HCl=====Mn2++2Cl-+Cl↑+
2 2 2 2
2HO( )
2
(3)除去Cl 中少量HCl气体的方法是将混合气体依次通入盛有饱和食盐水和浓HSO
2 2 4
的洗气瓶( )
(4)氯气在饱和食盐水中的溶解度小于在纯水中的溶解度( )
(5)制氯气时,用饱和NaHCO 溶液和浓硫酸净化气体( )
3
(6)用NaOH溶液吸收多余的Cl 时,导气管不能伸到液面以下,原因是防止倒吸(
2
)
[提醒]
实验注意事项(1)必须用浓盐酸,MnO 与稀盐酸不反应。
2
(2)为了减少制得的Cl 中HCl的含量,所以加热温度不宜过高,减少HCl的挥发。
2
(3)实验结束后,先使反应停止并排出装置中残留的 Cl ,再拆卸装置,避免污染空
2
气。
(4)尾气吸收时,不能用澄清石灰水吸收Cl ,因为溶液中Ca(OH) 浓度小,吸收不
2 2
完全。
2 对点速练
练点一 氯气的制法
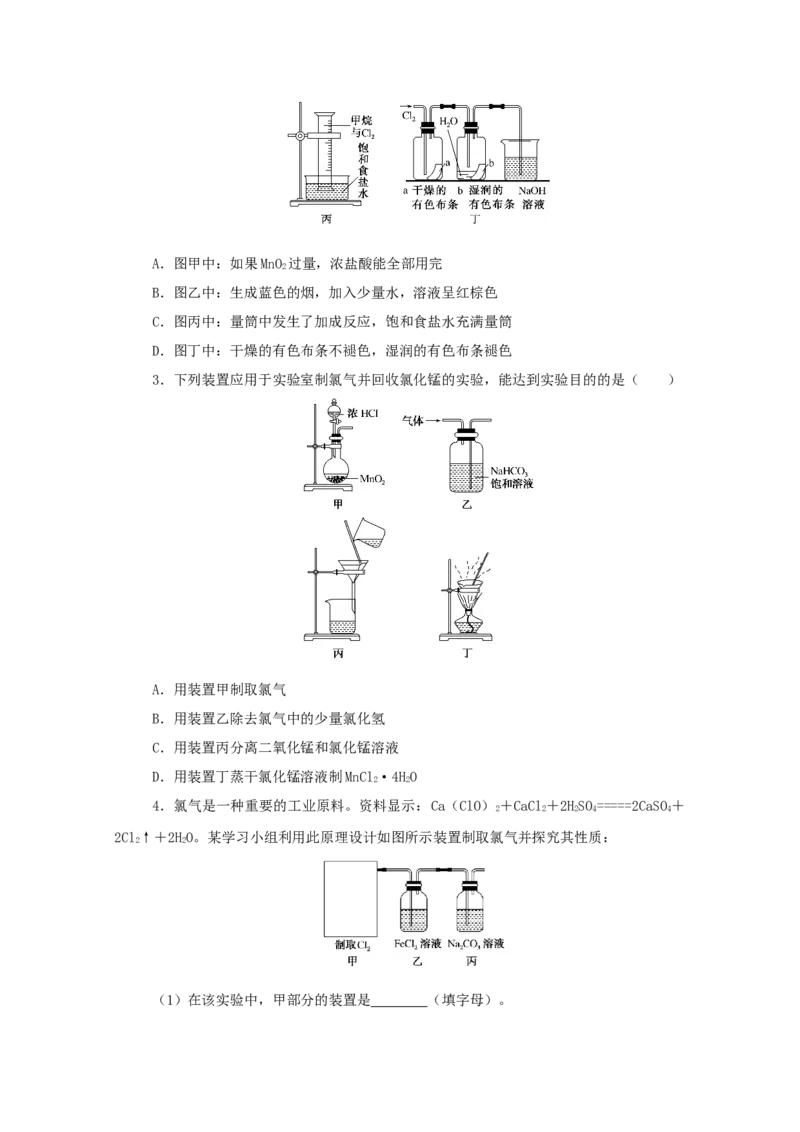
1.某化学小组用如图所示装置制取氯气。下列说法正确的是( )
A.该装置图中至少存在三处明显错误
B.该实验中收集氯气的方法不正确
C.如果需要得到干燥纯净的Cl ,只需在气体发生装置和收集装置之间连接一个装有
2
浓硫酸的洗气瓶即可
D.含有2 mol HCl的某浓盐酸与足量MnO 混合,在一定条件下反应,转移1 mol电子
2
练点二 氯气的拓展探究性实验
2.用如图装置制备并检验Cl 的性质,下列说法正确的是( )
2A.图甲中:如果MnO 过量,浓盐酸能全部用完
2
B.图乙中:生成蓝色的烟,加入少量水,溶液呈红棕色
C.图丙中:量筒中发生了加成反应,饱和食盐水充满量筒
D.图丁中:干燥的有色布条不褪色,湿润的有色布条褪色
3.下列装置应用于实验室制氯气并回收氯化锰的实验,能达到实验目的的是( )
A.用装置甲制取氯气
B.用装置乙除去氯气中的少量氯化氢
C.用装置丙分离二氧化锰和氯化锰溶液
D.用装置丁蒸干氯化锰溶液制MnCl·4HO
2 2
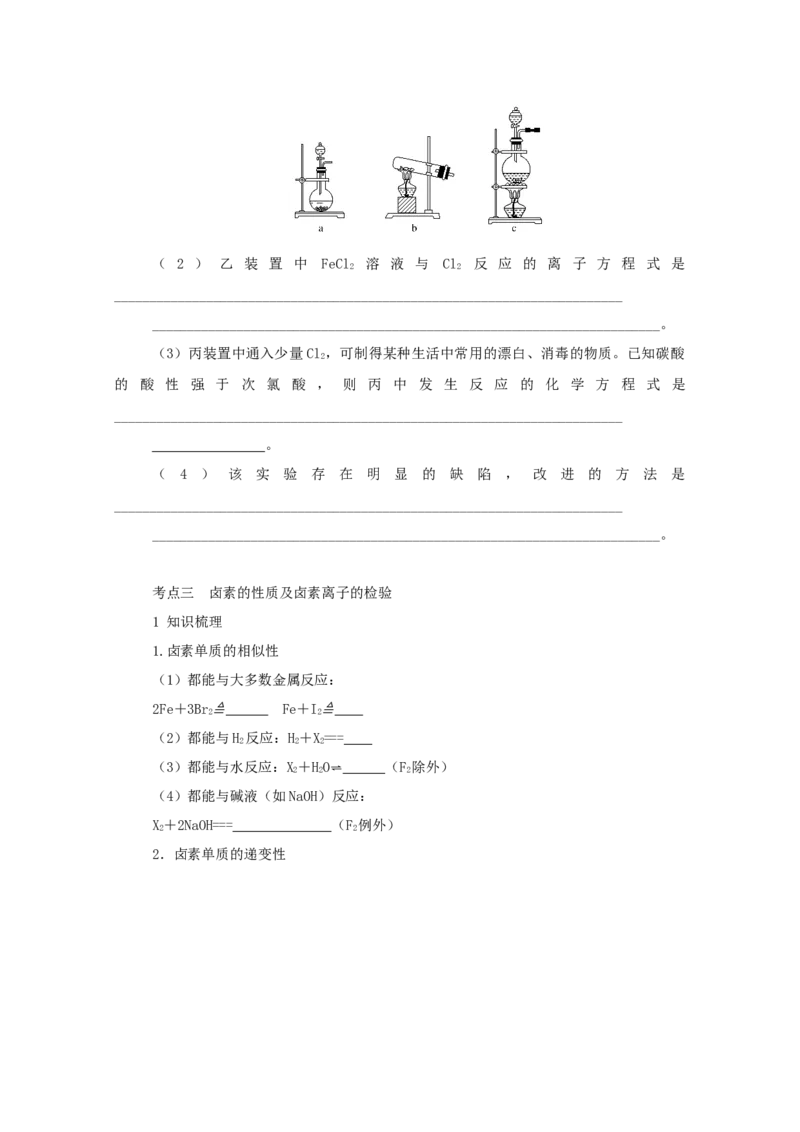
4.氯气是一种重要的工业原料。资料显示:Ca(ClO) +CaCl +2HSO=====2CaSO +
2 2 2 4 4
2Cl↑+2HO。某学习小组利用此原理设计如图所示装置制取氯气并探究其性质:
2 2
(1)在该实验中,甲部分的装置是 (填字母)。( 2 ) 乙 装 置 中 FeCl 溶 液 与 Cl 反 应 的 离 子 方 程 式 是
2 2
________________________________________________________________________
________________________________________________________________________。
(3)丙装置中通入少量Cl ,可制得某种生活中常用的漂白、消毒的物质。已知碳酸
2
的 酸 性 强 于 次 氯 酸 , 则 丙 中 发 生 反 应 的 化 学 方 程 式 是
________________________________________________________________________
。
( 4 ) 该 实 验 存 在 明 显 的 缺 陷 , 改 进 的 方 法 是
________________________________________________________________________
________________________________________________________________________。
考点三 卤素的性质及卤素离子的检验
1 知识梳理
1.卤素单质的相似性
(1)都能与大多数金属反应:
2Fe+3Br 2≜ Fe+I 2≜
(2)都能与H 反应:H+X===
2 2 2
(3)都能与水反应:X+HO (F 除外)
2 2 ⇌ 2
(4)都能与碱液(如NaOH)反应:
X+2NaOH=== (F 例外)
2 2
2.卤素单质的递变性(1)氯、溴、碘单质氧化性强弱顺序是 ;
(2)阴离子还原性由强到弱顺序是 ;
(3)Cl 能从Br-的溶液中置换出Br,离子方程式为 ;
2 2
(4)Br 能从I-的溶液中置换出I,离子方程式为 。
2 2
3.卤素离子的检验方法
(1)AgNO 溶液——沉淀法:
3
滴 加A3gNO
未知液溶液和稀硝酸生成
→
(2)氯水、萃取剂——显色法
(3)卤素单质溶于水或有机溶剂所呈现的颜色
单质 水 汽油(或苯) CCl
4
Cl 淡黄→黄绿 黄绿 黄绿
2
Br 黄→橙 橙→橙红 橙→橙红
2
I 深黄→褐 淡紫→紫红 紫→深紫
2[判断] (正确的打“√”,错误的打“×”)
(1)实验室保存液溴时要加少量水进行水封,不用橡胶塞( )
(2)向无色溶液中滴加氯水和CCl,振荡,静置,下层溶液显紫色说明原溶液中有I-
4
( )
(3)碘水中通入SO,反应的离子方程式为SO+I+HO===SO2− +2I-+2H+( )
2 2 2 2 3
(4)双氧水中加入稀HSO 和KI溶液的离子方程式为HO +2H++2I-===I +2HO(
2 4 2 2 2 2
)
(5)I-遇淀粉变蓝色( )
(6)类比Fe与Cl 的反应判断Fe与I 反应时生成FeI( )
2 2 3
(7)用AgNO 溶液可以鉴别KCl和KI( )
3
[提醒]
F、Br、I 的常用性质
2 2 2
1.Br 是常温下唯一呈液态的非金属单质;液溴易挥发且有毒,通常用水液封来保存。
2
2.I 易升华,I 遇淀粉变蓝。
2 2
3.Br 和I 都可被某些有机溶剂(如四氯化碳、苯)萃取。
2 2
4.F 不能从NaX溶液中置换出X(X代表Cl、Br、I)。
2 2
2 对点速练
练点一 卤素的性质
1.下列有关卤素的说法错误的是( )
A.从HF、HCl、HBr、HI酸性递增的事实,可推出F、Cl、Br、I的非金属性递增的规
律
B.HF、HCl、HBr、HI的热稳定性依次减弱,还原性依次增强
C.淀粉-碘化钾溶液在空气中变蓝,4I-+O+2HO===2I+4OH-
2 2 2
D.碘在碘化钾溶液中的溶解度大于在纯水中的溶解度
2.某化学小组用如图所示装置验证卤素单质氧化性的相对强弱。下列说法不正确的是
( )A.E处棉花球变成黄色,说明Cl 的氧化性比Br 强
2 2
B.F处棉花球变成蓝色,说明Br 的氧化性比I 强
2 2
C.E处发生反应的离子方程式为Cl+2Br-===2Cl-+Br
2 2
D.G装置中NaOH溶液与Cl 反应的离子方程式为2OH-+Cl===ClO-+Cl-+HO
2 2 2
3.一氯化碘(ICl)、三氯化碘(ICl)是卤素互化物,它们的性质与卤素单质相似。
3
(1)ICl 与水反应的产物可能为 (填化学式)。
3
( 2 ) ICl 在 常 温 下 与 烧 碱 溶 液 反 应 的 离 子 方 程 式 为
________________________________________________________________________
________________________________________________________________________,
该反应是否是氧化还原反应? (填“是”或“否”)。
练点二 卤化物的性质、卤素离子的检验
4.鉴别NaCl、NaBr、NaI可以选用的试剂是( )
①碘水、淀粉溶液 ②氯水、CCl ③溴水、苯 ④稀硝酸、AgNO 溶液 ⑤氯水、苯
4 3
⑥FeCl 溶液、CCl
3 4
A.①②④ B.②③⑥
C.②④⑤ D.④⑤⑥
5.下列叙述中正确的是( )
A.加碘食盐可用淀粉溶液检验其中的碘
B.某溶液加入氯水后振荡,再加入CCl 振荡,下层显示紫色,说明原溶液中一定含有
4
I-
C.某溶液中滴加AgNO 溶液和稀硝酸,产生淡黄色沉淀,说明原溶液中一定含有Br-
3
D.要除去HBr溶液中混有的单质Br,可用酒精萃取除去
2
6.实验室用如图所示装置制取溴化亚铁。D和d中均盛有液溴,E为外套电炉丝的瓷管,
e是两只耐高温的瓷皿,其中共盛有56 g细铁粉。实验开始时先将干燥、纯净的CO 气流通
2入D中,然后将铁粉加热至600 ℃~700 ℃,E管中反应开始。E中的反应为:
2Fe+3Br
2
===2FeBr
3
,2FeBr 3≜2FeBr
2
+Br
2
↑,最后将d中液溴滴入100 ℃~120 ℃的
D中,经过几小时的连续反应,在铁管的一端沉积有黄绿色鳞片状溴化亚铁80 g。
请回答:
(1)仪器d的名称 。
(2)导入的CO 不干燥,会在E中发生副反应,其含铁副产物为 ;若所得产
2
物中含此副产物,用化学方法检验。下列方案合理的是 。
A.取少量产物于试管中加入稀盐酸,再加入KSCN溶液
B.取少量产物于硬质大试管中,通入氢气,排尽空气后加热,用CuSO 检验生成的水蒸
4
气
C.用磁铁吸引,看产物能否被吸引
D.取少量产物于试管中加入蒸馏水,过滤看是否有黑色不溶物
(3)为防止污染空气,实验时应在F处连接盛有NaOH溶液的尾气吸收装置,反应的化
学 方 程 式 :
________________________________________________________________________
________________________________________________________________________。
(4)取产品10 g配制成250 mL溶液,取出25.00 mL用酸性KMnO 溶液滴定溶液中的
4
Fe2 + , 用 去 0.030 0 mol/L 酸 性 KMnO 溶 液 25.00 mL , 则 产 品 的 纯 度 为
4
________________________________________________________________________。
(5)利用除去杂质后的FeBr 可以验证Cl 、Fe3+、Br 的氧化性强弱。将你设计的实
2 2 2
验操作、预计的实验现象和实验结论(氧化性强弱)填写在下列表空格内:
实验操作 实验现象 氧化性强弱
① 溶液呈血红色 ②
③ ④ Cl>Br
2 2
本讲真题研练1.[2019·江苏卷,13]室温下进行下列实验,根据实验操作和现象所得到的结论正确
的是( )
选项 实验操作和现象 结论
向X溶液中滴加几滴新制氯水,振荡,
A X溶液中一定含有Fe2+
再加入少量KSCN溶液,溶液变为红色
向浓度均为0.05 mol·L-1的NaI、NaCl
B 混合溶液中滴加少量AgNO 溶液,有黄 K(AgI)>K(AgCl)
3 sp sp
色沉淀生成
向3 mL KI溶液中滴加几滴溴水,振
C Br 的氧化性比I 的强
荡,再滴加1 mL淀粉溶液,溶液显蓝色 2 2
用pH试纸测得:CHCOONa溶液的pH约
D 3 HNO 电离出H+的能力比CHCOOH的强
为9,NaNO 溶液的pH约为8 2 3
2
2.[高考选项组合]下列说法不正确的是( )
A.漂白粉可用于生活用水的消毒[2018·全国卷Ⅱ,7B]
B.石蕊溶液滴入氯水中,溶液变红,随后迅速褪色,不涉及氧化还原反应[2018·北京
卷,9B]
C.氯水具有较强的氧化性,可用于漂白纸张、织物等[2018·海南卷,5D]
D.清洗碘升华实验所用试管,先用酒精清洗,再用水清洗[2017·全国卷Ⅲ,9B]
3.[2016·上海卷,9]向新制氯水中加入少量下列物质,能增强溶液漂白能力的是(
)
A.碳酸钙粉末 B.稀硫酸
C.氯化钙溶液 D.二氧化硫水溶液
4.[2015·北京卷,11]某消毒液的主要成分为NaClO,还含有一定量的NaOH。下列用
来解释事实的方程式中,不合理的是(已知:饱和NaClO溶液的pH约为11)( )
A.该消毒液可用NaOH溶液吸收Cl 制备:Cl+2OH-===ClO-+Cl-+HO
2 2 2
B.该消毒液的pH约为12:ClO-+HO HClO+OH-
2 ⇌
C.该消毒液与洁厕灵(主要成分为 HCl)混用,产生有毒 Cl :2H++Cl-+ClO-
2
===Cl↑+HO
2 2
D.该消毒液加白醋生成HClO,可增强漂白作用:CHCOOH+ClO-===HClO+CHCOO-
3 3
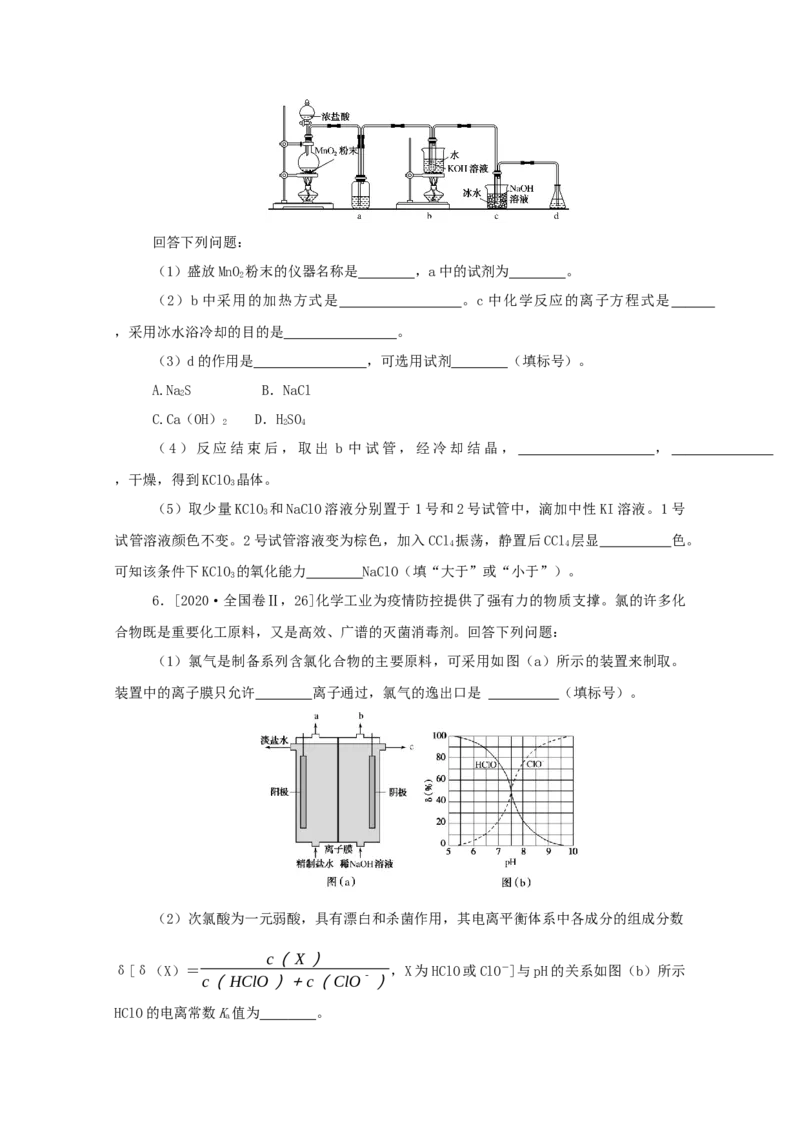
5.[2020·全国卷Ⅲ,26]氯可形成多种含氧酸盐,广泛应用于杀菌、消毒及化工领域
实验室中利用下图装置(部分装置省略)制备KClO 和NaClO,探究其氧化还原性质。
3回答下列问题:
(1)盛放MnO 粉末的仪器名称是 ,a中的试剂为 。
2
(2)b中采用的加热方式是 。c中化学反应的离子方程式是
,采用冰水浴冷却的目的是 。
(3)d的作用是 ,可选用试剂 (填标号)。
A.NaS B.NaCl
2
C.Ca(OH) D.HSO
2 2 4
(4)反应结束后,取出 b 中试管,经冷却结晶, ,
,干燥,得到KClO 晶体。
3
(5)取少量KClO 和NaClO溶液分别置于1号和2号试管中,滴加中性KI溶液。1号
3
试管溶液颜色不变。2号试管溶液变为棕色,加入CCl 振荡,静置后CCl 层显 色。
4 4
可知该条件下KClO 的氧化能力 NaClO(填“大于”或“小于”)。
3
6.[2020·全国卷Ⅱ,26]化学工业为疫情防控提供了强有力的物质支撑。氯的许多化
合物既是重要化工原料,又是高效、广谱的灭菌消毒剂。回答下列问题:
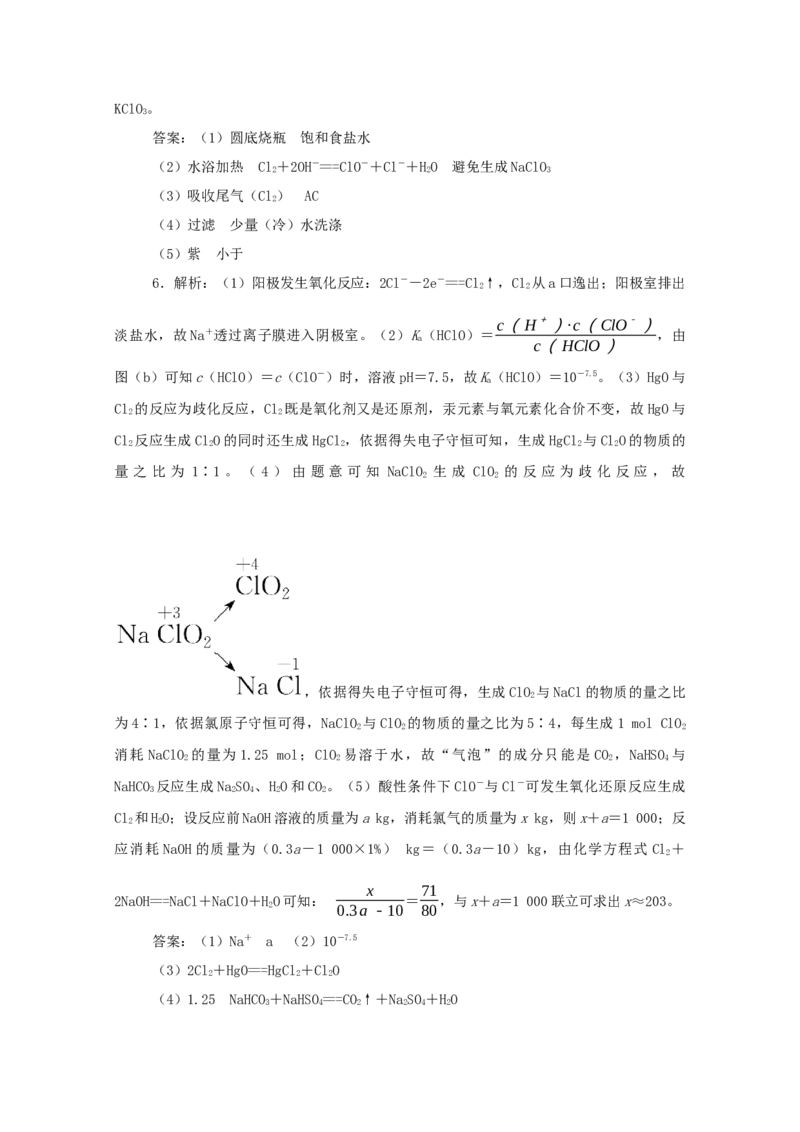
(1)氯气是制备系列含氯化合物的主要原料,可采用如图(a)所示的装置来制取。
装置中的离子膜只允许 离子通过,氯气的逸出口是 (填标号)。
(2)次氯酸为一元弱酸,具有漂白和杀菌作用,其电离平衡体系中各成分的组成分数
c(X)
δ[δ(X)= ,X为HClO或ClO-]与pH的关系如图(b)所示
c(HClO)+c(ClO-)
HClO的电离常数K值为 。
a(3)ClO为淡棕黄色气体,是次氯酸的酸酐,可由新制的HgO和Cl 反应来制备,该
2 2
反应为歧化反应(氧化剂和还原剂为同一种物质的反应)。上述制备 ClO的化学方程式为
2
________________________________________________________________________。
(4)ClO 常温下为黄色气体,易溶于水,其水溶液是一种广谱杀菌剂。一种有效成分
2
为NaClO 、NaHSO 、NaHCO 的“二氧化氯泡腾片”,能快速溶于水,溢出大量气泡,得到
2 4 3
ClO 溶液。上述过程中,生成ClO 的反应属于歧化反应,每生成1 mol ClO 消耗NaClO 的量
2 2 2 2
为 mol ; 产 生 “ 气 泡 ” 的 化 学 方 程 式 为
________________________________________________________________________
________________________________________________________________________。
(5)“84 消毒液”的有效成分为 NaClO,不可与酸性清洁剂混用的原因是
(用离子方程式表示)。工业上是将氯气通入到30%的NaOH溶液中来制备NaClO溶液,若
NaClO 溶液中 NaOH 的质量分数为 1%,则生产 1 000 kg 该溶液需消耗氯气的质量为
kg(保留整数)。
微专题·大素养 8
应用广泛的氯的含氧化合物
【知识基础】
1.氯的常见氧化物的性质
(1)一氧化二氯
性质:是次氯酸的酸酐,溶于水产生不稳定的次氯酸并最终变为盐酸
外观与性状:黄棕色气体,有刺激性气味。
制法:用新制备的黄色氧化汞与氯气反应可制得一氧化二氯:
HgO+2Cl===HgCl+ClO
2 2 2
同样也可以用氯气与潮湿的碳酸钠反应来制取:
2NaCO+HO+2Cl===2NaCl+2NaHCO+ClO
2 3 2 2 3 2
(2)二氧化氯
物理性质:是一种黄绿色到橙黄色的气体,极易溶于水。
制取:
Cl+2NaClO===2ClO↑+2NaCl
2 2 2或:5NaClO+4HCl===4ClO↑+5NaCl+2HO
2 2 2
用途:是一种广谱、高效的灭菌剂。
(3)ClO、ClO、ClO 分别为HClO、HClO、HClO 的酸酐。
2 3 2 5 2 7 2 3 4
2.氯的含氧酸
(1)氯的含氧酸的种类
氯的含氧酸有:HClO(次氯酸)、HClO (亚氯酸)、HClO (氯酸)、HClO (高氯
2 3 4
酸)。
(2)氯的含氧酸的性质
酸性:HClO>HClO>HClO>HClO
4 3 2
氧化性:HClO>HClO>HClO>HClO
2 3 4
3.氯的含氧酸盐
(1)NaClO(亚氯酸钠)
2
性质:黄绿色液体,呈碱性,是一种强氧化剂,遇酸放出ClO 气体。
2
用途:是一种高效氧化性漂白剂。主要用于棉纺、亚麻、纸浆漂白、食品消毒、水处
理、杀菌灭藻和鱼药制造。
(2)氯酸钾(KClO)
3
性质:是一种白色晶体,有毒,在冷水中溶解度较小,易溶于热水。是强氧化剂。
用途:可用作制造炸药,也可用来制造火柴、烟火。
【素养专练】
1.ClO是黄棕色具有强烈刺激性气味的气体,是一种强氧化剂,易溶于水且会与水反
2
应生成次氯酸,与有机物、还原剂接触或加热时会发生燃烧并爆炸。一种制取 ClO的装置如
2
图所示。
已知:ClO 的熔点为-116 ℃,沸点为 3.8 ℃;Cl 的沸点为-34.6 ℃;HgO+
2 2
2Cl===HgCl+ClO。
2 2 2
下列说法中不正确的是( )
A.装置②③中盛装的试剂依次是饱和食盐水和浓硫酸B.通入干燥空气的目的是将生成的ClO稀释,减小爆炸危险
2
C.从装置⑤中逸出气体的主要成分是ClO
2
D.装置④与⑤之间不用橡胶管连接,是为了防止橡胶管燃烧和爆炸
2.ClO 和NaClO 均具有漂白性,工业上用ClO 气体制NaClO 的工艺流程如图所示。
2 2 2 2
下列说法不正确的是( )
A.步骤a的操作包括过滤、洗涤和干燥
B.吸收器中生成NaClO 的离子方程式:2ClO+HO===2CIO− +O↑+2H+
2 2 2 2 2 2
C.工业上可将ClO 制成NaClO 固体,便于贮存和运输
2 2
D.通入空气的目的是驱赶出ClO,使其被吸收器充分吸收
2
3.世界环保联盟要求 ClO 逐渐取代 Cl 作为自来水消毒剂。已知:NaCl+
2 2
3HO=====NaClO+3H↑,2NaClO+4HCl===2ClO↑+Cl↑+2NaCl+2HO。
2 3 2 3 2 2 2
有关物质的熔、沸点如下表:
物质 熔点/℃ 沸点/℃
ClO -59 11
2
Cl -107 -34.6
2
ClO 的生产流程示意图如下:
2
该工艺中,需要补充的物质X为 (填化学式,下同),能参与循环的物质是
。 从 ClO 发 生 器 中 分 离 出 ClO , 可 采 用 的 方 法 是
2 2
。
4.ClO 是一种优良的消毒剂,浓度过高时易发生分解,常将其制成NaClO 固体,以便
2 2
运输和贮存。过氧化氢法制备NaClO 固体的实验装置如图1所示。
2
已知:2NaClO+HO+HSO===2ClO↑+O↑+NaSO+2HO
3 2 2 2 4 2 2 2 4 2
2ClO+HO+2NaOH===2NaClO+O↑+2HO
2 2 2 2 2 2
ClO 熔点-59 ℃、沸点11 ℃;HO 沸点150 ℃
2 2 2请回答:
( 1 ) 仪 器 A 的 作 用 是
________________________________________________________________________;
冰 水 浴 冷 却 的 目 的 是
________________________________________________________________________
________________________________________________________________________
(写两种)。
( 2 ) 空 气 流 速 过 快 或 过 慢 , 均 降 低 NaClO 产 率 , 试 解 释 其 原 因
2
________________________________________________________________________。
(3)Cl-存在时会催化ClO 的生成。反应开始时在三颈烧瓶中加入少量盐酸,ClO 的
2 2
生成速率大大提高,并产生微量氯气。该过程可能经两步反应完成,将其补充完整:
①________________________________________________________________________
(用离子方程式表示),②HO+Cl===2Cl-+O+2H+。
2 2 2 2
(4)HO 浓度对反应速率有影响。通过图2所示装置将少量30% H O 溶液浓缩至40%,
2 2 2 2
B处应增加一个设备。该设备的作用是 ,馏出物是 。
(5)抽滤法分离NaClO 过程中,下列操作不正确的是 。
2
A.为防止滤纸被腐蚀,用玻璃纤维代替滤纸进行抽滤
B.先转移溶液至漏斗,待溶液快流尽时再转移沉淀
C.洗涤沉淀时,应使洗涤剂快速通过沉淀
D.抽滤完毕,断开水泵与吸滤瓶间的橡皮管后,关闭水龙头第2讲 氯及其化合物 卤素
考点一
1知识梳理
1.黄绿 刺激性 毒 2 >
2.(1)2Fe+3Cl=====2FeCl Cu+Cl=====CuCl (2)H +Cl=====2HCl 苍白
2 3 2 2 2 2
白雾 爆炸 白雾 (3)Cl +HO H++Cl-+HClO (4)Cl +2OH-===Cl-+ClO-+HO
2 2 ⇌ 2 2
(5)Cl+2KI===2KCl+I Cl+SO+2HO===HSO+2HCl Cl+2Fe2+===2Fe3++2Cl-
2 2 2 2 2 2 4 2
3.(1)弱 2HClO=====2HCl+O↑ 棕色 (2)CaCl 和Ca(ClO) Ca(ClO)
2 2 2 2
2Cl +2Ca(OH) ===CaCl +Ca(ClO) +2HO 碱 氧化 Ca(ClO) +CO +HO===CaCO↓
2 2 2 2 2 2 2 2 3
+2HClO Ca(ClO)+CO+HO===CaCO↓+2HClO,2HClO=====2HCl+O↑
2 2 2 3 2
判断 答案:(1)× (2)× (3)× (4)× (5)√ (6)× (7)×
(8)×
2对点速练
1.解析:氯气与水反应生成盐酸和次氯酸,次氯酸有强氧化性,能够杀菌消毒,A项
正确;氯气与KI发生反应:Cl +2KI===2KCl+I ,反应中Cl 作氧化剂,B项正确;Cl 溶于
2 2 2 2
水为可逆反应,且生成的HClO为弱电解质,不可拆开,C项错误;Cl 与NaOH溶液发生反应
2
的化学方程式为Cl+2NaOH===NaCl+NaClO+HO,反应中Cl 既是氧化剂又是还原剂,D项正
2 2 2
确。
答案:C
2.解析:A项,氯水与二氧化硫反应生成无漂白性的物质,Cl +SO +2HO===4H++
2 2 2
SO2− +2Cl-,漂白性减弱,错误;B项,加入NaCl固体,c(Cl-)增大,Cl +HO H++Cl
4 2 2 ⇌
-+HClO平衡逆向移动,c(H+)减小,溶液的pH增大,错误;C项,氯水的pH=2,说明溶
液中c(H+)=0.01 mol·L-1,根据电荷守恒,c(H+)=c(Cl-)+c(ClO-)+c(OH
-),正确;D项,HClO的酸性弱于HCO ,正确的离子方程式为Cl +HCO===CO↑+Cl-+
2 3 2 2
HClO,错误。
答案:C
3.答案:(1)否 氯水已饱和,通入Cl 不再溶解,HClO浓度不增大
2(2)否 通入SO 发生SO+Cl+HO===4H++SO2− +2Cl-,HClO浓度减小
2 2 2 2 4
(3)能 加入CaCO 固体,发生CaCO+2H+===Ca2++CO↑+HO,平衡Cl+HO H++
3 3 2 2 2 2 ⇌
Cl-+HClO右移,HClO浓度增大
(4)能 加入NaCO 消耗H+,使Cl +HO H++Cl-+HClO平衡正向移动,HClO浓度
2 3 2 2 ⇌
增大
4.解析:ClO-具有强氧化性,可将Fe2+氧化,因而不能大量共存,A错误;Cl-与Ag+
反应生成AgCl沉淀,不能大量共存,B错误;ClO-具有强氧化性,可将SO 氧化为SO2− ,由
2 4
于ClO-过量,因此生成的H+与ClO-反应生成HClO,C正确;没有说明气体是否处于标准状
况,D错误。
答案:C
5.解析:A项没有还原剂,不可能将ClO-还原为Cl-,错误;B项生成HClO,光照分
解产生O,会产生气泡,正确。
2
答案:A
6.解析:(1)根据仪器D的形状和结构可知其为锥形瓶。根据“长进短出”的原则
可知应该选装置b。
(2)滴加盐酸速率应该慢,这样产生ClO 的速率也会慢,ClO 通过D时才能被充分吸
2 2
收。
(3)关闭B的活塞后,ClO 被完全吸收,而装置F中淀粉+KI溶液颜色不变,说明没
2
有I 单质生成,推知装置A中生成的Cl 被装置C中的药品吸收,可见装置C的作用是吸收
2 2
Cl。
2
(4)CIO− 在酸性条件下(H+)反应生成ClO ,同时生成Cl-、HO,其离子反应方程
2 2 2
式为5CIO− +4H+===Cl-+4ClO↑+2HO。ClO 具有强氧化性,根据实验目的,若释放出了
2 2 2 2
ClO ,则ClO 与淀粉+KI溶液反应生成I ,F中会出现蓝色,所以装置F的作用是验证是否
2 2 2
有ClO 生成。
2
(5)根据变化曲线,稳定剂Ⅰ释放出ClO 的速率快,保鲜时间相对较短,稳定剂Ⅱ释
2
放出ClO 的速率缓慢平稳,保鲜时间更长,所以选稳定剂Ⅱ。
2
答案:(1)锥形瓶 b (2)慢 (3)吸收Cl
2(4)4H++5CIO− ===Cl-+4ClO↑+2HO
2 2 2
验证是否有ClO 生成
2
(5)稳定剂Ⅱ 稳定剂Ⅱ可以缓慢释放ClO,能较长时间维持保鲜所需的浓度
2
考点二
1知识梳理
2.MnCl +Cl↑+2HO 饱和食盐水 浓HSO 排空气法 排饱和食盐水法 NaOH
2 2 2 2 4
淀粉碘化钾 蓝色石蕊
思考 答案:向上排气收集氯气 安全瓶作用,防止D中的液体倒吸进入集气管B中
吸收尾气,防止氯气扩散到空气中污染环境
判断 答案:(1)× (2)× (3)√ (4)√ (5)× (6)×
2对点速练
1.解析:A项,该装置的错误有:没有用酒精灯加热,MnO 不与浓盐酸发生反应,从
2
而得不到Cl;装置中没有用分液漏斗而采用长颈漏斗导致气体外逸和HCl的挥发;没有进行
2
尾气处理;B项,Cl 的密度比空气大,该收集方法正确;C项,要得到干燥纯净的Cl ,首先
2 2
应将气体通过饱和食盐水除去HCl,再通过浓硫酸除去水蒸气;D项,根据反应:MnO +4HCl
2
(浓)=====MnCl+Cl↑+2HO,盐酸浓度变稀后便不再反应,使产生的Cl 的物质的量小于
2 2 2 2
0.5 mol,转移的电子小于1 mol。
答案:A
2.解析:二氧化锰只能与浓盐酸反应,当盐酸浓度降低时,反应会停止,即盐酸不能
完全反应,故A错误;氯气与铜反应生成棕黄色的烟,加少量水所得溶液呈绿色,故 B错误;
氯气和甲烷在光照下发生取代反应,故C错误;干燥的氯气不具有漂白性,氯气与水反应生
成的HClO具有漂白性,所以只有湿润的有色布条褪色,故D正确。
答案:D
3.解析:A项,利用MnO 和浓盐酸制氯气,需要加热,故无法达到实验目的;B项,
2
洗气装置气体应该是长进短出,且Cl 和HCl都能与NaHCO 溶液反应,应用饱和食盐水除去
2 3
Cl 中的HCl,故无法达到实验目的;C项,MnO 不溶于水,MnCl 能溶于水,因此可以用过滤
2 2 2
法分离,正确;D项,加热时MnCl 会发生水解无法制得纯净的MnCl·4HO。
2 2 2
答案:C
4.答案:(1)c (2)2Fe2++Cl===2Fe3++2Cl-
2(3)Cl+2NaCO+HO===NaCl+NaClO+2NaHCO
2 2 3 2 3
(4)在丙装置后连接一个盛有氢氧化钠溶液的尾气处理装置
考点三
1知识梳理
1.(1)2FeBr FeI (2)2HX (3)HX+HXO (4)NaX+NaXO+HO
3 2 2
2.加深 升高 增大 减小 减弱 增强 (1)Cl >Br >I (2)I->Br->Cl-
2 2 2
(3)2Br-+Cl===2Cl-+Br (4)2I-+Br===2Br-+I
2 2 2 2
3.(1)白 浅黄 黄
判断 答案:(1)√ (2)√ (3)× (4)√ (5)× (6)× (7)√
2对点速练
1.解析:元素的非金属性强弱与其对应的氢化物溶液的酸性强弱无关,可根据其最高
价氧化物对应的水化物的酸性强弱进行比较,A错误;I 在KI溶液中存在I +I- I− ,可
2 2 ⇌ 3
使其溶解度增大,D正确。
答案:A
2.解析:在F处,可能是未反应完的Cl 与KI发生反应置换出I ,使淀粉变蓝色,不
2 2
能说明Br 的氧化性比I 强。
2 2
答案:B
3.答案:(1)HCl、HIO
2
(2)ICl+2OH-===Cl-+IO-+HO 否
2
4.解析:①NaCl、NaBr、NaI中加碘水和淀粉溶液均变蓝色;②氯气加入 NaBr、NaI
中后,再加CCl 萃取,下层分别为橙红色和紫红色,加入 NaCl中不发生反应,可以鉴别;
4
③溴水与NaCl、NaBr不反应,与NaI反应生成I ,用苯萃取后,前两种上层均为橙红色,无
2
法鉴别;④NaCl、NaBr、NaI与AgNO 溶液反应分别生成AgCl、AgBr、AgI沉淀,且均不溶于
3
稀HNO ,沉淀颜色依次为白色、淡黄色、黄色;⑤与②的原理相似,只是有色层在上层;
3
⑥FeCl 溶液只能氧化I-生成I,不能鉴别。
3 2
答案:C
5.解析:食盐加碘加入的是KIO,KIO 不能使淀粉变蓝,A错误。B中若原溶液中含有
3 3
I ,也会产生同样现象,B错误。由于酒精与水互溶,因此不能用酒精萃取溶液中的 Br ,D
2 2
错误。答案:C
6.解析:(1)仪器d为分液漏斗。
(2)若通入的CO 不干燥,则在E中Fe在高温下会与HO反应生成FeO ,故副产物为
2 2 3 4
FeO;FeO 与盐酸反应会生成FeCl、FeCl,加入KSCN溶液后溶液会变为血红色,但产物中
3 4 3 4 3 2
可能含有FeBr 会对检验造成干扰,A项错误;通入H ,排尽空气后加热只有FeO 会与H 反
3 2 3 4 2
应生成HO,故可通过无水CuSO 粉末是否变蓝检验是否含有FeO ,B项正确;铁单质也能被
2 4 3 4
磁化而被磁铁吸引,所以产物能被吸引不一定是四氧化三铁,C项错误;铁粉也是黑色不溶
物,所以取少量产物于试管中加入蒸馏水,过滤有黑色不溶物不一定是铁的氧化物,D项错
误。
(3)未反应的Br 会污染空气,可在F处连接盛有NaOH溶液的尾气吸收装置进行吸收,
2
反应的化学方程式为2NaOH+Br===NaBr+NaBrO+HO。
2 2
(4)反应的离子方程式为MnO+5Fe2++8H+===Mn2++5Fe3++4HO,可得关系式KMnO
2 4
250 mL
~MnO~5Fe2+,所以n(Fe2+)=n(FeBr)=0.030 0 mol·L-1×0.025 0 L×5×
2 25 mL
0.037 5 mol×216 g·mol-1
=0.037 5 mol,则产品的纯度为 ×100%=81.00%。
10 g
(5)氧化性:Cl>Br>Fe3+,还原性:Cl-Fe3+且Fe3+氧化性最弱,当加入过量氯水,此时可生成Br,可用四氯化碳
2 2
萃取判断,从而证明氧化性Cl>Br。
2 2
答案:(1)分液漏斗 (2)FeO(或四氧化三铁) B
3 4
(3)2NaOH+Br===NaBr+NaBrO+HO
2 2
(4)81.00%
(5)
实验操作 实验现象 氧化性强弱
①取一定量FeBr 溶于水,加入少量
2
(或几滴)氯水(或通入少量氯 ②Cl>Fe3+ Br>Fe3+
2 2
气),加入KSCN溶液。
③取少量FeBr 溶于水,加入过量氯
2
水(或通入足量氯气),加入四氯 ④四氯化碳 层呈棕红色
化碳,震荡。本讲真题研练
1.解析:检验Fe2+应先加KSCN溶液,溶液不变红色,再滴加新制氯水,溶液变红色,
A不正确;I-先沉淀,说明K (AgI)