文档内容
第5讲 海水资源的开发利用 环境保护和绿色化学
[考纲要求]
1.了解常见元素单质及其重要化合物对环境质量的影响。2.了解科学、技术、社会的
相互关系(如化学与生活、材料、能源、环境、生命过程、信息技术的关系等)。3.了解在
化工生产中遵照“绿色化学”思想的重要性。
考点一 海水资源的综合利用
1 知识梳理
1.水资源的利用
2.海水中化学资源的开发利用
(1)氯碱工业
①电解NaCl溶液:(写出化学方程式,下同)
________________________________________________________________________;
② 产 物 制 盐 酸 :
________________________________________________________________________;
③ 制 漂 白 液 :
________________________________________________________________________。
(2)海水提镁
海水――→Mg(OH) ――→ (溶液)―――――→MgCl·6HO――→
2 2 2
――→Mg。
(3)海水提溴
海水(酸化)――→ ―――→――→HBr――→Br(液)。
2
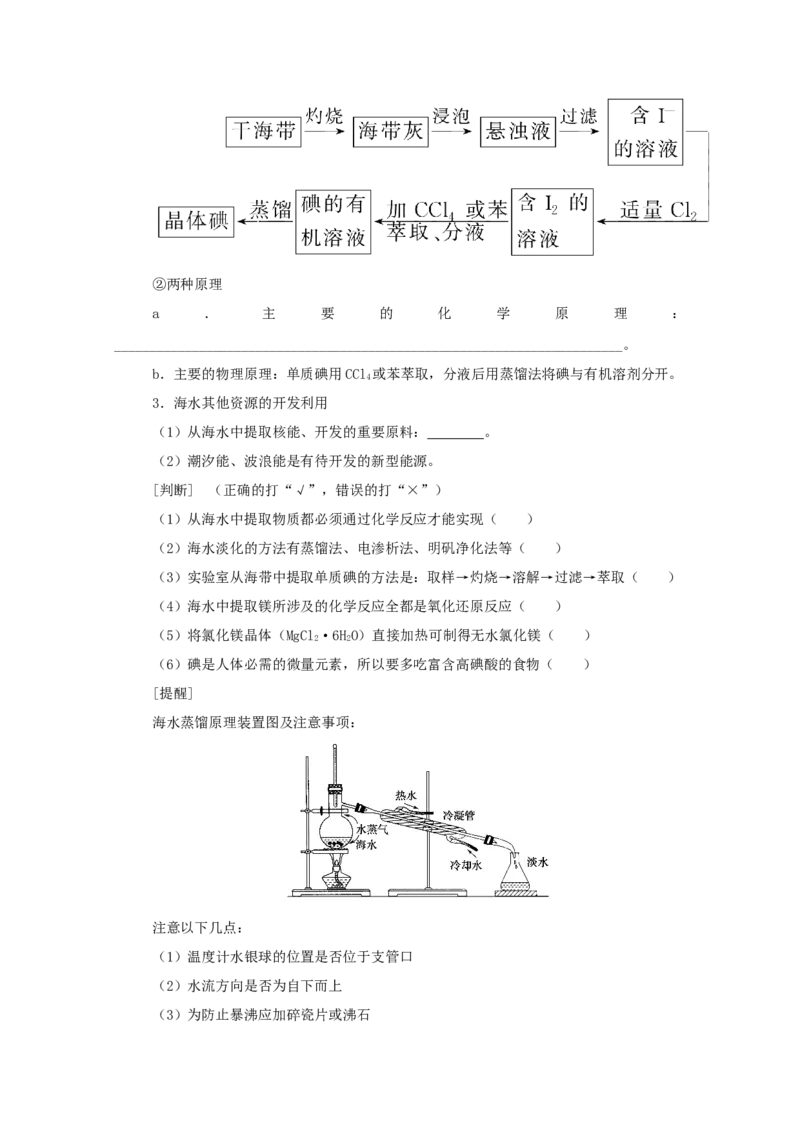
(4)海带提碘
①工艺流程②两种原理
a . 主 要 的 化 学 原 理 :
________________________________________________________________________。
b.主要的物理原理:单质碘用CCl 或苯萃取,分液后用蒸馏法将碘与有机溶剂分开。
4
3.海水其他资源的开发利用
(1)从海水中提取核能、开发的重要原料: 。
(2)潮汐能、波浪能是有待开发的新型能源。
[判断] (正确的打“√”,错误的打“×”)
(1)从海水中提取物质都必须通过化学反应才能实现( )
(2)海水淡化的方法有蒸馏法、电渗析法、明矾净化法等( )
(3)实验室从海带中提取单质碘的方法是:取样→灼烧→溶解→过滤→萃取( )
(4)海水中提取镁所涉及的化学反应全都是氧化还原反应( )
(5)将氯化镁晶体(MgCl·6HO)直接加热可制得无水氯化镁( )
2 2
(6)碘是人体必需的微量元素,所以要多吃富含高碘酸的食物( )
[提醒]
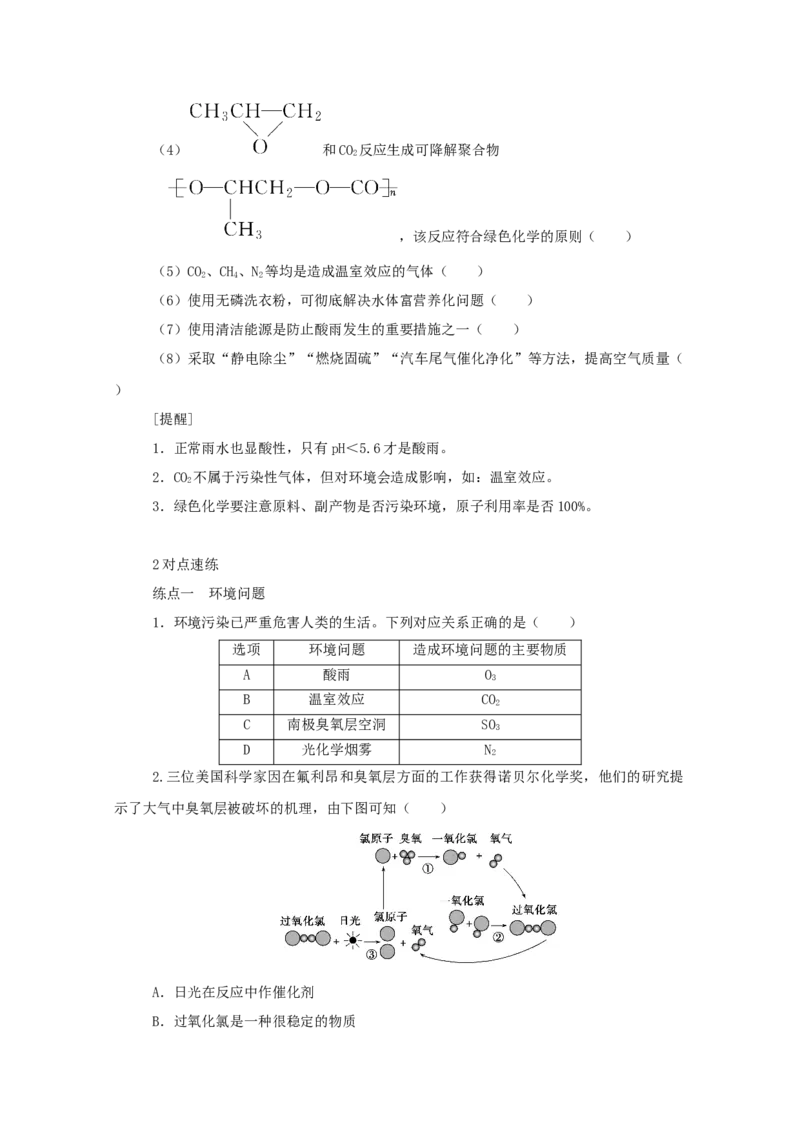
海水蒸馏原理装置图及注意事项:
注意以下几点:
(1)温度计水银球的位置是否位于支管口
(2)水流方向是否为自下而上
(3)为防止暴沸应加碎瓷片或沸石(4)应垫石棉网对蒸馏烧瓶加热
2 对点速练
练点一 提取碘的实验
1.从海带中提取碘的实验过程涉及下列操作,其中正确的是( )
2.为了从海带浸取液中提取碘,某同学设计了如图实验方案,下列说法正确的是(
)
A.①中反应的离子方程式:2I-+HO===I+2OH-
2 2 2
B.②中分液时含I 的CCl 溶液从分液漏斗上口倒出
2 4
C.③中得到的上层溶液中含有I-
D.操作Z的名称是加热
练点二 海水综合利用的流程分析
3.根据如图海水综合利用的工业流程图,判断下列说法正确的是( )已知:MgCl·6HO受热生成Mg(OH)Cl和HCl气体等。
2 2
A.过程①的提纯是物理过程,过程②通过氧化还原反应可产生2种单质
B.在过程③中将MgCl·6HO灼烧即可制得无水MgCl
2 2 2
C.在过程④、⑥反应中每氧化0.2 mol Br-需消耗2.24 L Cl
2
D.过程⑤反应后溶液呈强酸性,生产中需解决其对设备的腐蚀问题
4.从淡化海水中提取溴的流程如下:
―――→―――――――――→――――→→…→
下列有关说法不正确的是( )
A.X试剂可用NaSO 饱和溶液
2 3
B.步骤Ⅲ的离子反应:2Br-+Cl===2Cl-+Br
2 2
C.工业上每获得1 mol Br,需要消耗Cl 44.8 L
2 2
D.步骤Ⅳ包含萃取、分液和蒸馏
练后归纳
解答海水的工艺流程题目应注意的几点
(1)在过程中往往用到结晶、过滤、萃取、分液、蒸馏等实验操作,注意这些操作的
使用条件和操作方法的规范性。
(2)在制备过程中,涉及氧化还原反应、电解反应、水解平衡等化学原理。
(3)读懂流程图,抓住物质的流入、流出、挖掘反应条件和重要数据。
(4)绿色化学,使用无污染的物质、减少或不排放污染物、物质的循环使用。
考点二 环境保护与绿色化学
1 知识梳理1.环境污染
(1)环境问题
主要是指由于人类不合理地开发和利用自然资源而造成的生态环境的 ,以及工
农业生产和人类生活所造成的环境 。
(2)“三废”:主要是指 。
(3)大气污染物的来源
化石燃料的燃烧和工业生产过程中的废气及其携带的颗粒物。
(4)常见环境污染问题
(5)环境保护的措施
①工业废气携带颗粒物的回收利用。
②工业、生活污水经处理达标后排放,限制使用含氮、磷洗涤剂。
③回收、限制难降解塑料,研制 塑料。
2.绿色化学
[判断] (正确的打“√”,错误的打“×”)
(1)减少CO 的排放,可以减少酸雨的产生( )
2
(2)减少机动车尾气的排放,可有效降低雾霾的发生( )
(3)大量燃烧化石燃料是造成雾霾天气的重要因素( )(4) 和CO 反应生成可降解聚合物
2
,该反应符合绿色化学的原则( )
(5)CO、CH、N 等均是造成温室效应的气体( )
2 4 2
(6)使用无磷洗衣粉,可彻底解决水体富营养化问题( )
(7)使用清洁能源是防止酸雨发生的重要措施之一( )
(8)采取“静电除尘”“燃烧固硫”“汽车尾气催化净化”等方法,提高空气质量(
)
[提醒]
1.正常雨水也显酸性,只有pH<5.6才是酸雨。
2.CO 不属于污染性气体,但对环境会造成影响,如:温室效应。
2
3.绿色化学要注意原料、副产物是否污染环境,原子利用率是否100%。
2对点速练
练点一 环境问题
1.环境污染已严重危害人类的生活。下列对应关系正确的是( )
选项 环境问题 造成环境问题的主要物质
A 酸雨 O
3
B 温室效应 CO
2
C 南极臭氧层空洞 SO
3
D 光化学烟雾 N
2
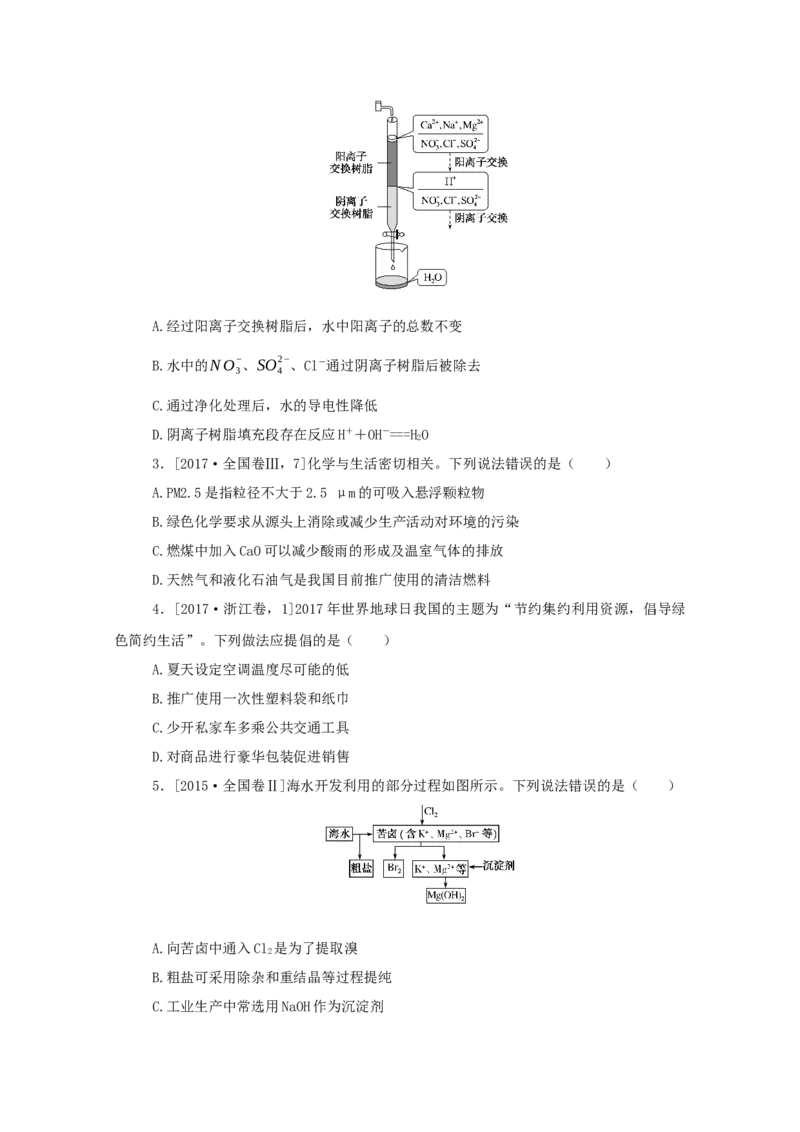
2.三位美国科学家因在氟利昂和臭氧层方面的工作获得诺贝尔化学奖,他们的研究提
示了大气中臭氧层被破坏的机理,由下图可知( )
A.日光在反应中作催化剂
B.过氧化氯是一种很稳定的物质C.过氧化氯的结构式为O—Cl—Cl—O
D.臭氧分子最终转变成氧气分子
3.当前,汽车尾气已经成为许多城市空气的主要污染源。研究表明,含TiO 的混凝土
2
或沥青可以部分消除汽车尾气中的氮氧化物,其原理如下:
下列关于该“消除”过程的叙述不正确的是( )
A.部分光能转变为化学能
B.消除总变化为NO+O+HO―→HNO
x 2 2 3
C.消除反应能全天候发生
D.使用纳米TiO 的消除效率更高
2
练后归纳
1.认识雾霾
雾霾——雾和霾的统称。空气中的灰尘、硫酸、硝酸等颗粒物组成的气溶胶系统造成
视觉障碍的叫霾。二氧化硫、氮氧化物以及颗粒物(PM)这三项是雾霾主要污染物,前两者
为气态污染物,最后一项颗粒物才是加重雾霾天气污染的罪魁祸首。
2.各种非金属元素的化合物对环境的影响
元素 化合物 主要来源 对环境的影响
CO 化石燃料燃烧 温室效应
2
C 碳氢 石油开采、 温室效应、
化合物 植物腐败 光化学烟雾
硝酸型酸雨、臭氧
NO 汽车尾气
x
空洞、光化学烟雾
N
铵盐、 化肥、农药、 水体富营养化:
硝酸盐 洗涤剂 赤潮、水华
S SO、SO 煤的燃烧 硫酸型酸雨
2 3
空调、
F、Cl 氟氯烃 臭氧空洞
冰箱制冷剂
水体富营养化:
P 磷酸盐 洗涤剂
赤潮、水华练点二 “绿色化学”思想
4.在“绿色化学工艺”中,理想状态是原子利用率为 100%。在用 CHC≡CH 合成
3
CH===C(CH)COOCH 的过程中,欲使原子利用率达到最高,还需要其他的反应物有( )
2 3 3
A.CO和CHOH B.CO 和HO
3 2 2
C.H 和CO D.CHOH和H
2 2 3 2
5.以下是与绿色化学、环境保护和人类健康息息相关的三个主题,请根据已知信息回
答有关问题:
(1)下列制备氯乙烷的反应中原子经济性最高的是(可多选) 。
A.CH===CH+HCl―→CHCHCl
2 2 3 2
B.CHCHOH+HCl―→CHCHCl+HO
3 2 3 2 2
C.CHCH+Cl――→CHCHCl+HCl
3 3 2 3 2
D.CH===CHCl+H――→CHCHCl
2 2 3 2
由上述四个反应可归纳出,原子经济性高的是 反应(填反应类型)。
(2)有毒物质的无害化也是绿色化学研究的内容之一。ClO 是一种性能优良的消毒剂,
2
还可将废水中少量的S2-、NO和CN-等有毒有害的还原性酸根离子氧化而去除。请写出用
ClO 将 废 水 中 剧 毒 的 CN - 氧 化 成 无 毒 气 体 的 离 子 方 程 式
2
________________________________________________________________________,
并 说 明 该 方 法 的 优 点
________________________________________________________________________
________________________________________________________________________。
(3)下图为某饮用水厂从天然水制备纯净水(去离子水)的工艺流程示意图:
活 性 炭 的 作 用 是
________________________________________________________________________;
O 消 毒 的 优 点 是
3
________________________________________________________________________。练后归纳
绿色化学的过程、目标及措施
本讲真题研练
1.[2020·江苏卷]阅读下列资料,完成(1)~(2)题。
海水晒盐后精制得到NaCl,氯碱工业电解饱和NaCl溶液得到Cl 和NaOH,以NaCl、
2
NH 、CO 等为原料可得到NaHCO ;向海水晒盐得到的卤水中通Cl 可制溴;从海水中还能提取
3 2 3 2
镁。
(1)下列关于Na、Mg、Cl、Br元素及其化合物的说法正确的是( )
A.NaOH的碱性比Mg(OH) 的强
2
B.Cl 得到电子的能力比Br 的弱
2 2
C.原子半径r:r(Br)>r(Cl)>r(Mg)>r(Na)
D.原子的最外层电子数n:n(Na)r(Mg)>r(Cl),C项错误;Na、Mg、Cl、
Br原子的最外层电子数分别为1、2、7、7,D项错误。
解析:(2)本题考查物质间的相互转化,考查的化学学科核心素养是变化观念与平衡
思想。Cl 与石灰乳反应可制得漂白粉,A项错误;NaCl+NH+CO+HO===NaHCO↓+NHCl,
2 3 2 2 3 4
2NaHCO=====NaCO +CO↑+HO,B项错误;由于氧化性Cl>Br>I ,则Cl +2NaBr===2NaCl
3 2 3 2 2 2 2 2 2
+Br ,Br +2NaI===2NaBr+I ,C项正确;电解MgCl 溶液不能得到单质镁,要得到单质
2 2 2 2
Mg,需电解熔融态的MgCl,D项错误。
2
答案:(1)A (2)C
2.解析:由图可知,经过阳离子交换树脂,Ca2+、Na+、Mg2+被H+替换,由电荷守恒
可知阳离子数目增多,A项错误;再经阴离子交换树脂得到纯净水,则NO− 、Cl-、SO2−
被
3 4
OH-替换,H+与OH-结合生成水:H++OH-===HO,水的导电能力减弱,B、C、D项正确。
2
答案:A
3.解析:A项,PM2.5是指粒径小于或等于2.5微米的颗粒物,正确;B项,绿色化学
就是要从源头上减少和消除工业生产对环境的污染,正确;C项,煤燃烧可生成二氧化硫和
二氧化碳等产物,加入的CaO可与SO 反应生成CaSO,进一步被氧气氧化为CaSO,从而减少
2 3 4
SO 的排放量,减少酸雨的形成,但CaO与CO 反应生成的CaCO 在高温下又会分解为CaO,故
2 2 3
不能吸收CO ,不能减少温室气体的排放量,错误;D项,天然气的主要成分是甲烷,液化石
2
油气的成分是丙烷、丁烷、丙烯和丁烯等,燃烧产物为CO 和HO,对环境无污染,所以这两
2 2
类燃料均是清洁燃料,正确。
答案:C
4.解析:A项,空调温度低,能源消耗增多,错误;B项,一次性塑料袋使用易引起
“白色污染”,纸巾的大量使用会造成森林的乱砍乱伐,错误;C项,少开私家车,一是减
少汽车尾气污染,二是节约能源,正确;D项,过度包装会引起资源浪费,错误。
答案:C
5.解析:本题考查海水开发利用中的化学知识,意在考查考生将化学知识应用到实际
生产中的能力。苦卤中含有Br-,通入Cl 可将Br-氧化生成Br,A项说法正确;粗盐中含有
2 2
Ca2+、SO2−
等杂质离子,故先除杂得NaCl和KCl的混合溶液,而NaCl的溶解度随温度变化
4
不大,故采用重结晶可以得到纯净的NaCl,B项说法正确;工业上沉淀海水中的Mg2+,采用Ca(OH) ,不用NaOH,因为NaOH的价格较贵,C项说法错误;Br 易挥发,用热气吹出后,
2 2
用SO 吸收,生成HSO 和HBr,富集后再用Cl 处理HBr生成Br,D项说法正确。
2 2 4 2 2
答案:C
微专题·大素养⑪
【素养专练】
1.答案:A
2.答案:A
3.解析:本题考查化学与生产、生活的联系,意在考查考生学以致用的能力。铁表面
镀锌,可以形成原电池,锌作负极,增强铁的抗腐蚀性,A项正确;聚乙烯塑料会引起白色
污染,B项错误;大量燃烧化石燃料造成污染,是造成雾霾天气的一种重要因素,C项正确;
重金属离子有毒,不能随意排放,D项正确。
答案:B
4.解析:A项,绿色食品是指产自优良生态环境,按照绿色食品标准生产,实行全程
质量控制并获得绿色食品标志使用权的安全、优质食用农产品及相关产品,错误;B项,合
理开发利用可燃冰(固态甲烷水合物),有助于缓解能源紧缺的状况,正确;C项,福尔马
林是甲醛的水溶液,有毒,不能用作食品的保鲜和消毒,错误;D项,用Ba(OH) 处理含
2
Cu2+的废水,又引入了重金属离子钡离子,不能消除水中重金属离子的污染,错误。
答案:B
5.解析:硅胶是一种高活性、吸水性材料,无毒无味,化学性质稳定,可用作食品干
燥剂,A正确;PO 极易吸水生成HPO、HPO,而HPO 有毒性,故不能用PO 作食品干燥剂,
2 5 3 3 4 3 2 5
B正确;CaCl 具有较强的吸水性,吸水后生成六水氯化钙(CaCl·6HO),故不能用六水氯
2 2 2
化钙作食品干燥剂,C错误;吸水性植物纤维无毒、无味,可用作食品干燥剂,D正确。
答案:C
6.解析:A项中煤的气化和液化均是化学变化,错误,符合题意;B项中“酸雨”
“臭氧层受损”“光化学烟雾”都与氮氧化物有关,正确,不符合题意;C项中采用催化转
换技术将汽车尾气中的NO 和CO转化为无毒的氮气和CO ,正确,不符合题意;D项中利用太
x 2
阳能等清洁能源代替化石燃料,有利于节约资源、保护环境,正确,不符合题意。
答案:A
7.解析:A项中绿色化学倡导环保,有积极影响,正确,不符合题意;B项中白色污
染是指塑料等难以降解的垃圾造成的污染,错误,符合题意;C项中二氧化碳和甲烷等气体能造成温室效应,正确,不符合题意;D项中含硫和含氮的氧化物会使雨水pH减小,正确,
不符合题意。
答案:B
8.解析:聚氯乙烯塑料袋会释放出含氯的有毒气体,因此不能用聚氯乙烯塑料袋包装
食品。
答案:A
9.解析:煤脱硫只能减少SO 的排放,减少酸雨的形成,煤的燃烧还是会增加大气中
2
的CO 含量,所以D项符合题意。
2
答案:D
10.解析:若有机体中的硫存在形式是 ,硫元素显-2价,故C正确;
大气中的SO 也可先氧化成HSO,亚硫酸再转化成硫酸形成酸雨,故D错误。
2 2 3
答案:D
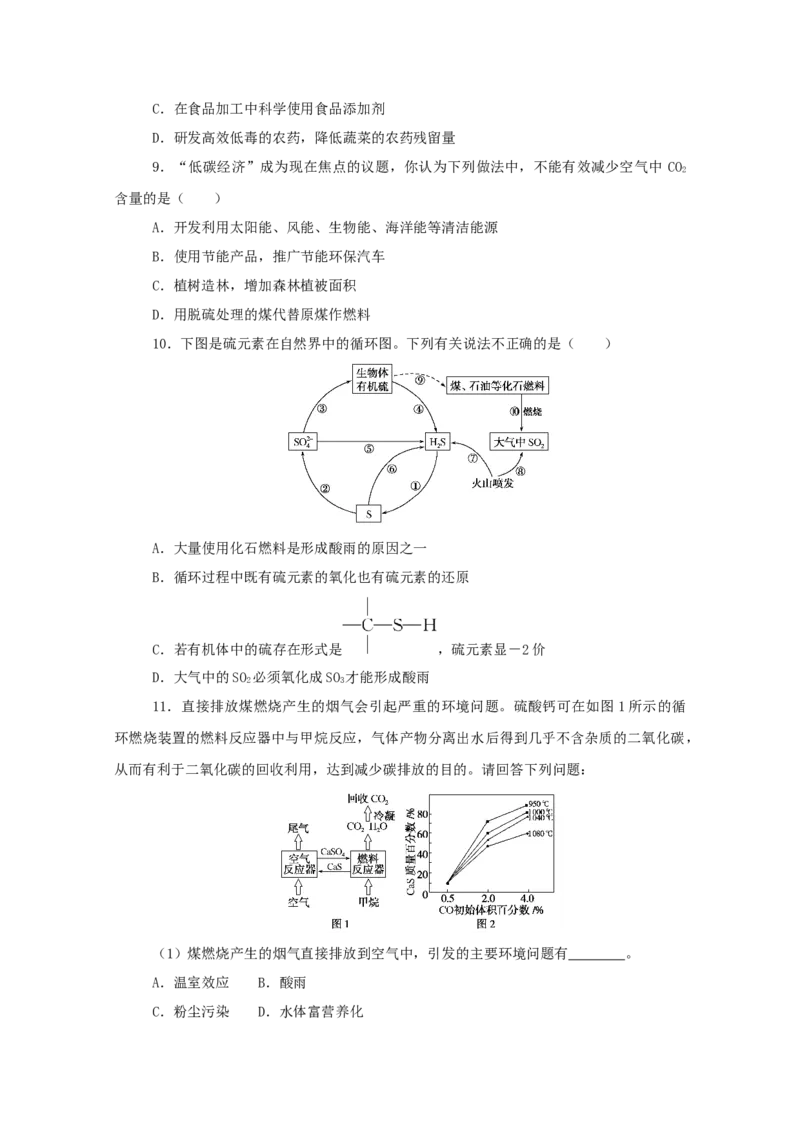
11.解析:(1)煤燃烧的产物中有CO 、烟尘及SO ,分别导致温室效应、粉尘污染和
2 2
酸雨;没有营养元素排入水中,不会引起水体富营养化。
(2) CO 与CaCO 反应生成易溶的Ca(HCO ) 。亚硫酸氢钙具有还原性,可被氧化为
2 3 3 2
硫酸钙。
(3)向该反应体系中投入石灰石,产生二氧化碳,使反应Ⅰ逆向进行,可降低反应体
系中二氧化硫的生成量,A项正确;由图可以看出最低温度的硫化钙的含量最高,B项正确,
D项错误;由图可以看出提高CO的初始体积百分数,可以提高硫化钙的含量,C项正确。
答案:(1)ABC (2)①Ca(HCO)(或碳酸氢钙)
3 2
②Ca(HSO)+O===CaSO+HSO
3 2 2 4 2 4
(3)ABC
12.解析:(1)污染治理要求能除掉有毒的物质,新生成的物质对环境无污染,物理
法与化学法的区别是是否有新物质生成。酸和碱性氧化物的反应为化学反应,为化学法,故
A错误;硫酸铜可溶,所以不能沉淀除去,故 B错误;含纯碱的废水,加石灰水反应生成沉
淀,为化学方法,故C正确。
(2)①氧化铝在水中不能水解,不能生成胶状物或絮状沉淀,不能用作混凝剂,而偏
铝酸钠、碱式氯化铝、氯化铁在溶液中易水解生成胶体可作为混凝剂;②混凝剂能使固体颗
粒沉淀,且混凝剂在水中发生水解是化学变化,故混凝剂除去悬浮物质的过程是物理和化学过程。
(3)反应中KOCN→N ,N元素化合价由-3价升高为0价,共升高6价,Cl→KCl,Cl
2 2
元素化合价由0价降低为-1价,共降低2价,化合价升降最小公倍数为6,故N 系数为1,
2
Cl 系数为 3,结合原子守恒配平其它物质的系数,平衡后方程式为:2KOCN+4KOH+
2
3Cl===2CO +N +6KCl+2HO;废水中KCN的质量为650 mg/L×20 L=13 000 mg=13 g,物
2 2 2 2
质的量为13 g/(65 g/mol)=0.2 mol,使KCN完全转化为无毒物质,应生成CO、N,整个
2 2
过程中C元素化合价由+2价升高为十4价,N元素化合价由-3价升高为0价,Cl元素化合
价由 0 价降低为-1 价,电子转移守恒可知 2×n(Cl ) =0.2 mol×(4-2)+0.2
2
mol×[0-(-3)],解得n(Cl )=0.5 mol,故需要氯气的质量为0.5 mol×71 g/mol=
2
35.5 g。
答案:(1)C (2)①B ②C
(3)2 4 3 2 1 6 2 35.5