文档内容
第2讲 化学平衡状态 化学平衡移动
[考纲要求]
1.了解化学反应的可逆性。
2.了解化学平衡建立的过程,掌握化学平衡特征。
3.理解外界条件(浓度、温度、压强、催化剂等)对化学平衡的影响,能用相关理论解
释其一般规律。
4.了解化学平衡的调控在生活、生产和科学研究领域中的重要作用。
考点一 可逆反应与化学平衡状态
1知识梳理
1.可逆反应
(1)定义
在________下既可以向正反应方向进行,同时又可以向逆反应方向进行的化学反应。
(2)特点
①二同:a.相同条件下;b.正、逆反应同时进行。
②一小:反应物与生成物同时存在;任一组分的________都小于100%。
(3)表示
在化学方程式中用“______”表示。
[思考]
对于可逆反应2SO+O 2SO ΔH<0,在混合气体中充入一定量的18O,经足够长的时
2 2⇌ 3 2
间后:
(1)18O存在于哪些分子中?
________________________________________________________________________
(2)二氧化硫分子的相对分子质量可能为________。
2.化学平衡状态
(1)概念
一定条件下的可逆反应,当反应进行到一定程度时,正反应速率和逆反应速率____,
反应物的浓度和生成物的浓度____,我们称为“化学平衡状态”,简称化学平衡。
(2)建立过程
在一定条件下,把某一可逆反应的反应物加入固定容积的密闭容器中。反应过程如下:如图所示:
(3)化学平衡的特点
[判断] (正确的打“√”,错误的打“×”)
(1)2HO2H↑+O↑为可逆反应( )
2 2 2
(2)二次电池的充、放电为可逆反应( )
(3)一个可逆反应达到的平衡状态就是这个反应在该条件下所能达到的限度( )
(4)对反应A(g)+B(g) C(g)+D(g),压强不随时间而变,说明反应已达平衡状态(
⇌
)
(5)对NO(g)+SO(g) SO(g)+NO(g)反应,当每消耗1 mol SO 的同时生成1 mol NO
2 2 ⇌ 3 3 2
时,说明反应达到平衡状态( )
(6)对于反应A(g)+B(g) 2C(g)+D(g),当密度保持不变,在恒温恒容或恒温恒压条
⇌
件下,均不能作为达到化学平衡状态的标志( )
(7)在2 L密闭容器内,800 ℃时反应2NO(g)+O(g) 2NO(g)体系中,当该容器内颜
2 ⇌ 2
色保持不变时能说明该反应已达到平衡状态( )
[提醒](1)化学反应的平衡状态可以从正反应方向建立,也可以从逆反应方向建立。
(2)化学反应达到化学平衡状态的正、逆反应速率相等,是指同一物质的消耗速率和生
成速率相等。
(3)化学反应达平衡状态时,各组分的浓度、百分含量保持不变,但不一定相等。
2对点速练
练点一 化学平衡状态的判断
1.一定温度下在一容积不变的密闭容器中发生可逆反应2X(g) Y(g)+Z(s),以下不
⇌
能说明该反应达到化学平衡状态的是( )
A.混合气体的密度不再变化
B.反应容器中Y的质量分数不变
C.X的分解速率与Y的消耗速率相等
D.单位时间内生成1 mol Y的同时生成2 mol X
2.在一定温度下的定容容器中,当下列物理量不再发生变化时:①混合气体的压强,
②混合气体的密度,③混合气体的总物质的量,④混合气体的平均相对分子质量,⑤混合气
体的颜色,⑥各反应物或生成物的浓度之比等于化学计量数之比,⑦某种气体的百分含量
(1)能说明2SO(g)+O(g) 2SO(g)达到平衡状态的是________。
2 2 ⇌ 3
(2)能说明I(g)+H(g) 2HI(g)达到平衡状态的是________。
2 2 ⇌
(3)能说明2NO(g) NO(g)达到平衡状态的是__________。
2 ⇌ 2 4
(4)能说明C(s)+CO(g) 2CO(g)达到平衡状态的是________。
2 ⇌
(5)能说明NHCOONH(s) 2NH(g)+CO(g)达到平衡状态的是________。
2 4 ⇌ 3 2
练点二 可逆反应与平衡观
3.反应2SO +O 2SO 达到平衡后,再向反应容器中充入含氧的同位素 的氧气,
2 2⇌ 3 18O
8
经过一段时间后, 原子存在于( )
18O
8
A.O B.SO
2 2
C.O 和SO D.O、SO 和SO
2 2 2 2 3
4.一定条件下,对于可逆反应X(g)+3Y(g) 2Z(g),若X,Y,Z的起始浓度分别为
⇌
c、c、c(均不为零),达到平衡时,X,Y,Z的浓度分别为0.1 mol·L-1、0.3 mol·L-1、
1 2 3
0.08 mol·L-1,则下列判断正确的是( )
A.c∶c=3∶1
1 2B.平衡时,Y和Z的生成速率之比为2∶3
C.X、Y的转化率不相等
D.c的取值范围为00,其他条件不变时升高温度,反应速率v(CO)和CO
2 ⇌ 2 2
的平衡转化率均增大( )
(5)CO(g)+HO(g) CO(g)+H(g) ΔH<0,在其他条件不变的情况下改变压强,平衡
2 ⇌ 2 2不发生移动,反应放出的热量不变( )
(6)合成氨反应需使用催化剂,说明催化剂可以促进该平衡向生成氨的方向移动( )
[提醒]
“惰性气体”对化学平衡的影响
(1)恒温、恒容条件
原平衡体系――→体系总压强增大―→体系中各组分的浓度不变―→平衡不移动。
(2)恒温、恒压条件
原平衡体系――→容器容积增大,各反应气体的分压减小―→体系中各组分的浓度同
倍数减小(等效于减压)
2对点速练
练点一 影响化学平衡移动的条件
1.将等物质的量的N 、H 气体充入某密闭容器中,在一定条件下,发生如下反应并达
2 2
到平衡:N (g)+3H (g) 2NH (g) ΔH<0。当改变某个条件并维持新条件直至新的平
2 2 ⇌ 3
衡时,下表中关于新平衡与原平衡的比较正确的是( )
选项 改变条件 新平衡与原平衡比较
A 增大压强 N 的浓度一定变小
2
B 升高温度 N 的转化率变小
2
H 的转化率不变,
2
C 充入一定量H
2
N 的转化率变大
2
D 使用适当催化剂 NH 的体积分数增大
3
2.在一体积可变的密闭容器中,加入一定量的 X、Y,发生反应mX(g) nY(g)
⇌
ΔH=Q kJ· mol-1。反应达到平衡时,Y的物质的量浓度与温度、气体体积的关系如下表所
示:下列说法正确的是( )
A.m>n
B.Q<0
C.温度不变,压强增大,Y的质量分数减少
D.体积不变,温度升高,平衡向逆反应方向移动
3.汽车尾气净化中的一个反应如下:
1
NO(g)+CO(g) N(g)+CO(g) ΔH=-373.4 kJ·mol-1
⇌ 2 2
2
在恒容的密闭容器中,反应达平衡后,改变某一条件,填写下列空白:
(1)升温时,平衡 (填“正向”“逆向”或“不”)移动;NO的转化率
(填“增大”或“减小”)。
(2)加压(通入惰性气体)时,平衡 (填“正向”“逆向”或“不”)移动;
CO的转化率 (填“增大”“不变”或“减小”)。
(3)加入催化剂时,平衡 (填“正向”“逆向”或“不”)移动;CO的转
化率 (填“增大”“减小”或“不变”)。
1
4.在密闭容器中,一定条件下进行如下反应:NO(g) +CO(g) N (g)+CO
⇌ 2 2
2
(g) ΔH=-373.4 kJ·mol-1,达到平衡后,为提高NO的转化率和该反应的速率,可采
取的措施是 。
①加催化剂同时升高温度 ②加催化剂同时增大压强 ③升高温度同时充入 N ④降
2
低温度同时增大压强
⑤增大CO的浓度
练后归纳
平衡移动的理解
平衡移动就是由一个“平衡状态→不平衡状态→新平衡状态”的过程。练点二 等效平衡
5.恒温恒压下,在一个容积可变的密闭容器中发生反应:A(g)+B(g) C(g),
⇌
若开始时通入1 mol A和1 mol B,达到平衡时生成a mol C。则下列说法错误的是( )
A.若开始时通入3 mol A和3 mol B,达到平衡时,生成的C的物质的量为3a mol
B.若开始时通入4 mol A、4 mol B和2 mol C,达到平衡时,C的物质的量一定大于
4 mol
C.若开始时通入2 mol A、2 mol B和1 mol C,达到平衡时,再通入3 mol C,则再
a
次达到平衡后,C的物质的量分数为
2−a
D.若在原平衡体系中,再通入1 mol A和1 mol B,混合气体的平均相对分子质量不
变
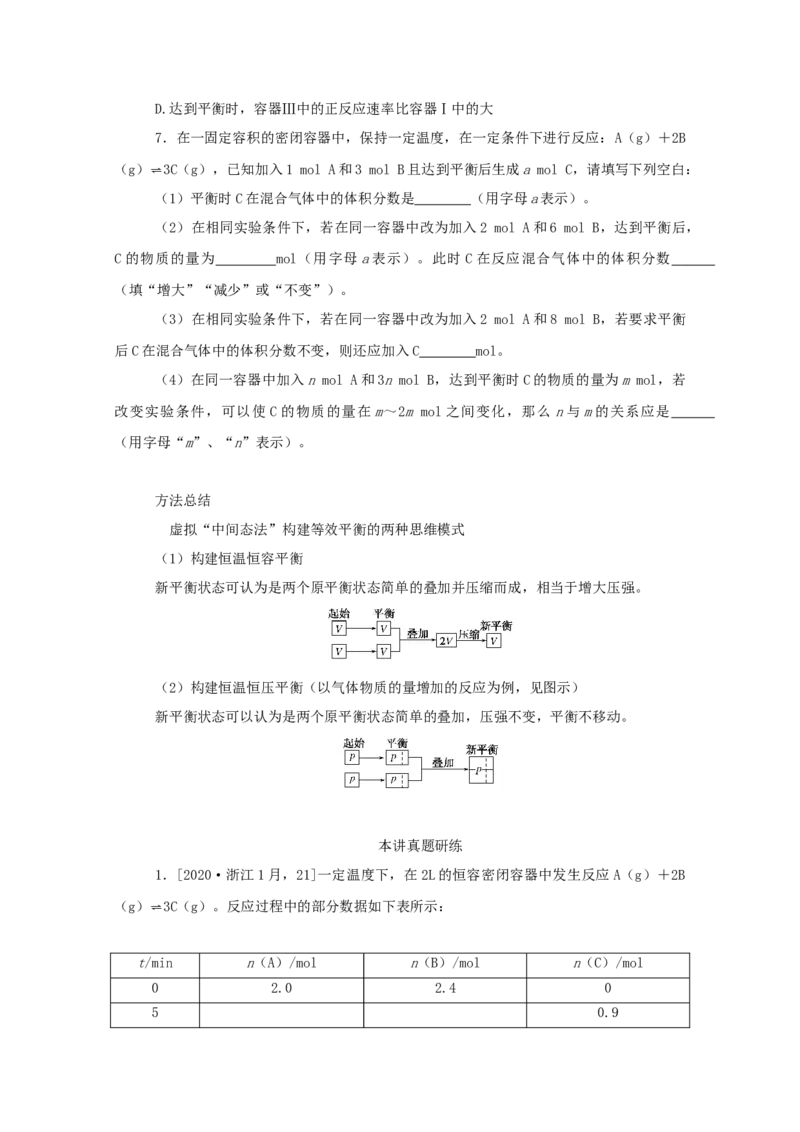
6.一定温度下,在3个体积均为1.0 L的恒容密闭容器中反应2H (g)+CO(g)
2
CHOH(g)达到平衡。下列说法正确的是( )
⇌ 3
A.该反应的正反应吸热
B.达到平衡时,容器Ⅰ中反应物转化率比容器Ⅱ中的大
C.达到平衡时,容器Ⅱ中c(H)大于容器Ⅲ中c(H)的两倍
2 2D.达到平衡时,容器Ⅲ中的正反应速率比容器Ⅰ中的大
7.在一固定容积的密闭容器中,保持一定温度,在一定条件下进行反应:A(g)+2B
(g) 3C(g),已知加入1 mol A和3 mol B且达到平衡后生成a mol C,请填写下列空白:
⇌
(1)平衡时C在混合气体中的体积分数是 (用字母a表示)。
(2)在相同实验条件下,若在同一容器中改为加入2 mol A和6 mol B,达到平衡后,
C的物质的量为 mol(用字母a表示)。此时C在反应混合气体中的体积分数
(填“增大”“减少”或“不变”)。
(3)在相同实验条件下,若在同一容器中改为加入2 mol A和8 mol B,若要求平衡
后C在混合气体中的体积分数不变,则还应加入C mol。
(4)在同一容器中加入n mol A和3n mol B,达到平衡时C的物质的量为m mol,若
改变实验条件,可以使 C的物质的量在m~2m mol之间变化,那么n与m的关系应是
(用字母“m”、“n”表示)。
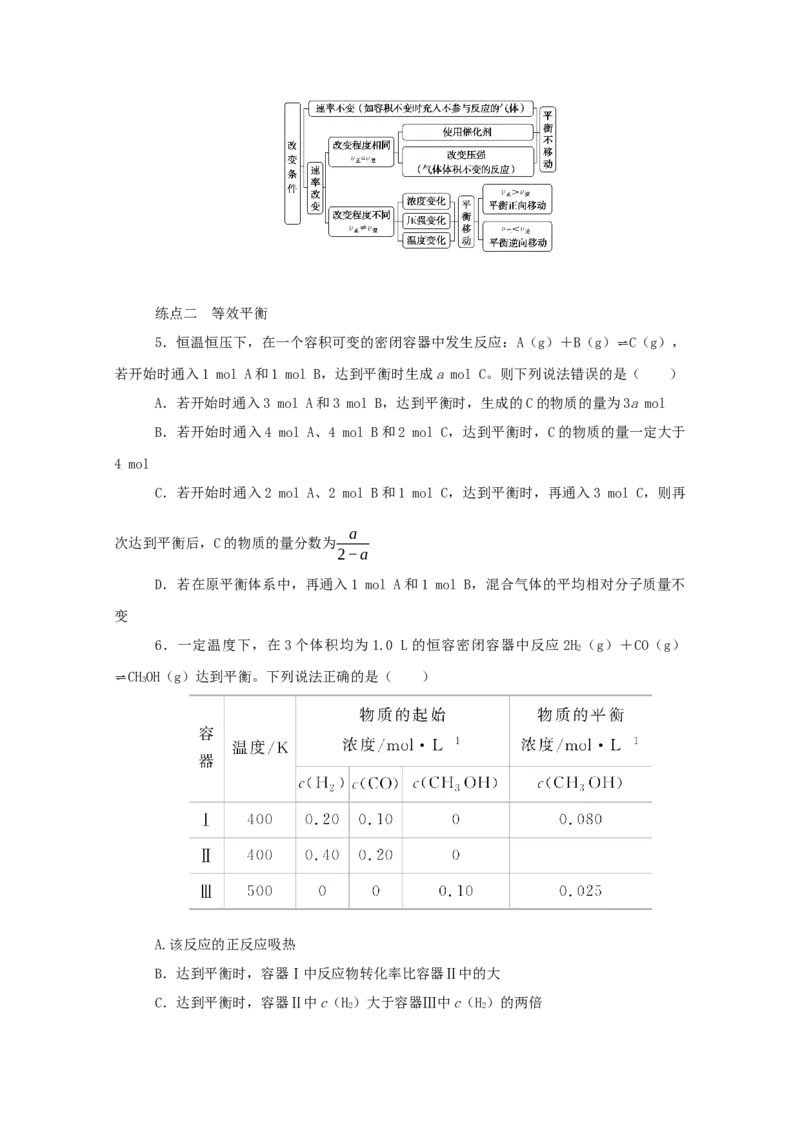
方法总结
虚拟“中间态法”构建等效平衡的两种思维模式
(1)构建恒温恒容平衡
新平衡状态可认为是两个原平衡状态简单的叠加并压缩而成,相当于增大压强。
(2)构建恒温恒压平衡(以气体物质的量增加的反应为例,见图示)
新平衡状态可以认为是两个原平衡状态简单的叠加,压强不变,平衡不移动。
本讲真题研练
1.[2020·浙江1月,21]一定温度下,在2L的恒容密闭容器中发生反应A(g)+2B
(g) 3C(g)。反应过程中的部分数据如下表所示:
⇌
t/min n(A)/mol n(B)/mol n(C)/mol
0 2.0 2.4 0
5 0.910 1.6
15 1.6
下列说法正确的是( )
A.0~5 min用A表示的平均反应速率为0.09 mol·L-1·min-1
B.该反应在10 min后才达到平衡
C.平衡状态时,c(C)=0.6 mol·L-1
D.物质B的平衡转化率为20%
2.[2020·浙江7月,20]一定条件下:2NO (g) NO (g) ΔH<0。在测定NO 的
2 ⇌ 2 4 2
相对分子质量时,下列条件中,测定结果误差最小的是( )
A.温度0 ℃、压强50 kPa
B.温度130 ℃、压强300 kPa
C.温度25 ℃、压强100 kPa
D.温度130 ℃、压强50 kPa
3.[2019·浙江4月,17]下列说法正确的是( )
A.H (g)+I (g) 2HI(g),其他条件不变,缩小反应容器体积,正逆反应速率
2 2 ⇌
不变
B.C(s)+HO(g) H(g)+CO(g),碳的质量不再改变说明反应已达平衡
2 ⇌ 2
C.若压强不再随时间变化能说明反应2A(?)+B(g) 2C(?)已达平衡,则A、
⇌
C不能同时是气体
D.1 mol N 和3 mol H 反应达到平衡时H 转化率为10%,放出热量Q ;在相同温度和
2 2 2 1
压强下,当2 mol NH 分解为N 和H 的转化率为10%时,吸收热量Q,Q 不等于Q
3 2 2 2 2 1
4.[2018·天津卷,5]室温下,向圆底烧瓶中加入1 mol C HOH和含1 mol HBr的氢
2 5
溴酸,溶液中发生反应:CHOH+HBr CHBr+HO,充分反应后达到平衡。已知常压下,
2 5 ⇌ 2 5 2
CHBr和CHOH的沸点分别为38.4 ℃和78.5 ℃。下列有关叙述错误的是( )
2 5 2 5
A.加入NaOH,可增大乙醇的物质的量
B.增大HBr浓度,有利于生成CHBr
2 5
C.若反应物均增大至2 mol,则两种反应物平衡转化率之比不变
D.若起始温度提高至60 ℃,可缩短反应达到平衡的时间
5.[2017·江苏卷,15](双选)温度为T时,在三个容积均为1 L的恒容密闭容器中
1
仅发生反应:2NO (g) 2NO(g)+O (g)(正反应吸热)。实验测得:v =v(NO )
2 ⇌ 2 正 2 消耗
=k c2(NO),v =v(NO) =2v(O) =k c2(NO)·c(O),k 、k 为速率常数,
正 2 逆 消耗 2 消耗 逆 2 正 逆
受温度影响。下列说法正确的是( )A.达平衡时,容器Ⅰ与容器Ⅱ中的总压强之比为4∶5
B.达平衡时,容器Ⅱ中c(O)/c(NO)比容器Ⅰ中的大
2 2
C.达平衡时,容器Ⅲ中NO的体积分数小于50%
D.当温度改变为T时,若k =k ,则T>T
2 正 逆 2 1
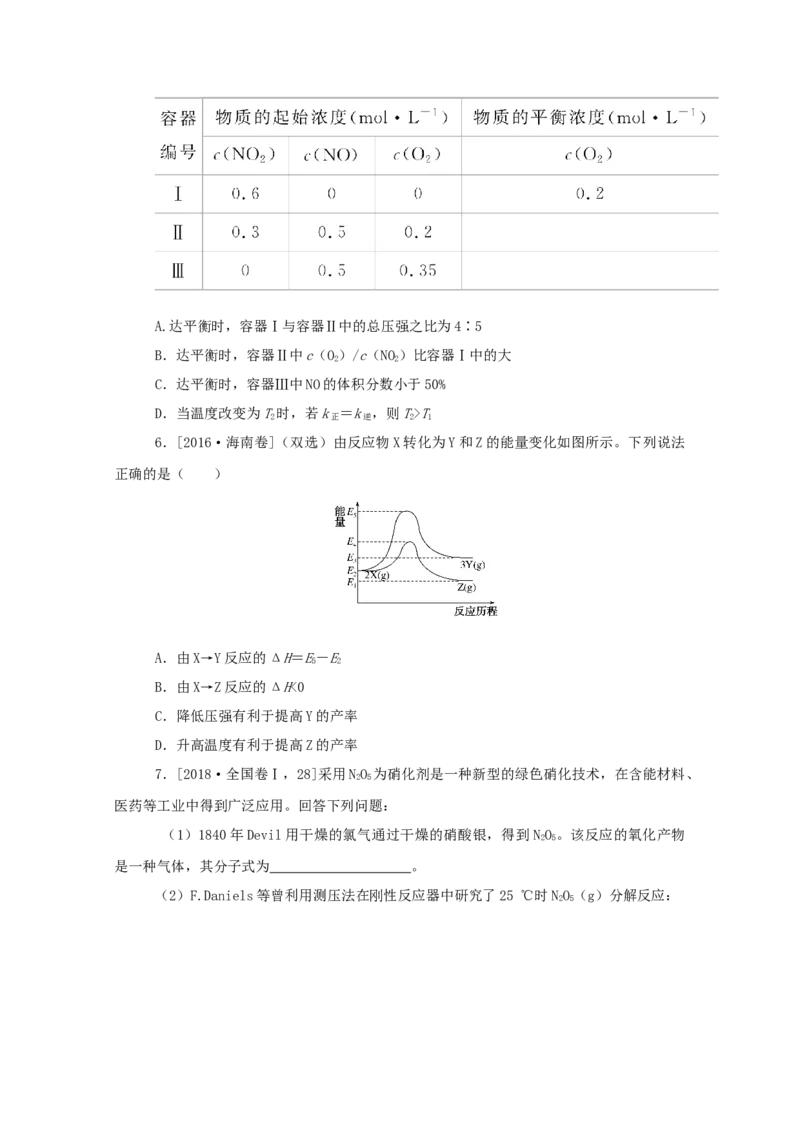
6.[2016·海南卷](双选)由反应物X转化为Y和Z的能量变化如图所示。下列说法
正确的是( )
A.由X→Y反应的ΔH=E-E
5 2
B.由X→Z反应的ΔH<0
C.降低压强有利于提高Y的产率
D.升高温度有利于提高Z的产率
7.[2018·全国卷Ⅰ,28]采用NO 为硝化剂是一种新型的绿色硝化技术,在含能材料、
2 5
医药等工业中得到广泛应用。回答下列问题:
(1)1840年Devil用干燥的氯气通过干燥的硝酸银,得到 NO 。该反应的氧化产物
2 5
是一种气体,其分子式为 。
(2)F.Daniels等曾利用测压法在刚性反应器中研究了25 ℃时NO(g)分解反应:
2 5其中NO 二聚为NO 的反应可以迅速达到平衡。体系的总压强p随时间t的变化如表所
2 2 4
示(t=∞时,NO(g)完全分解):
2 5
t/min 0 40 80 160 260 1 300 1 700 ∞
p/kPa 35.8 40.3 42.5 45.9 49.2 61.2 62.3 63.1
①已知:2NO(g)===2NO(g)+O(g)
2 5 2 4 2
ΔH=-4.4 kJ·mol-1
1
2NO(g)===NO(g) ΔH=-55.3 kJ·mol-1
2 2 4 2
1
则反应NO(g)===2NO(g)+ O(g)的ΔH= kJ·mol-1。
2 5 2 2
2
②研究表明,NO(g)分解的反应速率v=2×10-3×pNO(kPa·min-1)。t=62 min
2 5 2 5
时,测得体系中pO=2.9 kPa,则此时的pNO= kPa,v= kPa·min-1。
2 2 5
③若提高反应温度至 35 ℃,则 NO (g)完全分解后体系压强 p (35 ℃)
2 5 ∞
63.1 kPa ( 填 “ 大 于 ” “ 等 于 ” 或 “ 小 于 ” ) , 原 因 是
________________________________________________________________________。
④25 ℃时NO (g) 2NO (g)反应的平衡常数K= kPa (K为以分压表示
2 4 ⇌ 2 p p
的平衡常数,计算结果保留1位小数)。
(3)对于反应2NO(g)―→4NO(g)+O(g),R.A.Ogg提出如下反应历程:
2 5 2 2
第一步 NO NO+NO 快速平衡
2 5⇌ 2 3
第二步 NO+NO―→NO+NO+O 慢反应
2 3 2 2
第三步 NO+NO―→2NO 快反应
3 2
其中可近似认为第二步反应不影响第一步的平衡。下列表述正确的是 (填标
号)。
A.v(第一步的逆反应)>v(第二步反应)
B.反应的中间产物只有NO
3
C.第二步中NO 与NO 的碰撞仅部分有效
2 3
D.第三步反应活化能较高第2讲 化学平衡状态 化学平衡移动
考点一
1知识梳理
1.(1)同一条件 (2)转化率 (3)
思考 答案:(1)由于2SO
2
+O 22SO
3
为可逆反应,18O存在于O
2
、SO
3
、SO
2
三种物质的
分子中
(2)SO 的相对分子质量可能为64或66或68
2
2.(1)相等 一定 (2)最大 逐渐减小 逐渐增大
判断 答案:(1)× (2)× (3)√ (4)× (5)× (6)× (7)√
2对点速练
1.解析:X的分解速率与Y的消耗速率之比为2:1时,才能说明反应达到平衡状态,C
项说明反应未达到平衡状态。
答案:C
2.答案:(1)①③④⑦ (2)⑤⑦ (3)①③④⑤⑦ (4)①②③④⑦ (5)①②③
3.解析:可逆反应达到平衡状态,正、逆反应并没有停止,所以氧气中的 18O可通过
正反应进入SO 中,SO 中的18O又可通过逆反应而进入SO 中。
3 3 2
答案:D
4.解析:平衡浓度之比为1:3,转化浓度亦为1:3,故c:c=1:3,A、C不正确;平
1 2
衡时Y生成表示逆反应速率,Z生成表示正反应速率且v (Y):v (Z)应为3:2,B不正确;
生成 生成
由可逆反应的特点可知00,B、D项错误。
答案:C
3.答案:(1)逆向 减小 (2)不 不变 (3)不 不变
4.答案:②⑤
5.解析:选项A,开始时通入3 mol A和3 mol B,由于容器体积膨胀,保持恒压,
相当于将三个原容器叠加,各物质的含量与原平衡中的相同,C的物质的量为3a mol,正确;
选项B,无法确定平衡移动的方向,不能确定平衡时B的物质的量一定大于4 mol,错误;选
a
项C,根据题给数据可算出达到平衡时C的物质的量分数为 ,正确;选项D,这种条件
2-a
下混合气体的平均相对分子质量不变。
答案:B
6.解析:对比容器Ⅰ和Ⅲ可知两者投料量相当,若温度相同,最终建立等效平衡,但
Ⅲ温度高,平衡时c(CHOH)小,说明平衡向逆反应方向移动,即逆反应为吸热反应,正反应
3
为放热反应,A错误;Ⅱ相对于Ⅰ成比例增加投料量,相当于加压,平衡正向移动,转化率
提高,所以Ⅱ中转化率高,B错误;不考虑温度,Ⅱ中投料量是Ⅲ的两倍,相当于加压,平
衡正向移动,所以Ⅱ中c(H)小于Ⅲ中c(H)的两倍,且Ⅲ的温度比Ⅱ高,相对于Ⅱ,平衡向
2 2
逆反应方向移动,c(H)增大,C错误;对比Ⅰ和Ⅲ,温度相同,两者建立等效平衡两容器中
2
速率相等,但Ⅲ温度高,速率加快,D正确。
答案:D
7.解析:(1) A(g) + 2B(g) 3C(g)
起始物质的量: 1 mol 3 mol 0
转化物质的量: a/3 mol 2a/3 mol a mol
平衡物质的量: (1-a/3) mol (3-2a/3) mol a mol
a
依题意得C在混合气体中的体积分数是 a 2a =a/4。
1− +3− +a
3 3
(2)C的体积分数不变,物质的量是原来的2倍。
(3)只需将C完全转化为A和B后满足n(A):n(B)=1:3即可。
(4)若C的物质的量为m mol时,求得:n>m/3;若C的物质的量为2m mol时,求得:
n>2m/3;综合两种情况,n与m的关系应是n>2m/3。
答案:(1)a/4 (2)2a 不变 (3)6 (4)n>2m/3本讲真题研练
1.解析:本题考查化学反应速率和化学平衡的简单计算。根据化学方程式及题表中数
据可知,达到平衡时消耗0.4 mol A,消耗0.8 mol B,生成1.2 mol C,则平衡时C的物质
的量为1.2 mol,其物质的量浓度为0.6 mol·L-1,C正确;由反应的化学方程式及题表中数
据可算出0~5 min 内,消耗0.3 mol A,用A表示的平均反应速率为0.03 mol·L-1·min-
1,A错误;根据题表中数据知,0~10 min内消耗0.8 mol B,此时剩余1.6 mol B,则在10
0.8
min 时反应已经达到平衡,B 错误;平衡时消耗 0.8 mol B,则其平衡转化率为
2.4
×100%≈33.3%,D错误。
答案:C
2.解析:本题考查化学平衡知识,考查的化学核心素养是变化观念与平衡思想。测定
NO 的相对分子质量时,NO 越少越好,即使平衡逆向移动。正反应是气体分子数减小的放热
2 2 4
反应,要使平衡逆向移动,需减小压强、升高温度,则选D项。
答案:D
3.解析:对于反应H
2
(g)+I
2
(g)2HI(g),反应前后气体分子数相等,缩小反应容
器体积,平衡不移动,正逆反应速率增大相同的倍数,A项错误;碳的质量不变,说明正、
逆反应速率相等,反应已达平衡状态,B项正确;恒温恒容条件下,若A、C同时为气体,当
压强不变时,也能说明反应达到平衡状态,C项错误;设N
2
(g)+3H
2
(g)2NH
3
(g) ΔH=-
a(a>0) kJ·mol-1,1 mol N 和3 mol H 反应达到平衡时H 转化率为10%,放出热量Q =0.1a
2 2 2 1
kJ,当2 mol NH 分解为N 和H 的转化率为10%时,吸收热量Q=0.1a kJ,故Q=Q,D项错
3 2 2 2 1 2
误,故选B。
答案:B
4.解析:加入NaOH,c(HBr)减小,平衡向逆反应方向移动,乙醇的物质的量增大,A
项正确;增大HBr浓度,平衡向正反应方向移动,有利于生成CHBr,B项正确;若反应物按
2 5
照化学计量数之比加入溶液中,则各物质的平衡转化率相等,故反应物均增大至 2 mol,两
种反应物平衡转化率之比不变,C项正确;若起始温度提高至60 ℃,生成物CHBr为气态,
2 5
能够从反应体系中逸出,导致反应不断向正反应方向进行,因此不能缩短反应达到平衡的时
间,D项错误。
答案:D
5.解析:A项, 2NO
2
(g)2NO(g)+O
2
(g)
c(始)/(mol·L-1) 0.6 0 0
c(变)/(mol·L-1) 0.4 0.4 0.2
c(平)/(mol·L-1) 0.2 0.4 0.2
K===0.8,平衡时气体的总物质的量为0.8 mol。容器Ⅱ中起始气体的总物质的量
为1.0 mol,此时Q==K,平衡逆向移动,故容器Ⅱ中,<1,[另解:
c
容器Ⅱ中投料量相当于0.7 mol NO 、0.1 mol NO,容器Ⅰ中投料量为0.6 mol NO ,容器Ⅱ
2 2
相对于容器Ⅰ相当于多投入 0.1 mol NO ,相当于加压,平衡逆向移动,多投入 0.1 mol
2
NO,平衡逆向移动,减小],错误;C项,容器Ⅰ达到平衡状态时,NO的体积分数为50%,设
容器Ⅲ中平衡时NO的体积分数也为50%,
2NO
2
(g)2NO(g)+O
2
(g)
c(始)/(mol·L-1) 0 0.5 0.35
c(变)/(mol·L-1) x x 0.5x
c(平)/(mol·L-1) x 0.5-x 0.35-0.5x
则有=0.5,x=0.1,此时Q=4.8>K,平衡逆向移动,NO的体积分数小于50%,[另解:
c
容器Ⅲ的投料量改为0.6 mol NO和0.3 mol O ,则建立与容器Ⅰ等效的平衡,现在投料量减
2
少0.1 mol NO,增加0.05 mol O ,造成NO体积分数减小],正确;D项,达到平衡时,
2
v(正)=v(逆),有k c2(NO)=k c2(NO)·c(O),有==K,T时=K=0.8,T时=K=1,K
正 2 逆 2 1 2
值增大,说明平衡向正反应方向移动,正反应是吸热反应,说明温度升高,即T>T,正确。
2 1
答案:CD
6.解析:反应中的能量变化决定于反应物和生成物所具有的总能量的相对大小,由图
可知,X→Y反应的ΔH=E-E,X→Z反应的ΔH=E-E<0,反应放热,A项错误,B项正确;
3 2 1 2
由X生成Y的反应,即2X(g)3Y(g),是气体物质的量增大的反应,降低压强、平衡正向移
动,有利于提高Y的产率,C正确;X→Z的反应是放热反应,升高温度平衡逆向移动,不利
于提高Z的产率,D错误。
答案:BC
7.解析:(1)氯气与硝酸银反应生成NO ,氯气作氧化剂,还原产物为氯化银,又硝
2 5
酸银中氮元素、银元素已经是最高化合价,则只能是氧元素化合价升高,所以气体氧化产物
为O。
2
1
(2)① 将已知热化学方程式依次编号为 a、b,根据盖斯定律,由 ×a-b 得
2
1
NO(g)===2NO(g)+ O(g) ΔH== kJ·mol-1=+53.1 kJ·mol-1。②t=62 min时,体
2 5 2 2 2
系中pO=2.9 kPa,根据三段式法得
2
2N
2
O
5
(g)2N
2
O
4
(g)+O
2
(g)
起始 35.8 kPa 0 0
转化 5.8 kPa 5.8 kPa 2.9 kPa
62 min 30.0 kPa 5.8 kPa 2.9 kPa
则62 min时pNO =30.0 kPa,v=2×10-3×30.0 kPa·min-1=6.0×10-2 kPa·min-
2 5
1。③刚性反应容器的体积不变,25 ℃ N O(g)完全分解时体系的总压强为63.1 kPa,升高
2 5
温度,从两个方面分析:一方面是体积不变,升高温度,体系总压强增大;另一方面,2NO 2N
2
O
4
的逆反应是吸热反应,升温,平衡向生成NO
2
的方向移动,体系物质的量增大,
故体系总压强增大。④NO 完全分解生成NO 和O ,起始pNO =35.8 kPa,其完全分解时
2 5 2 4 2 2 5
pNO=35.8 kPa,pO=17.9 kPa,设25 ℃平衡时NO 转化了x,则
2 4 2 2 4
NO 2NO
2 4 2
平衡 35.8 kPa-x 2x
35.8 kPa-x+2x+17.9 kPa=63.1 kPa,解得x=9.4 kPa。平衡时,pNO =26.4
2 4
kPa,pNO=18.8 kPa,K==kPa=13.4 kPa。
2
(3)快速平衡,说明第一步反应的正、逆反应速率都较大,则第一步反应的逆反应速率
大于第二步反应的速率,A项正确;反应的中间产物除NO 外还有NO,B项错误;有效碰撞才
3
能发生反应,第二步反应慢,说明部分碰撞有效,C项正确;第三步反应快,说明反应活化
能较低,D项错误。
答案:(1)O
2
(2)①+53.1 ②30.0 6.0×10-2 ③大于 温度提高,体积不变,总压强增大;NO
2
二聚为放热反应,温度提高,平衡左移,体系物质的量增加,总压强增大 ④13.4
(3)AC