文档内容
第 3 讲 离子反应的应用
复习目标 1.掌握离子共存的条件,会判断溶液中离子能否大量共存。2.掌握常见离子的
检验,能根据实验现象推断溶液中的某些离子。
考点一 离子共存的判断
1.离子共存的本质
几种离子在同一溶液中能大量共存,就是指离子之间不发生任何反应;若离子之间能发生反
应,则不能大量共存。
2.判断离子能否大量共存的“四个要点”
判断多种离子能否大量共存于同一溶液中,归纳起来就是:一色、二性、三特殊、四反应。
(1)一色——溶液颜色
几种常见离子的颜色:
离子 Cu2+ Fe3+ Fe2+ MnO
溶液颜色 蓝色 棕黄色 浅绿色 紫红色
(2)二性——溶液的酸碱性
①在酸性溶液中,OH-及弱酸根阴离子(如CO、SO、S2-、CHCOO-等)不能大量存在。
3
②在碱性溶液中,H+及弱碱阳离子(如NH、Al3+、Fe3+等)不能大量存在。
(3)三特殊——三种特殊情况:
①AlO与HCO不能大量共存:AlO+HCO+HO===Al(OH) ↓+CO。
2 3
②“NO+H+”组合具有强氧化性,能与S2-、Fe2+、I-、SO等还原性的离子发生氧化还原
反应而不能大量共存。
③NH与CHCOO-、CO,Mg2+与HCO等组合中,虽然两种离子都能水解且水解相互促进,
3
但总的水解程度仍很小,它们在溶液中仍能大量共存。
(4)四反应——四种反应类型
四反应是指离子间通常能发生的四种类型的反应,能相互反应的离子显然不能大量共存。
①复分解反应:如Ba2+与SO,NH与OH-,H+与CHCOO-等。
3
②氧化还原反应:如Fe3+与I-、S2-,NO(H+)与Fe2+等。
③相互促进的水解反应:如Al3+与CO、HCO或AlO等。
④络合反应:如Fe3+与SCN-等。一、判断离子共存,注意附加条件
1.下列溶液中,离子一定能大量共存的有哪些?
(1)使酚酞溶液变红的溶液:Na+、Cl-、SO、Fe3+
(2)使紫色石蕊溶液变红的溶液:Fe2+、Mg2+、NO、Cl-
(3)常温下,c(H+)=1×10-13 mol·L-1的溶液中:NH、Al3+、SO、NO
(4)碳酸氢钠溶液:K+、SO、Cl-、H+
(5)含大量Fe3+的溶液中:NH、Na+、Cl-、SCN-
(6)强碱溶液中:Na+、K+、AlO、CO
(7)常温下,pH=1的溶液中:K+、Fe2+、Cl-、NO
(8)加入铝粉有氢气产生的溶液中:K+、Na+、CO、SO
(9)由水电离出的c (H+)=1×10-12 mol·L-1的溶液:Na+、K+、Cl-、NO
水
(10)c(H+)∶c(OH-)=1∶10-2的溶液:K+、Ba2+、ClO-、CO
(11)澄清透明的溶液中:Fe3+、Mg2+、Br-、Cl-
答案 (6)、(9)、(11)
溶液中离子共存的判断技巧
(1)审清题干要求的关键词语,如“一定大量共存”“可能大量共存”或“不能大量共存”
等。
(2)规避颜色陷阱,如“无色溶液”“透明溶液”等。
(3)注意离子共存的条件,如酸性、碱性及特殊离子存在。
二、因氧化还原反应不能大量共存的离子判断
2.(1)判断下表中所列离子能否发生氧化还原反应,能反应的打“√”,不能反应的打
“×”。
S2- SO I- Fe2+ Br- Cl-
MnO(H+) √ √ √ √ √ √
ClO- √ √ √ √ √ √(酸性)
NO(H+) √ √ √ √ — —
Fe3+ √ √ √ × × ×
(2)S2-与SO,Cl—与ClO—在碱性条件下能否大量共存:________(填“能”或“不能”)。写
出上述两组离子在酸性条件下反应的离子方程式:________________________________、
_____________________________________________________________________________。
答案 能 2S2-+SO+6H+===3S↓+3HO Cl-+ClO-+2H+===Cl↑+HO
2 2 2考点二 离子的检验和推断
1.常见阳离子的检验与推断依据
根据离子性质不同而在实验中所表现出的现象不同,可以把检验离子的方法归纳为三种类型:
①生成沉淀;②生成气体;③显现特殊颜色。
(1)依据生成的沉淀检验或推断
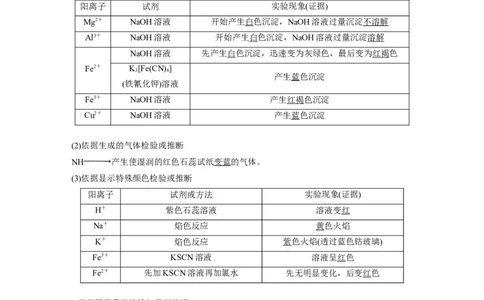
阳离子 试剂 实验现象(证据)
Mg2+ NaOH溶液 开始产生白色沉淀,NaOH溶液过量沉淀不溶解
Al3+ NaOH溶液 开始产生白色沉淀,NaOH溶液过量沉淀溶解
NaOH溶液 先产生白色沉淀,迅速变为灰绿色,最后变为红褐色
Fe2+ K[Fe(CN) ]
3 6
产生蓝色沉淀
(铁氰化钾)溶液
Fe3+ NaOH溶液 产生红褐色沉淀
Cu2+ NaOH溶液 产生蓝色沉淀
(2)依据生成的气体检验或推断
NH―――――→产生使湿润的红色石蕊试纸变蓝的气体。
(3)依据显示特殊颜色检验或推断
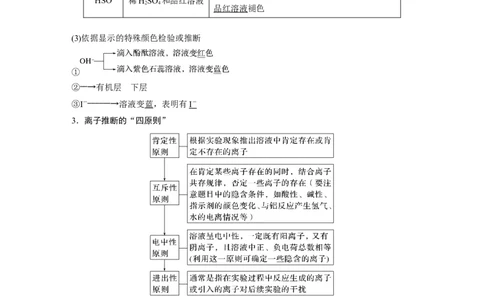
阳离子 试剂或方法 实验现象(证据)
H+ 紫色石蕊溶液 溶液变红
Na+ 焰色反应 黄色火焰
K+ 焰色反应 紫色火焰(透过蓝色钴玻璃)
Fe3+ KSCN溶液 溶液呈红色
Fe2+ 先加KSCN溶液再加氯水 先无明显变化,后变红色
2.常见阴离子的检验与推断依据
(1)依据生成的沉淀检验或推断
阴离子 试剂 实验现象(证据)
Cl- 产生白色沉淀:AgCl
Br- AgNO 溶液和稀HNO 产生淡黄色沉淀:AgBr
3 3
I- 产生黄色沉淀:AgI
SO 稀盐酸和BaCl 溶液 加稀盐酸无明显现象,再加BaCl 溶液产生白色沉淀
2 2
CO CaCl 2 溶液和稀盐酸 加CaCl 2 溶液产生白色沉淀,再加稀盐酸沉淀溶解,产生无色无味气体
(2)依据生成的气体检验或推断
阴离子 试剂 实验现象(证据)
CO 稀盐酸和澄清石灰水 产生无色、无味能使澄清石灰水变浑浊的气体
HCO 稀盐酸和澄清石灰水 产生无色、无味能使澄清石灰水变浑浊的气体
加稀硫酸产生有刺激性气味的气体,且气体能使
SO 稀HSO 和品红溶液
2 4
品红溶液褪色
加稀硫酸产生有刺激性气味的气体,且气体能使
HSO 稀HSO 和品红溶液
2 4
品红溶液褪色
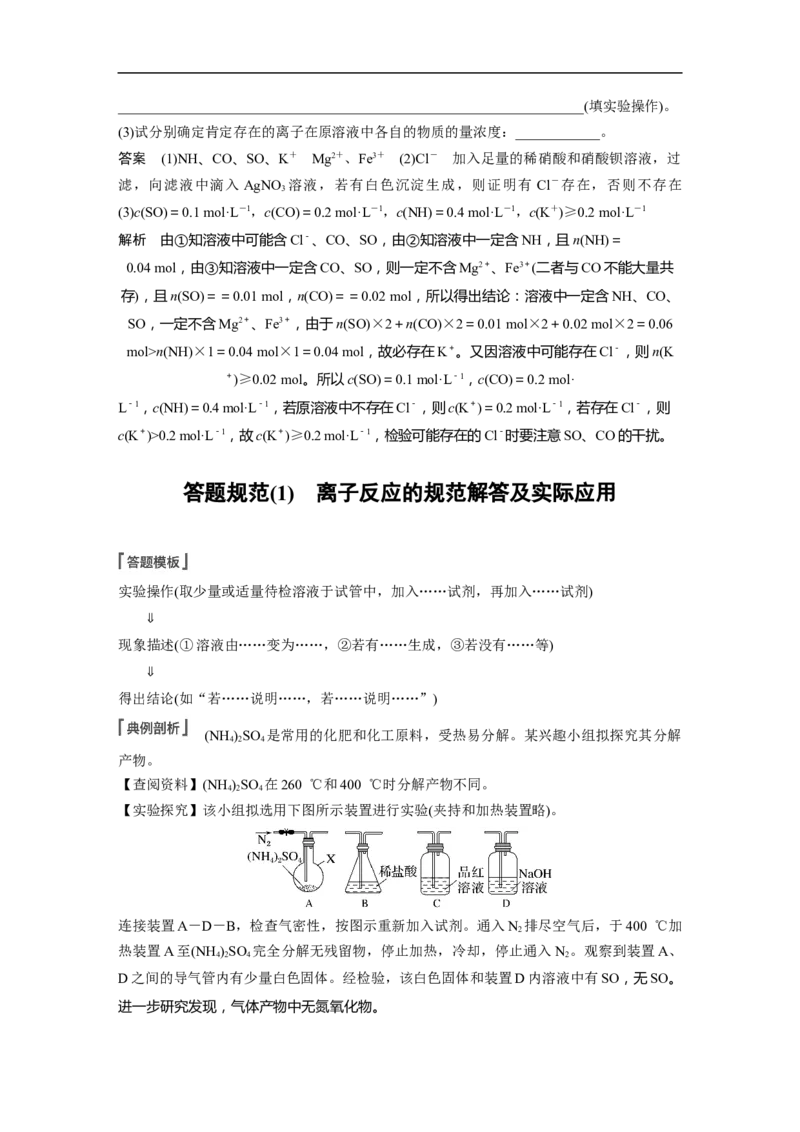
(3)依据显示的特殊颜色检验或推断
①
②――→有机层下层
③I-――――――→溶液变蓝,表明有 I -
3.离子推断的“四原则”
1.向某溶液中加入BaCl 溶液,有白色沉淀生成,再加入稀盐酸,沉淀不消失,则溶液中
2
一定存在SO( )
2.向某溶液中加入Ba(NO ) 溶液,产生不溶于稀HNO 的白色沉淀,则溶液中一定存在
3 2 3
SO( )
3.向某溶液中加入Ca(OH) 溶液,有白色沉淀生成,则溶液中一定存在CO( )
2
4.某溶液的焰色反应呈黄色,则溶液中一定有钠元素,不能确定是否有钾元素( )
5.无色溶液加入CCl 无现象,滴加氯水后CCl 层呈紫红色,则溶液中一定存在I-( )
4 46.向某溶液中加入稀盐酸,产生能使澄清石灰水变浑浊的气体,溶液中一定存在CO( )
答案 1.× 2.× 3.× 4.√ 5.√ 6.×
一、常见离子的检验及干扰因素的识别
1.下列关于离子检验的说法正确的是( )
A.检验溶液中是否含有Ba2+:取少量待测液,向其中加入少量稀硫酸,若有白色沉淀产生,
则溶液中含有Ba2+
B.检验用硫酸亚铁制得的硫酸铁中是否含有硫酸亚铁,可选用的试剂是酸性KMnO 溶液
4
C.检验溶液中是否含有CO:取少量待测液,向其中加入适量稀盐酸,观察是否有大量气
泡产生
D.在未知溶液中滴加BaCl 溶液出现白色沉淀,加稀硝酸,沉淀不溶解,说明该未知溶液
2
中存在SO或SO
答案 B
解析 如果溶液中含有Ca2+、Ag+等,向其中加入少量稀硫酸,会有硫酸钙、硫酸银等白色
沉淀产生,所以不能确定溶液中含有Ba2+,A项错误;硫酸亚铁可将酸性KMnO 还原而使
4
酸性KMnO 溶液褪色,B项正确;HCO、SO、HSO遇稀盐酸也可产生大量气泡,C项错误;
4
若存在Ag+,加入BaCl 溶液会产生氯化银白色沉淀,D项错误。
2
2.下列离子在未知溶液中的检验方法正确的是( )
选项 离子 检验方法
向样品中加入足量盐酸,将生成的无色无味的气体通入澄清石灰水中,
A CO
观察溶液是否变浑浊
向样品中先加入稀硝酸酸化,再滴加氯化钡溶液,观察是否有白色沉淀
B SO
生成
C Fe2+ 取少量溶液于试管中,加入酸性高锰酸钾溶液,观察溶液紫色是否褪去
取少量溶液于试管中,加入新制氯水,再加入淀粉溶液,观察溶液是否
D I-
变蓝色
答案 D
解析 A项,HCO会产生干扰,错误;B项,SO会产生干扰,错误;C项,使酸性高锰酸
钾溶液褪色的不一定是Fe2+,如SO等,错误;D项,氯气能把I-氧化成I ,淀粉遇碘变蓝,
2
因此可以检验I-的存在,正确。
离子检验中的常见干扰离子以及排除措施
待检离子 干扰离子 排除措施SO 加过量的Ba(NO ) 溶液
3 2
Cl- CO
加稀硝酸酸化
OH-
CO
SO SO 加盐酸酸化
Ag+
SO CO 加盐酸后将产生的气体通入品红溶液中,溶液褪色
CO SO 加硝酸后将产生的无色无味气体通入澄清石灰水中,溶液变浑浊
二、依据图像推断离子
3.某澄清溶液中含有下表离子中的一种或多种。
阳离子 Fe2+、Fe3+、Al3+
阴离子 SO、CO、SiO、I-、NO
分别取它的水溶液两份进行实验,结果如下:
①向一份溶液中加入过量盐酸,产生气泡,溶液颜色变深,但仍澄清;
②继续向①溶液中加入少许四氯化碳,振荡,静置,下层呈现紫红色,上层溶液呈现黄色;
③向另一份溶液中加入过量氢氧化钠溶液,产生沉淀质量与加入碱液的体积关系如图所示。
根据以上信息,回答下列问题:
(1)原溶液中肯定含有的离子是______________。
(2)①中生成的气体是____________(填化学符号),它具有的性质是____________(填字母)。
A.无色无味 B.能被NaOH溶液吸收
C.属于大气污染物 D.难溶于水
(3)①中发生反应的离子方程式有__________________________________________________。
(4)③中沉淀溶解的化学方程式是_______________________________________________。
答案 (1)Fe2+、Al3+、I-、NO
(2)NO ACD
(3)6I-+2NO+8H+===3I+2NO↑+4HO、
2 2
3Fe2++NO+4H+===3Fe3++NO↑+2HO
2
(4)Al(OH) +NaOH===NaAlO +2HO
3 2 2
解析 ①加入过量的盐酸,产生气泡,溶液颜色加深,但溶液仍为澄清,说明原溶液中一定
不含有SiO;②向①反应后溶液中加入少量CCl ,出现分层,下层为CCl 层,显紫红色,
4 4推出该溶液中含有I,即原溶液中含有I-,Fe3+具有强氧化性,能将I-氧化,因此原溶液中
2
一定不含有Fe3+,NO在酸性条件下具有强氧化性,将I-氧化成I ,本身被还原成NO,因
2
此原溶液一定含有NO,上层为水层,水层显黄色,则含有Fe3+,即原溶液中含有Fe2+,原
溶液中一定不含有CO;③根据图像推出原溶液中含有Al3+,溶液中一定不含有SO。
(1)根据上述分析,肯定含有的离子是Al3+、Fe2+、I-、NO;(2)①利用NO在酸性条件下具有
强氧化性,将Fe2+、I-氧化,离子方程式为6I-+2NO+8H+===3I +2NO↑+4HO、3Fe2+
2 2
+NO+4H+===3Fe3++NO↑+2HO,即①中产生的气体为NO,NO是一种无色、无味、
2
难溶于水,有毒的气体,不能与NaOH发生反应,故选项A、C、D正确。
(3)根据问题(2)的分析,可得离子方程式。
(4)向溶液中加入 NaOH 溶液,发生 Fe2++2OH -===Fe(OH) ↓、Al3++3OH -
2
===Al(OH) ↓,Al(OH) 呈两性,继续加入NaOH,发生Al(OH) +OH-===AlO+2HO。
3 3 3 2
三、从定性、定量的角度推断离子或物质
4.一瓶无色澄清的溶液,其中可能含有H+、NH、Na+、Al3+、Fe3+、I-、NO、CO、SO、
AlO。取该溶液进行以下实验:
①用pH试纸检验,溶液呈强酸性 ②取溶液适量,加入少量CCl 和数滴新制氯水,振荡,
4
CCl 层呈紫红色 ③该溶液的焰色反应没有黄色;根据以上实验结果,下列推断正确的是(
4
)
A.向该溶液中加入BaCl 不一定能观察到白色沉淀
2
B.可以确定没有Na+、Fe3+、CO、AlO,不能确定是否有NO
C.该溶液可能是NH NO 与HI的混合
4 3
D.一定没有Al3+、CO和NO
答案 A
解析 不能确定是否含SO,则向该溶液中加入BaCl 不一定能观察到白色沉淀,故A正确;
2
一定不含Na+、Fe3+、NO、CO、AlO,故B错误;该溶液中一定不含NO,故C错误;不
能确定是否含Al3+,故D错误。
5.有一混合物的水溶液,可能含有以下离子中的若干种:K+、NH、Cl-、Mg2+、Fe3+、
CO、SO,现取三份各100 mL溶液进行如下实验:
①向第一份中加入AgNO 溶液,有白色沉淀产生;
3
②向第二份中加入足量NaOH溶液后加热,收集到气体 0.896 L(标准状况);
③向第三份中加入足量BaCl 溶液,得到沉淀6.27 g,沉淀经足量盐酸洗涤后,剩余2.33
2
g。
试回答下列问题:
(1)肯定存在的离子有________,肯定不存在的离子有____________。
(2)可能存在的离子是________,为确定该离子是否存在,可取少许原溶液,然后
______________________________________________________________________________(填实验操作)。
(3)试分别确定肯定存在的离子在原溶液中各自的物质的量浓度:____________。
答案 (1)NH、CO、SO、K+ Mg2+、Fe3+ (2)Cl- 加入足量的稀硝酸和硝酸钡溶液,过
滤,向滤液中滴入 AgNO 溶液,若有白色沉淀生成,则证明有 Cl-存在,否则不存在
3
(3)c(SO)=0.1 mol·L-1,c(CO)=0.2 mol·L-1,c(NH)=0.4 mol·L-1,c(K+)≥0.2 mol·L-1
解析 由①知溶液中可能含Cl-、CO、SO,由②知溶液中一定含NH,且n(NH)=
0.04 mol,由③知溶液中一定含CO、SO,则一定不含Mg2+、Fe3+(二者与CO不能大量共
存),且n(SO)==0.01 mol,n(CO)==0.02 mol,所以得出结论:溶液中一定含NH、CO、
SO,一定不含Mg2+、Fe3+,由于n(SO)×2+n(CO)×2=0.01 mol×2+0.02 mol×2=0.06
mol>n(NH)×1=0.04 mol×1=0.04 mol,故必存在K+。又因溶液中可能存在Cl-,则n(K
+)≥0.02 mol。所以c(SO)=0.1 mol·L-1,c(CO)=0.2 mol·
L-1,c(NH)=0.4 mol·L-1,若原溶液中不存在Cl-,则c(K+)=0.2 mol·L-1,若存在Cl-,则
c(K+)>0.2 mol·L-1,故c(K+)≥0.2 mol·L-1,检验可能存在的Cl-时要注意SO、CO的干扰。
答题规范(1) 离子反应的规范解答及实际应用
实验操作(取少量或适量待检溶液于试管中,加入……试剂,再加入……试剂)
⇓
现象描述(①溶液由……变为……,②若有……生成,③若没有……等)
⇓
得出结论(如“若……说明……,若……说明……”)
(NH )SO 是常用的化肥和化工原料,受热易分解。某兴趣小组拟探究其分解
4 2 4
产物。
【查阅资料】(NH )SO 在260 ℃和400 ℃时分解产物不同。
4 2 4
【实验探究】该小组拟选用下图所示装置进行实验(夹持和加热装置略)。
连接装置A-D-B,检查气密性,按图示重新加入试剂。通入N 排尽空气后,于400 ℃加
2
热装置A至(NH )SO 完全分解无残留物,停止加热,冷却,停止通入N 。观察到装置A、
4 2 4 2
D之间的导气管内有少量白色固体。经检验,该白色固体和装置D内溶液中有SO,无SO。
进一步研究发现,气体产物中无氮氧化物。检验装置D内溶液中有SO,无SO的实验操作和现象是____________________________。
解题思路 (1)明确原理:依据题目要求,明确检验的原理,根据原理确定方法。如SO、SO
都与Ba2+产生沉淀,但BaSO 可溶于盐酸而BaSO 不溶于盐酸。
3 4
(2)叙述操作:取液体(水层少量液体)、加试剂(如加BaCl 溶液、加盐酸酸化等)。
2
(3)描述现象:观察产生沉淀及沉淀如何变化要明确具体。
(4)得出结论:由什么现象得出对应结论,如“若……说明……,若……说明……”。
答案 取少量装置D内溶液于试管中,滴加BaCl 溶液,生成白色沉淀,加入足量稀盐酸后,
2
沉淀完全溶解,放出无色有刺激性气味的气体
1.按要求回答下列问题:
(1)结晶析出NaSO·5H O,其中可能含有NaSO 、NaSO 等杂质。利用所给试剂设计实验,
2 2 3 2 2 3 2 4
检测产品中是否存在NaSO ,简要说明实验操作、现象和结论:_____________________。
2 4
已知NaSO·5H O遇酸易分解:SO+2H+===S↓+SO ↑+HO
2 2 3 2 2 2 2
供选择的试剂:稀盐酸、稀硫酸、稀硝酸、BaCl 溶液、AgNO 溶液
2 3
(2)榴石矿石可以看作由CaO、FeO、Fe O 、Al O 、SiO 组成。试设计实验证明榴石矿石中
2 3 2 3 2
含 有 FeO( 试 剂 任 选 , 说 明 实 验 操 作 与 现 象 ) :
_________________________________________。
答案 (1)取少量产品溶于足量稀盐酸,静置,取上层溶液(或过滤,取滤液)于一试管中,滴
加BaCl 溶液,若产生白色沉淀则说明含有NaSO 杂质(合理即可)
2 2 4
(2)取矿石少许,加稀硫酸充分溶解后,向其中滴加酸性高锰酸钾溶液,若紫色褪去,证明
矿石中含有FeO(不能加盐酸溶解)
2.为了探究AgNO 的氧化性,某化学兴趣小组设计了如下实验。
3
将光亮的铁丝伸入AgNO 溶液中,一段时间后将铁丝取出。为检验溶液中Fe的氧化产物,
3
将溶液中的Ag+除尽后,进行了如下实验,可选用试剂:KSCN溶液、K[Fe(CN) ]溶液、氯
3 6
水。
请完成下表:
操作 现象 结论
取少量除尽Ag+后的溶液于试管
存在Fe3+
中,加入KSCN溶液,振荡
取少量除尽Ag+后的溶液于试管
存在Fe2+
中,加入________,振荡
【实验结论】 Fe的氧化产物为Fe2+和Fe3+。
答案 溶液呈红色 K[Fe(CN) ]溶液 产生蓝色沉淀
3 6
解析 Fe3+遇KSCN 溶液,溶液变红色。由于氯水与 Fe2+反应现象不明显,应直接用
K[Fe(CN) ]溶液检验,如有蓝色沉淀出现,则证明Fe2+存在,否则不存在。
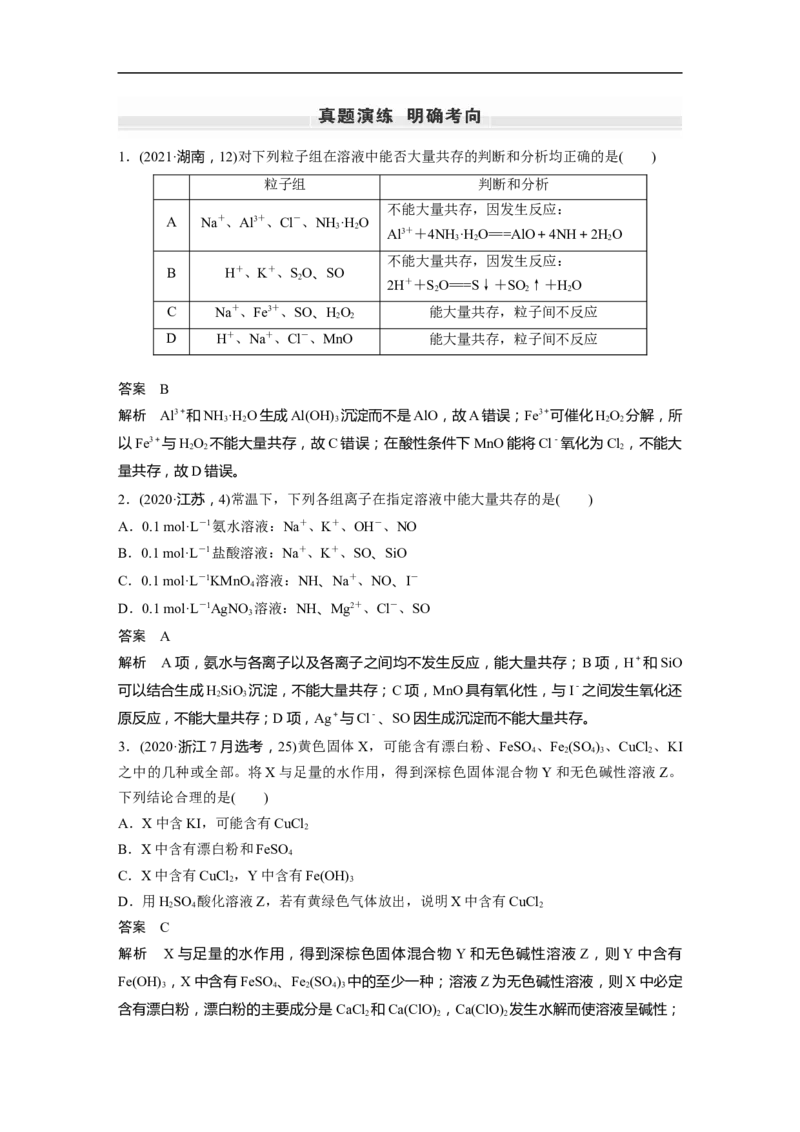
3 61.(2021·湖南,12)对下列粒子组在溶液中能否大量共存的判断和分析均正确的是( )
粒子组 判断和分析
不能大量共存,因发生反应:
A Na+、Al3+、Cl-、NH ·H O
3 2
Al3++4NH ·H O===AlO+4NH+2HO
3 2 2
不能大量共存,因发生反应:
B H+、K+、SO、SO
2
2H++SO===S↓+SO ↑+HO
2 2 2
C Na+、Fe3+、SO、HO 能大量共存,粒子间不反应
2 2
D H+、Na+、Cl-、MnO 能大量共存,粒子间不反应
答案 B
解析 Al3+和NH ·H O生成Al(OH) 沉淀而不是AlO,故A错误;Fe3+可催化HO 分解,所
3 2 3 2 2
以Fe3+与HO 不能大量共存,故C错误;在酸性条件下MnO能将Cl-氧化为Cl ,不能大
2 2 2
量共存,故D错误。
2.(2020·江苏,4)常温下,下列各组离子在指定溶液中能大量共存的是( )
A.0.1 mol·L-1氨水溶液:Na+、K+、OH-、NO
B.0.1 mol·L-1盐酸溶液:Na+、K+、SO、SiO
C.0.1 mol·L-1KMnO 溶液:NH、Na+、NO、I-
4
D.0.1 mol·L-1AgNO 溶液:NH、Mg2+、Cl-、SO
3
答案 A
解析 A项,氨水与各离子以及各离子之间均不发生反应,能大量共存;B项,H+和SiO
可以结合生成HSiO 沉淀,不能大量共存;C项,MnO具有氧化性,与I-之间发生氧化还
2 3
原反应,不能大量共存;D项,Ag+与Cl-、SO因生成沉淀而不能大量共存。
3.(2020·浙江7月选考,25)黄色固体X,可能含有漂白粉、FeSO 、Fe (SO ) 、CuCl 、KI
4 2 4 3 2
之中的几种或全部。将X与足量的水作用,得到深棕色固体混合物Y和无色碱性溶液Z。
下列结论合理的是( )
A.X中含KI,可能含有CuCl
2
B.X中含有漂白粉和FeSO
4
C.X中含有CuCl ,Y中含有Fe(OH)
2 3
D.用HSO 酸化溶液Z,若有黄绿色气体放出,说明X中含有CuCl
2 4 2
答案 C
解析 X与足量的水作用,得到深棕色固体混合物 Y和无色碱性溶液 Z,则 Y中含有
Fe(OH) ,X中含有FeSO 、Fe (SO ) 中的至少一种;溶液Z为无色碱性溶液,则X中必定
3 4 2 4 3
含有漂白粉,漂白粉的主要成分是CaCl 和Ca(ClO) ,Ca(ClO) 发生水解而使溶液呈碱性;
2 2 2Fe(OH) 呈红褐色,而Y是深棕色固体混合物,它除含Fe(OH) 外,还应含有Cu(OH) ,则
3 3 2
X中含CuCl ;在水溶液中Cu2+与I-会发生反应:2Cu2++4I-===2CuI↓+I ,则X中不含
2 2
KI。综上所述,X中含有漂白粉、CuCl ,不含KI,含FeSO 、Fe (SO ) 中的至少一种,
2 4 2 4 3
A、B错误,C正确;由于溶液Z中含CaCl 、Ca(ClO) ,用HSO 酸化,发生反应:Cl-+
2 2 2 4
ClO-+2H+===Cl↑+HO,产生黄绿色气体Cl,不能证明X中含CuCl ,D错误。
2 2 2 2
4.(2019·上海,12)能证明亚硫酸钠部分变质所需要的试剂是( )
A.硝酸钡,稀硫酸 B.稀盐酸,氯化钡
C.稀硫酸,氯化钡 D.稀硝酸,氯化钡
答案 B
解析 若要证明亚硫酸钠部分变质,须证明该样品中含有 NaSO 和NaSO ,检验步骤:取
2 3 2 4
少量样品置于试管中溶解,滴入盐酸后有气泡冒出,继续滴加盐酸至无气泡冒出后,再滴入
少量BaCl 溶液,有白色沉淀产生,则证明NaSO 部分变质。
2 2 3
5.(2016·全国卷Ⅱ,12)某白色粉末由两种物质组成,为鉴别其成分进行如下实验:
①取少量样品加入足量水仍有部分固体未溶解;再加入足量稀盐酸,有气泡产生,固体全部
溶解;
②取少量样品加入足量稀硫酸有气泡产生,振荡后仍有固体存在。
该白色粉末可能为( )
A.NaHCO 、Al(OH) B.AgCl、NaHCO
3 3 3
C.NaSO 、BaCO D.NaCO、CuSO
2 3 3 2 3 4
答案 C
解析 A项,向NaHCO 、Al(OH) 中加入足量稀硫酸有气泡产生,生成硫酸钠、硫酸铝、
3 3
二氧化碳和水,最终无固体存在,错误;B项,AgCl不溶于酸,固体不能全部溶解,错误;
C项,向亚硫酸钠和碳酸钡中加入足量水,碳酸钡不溶于水,加入稀盐酸,碳酸钡与盐酸反
应生成氯化钡、二氧化碳和水,固体全部溶解,再将样品加入足量稀硫酸,稀硫酸和碳酸钡
反应生成硫酸钡沉淀、二氧化碳和水,正确;D项,向NaCO 、CuSO 中加入足量稀硫酸,
2 3 4
振荡后无固体存在,错误。
课时精练
1.已知某溶液中存在H+、Ba2+、Fe3+三种阳离子,则其中可能大量存在的阴离子是( )
A.SO B.CO C.NO D.OH-
答案 C
2.(2022·漳州质检)常温下,下列各组离子能大量共存的是( )
A.Mg2+、Na+、MnO、SOB.Fe2+、NH、NO、H+
C.OH-、Na+、SO、Cu2+
D.Al3+、K+、CO、Cl-
答案 A
解析 Fe2+和NO、H+三者发生氧化还原反应不共存,B项错误;OH-和Cu2+生成沉淀不共
存,C项错误;Al3+和CO发生相互促进的水解反应不共存,D项错误。
3.(2019·江苏,4)室温下,下列各组离子在指定溶液中能大量共存的是( )
A.0.1 mol·L-1 NaOH溶液:Na+、K+、CO、AlO
B.0.1 mol·L-1 FeCl 溶液:K+、Mg2+、SO、MnO
2
C.0.1 mol·L-1 KCO 溶液:Na+、Ba2+、Cl-、OH-
2 3
D.0.1 mol·L-1 HSO 溶液:K+、NH、NO、HSO
2 4
答案 A
解析 B项,MnO可以氧化Fe2+,错误;C项,CO与Ba2+会发生反应生成BaCO 沉淀,错
3
误;D项,H+可以与HSO反应生成SO ,且酸性条件下NO会氧化HSO生成SO,错误。
2
4.下列各组微粒一定能大量共存的是( )
A.遇KSCN变红色的溶液中:Na+、Mg2+、CHCOOH、Cl-
3
B.某无色溶液中:OH-、K+、HClO、Ba2+
C.0.1 mol·L-1 Na S溶液中:K+、NH、NO、Al3+
2
D.常温下水电离出的c(H+)·c(OH-)=10-20的溶液中:Na+、Cl-、CO、SO
答案 A
解析 遇KSCN变红色的溶液中有Fe3+,Fe3+、Na+、Mg2+、CHCOOH、Cl-之间相互不反
3
应,能大量共存,A项正确;OH-和HClO发生反应而不能大量共存,B项错误;NaS溶液
2
中S2-和Al3+会发生相互促进的水解反应而不能大量共存,C项错误;常温下水电离出的
c(H+)·c(OH-)=10-20的溶液呈酸性或碱性,当溶液呈酸性时,CO会和H+反应,不能大量
共存,D项错误。
5.25 ℃时,下列各组离子在指定溶液中可能大量共存的是( )
A.pH=1的溶液中:Na+、K+、MnO、CO
B.由水电离出的c(H+)=1×10-13mol·L-1的溶液中:Cu2+、Mg2+、NO、SO
C.0.1 mol·L-1FeCl 溶液中:Fe2+、NH、SCN-、SO
3
D.无色溶液中:Cu2+、Al3+、NH、Cl-
答案 B
解析 pH=1的水溶液显酸性,溶液中含有大量的H+,CO在溶液中与H+结合生成水和二
氧化碳,不能大量共存,故A不符合题意;由水电离的c(H+)=1×10-13mol·L-1的溶液,水
的电离受到抑制,溶液可能呈酸性,也可能呈碱性,在酸性溶液中 Cu2+、Mg2+、NO、SO之间不发生任何反应,也不与H+反应,能够大量共存,碱性条件下Cu2+、Mg2+不能大量存
在,故B符合题意;Fe3+与SCN-反应生成络合物而不能大量共存,故C不符合题意;含
Cu2+的溶液呈蓝色,与无色不符,故D不符合题意。
6.下列各组澄清溶液中离子能大量共存,且滴入X试剂后发生反应的离子方程式书写正确
的是( )
选项 离子组 X试剂 离子方程式
A NH、Fe3+、SO、Br- 过量HS 2Fe3++HS===2Fe2++S↓+2H+
2 2
4H++3Fe2++NO===3Fe3++NO↑+
B Fe2+、K+、NO、Cl- 少量HI
2HO
2
C NH、Fe3+、AlO、Na+ 过量铜粉 2Fe3++Cu===2Fe2++Cu2+
D AlO、Na+、K+、HCO 少量HCl H++AlO+HO===Al(OH) ↓
2 3
答案 A
解析 碘离子的还原性强于二价铁离子,反应的离子方程式为 8H++6I-+2NO===3I↓+
2
2NO↑+4HO,B项错误;三价铁离子能够与偏铝酸根离子发生相互促进的水解反应生成
2
氢氧化铝和氢氧化铁沉淀,二者不共存,C项错误;碳酸氢根离子与偏铝酸根离子反应生成
碳酸根离子和氢氧化铝沉淀,二者不共存,D项错误。
7.对某无色溶液分别进行下列操作,所得现象和结论均正确的是( )
A.加入氨水,产生白色沉淀,证明原溶液中存在Al3+
B.加入AgNO 溶液,产生白色沉淀,证明原溶液中存在Cl-
3
C.加入盐酸酸化的BaCl 溶液,生成白色沉淀,证明原溶液中存在SO
2
D.加入NaOH溶液并加热,产生使湿润的红色石蕊试纸变蓝的气体,证明原溶液中存在
NH
答案 D
解析 A项,加入氨水,产生白色沉淀,该白色沉淀可能为氢氧化镁,原溶液中可能存在
Mg2+,错误;B项,加入AgNO 溶液,产生白色沉淀,该白色沉淀可能为碳酸银,原溶液
3
中可能含有CO,错误;C项,加入盐酸酸化的BaCl 溶液,生成白色沉淀,该白色沉淀可
2
能为氯化银,原溶液中可能含有Ag+,错误。
8.(2022·江西模拟)某溶液中可能存在Br-、CO、SO、Al3+、I-、Mg2+、Na+七种离子中的
某几种。现取该溶液进行实验,得到如下现象:
①向溶液中滴加足量氯水后,溶液变橙色,且有无色气泡冒出;②向所得橙色溶液中加入足
量BaCl 溶液,无沉淀生成;③向所得溶液中继续滴加淀粉溶液,溶液不变蓝色。
2
已知:5Cl+I+6HO===10HCl+2HIO
2 2 2 3
据此可以判断,该溶液中肯定不存在的离子组是( )
A.Al3+、Mg2+、SO B.Mg2+、CO、I-C.Al3+、SO、I- D.Al3+、Br-、SO
答案 A
解析 根据①可判断溶液中有Br-和CO,根据离子共存原则,不存在Al3+、Mg2+;根据②
可判断溶液中无SO;根据③不能确定是否含有I-,因为在①中氯水可能把I-氧化成了IO,
致使淀粉溶液不变蓝色。
9.某无色溶液中可能含有①Na+、②Ba2+、③Cl-、④Br-、⑤SO、⑥SO、⑦Fe2+中的
几种离子,依次进行下列实验,且每步所加试剂均过量,观察到的现象如下:
步骤 操作 现象
Ⅰ 用pH试纸检验 溶液的pH大于7
Ⅱ 向溶液中滴加氯水,再加入CCl ,振荡,静置 CCl 层呈橙红色
4 4
Ⅲ 取Ⅱ的上层溶液,加入Ba(NO ) 溶液和稀硝酸 有白色沉淀产生
3 2
将 Ⅲ 过滤,向滤液中加入AgNO 溶液和稀硝
3
Ⅳ 有白色沉淀产生
酸
下列结论正确的是( )
A.肯定含有的离子是①④⑤
B.肯定没有的离子是②⑤⑦
C.可能含有的离子是①②⑥
D.不能确定的离子是①③⑥
答案 A
解析 根据步骤Ⅰ,该溶液呈碱性,则该溶液是强碱弱酸盐溶液,所以一定存在 SO,则一
定不存在Ba2+;在碱性的无色溶液中,一定不存在Fe2+;溶液呈电中性,所以溶液中的阳
离子只能是Na+;步骤Ⅱ说明该溶液中一定存在Br-;步骤Ⅲ不能说明有SO存在,因为该
溶液中一定存在SO,加入氯水后SO被氧化为SO,与Ba(NO ) 反应生成BaSO 沉淀;步骤
3 2 4
Ⅳ不能确定Cl-的存在,因为加入的氯水中含有Cl-。因此一定存在的离子是①④⑤,一定
不存在的离子是②⑦,不能确定的离子是③⑥,故A正确。
10.有一混合溶液中含有以下离子的若干种:K+、Mg2+、NH、Ba2+、Cl-、CO、SO,现
有两份体积相同各为100 mL的该溶液进行如下实验:①向第一份溶液中加入足量的NaOH
溶液并加热后,收集到0.224 L的气体(标准状况下测定),并产生0.58 g白色沉淀;②向第
二份溶液中加入足量的BaCl 溶液,产生6.99 g白色沉淀。根据上述实验,以下推测正确的
2
是( )
A.K+可能存在
B.Ba2+一定不存在
C.可能存在CO
D.100 mL该溶液中若含有0.01 mol Cl-,则K+的物质的量浓度为0.04 mol·L-1答案 B
解析 ①第一份加过量NaOH溶液后加热,收集到气体的物质的量为=0.01 mol,0.01 mol
气体为氨气,溶液中一定含有NH,并且物质的量为0.01 mol,产生0.58 g白色沉淀,则溶
液中含有Mg2+,并且物质的量为=0.01 mol,由Mg2+与CO不能共存,得出一定不存在
CO;②第二份加足量BaCl 溶液后,生成白色沉淀,得到6.99 g固体,沉淀为硫酸钡,其物
2
质的量为=0.03 mol,说明原溶液存在0.03 mol的SO,一定不存在Ba2+,再根据电荷守恒,
得出一定存在K+,无法确定是否存在Cl-,据此进行解答。100 mL该溶液中若含有0.01
mol Cl-,则根据电荷守恒可知,n(K+)+2n(Mg2+)+n(NH)=2n(SO)+n(Cl-),n(K+)+
2×0.01 mol+0.01 mol=2×0.03 mol+0.01 mol,得n(K+)=
0.04 mol,K+的物质的量浓度为=0.4 mol·L-1,D项错误。
11.已知:5SO+2IO+2H+===I +5SO+HO。某含碘废水(pH约为8)中一定存在I ,可能
2 2 2
存在I-、IO中的一种或两种。请补充完整检验含碘废水中是否含有I-、IO的实验方案:取
适量含碘废水用 CCl 多次萃取、分液,直到水层用淀粉溶液检验不出有碘单质存在;
4
_____________________________________________________________________________。
实验中可供选择的试剂:稀盐酸、淀粉溶液、FeCl 溶液、NaSO 溶液。
3 2 3
答案 从水层取少量溶液,加入1~2 mL淀粉溶液,加稀盐酸酸化,滴加FeCl 溶液,若溶
3
液变蓝,说明废水中含有I-;若溶液不变蓝,说明废水中不含有I-。另从水层取少量溶液,
加入1~2 mL淀粉溶液,加稀盐酸酸化,滴加NaSO 溶液,若溶液变蓝,说明废水中含有
2 3
IO;若溶液不变蓝,说明废水中不含有IO
12.现有 NaCl、NaSO 和 NaNO 的混合物,选择适当的试剂除去杂质,从而得到纯净的
2 4 3
NaNO 晶体,相应的实验流程如图所示。
3
(1)写出实验流程中下列物质的化学式:试剂 X______,沉淀 A________。
(2)上述实验流程中①②③步均要进行的实验操作是__________(填操作名称),该过程中玻璃
棒的作用是____________。
(3)上述实验流程中加入过量 NaCO 溶液的目的是_________________________。
2 3
(4)按此实验方案得到的溶液3中肯定含有______(填化学式)杂质。为了解决这个问题,可以
向溶液3中加入适量的________(填化学式)。
答案 (1)AgNO BaSO (2)过滤 引流
3 4
(3)使溶液中的 Ag+、Ba2+完全沉淀 (4)Na CO HNO
2 3 3解析 (1)试剂X是为了除去氯离子的硝酸银溶液,沉淀A为钡离子结合硫酸根离子产生的
硫酸钡。(2)实验流程中①②③步均要进行沉淀和溶液的分离,固液分离应采用过滤操作,
过滤时要用玻璃棒引流。(3)溶液2中含有银离子和钡离子,加过量碳酸钠的目的是将银离
子和钡离子转变成沉淀除去。(4)溶液3中含有硝酸钠和过量的碳酸钠,应除去碳酸钠后进
行结晶操作,为不引入杂质离子应用适量的硝酸除去碳酸钠。