文档内容
第 26 讲 原子结构、核外电子排布
复习目标 1.了解元素、核素和同位素的含义。2.了解原子的构成,了解原子序数、核电荷
数、质子数、中子数、核外电子数以及它们之间的关系。3.了解原子核外电子排布规律,掌
握原子结构示意图。
考点一 原子结构 核素 同位素
1.原子构成
(1)构成微粒及作用
(2)微粒间的数量关系
①阳离子的核外电子数=质子数-所带电荷数。
②阴离子的核外电子数=质子数+所带电荷数。(3)微粒符号周围数字代表的信息
2.元素、核素、同位素
(1)元素、核素、同位素的概念及关系
(2)同位素
①天然存在同一元素的各核素所占原子百分数一般不变。
②同位素的“六同”与“三不同”
(3)常见的重要核素及其应用
核素 U C H H O
用途 核燃料 用于考古断代 制氢弹 示踪原子
1.中子数为10的氧原子:O( )
2.核聚变如H+H―→He+n,因为有新微粒生成,所以该变化是化学变化( )
3.Cl与Cl得电子能力几乎相同( )
4.一种元素只有一种核素,有多少种核素就有多少种原子( )
5.所有的原子中都含有质子和中子,任何离子都有电子( )
6.质量数就是元素的相对原子质量( )
7.质子数相同的微粒不一定属于同一种元素( )
答案 1.× 2.× 3.√ 4.× 5.× 6.×7.√
一、微粒中粒子数的计算
1.(1)1 mol H 18O与1 mol D O中子数之比为________________________________________。
2 2
(2)已知阴离子R2-的原子核内有n个中子,R原子的质量数为m,则w g R原子完全转化为
R2-时,含有电子的物质的量是_______________________________________________。
答案 (1)1∶1 (2) mol
解析 (2)质量数=质子数+中子数,则R的质子数为m-n,故R2-的核外电子数为(m-n+
2),w g R原子的物质的量为= mol,所以w g R2-含有电子的物质的量为
mol×(m-n+2)= mol。
二、元素、核素、同位素的概念辨析
2.现有下列9种微粒:H、H、C、C、N、Fe2+、Fe3+、O、O。按要求完成以下各题:
2 3
(1)H、H分别是氢元素的一种________,它们互称为________。
(2)互为同素异形体的微粒是________。
(3)Fe2+的中子数为________,核外电子数为____________________________________。
(4)上述9种微粒中有________种核素,含有________种元素。
答案 (1)核素 同位素 (2)O、O
2 3
(3)30 24 (4)5 5
解析 (1)H、H分别是氢元素的一种核素;H、H是质子数相同而中子数不同的氢元素的不
同原子,它们互称为同位素。
(2)O 和O 是同种元素组成的不同单质,为氧元素的同素异形体。
2 3
(3)Fe2+的中子数为56-26=30,核外电子数为26-2=24。
(4)9种微粒中有5种核素:H、H、C、C、N,有5种元素H、C、N、Fe、O。
求一定质量的某物质中粒子数的答题模板
物质的质量――――――――――→物质的量――――――――――――――――→指定粒子的物质的量――→粒子数。
考点二 原子核外电子排布
1.核外电子排布规律2.原子结构示意图
3.常见短周期元素原子核外电子排布规律
(1)电子层数与核外电子总数相等的元素是H。
(2)最外层有1个电子的元素是 H 、 Li 、 Na 。
(3)最外层有2个电子的元素是 He 、 Be 、 Mg 。
(4)最外层电子数等于次外层电子数的元素是 Be 、 Ar 。
(5)最外层电子数是次外层电子数2倍的元素是C;是次外层电子数3倍的元素是O;是次外
层电子数4倍的元素是Ne。
(6)最外层电子数是内层电子数一半的元素是 Li 、 P 。
(7)电子层数与最外层电子数相等的元素是 H 、 Be 、 Al 。
(8)电子总数为最外层电子数2倍的元素是Be。
(9)次外层电子数是最外层电子数2倍的元素是 Li 、 Si 。
4.核外电子排布与元素性质的关系
(1)金属元素原子的最外层电子数一般小于4,较易失去电子,形成阳离子,表现出还原性,
在化合物中显正化合价。
(2)非金属元素原子的最外层电子数一般大于或等于4,较易得到电子,活泼非金属原子易形
成阴离子,在化合物中主要显负化合价。
(3)稀有气体元素的原子最外层为8电子(氦为2电子)稳定结构,不易失去或得到电子,通常
表现为0价。
1.两种粒子,若核外电子排布完全相同,则其化学性质一定相同( )
2.某原子M层上电子数为L层电子数的4倍( )
3.某元素原子最外层电子数为1,该元素一定是金属元素( )
4.同一元素的不同核素原子核外电子排布不同( )
5.最外层电子数为8的粒子一定是稀有气体元素原子( )
6.除Li外的碱金属原子次外层都有8个电子( )
答案 1.× 2.× 3.× 4.× 5.× 6.√1.已知X、Y、Z都是短周期元素,它们的原子序数依次增大,X原子的电子层数与它的核
外电子总数相等,而Z原子的最外层电子数是次外层的3倍,Y和Z可以形成两种以上气态
化合物,则下列说法错误的是( )
A.Y和Z可以组成一种Y和Z的质量比为7∶8的化合物
B.X、Y、Z可以组成一种盐
C.X和Z可以组成原子个数比分别为1∶1和2∶1的常温下呈液态的两种化合物
D.由X、Y、Z三种元素中的任意两种组成的10电子微粒有2种
答案 D
解析 由题中信息易推出X、Y、Z分别是H、N、O。N、O可以组成NO,其中N、O两种
元素的质量比为 7∶8,A项正确;H、N、O可组成NH NO ,B项正确;H、O可组成
4 3
HO、HO 两种常温下呈液态的化合物,C项正确;H、N、O中的任意两种元素组成的10
2 2 2
电子微粒有HO、NH 、NH、OH-、HO+等,N与O不能组成10电子微粒,D项错误。
2 3 3
2.在第n电子层中,当它作为原子的最外电子层时,最多容纳的电子数与n-1层相同,当
它作为原子的次外层时,其电子数比n+1层最多能多10个,则此电子层是( )
A.K层 B.M层 C.L层 D.N层
答案 B
解析 第n电子层作为最外层时,最多只能容纳8个电子,所以n-1层应为8个电子,为L
层,则n应为M层;若第n电子层为次外层,则n+1为最外层,则次外层电子数最多为10
+8=18,则进一步证明n为M层。
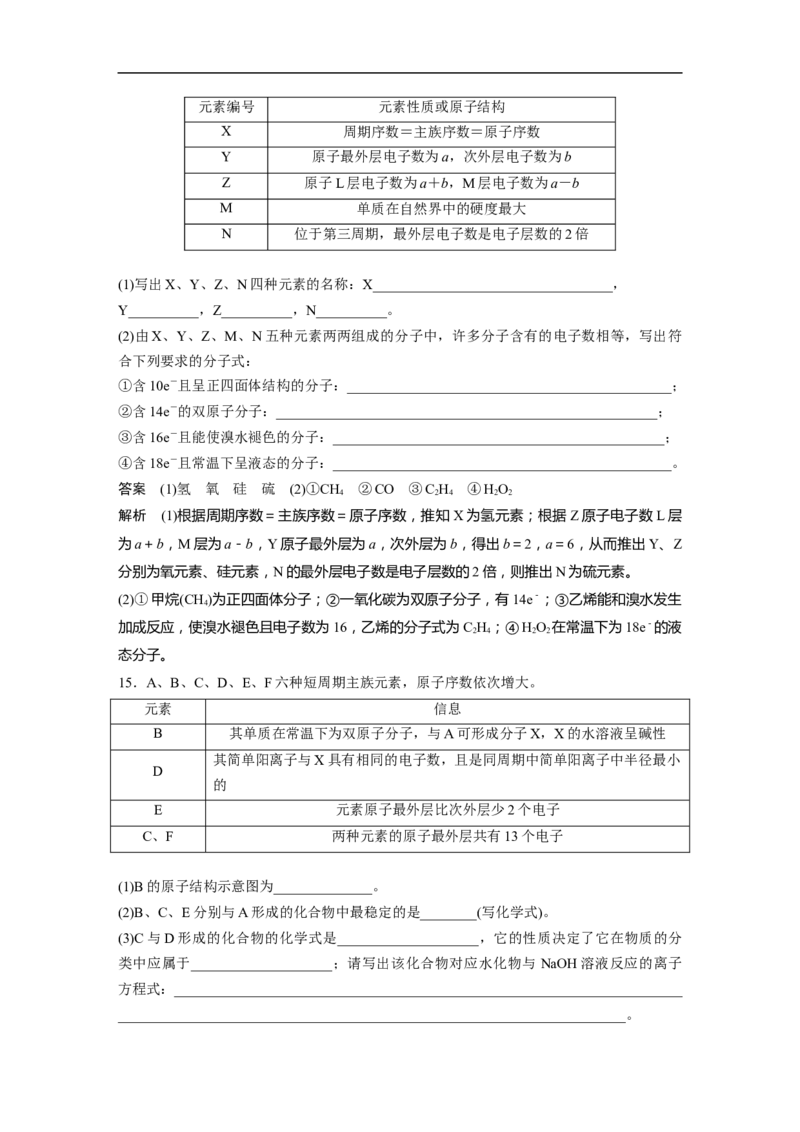
3.已知A、B、C、D是中学化学中常见的四种不同微粒。它们之间存在如图转化关系。
(1)如果A、B、C、D均是10电子的微粒,请写出:
A的化学式:__________;D的化学式:_______________________________________。
(2)如果A和C是18电子的微粒,B和D是10电子的微粒,请写出A与B在溶液中反应的
离子方程式:_______________________________________________________________。
答案 (1)NH(或HF) HO (2)H S+OH-===HS-+HO(或HS+2OH-===S2-+2HO)
2 2 2 2 2
解析 (1)10电子微粒A、B反应得到两种10电子微粒,应是NH+OH-=====NH ↑+HO
3 2
或HF+OH-===F-+HO,可推知A为NH,B为OH-,C为NH ,D为HO或A为HF,B
2 3 2
为OH-,C为F-,D为HO。(2)如果A、C均是18电子的粒子,B、D是10电子粒子,结
2
合转化关系,可推知A为HS,B为OH-,C为HS-或S2-,D为HO,A与B在溶液中反
2 2
应的离子方程式:HS+OH-===HS-+HO或HS+2OH-===S2-+2HO。
2 2 2 2寻找“10电子”微粒和“18电子”微粒的方法
(1)“10电子”微粒
(2)“18电子”微粒
1.(2021·广东1月适应性测试,4)“原子”原意是“不可再分”的意思。20世纪初,人们
才认识到原子不是最小的粒子。从电子层模型分析,Ca原子核外N能层中运动的电子数为(
)
A.8 B.2 C.18 D.10
答案 B
解析 Ca原子结构示意图为 ,第4层有2个电子,故 N能层运动的电子数有2
个,故选B。
2.(2021·浙江6月选考,6)下列说法正确的是( )
A.C 和C 互为同位素
60 70
B.C H 和C H 互为同系物
2 6 6 14
C.CO和CO 互为同素异形体
2
D.CHCOOH和CHOOCH是同一种物质
3 3
答案 B
解析 同种元素的不同种核素互为同位素,C 和C 为C元素的两种不同单质,不互为同位
60 70
素,A错误;C H 和C H 均为烷烃,二者结构类似,分子组成上相差4个“CH”原子团,
2 6 6 14 2
二者互为同系物,B正确;同种元素的不同种单质互称同素异形体,CO和CO 为C元素的
2
两种不同氧化物,二者不是单质,不互为同素异形体,C错误;两种物质的结构不同,不是同一种物质,二者互为同分异构体,D错误。
3.(2021·北京,2)下列有关放射性核素氚(H)的表述不正确的是( )
A.H原子核外电子数为1
B.H原子核内中子数为3
C.H 与H 化学性质基本相同
2 2
D.HO具有放射性
2
答案 B
4.(2021·河北,5)用中子轰击X原子产生α粒子(即氦核He)的核反应为X+n→Y+He。已
知元素Y在化合物中呈+1价。下列说法正确的是( )
A.HXO 可用于中和溅在皮肤上的NaOH溶液
3 3
B.Y单质在空气中燃烧的产物是YO
2 2
C.X和氢元素形成离子化合物
D.6Y和7Y互为同素异形体
答案 A
解析 HBO 为硼酸,NaOH溶液具有腐蚀性,若不慎将NaOH溶液溅到皮肤上,则需用大
3 3
量水冲洗,同时涂抹 HBO 以中和碱液,A 正确;Y 为 Li,在空气中燃烧的产物只有
3 3
LiO,B错误;X为B,与H元素会形成BH 或B H 等硼氢化合物,B元素与H元素以共价
2 3 2 4
键结合,属于共价化合物,C错误;6Li和7Li两者的质子数均为3,中子数不同,所以两者
互为同位素,D错误。
5.(2020·全国卷Ⅰ,11)1934年约里奥·居里夫妇在核反应中用α粒子(即氦核He)轰击金属原
子X,得到核素Y,开创了人造放射性核素的先河:X+He―→Y+n。其中元素X、Y的最
外层电子数之和为8。下列叙述正确的是( )
A.X的相对原子质量为26
B.X、Y均可形成三氯化物
C.X的原子半径小于Y的
D.Y仅有一种含氧酸
答案 B
解析 由守恒关系可知元素X的质量数为27,X的相对原子质量近似等于该原子的质量数,
A项错误;X与Y最外层电子数之和为8,质子数相差2,且X为金属元素,可推知X为Al
元素,Y为P元素,二者都有+3价,都可以形成三氯化物,B项正确;同一周期主族元素
自左向右,原子半径逐渐减小,故 Al的原子半径大于P,C项错误;P元素的含氧酸有
HPO 、HPO 、HPO 等,D项错误。
3 4 3 3 3 2
6.(2020·浙江1月选考,16)下列说法正确的是( )
A.同一原子,在离核较远的区域运动的电子能量较高B.原子核外电子排布,先排满K层再排L层、先排满M层再排N层
C.同一周期中,随着核电荷数的增加,元素的原子半径逐渐增大
D.同一周期中,ⅡA与ⅢA族元素原子的核电荷数都相差1
答案 A
解析 同一原子中,能量高的电子在离核较远的区域运动,A项正确;原子核外电子排布,
不是先排满M层再排N层,如钾原子的M层有8个电子,N层有1个电子,B项错误;同
周期中,随着核电荷数的增大,原子半径逐渐减小,C项错误;同周期ⅡA族和ⅢA族元
素原子序数之差可以是1或11或25,D项错误。
课时精练
1.镉(Cd)是一种重金属元素,有多种核素,下列关于Cd和Cd说法正确的是( )
A.Cd和Cd属于两种不同的元素
B.Cd和Cd质量数相同
C.Cd和Cd是同一种核素
D.Cd和Cd互为同位素
答案 D
解析 Cd和Cd都属于Cd元素,A错误;Cd的质量数为95,Cd的质量数为97,B错误;
具有一定数目质子和一定数目中子的原子称为核素,Cd和Cd属于不同种核素,C错误;质
子数相同而中子数不同的同一元素的不同原子互为同位素,Cd和Cd互为同位素,D正确。
2.有5种微粒分别是X、Z、Q+、R、M,其中所含元素种类为( )
A.2种 B.3种 C.4种 D.5种
答案 B
3.下列叙述正确的是( )
A.两种粒子,若核外电子排布完全相同,则其化学性质一定相同
B.凡单原子形成的离子,一定具有稀有气体元素原子的核外电子排布
C.两原子,如果核外电子排布相同,则一定属于同种元素
D.阴离子的核外电子排布一定与比它原子序数小的稀有气体元素原子的核外电子排布相同
答案 C
解析 两种粒子,若核外电子排布完全相同,则其化学性质不一定相同,如钠离子和氟离子,
A项错误;凡单原子形成的离子,不一定具有稀有气体元素原子的核外电子排布,如H+,
B项错误;两原子,如果核外电子排布相同,那么质子数相同,则一定属于同种元素,C项
正确;阴离子是原子得电子后的离子,则阴离子的核外电子排布与同周期的稀有气体元素原
子的核外电子排布相同,D项错误。4.下列离子化合物中,阴、阳离子的电子层结构相同的是( )
A.NaCl B.LiCl C.MgO D.NaS
2
答案 C
解析 A项,氯离子电子层比钠离子多一个,电子层结构不同,错误;B项,氯离子电子层
比锂离子多2个,电子层结构不同,错误;D项,硫离子比钠离子多1个电子层,电子层结
构不同,错误。
5.有A、B两种元素,已知元素A的核电荷数为a,且A3-与Bn+的电子排布完全相同,则
元素B的核电荷数为( )
A.a-n-3 B.a-n+3
C.a+n-3 D.a+n+3
答案 D
解析 A元素原子的核电荷数为a,原子中核电荷数=核内质子数=核外电子数,则其核外
电子数为a;A原子得到3个电子形成A3-,则A3-的核外电子数为a+3,B原子失去n个
电子形成Bn+,设B的核电荷数为x,由于A3-与Bn+的电子排布相同,则:a+3=x-n,解
得:x=a+n+3。
6.2020年4月,我国自主设计,被称为“人造太阳”的“东方超环”核聚变实验装置取得
重大突破,该核聚变的基础原料是海水中提取的氘和氚。下列叙述错误的是( )
A.氘原子的相对原子质量约为2
B.氚原子内中子数和核外电子数之差为1
C.氘原子和氚原子互为同位素
D.海水中的HO与DO互为同素异形体
2 2
答案 D
解析 氘原子的中子数为1,质子数为1,相对原子质量约为2,故A正确;氚原子内中子
数为2,核外电子数为1,故B正确;氘原子和氚原子的质子数均为1,中子数分别是1和
2,氘原子和氚原子互为同位素,故C正确;海水中的HO与DO是化合物,不是同种元素
2 2
组成的不同单质,不互为同素异形体,故D错误。
7.医学界通过用14C标记的C 发现了一种C 的羧酸衍生物,这种羧酸衍生物在特定条件
60 60
下可以通过断裂DNA抑制艾滋病毒的繁殖。下列有关14C的叙述正确的是( )
A.与12C 的碳原子化学性质不同
60
B.与14N含的中子数相同
C.14C 是12C 的同素异形体
60 60
D.与12C互为同位素
答案 D
解析 同一种元素的化学性质是一样的, 14C与12C 中碳原子的化学性质相同,故A错误;
60
14C和14N的中子数分别为8、7,故B错误;14C 与12C 是碳元素的同种单质,不互为同素
60 60异形体,故C错误。
8.镆(Mc)是一种人工合成的元素,同位素Mc的原子核内的中子数与核外电子数之和是(
)
A.58 B.173 C.288 D.403
答案 C
9.现有下列几组粒子:① N 、CO、C H ;② NH、HO+、OH-;③ C、O、CN-;
2 2 2 3
④PO、SO、ClO。对上述四组粒子归类正确的是( )
A.质子数相等、电子数和原子数不相等:①
B.质子数和电子数相等、原子数不相等:②
C.电子数相等、质子数和原子数不相等:③
D.原子数和电子数相等、质子数不相等:④
答案 D
解析 阳离子:电子总数=质子总数-所带的电荷总数;阴离子:电子总数=质子总数+所
带的电荷总数。①N 、CO、C H 的质子数和电子数都等于14,原子数不等;②NH、HO
2 2 2 3
+、OH-的原子数和质子数不等,电子数都为10;③C、O、CN-的原子数和电子数都相等,
质子数不同;④P、S、Cl所含的电子数分别为15、16、17,酸根离子中所含氧原子数均相
等,所带负电荷数依次为3、2、1,三种酸根离子所含的总电子数、原子数相等,但三种酸
根离子的质子数不相等。
10.下列说法正确的是( )
A.由H、D、T与16O、17O、18O相互结合为水,可得18种水分子,相对分子质量不同的水
分子种数为8种
B.H、D、T 互为同素异形体
2 2 2
C.H、D、T 在相同条件下的密度之比为1∶2∶3
2 2 2
D.氘、氚发生核聚变成为其他元素,属于化学变化
答案 C
解析 H、D、T组合有H、D、T、HD、HT、DT共6种,分别与16O、17O、18O构成水分
2 2 2
子,共有6×3=18种,相对分子质量介于18~24之间,相对分子质量不同的水分子种数共
有7种,A项错误;H、D、T 均为氢气单质,化学性质相同,属于化学范围内的同一种物
2 2 2
质,B项错误;H、D、T 在相同条件下的密度之比等于气体的相对分子质量之比,即三者
2 2 2
的密度之比为2∶4∶6=1∶2∶3,C项正确;氘、氚发生的核聚变属于核反应,不是化学
变化,D项错误。
11.据国外媒体报道,“火星快车”号和“金星快车”号探测器分别在火星和金星大气层中
发现了一种非常特殊的气态化合物。这种化合物的存在不但会导致金星上的温室效应被成倍
地放大,而且可能会在火星上也诱发温室效应。该化合物的化学式为16OC18O。下列说法正
确的是( )A.相同条件下,16OC18O与16OC16O的密度相同
B.16OC18O与16OC16O互为同位素
C.16OC18O与Na16O 反应生成的氧气中没有18O
2 2
D.16OC18O与16OC16O的化学性质不同
答案 C
解析 A 项,同温同压下,气体的密度之比等于相对分子质量之比,由于 16OC18O 与
16OC16O的相对分子质量不同,故二者的密度不同,错误;B项,质子数相同、中子数不同
的原子互为同位素,16OC18O与16OC16O为化合物,不互为同位素,错误;C项,在NaO 与
2 2
CO 的反应中,产物氧气中的氧原子来自过氧化钠,故16OC18O与Na16O 反应生成的氧气中
2 2 2
没有18O,均为16O,正确;D项,16OC18O与16OC16O的组成元素完全相同且结构相同,属
于同种物质,化学性质相同,错误。
12.某元素的一种同位素X原子的质量数为A,它与2H原子组成2H X分子,此分子含N个
m
中子,在a g 2H X中所含电子的物质的量是( )
m
A.(A-N+m)mol
B.(A-N)mol
C.(A-N+m)mol
D.(A-N+2m)mol
答案 D
解析 2H X分子含N个中子,则X原子含中子数为(N-m),由X原子的质量数为A可知,
m
质子数为(A-N+m),则每个2H X分子含有质子数为(A-N+2m),a g 2H X的物质的量为
m m
mol,因中性分子中质子数等于电子数,则 a g 2H X中所含电子的物质的量是(A-N+
m
2m)mol,故选D。
13.我国科学家通过测量SiO 中26Al和10Be两种核素的比例来确定“北京人”年龄,这种
2
测量方法叫铝铍测年法。下列关于26Al和10Be的说法不正确的是( )
A.10Be和9Be是中子数不同质子数相同的不同原子
B.10Be的原子核内中子数比质子数多
C.5.2 g 26Al3+中所含的电子数约为1.2×1023
D.26Al和26Mg的质子数、中子数和核外电子数都不相同
答案 C
解析 10Be和9Be互为同位素,中子数不同质子数相同,A项正确;10Be的原子核内,质子
数为4,中子数为10-4=6,中子数比质子数多,B项正确;5.2 g 26Al3+中所含的电子数约
为×(13-3)×N ≈1.2×1024,C项错误;26Al和26Mg的质子数分别为13、12,中子数分别
A
为13、14,核外电子数等于质子数,故两者所含质子数、中子数和核外电子数都不相同,D
项正确。
14.现有部分短周期主族元素的性质或原子结构如下表所示:元素编号 元素性质或原子结构
X 周期序数=主族序数=原子序数
Y 原子最外层电子数为a,次外层电子数为b
Z 原子L层电子数为a+b,M层电子数为a-b
M 单质在自然界中的硬度最大
N 位于第三周期,最外层电子数是电子层数的2倍
(1)写出X、Y、Z、N四种元素的名称:X__________________________________,
Y__________,Z__________,N__________。
(2)由X、Y、Z、M、N五种元素两两组成的分子中,许多分子含有的电子数相等,写出符
合下列要求的分子式:
①含10e-且呈正四面体结构的分子:______________________________________________;
②含14e-的双原子分子:______________________________________________________;
③含16e-且能使溴水褪色的分子:_______________________________________________;
④含18e-且常温下呈液态的分子:________________________________________________。
答案 (1)氢 氧 硅 硫 (2)①CH ②CO ③C H ④HO
4 2 4 2 2
解析 (1)根据周期序数=主族序数=原子序数,推知 X为氢元素;根据Z原子电子数L层
为a+b,M层为a-b,Y原子最外层为a,次外层为b,得出b=2,a=6,从而推出Y、Z
分别为氧元素、硅元素,N的最外层电子数是电子层数的2倍,则推出N为硫元素。
(2)①甲烷(CH)为正四面体分子;②一氧化碳为双原子分子,有14e-;③乙烯能和溴水发生
4
加成反应,使溴水褪色且电子数为16,乙烯的分子式为C H;④HO 在常温下为18e-的液
2 4 2 2
态分子。
15.A、B、C、D、E、F六种短周期主族元素,原子序数依次增大。
元素 信息
B 其单质在常温下为双原子分子,与A可形成分子X,X的水溶液呈碱性
其简单阳离子与X具有相同的电子数,且是同周期中简单阳离子中半径最小
D
的
E 元素原子最外层比次外层少2个电子
C、F 两种元素的原子最外层共有13个电子
(1)B的原子结构示意图为______________。
(2)B、C、E分别与A形成的化合物中最稳定的是________(写化学式)。
(3)C与D形成的化合物的化学式是____________________,它的性质决定了它在物质的分
类中应属于____________________;请写出该化合物对应水化物与NaOH溶液反应的离子
方程式:________________________________________________________________________
________________________________________________________________________。(4)F的单质在反应中常作________________剂,该单质的水溶液与E的低价氧化物反应的离
子方程式为_____________________________________________________________。
答案 (1) (2)H O (3)AlO 两性氧化物 Al(OH) +OH-===AlO+2HO
2 2 3 3 2
(4)氧化 Cl+SO +2HO===4H++2Cl-+SO
2 2 2
解析 A、B、C、D、E、F六种短周期主族元素,原子序数依次增大,X的水溶液显碱性,
则A为H,B为N;D的简单阳离子与X的电子数相同,且D是同周期中简单阳离子中半径
最小的,则D为Al;E元素原子最外层比次外层少2个电子,则E为S,F为Cl;C、F两
种元素的原子最外层共有13个电子,则C为O。