文档内容
第 31 讲 反应热的计算
复习目标 1.了解燃烧热的概念及能源利用的意义。2.了解中和反应反应热测定的方法。
3.掌握盖斯定律的内容及意义,并能进行有关反应热的计算。
考点一 反应热的测定 燃烧热 能源
1.中和反应反应热及其测定
(1)中和反应反应热
在稀溶液中,强酸和强碱发生中和反应生成1 mol H O(l)时所放出的热量。
2
(2)测定原理
ΔH=-
c=4.18 J·g-1·℃-1=4.18×10-3 kJ·g-1·℃-1;n为生成HO的物质的量。稀溶液的密度用
2
1 g·mL-1进行计算。
(3)装置如图
(4)注意事项
①碎泡沫塑料(或纸条)及泡沫塑料板的作用是保温、隔热,减少热量损失。
②为保证酸、碱完全中和,常采用碱稍稍过量(0.5 mol·L-1HCl、0.55 mol·L-1NaOH溶液等
体积混合)。
③实验时不能用铜丝搅拌棒代替环形玻璃搅拌棒的理由是铜丝导热性好,比用环形玻璃搅拌
棒误差大。
2.燃烧热
(1)燃烧热
(2)对完全燃烧的理解
燃烧元素 C H S N
稳定产物及状态 CO(g) HO(l) SO (g) N(g)
2 2 2 23.燃料的选择 能源
(1)燃料的选择原则
(2)能源及利用
1.煤油是可再生能源( )
2.H 燃烧过程中热能转化为化学能( )
2
3.化石燃料和植物燃料燃烧时放出的能量均来源于太阳能( )
4.开发利用各种新能源,减少对化石燃料的依赖,可以降低空气中PM 的含量( )
2.5
5.根据2H(g)+O(g)===2HO(l) ΔH=-571 kJ·mol-1可知,氢气的燃烧热为571 kJ·mol-1
2 2 2
( )
6.已知H+(aq)+OH-(aq)===HO(l) ΔH=-57.3 kJ·mol-1,则HSO 和Ba(OH) 反应的ΔH
2 2 4 2
=2×(-57.3 kJ·mol-1)( )
答案 1.× 2.× 3.√ 4.√ 5.× 6.×
一、燃烧热、中和反应反应热的含义
1.油酸甘油酯(相对分子质量为884)在体内代谢时可发生如下反应:
C H O(s)+80O(g)===57CO(g)+52HO(l)
57 104 6 2 2 2
已知燃烧1 kg该化合物释放出热量3.8×104 kJ,油酸甘油酯的燃烧热为( )
A.3.8×104 kJ·mol-1
B.-3.8×104 kJ·mol-1
C.3.4×104 kJ·mol-1
D.-3.4×104 kJ·mol-1答案 C
解析 燃烧热是指在101 kPa下,1 mol纯物质完全燃烧生成稳定的氧化物时所放出的热量,
则1 mol油酸甘油酯的燃烧热为×884 g·mol-1≈3.4×104 kJ·mol-1。
2.下列关于热化学反应的描述正确的是( )
A.已知H+(aq)+OH-(aq)===HO(l) ΔH=-57.3 kJ·mol-1,用含20.0 g NaOH的稀溶液与
2
稀盐酸反应测出的中和反应反应热为28.65 kJ·mol-1
B.CO(g)的燃烧热 ΔH=-283.0 kJ·mol-1,则反应 2CO(g)===2CO(g)+O(g)的ΔH=+
2 2
(2×283.0) kJ·mol-1
C.1 mol甲烷燃烧生成气态水和二氧化碳所放出的热量是甲烷的燃烧热
D.稀醋酸与稀NaOH溶液反应生成1 mol水,放出57.3 kJ热量
答案 B
解析 中和反应反应热是以生成1 mol H O(l)作为标准的,A不正确;有水生成的燃烧反应,
2
必须按液态水计算燃烧热,C不正确;稀醋酸是弱酸,电离过程需要吸热,放出的热量要小
于57.3 kJ,D不正确。
二、中和反应反应热的测定操作及误差分析
3.利用如图所示装置测定中和反应反应热的实验步骤如下:
①用量筒量取50 mL 0.50 mol·L-1盐酸倒入小烧杯中,测出盐酸温度;②用另一量筒量取
50 mL 0.55 mol·L-1 NaOH溶液,并用同一温度计测出其温度;③将NaOH溶液倒入小烧杯
中,设法使之混合均匀,测得混合液的最高温度。回答下列问题:
(1)NaOH溶液稍过量的原因是
。
(2)倒入NaOH溶液的正确操作是 (填字母,下同)。
A.沿玻璃棒缓慢倒入
B.分三次倒入
C.一次迅速倒入
(3)使盐酸与NaOH溶液混合均匀的正确操作是 。
A.用温度计小心搅拌
B.揭开硬纸片用玻璃棒搅拌
C.轻轻地振荡烧杯
D.用套在温度计上的环形玻璃搅拌棒轻轻地搅动(4)现将一定量的稀氢氧化钠溶液、稀氢氧化钙溶液、稀氨水分别和 1 L 1 mol·L-1的稀盐酸
恰好完全反应,其反应热分别为 ΔH 、ΔH 、ΔH ,则 ΔH 、ΔH 、ΔH 的大小关系为
1 2 3 1 2 3
。
(5)假设盐酸和氢氧化钠溶液的密度都是1 g·cm-3,又知中和反应后生成溶液的比热容c=4.18
J·
g-1·℃-1。为了计算中和反应反应热,某学生实验记录数据如下:
起始温度t/ ℃ 终止温度t/ ℃
1 2
实验序号
盐酸 氢氧化钠溶液 混合溶液
1 20.0 20.1 23.2
2 20.2 20.4 23.4
3 20.5 20.6 23.6
依据该学生的实验数据计算,该实验测得的中和反应反应热ΔH= (结果保留一位
小数)。
答案 (1)确保盐酸被完全中和 (2)C (3)D (4)ΔH=ΔH<ΔH (5)-51.8 kJ·mol-1
1 2 3
解析 (4)稀氢氧化钠溶液和稀氢氧化钙溶液中溶质都完全电离,它们的中和反应反应热相
同,稀氨水中的溶质是弱电解质,它与盐酸的反应中一水合氨的电离要吸收热量,故反应热
的数值要小一些。
考点二 盖斯定律及应用
1.盖斯定律
(1)内容
对于一个化学反应,无论是一步完成还是分几步完成,其反应热是相同的。即:化学反应的
反应热只与反应体系的始态和终态有关,而与反应的途径无关。
(2)意义
间接计算某些反应的反应热。
(3)应用
转化关系 反应热间的关系
aA――→B、A――→B ΔH= a Δ H
1 2
AB ΔH= - Δ H
1 2
ΔH= Δ H + Δ H
1 22.反应热的大小比较
(1)根据反应物的量的大小关系比较反应焓变的大小
①H(g)+O(g)===HO(g) ΔH
2 2 2 1
②2H(g)+O(g)===2HO(g) ΔH
2 2 2 2
反应②中H 的量更多,因此放热更多,故ΔH>ΔH。
2 1 2
(2)根据反应进行的程度大小比较反应焓变的大小
③C(s)+O(g)===CO(g) ΔH
2 3
④C(s)+O(g)===CO(g) ΔH
2 2 4
反应④中,C完全燃烧,放热更多,故ΔH>ΔH。
3 4
(3)根据反应物或生成物的状态比较反应焓变的大小
⑤S(g)+O(g)===SO (g) ΔH
2 2 5
⑥S(s)+O(g)===SO (g) ΔH
2 2 6
方法一:图像法,画出上述两反应能量随反应过程的变化曲线。
由图像可知:ΔH<ΔH。
5 6
方法二:通过盖斯定律构造新的热化学方程式。
由⑤-⑥可得S(g)===S(s) ΔH=ΔH-ΔH<0,故ΔH<ΔH。
5 6 5 6
(4)根据特殊反应的焓变情况比较反应焓变的大小
⑦2Al(s)+O(g)===Al O(s) ΔH
2 2 3 7
⑧2Fe(s)+O(g)===Fe O(s) ΔH
2 2 3 8
由⑦-⑧可得2Al(s)+Fe O(s)===2Fe(s)+Al O(s) ΔH
2 3 2 3
已知铝热反应为放热反应,ΔH=ΔH-ΔH<0,故ΔH<ΔH。
7 8 7 8
一、根据盖斯定律计算反应热
1.已知 (g)=== (g)+H(g)
2
ΔH=+100.3 kJ·mol-1①
1
H(g)+I(g)===2HI(g)
2 2
ΔH=-11.0 kJ·mol-1②
2对于反应: (g)+I(g)=== (g)+2HI(g)
2
ΔH= kJ·mol-1。
3
答案 +89.3
解析 根据盖斯定律,将反应①+反应②,则ΔH =ΔH +ΔH =(+100.3-11.0)kJ·mol-1=
3 1 2
+89.3 kJ·mol-1。
2.Deacon直接氧化法可按下列催化过程进行:
CuCl (s)===CuCl(s)+Cl(g)
2 2
ΔH=+83 kJ·mol-1
1
CuCl(s)+O(g)===CuO(s)+Cl(g)
2 2
ΔH=-20 kJ·mol-1
2
CuO(s)+2HCl(g)===CuCl (s)+HO(g)
2 2
ΔH=-121 kJ·mol-1
3
则4HCl(g)+O(g)===2Cl(g)+2HO(g)的ΔH= kJ·mol-1。
2 2 2
答案 -116
解析 将所给反应依次编号为①、②、③,根据盖斯定律,(①+②+③)×2可得:4HCl(g)
+O(g)===2Cl(g)+2HO(g) ΔH=[(+83 kJ·mol-1)+(-20 kJ·mol-1)+(-121 kJ·mol-1)]×2
2 2 2
=-116 kJ·mol-1。
二、根据盖斯定律书写热化学方程式
3.“嫦娥”五号预计在海南文昌发射中心发射,火箭的第一、二级发动机中,所用的燃料
为偏二甲肼和四氧化二氮,偏二甲肼可用肼来制备。用肼(N H)作燃料,四氧化二氮作氧化
2 4
剂,二者反应生成氮气和气态水。已知:
①N(g)+2O(g)===NO(g)
2 2 2 4
ΔH=+10.7 kJ·mol-1
②NH(g)+O(g)===N(g)+2HO(g)
2 4 2 2 2
ΔH=-543 kJ·mol-1
写出气态肼和NO 反应的热化学方程式:
2 4
。
答案 2NH(g)+NO(g)===3N(g)+4HO(g)
2 4 2 4 2 2
ΔH=-1 096.7 kJ·mol-1
解析 根据盖斯定律,由2×②-①得:
2NH(g)+NO(g)===3N(g)+4HO(g)
2 4 2 4 2 2
ΔH=2×(-543 kJ·mol-1)-(+10.7 kJ·mol-1)=-1 096.7 kJ·mol-1。
4.[2018·北京,27(1)]近年来,研究人员提出利用含硫物质热化学循环实现太阳能的转化与
存储。过程如下:反应 Ⅰ:2HSO (l)===2SO (g)+2HO(g)+O(g)
2 4 2 2 2
ΔH=+551 kJ·mol-1
1
反应Ⅲ:S(s)+O(g)===SO (g)
2 2
ΔH=-297 kJ·mol-1
3
反应Ⅱ的热化学方程式: 。
答案 3SO (g)+2HO(g)===2HSO (l)+S(s)
2 2 2 4
ΔH=-254 kJ·mol-1
2
解析 由题图可知,反应Ⅱ的化学方程式为3SO +2HO=====2HSO +S↓。根据盖斯定律,
2 2 2 4
反应Ⅱ=-(反应Ⅰ+反应Ⅲ)可得:3SO (g)+2HO(g)===2HSO (l)+S(s) ΔH=-254 kJ·
2 2 2 4 2
mol-1。
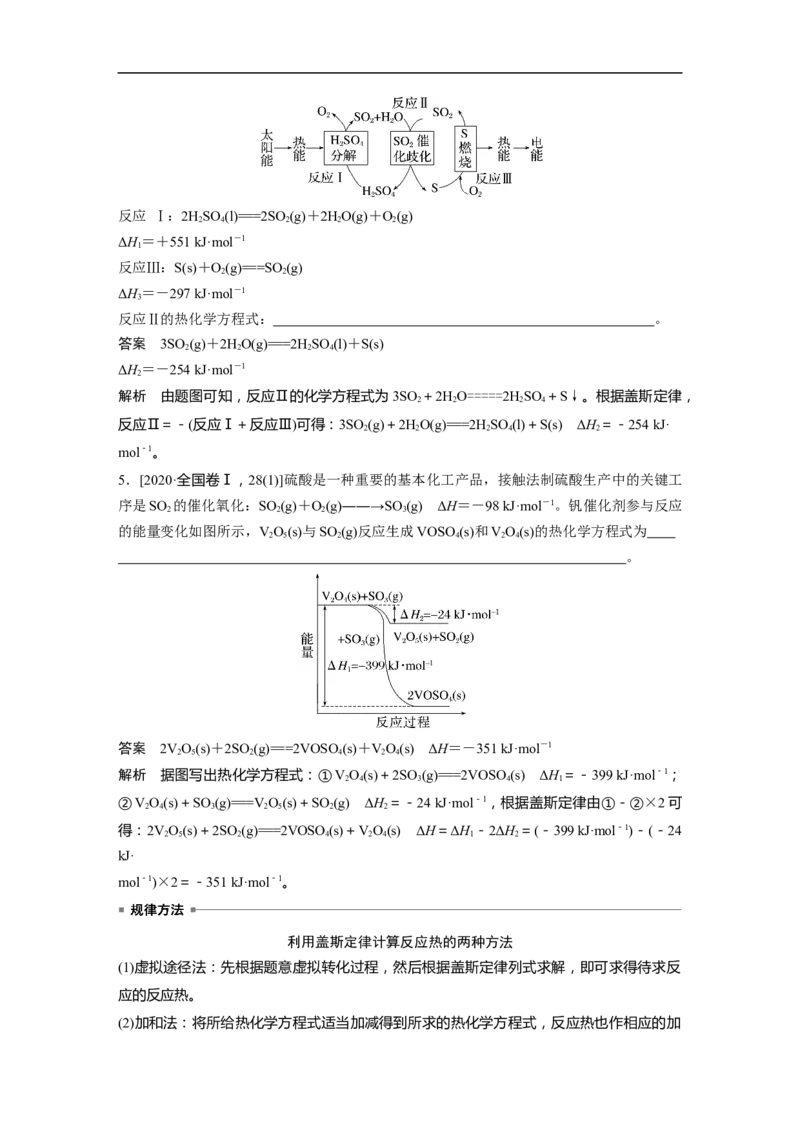
5.[2020·全国卷Ⅰ,28(1)]硫酸是一种重要的基本化工产品,接触法制硫酸生产中的关键工
序是SO 的催化氧化:SO (g)+O(g)――→SO (g) ΔH=-98 kJ·mol-1。钒催化剂参与反应
2 2 2 3
的能量变化如图所示,VO(s)与SO (g)反应生成VOSO(s)和VO(s)的热化学方程式为
2 5 2 4 2 4
。
答案 2VO(s)+2SO (g)===2VOSO(s)+VO(s) ΔH=-351 kJ·mol-1
2 5 2 4 2 4
解析 据图写出热化学方程式:①VO(s)+2SO (g)===2VOSO(s) ΔH =-399 kJ·mol-1;
2 4 3 4 1
②VO(s)+SO (g)===VO(s)+SO (g) ΔH =-24 kJ·mol-1,根据盖斯定律由①-②×2可
2 4 3 2 5 2 2
得:2VO(s)+2SO (g)===2VOSO(s)+VO(s) ΔH=ΔH -2ΔH =(-399 kJ·mol-1)-(-24
2 5 2 4 2 4 1 2
kJ·
mol-1)×2=-351 kJ·mol-1。
利用盖斯定律计算反应热的两种方法
(1)虚拟途径法:先根据题意虚拟转化过程,然后根据盖斯定律列式求解,即可求得待求反
应的反应热。
(2)加和法:将所给热化学方程式适当加减得到所求的热化学方程式,反应热也作相应的加减运算。 流程如下:
三、反应热的比较
6.已知:①S(g)+O(g)===SO (g) ΔH;
2 2 1
②S(s)+O(g)===SO (g) ΔH;
2 2 2
③2HS(g)+O(g)===2S(s)+2HO(l) ΔH;
2 2 2 3
④2HS(g)+3O(g)===2SO (g)+2HO(l) ΔH;
2 2 2 2 4
⑤SO (g)+2HS(g)===3S(s)+2HO(l) ΔH
2 2 2 5
下列关于上述反应焓变的判断不正确的是( )
A.ΔH<ΔH
1 2
B.ΔH<ΔH
3 4
C.ΔH=ΔH-ΔH
5 3 2
D.2ΔH=3ΔH-ΔH
5 3 4
答案 B
解析 等量的S具有的能量:S(g)>S(s),则等量的S(g)完全燃烧生成SO (g)放出的热量多,
2
故ΔH<ΔH ,A正确;等量的HS(g)完全燃烧生成SO (g)放出的热量比不完全燃烧生成S(s)
1 2 2 2
放出的热量多,则ΔH>ΔH ,B错误;根据盖斯定律,由③-②可得⑤,则有ΔH =ΔH -
3 4 5 3
ΔH,C正确;根据盖斯定律,由③×3-⑤×2可得④,则2ΔH=3ΔH-ΔH,D正确。
2 5 3 4
7.室温下,将1 mol的CuSO ·5H O(s)溶于水会使溶液温度降低,热效应为ΔH ,将1 mol
4 2 1
的CuSO (s)溶于水会使溶液温度升高,热效应为ΔH ;CuSO ·5H O(s)受热分解的化学方程
4 2 4 2
式为CuSO ·5H O(s)===CuSO (s)+5HO(l),热效应为ΔH。下列判断正确的是( )
4 2 4 2 3
A.ΔH>ΔH B.ΔH<ΔH
2 3 1 3
C.ΔH+ΔH=ΔH D.ΔH+ΔH>ΔH
1 3 2 1 2 3
答案 B
解析 根据题意知,CuSO ·5H O(s)溶于水会使溶液温度降低,热化学方程式为
4 2
CuSO ·5H O(s)===Cu2+(aq)+SO(aq)+5HO(l) ΔH >0;CuSO (s)溶于水会使溶液温度升高,
4 2 2 1 4
热化学方程式为CuSO (s)===Cu2+(aq)+SO(aq) ΔH <0;根据盖斯定律知,CuSO ·5H O(s)
4 2 4 2受热分解的热化学方程式为CuSO ·5H O(s)===CuSO (s)+5HO(l) ΔH=ΔH-ΔH>0。
4 2 4 2 3 1 2
四、能量图像的分析与应用
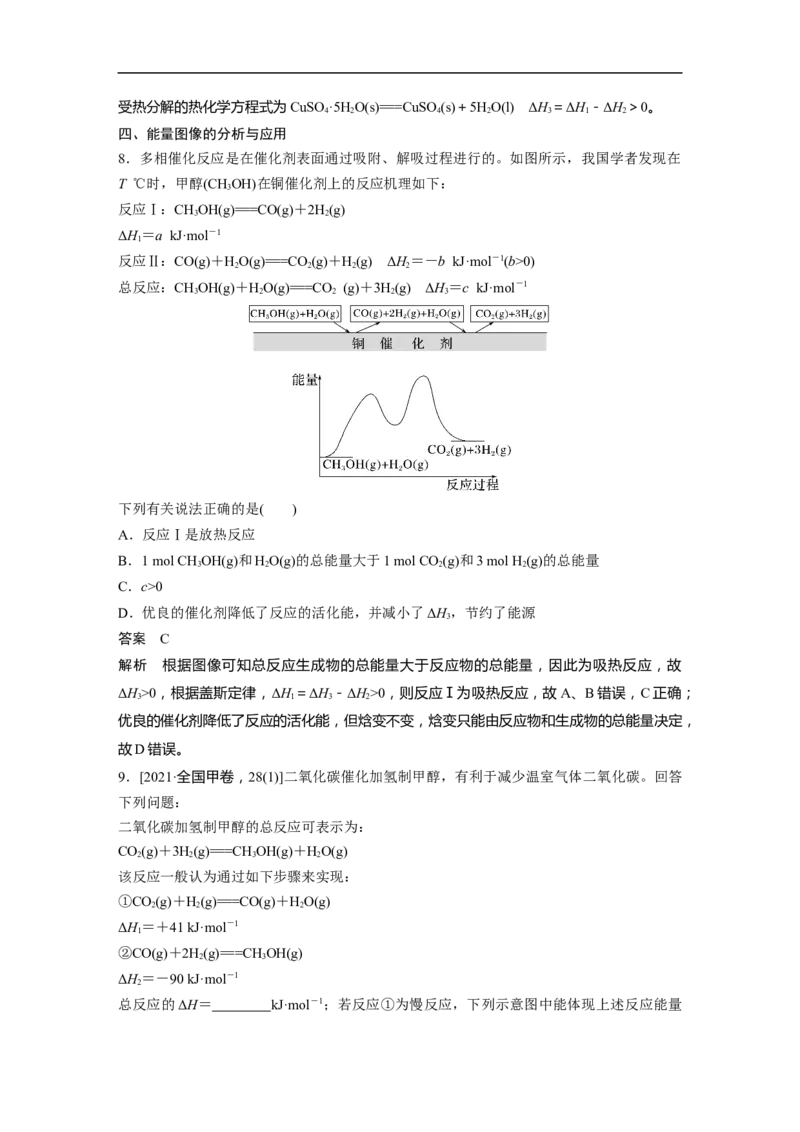
8.多相催化反应是在催化剂表面通过吸附、解吸过程进行的。如图所示,我国学者发现在
T ℃时,甲醇(CHOH)在铜催化剂上的反应机理如下:
3
反应Ⅰ:CHOH(g)===CO(g)+2H(g)
3 2
ΔH=a kJ·mol-1
1
反应Ⅱ:CO(g)+HO(g)===CO(g)+H(g) ΔH=-b kJ·mol-1(b>0)
2 2 2 2
总反应:CHOH(g)+HO(g)===CO (g)+3H(g) ΔH=c kJ·mol-1
3 2 2 2 3
下列有关说法正确的是( )
A.反应Ⅰ是放热反应
B.1 mol CH OH(g)和HO(g)的总能量大于1 mol CO (g)和3 mol H (g)的总能量
3 2 2 2
C.c>0
D.优良的催化剂降低了反应的活化能,并减小了ΔH,节约了能源
3
答案 C
解析 根据图像可知总反应生成物的总能量大于反应物的总能量,因此为吸热反应,故
ΔH>0,根据盖斯定律,ΔH =ΔH -ΔH>0,则反应Ⅰ为吸热反应,故A、B错误,C正确;
3 1 3 2
优良的催化剂降低了反应的活化能,但焓变不变,焓变只能由反应物和生成物的总能量决定,
故D错误。
9.[2021·全国甲卷,28(1)]二氧化碳催化加氢制甲醇,有利于减少温室气体二氧化碳。回答
下列问题:
二氧化碳加氢制甲醇的总反应可表示为:
CO(g)+3H(g)===CHOH(g)+HO(g)
2 2 3 2
该反应一般认为通过如下步骤来实现:
①CO(g)+H(g)===CO(g)+HO(g)
2 2 2
ΔH=+41 kJ·mol-1
1
②CO(g)+2H(g)===CHOH(g)
2 3
ΔH=-90 kJ·mol-1
2
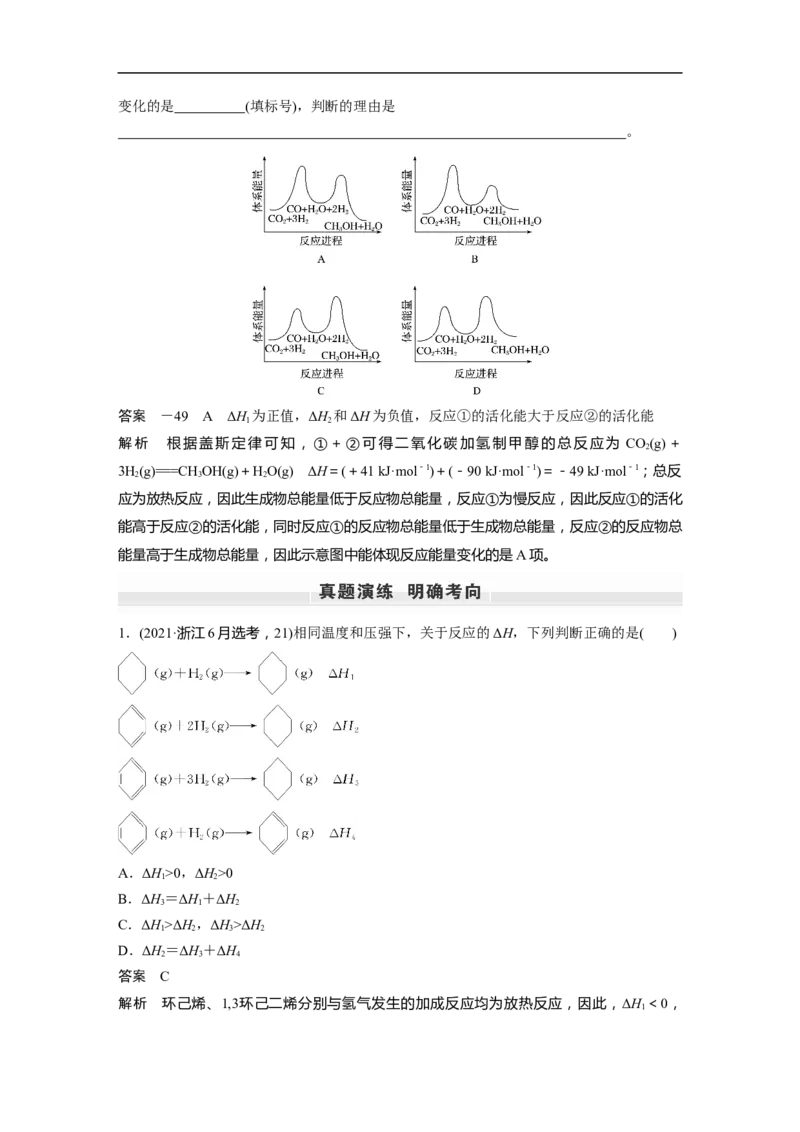
总反应的ΔH= kJ·mol-1;若反应①为慢反应,下列示意图中能体现上述反应能量变化的是 (填标号),判断的理由是
。
答案 -49 A ΔH 为正值,ΔH 和ΔH为负值,反应①的活化能大于反应②的活化能
1 2
解析 根据盖斯定律可知,①+②可得二氧化碳加氢制甲醇的总反应为 CO(g)+
2
3H(g)===CHOH(g)+HO(g) ΔH=(+41 kJ·mol-1)+(-90 kJ·mol-1)=-49 kJ·mol-1;总反
2 3 2
应为放热反应,因此生成物总能量低于反应物总能量,反应①为慢反应,因此反应①的活化
能高于反应②的活化能,同时反应①的反应物总能量低于生成物总能量,反应②的反应物总
能量高于生成物总能量,因此示意图中能体现反应能量变化的是A项。
1.(2021·浙江6月选考,21)相同温度和压强下,关于反应的ΔH,下列判断正确的是( )
A.ΔH>0,ΔH>0
1 2
B.ΔH=ΔH+ΔH
3 1 2
C.ΔH>ΔH,ΔH>ΔH
1 2 3 2
D.ΔH=ΔH+ΔH
2 3 4
答案 C
解析 环己烯、1,3环己二烯分别与氢气发生的加成反应均为放热反应,因此,ΔH <0,
1ΔH <0 ,A不正确;苯分子中没有碳碳双键,其中的碳碳键是介于单键和双键之间的特殊
2
的共价键,因此,其与氢气完全加成的反应热不等于环己烯、1,3环己二烯分别与氢气发生
的加成反应的反应热之和,即ΔH≠ΔH +ΔH ,B不正确;由于1 mol 1,3环己二烯与氢气
3 1 2
完全加成后消耗的氢气是等量环己烯的2倍,故其放出的热量更多,则ΔH>ΔH;苯与氢气
1 2
发生加成反应生成1,3环己二烯的反应为吸热反应(ΔH>0),根据盖斯定律可知,苯与氢气完
4
全加成的反应热:ΔH=ΔH+ΔH,因此ΔH>ΔH,ΔH=ΔH-ΔH,C正确,D不正确。
3 4 2 3 2 2 3 4
2.[2021·广东,19(1)]我国力争于2030年前做到碳达峰,2060年前实现碳中和。CH 与CO
4 2
重整是CO 利用的研究热点之一。该重整反应体系主要涉及以下反应:
2
(a)CH(g)+CO(g)2CO(g)+2H(g) ΔH
4 2 2 1
(b)CO (g)+H(g)CO(g)+HO(g) ΔH
2 2 2 2
(c)CH(g)C(s)+2H(g) ΔH
4 2 3
(d)2CO(g)CO(g)+C(s) ΔH
2 4
(e)CO(g)+H(g)HO(g)+C(s) ΔH
2 2 5
根据盖斯定律,反应a的ΔH = (写出一个代数式即可)。
1
答案 ΔH+ΔH-ΔH(或ΔH-ΔH)
2 3 5 3 4
解析 根据题目所给出的反应方程式关系可知,(a)=(b)+(c)-(e)=(c)-(d),根据盖斯定律
则有ΔH=ΔH+ΔH-ΔH=ΔH-ΔH。
1 2 3 5 3 4
3.(2020·北京,12)依据图示关系,下列说法不正确的是( )
A.石墨燃烧是放热反应
B.1 mol C(石墨)和1 mol CO分别在足量O 中燃烧,全部转化为CO,前者放热多
2 2
C.C(石墨)+CO(g)===2CO(g) ΔH=ΔH-ΔH
2 1 2
D.化学反应的ΔH,只与反应体系的始态和终态有关,与反应途径无关
答案 C
解析 所有的燃烧反应都是放热反应,根据图示,C(石墨)+O (g)===CO(g) ΔH=
2 2 1
-393.5 kJ·mol-1,ΔH <0,则石墨燃烧是放热反应,故A正确;1 mol C(石墨)和1 mol CO
1
分别在足量O 中燃烧,全部转化为CO,1 mol C(石墨)放热多,故B正确;①C(石墨)+
2 2
O(g)===CO(g) ΔH=-393.5 kJ·mol-1,②CO(g)+O(g)===CO(g) ΔH=-283.0 kJ·
2 2 1 2 2 2
mol-1,根据盖斯定律①-②×2可得:C(石墨)+CO(g)===2CO(g) ΔH=ΔH-2ΔH,故C
2 1 2
错误。
4.(2019·浙江4月选考,23)MgCO 和CaCO 的能量关系如图所示(M=Ca、Mg):
3 3已知:离子电荷相同时,半径越小,离子键越强。下列说法不正确的是( )
A.ΔH(MgCO )>ΔH(CaCO)>0
1 3 1 3
B.ΔH(MgCO )=ΔH(CaCO)>0
2 3 2 3
C.ΔH(CaCO)-ΔH(MgCO )=ΔH(CaO)-ΔH(MgO)
1 3 1 3 3 3
D.对于MgCO 和CaCO ,ΔH+ΔH>ΔH
3 3 1 2 3
答案 C
解析 根据盖斯定律,得ΔH=ΔH +ΔH +ΔH ,又已知Ca2+半径大于Mg2+半径,所以
1 2 3
CaCO 的离子键强度弱于MgCO 的离子键强度,CaO的离子键强度弱于MgO的离子键强度。
3 3
A项,ΔH 表示断裂MCO 中的离子键形成M2+和CO所吸收的能量,离子键强度越大,吸
1 3
收的能量越大,因而ΔH(MgCO )>ΔH(CaCO)>0,正确;B项,ΔH 表示断裂CO中共价
1 3 1 3 2
键形成O2-和CO 吸收的能量,与M2+无关,因而ΔH(MgCO )=ΔH(CaCO)>0,正确;C
2 2 3 2 3
项,由以上分析可知ΔH(CaCO)-ΔH(MgCO )<0,而ΔH 表示形成MO离子键所放出的能
1 3 1 3 3
量,ΔH 为负值,CaO的离子键强度弱于MgO,因而ΔH(CaO)>ΔH(MgO),ΔH(CaO)-
3 3 3 3
ΔH(MgO)>0,错误;D项,由以上分析可知ΔH +ΔH>0,ΔH<0,故ΔH +ΔH >ΔH ,正
3 1 2 3 1 2 3
确。
课时精练
1.未来新能源的特点是资源丰富,在使用时对环境无污染或污染很小,且可以再生。下列
符合未来新能源标准的是( )
①天然气 ②煤 ③核能 ④石油 ⑤太阳能 ⑥生物质能 ⑦风能 ⑧氢能
A.①②③④ B.⑤⑥⑦⑧
C.③⑤⑥⑦⑧ D.③④⑤⑥⑦⑧
答案 B
解析 天然气、煤、石油都是化石能源,不可再生,因此不属于未来新能源,①②④不符合
题点;核能使用不当的话对环境有污染,且不可再生,故核能不属于未来新能源,③不符合
题意。
2.已知:①2H(g)+O(g)===2HO(g) ΔH=-483.6 kJ·mol-1;②H(g)+S(g)===HS(g)
2 2 2 2 2
ΔH=-20.1 kJ·mol-1,下列判断正确的是( )
A.若反应②中改用固态硫,则消耗1 mol S(s)反应放出的热量小于20.1 kJ
B.从焓变数值知,单质硫与氧气相比,更容易与氢气化合C.由①②知,水的热稳定性弱于硫化氢
D.氢气的燃烧热ΔH=-241.8 kJ·mol-1
答案 A
解析 固体变为气体,吸收热量,若反应②中改用固态硫,则消耗1 mol S(s)反应放出的热
量小于20.1 kJ,A项正确;由热化学方程式可知,1 mol氢气与氧气反应放出的热量比1
mol氢气与硫反应放出的热量多221.7 kJ,说明氧气与单质硫相比更容易与氢气化合,B项
错误;无法直接比较水和硫化氢的热稳定性,C项错误;燃烧热为101 kPa下,1 mol纯物
质完全燃烧生成稳定的氧化物时所放出的热量,反应①生成的是气态水而不是液态水,D项
错误。
3.某同学设计如图所示实验,探究反应中的能量变化。
下列判断正确的是( )
A.由实验可知,(a)、(b)、(c)所涉及的反应都是放热反应
B.将实验(a)中的铝片更换为等质量的铝粉后释放出的热量有所增加
C.实验(c)中将环形玻璃搅拌棒改为铁质搅拌棒对实验结果没有影响
D.若用NaOH固体测定中和反应反应热,则测定结果偏高
答案 D
解析 A项,Ba(OH) ·8H O与NH Cl的反应属于吸热反应,错误;B项,铝片更换为铝粉,
2 2 4
没有改变反应的本质,放出的热量不变,错误;C项,铁质搅拌棒导热性好,热量损失较大,
错误;D项,NaOH固体溶于水时放热,使测定结果偏高,正确。
4.分别向1 L 0.5 mol·L-1的Ba(OH) 溶液中加入①浓硫酸;②稀硫酸;③稀硝酸,恰好完
2
全反应时的热效应分别为ΔH、ΔH、ΔH,下列关系正确的是( )
1 2 3
A.ΔH>ΔH>ΔH B.ΔH<ΔH<ΔH
1 2 3 1 2 3
C.ΔH>ΔH=ΔH D.ΔH=ΔH<ΔH
1 2 3 1 2 3
答案 B
解析 混合时浓硫酸在被稀释的过程中放热;浓、稀硫酸在与 Ba(OH) 反应时还会形成
2
BaSO 沉淀,Ba2+、SO之间形成化学键的过程中也会放出热量。因放热反应的ΔH取负值,
4故ΔH<ΔH<ΔH。
1 2 3
5.Li/Li O体系的能量循环如图所示。下列说法正确的是( )
2
A.ΔH<0
3
B.ΔH+ΔH+ΔH=ΔH
3 4 5 6
C.ΔH>ΔH
6 5
D.ΔH+ΔH+ΔH+ΔH+ΔH+ΔH=0
1 2 3 4 5 6
答案 C
解析 由O 的气态分子变为气态原子,需要断裂分子中的化学键,因此要吸收能量,
2
ΔH>0,A项错误;物质含有的能量只与物质的始态与终态有关,与反应途径无关,根据物
3
质转化关系可知,ΔH +ΔH +ΔH +ΔH +ΔH =ΔH ,B、D两项错误;ΔH +ΔH +ΔH +
1 2 3 4 5 6 1 2 3
ΔH+ΔH=ΔH,ΔH>0,ΔH>0,ΔH>0,ΔH>0,所以ΔH>ΔH,C项正确。
4 5 6 1 2 3 4 6 5
6.已知碳、一氧化碳、晶体硅的燃烧热分别是ΔH 、ΔH 、ΔH ,则工业冶炼晶体硅的反应
1 2 3
为2C(s)+SiO(s)===Si(s)+2CO(g) ΔH。则下列判断正确的是( )
2 4
A.ΔH>ΔH
1 2
B.2ΔH-2ΔH-ΔH=ΔH
1 2 3 4
C.C(s)+O(g)===CO(g) ΔH
2 1
D.Si+O===SiO ΔH
2 2 3
答案 B
解析 1 mol C完全燃烧放出的热量大于1 mol CO完全燃烧放出的热量,ΔH<ΔH ,A错误;
1 2
根据题给信息,可分别得到热化学方程式:①C(s)+O (g)===CO(g) ΔH,②CO(g)+
2 2 1
O(g)===CO(g) ΔH ,③Si(s)+O(g)===SiO(s) ΔH ,将①×2-②×2-③得,2C(s)+
2 2 2 2 2 3
SiO(s)===Si(s)+2CO(g) ΔH=2ΔH-2ΔH-ΔH,B正确。
2 4 1 2 3
7.对于反应a:C H(g)C H(g)+H(g),反应b:2CH(g)C H(g)+2H(g),当升高温
2 4 2 2 2 4 2 4 2
度时平衡都向右移动。①C(s)+2H(g)===CH(g) ΔH ;②2C(s)+H(g)===C H(g) ΔH ;
2 4 1 2 2 2 2
③2C(s)+2H(g)===C H(g) ΔH 。则①②③中ΔH 、ΔH 、ΔH 的大小顺序排列正确的是(
2 2 4 3 1 2 3
)
A.ΔH>ΔH>ΔH
1 2 3
B.ΔH>ΔH>ΔH
2 3 1
C.ΔH>ΔH>ΔH
2 1 3
D.ΔH>ΔH>ΔH
3 2 1
答案 B解析 对于反应a、反应b,升高温度平衡都向右移动,故二者均为吸热反应,ΔH>0、
a
ΔH>0。经分析知a=②-③,ΔH=ΔH -ΔH>0,推知ΔH>ΔH ;b=③-2×①,故ΔH
b a 2 3 2 3 b
=ΔH-2ΔH>0,推知ΔH>2ΔH>ΔH。
3 1 3 1 1
8.发射运载火箭使用的是以液氢为燃料、液氧为氧化剂的高能低温推进剂,已知:
①H(g)===H(l) ΔH=-0.92 kJ·mol-1
2 2 1
②O(g)===O(l) ΔH=-6.84 kJ·mol-1
2 2 2
下列说法正确的是( )
A.H(g)与O(g)反应生成HO(g)放热483.6 kJ·mol-1
2 2 2
B.氢气的燃烧热ΔH=-241.8 kJ·mol-1
C.火箭中液氢燃烧的热化学方程式为2H(l)+O(l)===2HO(g) ΔH=-474.92 kJ·mol-1
2 2 2
D.HO(g)===HO(l) ΔH=-88 kJ·mol-1
2 2
答案 C
解析 由题图可知,每2 mol H (g)与1 mol O (g)反应生成2 mol H O(g)放热483.6 kJ,选项
2 2 2
中未指明反应物的物质的量,故A错误;氢气的燃烧热ΔH=- kJ·mol-1=-285.8 kJ·
mol-1,故 B 错误;由盖斯定律可知,火箭中液氢燃烧的热化学方程式为 2H(l)+
2
O(l)===2HO(g) ΔH=-483.6 kJ·mol-1-(-0.92×2-6.84)kJ·mol-1=-474.92 kJ·mol-1,
2 2
故C正确;HO(g)===HO(l) ΔH=-44 kJ·mol-1,故D错误。
2 2
9.(2022·湖南汨罗市高三检测)如图是金属镁和卤素单质(X )反应的能量变化示意图。下列
2
说法正确的是( )
A.热稳定性:MgF