文档内容
重点题空热练(一) 仪器连接、操作先后顺序集训
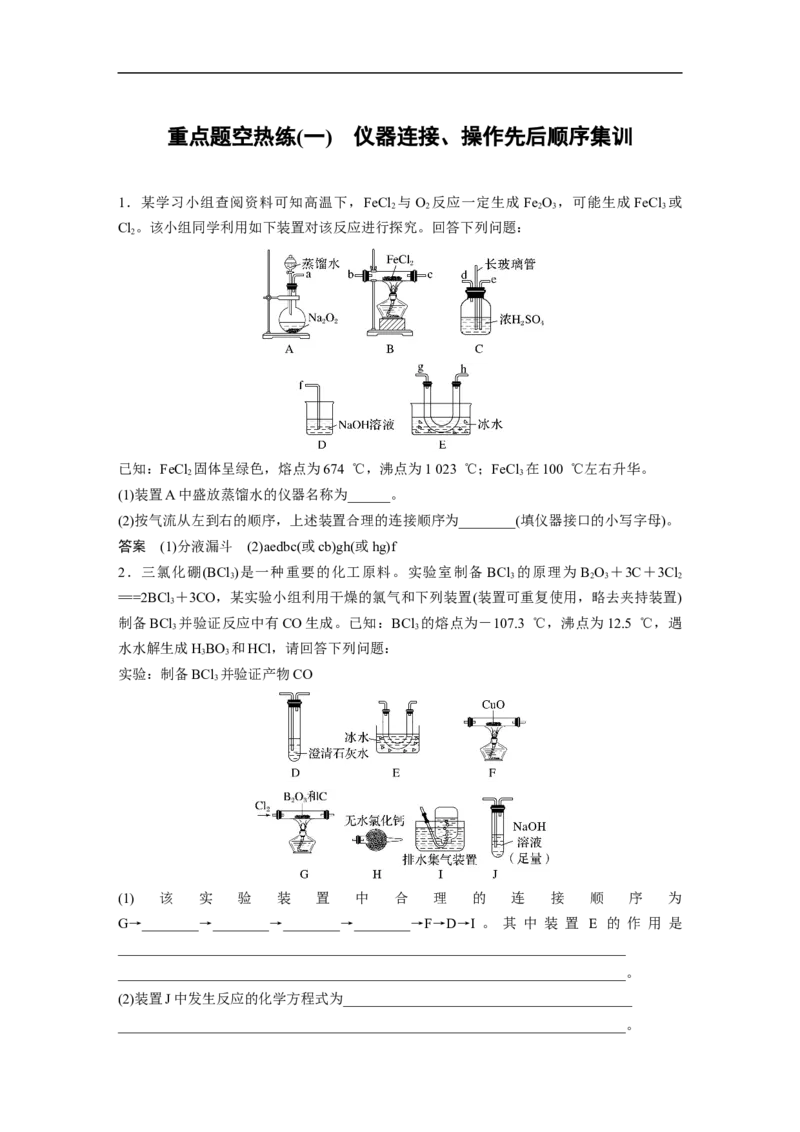
1.某学习小组查阅资料可知高温下,FeCl 与O 反应一定生成Fe O ,可能生成FeCl 或
2 2 2 3 3
Cl。该小组同学利用如下装置对该反应进行探究。回答下列问题:
2
已知:FeCl 固体呈绿色,熔点为674 ℃,沸点为1 023 ℃;FeCl 在100 ℃左右升华。
2 3
(1)装置A中盛放蒸馏水的仪器名称为______。
(2)按气流从左到右的顺序,上述装置合理的连接顺序为________(填仪器接口的小写字母)。
答案 (1)分液漏斗 (2)aedbc(或cb)gh(或hg)f
2.三氯化硼(BCl )是一种重要的化工原料。实验室制备 BCl 的原理为 B O +3C+3Cl
3 3 2 3 2
===2BCl +3CO,某实验小组利用干燥的氯气和下列装置(装置可重复使用,略去夹持装置)
3
制备BCl 并验证反应中有CO生成。已知:BCl 的熔点为-107.3 ℃,沸点为12.5 ℃,遇
3 3
水水解生成HBO 和HCl,请回答下列问题:
3 3
实验:制备BCl 并验证产物CO
3
(1) 该 实 验 装 置 中 合 理 的 连 接 顺 序 为
G→________→________→________→________→F→D→I 。 其 中 装 置 E 的 作 用 是
________________________________________________________________________
________________________________________________________________________。
(2)装置J中发生反应的化学方程式为_________________________________________
________________________________________________________________________。答案 (1)E H J H 将BCl 冷凝为液态分离出来
3
(2)2NaOH+Cl===NaCl+NaClO+HO
2 2
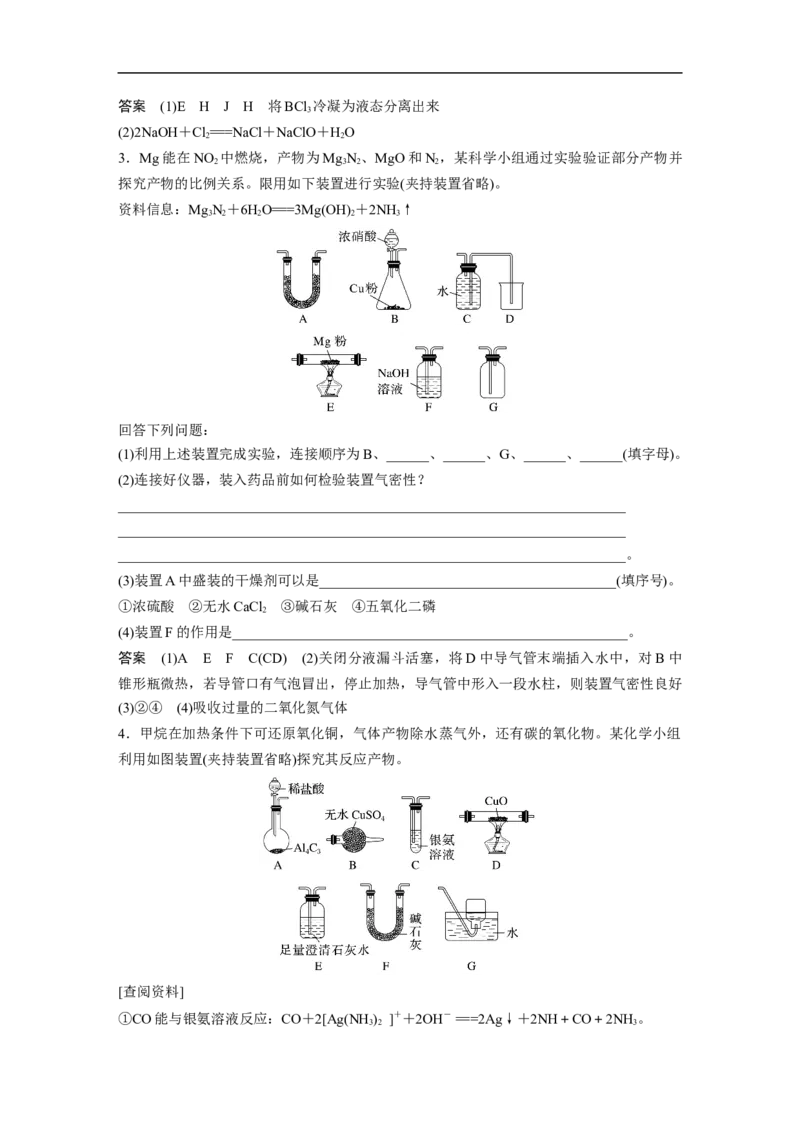
3.Mg能在NO 中燃烧,产物为MgN 、MgO和N ,某科学小组通过实验验证部分产物并
2 3 2 2
探究产物的比例关系。限用如下装置进行实验(夹持装置省略)。
资料信息:MgN+6HO===3Mg(OH) +2NH ↑
3 2 2 2 3
回答下列问题:
(1)利用上述装置完成实验,连接顺序为B、______、______、G、______、______(填字母)。
(2)连接好仪器,装入药品前如何检验装置气密性?
________________________________________________________________________
________________________________________________________________________
________________________________________________________________________。
(3)装置A中盛装的干燥剂可以是__________________________________________(填序号)。
①浓硫酸 ②无水CaCl ③碱石灰 ④五氧化二磷
2
(4)装置F的作用是________________________________________________________。
答案 (1)A E F C(CD) (2)关闭分液漏斗活塞,将D中导气管末端插入水中,对B中
锥形瓶微热,若导管口有气泡冒出,停止加热,导气管中形入一段水柱,则装置气密性良好
(3)②④ (4)吸收过量的二氧化氮气体
4.甲烷在加热条件下可还原氧化铜,气体产物除水蒸气外,还有碳的氧化物。某化学小组
利用如图装置(夹持装置省略)探究其反应产物。
[查阅资料]
①CO能与银氨溶液反应:CO+2[Ag(NH) ]++2OH- ===2Ag↓+2NH+CO+2NH 。
3 2 3②Cu O为红色,不与Ag+反应,能发生反应:Cu O+2H+===Cu2++Cu+HO。
2 2 2
回答下列问题:
(1)装置A中反应的化学方程式为______________________________________________。
(2)按气流方向各装置从左到右的连接顺序为A→__________________________________(填
字母)。
(3)实验中滴加稀盐酸的操作为________________________________________________
________________________________________________________________________。
(4)已知气体产物中含有CO,则装置C中可观察到的现象是________________________;
装置F的作用为______________________________________________________________。
答案 (1)AlC +12HCl===3CH↑+4AlCl
4 3 4 3
(2)F→D→B→E→C→G (3)先打开分液漏斗上口的玻璃塞(或先使分液漏斗上口的玻璃塞的
凹槽对准漏斗上的小孔),再将分液漏斗下面的旋塞打开,使稀盐酸缓慢滴下 (4)试管内有
银镜生成 除去甲烷中的 HCl 气体和水蒸气
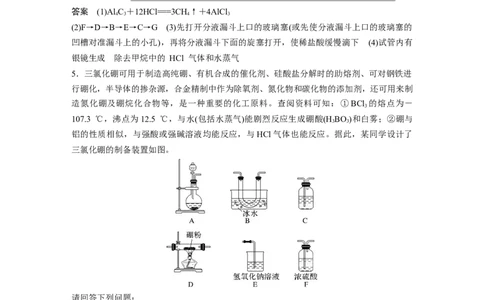
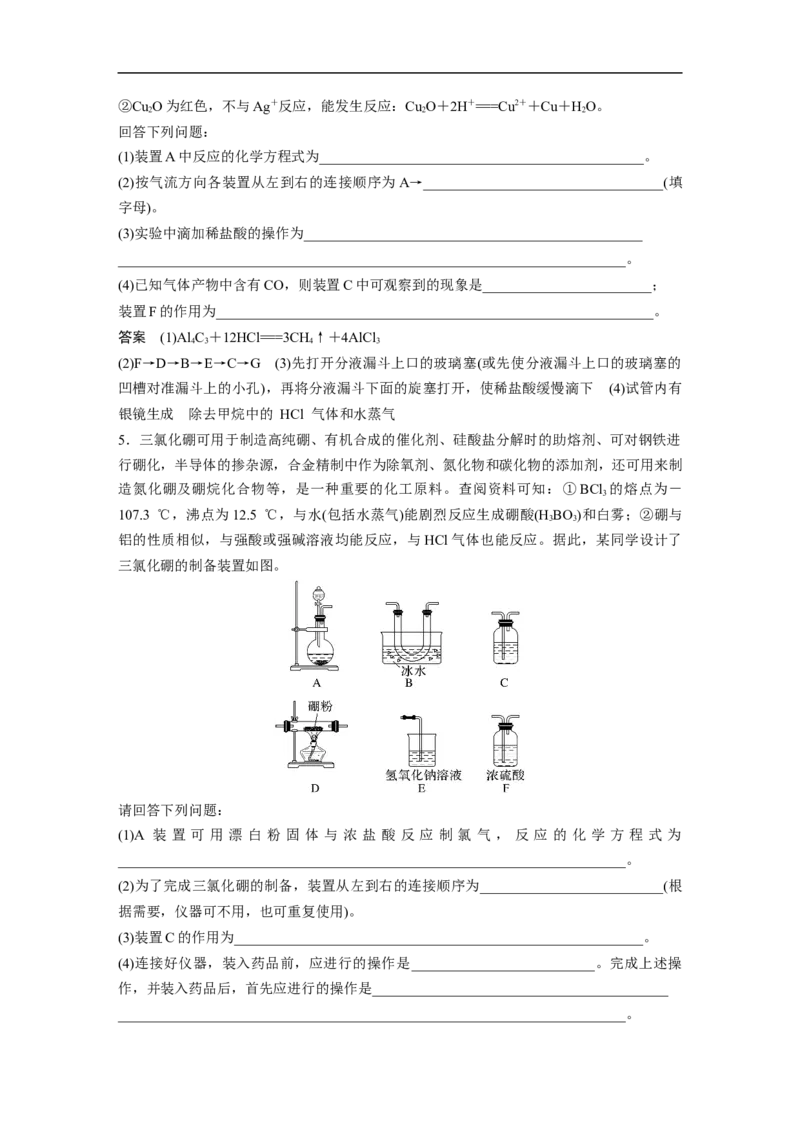
5.三氯化硼可用于制造高纯硼、有机合成的催化剂、硅酸盐分解时的助熔剂、可对钢铁进
行硼化,半导体的掺杂源,合金精制中作为除氧剂、氮化物和碳化物的添加剂,还可用来制
造氮化硼及硼烷化合物等,是一种重要的化工原料。查阅资料可知:①BCl 的熔点为-
3
107.3 ℃,沸点为12.5 ℃,与水(包括水蒸气)能剧烈反应生成硼酸(H BO)和白雾;②硼与
3 3
铝的性质相似,与强酸或强碱溶液均能反应,与HCl气体也能反应。据此,某同学设计了
三氯化硼的制备装置如图。
请回答下列问题:
(1)A 装 置 可 用 漂 白 粉 固 体 与 浓 盐 酸 反 应 制 氯 气 , 反 应 的 化 学 方 程 式 为
________________________________________________________________________。
(2)为了完成三氯化硼的制备,装置从左到右的连接顺序为__________________________(根
据需要,仪器可不用,也可重复使用)。
(3)装置C的作用为__________________________________________________________。
(4)连接好仪器,装入药品前,应进行的操作是__________________________。完成上述操
作,并装入药品后,首先应进行的操作是__________________________________________
________________________________________________________________________。答案 (1)Ca(ClO) +4HCl(浓)===CaCl +2Cl↑+2HO (2)ACFDBFE (3)除去Cl 中混有的
2 2 2 2 2
HCl气体,防止其与硼发生副反应(生成H 与Cl 混合共热有爆炸危险) (4)检查装置气密性
2 2
打开分液漏斗活塞,通一段时间Cl
2
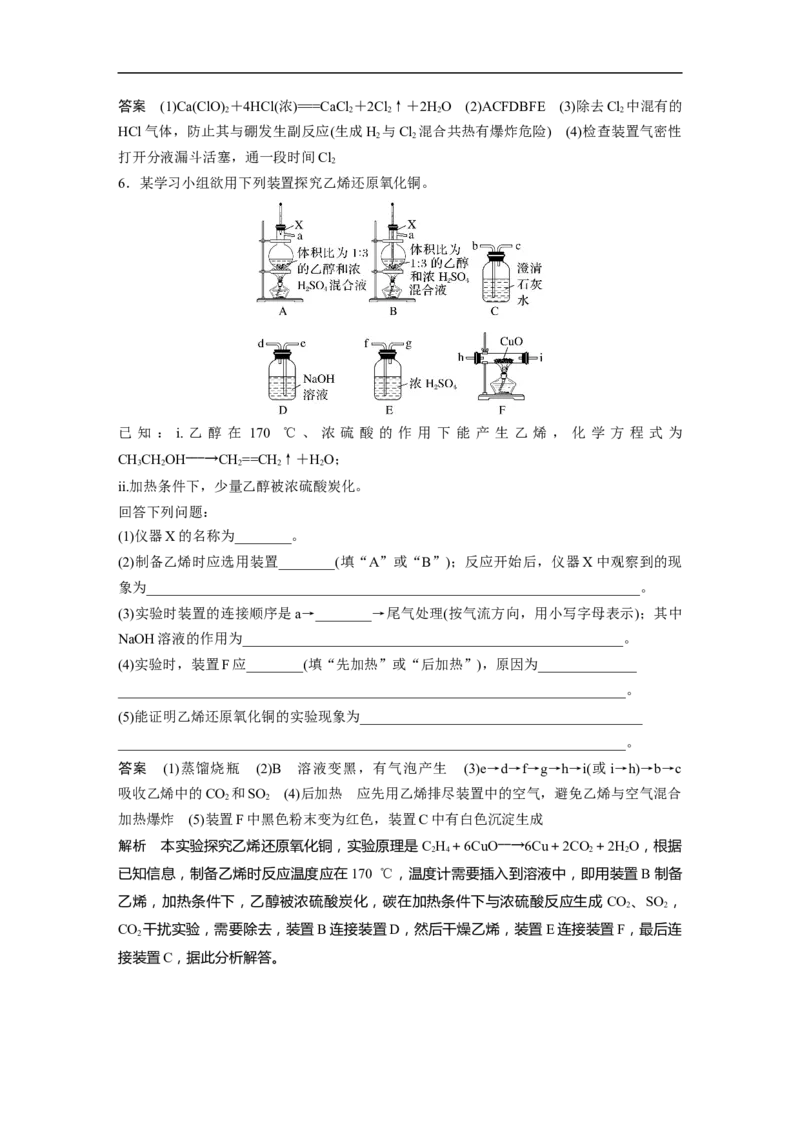
6.某学习小组欲用下列装置探究乙烯还原氧化铜。
已 知 : i. 乙 醇 在 170 ℃ 、 浓 硫 酸 的 作 用 下 能 产 生 乙 烯 , 化 学 方 程 式 为
CHCHOH―――→CH==CH↑+HO;
3 2 2 2 2
ii.加热条件下,少量乙醇被浓硫酸炭化。
回答下列问题:
(1)仪器X的名称为________。
(2)制备乙烯时应选用装置________(填“A”或“B”);反应开始后,仪器X中观察到的现
象为______________________________________________________________________。
(3)实验时装置的连接顺序是a→________→尾气处理(按气流方向,用小写字母表示);其中
NaOH溶液的作用为______________________________________________________。
(4)实验时,装置F应________(填“先加热”或“后加热”),原因为______________
________________________________________________________________________。
(5)能证明乙烯还原氧化铜的实验现象为________________________________________
________________________________________________________________________。
答案 (1)蒸馏烧瓶 (2)B 溶液变黑,有气泡产生 (3)e→d→f→g→h→i(或i→h)→b→c
吸收乙烯中的CO 和SO (4)后加热 应先用乙烯排尽装置中的空气,避免乙烯与空气混合
2 2
加热爆炸 (5)装置F中黑色粉末变为红色,装置C中有白色沉淀生成
解析 本实验探究乙烯还原氧化铜,实验原理是C H +6CuO――→6Cu+2CO +2HO,根据
2 4 2 2
已知信息,制备乙烯时反应温度应在170 ℃,温度计需要插入到溶液中,即用装置B制备
乙烯,加热条件下,乙醇被浓硫酸炭化,碳在加热条件下与浓硫酸反应生成 CO 、SO ,
2 2
CO 干扰实验,需要除去,装置B连接装置D,然后干燥乙烯,装置E连接装置F,最后连
2
接装置C,据此分析解答。