文档内容
2025届高三化学一轮专题复习讲义(05)
专题二 物质结构
2-1 元素周期律与元素周期表(1课时)
【复习目标】
1.了解元素周期表(长式)的结构(周期、族)及其应用。掌握同一周期、同一主族元素的原
子结构与元素性质的递变规律。
2.理解元素(主族和零族)原子结构、在周期表中的位置、性质及其它们之间的关系。
3.知道化学键的含义。能用电子式、结构式和结构简式表示一些常见物质的结构。能识
别典型的离子化合物和共价化合物。
【重点突破】
1.同周期、同主族元素性质及其递变性规律。
2.“位——构——性”的推断及应用。
【真题再现】
例1.(2023·江苏卷)元素C、Si、Ge位于周期表中IVA族 。下列说法正确的是
A.原子半径:r(C) >r(Si) >r(Ge)
B.第一电离能:I(C) <I(Si) <I(Ge)
1 1 1
C.碳单质、晶体硅、SiC均为共价晶体
D.可在周期表中元素Si附近寻找新半导体材料
解析:A项,同主族元素原子半径从上往下原子半径增大,故原子半径:r(C) < r(Si) <
r(Ge),错误;B项,同周期主族元素,从上往下原子半径增大,更易失电子,第一电离能:
I(C) > I(Si) > I(Ge),错误;C项,晶体硅、SiC均为共价晶体,碳单质中金刚石为共价
1 1 1
晶体,而石墨为混合晶体,C 为分子晶体,错误;D项,周期表中元素Si附近存在许多准
60
金属,可在其周围寻找半导体材料,正确。
答案:D
例2.(2022·江苏卷)工业上电解熔融Al O 和冰晶石(Na AlF)的混合物可制得铝。下列说法
2 3 3 6
正确的是
A.半径大小:r(Al3+) < r(Na+) B.电负性大小:χ(F)<χ(O)
C.电离能大小:I(O) <I(Na) D.碱性强弱:NaOH<Al(OH)
1 1 3
解析:A项,核外电子数相同时,核电荷数越大,半径越小,故半径大小为r(Al3+)<r(Na+),正
确;B项,同周期元素核电荷数越大电负性越大,故χ(F)>χ(O),错误;C项,同周期从左
往右第一电离能呈增大趋势,同主族从上往下第一电离能呈减小趋势,故电离能大小为
I(O)>I(Na),错误;D项,元素金属性越强,其最高价氧化物对应水化物的碱性越强,故
1 1
碱性强弱为NaOH >Al(OH) ,错误。
3
答案:A
【知能整合】
1.金属性、非金属性强弱的判断方法
INCLUDEPICTURE "E:\\2020赵瑊\\二轮\\大二轮 化学 通用\\word\\W440.TIF" \*
MERGEFORMATINET INCLUDEPICTURE "E:\\2020赵瑊\\二轮\\大二轮 化学 通用\\word\
\W440.TIF" \* MERGEFORMATINET INCLUDEPICTURE "E:\\2020赵瑊\\二轮\\大二轮 化
学 通用\\word\\W440.TIF" \* MERGEFORMATINET INCLUDEPICTURE "G:\\盐城二轮\\全
书完整的Word版文档\\W440.TIF" \* MERGEFORMATINETINCLUDEPICTURE "E:\\2020赵瑊\\二轮\\大二轮 化学 通用\\word\\W441.TIF" \*
MERGEFORMATINET INCLUDEPICTURE "E:\\2020赵瑊\\二轮\\大二轮 化学 通用\\word\
\W441.TIF" \* MERGEFORMATINET INCLUDEPICTURE "E:\\2020赵瑊\\二轮\\大二轮 化
学 通用\\word\\W441.TIF" \* MERGEFORMATINET INCLUDEPICTURE "G:\\盐城二轮\\全
书完整的Word版文档\\W441.TIF" \* MERGEFORMATINET
2.同周期、同主族元素性质的递变规律
性质 同周期(自左而右) 同主族(自上而下)
金属性 减弱 增强
非金属性 增强 减弱
最高正价升高 (O、F除
主要化合价 最高正价相同 (O、F除外)
外)
最高价氧化物对应水
酸性增强;碱性减弱 酸性减弱;碱性增强
化物的酸、碱性
非金属气态氢化物的
增强 减弱
稳定性
原子半径 减小 增大
电负性 增强 减弱
增大趋势(IIA族与IIIA
第一电离能 减小
族、VA族与VIA反常)
例3.(2021·江苏卷)前4周期主族元素X、Y、Z、W的原子序数依次增大,X是空气中含量最
多的元素,Y的周期序数与族序数相等,基态时Z原子3p原子轨道上有5个电子,W与
Z处于同一主族。下列说法正确的是
A.原子半径:r(X)<r(Y)<r(Z)<r(W)
B.X的第一电离能比同周期相邻元素的大
C.Y的最高价氧化物对应水化物的酸性比Z的强
D.Z的简单气态氢化物的热稳定性比W的弱
解析:前4周期主族元素X、Y、Z、W的原子序数依次增大,X是空气中含量最多的元素,则
X为N元素;Y的周期序数与族序数相等,则Y为Al;基态时Z原子3p原子轨道上有5
个电子,则Z为Cl;W与Z处于同一主族,则W为Br。A项,根据同周期从左到右原子
半径逐渐减小,同主族从上到下原子半径逐渐增大,因此原子半径:r(X) <r(z) <r(y)
<r(w),错误;B项,根据同周期从左到右第一电离能呈增大趋势,但N的2p处于半充满
状态,因此X(N)的第一电离能比同周期相邻元素的大,正确;C项,同周期元素原子序数
增大,其最高价氧化物对应水化物的酸性逐渐增强,则Al(OH) <HClO,错误;D项,同
3 4
主族原子序数增大,非金属性逐渐减弱,简单氢化物的稳定性逐渐减弱,所以Z的简单气态氢化物的热稳定性比W的强,错误。
答案:B
例4.(2021·江苏适应性)13Al、15P、16S、17Cl是周期表中的短周期主族元素。下列有关说法正
确的是
A.元素Al在周期表中位于第4周期ⅢA族
B.元素P的简单气态氢化物的化学式为PH
4
C.第一电离能:I(Al) <I(P) <I(S)
1 1 1
D.最高价氧化物的水化物的酸性:HPO <HSO <HClO
3 4 2 4 4
解析:A项,Al原子3个电子层,位于第3周期IIIA族,错误;B项,P原子最外层5个电子,
与氢原子共用三对电子,简单气态氢化物的化学式为PH ,错误;C项,同一周期,从左到
3
右,第一电离能呈现增大的趋势, VA族与VIA族反常,所以第一电离能:I(Al) <I(S)
1 1
<I(P),错误;D项,非金属性:P<S<Cl,酸性:HPO <HSO <HClO,正确。
1 3 4 2 4 4
答案:D
【知能整合】
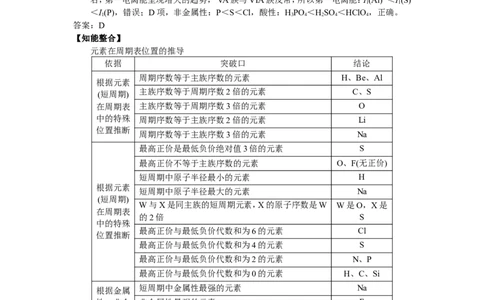
元素在周期表位置的推导
依据 突破口 结论
周期序数等于主族序数的元素 H、Be、Al
根据元素
(短周期)
主族序数等于周期序数2倍的元素 C、S
在周期表 主族序数等于周期序数3倍的元素 O
中的特殊 周期序数等于主族序数2倍的元素 Li
位置推断
周期序数等于主族序数3倍的元素 Na
最高正价是最低负价绝对值3倍的元素 S
最高正价不等于主族序数的元素 O、F(无正价)
短周期中原子半径最小的元素 H
根据元素
短周期中原子半径最大的元素 Na
(短周期)
W与X是同主族的短周期元素,X的原子序数是W W是O,X是
在周期表
的2倍 S
中的特殊
最高正价与最低负价代数和为6的元素 Cl
位置推断
最高正价与最低负价代数和为4的元素 S
最高正价与最低负价代数和为2的元素 N、P
最高正价与最低负价代数和为0的元素 H、C、Si
短周期中金属性最强的元素 Na
根据金属
性、非金 非金属性最强的元素 F
属性推断
应用最广泛的半导体材料 Si
空气中含量最多的元素 N
根据含
地壳中含量最多的元素 O
量推断
地壳中含量最多的金属元素 Al
Al、Al O、
2 3
既能与强酸反应又能与强碱反应的常见物质 Al(OH) 、
3
根据特殊 NaHCO 3
性质推断 形成化合物种类最多、其单质是硬度最大的物质的
C
元素
气态氢化物溶于水显碱性的元素 N密度最小的气体 H
2
气态氢化物能和它的氧化物在常温下反应生成该元
S
素的单质的元素
气态氢化物和最高价氧化物对应的水化物能反应生
N
成离子化合物的元素
同主族并且能够形成离子化合物的两种元素 H、Na
同周期的三种元素,最高价氧化物对应水化物两两 Na、Al、S(或
之间反应生成盐和水 Cl)
【体系再构】
【随堂反馈】
基础训练
1.镆(Mc)是115号元素,其原子核外最外层电子数是5。下列说法不正确的是
A.Mc的原子核外有115个电子 B.Mc是第七周期第VA族元素
C.Mc在同族元素中金属性最强D.Mc的原子半径小于同族非金属元素原子
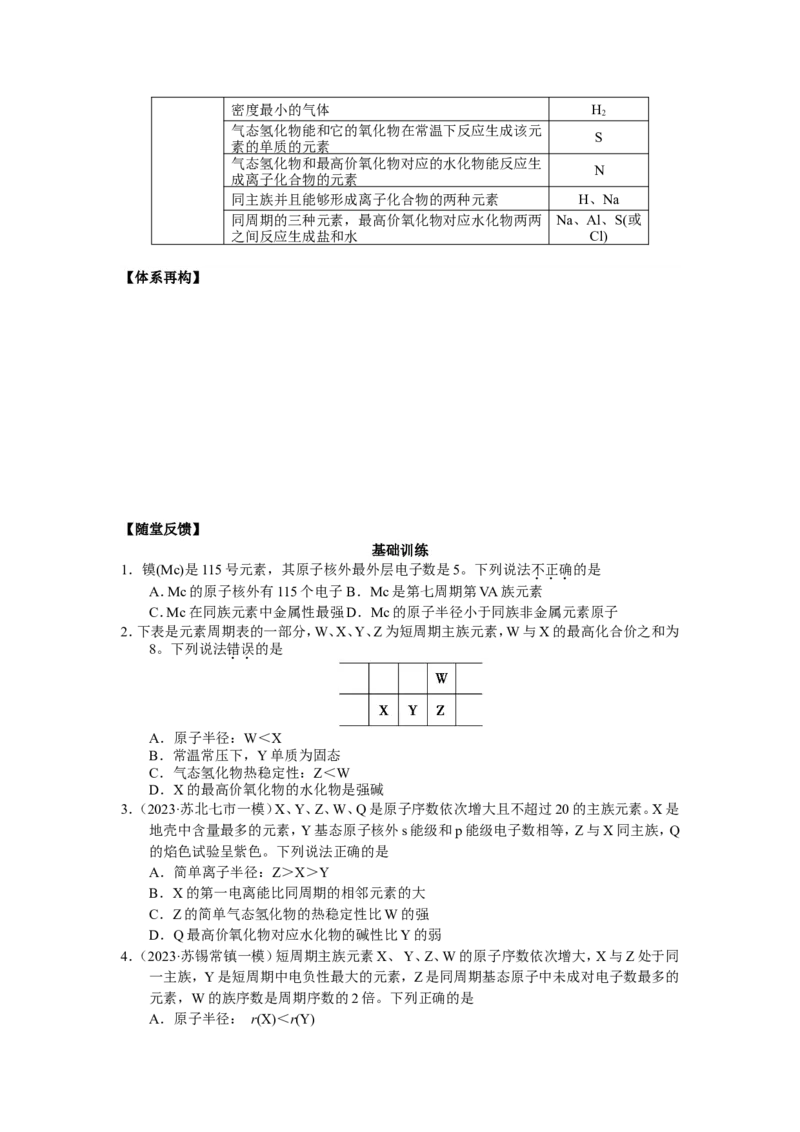
2.下表是元素周期表的一部分,W、X、Y、Z为短周期主族元素,W与X的最高化合价之和为
8。下列说法错误的是
A.原子半径:W<X
B.常温常压下,Y单质为固态
C.气态氢化物热稳定性:Z<W
D.X的最高价氧化物的水化物是强碱
3.(2023·苏北七市一模)X、Y、Z、W、Q是原子序数依次增大且不超过20的主族元素。X是
地壳中含量最多的元素,Y基态原子核外s能级和p能级电子数相等,Z与X同主族,Q
的焰色试验呈紫色。下列说法正确的是
A.简单离子半径:Z>X>Y
B.X的第一电离能比同周期的相邻元素的大
C.Z的简单气态氢化物的热稳定性比W的强
D.Q最高价氧化物对应水化物的碱性比Y的弱
4.(2023·苏锡常镇一模)短周期主族元素X、 Y、Z、W的原子序数依次增大,X与Z处于同
一主族,Y是短周期中电负性最大的元素,Z是同周期基态原子中未成对电子数最多的
元素,W的族序数是周期序数的2倍。下列正确的是
A.原子半径: r(X)<r(Y)B.Z的第一电离能比W的小
C.元素Z在周期表中位于第3周期VA族
D.X的简单气态氢化物的热稳定性比Z的弱
5.(2023·盐城二模)由SiCl 制备高纯SiH 的反应为SiCl +LiAlH 乙醚 SiH↑+LiCl+AlCl 。下
4 4 4 4 4 3
列说法正确的是
A.热稳定性:HCl>SiH B.离子半径:r(Li+)>r(H-)
4
C.第一电离能:I(Al)>I(Cl) D.共价键的极性:Si-Cl>Al-Cl
1 1
拓展训练
6.(2023·南通二模)X、Y、Z、W是原子序数依次增大的四种短周期元素。X和Y的基态原子
s能级电子总数均等于其p能级电子总数,Z原子的最外层电子数是Y原子最外层电子
数的2倍,W和X位于同一主族。下列说法不正确的是
A.Z单质可用于制作半导体材料
B.元素Z、W的最高价氧化物对应的水化物都是强酸
C.元素X的简单气态氢化物的热稳定性比W的强
D.简单离子半径:r(W)>r(X)>r(Y)
7.(2023·广东卷)化合物XYZ ME 可作肥料,所含的5种元素位于主族,在每个短周期均有
4 4
分布,仅有Y和M同族。Y的基态原子价层p轨道半充满,X的基态原子价层电子排布
式为nsn-1,X与M同周期,E在地壳中含量最多。下列说法正确的是
A.电负性:E>Y>Z
B.氢化物沸点:M>Y>E
C.第一电离能:X>E>Y
D.YZ 和YE的空间结构均为三角锥形
3
8.(2023·湖南高考)日光灯中用到的某种荧光粉的主要成分为3W(ZX)·WY。已知:X、Y、
3 4 2 2
Z和W为原子序数依次增大的前20号元素,W为金属元素。基态X原子s轨道上的电
子数和p轨道上的电子数相等,基态X、Y、Z原子的未成对电子数之比为2︰1︰3。下列
说法正确的是
A.电负性:X>Y>Z>W
B.原子半径:X<Y<Z<W
C.Y和W的单质都能与水反应生成气体
D.Z元素最高价氧化物对应的水化物具有强氧化性
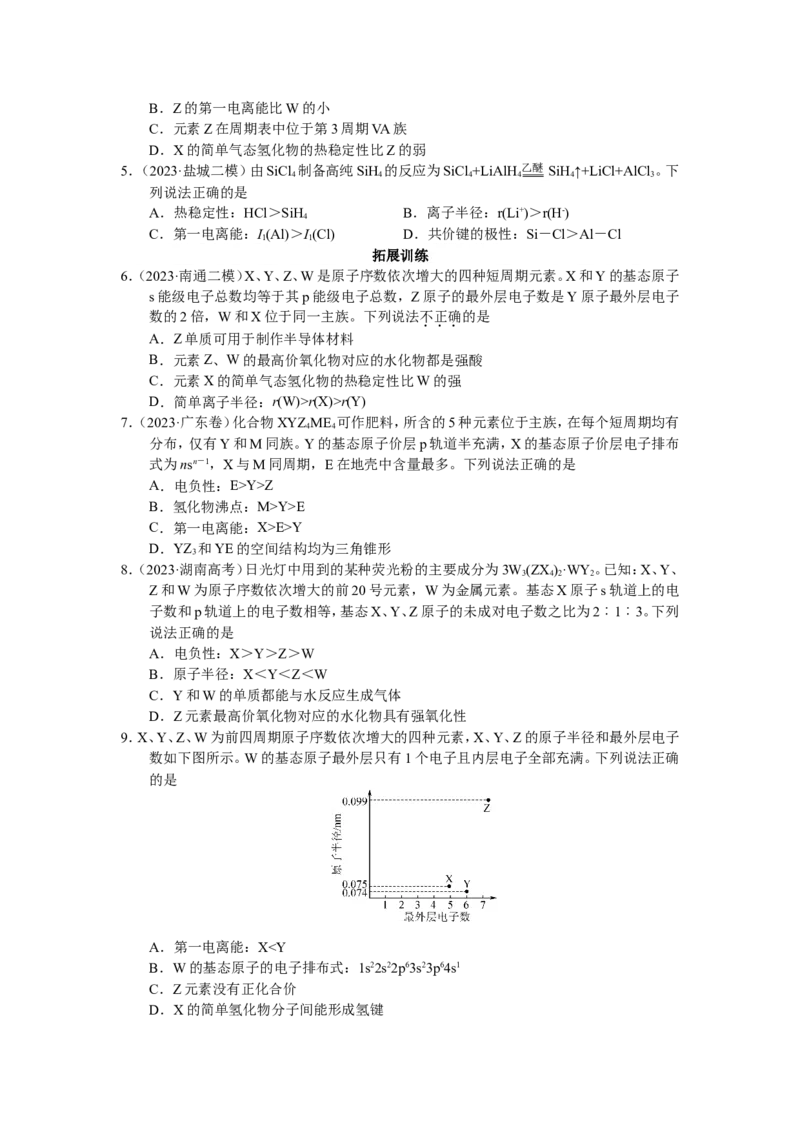
9.X、Y、Z、W为前四周期原子序数依次增大的四种元素,X、Y、Z的原子半径和最外层电子
数如下图所示。W的基态原子最外层只有1个电子且内层电子全部充满。下列说法正确
的是
A.第一电离能:X