文档内容
2025届高三化学一轮专题复习讲义(15)
专题三 基本理论
3-8 沉淀溶解平衡(1课时)
【复习目标】
1.认识难溶电解质的沉淀溶解平衡的概念、特征和影响因素。
2.理解难溶电解质的沉淀溶解平衡在沉淀的生成、溶解、转化中的应用。
3.溶度积常数的概念、表达式及在计算中的应用。
【重点突破】
难溶电解质的沉淀溶解平衡在沉淀的生成、溶解、转化中的应用。
【真题再现】
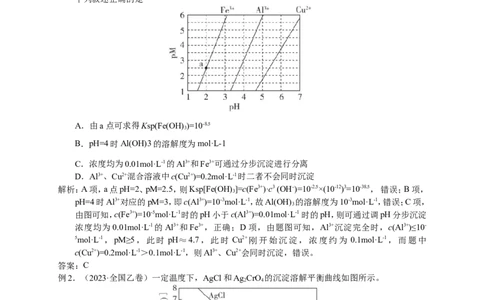
例1.(2023·全国甲卷)下图为Fe(OH) 、Al(OH) 和Cu(OH) 在水中达沉淀溶解平衡时的pM-pH
3 3 2
关系图(pM= -lg[c(M)/ ( mol·L-1);c(M) ≤10-5 mol·L-1 可认为M离子沉淀完全)。
下列叙述正确的是
A.由a 点可求得Ksp(Fe(OH) )=10-8.5
3
B.pH=4时Al(OH)3的溶解度为mol·L-1
C.浓度均为0.01mol·L-1的Al3+和Fe3+可通过分步沉淀进行分离
D.Al3+、Cu2+混合溶液中c(Cu2+)=0.2mol·L-1时二者不会同时沉淀
解析:A项,a点pH=2、pM=2.5,则Ksp[Fe(OH) ]=c(Fe3+)·c3 (OH-)=10-2.5×(10-12)3=10-38.5, 错误;B项,
3
pH=4时Al3+对应的pM=3,即c(Al3+)=10-3mol·L-1,故Al(OH) 的溶解度为10-3mol·L-1,错误;C项,
3
由图可知,c(Fe3+)=10-5mol·L-1时的pH小于c(Al3+)=0.01mol·L-1 时的pH,则可通过调pH分步沉淀
浓度均为0.01mol·L-1的Al3+和Fe3+,正确;D项,由题图可知,Al3+沉淀完全时,c(Al3+)≤10-
5mol·L-1,pM≥5,此时 pH≈4.7,此时 Cu2+刚开始沉淀,浓度约为 0.1mol·L-1,而题中
c(Cu2+)=0.2mol·L-1>0.1mol·L-1,则Al3+、Cu2+会同时沉淀,错误。
答案:C
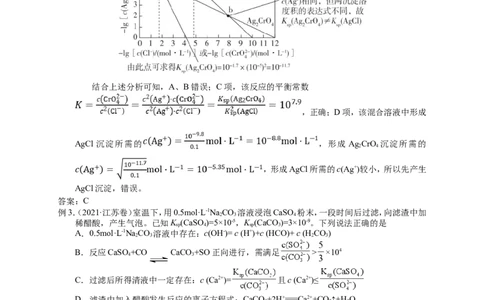
例2.(2023·全国乙卷)一定温度下,AgCl和Ag CrO 的沉淀溶解平衡曲线如图所示。
2 4
下列说法正确的是
A.a点条件下能生成Ag CrO 沉淀,也能生成AgCl沉淀
2 4B.b点时,c(Cl-)= c (CrO),Ksp(AgCl)=Ksp(Ag CrO)
2 4
C.Ag CrO+2Cl- 2AgCl+CrO的平衡常数K=107.9
2 4
D.向NaCl、NaCrO 均为0.1mol·L-1的混合溶液中滴加AgNO 溶液,先产生Ag CrO 沉淀
2 4 3 2 4
解析:
结合上述分析可知,A、B错误;C项,该反应的平衡常数
,正确;D项,该混合溶液中形成
AgCl 沉淀所需的 ,形成 Ag CrO 沉淀所需的
2 4
,形成AgCl所需的c(Ag+)较小,所以先产生
AgCl沉淀,错误。
答案:C
例3.(2021·江苏卷)室温下,用0.5mol·L-1NaCO 溶液浸泡CaSO 粉末,一段时间后过滤,向滤渣中加
2 3 4
稀醋酸,产生气泡。已知K (CaSO)=5×10-5,K (CaCO)=3×10-9。下列说法正确的是
sp 4 sp 3
A.0.5mol·L-1NaCO 溶液中存在:c(OH-)= c (H+)+c (HCO)+ c (H CO)
2 3 2 3
B.反应CaSO+CO CaCO +SO正向进行,需满足 > ×104
4 3
C.过滤后所得清液中一定存在:c (Ca2+)= 且c (Ca2+)≤
D.滤渣中加入醋酸发生反应的离子方程式:CaCO +2H+===Ca2++CO ↑+H O
3 2 2
解析:A项,0.5mol·L-1NaCO 溶液中存在质子守恒:c(OH-)=c (H+)+c (HCO )+2c (H CO),错误;B项,
2 3 2 3
该反应的平衡常数 K= = = = = ×104,当浓度商
<K时,反应正向进行,错误;C项,上层清液为碳酸钙的保护溶液,所以清液中满足c
(Ca2+)= ,由于硫酸钙沉淀转化为碳酸钙沉淀,所以清液为硫酸钙的不饱和溶液,则
c(Ca2+)≤ ,正确;D项,醋酸为弱酸,不能拆成离子形式,错误。
答案:C
例4.(高考卷组合)下列说法正确的是选项 实验 现象 结论
向2支盛有2mL相同浓度硝酸银溶液的
一支试管中产生黄色沉
A 试管中分别加入2滴相同浓度的NaCl和 K (AgI)K (Ag S)
入AgNO 与AgCl的浊液中 黑色沉淀 sp sp 2
3
解析:A项,根据题中描述可知黄色沉淀为AgI,另一支试管中无明显现象,说明没有AgCl析出,证明
K (AgI)K [Cu(OH) ]
混合溶液中逐滴加入氨水 淀 sp 2 sp 2
前者无现象,后
分别向相同浓度的ZnSO 溶液和
D 4 者有黑色沉淀 Ksp(CuS) > Ksp(ZnS)
CuSO 溶液中通入HS
4 2 生成
3.某兴趣小组进行下列实验:
①将0.1 mol·L-1 MgCl 溶液和0.5 mol·L-1 NaOH溶液等体积混合得到浊液
2
②取少量①中浊液,滴加0.1 mol·L-1 FeCl 溶液,出现红褐色沉淀
3
③将①中浊液过滤,取少量白色沉淀,滴加0.1 mol·L-1 FeCl 溶液,白色沉淀变为红褐色沉淀
3
④另取少量白色沉淀,滴加饱和NH Cl溶液,沉淀溶解
4
下列说法中不正确的是
A.将①中所得浊液过滤,所得滤液中含少量Mg2+
B.①中浊液中存在沉淀溶解平衡:Mg(OH) (s) Mg2+(aq)+2OH-(aq)
2
C.实验②和③均能说明Fe(OH) 比Mg(OH) 难溶
3 2
D.NH Cl溶液中的NH可能是④中沉淀溶解的原因
4
4.25 ℃时,K (AgCl)=1.56×10-10,K (Ag CrO)=9.0×10-12,下列说法正确的是
sp sp 2 4
A.在AgCl和Ag CrO 共存的悬浊液中,
2 4
B.向Ag CrO 悬浊液中加入NaCl浓溶液,Ag CrO 不可能转化为AgCl
2 4 2 4
C.向AgCl饱和溶液中加入NaCl晶体,有AgCl析出且溶液中c(Cl-)=c(Ag+)
D.向同浓度的NaCrO 和NaCl混合溶液中滴加AgNO 溶液,AgCl先析出
2 4 3
5.在一混合溶液中含有KCl、KBr、KCrO,其浓度均为0.01 mol·L-1,向溶液中逐滴加入0.01 mol·L-1
2 4
AgNO 溶液时,最先和最后沉淀的物质分别是(已知:AgCl、AgBr、Ag CrO 的K 分别为1.77×10-
3 2 4 sp
10、5.35×10-13、1.12×10-12)
A.AgBr、AgCl B.Ag CrO、AgCl C.AgBr、Ag CrO D.同时沉淀
2 4 2 4
6.自然界中原生铜的硫化物经氧化、淋滤后变成CuSO 溶液,遇到闪锌矿(ZnS)可慢慢转变为铜蓝
4
(CuS)。已知:K (ZnS)=2×10-22,K (CuS)=6×10-36。下列说法不正确的是
sp sp
A.基态Cu+转化基态Cu2+,失去3d轨道上的电子
B.1个ZnS晶胞(如图)中含4个S2-
C.反应ZnS(s)+Cu2+(aq) CuS(s)+Zn2+(aq)正向进行,
需满足
D.生成铜蓝后的溶液中一定存在:c= 且c<
拓展训练
7.为研究沉淀的生成及其转化,某小组进行如图实验。①中现象:产生红色沉淀,②中现象:溶液先浑
浊,后来澄清,③中现象:产生白色沉淀。关于该实验的分析不正确的是A.①浊液中存在平衡:Ag CrO(s) 2Ag+(aq)+CrO(aq)
2 4
B.②中溶液变澄清的原因:AgOH+2NH ·H O===[Ag(NH )]OH+2HO
3 2 3 2 2
C.③中颜色变化说明有AgCl生成
D.该实验可以证明AgCl比Ag CrO 更难溶
2 4
8.室温下,用饱和NaCO 溶液浸泡BaSO 粉末,一段时间后过滤,向滤渣中加入盐酸,产生气泡。已
2 3 4
知K (BaSO)=1.1×10-10,K (BaCO)=2.6×10-9。下列说法正确的是
sp 4 sp 3
A.NaCO 饱和溶液中存在:c(OH-)=c(H+)+c(HCO)+c(H CO)
2 3 2 3
B.反应BaSO(s)+CO(aq) BaCO (s)+SO(aq)正向进行,需满足
4 3
C.过滤后所得的滤液中一定存在:c(Ba2+)= ,且c(SO)>c(CO)
D.滤渣中加入盐酸发生反应的离子方程式:CO+2H+===CO ↑+HO
2 2
9.已知:K (FeS)=6×10-18,K (CuS)=1×10-36。室温下,向CuSO 溶液中加入FeS粉末,一段时间后过
sp sp 4
滤,向滤渣中加入足量稀硫酸,固体部分溶解。下列说法正确的是
A.室温下,CuS的溶解度大于FeS
B.反应FeS(s)+Cu2+(aq) CuS(s)+Fe2+(aq)正向进行,需满足 <6×1018
C.生成CuS后的溶液中一定存在:c(S2-)= ,且c(S2-)>
D.滤渣中加入稀硫酸发生反应的离子方程式为CuS+2H+===Cu2++HS↑
2
【随堂反馈】答案
1.B 2.C 3.C 4.D 5.C 6.D 7.D 8.B 9.B
【课后作业】
1.下列依据实验操作及现象所得出的结论正确的是
选项 实验操作 现象 结论
向浓度均为0.1mol·L-1 NaCl和NaI混
A 出现黄色沉淀 K (AgCl)<K (AgI)
合溶液中滴加少量AgNO 溶液 sp sp
3
向2mL0.01mol·L-1的AgNO 溶液中滴
3 先产生白色沉淀,后
B 加几滴同浓度的NaCl溶液后,滴加 证明 K (AgI)<K (AgCl)
出现黄色沉淀 sp sp
KI 溶液
向10 mL 0.2 mol·L-1 ZnSO 溶液中加
4 先产生白色沉淀,然 相同温度下,溶度积常数:
C 入10 mL 0.4 mol·L-1 Na S溶液,再滴
2 后沉淀变黑 K (CuS)<K (ZnS)
加CuSO 溶液 sp sp
4
向盛有2mLNa S的溶液加入过量
2 白色沉淀逐渐变为黑
D ZnSO 溶液,再逐滴加入同浓度的 K (CuS)105,PbSO 可以比较彻底的转化为PbCO
4 3
(2)反应BaSO(s)+CO(aq)= BaCO (s)+SO(aq)的平衡常数K==0.04<<105,反应正向进行的程度有
4 3
限
(3)Fe2+ Pb+H O+2HAc===Pb(Ac) +2H O 作还原剂
2 2 2 2
(4)Fe(OH) 、Al(OH)
3 3
(5)Ba2+、Na+