文档内容
课时检测(三十) 常见无机物的转化
1.下列选项所示的物质间转化均能实现的是( )
A.NaCl(aq)――→Cl (g)――→漂白粉(s)
2
B.NaCl(aq)――→NaHCO (s)――→Na CO (s)
3 2 3
C.NaBr(aq)――→Br (aq)――→I(aq)
2 2
D.Mg(OH) (s)――→MgCl (aq)――→Mg(s)
2 2
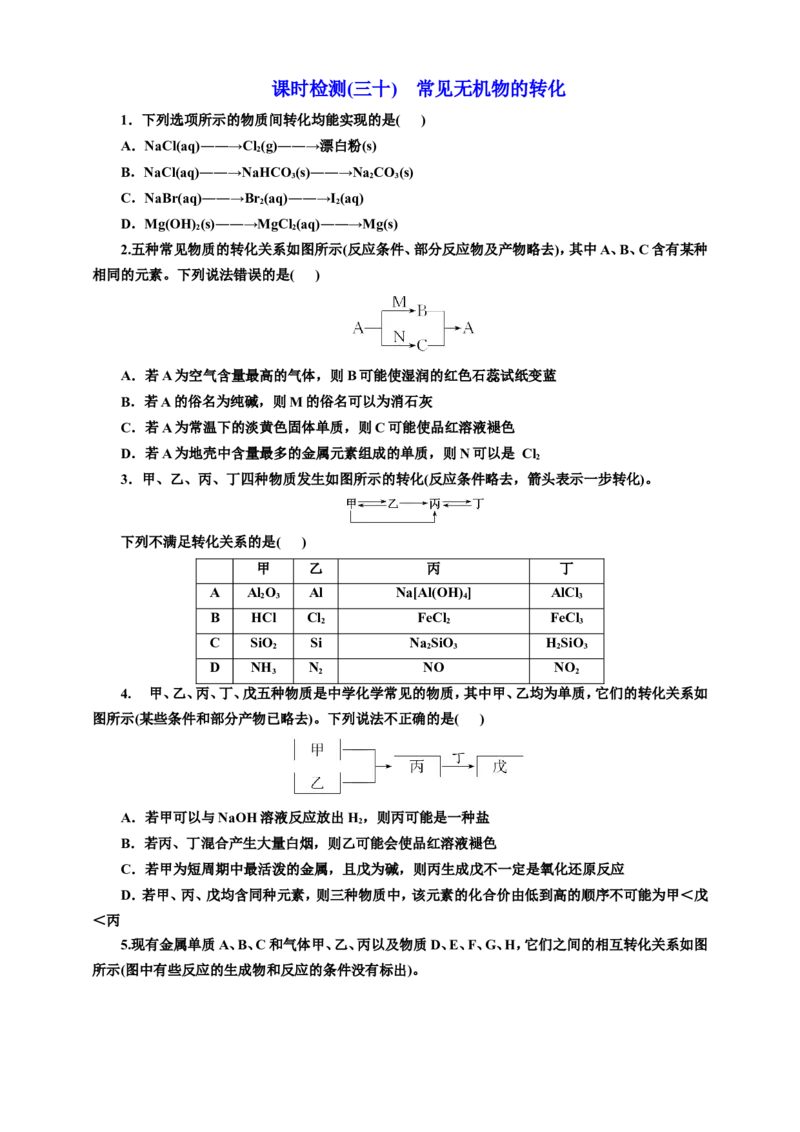
2.五种常见物质的转化关系如图所示(反应条件、部分反应物及产物略去),其中A、B、C含有某种
相同的元素。下列说法错误的是( )
A.若A为空气含量最高的气体,则B可能使湿润的红色石蕊试纸变蓝
B.若A的俗名为纯碱,则M的俗名可以为消石灰
C.若A为常温下的淡黄色固体单质,则C可能使品红溶液褪色
D.若A为地壳中含量最多的金属元素组成的单质,则N可以是 Cl
2
3.甲、乙、丙、丁四种物质发生如图所示的转化(反应条件略去,箭头表示一步转化)。
下列不满足转化关系的是( )
甲 乙 丙 丁
A Al O Al Na[Al(OH) ] AlCl
2 3 4 3
B HCl Cl FeCl FeCl
2 2 3
C SiO Si Na SiO HSiO
2 2 3 2 3
D NH N NO NO
3 2 2
4. 甲、乙、丙、丁、戊五种物质是中学化学常见的物质,其中甲、乙均为单质,它们的转化关系如
图所示(某些条件和部分产物已略去)。下列说法不正确的是( )
A.若甲可以与NaOH溶液反应放出H,则丙可能是一种盐
2
B.若丙、丁混合产生大量白烟,则乙可能会使品红溶液褪色
C.若甲为短周期中最活泼的金属,且戊为碱,则丙生成戊不一定是氧化还原反应
D.若甲、丙、戊均含同种元素,则三种物质中,该元素的化合价由低到高的顺序不可能为甲<戊
<丙
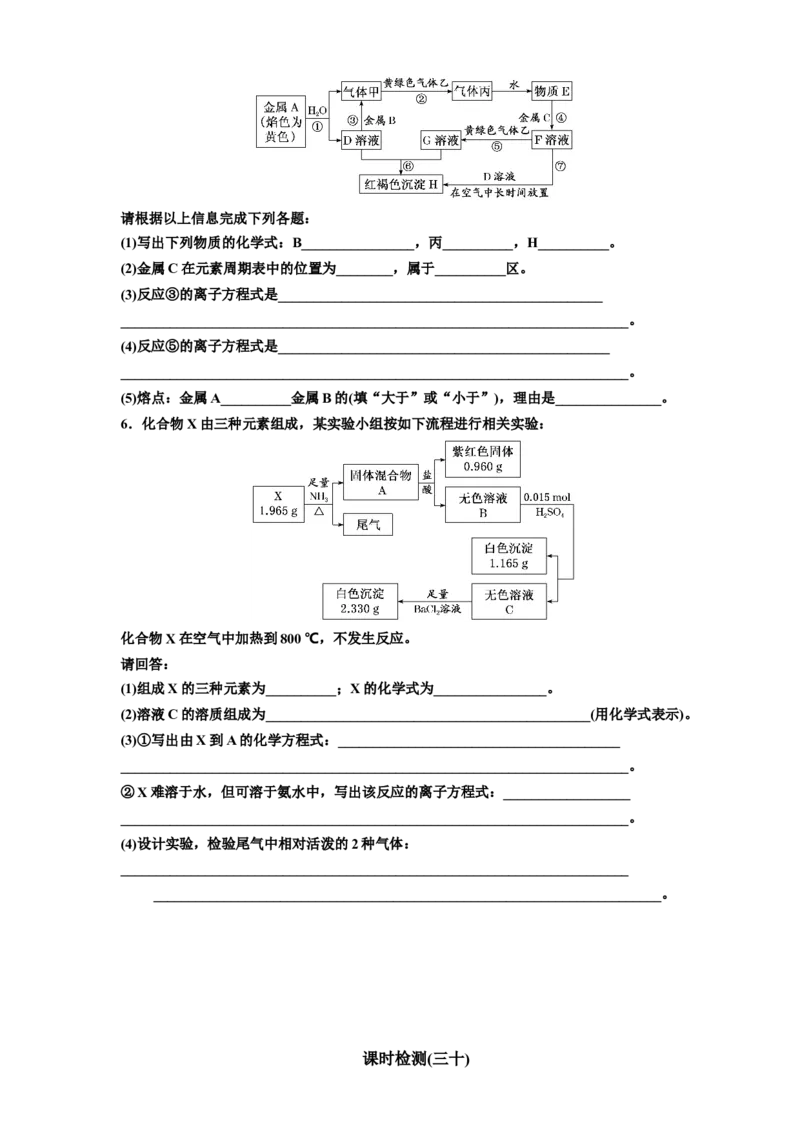
5.现有金属单质A、B、C和气体甲、乙、丙以及物质D、E、F、G、H,它们之间的相互转化关系如图
所示(图中有些反应的生成物和反应的条件没有标出)。请根据以上信息完成下列各题:
(1)写出下列物质的化学式:B________________,丙__________,H__________。
(2)金属C在元素周期表中的位置为________,属于__________区。
(3)反应③的离子方程式是______________________________________________
________________________________________________________________________。
(4)反应⑤的离子方程式是_______________________________________________
________________________________________________________________________。
(5)熔点:金属A__________金属B的(填“大于”或“小于”),理由是_______________。
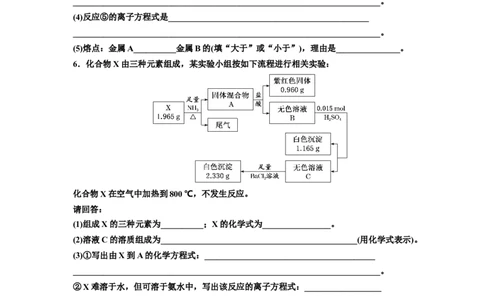
6.化合物X由三种元素组成,某实验小组按如下流程进行相关实验:
化合物X在空气中加热到800 ℃,不发生反应。
请回答:
(1)组成X的三种元素为__________;X的化学式为________________。
(2)溶液C的溶质组成为______________________________________________(用化学式表示)。
(3)①写出由X到A的化学方程式:________________________________________
________________________________________________________________________。
②X难溶于水,但可溶于氨水中,写出该反应的离子方程式:__________________
________________________________________________________________________。
(4)设计实验,检验尾气中相对活泼的2种气体:
________________________________________________________________________
________________________________________________________________________。
课时检测(三十)1.C 石灰水中Ca(OH) 浓度太小,一般用氯气和石灰乳反应制取漂白粉,故A错误;碳酸的酸
2
性弱于盐酸,所以二氧化碳与氯化钠溶液不反应,故B错误;氧化性:Cl >Br >I ,所以氯气可以氧化
2 2 2
NaBr得到溴单质,溴单质可以氧化碘化钠得到碘单质,故C正确;电解氯化镁溶液无法得到镁单质,
阳极氯离子放电生成氯气,阴极水电离出的氢离子放电产生氢气,同时产生大量氢氧根离子,与镁离
子产生沉淀,故D错误。
2.D 若A为N,M为H,N为O,则B、C分别为NH 、NO,NH 和NO在一定条件下反应可生
2 2 2 3 3
成N,A正确;若A为Na CO ,M为Ca(OH) ,N为CO ,则B、C分别为NaOH、NaHCO ,NaOH和
2 2 3 2 2 3
NaHCO 反应生成Na CO 和HO,B正确;若A为S,M为H,N为O,则B、C分别为HS、SO ,HS
3 2 3 2 2 2 2 2 2
和SO 反应生成S和HO,C正确;若A为Al,则B、C中Al元素均为正价,B与C不可能反应生成
2 2
Al,D错误。
3.B 电解熔融状态下的 Al O 可以制得Al,Al与O 在常温或加热的条件下反应可以生成
2 3 2
Al O,Al O、Al可相互转化,Al O、Al均能与NaOH反应生成Na[Al(OH) ],Na[Al(OH) ]与过量的盐
2 3 2 3 2 3 4 4
酸反应生成AlCl ,AlCl 与过量的NaOH反应生成Na[Al(OH) ],Na[Al(OH) ]和AlCl 可相互转化,A
3 3 4 4 3
满足转化关系;浓盐酸与二氧化锰在加热条件下可以制得Cl ,Cl 与水反应生成HCl,HCl和Cl 可相
2 2 2
互转化,HCl与Fe反应生成FeCl,Cl 与Fe反应直接生成最高价态的FeCl,则乙→丙无法一步转化,
2 2 3
FeCl 与Cl 反应生成FeCl,FeCl 与Fe反应生成FeCl,FeCl 和FeCl 可相互转化,B不满足转化关
2 2 3 3 2 2 3
系;SiO 与C反应生成Si,Si与O 反应生成SiO ,Si、SiO 可相互转化,Si、SiO 均能与NaOH反应生
2 2 2 2 2
成Na SiO ,Na SiO 与强酸反应生成HSiO ,HSiO 与NaOH反应生成Na SiO ,Na SiO 、HSiO 可
2 3 2 3 2 3 2 3 2 3 2 3 2 3
相互转化,C满足转化关系;NH 与O 在催化氧化的条件下可生成N,N 与H 在高温、高压和催化剂
3 2 2 2 2
的条件下可反应生成NH ,NH 、N 可相互转化,NH 、N 均能与O 反应生成NO,NO与O 反应生成
3 3 2 3 2 2 2
NO ,NO 与水反应生成NO,NO和NO 可相互转化,D满足转化关系。
2 2 2
4.D 甲为单质,若甲可以与NaOH溶液反应放出H,则甲为Al或Si,所以丙可能是一种盐,例
2
如氯化铝等,故A正确;丙、丁混合产生白烟,则丙、丁可为HCl和NH 或HNO 和NH 等,甲、乙均为
3 3 3
单质,则乙可能是氯气、氢气或氮气,如果是氯气,则会使品红溶液褪色,故B正确;若甲为短周期中最
活泼的金属,且戊为碱,则甲为Na,乙为氧气,所以丙可以为氧化钠或过氧化钠,当丙为氧化钠时,丙
生成戊(Na O+HO===2NaOH)不是氧化还原反应,故C正确;若甲、丙、戊含有同一种元素,例如当
2 2
甲为铁、乙为氯气、丙为氯化铁、丁为硫化氢等具有还原性的物质、戊为氯化亚铁时,则含Fe元素的物
质中Fe的化合价由低到高的顺序为甲<戊<丙,故D错误。
5.解析:金属单质A、B、C和气体甲、乙、丙以及物质D、E、F、G、H,它们之间的相互转化关系如
题图;A焰色试验为黄色,为钠;钠和水生成氢氧化钠和氢气,甲为氢气、D为氢氧化钠;氢氧化钠和铝
生成氢气,B为铝;氢气和黄绿色气体氯气生成氯化氢,则乙为氯气、丙为氯化氢;氯化氢溶于水得到
盐酸,E为盐酸;氢氧化钠和氯化铁生成红褐色沉淀氢氧化铁,氯气和氯化亚铁生成氯化铁,铁和盐酸
生成氯化亚铁,则C为铁、F为氯化亚铁、G为氯化铁、H为氢氧化铁;氯化亚铁和氢氧化钠生成氢氧
化亚铁,氢氧化亚铁在空气中被氧气氧化为氢氧化铁;(1)由分析可知,B:Al,丙:HCl,H:Fe(OH) 。(2)
3
金属C为铁,为26号元素,在元素周期表中的位置为第四周期第Ⅷ族,属于d区;(3)反应③为铝和氢
氧化钠生成氢气和偏铝酸钠,离子方程式是2Al+2OH-+6HO===2[Al(OH) ]+3H↑;(4)反应⑤为氯
2 4 2
气和氯化亚铁生成氯化铁,离子方程式是2Fe2++Cl ===2Fe3++2Cl-;(5)熔点:金属A小于金属B,理
2
由是铝原子半径小于钠原子且价电子数大于钠,故金属键键能更大,熔点更高。
答案:(1)Al HCl Fe(OH) (2)第四周期第Ⅷ族 d
3(3)2Al+2OH-+6HO===2[Al(OH) ]+3H↑
2 4 2
(4)2Fe2++Cl ===2Fe+2Cl- (5)小于 铝原子半径小于钠原子且价电子数大于钠,故金属键键
2
能更大
6.解析:化合物X由三种元素组成,在加热条件下和足量氨气反应生成固体混合物A,A和盐酸
反应生成的紫红色固体应该是Cu,无色溶液B中加入稀硫酸生成的白色沉淀应该是BaSO ,无色溶
4
液C中加入足量BaCl 溶液生成的白色沉淀应该是BaSO 。(1)根据以上分析可知Cu的物质的量是=
2 4
0.015 mol,第一次生成硫酸钡的物质的量是=0.005 mol,第二次生成硫酸钡的物质的量是=0.01 mol,
因此1.965 g X中一定含有0.960 g Cu、0.005 mol×137 g·mol-1=0.685 g Ba,二者质量之和是1.645 g<
1.965 g,相差0.32 g,根据原子守恒可知应该是氧元素,物质的量是=0.02 mol,所以组成X的三种元
素为Ba、Cu、O,Ba、Cu、O三种原子的个数之比是1∶3∶4,X的化学式为BaCu O。(2)根据氯原子
3 4
守恒以及溶液C仍然能与氯化钡反应生成硫酸钡可知溶液C的溶质组成为HCl、HSO 。(3)①反应中
2 4
Cu元素化合价降低被还原,则氨气中氮元素化合价升高,被氧化生成氮气,根据原子守恒可知由X到
A的化学方程式为2NH +BaCu O=====Ba(OH) +3Cu+N+2HO。②X难溶于水,但可溶于氨水
3 3 4 2 2 2
中,说明有[Cu(NH )]2+生成,所以该反应的离子方程式为BaCu O+12NH ·HO===3[Cu(NH )]2++
3 4 3 4 3 2 3 4
Ba2++8OH-+8HO。(4)反应中氨气可能过量,高温下水是气态,氮气性质稳定,所以需要检验的是氨
2
气和水蒸气。实验方案为将湿润的红色石蕊试纸置于尾气出口处,若变蓝,说明尾气中有NH ;将尾气
3
通入冷的集气瓶中,若有液珠,说明有HO。
2
答案:(1)Ba、Cu、O BaCu O (2)HCl、HSO
3 4 2 4
(3)①2NH +BaCu O=====Ba(OH) +3Cu+N+2HO
3 3 4 2 2 2
②BaCu O+12NH ·HO===3[Cu(NH )]2++Ba2++8OH-+8HO
3 4 3 2 3 4 2
(4)将湿润的红色石蕊试纸置于尾气出口处,若变蓝,说明尾气中有NH ;将尾气通入冷的集气瓶
3
中,若有液珠,说明有HO
2