文档内容
氯&卤素作业题
作业题目难度分为 3 档:三星☆☆☆(基础题目)
四星☆☆☆☆(中等题目)
五星☆☆☆☆☆(较难题目)
本套作业题目 1-9,17 题为三星,10-11,13,15-16,18-20 为四星,12,14,21 为五
星。
1.生活中可以用氯气灌洞的方法来消灭田鼠,这是利用了氯气的哪些性质:
①密度比空气大 ②易液化 ③能溶于水 ④有毒( ) ☆☆☆
A.①② B.③④ C.①③④ D.①④
【解答】
氯气可以用来消灭田鼠利用了它的毒性,使田鼠中毒死亡;将氯气通过软管灌入
田鼠洞中,氯气的相对分子质量比空气的大,所以密度比空气的大,与空气混合
时,在混合气体的下部,所以能够被田鼠呼吸,从而达到灭鼠目的。
故选 D.
2.当不慎有大量 Cl 逸到周围空气里时,可用浸有一定浓度的下列物质溶液的
2
毛巾捂住鼻子,该物质是( ) ☆☆☆
A.NaOH B.NaCl C.NH•HO D.NaHCO
3 2
3
【解答】
A.NaOH 虽能与氯气反应,达到吸收氯气的效果,但浓 NaOH 的腐蚀性强,不能
用浸有浓 NaOH 溶液的毛巾捂住鼻子,故 A 错误;
B.NaCl 不与氯气反应,且 NaCl 溶液抑制氯气的溶解,则不能用浸有 NaCl 溶液
的毛巾捂住鼻子来防止吸入氯气中毒,故 B 错误;
C.氨气本身具有刺激性,对人体有害,不能用氨水吸水氯气,故 C 错误;
第 1页(共 14页)D.NaHCO 溶液显碱性,碱性较弱,能与氯气反应而防止吸入氯气中毒,则可以
3
用浸有 NaHCO 溶液的毛巾捂住鼻子,故 D 正确;
3
故选 D.
3.据美国有线电视网的消息,2011 年 7 月 13 日,巴格达东部的萨德尔城一家
污水处理厂发生氯气泄露事故,导致五百多人中毒.救援人员在现场的下列处理
方法和过程较合理的是:( ) ☆☆☆
①及时将人群顺风转移到地势较高的地方;
②用高压水枪向空中喷洒含碱性物质的水溶液;
③被转移人群可戴上用稀 NaCO 溶液处理过的口罩;
2 3
④被转移人群应戴上用浓 NaOH 溶液处理过的口罩;
⑤及时清理现场,检查水源和食物等是否被污染.
A.②③⑤ B.①②③ C.②④⑤ D.①②③⑤
【解答】
①氯气密度比空气大,有毒,氯气会聚结在地势较低的地方,人群在地势较低的
地方,会中毒,应向较高的地势转移,顺风转移容易吸入过多的氯气中毒,故①
不合理;
②氯气能溶于水,易被碱溶液吸收(它会和碱反应生成盐和水),用高压水枪向
空中喷洒含弱碱性物质的水溶,能吸收氯气,防止空气污染,故②合理;
③氯气能溶于水,易被碱性溶液吸收(它会和碱反应生成盐和水),碳酸钠溶液
呈碱性,可以吸收氯气,故③合理;
④氯气能溶于水,易被碱溶液吸收(它会和碱反应生成盐和水),用浓 NaOH 溶液
处理过的口罩能吸收氯气,防止空气污染,但氢氧化钠溶液是强碱具有腐蚀性,
故④不合理;
⑤;氯气是有毒气体危害人的身体和环境,及时清理现场,检查水源和食物等是
否被污染,故⑤合理;
所以正确的做法②③⑤
故选 A.
第 2页(共 14页)4.下列有关于 Cl 的说法中,不正确的是( ) ☆☆☆
2
A.Cl 是一种黄绿色、密度比空气大的有毒气体
2
B.红热的铁丝在 Cl 中剧烈燃烧,产生白色烟雾
2
C.工业上用 Cl 和石灰乳为原料制造漂白粉
2
D.Cl 能与水反应生成盐酸和次氯酸
2
【解答】
A.Cl 是一种黄绿色、密度比空气大的有毒气体,故 A 正确;
2
B.氯气与铁反应生成氯化铁,反应产生棕褐色的烟,故 B 错误;
C.氯气与氢氧化钙反应生成氯化钙、次氯酸钙和水,工业上用 Cl 和石灰乳为
2
原料制造漂白粉,故 C 正确;
D.Cl 能与水反应生成盐酸和次氯酸,Cl+HO═HCl+HClO,故 D 正确;
2 2 2
故选:B.
5.下列说法不正确的是( ) ☆☆☆
A.Cl 能使湿润的有色布条褪色,所以 Cl 具有漂白性
2 2
B.红热的铁丝在 Cl 中剧烈燃烧,反应生成 FeCl
2
3
C.利用溴单质的氧化性可以把碘离子转化为碘单质
D.实验室常用 NaOH 溶液吸收多余的 Cl 以避免污染
2
【解答】
A.氯气和水反应生成盐酸和次氯酸,次氯酸具有漂白作用,氯气无漂白作用,
故 A 错误;
B.氯气具有强氧化性氧化变价金属为高价态化合物,红热的铁丝在 Cl 中剧烈
2
燃烧,反应生成 FeCl,故 B 正确;
3
C.溴单质氧化性大于碘单质,溴单质氧化碘离子生成碘单质,故 C 正确;
D.氯气有毒不能排放到空气中,需要用氢氧化钠溶液吸收,故 D 正确;
故选 A.
第 3页(共 14页)6.下列有关氯水的表述不正确的是( ) ☆☆☆
A.向氯水中加入碳酸钙粉末,能提高溶液中 HClO 的浓度
B.氯水中含有 7 种微粒,其可以与 AgNO、FeBr 等多种物质反应
3 2
C.蓝色石蕊试纸放入氯水中先变红后褪色
D.氯水可以导电,说明氯气是电解质
【解答】
A.氯水中含有盐酸,盐酸和碳酸钙反应生成二氧化碳,碳酸的酸性大于次氯酸,
抑制次氯酸电离,所以能提高 HClO 的浓度,故 A 正确;
B.氯水中含有氯离子、氢离子、次氯酸根离子、氢氧根离子,含有水分子、氯
气分子、次氯酸分子,氯离子和硝酸银反应生成氯化银白色沉淀,氯气和氯化亚
铁发生氧化还原反应生成氯化铁,故 B 正确;
C.氯水中含有氢离子溶液显酸性,蓝色石蕊试纸遇酸变红色,氯水中含有次氯
酸,次氯酸具有漂白性,所以变红的试纸有变成无色,故 C 正确;
D.电解质必须是化合物,氯水是混合物,不属于电解质,故 D 错误;
故选:D.
7.在氯水中存在多种分子和离子,它们在不同的反应中表现各自的性质.下列
实验现象和结论一致且正确的是( ) ☆☆☆
A.加入有色布条,一会儿有色布条褪色,说明溶液中有 Cl 存在
2
B.溶液呈黄绿色,且有刺激性气味,说明有 Cl 分子存在
2
C.先加入盐酸酸化,再加入 AgNO 溶液产生白色沉淀,说明有 Cl﹣存在
3
D.加入 NaOH 溶液,氯水黄绿色消失,说明有 HClO 分子存在
【解答】
A、次氯酸有强氧化性能使有色布条褪色,向氯水中加入有色布条,一会儿有色
布条褪色,说明溶液中有 HClO 存在,故 A 错误.
第 4页(共 14页)B、氯气是黄绿色气体,且有刺激性气味,如果氯水溶液呈黄绿色,且有刺激性
气味,说明有 Cl 分子存在,故 B 正确.
2
C、盐酸中含有氯离子,向氯水中加入盐酸后再加入硝酸银溶液生成氯化银白色
沉淀,不能说明氯水中含有氯离子,故 C 错误.
D、Cl+HO HCl+HClO,该反应是可逆反应,向氯水中加入氢氧化钠溶液,氯水
2 2
黄绿色消失,说明氯水溶液呈酸性,不能证明含有次氯酸,故 D 错误.
⇌
故选 B.
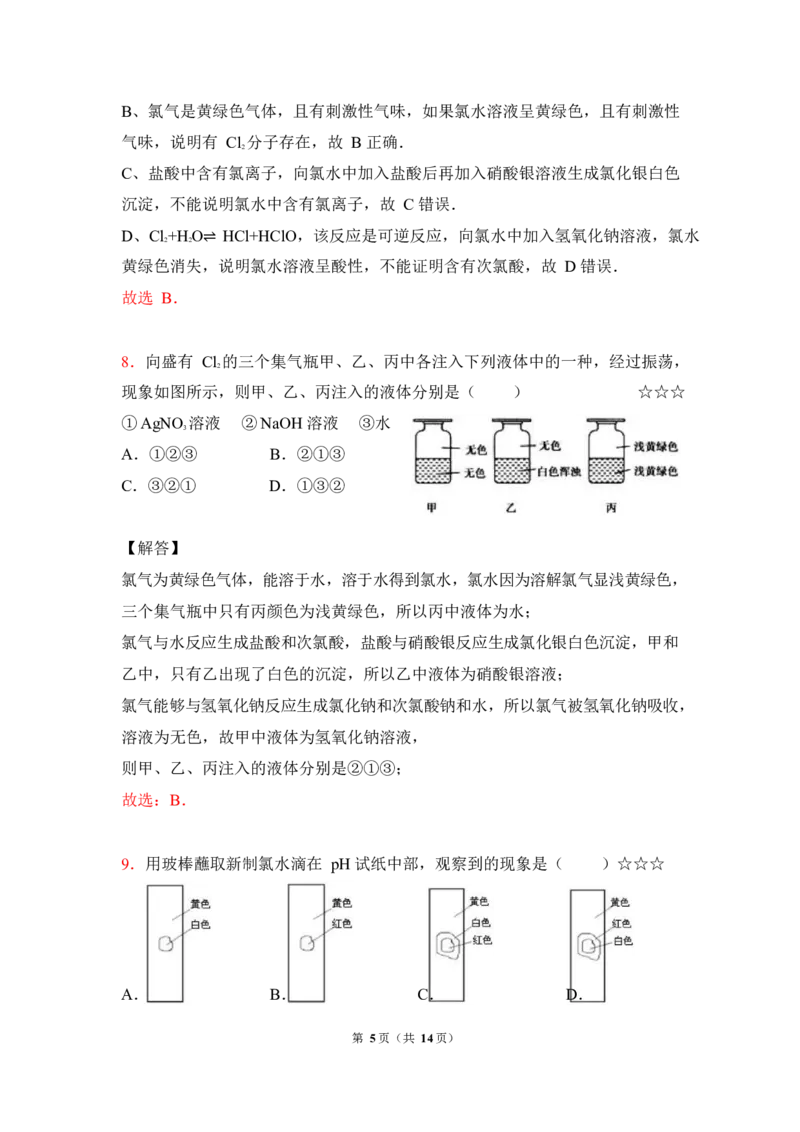
8.向盛有 Cl 的三个集气瓶甲、乙、丙中各注入下列液体中的一种,经过振荡,
2
现象如图所示,则甲、乙、丙注入的液体分别是( ) ☆☆☆
①AgNO 溶液 ②NaOH 溶液 ③水
3
A.①②③ B.②①③
C.③②① D.①③②
【解答】
氯气为黄绿色气体,能溶于水,溶于水得到氯水,氯水因为溶解氯气显浅黄绿色,
三个集气瓶中只有丙颜色为浅黄绿色,所以丙中液体为水;
氯气与水反应生成盐酸和次氯酸,盐酸与硝酸银反应生成氯化银白色沉淀,甲和
乙中,只有乙出现了白色的沉淀,所以乙中液体为硝酸银溶液;
氯气能够与氢氧化钠反应生成氯化钠和次氯酸钠和水,所以氯气被氢氧化钠吸收,
溶液为无色,故甲中液体为氢氧化钠溶液,
则甲、乙、丙注入的液体分别是②①③;
故选:B.
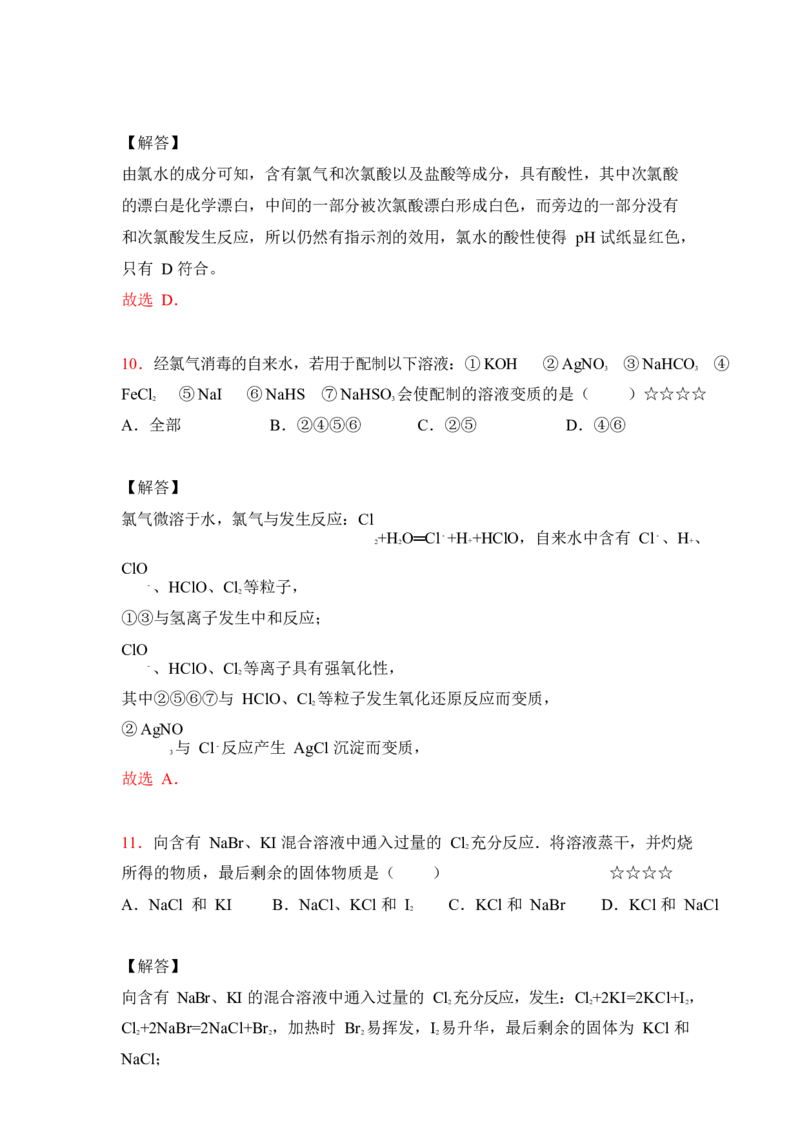
9.用玻棒蘸取新制氯水滴在 pH 试纸中部,观察到的现象是( )☆☆☆
A. B. C. D.
第 5页(共 14页)【解答】
由氯水的成分可知,含有氯气和次氯酸以及盐酸等成分,具有酸性,其中次氯酸
的漂白是化学漂白,中间的一部分被次氯酸漂白形成白色,而旁边的一部分没有
和次氯酸发生反应,所以仍然有指示剂的效用,氯水的酸性使得 pH 试纸显红色,
只有 D 符合。
故选 D.
10.经氯气消毒的自来水,若用于配制以下溶液:①KOH ②AgNO ③NaHCO ④
3 3
FeCl ⑤NaI ⑥NaHS ⑦NaHSO 会使配制的溶液变质的是( )☆☆☆☆
2 3
A.全部 B.②④⑤⑥ C.②⑤ D.④⑥
【解答】
氯气微溶于水,氯气与发生反应:Cl
2
+H
2
O═Cl﹣+H
+
+HClO,自来水中含有 Cl﹣、H
+
、
ClO
﹣、HClO、Cl 等粒子,
2
①③与氢离子发生中和反应;
ClO
﹣、HClO、Cl 等离子具有强氧化性,
2
其中②⑤⑥⑦与 HClO、Cl 等粒子发生氧化还原反应而变质,
2
②AgNO
与 Cl﹣反应产生 AgCl 沉淀而变质,
3
故选 A.
11.向含有 NaBr、KI 混合溶液中通入过量的 Cl 充分反应.将溶液蒸干,并灼烧
2
所得的物质,最后剩余的固体物质是( ) ☆☆☆☆
A.NaCl 和 KI B.NaCl、KCl 和 I C.KCl 和 NaBr D.KCl 和 NaCl
2
【解答】
向含有 NaBr、KI 的混合溶液中通入过量的 Cl 充分反应,发生:Cl+2KI=2KCl+I,
2 2 2
Cl+2NaBr=2NaCl+Br,加热时 Br 易挥发,I 易升华,最后剩余的固体为 KCl 和
2 2 2 2
NaCl;第 6页(共 14页)故选 D.
12.标准状况下有 22.4L 氯气和氢气的混合气体,在一密闭容器中使其充分反
应.冷却后将此气体与 1L 1mol/L NaOH 溶液充分反应,最后此溶液( )
☆☆☆☆☆
A.一定显酸性 B.一定显碱性
C.可能显酸性,可能显碱性,也可能中性 D.以上无正确答案
【解答】
混合气体的物质的量为 n= ,
当 n(Cl)=n(H)=0.5mol 时,
2 2
Cl+H 2HCl, HCl+NaOH=NaCl+HO
2 2 2
1 2 1 1
0.5mol 1mol 1mol 1mol
当氯化氢和氢氧化钠恰好反应时,溶液显中性;
当 n(Cl)>n(H)=0 时,气体全部为氯气,所以和氢氧化钠发生的反应为:
2 2
Cl+2NaOH=NaCl+NaClO+HO
2 2
1 2
0.5mol 1mol
与氢氧化钠反应的氯气为 0.5mol,剩余的 0.5mol 氯气和水反应,
Cl+HO=HCl+HClO
2 2
所以反应后的溶液呈酸性;
当 n(H)>n(Cl)=0 时,气体全部为氢气,氢气和氢氧化钠溶液不反应,所
2 2
以溶液呈碱性.
故选 C.
13.下列与 Cl 有关的说法正确的是( ) ☆☆☆☆
2
A.0.1 mol Cl 与足量 NaOH 溶液反应,转移 0.2 mol 电子
2
第 7页(共 14页)B.1 mol Fe 与 1 mol Cl 反应转移 3 mol 电子
2
C.含有 4 mol HCl 的浓盐酸与足量 MnO 反应,生成 1 mol Cl
2
2
D.Cl 通入 FeCl 溶液中,然后加 KSCN 溶液,溶液变红
2 2
【解答】
A.Cl+2NaOH=NaCl+NaClO+HO,该反应中 Cl 元素化合价由 0 价变为+1 价、﹣1
2 2
价,1mol 氯气参加反应转移电子 1mol,则 0.1mol Cl 与足量 NaOH 溶液反应,
2
转移 0.1mol 电子,故 A 错误;
B.2Fe+3Cl 2FeCl,根据方程式知,1molFe 完全反应需要氯气 1.5mol,
2 3
实际上有 1mol 氯气,则铁有剩余,1mol 氯气生成氯离子转移 2mol 电子,故 B
错误;
C.稀盐酸和二氧化锰不反应,所以含有 4mol HCl 的浓盐酸与足量 MnO 反应,
2
生成 Cl 的物质的量小于 1mol,故 C 错误;
2
D.氯气具有强氧化性,将亚铁氧化成铁离子,所以加入 KSCN 溶液,溶液变红,
故 D 正确;
故选 D.
14.下列各组物质混合后,再加热蒸干并在 300℃时充分灼烧至质量不变,最终
可能得到纯净物的是( ) ☆☆☆☆☆
A.向 FeSO 溶液中通入 Cl B.向 KI 和 NaBr 混合溶液中通入 Cl
4 2
2
C.向 NaAlO 溶液中加入 HCl 溶液 D.向 NaHCO 溶液中加入 NaO 粉末
2 3 2 2
【解答】
A.FeSO 溶液和过量 Cl 反应生成 Fe(SO) 和 FeCl,Fe(SO) 加热水解生成
4 2 2 4 3 3 2 4 3
氢氧化铁和硫酸,硫酸难挥发,再加热蒸干并在 300℃时充分灼烧至质量不变得
到硫酸铁;FeCl 加热水解生成氢氧化铁和氯化氢,灼烧后氢氧化铁分解产生氧
3
化铁和水,所以得到的是 Fe(SO) 和 FeO 混合物,故 A 错误;
2 4 3 2 3
第 8页(共 14页)B.因 KI 、NaBr 在高温下不会分解,氯气会把碘和溴氧化出来,加热蒸干、灼
烧至质量不变,碘升华,溴和水挥发,加热蒸干、灼烧,残留固体为 KCl、NaCl
混合物,故 B 错误;
C.向 NaAlO 溶液中加入适量 HCl 溶液反应生成氢氧化铝和氯化钠,过量时生成
2
氯化钠和氯化铝溶液,加热蒸发得到氢氧化铝和氯化钠混合物,加热蒸干、灼烧,
残留固体为氧化铝和氯化钠,故 C 错误;
D.1mol 过氧化钠与水反应生成 2mol 氢氧化钠,2mol 氢氧化钠与 2mol 碳酸氢钠
按恰好反应生成碳酸钠,加热蒸干、灼烧,残留固体为碳酸钠,故 D 正确;
故选 D.
15.实验室用下列两种方法制氯气:①用含 HCl 146g 的浓盐酸与足量的 MnO 反
2
应;②用 87g MnO 与足量浓盐酸反应.所得的氯气( ) ☆☆☆☆
2
A.①比②多 B.②比①多 C.一样多 D.无法比较
【解答】
反应化学方程式为 MnO+4HCl MnCl+Cl↑+2HO;
2 2 2 2
理论计算:①含 HCl 146g 的浓盐酸与足量的 MnO 反应,4HCl~Cl,可得氯气
2 2
1mol,但随盐酸浓度变稀,溶质 HCl 不可能全部反应,故实际生成氯气应小于
1mol;
②用 87g MnO 与足量浓盐酸反应,因为浓盐酸足量,可以使 87g MnO 全部反应,
2 2
故生成氯气为 1mol;所以②>①;
故选 B.
16.实验室制 Cl 的反应为 4HCl(浓)+MnO MnCl+Cl↑+2HO.下列说法
2 2 2 2 2
错误的是( ) ☆☆☆☆
A.还原剂是 HCl,氧化剂是 MnO
2
B.每生成 1mol Cl,转移电子的物质的量为 2 mol
2
C.每消耗 1mol MnO,起还原剂作用的 HCl 消耗 4mol
2
D.生成的 Cl 中,除含有一些水蒸气外,还含有 HCl 杂质
2
第 9页(共 14页)【解答】
A.反应中 Cl 元素的化合价升高,HCl 被氧化,为还原剂,Mn 元素的化合价降低,
为氧化剂,故 A 正确;
B.根据化合价的变化可知,反应中 Cl 元素的化合价由﹣1 价升高到 0 价,每生
成 1mol Cl,转移电子的物质的量为 2mol,故 B 正确;
2
C.每消耗 1mol MnO,起还原剂作用的 HCl 消耗 2mol,另一部分的 HCl 起到酸
2
性的作用,故 C 错误;
D.由于盐酸易挥发,且反应在加热条件下进行,则生成的 Cl 中,除含有一些
2
水蒸气外,还含有 HCl 杂质,故 D 正确.
故选 C.
17.在同温同压下将 SO 和 Cl 按 1:1 体积比混合后,通入 BaCl 和品红的混合
2 2 2
溶液中,下列说法正确的是( ) ☆☆☆
A.溶液褪色,无沉淀生成 B.溶液不褪色,无沉淀生成
C.溶液褪色,有沉淀生成 D.溶液不褪色,有沉淀生成
【解答】
SO 和 Cl 按 1:1 体积比混合后,通入 BaCl 和品红的混合溶液中发生反应:
2 2 2
SO+Cl+2HO=HSO+2HCl;故溶液不褪色,有白色沉淀产生;
2 2 2 2 4
故选 D.
18.下列物质,能使干燥的蓝色石蕊试纸先变红又褪色的是( ) ☆☆☆☆
①氯气 ②液氯 ③新制氯水 ④敞口放置的久置氯水
⑤盐酸 ⑥用盐酸酸化的漂白粉溶液.
A.②③ B.①②③④ C.③⑥ D.③④⑥
【解答】
①氯气不能使干燥的石蕊试纸褪色,故①错误;
第 10页(共 14页)②液氯不能使干燥的石蕊试纸褪色,故②错误;
③新制氯水中含有 HCl 和 HClO,能使干燥的蓝色石蕊试纸先变红后褪色,故③
正确;
④敞口放置的久置氯水是盐酸,盐酸具有酸性能使蓝色石蕊试纸变红,但盐酸没
有漂白性,所以不能使试纸褪色,故④错误;
⑤盐酸具有酸性能使蓝色石蕊试纸变红,但盐酸没有漂白性,所以不能使试纸褪
色,故⑤错误;
⑥用盐酸酸化的漂白粉溶液中含有 HCl 和 HClO,能使干燥的蓝色石蕊试纸先变
红后褪色,故⑥正确;
故选 C.
19.氯气是一种重要的工业原料,工业上利用反应 3Cl+2NH═N+6HCl 检查氯气
2 3 2
管道是否漏气.下列说法错误的是( ) ☆☆☆☆
A.该反应中 NH 被还原 B.该反应利用了 Cl 的强氧化性
3 2
C.若管道漏气遇氨就会产生白烟 D.生成 1mol N 有 6mol 电子转移
2
【解答】
A.N 元素化合价由﹣3 价升高到 0 价,被氧化,故 A 错误;
B.Cl 元素化合价降低,被还原,Cl 为氧化剂,故 B 正确;
2
C.反应生成 HCl,NH 可与 HCl 反应生成氯化铵,有白烟生成,故 C 正确;
3
D.N 元素化合价由﹣3 价升高到 0 价,则生成 1molN 时有 6mol 电子转移,故 D
2
正确.
故选 A.
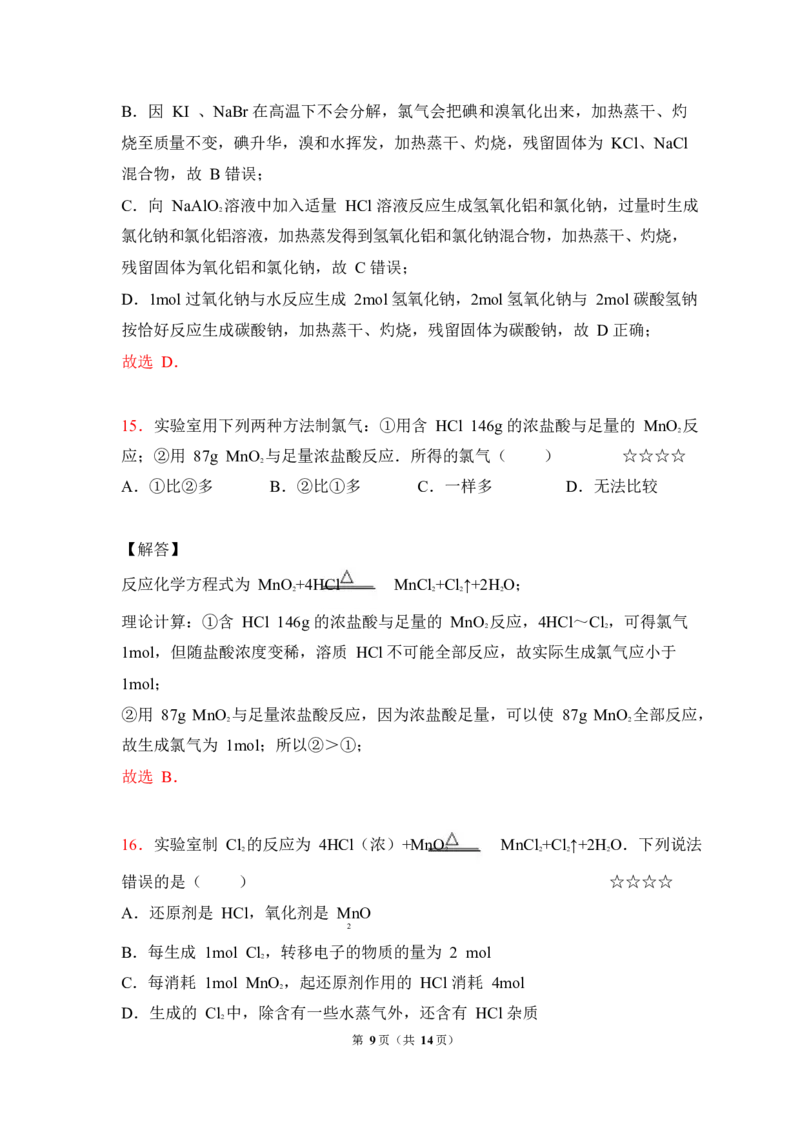
20.如图是实验室制备氯气并进行一系列相关实验的装置(夹持及加热仪器已略).
☆☆☆☆
第 11页(共 14页)(1)制备氯气选用的药品为固体二氧化锰和浓盐酸,则相关的化学反应方程式
为:___________________________;装置 B 中饱和食盐水的作用是
___________________;同时装置 B 亦是安全瓶,监测实验进行时 C 中是否发生
堵塞,请写出发生堵塞时 B 中的现象
__________________________________________.
(2)装置 C 的实验目的是验证氯气是否具有漂白性,为此 C 中Ⅰ、Ⅱ、Ⅲ依次
放入______.
a b c d
I 干燥的有色布条 干燥的有色布条 湿润的有色布条 湿润的有色布条
Ⅱ 碱石灰 硅胶 浓硫酸 无水氯化钙
Ⅲ 湿润的有色布条 湿润的有色布条 干燥的有色布条 干燥的有色布条
【解答】
(1)二氧化锰与浓盐酸在加热条件下反应生成氯化锰、氯气和水,化学方程式:
MnO+4HCl(浓) MnCl+Cl↑+2HO;制备的氯气中含有氯化氢,氯化氢在
2 2 2 2
饱和食盐水中溶解度较大,氯气在饱和食盐水中溶解度不大,所以可以用 B 中饱
和食盐水吸收氯气中的氯化氢;监测实验进行时 C 中是否发生堵塞,发生堵塞时
B 中的,压强增大,气体将溶液压入长颈漏斗 B 中,形成水柱;
故答案为:MnO+4HCl(浓) MnCl+Cl↑+2HO;除去 Cl 中的 HCl;B 中
2 2 2 2 2
长颈漏斗中液面上升,形成水柱;
(2)装置 C 的实验目的是验证氯气是否具有漂白性,验证氯气是否具有漂白性,
要验证干燥氯气无漂白性,湿润的有色布条中,氯气和水反应生成次氯酸具有漂
白性,选项中 ab 的Ⅱ中都是干燥剂,再通入湿润的有色布条不能验证氯气的漂
第 12页(共 14页)白性;c 中 II 为固体干燥剂,不能为浓硫酸,所以 C 中 I、II、III 依次放入湿
润的有色布条、无水氯化钙、干燥的有色布条,所以选 d。
故答案为:d.
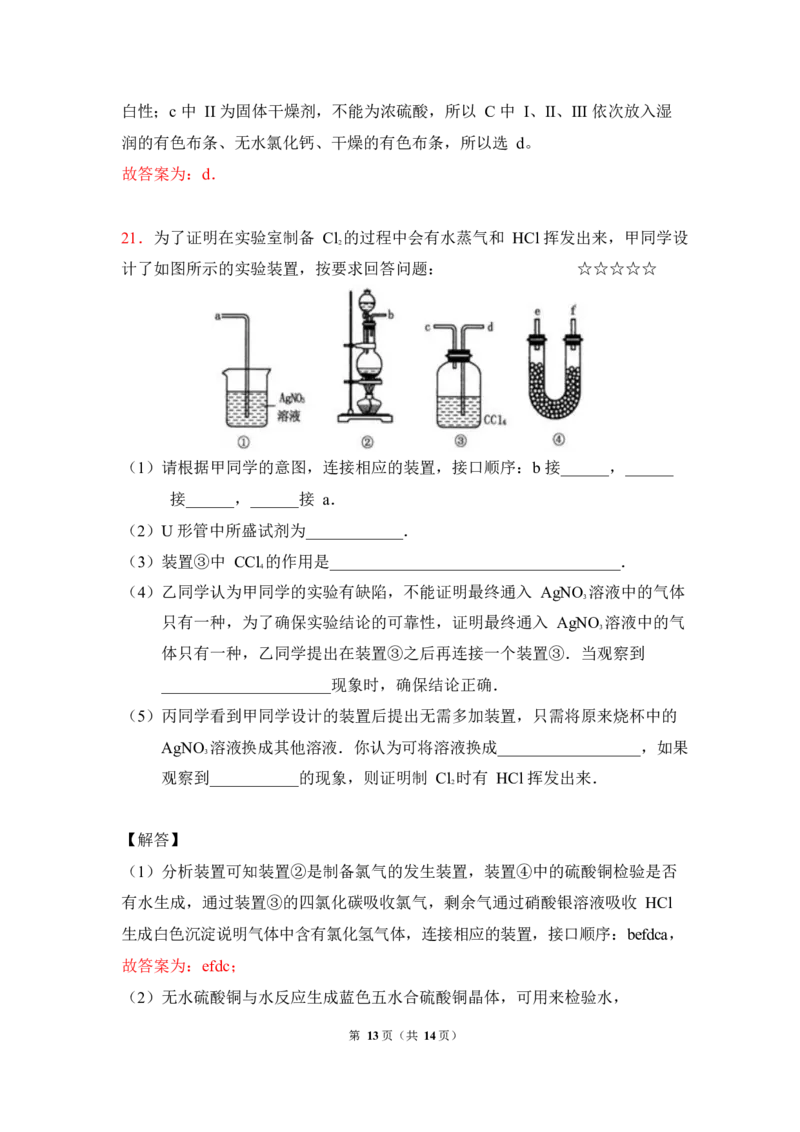
21.为了证明在实验室制备 Cl 的过程中会有水蒸气和 HCl 挥发出来,甲同学设
2
计了如图所示的实验装置,按要求回答问题: ☆☆☆☆☆
(1)请根据甲同学的意图,连接相应的装置,接口顺序:b 接______,______
接______,______接 a.
(2)U 形管中所盛试剂为____________.
(3)装置③中 CCl 的作用是____________________________________.
4
(4)乙同学认为甲同学的实验有缺陷,不能证明最终通入 AgNO 溶液中的气体
3
只有一种,为了确保实验结论的可靠性,证明最终通入 AgNO 溶液中的气
3
体只有一种,乙同学提出在装置③之后再连接一个装置③.当观察到
_____________________现象时,确保结论正确.
(5)丙同学看到甲同学设计的装置后提出无需多加装置,只需将原来烧杯中的
AgNO 溶液换成其他溶液.你认为可将溶液换成__________________,如果
3
观察到___________的现象,则证明制 Cl 时有 HCl 挥发出来.
2
【解答】
(1)分析装置可知装置②是制备氯气的发生装置,装置④中的硫酸铜检验是否
有水生成,通过装置③的四氯化碳吸收氯气,剩余气通过硝酸银溶液吸收 HCl
生成白色沉淀说明气体中含有氯化氢气体,连接相应的装置,接口顺序:befdca,
故答案为:efdc;
(2)无水硫酸铜与水反应生成蓝色五水合硫酸铜晶体,可用来检验水,
第 13页(共 14页)故答案为:无水 CuSO;
4
(3)氯气易溶于四氯化碳溶液,可用来吸收氯气,
故答案为:吸收 Cl;
2
(4)①装置用来检验 HCl 气体,为了确保实验结论的可靠性,应排除氯气的干
扰,在③吸收氯气之后要检验氯气是否完全除去,在装置③之后再连接一个装置
③,当观察到现象第一个装置③中 CCl 显浅黄绿色,第二个装置③中 CCl 无颜
4 4
色变化时,能确保结论正确,
故答案为:第一个装置③中 CCl4 显浅黄绿色,第二个装置③中 CCl 无颜色变化;
4
(5)将原来烧杯中的 AgNO 溶液换成石蕊试液,气体通过紫色石蕊试液变红而
3
不退色,证明制 Cl 时有 HCl 挥发出来,
2
故答案为:紫色石蕊试液;紫色石蕊试液变红而不退色.
第 14页(共 14页)