文档内容
专练 28 热化学方程式的书写及正误判断
1.运载火箭以液氢为燃烧剂,液氧为氧化剂。已知:
Ⅰ.H (g)===H (l) ΔH=-0.92 kJ·mol-1
2 2
Ⅱ.O (g)===O (l) ΔH=-6.84 kJ·mol-1
2 2
下列说法正确的是( )
A.氢气的燃烧热ΔH=-241.8 kJ·mol-1
B.火箭中液氢燃烧的热化学方程式为
2H(l)+O(l)===2H O(g) ΔH=-474.92 kJ·mol-1
2 2 2
C.2 mol H (g)与1 mol O (g)所具有的总能量比2 mol H O(g)所具有的总能量低
2 2 2
D.HO(g)变成HO(l)的过程中,断键吸收的能量小于成键放出的能量
2 2
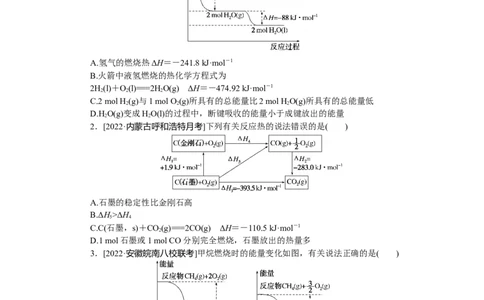
2.[2022·内蒙古呼和浩特月考]下列有关反应热的说法错误的是( )
A.石墨的稳定性比金刚石高
B.ΔH>ΔH
5 4
C.C(石墨,s)+CO(g)===2CO(g) ΔH=-110.5 kJ·mol-1
2
D.1 mol石墨或1 mol CO分别完全燃烧,石墨放出的热量多
3.[2022·安徽皖南八校联考]甲烷燃烧时的能量变化如图,有关说法正确的是( )
A.图甲中反应为CH(g)+2O(g)===CO (g)+2HO(l) ΔH=+890.3 kJ·mol-1
4 2 2 2
B.图乙中反应为CH(g)+O(g)===CO(g)+2HO(g) ΔH=-607.3 kJ·mol-1
4 2 2
C.由图可以推得:CO(g)+O(g)===CO (g) ΔH=-283 kJ·mol-1
2 2
D.由图可以推知:等物质的量的CO 和CO,CO 具有的能量高
2 2
4.[2022·湖南辰溪县博雅中学月考]下列热化学方程式书写正确的是(ΔH的绝对值均正确)( )
A.C HOH(l)+3O(g)===2CO (g)+3HO(g) ΔH=-1 367.0 kJ·mol-1(燃烧热)
2 5 2 2 2
B.NaOH(aq)+HCl(aq)===NaCl(aq)+HO(l) ΔH=+57.3 kJ·mol-1(中和热)
2
C.S(s)+O(g)===SO(g) ΔH=-296.8 kJ·mol-1(反应热)
2 2
D.2NO ===O +2NO ΔH=+116.2 kJ·mol-1(反应热)
2 2
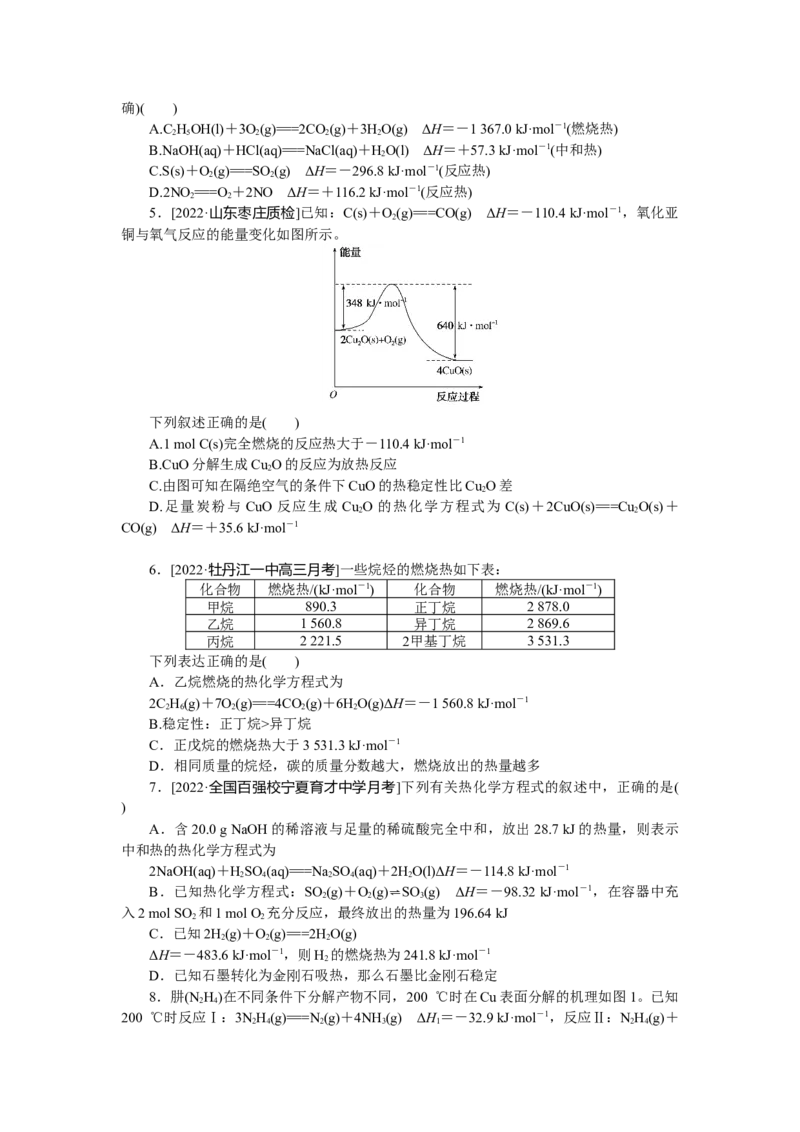
5.[2022·山东枣庄质检]已知:C(s)+O(g)===CO(g) ΔH=-110.4 kJ·mol-1,氧化亚
2
铜与氧气反应的能量变化如图所示。
下列叙述正确的是( )
A.1 mol C(s)完全燃烧的反应热大于-110.4 kJ·mol-1
B.CuO分解生成Cu O的反应为放热反应
2
C.由图可知在隔绝空气的条件下CuO的热稳定性比Cu O差
2
D.足量炭粉与 CuO 反应生成 Cu O 的热化学方程式为 C(s)+2CuO(s)===Cu O(s)+
2 2
CO(g) ΔH=+35.6 kJ·mol-1
6.[2022·牡丹江一中高三月考]一些烷烃的燃烧热如下表:
化合物 燃烧热/(kJ·mol-1) 化合物 燃烧热/(kJ·mol-1)
甲烷 890.3 正丁烷 2 878.0
乙烷 1 560.8 异丁烷 2 869.6
丙烷 2 221.5 2甲基丁烷 3 531.3
下列表达正确的是( )
A.乙烷燃烧的热化学方程式为
2C H(g)+7O(g)===4CO (g)+6HO(g)ΔH=-1 560.8 kJ·mol-1
2 6 2 2 2
B.稳定性:正丁烷>异丁烷
C.正戊烷的燃烧热大于3 531.3 kJ·mol-1
D.相同质量的烷烃,碳的质量分数越大,燃烧放出的热量越多
7.[2022·全国百强校宁夏育才中学月考]下列有关热化学方程式的叙述中,正确的是(
)
A.含20.0 g NaOH的稀溶液与足量的稀硫酸完全中和,放出28.7 kJ的热量,则表示
中和热的热化学方程式为
2NaOH(aq)+HSO (aq)===Na SO (aq)+2HO(l)ΔH=-114.8 kJ·mol-1
2 4 2 4 2
B.已知热化学方程式:SO
2
(g)+O
2
(g)⇌SO
3
(g) ΔH=-98.32 kJ·mol-1,在容器中充
入2 mol SO 和1 mol O 充分反应,最终放出的热量为196.64 kJ
2 2
C.已知2H(g)+O(g)===2H O(g)
2 2 2
ΔH=-483.6 kJ·mol-1,则H 的燃烧热为241.8 kJ·mol-1
2
D.已知石墨转化为金刚石吸热,那么石墨比金刚石稳定
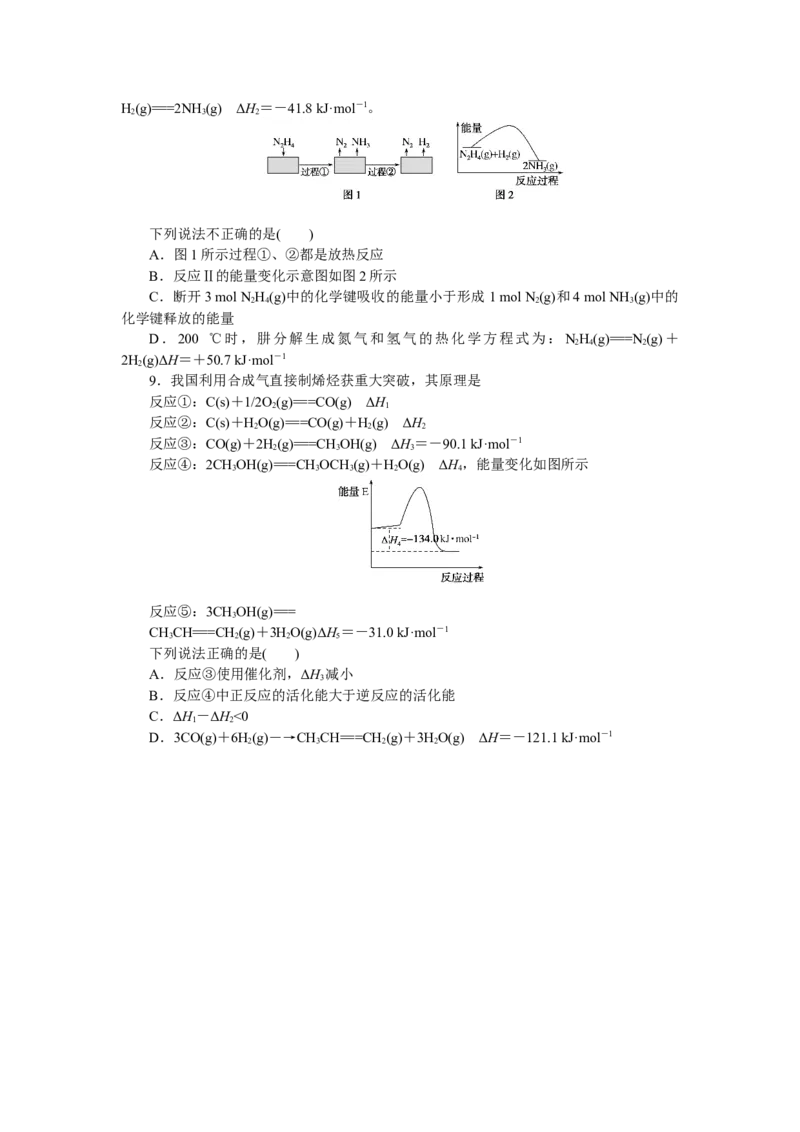
8.肼(N H)在不同条件下分解产物不同,200 ℃时在Cu表面分解的机理如图1。已知
2 4
200 ℃时反应Ⅰ:3NH(g)===N (g)+4NH (g) ΔH =-32.9 kJ·mol-1,反应Ⅱ:NH(g)+
2 4 2 3 1 2 4H(g)===2NH(g) ΔH=-41.8 kJ·mol-1。
2 3 2
下列说法不正确的是( )
A.图1所示过程①、②都是放热反应
B.反应Ⅱ的能量变化示意图如图2所示
C.断开3 mol N H(g)中的化学键吸收的能量小于形成1 mol N (g)和4 mol NH (g)中的
2 4 2 3
化学键释放的能量
D.200 ℃时,肼分解生成氮气和氢气的热化学方程式为:NH(g)===N (g)+
2 4 2
2H(g)ΔH=+50.7 kJ·mol-1
2
9.我国利用合成气直接制烯烃获重大突破,其原理是
反应①:C(s)+1/2O (g)===CO(g) ΔH
2 1
反应②:C(s)+HO(g)===CO(g)+H(g) ΔH
2 2 2
反应③:CO(g)+2H(g)===CH OH(g) ΔH=-90.1 kJ·mol-1
2 3 3
反应④:2CHOH(g)===CH OCH (g)+HO(g) ΔH,能量变化如图所示
3 3 3 2 4
反应⑤:3CHOH(g)===
3
CHCH===CH (g)+3HO(g)ΔH=-31.0 kJ·mol-1
3 2 2 5
下列说法正确的是( )
A.反应③使用催化剂,ΔH 减小
3
B.反应④中正反应的活化能大于逆反应的活化能
C.ΔH-ΔH<0
1 2
D.3CO(g)+6H(g)―→CHCH===CH (g)+3HO(g) ΔH=-121.1 kJ·mol-1
2 3 2 2