文档内容
专练 28 热化学方程式的书写及正误判断
一、单项选择题
1.[2022·湖南博雅中学月考]下列热化学方程式书写正确的是(ΔH的绝对值均正确)(
)
A.C HOH(l)+3O(g)===2CO (g)+3HO(g)
2 5 2 2 2
ΔH=-1 367.0 kJ·mol-1(燃烧热)
B.NaOH(aq)+HCl(aq)===NaCl(aq)+HO(l)
2
ΔH=+57.3 kJ·mol-1(中和热)
C.S(s)+O(g)===SO(g)
2 2
ΔH=-296.8 kJ·mol-1(反应热)
D.2NO ===O +2NO
2 2
ΔH=+116.2 kJ·mol-1(反应热)
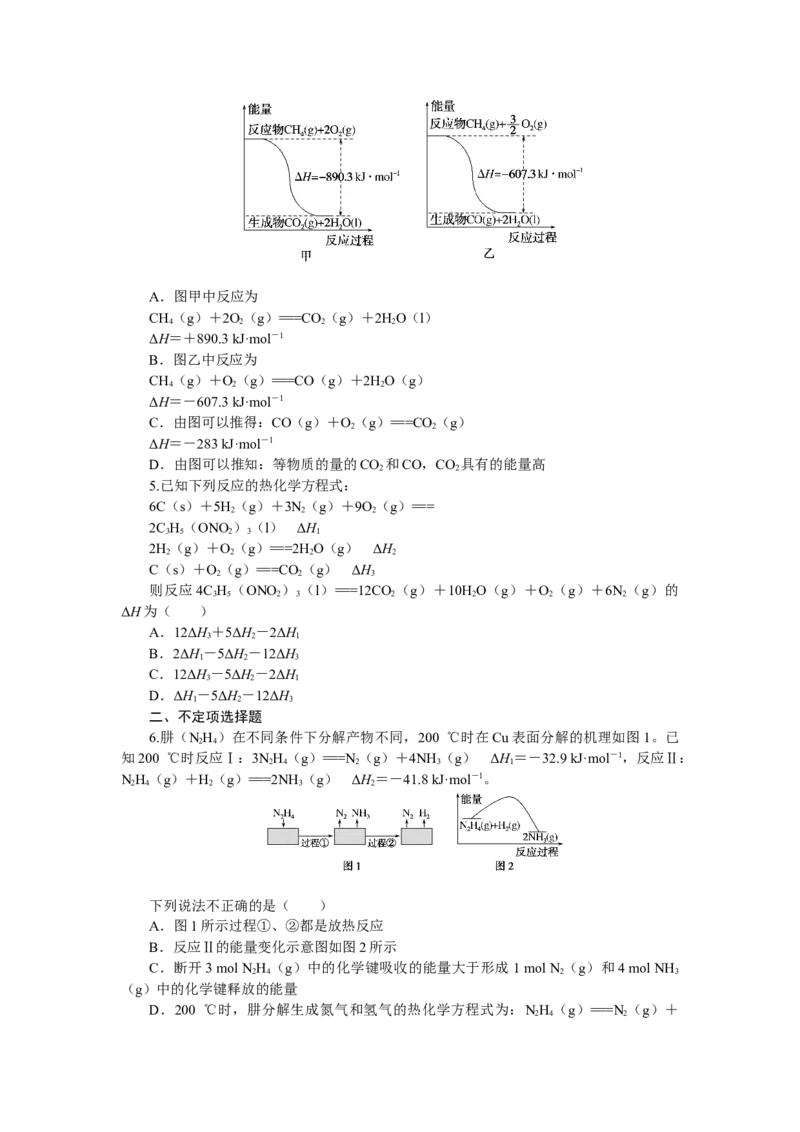
2.[2022·山东枣庄质检]已知:C(s)+O (g)===CO(g) ΔH=-110.4 kJ·mol-1,
2
氧化亚铜与氧气反应的能量变化如图所示。
下列叙述正确的是( )
A.1 mol C(s)完全燃烧的反应热大于-110.4 kJ·mol-1
B.CuO分解生成Cu O的反应为放热反应
2
C.由图可知在隔绝空气的条件下CuO的热稳定性比Cu O差
2
D.足量炭粉与CuO反应生成Cu O的热化学方程式为C(s)+2CuO(s)===Cu O
2 2
(s)+CO(g)
ΔH=+35.6 kJ·mol-1
3.[2022·黑龙江大庆实验中学月考]已知H 的燃烧热为ΔH=-285.8 kJ·mol-1,CO的燃
2
烧热为ΔH=-282.8 kJ·mol-1;现有H 和CO组成的混合气体5.6 L(标准状况),经充分
2
燃烧后,放出总热量为71.15 kJ,并生成液态水。下列说法正确的是( )
A.CO燃烧的热化学方程式为 2CO(g)+O (g)===2CO (g) ΔH=-282.8
2 2
kJ·mol-1
B.H 燃烧的热化学方程式为2H(g)+O(g)===2H O(g) ΔH=-571.6 kJ·mol
2 2 2 2
-1
C.燃烧前混合气体中CO的体积分数为60%
D.燃烧后的产物全部与足量的过氧化钠作用可产生0.125 mol O
2
4.甲烷燃烧时的能量变化如图,有关说法正确的是( )A.图甲中反应为
CH(g)+2O(g)===CO (g)+2HO(l)
4 2 2 2
ΔH=+890.3 kJ·mol-1
B.图乙中反应为
CH(g)+O(g)===CO(g)+2HO(g)
4 2 2
ΔH=-607.3 kJ·mol-1
C.由图可以推得:CO(g)+O(g)===CO (g)
2 2
ΔH=-283 kJ·mol-1
D.由图可以推知:等物质的量的CO 和CO,CO 具有的能量高
2 2
5.已知下列反应的热化学方程式:
6C(s)+5H(g)+3N(g)+9O(g)===
2 2 2
2C H(ONO)(l) ΔH
3 5 2 3 1
2H(g)+O(g)===2H O(g) ΔH
2 2 2 2
C(s)+O(g)===CO (g) ΔH
2 2 3
则反应4C H (ONO ) (l)===12CO (g)+10HO(g)+O (g)+6N (g)的
3 5 2 3 2 2 2 2
ΔH为( )
A.12ΔH+5ΔH-2ΔH
3 2 1
B.2ΔH-5ΔH-12ΔH
1 2 3
C.12ΔH-5ΔH-2ΔH
3 2 1
D.ΔH-5ΔH-12ΔH
1 2 3
二、不定项选择题
6.肼(NH )在不同条件下分解产物不同,200 ℃时在Cu表面分解的机理如图1。已
2 4
知200 ℃时反应Ⅰ:3NH (g)===N (g)+4NH (g) ΔH =-32.9 kJ·mol-1,反应Ⅱ:
2 4 2 3 1
NH(g)+H(g)===2NH(g) ΔH=-41.8 kJ·mol-1。
2 4 2 3 2
下列说法不正确的是( )
A.图1所示过程①、②都是放热反应
B.反应Ⅱ的能量变化示意图如图2所示
C.断开3 mol N H (g)中的化学键吸收的能量大于形成1 mol N (g)和4 mol NH
2 4 2 3
(g)中的化学键释放的能量
D.200 ℃时,肼分解生成氮气和氢气的热化学方程式为:NH (g)===N (g)+
2 4 22H(g) ΔH=+50.7 kJ·mol-1
2
7.下列有关热化学方程式的叙述,正确的是( )
A.1 mol甲烷燃烧生成气态水和二氧化碳所放出的热量是甲烷的燃烧热
B.由N
2
O
4
(g) ⇌2NO
2
(g) ΔH=-56.9 kJ·mol-1,可知将1 mol N
2
O
4
(g)置于密
闭容器中充分反应后放出热量为56.9 kJ
C.由H+(aq)+OH-(aq)===H O(l)
2
ΔH=-57.3 kJ·mol-1,可知:含1 mol CH COOH的溶液与含1 mol NaOH的溶液混合
3
放出热量为57.3 kJ
D.已知101 kPa时,2C(s)+O (g)===2CO(g) ΔH=-221 kJ·mol-1,则1
2
mol碳完全燃烧生成CO 放出的热量大于110.5 kJ
2
8.[2022·经典习题选萃]化学上规定稳定单质的生成热为0;可用物质的生成热表示该物
质的相对能量高低。氮的几种氧化物的相对能量如下表所示(25 ℃,105 Pa条件下):
物质及状态 NO(g) NO(g) NO (g) NO(l) NO(g)
2 2 2 4 2 5
相对能量
82 90 33 -20 11
(kJ·mol-1)
下列推断不正确的是( )
A.在5种氮的氧化物中,NO最活泼
B.N
2
O
4
(l) ⇌2NO
2
(g) ΔH=-86 kJ·mol-1
C.NO(g)===2NO(g)+O(g)
2 5 2 2
ΔH=+55 kJ·mol-1
D.1 mol N O(g)分解成N(g)和O(g)需要放出82 kJ能量
2 2 2
三、非选择题
9.(1)晶体硅(熔点1 410 ℃)是良好的半导体材料。由粗硅制纯硅过程如下:
Si(粗)――→SiCl ――→SiCl (纯)――→Si(纯)
4 4
写出SiCl 的电子式: ;在上述由SiCl 制纯硅的反应中,测得每生成 1.12 kg
4 4
纯 硅 需 吸 收 a kJ 热 量 , 写 出 该 反 应 的 热 化 学 方 程 式 :
________________________________________________________________________。
(2)已知AX 的熔点和沸点分别为-93.6 ℃和76 ℃,AX 的熔点为167 ℃。室温时
3 5
AX 与气体 X 反应生成 1 mol AX ,放出热量 123.8 kJ。该反应的热化学方程式为
3 2 5
。
(3)CuCl(s)和O 反应生成CuCl (s)和一种黑色固体。在25 ℃、101 kPa下,已
2 2
知该反应每消耗 1 mol CuCl(s),放热 44.4 kJ,该反应的热化学方程式是
。
(4)汽车发动机工作时会引发N 和O 反应,其能量变化示意图如下:
2 2
――→2NO(g)
写 出 该 反 应 的 热 化 学 方 程 式 :
________________________________________________________________________
________________________________________________________________________。
(5)用Cl 生产某些含氯有机物时会产生副产物HCl。利用反应A,可实现氯的循环
2
利用。
反应A:4HCl+O2Cl+2HO
2 2 2
已知:ⅰ.反应A中,4 mol HCl被氧化,放出115.6 kJ的热量。
ⅱ.①HO的电子式是 。
2
② 反 应 A 的 热 化 学 方 程 式 是
________________________________________________________________________。
③断开1 mol H—O 键与断开 1 mol H—Cl键所需能量相差约为 kJ,HO中
2
H—O键比HCl中H—Cl键 (填“强”或“弱”)。