文档内容
专练 56 晶体结构与性质
一、单项选择题
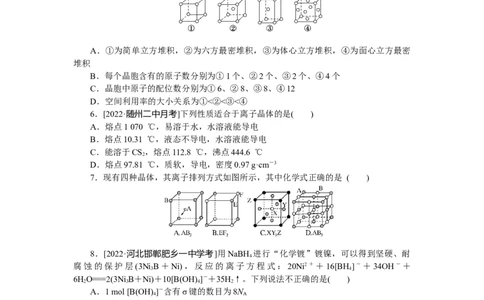
1.
[2021·辽宁卷]单质硫和氢气在低温高压下可形成一种新型超导材料,其晶胞如图。下
列说法错误的是( )
A.S位于元素周期表p区
B.该物质的化学式为HS
3
C.S位于H构成的八面体空隙中
D.该晶体属于分子晶体
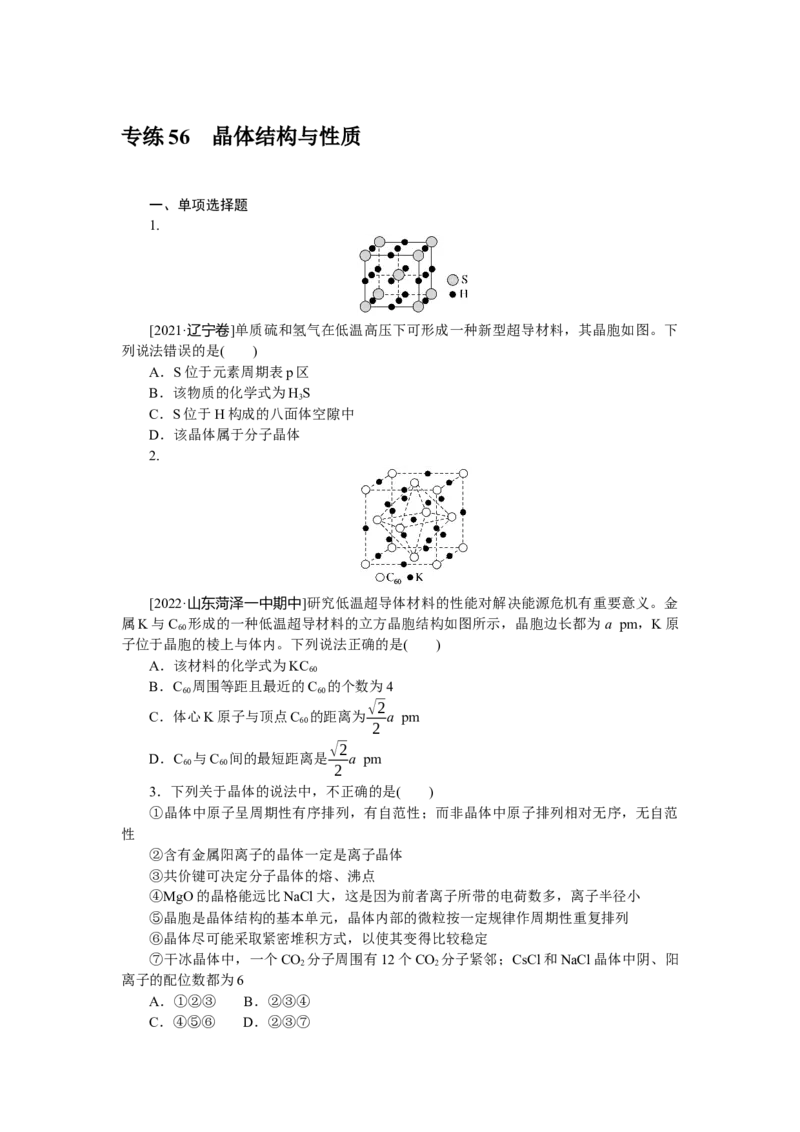
2.
[2022·山东菏泽一中期中]研究低温超导体材料的性能对解决能源危机有重要意义。金
属K与C 形成的一种低温超导材料的立方晶胞结构如图所示,晶胞边长都为 a pm,K原
60
子位于晶胞的棱上与体内。下列说法正确的是( )
A.该材料的化学式为KC
60
B.C 周围等距且最近的C 的个数为4
60 60
√2
C.体心K原子与顶点C 的距离为 a pm
60
2
√2
D.C 与C 间的最短距离是 a pm
60 60
2
3.下列关于晶体的说法中,不正确的是( )
①晶体中原子呈周期性有序排列,有自范性;而非晶体中原子排列相对无序,无自范
性
②含有金属阳离子的晶体一定是离子晶体
③共价键可决定分子晶体的熔、沸点
④MgO的晶格能远比NaCl大,这是因为前者离子所带的电荷数多,离子半径小
⑤晶胞是晶体结构的基本单元,晶体内部的微粒按一定规律作周期性重复排列
⑥晶体尽可能采取紧密堆积方式,以使其变得比较稳定
⑦干冰晶体中,一个CO 分子周围有12个CO 分子紧邻;CsCl和NaCl晶体中阴、阳
2 2
离子的配位数都为6
A.①②③ B.②③④
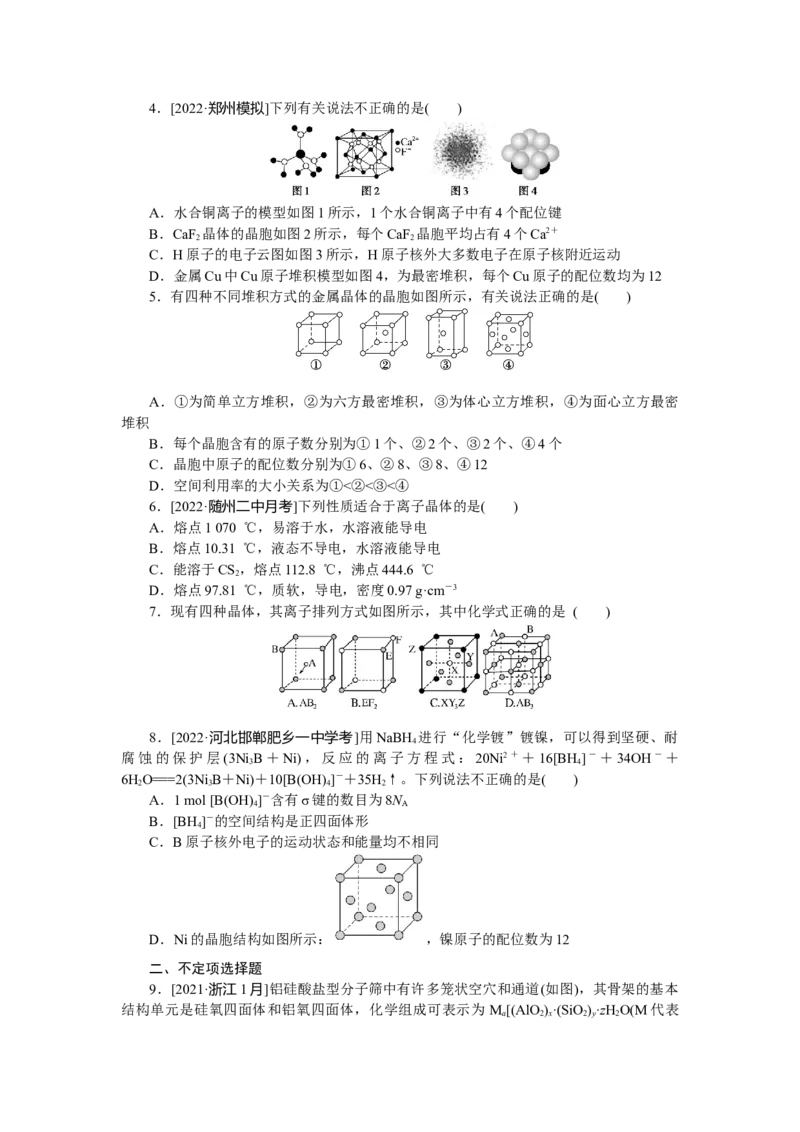
C.④⑤⑥ D.②③⑦4.[2022·郑州模拟]下列有关说法不正确的是( )
A.水合铜离子的模型如图1所示,1个水合铜离子中有4个配位键
B.CaF 晶体的晶胞如图2所示,每个CaF 晶胞平均占有4个Ca2+
2 2
C.H原子的电子云图如图3所示,H原子核外大多数电子在原子核附近运动
D.金属Cu中Cu原子堆积模型如图4,为最密堆积,每个Cu原子的配位数均为12
5.有四种不同堆积方式的金属晶体的晶胞如图所示,有关说法正确的是( )
A.①为简单立方堆积,②为六方最密堆积,③为体心立方堆积,④为面心立方最密
堆积
B.每个晶胞含有的原子数分别为①1个、②2个、③2个、④4个
C.晶胞中原子的配位数分别为①6、②8、③8、④12
D.空间利用率的大小关系为①<②<③<④
6.[2022·随州二中月考]下列性质适合于离子晶体的是( )
A.熔点1 070 ℃,易溶于水,水溶液能导电
B.熔点10.31 ℃,液态不导电,水溶液能导电
C.能溶于CS,熔点112.8 ℃,沸点444.6 ℃
2
D.熔点97.81 ℃,质软,导电,密度0.97 g·cm-3
7.现有四种晶体,其离子排列方式如图所示,其中化学式正确的是 ( )
8.[2022·河北邯郸肥乡一中学考]用NaBH 进行“化学镀”镀镍,可以得到坚硬、耐
4
腐蚀的保护层(3NiB+Ni),反应的离子方程式:20Ni2++16[BH]-+34OH-+
3 4
6HO===2(3Ni B+Ni)+10[B(OH) ]-+35H↑。下列说法不正确的是( )
2 3 4 2
A.1 mol [B(OH) ]-含有σ键的数目为8N
4 A
B.[BH]-的空间结构是正四面体形
4
C.B原子核外电子的运动状态和能量均不相同
D.Ni的晶胞结构如图所示: ,镍原子的配位数为12
二、不定项选择题
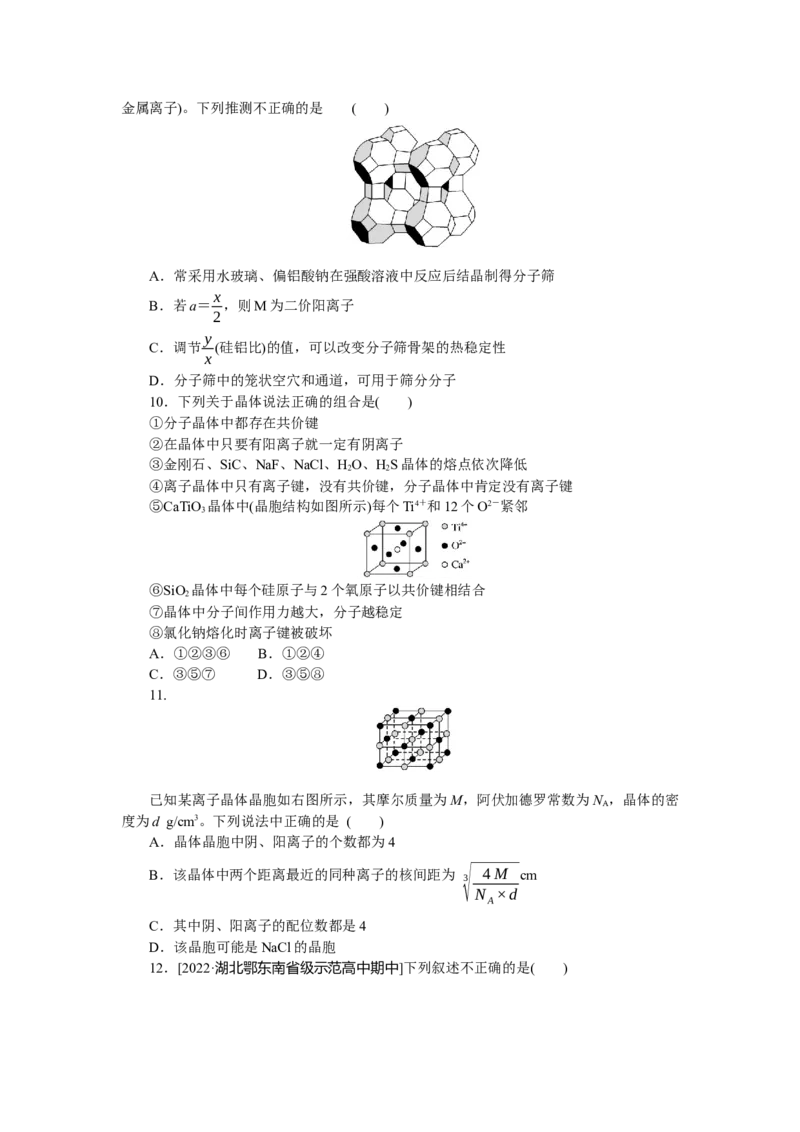
9.[2021·浙江1月]铝硅酸盐型分子筛中有许多笼状空穴和通道(如图),其骨架的基本
结构单元是硅氧四面体和铝氧四面体,化学组成可表示为 M[(AlO )·(SiO)·zHO(M代表
a 2 x 2 y 2金属离子)。下列推测不正确的是 ( )
A.常采用水玻璃、偏铝酸钠在强酸溶液中反应后结晶制得分子筛
x
B.若a= ,则M为二价阳离子
2
y
C.调节 (硅铝比)的值,可以改变分子筛骨架的热稳定性
x
D.分子筛中的笼状空穴和通道,可用于筛分分子
10.下列关于晶体说法正确的组合是( )
①分子晶体中都存在共价键
②在晶体中只要有阳离子就一定有阴离子
③金刚石、SiC、NaF、NaCl、HO、HS晶体的熔点依次降低
2 2
④离子晶体中只有离子键,没有共价键,分子晶体中肯定没有离子键
⑤CaTiO 晶体中(晶胞结构如图所示)每个Ti4+和12个O2-紧邻
3
⑥SiO 晶体中每个硅原子与2个氧原子以共价键相结合
2
⑦晶体中分子间作用力越大,分子越稳定
⑧氯化钠熔化时离子键被破坏
A.①②③⑥ B.①②④
C.③⑤⑦ D.③⑤⑧
11.
已知某离子晶体晶胞如右图所示,其摩尔质量为M,阿伏加德罗常数为N ,晶体的密
A
度为d g/cm3。下列说法中正确的是 ( )
A.晶体晶胞中阴、阳离子的个数都为4
B.该晶体中两个距离最近的同种离子的核间距为 √ 4M cm
3
N ×d
A
C.其中阴、阳离子的配位数都是4
D.该晶胞可能是NaCl的晶胞
12.[2022·湖北鄂东南省级示范高中期中]下列叙述不正确的是( )A.LiS晶胞结构如图甲,S2-的配位数是8
2
B.某镍白铜合金的立方晶胞结构如图乙,晶胞中铜原子与镍原子的数量比为3∶1
C.氯化钠晶胞如图丙,离钠离子最近的钠离子有6个
D.铜与氧形成的晶胞如图丁,晶胞中Cu均匀地分散在立方体内部,a、b的坐标参数
分别为(0,0,0)、(1 1 1),则d的坐标参数为(3 3 1)
, , , ,
2 2 2 4 4 4