文档内容
专项 02 离子反应与氧化还原反应
该专题分为两个板块
【1】知识清单
一、离子反应
1. 离子方程式正误判断的基本方法
2. 与量有关离子方程式的书写
3. 离子能否大量共存的判断
4. 离子推断的“原则”
二、氧化还原反应
1. 基本概念和常用价态
2. 熟知常见的氧化剂与还原剂及其产物形式
3. 掌握氧化还原反应的规律
【2】专项练习
【1】知识清单
一、离子反应
1. 离子方程式正误判断的基本方法
①是否符合事实——离子反应要符合客观事实。
②要书写规范——化学式与离子符号书写正确、合理。易溶易电离的物质写成离子形式。难容难电离的物
质写成分子形式。
强酸(6大强酸):HCl、HSO 、HNO、HI、HBr、HClO
2 4 3 4
强碱(4大强碱):NaOH、KOH、Ca(OH) 、Ba(OH)
2 2
③符号正确书写——“=====”“ ”“↑”“↓”等符号使用要正确。
④三大守恒——离子方程式两边应同时满足质量守恒、电荷守恒、得失电子守恒。
⑤明确用量问题——看清题目中用量问题“少量”“过量”“滴加”。
⑥仔细检查——结合书写离子方程式过程中易出现的错误,细心检查。
2. 与量有关离子方程式的书写
(1)过量与少量型
书写原则是“以少定多”,即先根据题给条件判断“少量物质”,以“少量物质”的计量数(充分反应)确
定所需“过量物质”的计量数。如向Ca(HCO ) 溶液中加入过量NaOH溶液的离子方程式的书写方法为
3 2①如向FeBr 溶液中通入少量Cl: 2Fe 2 + + Cl ===2Fe 3 + + 2Cl -
2 2 2
②如向FeBr 溶液中通入足量Cl: 2Fe 2 + + 4Br - + 3Cl ===2Fe 3 + + 2Br + 6C l - 。
2 2 2 2
(2)定量型
首先根据题给条件中反应物的物质的量,结合“以少定多”的原则及离子反应的顺序,逐步写出各步反应
的离子方程式,然后把各步离子方程式相加即可得到总反应的离子方程式。如明矾与含等物质的量的
Ba(OH) 溶液反应的离子方程式书写方法为
2
如向100 mL 1 mol/L FeBr 溶液中通入2.24 L(标况下)Cl : 2F e 2 + + 2B r - + 2C l ===2Fe 3 + + Br + 4C l - 。
2 2 2 2
(3)反应先后顺序型
①复分解反应型
如某溶液中含有H+、NH +、Al3+,向溶液中逐滴加入NaOH溶液,
4
首先,H+与OH-反应 : H + + OH - ===H O;
2
其次,Al3+与OH-反应生成白色沉淀: Al 3 + + 3OH - ===Al(OH) ↓;
3
再者,NH +与OH-反应:NH + + OH - ===NH ·H O;
4 4 3 2
最后,Al(OH) 与OH-反应:Al(OH) + OH - ===AlO - + 2H O 或Al(OH) + OH - ===[Al(OH ) ] - 。
3 3 2 2 3 4
②氧化还原反应型
依据氧化还原反应的强弱规律,同一氧化剂与多种还原剂反应,还原性强的还原剂优先发生反应;同一还
原剂与多种氧化剂反应,氧化性强的氧化剂优先发生反应。
如向含Fe3+、Cu2+、H+的溶液中加入锌粉。
首先Fe3+与Zn反应: 2Fe 3 + + Zn===Zn 2 + + 2Fe 2 + ;
其次Cu2+与Zn反应: Zn + Cu 2 + ===Cu + Zn 2 + ;
最后H+与Zn反应: Zn + 2H + ===Zn 2 + + H ↑。
2
3.离子能否大量共存的判断
(1)常见的隐含条件类型
颜色 无色溶液
①pH<7
酸性 ②使甲基橙(或石蕊)变红的溶液
条件 ③=1×10-13 mol/L
④0.1 mol/L HCl溶液
①pH>7
碱性 ②使酚酞变红(或石蕊变蓝)
条件 ③=1×10-12的溶液
④0.1 mol/L NaOH溶液
酸性
①与Al反应能放出H 的溶液
2
或
②水电离的c(H+)=1×10-13 mol/L的溶液
碱性
(2)不能大量共存的原因
发生复分解反应(有沉淀、弱电解质、气 Ba2+与SO 2-、CO2-,H+与HCO -、OH-、
4 3 3
体生成) CHCOO-,Ca2+与SO 2-、CO2-等不能大量共存
3 4 3
Fe2+与NO -(在酸性溶液中),S2-与SO 2-(在酸性
3 3
发生氧化还原反应 溶液中),Fe2+与ClO-、MnO -,Fe3+与I-不能大
4
量共存
有络合物生成的反应 Fe3+与SCN-、Cu2+与氨水不能大量共存
水解相互促进反应 Al3+与CO-、HCO -,Al3+与AlO-不能大量共存
3 3 2
4.离子推断的“四大原则”
(1)肯定性原则:根据实验现象推出溶液中肯定存在或肯定不存在的离子(常见的有色离子:Fe2+、Fe3+、
Cu2+、MnO -等)。
4
(2)互斥性原则:在肯定某些离子存在的同时,结合离子共存的规律,否定一些离子的存在(要注意题目中
的隐含条件,如酸性、碱性、指示剂的颜色变化、与铝反应产生H、水的电离情况等)。
2
(3)电中性原性:溶液呈电中性,有阳离子,一定有阴离子,且溶液中正电荷总数与负电荷总数相等。
(4)进出性原则:通常是在实验过程中使用,是指在实验过程中反应生成的离子或引入的离子对后续实验的
干扰。
二、氧化还原反应
1.基本概念和常用价态
(1)线索图示(2)常见元素化合价
NaClO(Cl: + 3)、ClO (Cl: + 4)、CuCl(Cu: + 1)、NH(N: - 2)、NaBH (H: - 1)、KCr O(Cr: + 6)、
2 2 2 4 4 2 2 7
NaCrO(Cr: + 6)、HC O(C: + 3)、NaSO(S: + 2)、MnO(OH) (Mn: + 4)、KFeO(Fe: + 6)、
2 4 2 2 4 2 2 3 2 2 4
CuFeS(Fe: + 2、S: - 2)、LiNH(N: - 3)、LiCoO (Co: + 3)、HCN(N: - 3、C: + 2)。
2 2 2
2.熟知常见的氧化剂与还原剂
(1)常见的氧化剂与还原产物
氧化剂 还原产物
Mn 2 + ( 酸性 ) 、 MnO ( 中性或弱酸性 ) 、
2
KMnO
4
MnO 2 - ( 碱性 )
4
KCr O(酸性) Cr 3 +
2 2 7
浓硝酸、稀硝酸 NO 、 NO
2
X(卤素单质) X -
2
HO H O( 酸性 ) 、 OH - ( 碱性 )
2 2 2
NaClO(ClO-) Cl - 或 Cl
2
NaClO Cl 或 ClO 或 C l -
3 2 2
(2)常见的还原剂与氧化产物
还原剂 氧化产物
Fe 3 + ( 较强酸性 ) 、 Fe(OH)
3
Fe2+
( 弱酸性至碱性 )
SO (或HSO 、
2 2 3
SO 2-
4
SO、SO)
2
S2-(H S) S 、 SO ( 或 SO 2 - ) 、 SO 2-
2 2 3 4
HC O(或C O) CO ( 酸性 ) 、 CO 2 - ( 碱性 )
2 2 4 2 2 3
HO O
2 2 2
I-(HI) I ( 或 IO - )
2 3
CO CO
2
金属单质(如Fe) Fe 2 + ( 与强氧化剂反应生成 Fe 3 + )
[注意] 水溶液中常见的“两大顺序”
(1)氧化性强弱顺序: MnO (H + )>Ag + >Fe 3 + >Cu 2 + >H + >Fe 2 + ;(2)还原性强弱顺序: S 2 - >SO >I - >Fe 2 + >Br - >Cl - 。
3.掌握氧化还原反应的规律
(1)“四大”规律
①强弱规律——比较物质的氧化性或还原性强弱。氧化性:氧化剂>氧化产物;还原性:还原剂>还原产物。
②价态律——判断氧化还原反应的产物,同种元素不同价态之间发生反应“只靠拢,不交叉”。
③先后律——同一氧化剂与几种还原剂反应,先与还原性强的发生反应,再与还原性弱的发生反应。
同一还原剂与几种氧化剂反应,先与氧化性强的发生反应,再与氧化性弱的发生反应。
④守恒律——得失电子守恒,质量守恒,原子守恒
(2)写出证明氧化性、还原性强弱的离子方程式。
①氧化性强弱顺序:KMnO >Cl>Br >Fe 3 + >Cu 2 + 。
4 2 2
a.KMnO>Cl:2MnO - + 10Cl - + 16H + == =2Mn 2 + + 5Cl ↑ + 8H O。
4 2 4 2 2
b.Cl>Br :Cl + 2B r - == =B r + 2C l - 。
2 2 2 2
c.Br >Fe3+: 2Fe 2 + + Br == =2Fe 3 + + 2Br - 。
2 2
d.Fe3+>Cu2+: 2Fe 3 + + Cu == =2Fe 2 + + Cu 2 + 。
②还原性强弱顺序:SO >I - >Fe 2 + >Br - >Cl - 。
2
a.SO >I-:I + SO + 2H O == =2I - + 4H + + SO 2-。
2 2 2 2 4
b.I->Fe2+: 2Fe 3 + + 2I - == =I + 2F e 2 + 。
2
c.Fe2+>Br-:Br + 2F e 2 + == =2B r - + 2F e 3 + 。
2
d.Br->Cl-:Cl + 2B r - == =B r + 2C l - 。
2 2
【2】专项练习
1.(宁夏青铜峡市高级中学2021届高三12月月考理综化学试题)下列反应的离子方程式不正确的是
A.在含有等物质的量的Fe(NO ) 和KI组成的混合溶液中滴入稀盐酸:3Fe2++4H++ =3Fe3++NO↑+
3 2
2HO
2
B.4mol·L-1的NaAlO 溶液和7mol·L-1的盐酸等体积均匀混合:4 +7H++H O=3Al(OH) ↓+Al3+
2 2 3
C.NH HCO 溶液与足量的NaOH溶液混合加热: + +2OH- NH ↑+ +2HO
4 3 3 2
D.等物质的量浓度、等体积的Ca(HCO ) 溶液与氢氧化钠溶液相混合:Ca2++ +OH-=CaCO ↓+HO
3 2 3 2
【答案】A【详解】A.在含有等物质的量的Fe(NO ) 和KI组成的混合溶液中滴入稀盐酸,NO -与H+形成硝酸体系,
3 2 3
具有强氧化性,而I-的还原性大于Fe2+,I-先被氧化,即先发生反应2NO -+6I-+8H+=3I +4H O+2NO↑,A错
3 2 2
误;
B.4mol·L-1的NaAlO 溶液和7mol·L-1的盐酸等体积均匀混合,4molH+先与4molAlO-反应生成
2 2
4molAl(OH) 沉淀,生成的1molAl(OH) 再与3molH+反应生成1molAl3+,总反应的离子方程式为4AlO-
3 3 2
+7H++H O=3Al(OH) ↓+Al3+,B正确;
2 3
C.NH HCO 溶液与足量的NaOH溶液混合加热,由于OH-过量,NH +和HCO -都与OH-反应,离子方程
4 3 4 3
式为NH ++HCO -+2OH- NH ↑+CO2-+2HO,C正确;
4 3 3 3 2
D.等物质的量浓度、等体积的Ca(HCO ) 溶液与氢氧化钠溶液反应,Ca(HCO ) 过量,此时可以把NaOH
3 2 3 2
看做1,离子方程式为Ca2++HCO -+OH-=CaCO ↓+HO,D正确;
3 3 2
故选A。
2.(2021年·广东卷))宏观辨识与微观探析是化学学科核心素养之一。下列物质性质实验对应的反应方
程式书写正确的是
A. 放入水中:
B. 通过灼热铁粉:
C.铜丝插入热的浓硫酸中:
D. 通入酸性 溶液中:
【答案】D
【详解】A.NaO 放入水中化学方程式应该是:2NaO+2H O=4NaOH+O ↑,A选项中氧元素不守恒,A
2 2 2 2 2 2
错误;
B.HO(g)通过灼热铁粉应高温条件下生成四氧化三铁和氢气,B错误;
2
C.铜丝插入热的浓硫酸中生成的气体不是氢气,应是二氧化硫,C错误;
D.SO 通入酸性KMnO 溶液中,SO 被MnO -氧化为SO 2-,MnO -被SO 还原为Mn2+,再根据得失电子守
2 4 2 4 4 4 2
恒、电荷守恒和元素守恒可得离子方程式为5SO +2H O+2MnO -=5SO2-+4H++2Mn2+,D正确;
2 2 4 4
故选D。
3.(2022年安徽芜湖高三上学期12月教学中期考试)下列指定反应的离子方程式书写正确的是A.工业上生产漂白粉的原理:Cl+2OH−=Cl−+ClO−+H O
2 2
B.四氧化三铁溶于足量稀硝酸:3Fe O+28H++NO =9Fe3++NO↑+14HO
3 4 2
C.向硫酸氢铵溶液中滴入少量氢氧化钠溶液:NH +OH−=NH·H O
3 2
D.氯化银悬浊液滴入过量氨水变澄清:Ag++2NH·H O= Ag(NH) +2H O
3 2 3 2
【答案】B
【详解】A.工业将Cl 通入石灰乳中制备漂白粉,在书写离子方程式时石灰乳不能拆成离子形式,A错误;
2
B.Fe O 与足量稀硝酸反应后,铁元素均生成Fe3+,稀硝酸对应还原产物NO,对应离子方程式为:
3 4
3Fe O+28H++NO -=9Fe3++NO↑+14HO,B正确;
3 4 3 2
C.NH HSO 溶液中主要含有NH +、H+、SO 2-,加入少量NaOH溶液,H+与NaOH反应,对应离子方程
4 4 4 4
式为:H++OH-=H O,C错误;
2
D.AgCl溶于氨水形成银氨配离子,对应离子方程式为:AgCl+2NH·H O=[Ag(NH)]++Cl-+2H O,D错误;
3 2 3 2 2
故答案选B。
4.下列各组离子,在指定条件下,一定能大量共存的是:
①某无色透明的酸性溶液中:Cl-、Na+、CrO2-、SO 2-
4 4
②水电离产生的c(H+)=10-12mol·L-1的溶液中:K+、Ba2+、Cl-、NO -
3
③使紫色石蕊试液变红的溶液中:Fe2+、Mg2+、NO -、Cl-
3
④加入过量NaOH溶液后可得到澄清溶液:K+、Ba2+、 HCO -、C1-
3
⑤c(H+)<c(OH-)的溶液中:ClO-、Cl-、K+、Na+
⑥在酸性高锰酸钾溶液中:Na+、NH +、I-、ClO-
4
⑦能使pH试纸变深蓝色的溶液中:Na+、AlO-、K+、CO2-
2 3
A.①③④⑥⑦ B.②③⑤⑦ C.②⑤⑦ D.②④⑤⑦
【答案】C
【解析】本题考查的是离子共存,是高考的常考题型,限制条件下的离子共存考查更受青睐。
①中离子选项D中CrO2-为黄色;③中在紫色石蕊试液变红的溶液,酸性溶液中,NO -具有强氧化性,
4 3
可将Fe2+氧化(但不能将Cl-氧化);④中加入过量NaOH溶液后Ba2+、 HCO -、OH- 会反应生成碳酸钡沉
3
淀;⑥酸性高锰酸钾溶液中:还原性的I-与氧化性强的酸性高锰酸钾会发生氧化还原反应。
5.(2021年6月浙江省普通高校招生选考化学试题)不能正确表示下列变化的离子方程式是
A.碳酸镁与稀盐酸反应:B.亚硫酸氢钠的水解:
C.锌溶于氢氧化钠溶液:
D.亚硝酸钠与氯化铵溶液受热反应:
【答案】A
【详解】A.碳酸镁与稀盐酸反应生成氯化镁、二氧化碳和水,反应的离子方程式为MgCO +2H+=Mg2+
3
+H O+CO↑,故A错误;
2 2
B.亚硫酸氢钠是弱酸的酸式盐,在溶液中水解生成亚硫酸和氢氧化钠,水解的离子方程式为HSO -+H O
3 2
HSO +OH-,故B正确;
2 3
C.锌与氢氧化钠溶液反应生成偏锌酸钠和氢气,反应的离子方程式为Zn+2OH-+2H O=[Zn(OH) ]-+H ↑,
2 4 2
故C正确;
D.亚硝酸钠溶液与氯化铵溶液共热反应生成氯化钠、氮气和水,反应的离子方程式为NO -+NH+
2 4
N↑+2H O,故D正确;
2 2
故选A。
6.(重庆市第八中学2021届高三高考适应性月考(五)化学试题)下列方程式书写正确的是
A.向FeSO 溶液中加入NH HCO 溶液得到FeCO 沉淀:Fe2++2 =FeCO ↓+CO ↑+H O
4 4 3 3 3 2 2
B.NaOH溶液与过量HC O 溶液反应:HC O+2OH-= +2H O
2 2 4 2 2 4 2
C.Fe (SO ) 溶液和过量HS反应的离子方程式:2Fe3++3H S=2FeS↓+6H++S↓
2 4 3 2 2
D.NH
4
Cl溶于D
2
O中: +D
2
O⇌NH
3
·D
2
O+H+
【答案】A
【详解】A.FeSO 与NH HCO 反应得到FeCO 沉淀:Fe2++2HCO -=FeCO ↓+CO ↑+H O,A正确;
4 4 3 3 3 3 2 2
B.过量HC O 溶液与碱反应应生成HC O-,离子反应式:HC O+OH-=HC O-+H O,故B错误;
2 2 4 2 4 2 2 4 2 4 2
C.Fe (SO ) 过量,不会生成FeS,正确的离子方程式:2Fe3++H S═2Fe2++S↓+2H+,故C错误;
2 4 3 2
D.NH
4
Cl溶于D
2
O中,NH
4
+水解使溶液呈酸性,水解离子方程式: NH
4
++D
2
O⇌ NH
3
·HDO +D+,故D错
误;
故选A。
7.(2021年高考全国乙卷化学试题)下列过程中的化学反应,相应的离子方程式正确的是A.用碳酸钠溶液处理水垢中的硫酸钙:
B.过量铁粉加入稀硝酸中:
C.硫酸铝溶液中滴加少量氢氧化钾溶液:
D.氯化铜溶液中通入硫化氢:
【答案】A
【详解】A.硫酸钙微溶,用碳酸钠溶液处理水垢中的硫酸钙转化为难溶的碳酸钙,离子方程式为:
,故A正确;
B.过量的铁粉与稀硝酸反应生成硝酸亚铁、一氧化氮和水,离子方程式应为:3Fe+8H++2N =3Fe2+
+2NO↑+4HO,故B错误;
2
C.硫酸铝溶液与少量氢氧化钾溶液反应生成氢氧化铝沉淀和硫酸钾,离子方程式应为:Al3++3OH-
=Al(OH) ↓,故C错误;
3
D.硫化氢为弱电解质,书写离子方程式时不能拆,离子方程式应为:Cu2++H S=CuS↓+2H+,故D错误;
2
答案选A。
8.下列过程中的化学反应,相应的离子方程式正确的是
A.用碳酸钠溶液处理水垢中的硫酸钙: +CaSO =CaCO +
4 3
B.酸性高锰酸钾溶液和草酸溶液反应:2 +16H++5 ═2Mn2++10CO ↑+8H O
2 2
C.硫酸铝溶液中滴加少量氢氧化钾溶液:Al3++4OH-= +2H O
2
D.氯化铜溶液中通入硫化氢:Cu2++S2-=CuS↓
【答案】A
【详解】A.硫酸钙微溶,用碳酸钠溶液处理水垢中的硫酸钙转化为难溶的碳酸钙,离子方程式为:CO2-
3
+CaSO =CaCO +SO2-,故A正确;
4 3 4
B.酸性高锰酸钾溶液和草酸溶液反应,草酸为弱酸:2MnO -+6H++5H C O═2Mn2++10CO ↑+8H O,故B
4 2 2 4 2 2
错误;
C.硫酸铝溶液与少量氢氧化钾溶液反应生成氢氧化铝沉淀和硫酸钾,离子方程式应为:Al3++3OH-=Al(OH) ↓,故C错误;
3
D.硫化氢为弱电解质,书写离子方程式时不能拆,离子方程式应为:Cu2++H S=CuS↓+2H+,故D错误;
2
答案选A。
9.下列离子方程式正确的是
A.磁性氧化铁溶于稀硝酸:3Fe2++4H++ =3Fe3++NO↑+2HO
2
B.用过量氨水吸收工业尾气中的SO :2NH ·H O+SO =2 + +H O
2 3 2 2 2
C.酸性溶液中KIO 与KI反应生成I: +I-+6H+=I +3H O
3 2 2 2
D.NaClO溶液中加入少量FeSO 溶液:2Fe2++ClO-+2H+=Cl-+2Fe3++H O
4 2
【答案】B
【详解】A.磁性氧化铁溶于稀硝酸,发生化学反应生成硝酸铁、一氧化氮和水,由于磁性氧化铁难溶于
水,在离子方程式中保留化学式,其离子方程式为3Fe O+28H++NO -═9Fe3++NO↑+14HO,故A错误;
3 4 3 2
B.用过量氨水吸收工业尾气中的SO ,发生化学反应生成亚硫酸铵和水,其离子方程式为
2
2NH ·H O+SO =2NH ++SO 2-+H O,故B正确;
3 2 2 4 3 2
C.酸性溶液中KIO 与KI反应生成I,其离子方程式为IO -+5I-+6H+═3I +3H O,故C错误;
3 2 3 2 2
D.NaClO溶液显碱性,NaClO溶液中加入少量FeSO 溶液,二者发生氧化还原反应,其离子方程式为
4
5HO+2Fe2++5ClO-=Cl-+2Fe(OH) ↓+4HClO,故D错误;
2 3
答案为B。
10.下列事实与所对应的离子方程式正确的是
A.室温下,测定醋酸钠溶液的pH > 7:CHCOONa === CH COO-+Na+
3 3
B.实验室用氯化铝溶液和氨水制备氢氧化铝:Al3+ +3OH- === Al(OH) ↓
3
C.用稀硫酸除去硫酸钠溶液中少量的硫代硫酸钠:NaSO + 2H+ === SO ↑ + S↓+ 2Na+ + H O
2 2 3 2 2
D.用碳酸钠溶液处理锅炉水垢中的硫酸钙:CaSO(s) + CO 2-(aq) === CaCO (s) + SO 2-(aq)
4 3 3 4
【答案】D
【详解】A、CHCOONa属于强碱弱酸盐,CHCOO-发生水解,CHCOO-+HO CHCOOH+OH-,
3 3 3 2 3
是溶液显碱性,故A错误;
B、NH ·H O是弱碱,不能拆写成离子形式,正确的是Al3++3NH ·H O=Al(OH) ↓+3NH +,故B错误;
3 2 3 2 3 4
C、NaSO 是可溶的强电解质,需要拆写成离子形式,正确的是SO2-+2H+=SO↑+S↓+HO,故C错误;
2 2 3 2 3 2 2
D、CaSO 是微溶物,CaCO 是难溶物,因此可以发生CaSO(s) + CO 2-(aq) = CaCO (s) + SO 2-(aq),故D正
4 3 4 3 3 4
确。11.下列表示对应化学反应的离子方程式正确的是
A.泡沬灭火器的原理 溶液与 溶液混合:
B.用惰性电极电解 溶液:
C.用稀硫酸除去硫酸钠溶液中少量的硫代硫酸钠:
D.用碳酸钠溶液处理锅炉水垢中的硫酸钙:
【答案】D
【详解】A.泡沫灭火器原理是Al (SO ) 溶液与NaHCO 溶液发生双水解反应生成二氧化碳,是一完全反
2 4 3 3
应,离子反应为Al3++3HCO-=Al(OH) ↓+3CO ↑,故A错误;
3 3 2
B.用惰性电极电解MgCl 溶液,阳极是氯离子失电子生成氯气,阴极是水中氢离子得电子生成氢气,同
2
时生成氢氧化镁沉淀,离子方程式为Mg2++2Cl-+2H O Mg(OH) ↓+Cl↑+H ↑,故B错误;
2 2 2 2
C.用稀硫酸除去硫酸钠溶液中少量的硫代硫酸钠,离子方程式:SO2-+2H+═SO ↑+S↓+H O,故C错误;
2 3 2 2
D.用碳酸钠溶液处理锅炉水垢中的硫酸钙,发生沉淀转化,离子方程式为:CaSO(s)+CO2-(aq)=CaCO (s)
4 3 3
+SO2-(aq),故D正确;
4
故选:D。
12.(辽宁省沈阳市郊联体2021届高三下学期一模考试化学试题)下列对应离子方程式书写正确的是
A. 溶于稀硝酸:
B.将 通入碱性 溶液中:
C.将 通入酸性 溶液中:
D.向 溶液中加入足量 溶液:
【答案】C
【详解】A.Cu O溶于硝酸被氧化,反应的离子方程式为: 3Cu O+2NO -+14H+=6Cu2++7H O+2NO↑,故A
2 2 3 2
错误;
B.将Cl 通入碱性KMnO 溶液中,离子方程式:Cl+2MnO-=2MnO- +2Cl-,故B错误;
2 2 4 2 2 4
C.将SO 通入酸性FeCl 溶液中,离子方程式:SO +2Fe3++2H O=2Fe2++SO2-+4H+,故C正确;
2 3 2 2 4D.向NH Fe (SO ) 溶液中加入足量Ba (OH) 溶液,离子方程式:NH ++Fe3++2SO2-+2Ba2++4OH-
4 4 2 2 4 4
=2BaSO ↓+Fe (OH) ↓+NH·H O,故D错误;
4 3 3 2
故选C。
13.(湖南省百校联考2021届高三8月联考化学试题)下列化学方程式中,不能正确表达反应颜色变化的
是
A.将灼热的铜丝(黑色)插入乙醇中,铜丝重新变光亮:2CuO 2Cu+O ↑
2
B.向洒落于地面的汞珠上撒少量硫粉,汞珠表面变黑:Hg+S=HgS
C.向AgCl浊液中通入HS,浊液变黑:2AgCl+H S=Ag S+2HCl
2 2 2
D.向氯气中通入氨气,黄绿色消失并产生白烟:3Cl+8NH=N+6NHCl
2 3 2 4
【答案】A
【详解】A.铜丝重新变亮是氧化铜和乙醇反应生成铜单质和乙醛,化学方程式为CuO+CHCHOH
3 3
Cu+CH CHO+H O,选项解释错误,故A符合题意;
3 2
B.向洒落于地面的汞珠上撒少量硫粉,汞珠表面变黑是因为Hg被S单质氧化生成硫化汞,选项解释正确,
故B不符合题意;
C.Ag S比AgCl更容易沉淀,且为黑色,所以向AgCl浊液中通入HS发生沉淀的转化2AgCl+H S=
2 2 2
Ag S+2HCl,浊液变黑,选项解释正确,故C不符合题意;
2
D.向氯气中通入氨气,氯气被氨气还原,生成氮气和氯化铵,选项解释正确,故D不符合题意;
综上所述答案为A。
14.某溶液中可能含有Na+、NH 、SO 、SO 、Cl-、Fe2+、Fe3+、CO 中的若干种,且各离子浓度相同,
为确定其组成现进行如下实验:
①向溶液中加入足量硝酸酸化的Ba(NO ) 溶液,产生白色沉淀,过滤
3 2
②向①中的滤液中加入足量的NaOH溶液,有沉淀产生,微热,有气体产生
下列说法正确的是
A.无法确定原溶液中是否存在SO
B.是否存在Na+需要通过焰色反应来确定
C.CO 肯定不存在,Fe2+、Fe3+至少有一种D.溶液中存在NH 、SO 、Cl-、Fe2+
【答案】D
【详解】A.由上分析,原溶液中不存在SO 2-,A项错误;
3
B.由上分析,原溶液中一定存在NH +、SO 2-,根据各离子浓度均相同及电荷守恒可知溶液中还存在
4 4
Fe2+、Cl-,不存在Na+,B项错误;
C.由上分析,CO2-肯定不存在,存在Fe2+,不存在Fe3+,C项错误;
3
D.由上分析,结合B选项,溶液中存在NH +、SO 2-、Cl-、Fe2+,D项正确;
4 4
答案选D。
15.(2021重庆高三模拟考试)能正确表示下列化学反应的离子方程式是()
A.电解氯化镁溶液:Mg2++2H O+2Cl- H↑+Cl↑+Mg(OH) ↓
2 2 2 2
B.硫酸镁溶液跟氢氧化钡溶液反应:SO +Ba2+=BaSO ↓
4
C.金属镁与醋酸反应,有氢气产生:Mg+2H+=Mg2++H ↑
2
D.碳酸钠溶液与盐酸反应,有气泡逸出:NaCO+2H+=2Na++H O+CO↑
2 3 2 2
【答案】A
【详解】A.用惰性电极电解氯化镁溶液的离子反应为Mg2++2H O+2Cl- H↑+Cl↑+Mg(OH) ↓,
2 2 2 2
故A正确;
B.硫酸镁溶液跟氢氧化钡溶液反应:Mg2++2OH-+SO2-+Ba2+═BaSO ↓+Mg(OH) ↓,故B错误;
4 4 2
C.醋酸为弱酸,应写成化学式,正确的离子方程式为 Mg+2CHCOOH=2CH COO-+Mg2++H ↑,故C错误;
3 3 2
D.碳酸钠溶液与盐酸反应,有气泡逸出的离子反应为CO2-+2H+═H O+CO↑,故D错误;
3 2 2
故选:A。
16.(2021届重庆市西南大学附属中月考)常温下,下列各组离子一定能在指定溶液中大量共存的是
A.滴加KSCN溶液显红色的溶液中:Fe2+、K+、NO 、I-
B.0.1 mol·L-1的NaCO 溶液中:Al3+、K+、NO 、SO
2 3
C. =10-12的溶液中:NH 、Cl-、NO 、SOD.水电离产生的c(H+)=10-12 mol·L-1的溶液中:Na+、NH 、Cl-、MnO
【答案】C
【详解】
A.滴加KSCN溶液显红色的溶液中含有Fe3+,会和I-发生氧化还原反应而不能大量共存,故A不符合题
意;
B.碳酸根和铝离子会发生双水解而不能大量共存,故B不符合题意;
C. =10-12的溶液显酸性,酸性溶液中四种离子相互之间不反应,也不与氢离子反应,可以大量
共存,故C符合题意;
D.水电离产生的c(H+)=10-12 mol·L-1的溶液中水的电离受到抑制,可能是酸溶液或碱溶液,碱溶液中铵
根不能大量存在,酸溶液中高锰酸根和氯离子发生氧化还原反应而不能大量共存,故D不符合题意;
答案为C。
17.下列指定化学反应的离子方程式不正确的是
A.方铅矿(PbS)遇CuSO 溶液生成铜蓝(CuS):Cu2+ + PbS=CuS + Pb2+
4
B.CaCl 溶液中依次通入足量NH 和少量CO:Ca2+ + 2NH + CO + H O=CaCO ↓+ 2NH
2 3 2 3 2 2 3
C.将Cu O与稀HNO 混合:3Cu O + 14H++ 2NO =6Cu2+ + 2NO↑+ 7HO
2 3 2 2
D.向碳酸氢钙溶液中加入足量石灰水:Ca2+ + HCO + OHˉ =CaCO ↓+ H O
3 2
【答案】A
【详解】
A.方铅矿(PbS)遇CuSO 溶液生成铜蓝(CuS),发生沉淀的转化,离子方程式应为Cu2+ +SO 2- +PbS CuS
4 4
+ PbSO ,故A错误;
4
B.CaCl 溶液中先通入NH 使溶液显碱性,之后通入少量CO 反应生成碳酸钙沉淀,离子方程式为Ca2+ +
2 3 2
2NH + CO + H O=CaCO ↓+ 2NH +,故B正确;
3 2 2 3 4
C.将Cu O与稀HNO 混合,硝酸根在酸性环境中将+1价的铜氧化,自身被还原成NO,结合电子守恒和
2 3
元素守恒可得离子方程式为3Cu O + 14H++ 2NO -=6Cu2+ + 2NO↑+ 7HO,故C正确;
2 3 2
D.碳酸氢钙溶液中加入足量石灰水,碳酸氢根完全,而氢氧根有剩余,所以离子方程式为Ca2+ + HCO +
OHˉ =CaCO ↓+ H O,故D正确;
3 2答案为A。
18.(河北省张家口市2021届高三上学期第一次质量检测化学试题)下列离子方程式的书写正确的是
A.氢氧化钠溶液与过量的碳酸氢钙溶液反应:OH-+Ca2++HCO =CaCO ↓+HO
3 2
B.大理石与醋酸反应:CO +2CHCOOH=2CHCOO-+HO+CO↑
3 3 2 2
C.氢氧化钡溶液和稀硫酸恰好中和:Ba2++OH-+H++SO =BaSO↓+HO
4 2
D.铜与稀硝酸的反应:Cu+4H++2NO =Cu2++2NO ↑+2HO
2 2
【答案】A
【详解】A.氢氧化钠溶液与过量的碳酸氢钙溶液反应,说明氢氧根离子全部反应完,则离子方程式为:
OH-+Ca2++HCO -=CaCO ↓+HO,A正确;
3 3 2
B.大理石与醋酸反应,大理石是难溶物,不能拆成离子形式,则离子方程式正确的是:CaCO +
3
2CHCOOH=Ca2++2CH COO-+HO+CO↑,B错误;
3 3 2 2
C.氢氧化钡溶液和稀硫酸恰好中和,要符合离子配比,应该是两个氢氧根离子,则离子方程式正确的是:
Ba2++2OH-+2H++SO 2-=BaSO↓+2HO,C错误;
4 4 2
D.铜与稀硝酸的反应生成的气体是一氧化氮气体,则离子方程式正确的是:3Cu+8H++2NO -=3Cu2++
3
2NO↑+4HO ,D错误 ;
2
故答案为:A。
19.下列化学用语解释事实或过程正确的是
A.Fe O 溶于过量稀硝酸中:Fe O+8H+=2Fe3++Fe2++4H O
3 4 3 4 2
B.乙酸和乙醇的酯化反应:CHCHOH+CH CO18OH CHCO18OCH CH+H O
3 2 3 3 2 3 2
C.用足量氨水吸收烟气中的二氧化硫:SO +2OH-= +H O
2 2
D.向少量Mg(OH) 悬浊液中加入适量的饱和NH Cl溶液,固体溶解:Mg(OH) +2 Mg2++2NH·H O
2 4 2 3 2
【答案】D
【详解】A.四氧化三铁被硝酸氧化生成硝酸铁和一氧化氮和水,故离子方程式错误,故A错误;
B.乙酸和乙醇反应生成乙酸乙酯和水,反应过程中乙酸中羟基上的氧原子到水分子中,故B错误;
C.氨水和二氧化硫反应,氨水是弱碱,不能拆成离子形式,故C错误;
D.氢氧化镁和氯化铵反应,生成氯化镁和氨水,离子方程式为Mg(OH) +2NH + Mg2++2NH·H O,故D
2 4 3 2正确。
故选D。
20.(重庆市西南大学附属中学校高2021届高三第二次月考化学试题)能正确表示下列变化的离子方程式
是
A.电解MgCl 溶液:Mg2++2Cl- Mg+Cl ↑
2 2
B.草酸(H C O)滴入KMnO 酸性溶液中:5C O +2MnO +16H+=10CO ↑+2Mn2++8H O
2 2 4 4 2 2 2
C.Ca(ClO) 溶液中滴入少量的SO :Ca2++2ClO-+SO+H O=CaSO+2HClO
2 2 2 2 3
D.FeSO 溶液与NaHCO 溶液混合生成FeCO 沉淀:Fe2++2HCO =FeCO ↓+H O+CO↑
4 3 3 3 2 2
【答案】D
【详解】
A.电解熔融MgCl :Mg2++2Cl- Mg+Cl ↑,电解MgCl 溶液生成氢气、氯气、氢氧化镁,故A错误;
2 2 2
B.草酸是弱酸,草酸(H C O)滴入KMnO 酸性溶液中,反应的离子方程式是5HC O+2MnO-
2 2 4 4 2 2 4 4
+6H+=10CO ↑+2Mn2++8H O,故B错误;
2 2
C.Ca(ClO) 溶液中滴入少量的SO ,反应的离子方程式是 Ca2+ + 3ClO- + SO + H O = CaSO ↓ + Cl- +
2 2 2 2 4
2HClO,故C错误;
D.FeSO 溶液与NaHCO 溶液混合生成FeCO 沉淀、硫酸钠、水、二氧化碳,反应的离子方程式是Fe2+
4 3 3
+2HCO-=FeCO ↓+H O+CO↑,故D正确;
3 3 2 2
答案选D。
21.(重庆市西南大学附属中学校高2021届高三第二次月考化学试题)常温下,下列各组离子在指定溶液
中能大量共存的是
A.澄清透明的溶液中:Na+、H+、MnO 、O
B. =1×10-12的溶液中:K+、Na+、CO 、AlO
C.pH=7的溶液中:Fe3+、Cu2+、NO 、SO
D.能使甲基橙变红的溶液中:Na+、Ca2+、S2-、SO【答案】B
【详解】A.O2-遇水发生剧烈反应,不能在水溶液中存在,与酸也反应,不能大量共存,故A不选;
2
B.K =c(H+)c(OH-)=1×10-14,则 =1×10-12的溶液中c(H+)=10-13mol/L,c(OH-)=1×10-1mol/L,该溶液呈
w
碱性,溶液中存在大量氢氧根离子,K+、Na+、CO2-、AlO-之间不反应,都不与氢氧根离子反应,在溶液
3 2
中不能大量共存,故B选;
C.pH=7的溶液中Fe3+会发生水解,不能大量存在,故C不选;
D.能使甲基橙变红的溶液呈酸性,溶液中存在大量氢离子,S2-、SO 2-会与氢离子反应,在酸性溶液中不
3
能大量共存,故D错误;
故选B。
22.下列有关反应的离子方程式书写正确的是
A.澄清石灰水中加入足量小苏打:2HCO +2OH-+Ca2+=CaCO ↓+CO +2H O
3 2
B.FeO与稀硝酸反应:FeO+2H+=Fe2++H O
2
C.将少量SO 通入NaC1O溶液中:SO +ClO-+H O=SO +Cl-+2H+
2 2 2
D.向FeI 溶液中通人过量氯气:2Fe2++2I-+2Cl=2Fe3++I +4Cl-
2 2 2
【答案】A
【详解】A.小苏打过量,故钙离子和氢氧根以2:1完全反应,离子方程式为:2HCO +2OH-
+Ca2+=CaCO ↓+CO +2H O ,A正确;
3 2
B.FeO与稀硝酸发生氧化还原反应,离子方程式为: ,B错误;
C.将少量SO 通入NaC1O溶液中先发生氧化还原反应生成硫酸和氯化钠,由于次氯酸钠过量,生成的氢
2
离子与次氯酸根继续反应生成次氯酸,离子方程式为:SO +3ClO-+H O=SO +Cl-+2HClO,C错误;
2 2
D.向FeI 溶液中通人过量氯气,碘离子和亚铁离子按2:1被完全氧化,离子方程式为:2Fe2++4I-
2
+3Cl=2Fe3++2I +6Cl-,D错误;
2 2
故选A。
23.(湖南省长郡十五校2021届高三下学期第二次联考化学试题)下列反应的离子方程式书写正确的是
A.将少量氯气通人Fel 溶液中;
2B.向稀硝酸银溶液中滴加稀氨水至过量:
C.往2.0mL。1.0mol/L的AlCl ,溶液中加入7.0mL1.0mol/L的NaOH溶液充分反应:
3
D.将等浓度的NaHCO 溶液和Ba(OH) 溶液等体积充分混合:
3 2
【答案】C
【详解】A.将少量氯气通入FeI 溶液中,Cl 先与I-反应,选项A错误;
2 2
B.向稀硝酸银溶液中滴加稀氨水至过量反应应为 ,选项B错误;
C.由题可得AlCl 与NaOH的物质的量之比为2:7,故反应为 ,
3
选项C正确;
D.将等浓度的NaHCO 溶液和Ba(OH) 溶液等体积充分混合,NaHCO 与Ba(OH) 的物质的量之比为1:1,
3 2 3 2
故反应应为 ,选项D错误。
答案选C。
24.下列用于解释事实的化学用语书写正确的是
A.氯气溶于水:Cl
2
+H
2
O⇌2H++Cl-+ClO-
B.明矾[KAl(SO
4
)
2
∙12H
2
O]作净水剂:Al3++3H
2
O⇌ Al(OH)
3
↓+3H+
C.铜作电极电解NaCl溶液初始阶段:Cu+2H O Cu(OH) + H ↑
2 2 2
D.饱和NaCO 溶液处理水垢中的CaSO:Ca2++CO =CaCO ↓
2 3 4 3
【答案】C
【详解】A.次氯酸是弱酸不能拆,Cl
2
+H
2
O⇌H++Cl-+HClO,A用语错误;
B.明矾水解生成氢氧化铝胶体,不是沉淀,Al3++3H
2
O⇌ Al(OH)
3
(胶体)+3H+,B用语错误;
C.Cu作阳极,参与反应,失电子生成铜离子,阴极水得电子生成氢气和氢氧根离子,铜离子与氢氧根离
子反应生成氢氧化铜,总反应式Cu+2H O Cu(OH) +H ↑,C用语正确;
2 2 2D.CaSO 为微溶物,在离子方程式中也不能拆分,正确的离子方程式为CaSO+CO =CaCO +SO ,D用
4 4 3
语错误;
答案为C。
25.对下列物质所含离子的检验中,作出的判断错误的是
A.灼烧白色粉末,火焰呈黄色,证明原粉末中一定有Na+,可能有K+
B.某溶液与浓NaOH溶液共热,若产生使湿润红色石蕊试纸变蓝的气体,则说明原溶液中一定存在NH
C.向某溶液中加入足量稀盐酸,静置后取上层清液再加BaCl 溶液,产生白色沉淀,说明原溶液中一定含
2
有SO
D.向某溶液中加入稀盐酸,产生的无色无味气体能使澄清石灰水变浑浊,说明原溶液中一定含有CO
【答案】D
【详解】A.灼烧白色粉末,火焰呈黄色,证明原粉末中一定有Na+,但由于没有通过蓝色钴玻璃观察火
焰,因此不能确定溶液中是否含有K+,则溶液中可能有K+也可能不含有K+,A正确;
B.某溶液与浓NaOH溶液共热,若产生使湿润红色石蕊试纸变蓝的气体,说明产生的气体是碱性气体
NH ,则原溶液中一定存在NH ,B正确;
3
C.向某溶液中加入足量稀盐酸,静置后取上层清液再加BaCl 溶液,由产生白色沉淀是BaSO,则说明原
2 4
溶液中一定含有SO ,C正确;
D.向某溶液中加入稀盐酸,产生的无色无味气体能使澄清石灰水变浑浊,说明原溶液中可能含有CO ,
也可能含有 ,D错误;
故合理选项是D。
26.已知某溶液仅含有 5 种离子(不考虑水的电离),其含量均为 1mol,它们可能是 K+、Ba2+、Fe2+、
Al3+、Fe3+、Mg2+、OH-、HCO -、CO2-、Cl-、NO -和 SO 2-中的 5 种。为确定该溶液中所含的离子,
3 3 3 4
向该溶液中加入足量稀盐酸,观察到有无色气体产生,且经确认反应前后溶液中的阴离子组成成分没有变
化。则下列说法正确的是( )
A.原溶液中可能含有K+,将产生的无色气体通入澄清石灰水中,石灰水变浑浊B.原溶液中一定含有 Cl-和 NO -,可能含有 SO 2-,反应生成的无色气体遇空气变红棕色
3 4
C.原溶液中所含的阳离子为 Fe2+、Mg2+,加入稀盐酸所发生的反应为3Fe2++4H++NO -=3Fe3++NO↑+
3
2HO
2
D.若向原溶液中加入过量NaOH 溶液,将所得沉淀过滤、洗涤、灼烧到恒重,得到的固体质量为200 g
【答案】C
【分析】加入足量稀盐酸,有无色气体产生,且反应前后溶液中的阴离子种类没有变化,生成的气体应该
为NO,说明原溶液中含有Cl-和NO -,肯定无OH-、HCO -和CO2-;无色气体是NO,而阳离子中一定含
3 3 3
有Fe2+,因原溶液中含有5种等物质的量的离子,根据电荷守恒则阴离子还含有SO 2-,阳离子还含有Mg2
4
+。即含有1 mol Cl-,1 mol NO -,1 mol SO 2-,1 mol Fe2+,1 mol Mg2+。
3 4
【详解】A.原溶液中不含有K+,生成的气体是NO,不能使石灰水变浑浊,故A错误。
B.原溶液中一定含有 Cl-和 NO -,一定含有 SO 2-,反应生成的无色气体NO遇空气变红棕色,故B错
3 4
误。
C.Fe2+具有还原性,NO -在酸性条件下具有氧化性,发生氧化还原反应3Fe2++4H++NO -=3Fe3++NO↑
3 3
+2HO,故C正确。
2
D.向原溶液中加入过量NaOH溶液,生成的沉淀经过过滤、洗涤、灼烧得到0.5 molFe O 和1 molMgO,
2 3
共120 g,故D项错误。本题选C。
27.(重庆市2021年普通高中学业水平选择考适应性测试化学试题)下列指定反应的离子方程式正确的是
A.氯化铁溶液腐蚀铜箔:2Fe3++Cu= 2Fe2++Cu2+
B.氢氧化钠溶液吸收氯气:Cl+OH- = Cl- +HClO
2
C.氯化铝溶液与浓氨水混合:A13++4NH·H O= +4 +2H O
3 2 2
D.氢氧化镁固体溶解于氯化铵溶液:Mg(OH) +2H+=Mg2++2H O
2 2
【答案】A
【详解】A. 氯化铁溶液腐蚀铜箔得到氯化亚铁和氯化铜:2Fe3++Cu= 2Fe2++Cu2+,A正确;
B. 氢氧化钠溶液吸收氯气生成氯化钠、次氯酸钠和水: ,B错误;
C. 氯化铝溶液与浓氨水混合生成氢氧化铝沉淀: A13++3NH·H O= +3 +2H O ,C错误;
3 2 2
D. 氢氧化镁固体溶解于氯化铵溶液:可能是铵根水解生成的H+中和氢氧化镁电离出的OH−,导致沉淀
溶解,也有可能是铵根与氢氧化镁电离出的OH−生成弱电解质一水合氨, 导致沉淀溶解,Mg(OH) +2
2
=Mg2++2NH·H O,D错误;
3 2答案选A。
28.(浙江省北斗星盟2021-2022学年高二下学期5月阶段性联考化学试题)下列过程中的化学反应所对
应的离子方程式正确的是:
A.苯酚钠溶液中通入少量 :
B.将水垢中的 浸泡在饱和碳酸钠溶液中:
C.向酸性高锰酸钾溶液中滴加少量双氧水褪色:
D.Fe与稀硝酸反应,当 时:
【答案】D
【详解】A.由于酸性:HCO>C HOH> ,根据以强制弱的原理,苯酚钠溶液中通入少量CO 的离
2 3 6 5 2
子方程式为: ,故A项错误;
B.CaSO 溶解度大于碳酸钙,所以将水垢中的CaSO 浸泡在饱和碳酸钠溶液中,发生沉淀转换,发生的
4 4
离子方程式为 ,故B项错误;
C.向酸性高锰酸钾溶液中滴加少量双氧水,发生氧化还原反应,溶液褪色,离子方程式为
,故C项错误;
D.Fe与稀硝酸反应,当n(Fe):n(HNO )=1:2时,硝酸不足反应生成硝酸亚铁,离子方程式为
3
,故D项正确;
答案选D。
29.(河南省部分重点高中2021-2022学年高三上学期12月适应性检测化学试题)下列过程中的化学反应
对应的离子方程式正确的是
A.用K[Fe(CN) ]溶液检测FeCl 溶液中的Fe2+:
3 6 2
B.向稀硫酸中加入少量金属铜:C.用醋酸溶液处理水垢中的氢氧化镁:
D.向 溶液中滴加过量Ba(OH) 溶液:
2
【答案】A
【详解】A.Fe2+与[Fe(CN) ]3-反应生成难溶物Fe [Fe(CN) ],A项正确;
6 3 6 2
B.铜与稀硫酸不反应,B项错误;
C.醋酸是弱电解质,应写分子式,C项错误;
D.Ba(OH) 溶液过量时Al3+应转化为 ,D项错误;
2
故选A。
30.(湖南省常德市2021-2022学年高三上学期期末检测化学试题)对下列粒子组在溶液中能否大量共存
的判断和分析均正确的是
选项 离子组 判断与分析
A
、 、 、 不能大量共存,主要原因是 与 反应产生 沉淀
B 、 、 、 不能大量共存,因发生反应:
C 、 、 、 不能大量共存, 会催化 分解
D 、 、 、 能大量共存
A.A B.B C.C D.D
【答案】C
【详解】A.不能大量共存,主要原因是 与 发生双水解反应,反应生成氢氧化铝和二氧化碳,故
A错误;
B.不能大量共存,因发生反应: ,故B错误;
C.不能大量共存, 会催化 分解生成水和氧气,故C正确;
D.不能大量共存,酸性高锰酸钾能将乙醇氧化,故D错误;故选C。
31.(重庆市九龙坡区2022届高三上学期期中考试化学试题)氯气是一种重要的工业原料,液氯储存区贴
有的说明卡如下:
包装 钢瓶
储运要
远离金属粉末、氨、烃类、醇类物质;设置氯气检测仪
求
泄漏处
NaOH或 溶液吸收
理
下列解释事实的方程式错误的是A.氯气用于自来水消毒:
B.电解饱和食盐水制取 :
C.浓氨水检验泄漏的氯气,产生白烟:
D.氯气“泄漏处理”中 溶液的作用:
【答案】D
【详解】A. ,HClO具有强氧化性可用于杀菌消毒,A正确;
B.电解饱和食盐水生成氢气、氯气和氢氧化钠,电解方程式为2Cl- +2H O 2OH-+ H ↑+Cl↑,B正
2 2 2
确;
C.氯气具有强氧化性,可氧化氨气生成氮气,同时因生成氯化铵而产生白烟,方程式为8NH + 3Cl ==
3 2
6NH Cl + N ,C正确;
4 2
D.氯气与亚硫酸氢钠溶液发生氧化还原反应生成硫酸根离子,反应的离子方程式为
,D错误;
故答案选D。
32.(重庆市九龙坡区2022届高三上学期期中考试化学试题)某试液中只可能大量含有 、 、、 、 、 、 、 中的若干种离子,且所含离子浓度均相等(忽略单一水解),实验如
下,下列说法正确的是
A.原溶液中大量存在 、 、 、
B.沉淀A为 ,沉淀C为 、
C.滤液X中大量存在的阳离子有 、 和
D.无法确定原试液中是否大量含有 、
【答案】A
【分析】由题干信息可知,加入过量稀硫酸无明显变化,说明无 、Ba2+和 ,加入硝酸钡有气体,
说明有亚铁离子存在且被氧化,沉淀为硫酸钡,加入NaOH有气体,说明存在铵根离子,气体为氨气,沉
淀B为红褐色氢氧化铁沉淀,通入少量CO 产生沉淀,先与OH-、Ba2+反应,沉淀C为碳酸钡,不能说明
2
存在Al3+,因为存在的离子浓度均为相同,从电荷的角度出发,只能含有 、Fe2+、Cl-、 才能保证
电荷守恒,Na+必然不能存在,据此分析解题。
【详解】A.由分析可知,原溶液中大量存在 、 、 、 ,A正确;
B.由分析可知,沉淀A为 ,沉淀C为 ,B错误;
C.由分析可知,加入硝酸钡有气体,说明有亚铁离子存在且被氧化,故滤液X中大量存在的阳离子有
、 和 ,C错误;
D.由分析可知,原试液中一定含有大量的 ,一定不含 ,D错误;
故答案为:A。
33.(重庆市第一中学2021-2022学年高三上学期第三次月考化学试题)下列离子方程式正确的是A.向铬酸钾溶液中滴加几滴浓硫酸:
B.铅蓄电池充电时,阴极的电极反应:
C.向氯化银悬浊液中滴加碘化钠溶液:
D.亚硫酸在水中的电离方程式:
【答案】A
【详解】A.向铬酸钾溶液中滴加几滴浓硫酸,氢离子浓度增大,发生反应
,故A正确;
B.铅蓄电池充电时,阴极的电极反应 ,故B错误;
C.向氯化银悬浊液中滴加碘化钠溶液,氯化银转化为碘化银沉淀, ,故
C错误;
D.亚硫酸是弱酸,在水溶液中分步电离,亚硫酸在水中的电离方程式 、
,故D错误;
选A。
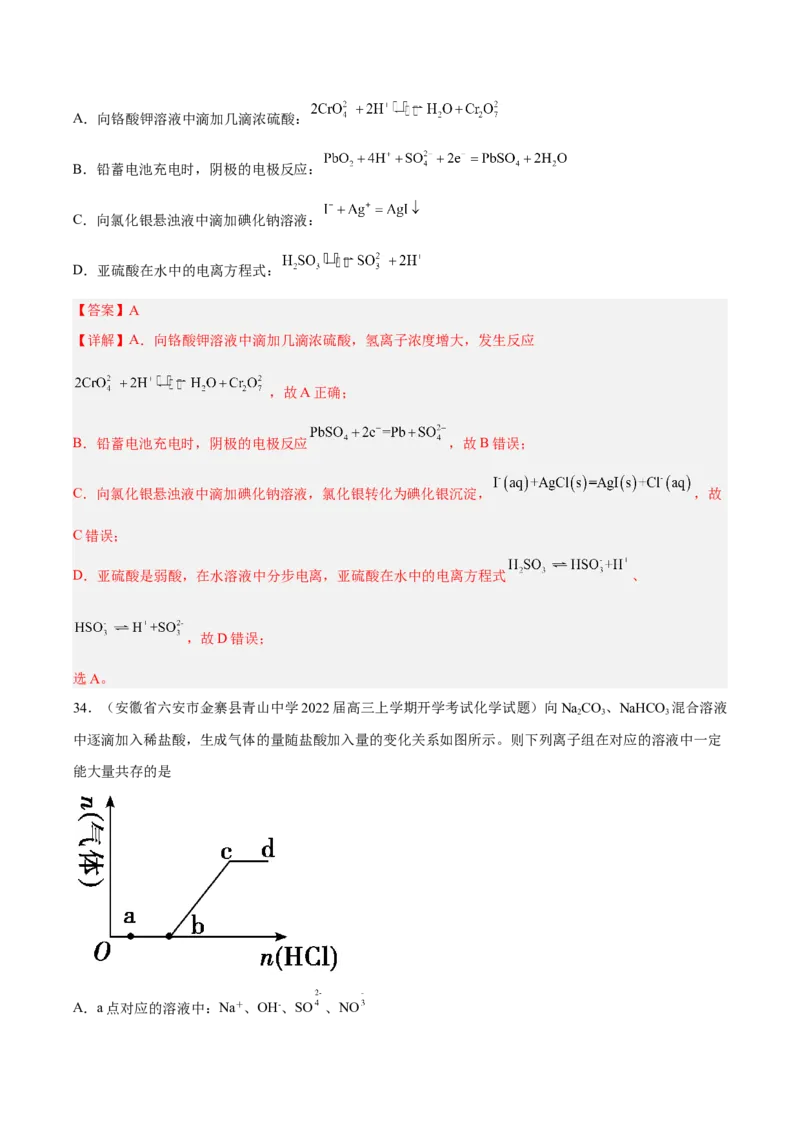
34.(安徽省六安市金寨县青山中学2022届高三上学期开学考试化学试题)向NaCO、NaHCO 混合溶液
2 3 3
中逐滴加入稀盐酸,生成气体的量随盐酸加入量的变化关系如图所示。则下列离子组在对应的溶液中一定
能大量共存的是
A.a点对应的溶液中:Na+、OH-、SO 、NOB.b点对应的溶液中:K+、Ca2+、AlO 、Cl-
C.c点对应的溶液中:Na+、Ca2+、NO 、Cl-
D.d点对应的溶液中:F-、NO 、Fe2+、Ag+
【答案】C
【分析】b点前没有气体产生,所以O-b段的反应为CO +H+=HCO
【详解】A.a点滴入盐酸时没有气体产生,且直到b点开始产生气体,则a点溶液中溶质为NaCO、
2 3
NaHCO ,HCO 不能和氢氧根大量共存,A不符合题意;
3
B.b点时开始产生气体,说明CO 恰好完全反应,此时溶液中的溶质为NaHCO ,HCO 与AlO 可以反
3
应生成氢氧化铝沉淀,B不符合题意;
C.c点恰好不再产生气体,溶质为NaCl,四种离子相互之间不反应,也不与氯化钠反应,可以大量共存,
C符合题意;
D.d盐酸过量,溶质为NaCl和HCl,F-和H+结合生成弱电解质HF,Ag+和氯离子生成沉淀,酸性环境中
NO 可以把Fe2+氧化,D不符合题意;
综上所述答案为C。
35.(天津市滨海新区七所重点学校2021-2022学年高三下学期联考化学试题)下列离子方程式的书写及
评价均合理的是
选
离子方程式 评价
项
将2molCl 通入含有1molFeI 的溶液中:2Fe2++2I-+2Cl=2Fe3+ 正确:Cl 过量,可将Fe2+、
A 2 2 2 2
+I +4Cl- I-均氧化
2
正确:酸与碱反应生成盐和
B 向Fe(OH) 中加入氢碘酸溶液:Fe(OH) +3H+=Fe3++3H O
3 3 2 水
正确:说明酸性HSO 强于
C 过量SO 通入NaClO溶液中:SO +H O+ClO-=HClO+HSO 2 3
2 2 2 HClO
已知酸性:HCO>HCN>HCO 。则向NaCN溶液中通入少量 正确:NaCN和CO 的反应
D 2 3 2
产物与对应酸性强弱有关
的CO 时:CN-+CO +H O=HCN+HCO
2 2 2A.A B.B C.C D.D
【答案】D
【详解】A.将2molCl 通入到含1molFeI 的溶液中,氯气过量,亚铁离子和碘离子都被氧化,正确的离子
2 2
方程式为:2Fe2++4I-+4Cl=2Fe3++6Cl-+2I ,故A错误;
2 2
B.铁离子具有氧化性,碘离子具有还原性,两者发生氧化还原反应生成亚铁离子和碘单质,反应的离子
反应为:2Fe(OH) +2I-+6H+═2Fe2++I +6H O,故B错误;
3 2 2
C.过量SO 通入到NaClO溶液中,SO 有强还原性,ClO-有强氧化性,发生氧化还原反应,正确的离子
2
方程式为:SO +H O+ClO-=2H++SO +Cl-,故C错误;
2 2
D.酸性:HCO>HCN>HCO ,则向NaCN溶液中通入少量的CO 时的离子方程式为:CN-
2 3 2
+CO +H O═HCN+ HCO ,故D正确;
2 2
故选:D。
36.(安徽省百校联盟2021-2022学年高三上学期12月联考化学试题)下列各项中,对应的离子方程式书
写正确的是
A.向 溶液中加入过量浓氨水:
B.向 溶液中加入少量 溶液制备
C.向 溶液中通入少量
D.向 溶液中加入过量 溶液:
【答案】B
【详解】A.氨水过量,故 应转化为 ,A错误;
B.根据原子守恒和质子守恒可知离子方程式书写正确,B正确;C.Cl 少量,即NaSO 过量,则产物中的 会继续与 反应生成 ,C错误;
2 2 3
D.漏写了 和 生成BaSO 沉淀的反应,D错误;
4
故答案为:B。
37.(重庆市主城区2022届高三第二次学业教学质量抽测化学试题)某稀溶液中含有HCO 、SO 、CO
、CHCOO-、NH 、Na+等多种离子。若向其中加入适量的NaO 固体后,原溶液中离子浓度(不考虑水
3 2 2
解)基本保持不变的微粒是
A.SO B.CO C.CHCOO- D.NH
3
【答案】C
【详解】向稀溶液中加入过氧化钠后, ,钠离子浓度增大;亚硫酸根离子被
氧气氧化,浓度变小;碳酸氢根与氢氧根反应: ,碳酸氢根离子浓度减小,碳
酸根离子浓度增大;铵根离子与生成的氢氧根离子反应: ,浓度减小,只有醋酸
根离子浓度不变,故选C。
38.(重庆一中2021-2022学年高三下学期5月月考化学试题)表示下列反应的离子方程式正确的是
A.硫酸铝溶液中加入足量氢氧化钡:
B.二氧化碳通入氯化钙溶液:
C.用足量次氯酸钙溶液吸收二氧化硫:
D.石灰乳和醋酸溶液混合:
【答案】C
【详解】A.硫酸铝溶液中加入足量氢氧化钡: ,A
错误;
B.二氧化碳通入氯化钙溶液不发生反应,B错误;C.用足量次氯酸钙溶液吸收二氧化硫,发生氧化还原反应同时生成次氯酸,离子方程式正确,C正确;
D.石灰乳主要成分为氢氧化钙,不可拆,离子方程式为: ,
D错误;
故选C。
39.(重庆市2022届高三质量调研抽查第三次考试化学试题)下列反应对应的离子方程式书写正确的是
A.向 溶液中通入过量 制 :
B.将Na单质放入 中:
C. 的悬浊液中同时加入NaOH溶液和 制 :
D.用惰性电极电解NaCl溶液:
【答案】A
【详解】A.过量二氧化碳反应生成碳酸氢钠,向 溶液中通入过量 :
,故A正确;
B.将Na单质放入 中离子方程式为: ,故B错误;
C. 的悬浊液中同时加入NaOH溶液和 离子方程式为 :
,故C错误;
D.用惰性电极电解NaCl溶液离子方程式: ,故D错误;
故答案为A。
40.(湖南省衡阳市2021-2022学年高一下学期期中考试化学试题)宏观辨识与微观探析是化学学科核心
素养之一。下列实验或原理对应的离子方程式书写错误的是A.实验室盛放NaOH溶液的试剂瓶用磨砂玻璃塞,可能发生:SiO+2OH-=SiO +H O
2 2
B.亚硫酸钠溶液与足量氯气反应:SO +Cl+H O=SO +2Cl-+2H+
2 2
C.用醋酸除去水垢中的碳酸钙:CaCO +2H+=Ca2++CO ↑+H O
3 2 2
D.同物质的量浓度同体积的NH HSO 溶液与NaOH溶液混合:H++OH-=H O
4 4 2
【答案】C
【详解】A. 实验室盛放NaOH溶液的试剂瓶用磨砂玻璃塞,可能发生二氧化硅溶于碱生成硅酸盐:
SiO+2OH-=SiO +H O,故A正确;
2 2
B. 亚硫酸钠溶液与足量氯气反应生成硫酸:SO +Cl+H O=SO +2Cl-+2H+,故B正确;
2 2
C. 醋酸是弱电解质,用醋酸除去水垢中的碳酸钙:CaCO +2CH COOH=Ca2++CO ↑+H O+2CHCOO-,故
3 3 2 2 3
C错误;
D. 同物质的量浓度同体积的NH HSO 溶液与NaOH溶液混合后,先发生中和反应,即氢氧根离子中和
4 4
氢离子:H++OH-=H O,故D正确;
2
故选C。
41.(黑龙江省青冈县第一中学校2022届高三上学期期初考试化学试题)常温下,下列各组离子在指定溶
液中一定能大量共存的是
A.使甲基橙变红的溶液中:Na+、Cl-、CHCOO−、Fe2+
3
B.水电离的OH-浓度为10-12mol·L-1的溶液中:Mg2+、NH 、AlO 、SO
C.无色溶液中:Al3+、NO 、Cl-、SO
D.c(H C O)=0.5mol·L−1溶液中:Na+、K+、MnO 、Cl-
2 2 4
【答案】C
【详解】A.使甲基橙变红的溶液为酸性溶液,酸性溶液中醋酸根离子会与氢离子反应生成醋酸,不能大
量共存,故A错误;
B.铵根离子和偏铝酸根离子在溶液中会发生双水解反应,不能大量共存,故B错误;
C.Al3+、NO 、Cl-、SO 四种离子在无色溶液中不发生任何反应,能大量共存,故C正确;
D.草酸溶液中,具有强氧化性的高锰酸根离子会与草酸溶液发生氧化还原反应,不能大量共存,故D错误;
故选C。
42.(北京市海淀区2021-2022学年高三上学期期末考试化学试题)下列方程式与所给事实不相符的是
A.浓硝酸用棕色瓶保存:
B.过量碳酸氢钠与氢氧化钡溶液反应:
C.硫酸铵溶液显酸性:
D.电解精炼铜的阳极反应:
【答案】D
【详解】A.硝酸见光易分解,生成二氧化氮、氧气和水,故用棕色瓶保存,A正确;
B.过量的碳酸氢钠与氢氧化钡反应生成碳酸钡、碳酸钠和水,改成离子反应正如B选项,B正确;
C.硫酸铵溶液中铵根离子水解生成一水合氨和氢离子,C正确;
D. 电解精炼铜的阳极反应是Cu-2e−=Cu2+,D错误;
故选D。