文档内容
第八篇 化学实验
专项 55 “减压操作”微应用
化学实验常用到“减压操作”,也频频出现实验综合题中,以考查考生分析问题解决问题能力。主要
包括两类:
(1)以降低液体沸点为目的。液体沸腾也就是在某一温度条件下液体蒸汽压等于外压,外压降低则饱和
蒸汽压降低,导致液体沸点降低。即液体化合物的沸点与外界压力密切相关。当外界压力降低时,液体沸
腾温度就会降低,即沸点下降。这种“减压”共四类:减压蒸馏(减压分馏);减压蒸发(减压浓缩);减压干
燥(真空干燥);水蒸气蒸馏。
(2)以液体顺利“流出”为目的。通过改变盛装液体容器的内外气压,产生压力差,利用气压差使容器
中的液体顺利“流出”。这种“减压”常见共三类:喷泉实验;减压过滤(吸滤或抽滤);恒压漏斗。
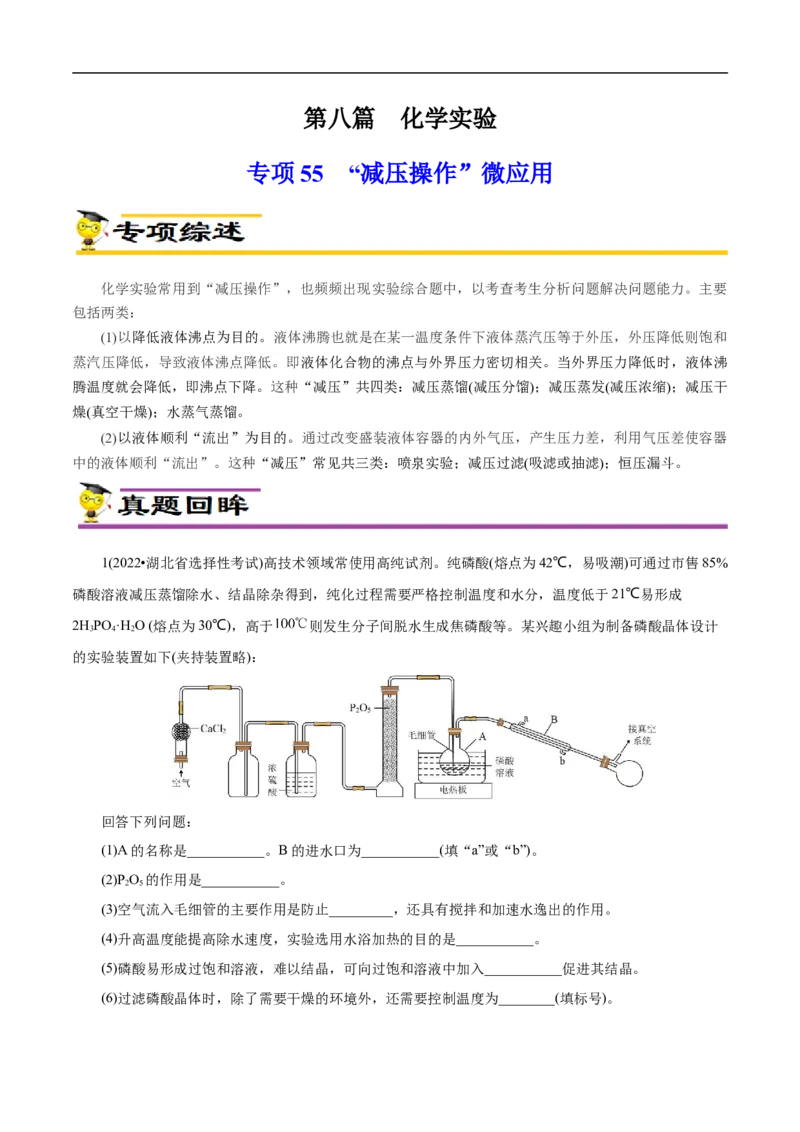
1(2022•湖北省选择性考试)高技术领域常使用高纯试剂。纯磷酸(熔点为42℃,易吸潮)可通过市售85%
磷酸溶液减压蒸馏除水、结晶除杂得到,纯化过程需要严格控制温度和水分,温度低于21℃易形成
2HPO ·H O (熔点为30℃),高于 则发生分子间脱水生成焦磷酸等。某兴趣小组为制备磷酸晶体设计
3 4 2
的实验装置如下(夹持装置略):
回答下列问题:
(1)A的名称是___________。B的进水口为___________(填“a”或“b”)。
(2)P O 的作用是___________。
2 5
(3)空气流入毛细管的主要作用是防止_________,还具有搅拌和加速水逸出的作用。
(4)升高温度能提高除水速度,实验选用水浴加热的目的是___________。
(5)磷酸易形成过饱和溶液,难以结晶,可向过饱和溶液中加入___________促进其结晶。
(6)过滤磷酸晶体时,除了需要干燥的环境外,还需要控制温度为________(填标号)。A.<20℃ B.30~35℃ C.42~100℃
(7)磷酸中少量的水极难除去的原因是___________。
【答案】(1) 圆底烧瓶 b (2)干燥气体
(3)溶液沿毛细管上升 (4)使溶液受热均匀
(5)磷酸晶体 (6)C (7)磷酸可与水分子间形成氢键
【解析】空气通过氯化钙除水,经过安全瓶后通过浓硫酸除水,然后通过五氧化二磷,干燥的空气流
入毛细管对烧瓶中的溶液进行搅拌,同时还具有加速水逸出和防止溶液沿毛细管上升的作用,将85%磷酸
溶液进行减压蒸馏除水、结晶除杂得到纯磷酸。 (1)由仪器构造可知,仪器A为圆底烧瓶,仪器B为直形
冷凝管,泠凝水应从b口近、a口出,形成逆流冷却,使冷却效果更好。(2)纯磷酸制备过程中要严格控制
温度和水分,因此五氧化二磷的作用为干燥气体。(3)空气流入毛细管可以对烧瓶中的溶液进行搅拌,使受
热均匀,同时还具有加速水逸出和防止溶液沿毛细管上升的作用。(4)升高温度能提高除水速度,而纯磷酸
制备过程中要严格控制温度,水浴加热可以避免直接加热造成的过度剧烈与温度的不可控性,使溶液受热
均匀。(5)过饱和溶液暂时处于亚稳态,当加入一些固体的晶体或晃动时可使此状态失去平衡,过多的溶质
就会结晶,因此可向磷酸的过饱和溶液中加入磷酸晶体促进其结晶。(6)纯磷酸纯化过程中,温度低于21℃
易形成2HPO ·H O (熔点为30℃),高于1000℃则发生分子间脱水生成焦磷酸,纯磷酸的熔点为42℃,因
3 4 2
此过滤磷酸晶体时,除了需要干燥的环境外,还需要控制温度为42 100℃,答案选C。(7)磷酸的结构式为:
∼
,分子中含羟基,可与水分子间形成氢键,因此磷酸中少量的水极难除去。
2.(2022·浙江省1月选考)某兴趣小组用四水醋酸锰[(CH COO) Mn·4H O]和乙酰氯(CHCOCl)为原料制
3 2 2 3
备无水二氯化锰,按如图流程开展了实验(夹持仪器已省略):已知:①无水二氯化锰极易吸水潮解,易溶于水、乙醇和醋酸,不溶于苯。
②制备无水二氯化锰的主要反应:(CHCOO) Mn+CHCOCl MnCl ↓+2(CH COO) O。
3 2 3 2 3 2
③乙酰氯遇水发生反应:CHCOCl+H O→CH COOH+HCl。
3 2 3
请回答:
(1)步骤Ⅰ:所获固体主要成分是_________(用化学式表示)。
(2)步骤Ⅰ在室温下反应,步骤Ⅱ在加热回流下反应,目的分别是________。
(3)步骤Ⅲ:下列操作中正确的是_________。
A.用蒸馏水润湿滤纸,微开水龙头,抽气使滤纸紧贴在漏斗瓷板上
B.用倾析法转移溶液,开大水龙头,待溶液快流尽时再转移沉淀
C.用乙醇作为洗涤剂,在洗涤沉淀时,应开大水龙头,使洗涤剂快速通过沉淀物
D.洗涤结束后,将固体迅速转移至圆底烧瓶进行后续操作
(4)步骤Ⅳ:①奖装有粗产品的圆底烧瓶接到纯化装置(图2)上,打开安全瓶上旋塞,打开抽气泵,关
闭安全瓶上旋塞,开启加热器,进行纯化。请给出纯化完成后的操作排序:________。
纯化完成→(_____)→(_____)→(_____)→(_____)→将产品转至干燥器中保存
a.拔出圆底烧瓶的瓶塞
b.关闭抽气泵
c.关闭加热器,待烧瓶冷却至室温
d.打开安全瓶上旋塞
②图2装置中U形管内NaOH固体的作用是_______________________。
(5)用滴定分析法确定产品纯度。甲同学通过测定产品中锰元素的含量确定纯度;乙同学通过测定产品
中氯元素的含量确定纯度。合理的是_________(填“甲”或“乙”)同学的方法。
【答案】(1)(CH COO) Mn
3 2
(2)步骤Ⅰ脱去四水醋酸锰的结晶水并防止生成MnCl ;步骤Ⅱ加热回流促进反应生成MnCl
2 2
(3)ABD
(4)cdba 防止可能产生的酸性气体进入抽气泵;防止外部水气进入样品
(5)乙
【解析】(1)根据制备无水二氯化锰的主要反应:(CHCOO) Mn+CHCOCl MnCl ↓+2(CH COO) O
3 2 3 2 3 2
以及乙酰氯遇水发生反应:CHCOCl+H O→CH COOH+HCl可判断步骤Ⅰ中利用CHCOCl吸水,因此所
3 2 3 3
获固体主要成分是(CHCOO) Mn。(2)由于步骤Ⅰ脱去四水醋酸锰的结晶水并防止生成MnCl ,因此步骤Ⅰ
3 2 2
在室温下反应;而步骤Ⅱ加热回流促进反应生成MnCl ,所以步骤Ⅱ需要在加热回流下反应。(3)A项,滤
2纸略小于布氏漏斗,但要把所有的孔都覆盖,并用蒸馏水润湿滤纸,微开水龙头,抽气使滤纸紧贴在漏斗
瓷板上,故A正确;B项,用倾析法转移溶液,开大水龙头,待溶液快流尽时再转移沉淀,故B正确;C
项,用抽滤洗涤沉淀时,抽滤速率不能过快,故C错误;D项,由于无水二氯化锰极易吸水潮解,洗涤结
束后,将固体迅速转移至圆底烧瓶进行后续操作,故D正确;故选ABD;(4)①纯化完成后首先关闭加热
器,待烧瓶冷却至室温,然后打开安全瓶上旋塞,关闭抽气泵,最后拔出圆底烧瓶的瓶塞,将产品转至干
燥器中保存,故故选cdba;②由于可能混有酸性气体且无水二氯化锰极易吸水潮解,因此图2装置中U形
管内NaOH固体的作用是防止可能产生的酸性气体进入抽气泵,同时防止外部水气进入样品。(5)由于无水
二氯化锰极易吸水潮解,且锰离子水解,所以应该通过测定产品中氯元素的含量确定纯度,所以合理的是
乙同学的方法。
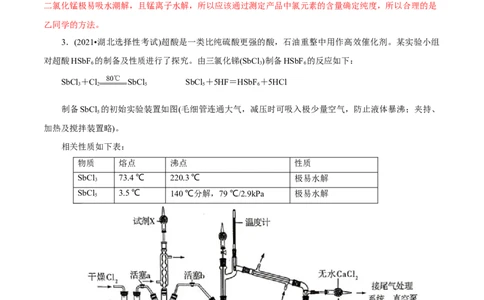
3.(2021•湖北选择性考试)超酸是一类比纯硫酸更强的酸,石油重整中用作高效催化剂。某实验小组
对超酸HSbF 的制备及性质进行了探究。由三氯化锑(SbCl )制备HSbF 的反应如下:
6 3 6
80℃
SbCl +Cl SbCl SbCl +5HF=HSbF +5HCl
3 2 5 5 6
制备SbCl 的初始实验装置如图(毛细管连通大气,减压时可吸入极少量空气,防止液体暴沸;夹持、
5
加热及搅拌装置略)。
相关性质如下表:
物质 熔点 沸点 性质
SbCl 73.4 ℃ 220.3 ℃ 极易水解
3
SbCl 3.5 ℃ 140 ℃分解,79 ℃/2.9kPa 极易水解
5
回答下列问题:
(1)实验装置中两个冷凝管 (填“能”或“不能”)交换使用。
(2)试剂X的作用为 、 。
(3)反应完成后,关闭活塞a、打开活塞b,减压转移 (填仪器名称)中生成的至双口烧瓶
中。用真空泵抽气减压蒸馏前,必须关闭的活塞是(填“a”或“b”);用减压蒸馏而不用常压蒸馏的主要原因是 。
(4)实验小组在由SbCl 制备HSbF 时,没有选择玻璃仪器,其原因为 。(写化学反应
5 6
方程式)
(5)为更好地理解超酸的强酸性,实验小组查阅相关资料了解得:弱酸在强酸性溶剂中表现出碱的性质,
如冰醋酸与纯硫酸之间的化学反应方程式为
CHCOOH+HSO =[CHC(OH) ][HSO ]
3 2 4 3 2 4
以此类推,HSO 与HSbF 之间的化学反应方程式为 。
2 4 6
(6)实验小组在探究实验中发现蜡烛可以溶解于中,同时放出氢气。已知烷烃分子中碳氢键的活性大小
顺序为:甲基(-CH)<亚甲基(-CH -)<次甲基( )。写出 2-甲基丙烷与反应的离子方程式
3 2
。
【答案】(除标明外,每空2分)
(1)不能(1分)
(2)吸收氯气,防止污染空气(1分)防止空气中的水蒸气进入三口烧瓶使SbCl 、SbCl 水解(1分)
3 5
(3)三口烧瓶(1分)b 防止SbCl 分解
5
(4)SiO+4HF=SiF↑+2HO
2 4 2
(5)H SO +HSbF =[H SO ][SbF ]
2 4 6 3 4 6
(6)
【解析】(1)与直形冷凝管相比,球形冷凝管的冷却面积大,冷却效果好;但是,由于球形冷凝管的内
芯管为球泡状,容易在球部积留蒸馏液,故不适宜用于倾斜式蒸馏装置(不用于冷凝蒸馏的蒸气),多用于
垂直冷凝回馏装置(制备物质),故实验装置中两个冷凝管不能交换使用。(2)根据表中提供信息,SbCl ,
3
SbCl 极易水解,知试剂X的作用是防止空中水蒸气进入三口烧瓶,同时吸收氯气,防止污染空气。(3)由
5
实验装置知,反应完成后,关闭活塞a,打开活塞b,减压转移三口烧瓶中生成的SbCl 至双口烧瓶中。减
5
压蒸馏前,必须关闭活塞b,以保证装置密封,便于后续抽真空。根据表中提供信息知,SbCl 容易分解,
5
用减压蒸馏而不用常压蒸馏,可以防止温度过高,而使SbCl 分解。(4)由SbCl 制备HSbF 时,需要用到
5 5 6
HF,而HF可与玻璃中二氧化硅反应,故不能选择玻璃仪器。(5)硫酸与超强酸反应时,表现出碱的性质,
即结合氢离子,即HSO +HSbF =[H SO ][SbF ]。(6)2-甲基丙烷的结构简式为(CH)CH,根据题目信息
2 4 6 3 4 6 3 3知,CH上氢容易参与反应,电离出氢阴离子,与超强酸电离的阳离子结合生成氢气。主要离子方程式为
。
4.(2019•新课标Ⅱ卷)咖啡因是一种生物碱(易溶于水及乙醇,熔点234.5℃,100℃以上开始升华),有
兴奋大脑神经和利尿等作用。茶叶中含咖啡因约 1%~5%、单宁酸(K 约为 10−6,易溶于水及乙醇)约
a
3%~10%,还含有色素、纤维素等。实验室从茶叶中提取咖啡因的流程如下图所示。
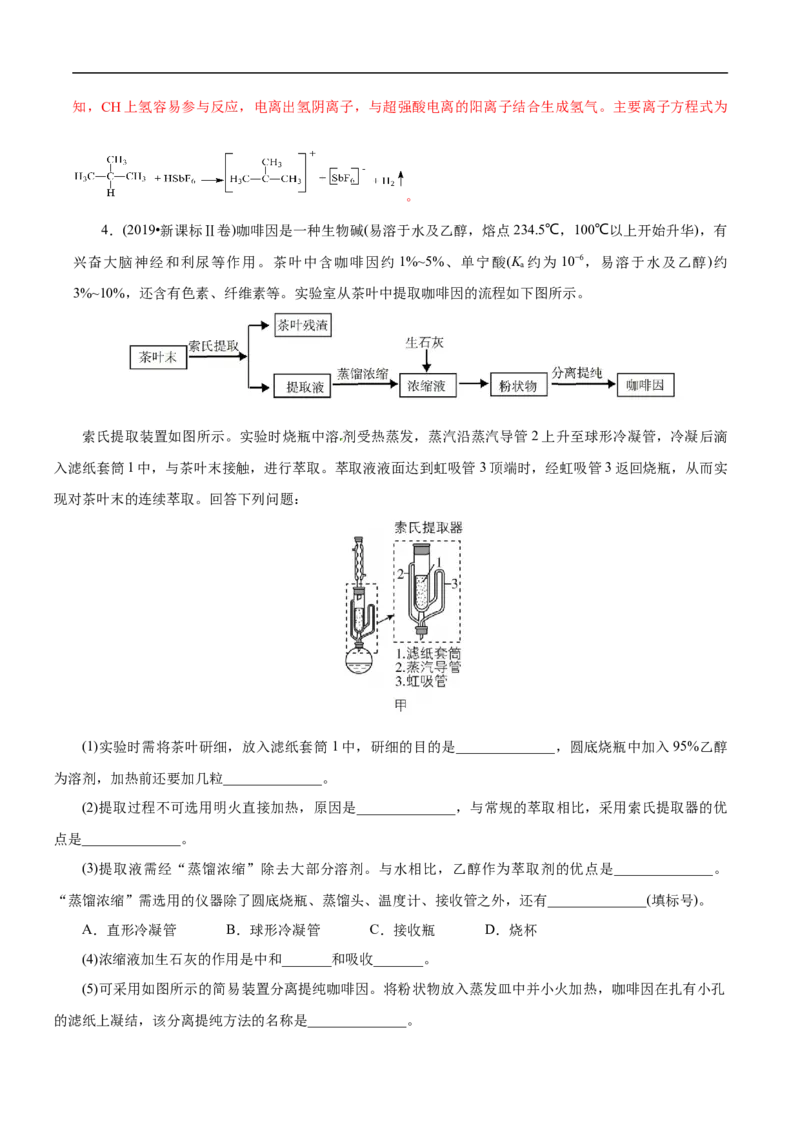
索氏提取装置如图所示。实验时烧瓶中溶剂受热蒸发,蒸汽沿蒸汽导管2上升至球形冷凝管,冷凝后滴
入滤纸套筒1中,与茶叶末接触,进行萃取。萃取液液面达到虹吸管3顶端时,经虹吸管3返回烧瓶,从而实
现对茶叶末的连续萃取。回答下列问题:
(1)实验时需将茶叶研细,放入滤纸套筒1中,研细的目的是______________,圆底烧瓶中加入95%乙醇
为溶剂,加热前还要加几粒______________。
(2)提取过程不可选用明火直接加热,原因是______________,与常规的萃取相比,采用索氏提取器的优
点是______________。
(3)提取液需经“蒸馏浓缩”除去大部分溶剂。与水相比,乙醇作为萃取剂的优点是______________。
“蒸馏浓缩”需选用的仪器除了圆底烧瓶、蒸馏头、温度计、接收管之外,还有______________(填标号)。
A.直形冷凝管 B.球形冷凝管 C.接收瓶 D.烧杯
(4)浓缩液加生石灰的作用是中和_______和吸收_______。
(5)可采用如图所示的简易装置分离提纯咖啡因。将粉状物放入蒸发皿中并小火加热,咖啡因在扎有小孔
的滤纸上凝结,该分离提纯方法的名称是______________。【答案】(1)增加固液接触面积,提取充分 沸石
(2)乙醇易挥发,易燃 使用溶剂量少,可连续萃取(萃取效率高)
(3)乙醇沸点低,易浓缩 AC (4)单宁酸 水 (5)升华
【解析】(1)萃取时将茶叶研细可以增加固液接触面积,从而使提取更充分;由于需要加热,为防止液体
暴沸,加热前还要加入几粒沸石;(2)由于乙醇易挥发,易燃烧,为防止温度过高使挥发出的乙醇燃烧,因此
提取过程中不可选用明火直接加热;根据题干中的已知信息可判断与常规的萃取相比较,采用索式提取器的
优点是使用溶剂量少,可连续萃取(萃取效率高);(3)乙醇是有机溶剂,沸点低,因此与水相比较乙醇作为萃
取剂的优点是乙醇沸点低,易浓缩;蒸馏浓缩时需要冷凝管,为防止液体残留在冷凝管中,应该选用直形冷
凝管,而不需要球形冷凝管,A正确,B错误;为防止液体挥发,冷凝后得到的馏分需要有接收瓶接收馏分,
而不需要烧杯,C正确,D错误,故选AC。(4)由于茶叶中还含有单宁酸,且单宁酸也易溶于水和乙醇,因此
浓缩液中加入氧化钙的作用是中和单宁酸,同时也吸收水;(5)根据已知信息可知咖啡因在100℃以上时开始
升华,因此该分离提纯方法的名称是升华。
1.减压蒸馏(分馏)
操作原理:减压蒸馏就是在低于大气压力下进行的蒸馏操作。它是分离和提纯沸点高、热稳定性差的
有机化合物的重要方法。利用上述原理,在蒸馏装置上连接真空泵,使系统内压降低,从而使液体化合物
在较低温度下沸腾而被蒸出。如苯甲醛常压下沸点为 179℃/101.3kPa (760mmHg),当压力降到
6.7kPa(50mmHg)时,沸点为95℃;水杨酸乙酪常压下(760mmHg) 沸点为234℃,而在20mmHg时沸点为
l18℃。
适用对象:在常压蒸馏是未达到沸点即已受热分解、氧化或聚合的物质。
2.减压蒸发(浓缩)
减压蒸发也称为减压浓缩或真空蒸发。
操作原理:在密闭的容器内,抽真空使液体处于一个大气压下的环境,从而降低水的沸腾温度,以此
进行蒸发浓缩。
操作优点:①由于压力降低,溶液的沸点降低,能防止或减少热敏性物质的分解;②增大传热温度差,
强化蒸发操作;③不断地排除溶剂蒸气,有利于蒸发顺利进行;3.减压干燥(真空干燥)
操作原理:减压干燥的干燥原理是湿物料表面处水分气化的结果,使百物料内部与表面之间产生水分
浓度差,从而使物体干燥。
适用对象:经过纯化后,准备进行分析鉴定(元素定量、波谱鉴定等)的易在空气氧化的样品。
4.水蒸气蒸馏
操作原理:水蒸气蒸馏是纯化分离有机化合物的重要方法之一。 当水和不(或难)溶于水的化合物一起
存在时,整个体系的蒸气压力根据道尔顿分压定律,应为各组分蒸气压力之和。 即:P=P + P (PA为与
水 A
水不(或难)溶化合物的蒸气压)当P与外界大气压相等时,混合物就沸腾。这时的温度即为它们的沸点,所
以混合物的沸点将比任何一组分的沸点都要低一些。而且在低于1000C的温度下随水蒸汽一起蒸馏出来。
适用对象:水蒸气蒸馏法适合分离那些在其沸点附近容易分解的物质,也适用于从不挥发物质或树脂
状物质中分离出所需的组分(如天然产物香精油、生物碱等)
5.减压过滤(吸虑或抽滤)
操作原理:利用装置中的抽气泵给吸滤瓶减压,造成瓶内与布氏漏斗液面上的压力差,从而加快过滤
速率,吸滤瓶用于承接滤液。安全瓶用于防止水泵中水产生溢流而倒灌入吸滤瓶中。
适用对象:减压过滤不宜用于过滤胶状沉淀或颗粒太小的沉淀。胶状沉淀在快速过滤时易透过滤纸;
沉淀颗粒太小则易在滤纸上形成一层致密的沉淀,溶液不易透过。
6.恒压滴液漏斗
操作原理:通过支插管保证液面上下的压强一致,从而使得液体能够顺利流下。一般的漏斗流下液体
时,如果下方容器是封闭的,流出的液体会挤占原有气体的空间,导致容器内的压强不断知增加,这压强
(实际上是液体道上下的压强差)作用在漏斗内的液体上会提供向上的推力,使得液体不能流下。因此一般
的(长颈、分液)漏斗容易导致液体难以流出(堵塞)。装置示意图如图3所示。
图3:恒压滴液漏斗(蓝色方框内)
使用对象:一般在封闭体系中用恒压漏斗,比如绝大部分的有机合成实验,因其有机溶剂易挥发、需
要隔绝空气(氧气)等。恒压滴液漏斗在上述实验中与烧瓶(或其他反应容器)紧密连接(一般都为标准磨口),
漏斗也要用塞子密封。此外,因恒压滴液漏斗是合成实验的常规仪器,均为标准磨口,连接方便,一些不
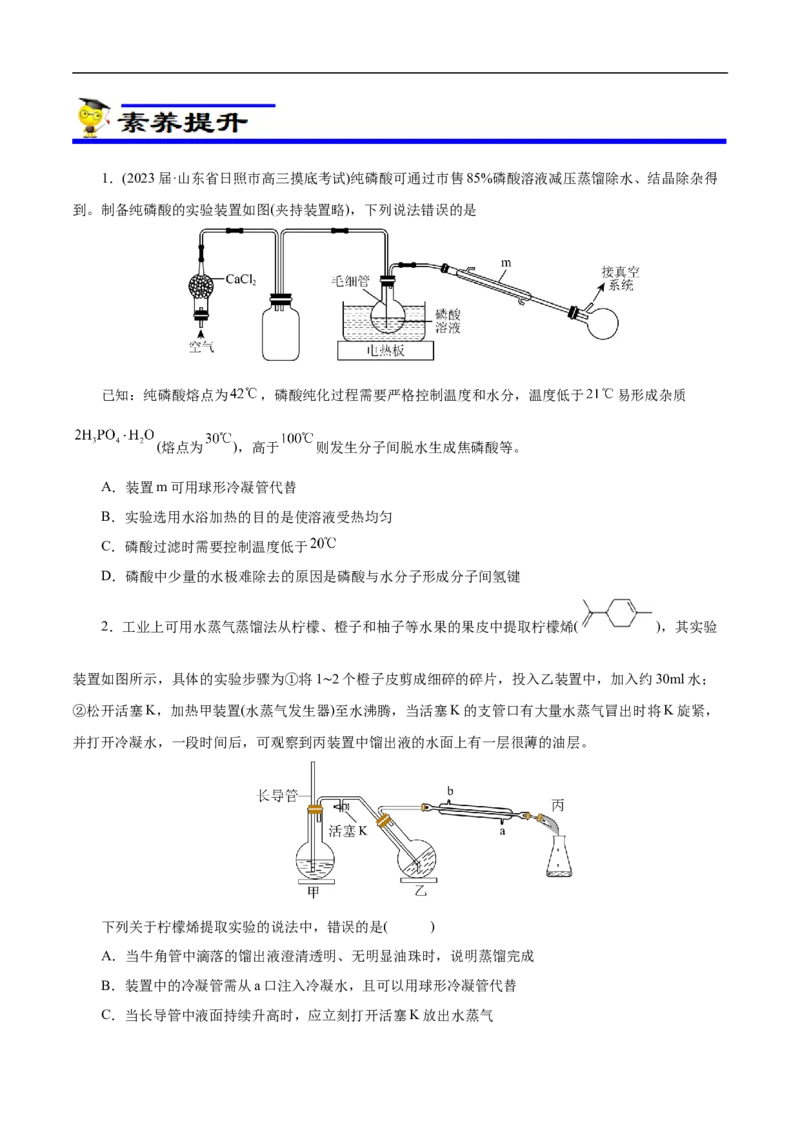
需要封闭或条件宽松的滴加过程(比如滴加水),也常用恒压滴液漏斗。1.(2023届·山东省日照市高三摸底考试)纯磷酸可通过市售85%磷酸溶液减压蒸馏除水、结晶除杂得
到。制备纯磷酸的实验装置如图(夹持装置略),下列说法错误的是
已知:纯磷酸熔点为 ,磷酸纯化过程需要严格控制温度和水分,温度低于 易形成杂质
(熔点为 ),高于 则发生分子间脱水生成焦磷酸等。
A.装置m可用球形冷凝管代替
B.实验选用水浴加热的目的是使溶液受热均匀
C.磷酸过滤时需要控制温度低于
D.磷酸中少量的水极难除去的原因是磷酸与水分子形成分子间氢键
2.工业上可用水蒸气蒸馏法从柠檬、橙子和柚子等水果的果皮中提取柠檬烯( ),其实验
装置如图所示,具体的实验步骤为①将1 2个橙子皮剪成细碎的碎片,投入乙装置中,加入约30ml水;
②松开活塞K,加热甲装置(水蒸气发生器∼)至水沸腾,当活塞K的支管口有大量水蒸气冒出时将K旋紧,
并打开冷凝水,一段时间后,可观察到丙装置中馏出液的水面上有一层很薄的油层。
下列关于柠檬烯提取实验的说法中,错误的是( )
A.当牛角管中滴落的馏出液澄清透明、无明显油珠时,说明蒸馏完成
B.装置中的冷凝管需从a口注入冷凝水,且可以用球形冷凝管代替
C.当长导管中液面持续升高时,应立刻打开活塞K放出水蒸气D.实验结束后,可以通过分液、蒸馏的方法得到高纯度的精油
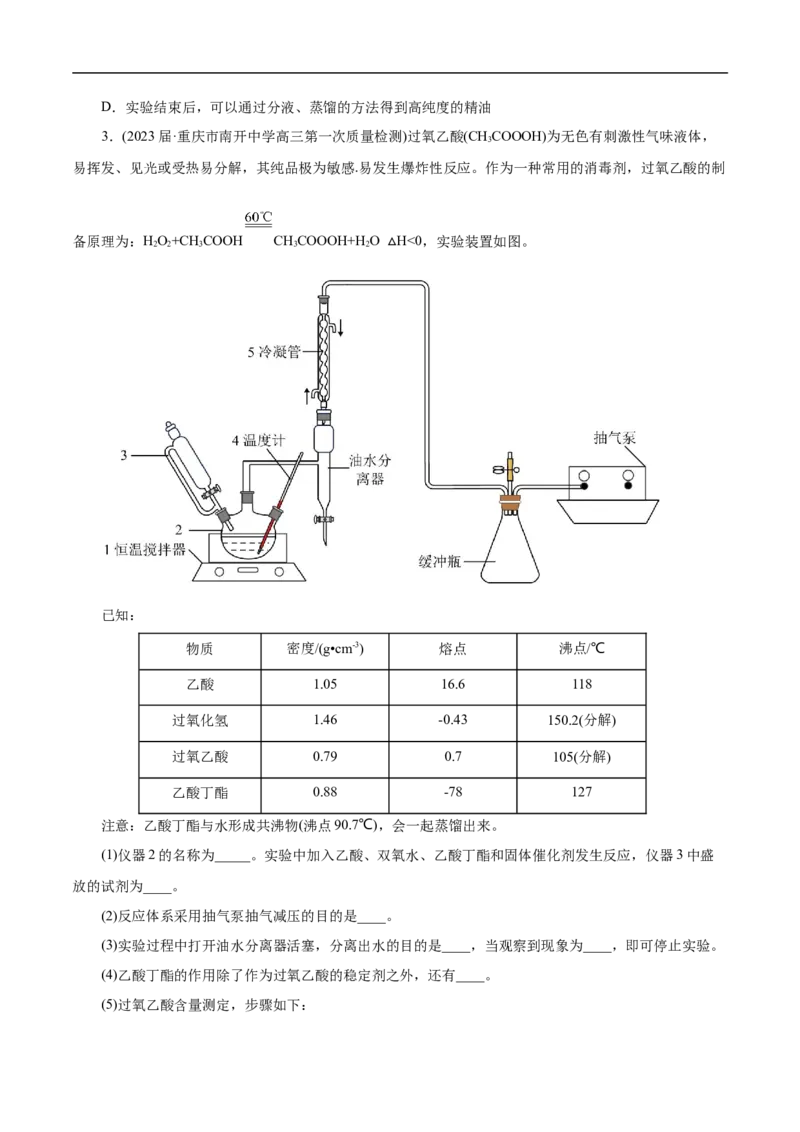
3.(2023届·重庆市南开中学高三第一次质量检测)过氧乙酸(CHCOOOH)为无色有刺激性气味液体,
3
易挥发、见光或受热易分解,其纯品极为敏感.易发生爆炸性反应。作为一种常用的消毒剂,过氧乙酸的制
备原理为:HO+CH COOH CHCOOOH+H O H<0,实验装置如图。
2 2 3 3 2
△
已知:
物质 密度/(g•cm-3) 熔点 沸点/℃
乙酸 1.05 16.6 118
过氧化氢 1.46 -0.43 150.2(分解)
过氧乙酸 0.79 0.7 105(分解)
乙酸丁酯 0.88 -78 127
注意:乙酸丁酯与水形成共沸物(沸点90.7℃),会一起蒸馏出来。
(1)仪器2的名称为_____。实验中加入乙酸、双氧水、乙酸丁酯和固体催化剂发生反应,仪器3中盛
放的试剂为____。
(2)反应体系采用抽气泵抽气减压的目的是____。
(3)实验过程中打开油水分离器活塞,分离出水的目的是____,当观察到现象为____,即可停止实验。
(4)乙酸丁酯的作用除了作为过氧乙酸的稳定剂之外,还有____。
(5)过氧乙酸含量测定,步骤如下:I.准确称取1.00g过氧乙酸样液,定容于100mL容瓶中。
II.取10.00mL上述溶液,用0.01mol/L酸性KMnO 溶液滴定至溶液出现浅红色(除去过氧乙酸试样中剩
4
余HO)。
2 2
III.加入过量KI溶液,摇匀,用0.01000mol/LNa SO 标准液滴定至终点,消耗NaSO 溶液
2 2 3 2 2 3
50.00mL。
已知:SO +I =S O +2I-
2 2 2
①过氧乙酸被I-还原,还原产物之一为乙酸,其离子方程式为____。
②过氧乙酸样液中过氧乙酸的质量分数为____。
③用该法测定过氧乙酸含量比实际含量偏高的原因是(不考虑实验操作产生的误差)____。
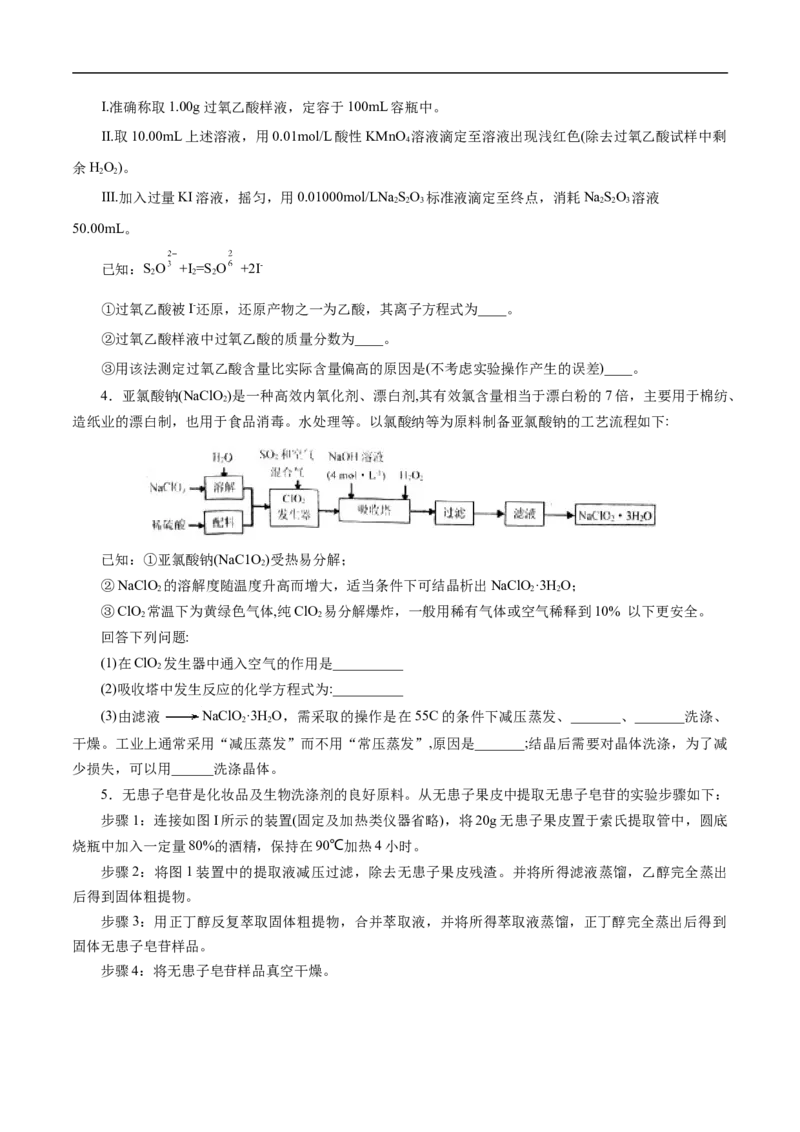
4.亚氯酸钠(NaClO)是一种高效内氧化剂、漂白剂,其有效氯含量相当于漂白粉的7倍,主要用于棉纺、
2
造纸业的漂白制,也用于食品消毒。水处理等。以氯酸纳等为原料制备亚氯酸钠的工艺流程如下:
已知:①亚氯酸钠(NaC1O )受热易分解;
2
②NaClO 的溶解度随温度升高而增大,适当条件下可结晶析出NaClO·3H O;
2 2 2
③ClO 常温下为黄绿色气体,纯ClO 易分解爆炸,一般用稀有气体或空气稀释到10% 以下更安全。
2 2
回答下列问题:
(1)在ClO 发生器中通入空气的作用是__________
2
(2)吸收塔中发生反应的化学方程式为:__________
(3)由滤液 NaClO·3H O,需采取的操作是在55C的条件下减压蒸发、_______、_______洗涤、
2 2
干燥。工业上通常采用“减压蒸发”而不用“常压蒸发”,原因是_______;结晶后需要对晶体洗涤,为了减
少损失,可以用______洗涤晶体。
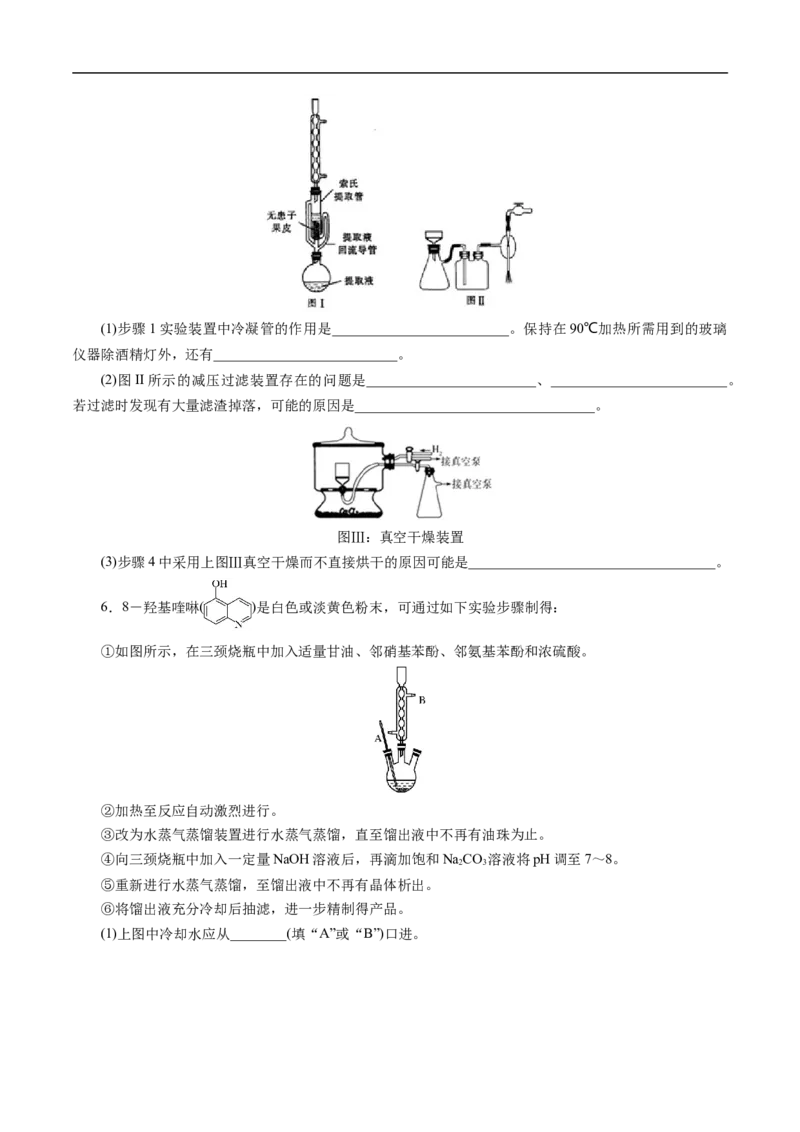
5.无患子皂苷是化妆品及生物洗涤剂的良好原料。从无患子果皮中提取无患子皂苷的实验步骤如下:
步骤1:连接如图I所示的装置(固定及加热类仪器省略),将20g无患子果皮置于索氏提取管中,圆底
烧瓶中加入一定量80%的酒精,保持在90℃加热4小时。
步骤2:将图1装置中的提取液减压过滤,除去无患子果皮残渣。并将所得滤液蒸馏,乙醇完全蒸出
后得到固体粗提物。
步骤3:用正丁醇反复萃取固体粗提物,合并萃取液,并将所得萃取液蒸馏,正丁醇完全蒸出后得到
固体无患子皂苷样品。
步骤4:将无患子皂苷样品真空干燥。(1)步骤1实验装置中冷凝管的作用是_________________________。保持在90℃加热所需用到的玻璃
仪器除酒精灯外,还有__________________________。
(2)图II所示的减压过滤装置存在的问题是________________________、_________________________。
若过滤时发现有大量滤渣掉落,可能的原因是__________________________________。
图Ⅲ:真空干燥装置
(3)步骤4中采用上图Ⅲ真空干燥而不直接烘干的原因可能是___________________________________。
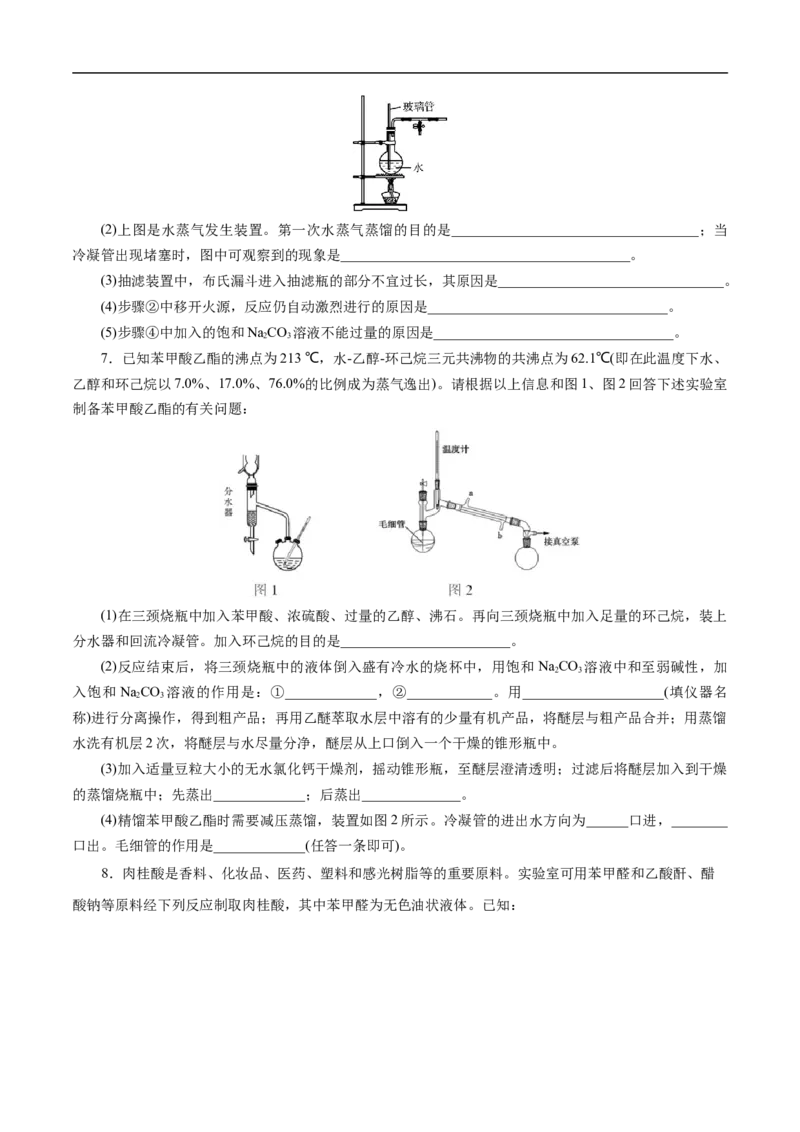
6.8-羟基喹啉( )是白色或淡黄色粉末,可通过如下实验步骤制得:
①如图所示,在三颈烧瓶中加入适量甘油、邻硝基苯酚、邻氨基苯酚和浓硫酸。
②加热至反应自动激烈进行。
③改为水蒸气蒸馏装置进行水蒸气蒸馏,直至馏出液中不再有油珠为止。
④向三颈烧瓶中加入一定量NaOH溶液后,再滴加饱和NaCO 溶液将pH调至7~8。
2 3
⑤重新进行水蒸气蒸馏,至馏出液中不再有晶体析出。
⑥将馏出液充分冷却后抽滤,进一步精制得产品。
(1)上图中冷却水应从________(填“A”或“B”)口进。(2)上图是水蒸气发生装置。第一次水蒸气蒸馏的目的是___________________________________;当
冷凝管出现堵塞时,图中可观察到的现象是_________________________________________。
(3)抽滤装置中,布氏漏斗进入抽滤瓶的部分不宜过长,其原因是________________________________。
(4)步骤②中移开火源,反应仍自动激烈进行的原因是__________________________________。
(5)步骤④中加入的饱和NaCO 溶液不能过量的原因是__________________________________。
2 3
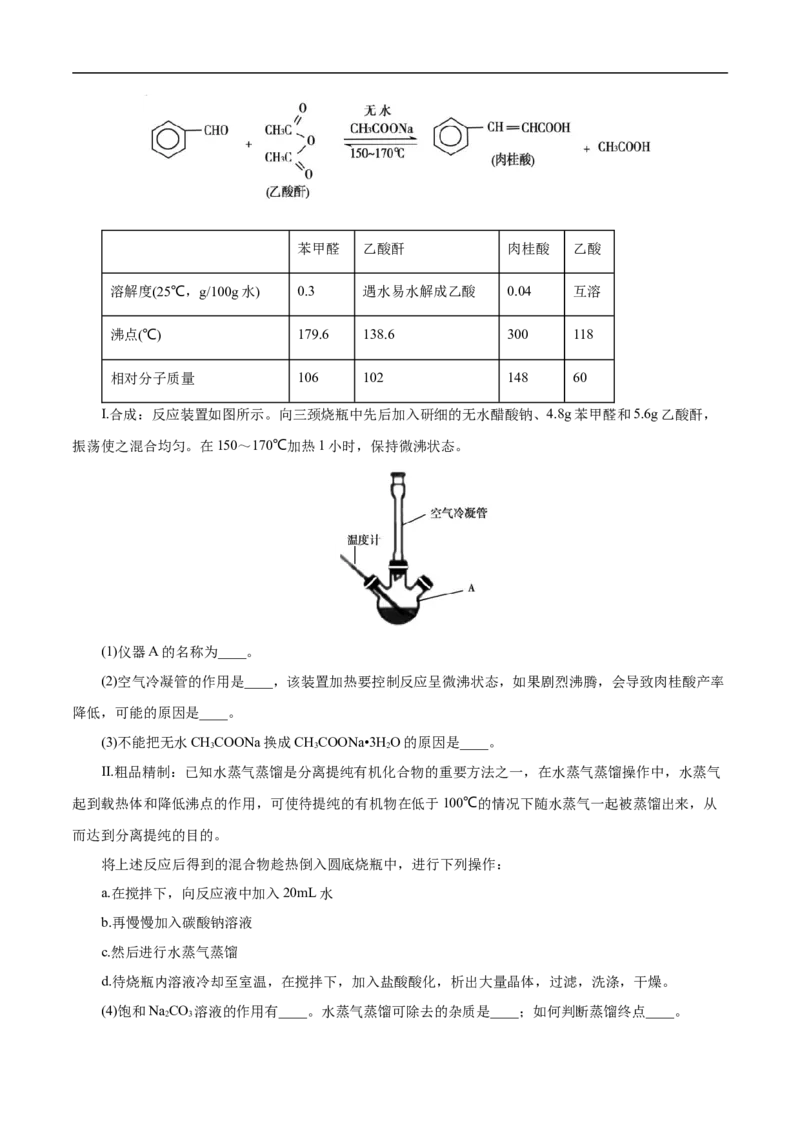
7.已知苯甲酸乙酯的沸点为213 ℃,水-乙醇-环己烷三元共沸物的共沸点为62.1℃(即在此温度下水、
乙醇和环己烷以7.0%、17.0%、76.0%的比例成为蒸气逸出)。请根据以上信息和图1、图2回答下述实验室
制备苯甲酸乙酯的有关问题:
(1)在三颈烧瓶中加入苯甲酸、浓硫酸、过量的乙醇、沸石。再向三颈烧瓶中加入足量的环己烷,装上
分水器和回流冷凝管。加入环己烷的目的是________________________。
(2)反应结束后,将三颈烧瓶中的液体倒入盛有冷水的烧杯中,用饱和NaCO 溶液中和至弱碱性,加
2 3
入饱和NaCO 溶液的作用是:①_____________,②____________。用____________________(填仪器名
2 3
称)进行分离操作,得到粗产品;再用乙醚萃取水层中溶有的少量有机产品,将醚层与粗产品合并;用蒸馏
水洗有机层2次,将醚层与水尽量分净,醚层从上口倒入一个干燥的锥形瓶中。
(3)加入适量豆粒大小的无水氯化钙干燥剂,摇动锥形瓶,至醚层澄清透明;过滤后将醚层加入到干燥
的蒸馏烧瓶中;先蒸出_____________;后蒸出______________。
(4)精馏苯甲酸乙酯时需要减压蒸馏,装置如图2所示。冷凝管的进出水方向为______口进,________
口出。毛细管的作用是_____________(任答一条即可)。
8.肉桂酸是香料、化妆品、医药、塑料和感光树脂等的重要原料。实验室可用苯甲醛和乙酸酐、醋
酸钠等原料经下列反应制取肉桂酸,其中苯甲醛为无色油状液体。已知:苯甲醛 乙酸酐 肉桂酸 乙酸
溶解度(25℃,g/100g水) 0.3 遇水易水解成乙酸 0.04 互溶
沸点(℃) 179.6 138.6 300 118
相对分子质量 106 102 148 60
I.合成:反应装置如图所示。向三颈烧瓶中先后加入研细的无水醋酸钠、4.8g苯甲醛和5.6g乙酸酐,
振荡使之混合均匀。在150~170℃加热1小时,保持微沸状态。
(1)仪器A的名称为____。
(2)空气冷凝管的作用是____,该装置加热要控制反应呈微沸状态,如果剧烈沸腾,会导致肉桂酸产率
降低,可能的原因是____。
(3)不能把无水CHCOONa换成CHCOONa•3H O的原因是____。
3 3 2
II.粗品精制:已知水蒸气蒸馏是分离提纯有机化合物的重要方法之一,在水蒸气蒸馏操作中,水蒸气
起到载热体和降低沸点的作用,可使待提纯的有机物在低于100℃的情况下随水蒸气一起被蒸馏出来,从
而达到分离提纯的目的。
将上述反应后得到的混合物趁热倒入圆底烧瓶中,进行下列操作:
a.在搅拌下,向反应液中加入20mL水
b.再慢慢加入碳酸钠溶液
c.然后进行水蒸气蒸馏
d.待烧瓶内溶液冷却至室温,在搅拌下,加入盐酸酸化,析出大量晶体,过滤,洗涤,干燥。
(4)饱和NaCO 溶液的作用有____。水蒸气蒸馏可除去的杂质是____;如何判断蒸馏终点____。
2 3(5)若得到的肉桂酸晶体产品不纯,应采用____法可得到纯度更高的产品。
(6)若最后得到纯净的肉桂酸5.2g,则该反应中的产率是____(保留两位有效数字)。
9.苯胺又名氨基苯是最重要的胺类物质之一,可作为炸药中的稳定剂、汽油中的防爆剂,也可作为
医药磺胺药的原料等。苯胺为无色油状液体,有特殊气味,可用水蒸气蒸馏提纯。用纳米铁粉还原硝基苯
制备苯胺的原理及装置图(略去夹持装置和加热装置)如下:
4 +9Fe+4H O 4 +3Fe O
2 3 4
已知部分有机物的一些数据如下表:
相对分 密度(g/ 熔点 沸点
名称 溶解性
子质量 mL) (℃) (℃)
硝基苯 123 1.20 5.7 210.8 难溶于水,易溶于乙醇、乙醚
苯胺 93 1.02 -6.3 184.4 难溶于水,易溶于乙醇、乙醚
乙醚 74 0.71 -116.3 34.6 微溶于水,易溶于乙醇
I.合成:在装置1中的仪器X中,加入9g纳米铁粉、20mL水、1mL冰醋酸,加热至煮沸,煮沸后冷
却至室温,再将8.0mL硝基苯逐滴加入(该反应强烈放热),搅拌、加热、回流半小时,至反应完全。
II.分离提纯:将装置1改为装置2进行水蒸气蒸馏,取装置2中的馏出物约5-6mL,转移至分液漏斗
中,分离出有机层后,水层加入1.3gNaCl固体,用乙醚萃取3次(每次用7.0mL乙醚),合并有机层和乙醚
萃取液,加入粒状NaOH干燥,过滤后转移至干燥的圆底烧瓶中,水浴蒸去乙醚,残留物再利用装置3蒸
馏并收集温度T℃时的馏分。
请回答下列问题:
(1)加入硝基苯时,“逐滴加入”的目的是_______。
(2)分离提纯过程中加入NaCl固体的作用是_______。
(3)装置2中长导管B的作用是_______。
(4)“水蒸气蒸馏”结束后,应先打开止水夹T,再停止对“水蒸气发生装置”加热,目的是____。(5)利用装置3蒸馏时,温度的范围为_______,实验结束得到产物6.5mL,则苯胺的产率为_______(保
留三位有效数字)。
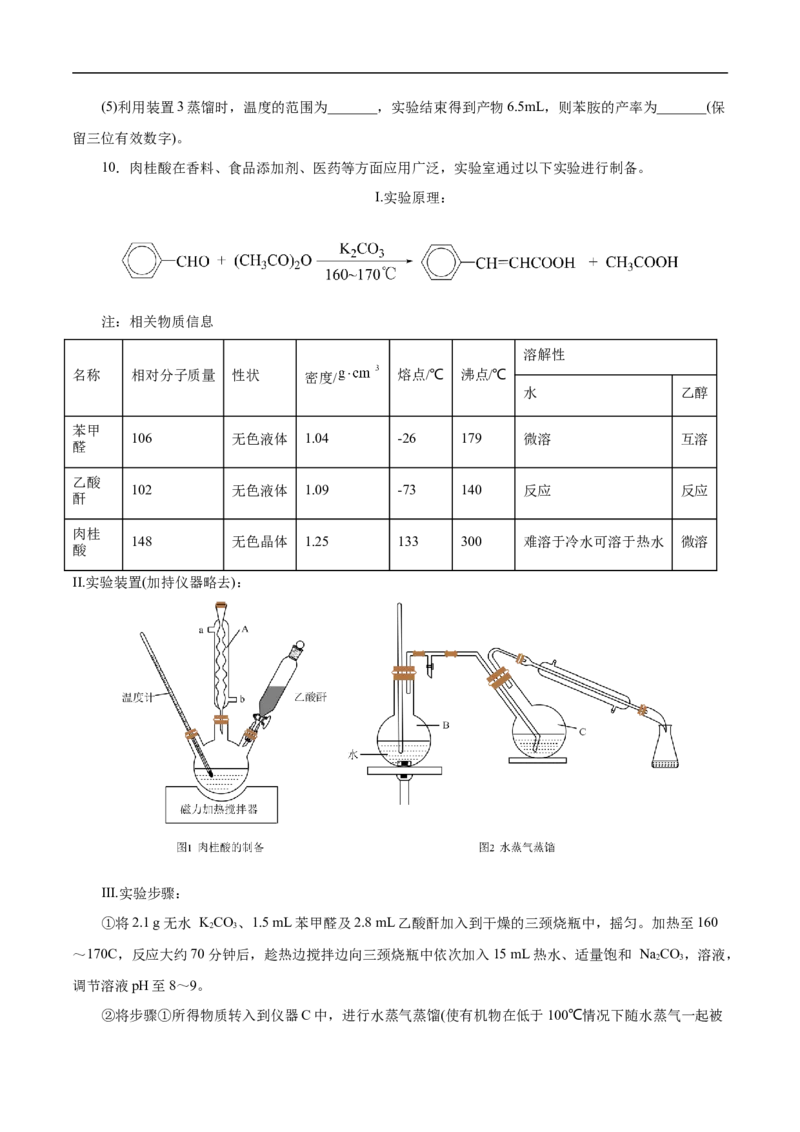
10.肉桂酸在香料、食品添加剂、医药等方面应用广泛,实验室通过以下实验进行制备。
I.实验原理:
注:相关物质信息
溶解性
名称 相对分子质量 性状 密度/ 熔点/℃ 沸点/℃
水 乙醇
苯甲
106 无色液体 1.04 -26 179 微溶 互溶
醛
乙酸
102 无色液体 1.09 -73 140 反应 反应
酐
肉桂
148 无色晶体 1.25 133 300 难溶于冷水可溶于热水 微溶
酸
II.实验装置(加持仪器略去):
III.实验步骤:
①将2.1 g无水 KCO、1.5 mL苯甲醛及2.8 mL乙酸酐加入到干燥的三颈烧瓶中,摇匀。加热至160
2 3
~170C,反应大约70分钟后,趁热边搅拌边向三颈烧瓶中依次加入15 mL热水、适量饱和 NaCO,溶液,
2 3
调节溶液pH至8~9。
②将步骤①所得物质转入到仪器C中,进行水蒸气蒸馏(使有机物在低于100℃情况下随水蒸气一起被蒸馏出来)。蒸馏结束,稍待冷却,加入少量活性炭,加热脱色,趁热抽滤。向冷却至室温的滤液中加盐酸
调pH至1,抽滤,冰水洗涤、干燥,得到粗产品。
③向粗产品中加入适量75%乙醇,重结晶,干燥后称重,得1.5 g较纯净产品。
回答下列问题:
(1)仪器A的名称为_______,其中a端为_______(填“进水口”或“出水口);仪器B中长导管的作用
是_______。
(2)加入药品前,三颈烧瓶必须确保干燥的原因是_______。
(3)步骤①加入 NaCO 的作用是_______。
2 3
(4)水蒸气蒸馏操作过程中,随水蒸气蒸馏出来的有机物是_______;判断蒸馏结束的现象是_______。
(5)已知产率= ,计算该实验肉桂酸的产率为_______(保留至小数点后一位)。