文档内容
专项训练 杂化轨道类型的判断(解析版)
一、单选题
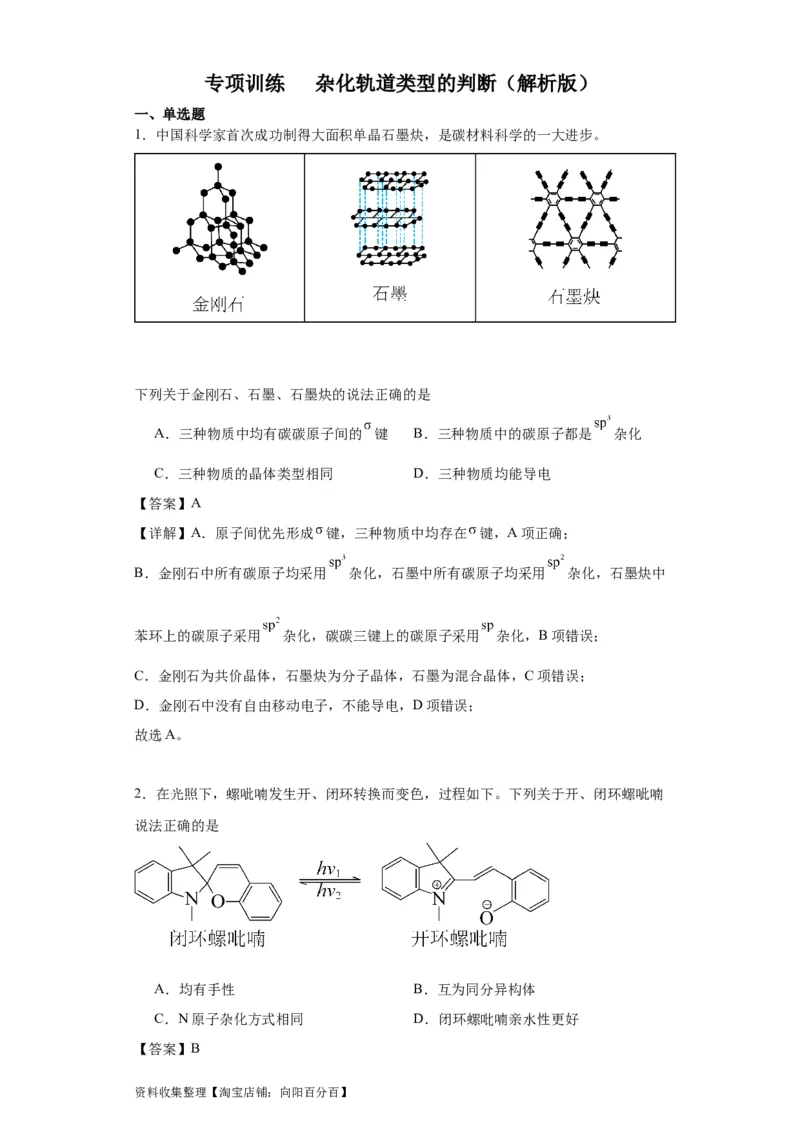
1.中国科学家首次成功制得大面积单晶石墨炔,是碳材料科学的一大进步。
下列关于金刚石、石墨、石墨炔的说法正确的是
A.三种物质中均有碳碳原子间的 键 B.三种物质中的碳原子都是 杂化
C.三种物质的晶体类型相同 D.三种物质均能导电
【答案】A
【详解】A.原子间优先形成 键,三种物质中均存在 键,A项正确;
B.金刚石中所有碳原子均采用 杂化,石墨中所有碳原子均采用 杂化,石墨炔中
苯环上的碳原子采用 杂化,碳碳三键上的碳原子采用 杂化,B项错误;
C.金刚石为共价晶体,石墨炔为分子晶体,石墨为混合晶体,C项错误;
D.金刚石中没有自由移动电子,不能导电,D项错误;
故选A。
2.在光照下,螺呲喃发生开、闭环转换而变色,过程如下。下列关于开、闭环螺呲喃
说法正确的是
A.均有手性 B.互为同分异构体
C.N原子杂化方式相同 D.闭环螺吡喃亲水性更好
【答案】B
资料收集整理【淘宝店铺:向阳百分百】【详解】A.手性碳是连有四个不同的原子或原子团的碳原子,闭环螺吡喃含有一个
手性碳原子 ,因此具有手性,开环螺吡喃不含手性碳原子,
不具备手性,故A错误;
B.根据它们的结构简式,分子式均为C H NO,它们结构不同,因此互为同分异构
19 19
体,故B正确;
C.闭环螺吡喃中N原子杂化方式为sp3,开环螺吡喃中N原子杂化方式为sp2,故C
错误;
D.开环螺吡喃中氧原子显负价,电子云密度大,容易与水分子形成分子间氢键,水
溶性增大,因此开环螺吡喃亲水性更好,故D错误;
答案为B。
3.一种合成布洛芬高分子载体药物的单体的结构简式如图所示,下列说法错误的是
A.1mol该单体最多可与 加成
B.该单体可发生取代反应、加聚反应
C.该单体中碳原子的杂化方式有 、 两种
D.该单体分子中最少有8个碳原子处于同一平面上
【答案】A
【详解】A.1mol苯环可与 加成,1mol碳碳双键可与 加成,酯基与
不能发生加成反应,故1mol该单体最多可与 加成,A项错误;
B.分子中含有的酯基可以发生水解反应,即取代反应,含有的碳碳双键可以发生加聚
反应,B项正确;
C.连接四个单键的碳原子为 杂化,碳氧双键、碳碳双键、苯环上的碳原子为 杂
化,C项正确;
D.苯环上的6个碳原子和取代苯环上氢原子的2个碳原子一定处于同一平面,D项正
资料收集整理【淘宝店铺:向阳百分百】确;
答案选A。
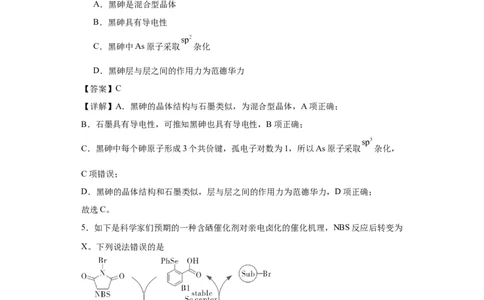
4.近年来,黑砷在催化电解水方面的研究受到关注,其晶体结构(如图)与石墨类似。
下列说法不正确的是
A.黑砷是混合型晶体
B.黑砷具有导电性
C.黑砷中As原子采取 杂化
D.黑砷层与层之间的作用力为范德华力
【答案】C
【详解】A.黑砷的晶体结构与石墨类似,为混合型晶体,A项正确;
B.石墨具有导电性,可推知黑砷也具有导电性,B项正确;
C.黑砷中每个砷原子形成3个共价键,孤电子对数为1,所以As原子采取 杂化,
C项错误;
D.黑砷的晶体结构和石墨类似,层与层之间的作用力为范德华力,D项正确;
故选C。
5.如下是科学家们预期的一种含硒催化剂对亲电卤化的催化机理,NBS反应后转变为
X。下列说法错误的是
A.反应方程式为 B.B1到B1—Br发生了氧化
C.Br—Br中的Se为 杂化 D.Se为p区元素
【答案】B
【详解】此题答案可能不正确,如您有正确答案请联系总部编辑qq:807204649。
资料收集整理【淘宝店铺:向阳百分百】6.下列关于 、 、 三种微粒的说法不正确的是
A.三种微粒所含有的电子数相等
B.三种微粒中氮原子的杂化方式相同
C.三种微粒的空间构型相同
D.键角大小关系:NH >NH>NH
3
【答案】C
【详解】A. 、 、 三种微粒,每个 、 、 所含有的电子数都
为10个,故A正确;
B.铵根离子中氮原子价层电子对个数=σ键个数+孤电子对个数=4+ (5−1−4×1)=4,所
以其采用sp3杂化,氨气分子中价层电子对个数=σ键个数+孤电子对个数=3+ (5-
3×1)=4,所以氮原子杂化方式是sp3, 中氮原子价层电子对个数=σ键个数+孤电子
对个数=2+ (5−1×2+1) =4,所以其采用sp3杂化,故B正确;
C.根据三种微粒的杂化方式可知,铵根离子为正四面体结构;氨气分子空间构型为三
角锥形, 空间构型为V形,故C错误;
D.铵根离子中,含0对孤电子,氨气分子中含1对孤电子,NH 含2对孤电子,含有
孤电子对越多,分子中的键角越小,所以键角大小关系:NH >NH>NH ,故D正确;
3
故选C。
7.X、Y、Z、W是原子序数依次增大的短周期主族元素,其中X、W元素的价电子
数等于其周期数,Z是地壳中含量最多的元素。它们形成的一种化合物M结构式如右
图,下列说法正确的是:
资料收集整理【淘宝店铺:向阳百分百】A.化合物M中,W、Z、Y的均为 杂化
B.X和Z的单质都属于非极性分子
C.氢化物的沸点:YN>C>H
【答案】D
【详解】A. 中的铁元素为+3价,溶液中含有Fe3+,加入KSCN溶液时,
发生如下反应:Fe3++3SCN- Fe(SCN) ,溶液变红,A错误;
3
B. 的空间构型为 ,杂化类型是 ,空间结构为正四面体,B错误;
C. 中C形成两个单键,因此C原子采取sp杂化,C错误;
D.同一周期从左到右元素电负性递增,因此O>N>C,同一主族,自上而下元素电负
性递减,并且元素的非金属性越强,其电负性越大,因此C>H,所以电负性的大小
O>N>C>H,D正确;
故选D。
14.黑矾 的结构如图。下列说法错误的是
资料收集整理【淘宝店铺:向阳百分百】A. 可表示为
B. 和 中的S均为 杂化
C. 中 与 的作用力类型分别是配位键、氢键、
氢键
D. 中所有水分子的 夹角完全相同
【答案】D
【详解】A.Fe2+的价层电子对排布式为3d6,可以与6个HO形成配位键,因此
2
可表示为 ,A正确;
B.价层电子对数=σ+中心原子孤电子对, :3+1=4, :4+0=4, 和
中的S均为 杂化,B正确;
C.Fe2+的价层电子对排布式为3d6,可以与6个HO形成配位键,氢原子和F、O、N
2
相连可以形成氢键,HO和HO、 均可以形成分子间氢键,C正确;
2 2
D. 结晶水中的 为109°28’,而与Fe2+形成配位键的
HO,由于空间结构的影响键角会变小,D错误;
2
故选D。
15.科学家早就预言 、 (M代表碱金属)的存在,并通过计算确认
可由 和 在大于20GPa的条件下合成,其中 比 、 稳
定。下列有关推测正确的是
A.热稳定性:
资料收集整理【淘宝店铺:向阳百分百】B. 中,C原子杂化方式为
C. 中,C原子杂化方式为
D.合成 的温度应该选择高温
【答案】C
【详解】A.类比其他酸和对应的盐的热稳定性,可以得出结论: ,
A错误;
B.碳酸根中C原子采取 杂化,B错误;
C. 中C原子采取 杂化,C正确;
D. 高温时会分解生成 和 ,D错误;
故选C。
16.新型分子N 呈首尾不分的链状结构,其中N原子共有四种成键方式,除端位外,
8
其他N原子采用3种不同的杂化轨道成键,若N 分子中形式电荷为0的N原子数为
8
x,采用sp2杂化的N原子数为y,采用sp3杂化的N原子数为z,则x、y、z分别为
A.4,2,2 B.3,3,2 C.3,2,3 D.4,2,3
【答案】A
【详解】根据价键规则,可写出N 分子的路易斯结构式 ,N 分
8 8
子中形式电荷为0的N原子数为4,采用sp2杂化的N原子数为2,采用sp3杂化的N原
子数为2,故选A。
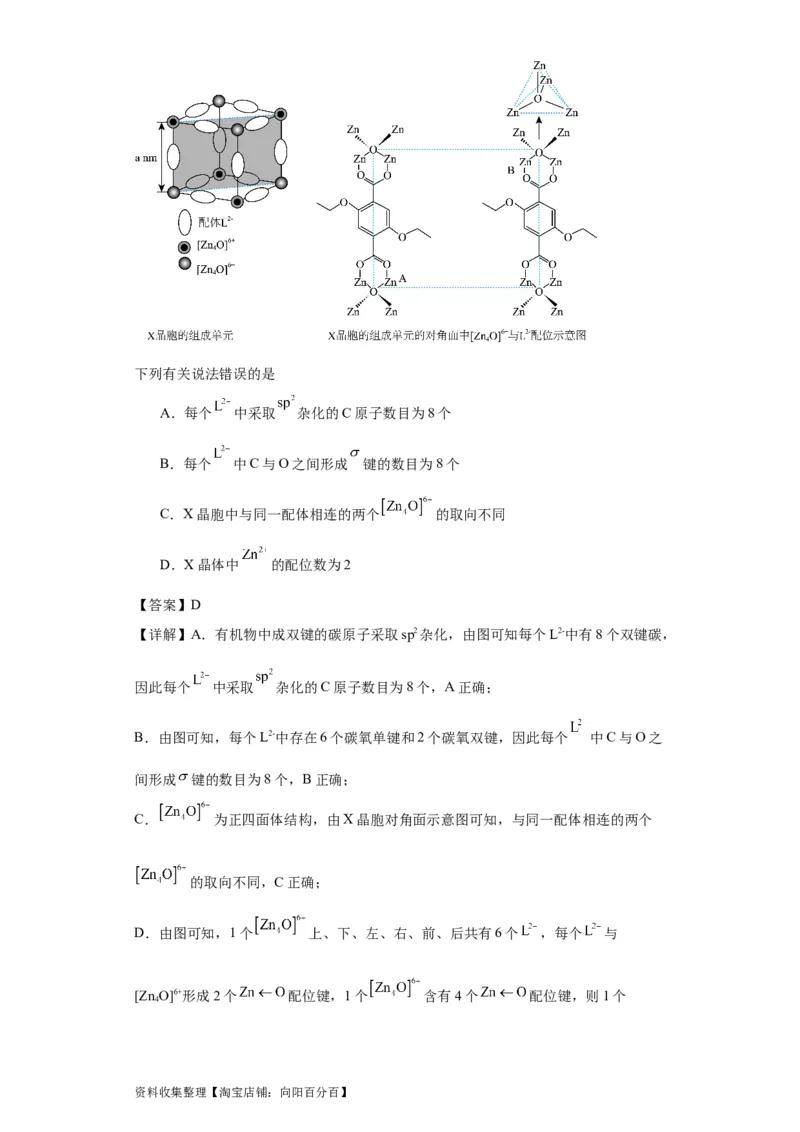
17.配位化合物X由配体 和具有正四面体结构的 组成。化合物X晶体具有
面心立方结构,其晶胞由8个结构相似的组成单元(如图)构成。
资料收集整理【淘宝店铺:向阳百分百】下列有关说法错误的是
A.每个 中采取 杂化的C原子数目为8个
B.每个 中C与O之间形成 键的数目为8个
C.X晶胞中与同一配体相连的两个 的取向不同
D.X晶体中 的配位数为2
【答案】D
【详解】A.有机物中成双键的碳原子采取sp2杂化,由图可知每个L2-中有8个双键碳,
因此每个 中采取 杂化的C原子数目为8个,A正确;
B.由图可知,每个L2-中存在6个碳氧单键和2个碳氧双键,因此每个 中C与O之
间形成 键的数目为8个,B正确;
C. 为正四面体结构,由X晶胞对角面示意图可知,与同一配体相连的两个
的取向不同,C正确;
D.由图可知,1个 上、下、左、右、前、后共有6个 ,每个 与
[Zn O]6+形成2个 配位键,1个 含有4个 配位键,则1个
4
资料收集整理【淘宝店铺:向阳百分百】中 形成的配位键数目为 ,1个 的配位数为4,D正确;
故选D。
18.新型储氢材料是开发利用氢能的重要研究方向。某种新型储氢材料的晶胞如图,
八面体中心为金属离子铁,顶点均为 配体;四面体中心为硼原子,顶点均为氢原
子。下列说法错误的是
A.材料中硼原子采用sp3杂化方式
B.化学式为
C.金属离子的价电子排布式为
D.该化合物中存在离子键、极性键和配位键
【答案】B
【详解】A.从图中可知,B原子的价层电子对数为4+0=4,杂化方式为sp3杂化,A
正确;
B.八面体中心为亚铁离子,顶点为NH 配体,则一个八面体表示为Fe(NH ),根据均
3 3 6
摊法,黑球位于顶点和面心,则黑球个数为 =4,白球位于晶胞内,其个数
为8,白球表示为BH,则该物质的化学式为 ,B错误;
4
C.Fe的电子排布式为[Ar]3d64s2,+2价的铁价电子排布式为3d6,C正确;
D.该化合物中Fe(NH ) 与BH 之间形成离子键,NH 内部存在极性键,亚铁离子和
3 6 4 3
NH 形成配位键,D正确;
3
故答案选B。
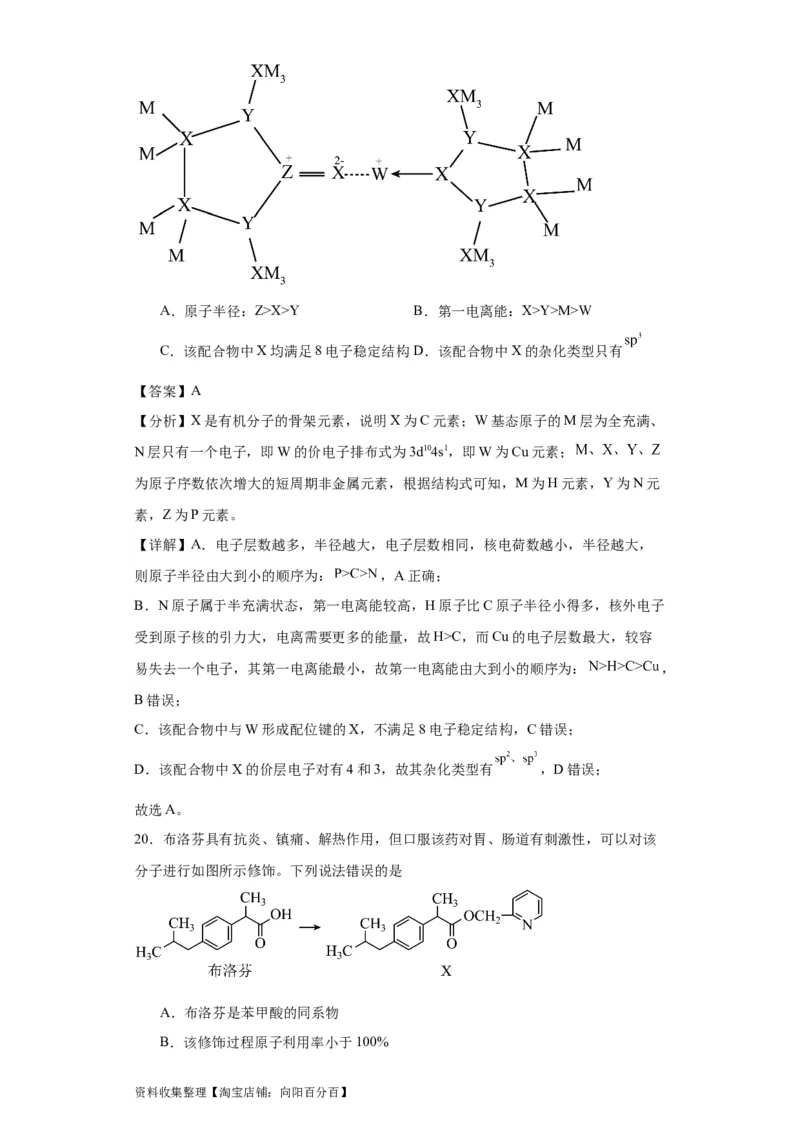
19.某化合物结构如图所示,其中M、X、Y、Z为原子序数依次增大的短周期非金属
元素,X是有机分子的骨架元素,W基态原子的M层为全充满、N层只有一个电子。
下列说法正确的是
资料收集整理【淘宝店铺:向阳百分百】A.原子半径:Z>X>Y B.第一电离能:X>Y>M>W
C.该配合物中X均满足8电子稳定结构 D.该配合物中X的杂化类型只有
【答案】A
【分析】X是有机分子的骨架元素,说明X为C元素;W基态原子的M层为全充满、
N层只有一个电子,即W的价电子排布式为3d104s1,即W为Cu元素;
为原子序数依次增大的短周期非金属元素,根据结构式可知,M为H元素,Y为N元
素,Z为P元素。
【详解】A.电子层数越多,半径越大,电子层数相同,核电荷数越小,半径越大,
则原子半径由大到小的顺序为: ,A正确;
B.N原子属于半充满状态,第一电离能较高,H原子比C原子半径小得多,核外电子
受到原子核的引力大,电离需要更多的能量,故H>C,而Cu的电子层数最大,较容
易失去一个电子,其第一电离能最小,故第一电离能由大到小的顺序为: ,
B错误;
C.该配合物中与W形成配位键的X,不满足8电子稳定结构,C错误;
D.该配合物中X的价层电子对有4和3,故其杂化类型有 ,D错误;
故选A。
20.布洛芬具有抗炎、镇痛、解热作用,但口服该药对胃、肠道有刺激性,可以对该
分子进行如图所示修饰。下列说法错误的是
A.布洛芬是苯甲酸的同系物
B.该修饰过程原子利用率小于100%
资料收集整理【淘宝店铺:向阳百分百】C.X分子中的碳原子有 、 两种杂化形式
D.X分子中有10种化学环境不同的氢原子
【答案】D
【详解】A.布洛芬中含有羧基和饱和烷烃基,是苯甲酸的同系物,A正确;
B.该修饰过程发生取代反应,所以原子利用率小于100%,B正确;
C.X分子中本换上的碳原子有 杂化,饱和碳原子为 杂化,C正确;
D.根据X分子结构,含有12种化学环境不同的氢原子,D错误;
故选D。
资料收集整理【淘宝店铺:向阳百分百】