文档内容
专题 03 离子反应方程式与离子共存
1.(2022·吉林省吉林市第一次调研)常温下,下列各组离子在指定溶液中一定能大量共存的是 ( )
A.pH=12的溶液中:K+、Na+、Br-、AlO
B. =10-12的溶液中:NH 、Cu2+、CO 、SO
C.滴加KSCN溶液显红色的溶液中:NH 、K+、Cl-、I-
D.水电离的c(OH−)=1×10−13mol·L-1的溶液中:K+、Cl−、CHCOO−、Cu2+
3
2.(2022·山东省济南市历城第二中学模拟)某溶液含有K+、Fe3+、SO 、CO 、I-中的几种。取样,
滴加KSCN溶液后显血红色。为确定该溶液的组成,还需检验的离子是 ( )
A.K+ B.I- C.SO D.CO
3.(2022·山西省榆社中学模拟)某溶液中可能含有H+、NH 、Mg2+、Al3+、Fe3+、CO 、SO 、NO
中的几种。
①若加入锌粒,产生无色无味的气体;
②若加入NaOH溶液,产生白色沉淀,且产生的沉淀量与加入NaOH的物质的量之间的关系如图所示。则
下列说法正确的是( )
A.溶液中的阳离子只有H+、Mg2+、Al3+
B.溶液中n(NH )=0.2 mol
C.溶液中一定不含CO ,可能含有SO 和NO
D.n(H+)∶n(Al3+)∶n(Mg2+)=1∶1∶1
4.(2022·浙江省杭州第二中学模拟)下列离子方程式正确的是 ( )
A.碳酸氢钠溶液中加入氢氧化钠溶液:HCO +OH-=CO +H O
2 2
B.向 Fe(OH) 中加入氢碘酸溶液:Fe(OH) +3H+= Fe3++3H O
3 3 2
C.NaSO 与稀 HSO 混合:SO +2H+= S↓+SO ↑+H O
2 2 3 2 4 2 2 2
D.铜和浓硝酸反应:3Cu+8H++2NO =3Cu2++2NO↑+4HO
25.(2022·黑龙江省伊春市伊美区第二中学模拟)下列指定反应的离子方程式正确的是 ( )
A.将铜插入稀硝酸中:Cu+4H++2NO–=Cu2++2NO↑+H O
3 2 2
B.向Fe (SO ) 溶液中加入过量铁粉:Fe3++Fe=2Fe2+
2 4 3
C.向Al (SO ) 溶液中加入过量氨水:Al3++3NH·H O=Al(OH) ↓+3NH+
2 4 3 3 2 3 4
D.向NaSiO 溶液中滴加稀盐酸:NaSiO+2H+=H SiO↓+2Na+
2 3 2 3 2 3
6.(2022·安徽省马鞍山市模拟)制备(NH )Fe(SO )·6H O的实验中,需对过滤出产品的母液(pH<1)进行
4 2 4 2 2
处理。室温下,分别取母液并向其中加入指定物质,反应后的溶液中主要存在的一组离子正确的是 (
)
A.通入过量Cl:Fe2+、H+、NH +、Cl–、SO 2–
2 4 4
B.加入少量NaClO溶液:NH +、Fe2+、H+、SO 2–、ClO–
4 4
C.加入过量NaOH溶液:Na+、Fe2+、NH +、SO 2–、OH–
4 4
D.加入过量NaClO和NaOH的混合溶液:Na+、SO 2–、Cl–、ClO–、OH–
4
1.(2022·云贵川桂四省联合考试)下列指定反应的离子方程式书写正确的是( )
A.四氧化三铁溶于足量稀硝酸:3Fe O+28H++ =9Fe3+ +NO↑+14HO
3 4 2
B.工业上生产漂白粉的原理:Cl +2OH-= C1- +ClO- +H O
2 2
C.向硫酸氢铵溶液中滴入少量氢氧化钠溶液: +OH-=NH· H O
3 2
D.向酸性高锰酸钾溶液中滴入少量HO 溶液: +6H ++7H O=2Mn2++6O ↑+10H O
2 2 2 2 2 2
2.(2022·湖南省永州市第一次模拟)下列离子反应方程式正确的是( )
A.向硫酸铝溶液中滴加碳酸钠溶液:2Al3++3CO =Al(CO)↓
2 3 3
B.氧化亚铁溶于稀硝酸:FeO+2H+=Fe2++HO
2
C.向碳酸氢铵溶液中加入足量石灰水: Ca2++HCO +OH-=CaCO ↓+HO
3 2
D.向硫化钠溶液中通入过量SO :2S2-+5SO +2HO=3S↓+4HSO
2 2 2
3.(2022·吉林省吉林市第一次调研)由硫铁矿烧渣(主要成分:Fe O、Fe O 和FeO)得到绿矾
3 4 2 3
(FeSO ·7H O),再通过绿矾制备铁黄[FeO(OH)]的流程:烧渣 溶液 绿矾
4 2
铁黄。已知:FeS 和铁黄均难溶于水。下列说法正确的是( )
2
A.步骤①可用盐酸来溶解烧渣
B.步骤②涉及的离子反应为S2-+8Fe3++4H O=8Fe2++SO +8H+
2
C.步骤③将溶液加热到有少量晶膜出现时停止加热,再冷却结晶析出绿矾
D.步骤④反应条件控制时要让氨气过量,控制强碱性环境,可以提高产品纯度
4.(2022·福建省龙岩市模拟)某混合溶液中可能含有的离子如下表所示:可能大量含有的阳离子 H+、Ag+、Mg2+、Al3+、NH 、Fe3+
可能大量含有的阴离子 Cl-、Br-、I-、CO 、[Al(OH) ]‒
4
为探究其成分,进行了以下探究实验。
(1)探究一:甲同学取一定量的混合溶液,向其中逐滴加入氢氧化钠溶液,产生沉淀的物质的量(n)与加入氢
氧化钠溶液的体积(V)的关系如图所示:
①该溶液中一定不存在的阳离子是___________,写出含有的阳离子及其对应的物质的量浓度之比为
__________________。
②写出向其中逐滴加入氢氧化钠溶液体积为5V→8V 过程中发生反应的离子方程式_____________。
0 0
(2)探究二:乙同学检测到该溶液中含有大量的Cl-、Br-、I-,若向1 L该混合溶液中通入一定量的Cl,
2
溶液中Cl-、Br-、I-的物质的量与通入Cl 的体积(标准状况)的关系如下表所示,分析后回答下列问
2
题:
Cl 的体积(标准状况) 11.2 L 22.4 L 28.0 L
2
n(Cl-) 2.5 mol 3.5 mol 4.0 mol
n(Br-) 3.0 mol 2.5 mol 2.0 mol
n(I-) x mol 0 0
①当起始至通入Cl 的体积为11.2 L(标准状况)时,溶液中发生反应的离子方程式为_______。
2
②上表中x= ______ mol。
③原溶液中I- 的物质的量浓度为______。
5.(2022·山东省济宁市兖州区教学研究室高三期中)铈、铬、钛、镍虽不是中学阶段常见的金属元素,但
在工业生产中有着重要作用。
(1)二氧化铈(CeO)在平板电视显示屏中有着重要应用。CeO 在稀硫酸和HO 的作用下可生成Ce3+,CeO
2 2 2 2 2
在该反应中作___________剂。
(2)自然界Cr主要以+3价和+6价存在。+6价的Cr能引起细胞的突变,可以用亚硫酸钠将其还原为+3价的
铬。完成并配平下列离子方程式:___________
___________Cr O2-+___________ SO 2-+ =___________Cr3++___________ SO 2-+___________HO
2 7 3 4 2
(3)钛(Ti)被誉为“二十一世纪的金属”,工业上在550℃时用钠与四氯化钛反应可制得钛,该反应的化学方
程式是___________。
(4) NiSO ·xHO是一种绿色易溶于水的晶体,广泛用于镀镍、电池等,可由电镀废渣(除镍外,还含有铜、
4 2
锌、铁等元素)为原料获得。操作步骤如下:①向滤液Ⅰ中加入FeS是为了除去 、 等杂质。
②对滤液Ⅱ先加HO 再调pH,调pH的目的是___________。
2 2
③滤液Ⅲ溶质的主要成分是NiSO ,加NaCO 过滤后,再加适量稀硫酸溶解又生成NiSO ,这两步操作的
4 2 3 4
目的是___________。
④为测定NiSO ·xHO晶体中x的值,称取26.3g晶体加热至完全失去结晶水,剩余固体15.5g,则x的值等
4 2
于___________。
6.(2022·重庆市名校联盟高三第一次联考)某透明溶液中可能含有 、Fe3+、Al3+、NH +、 、I-、NO -、
4 3
SO 2-中的几种,为了确认溶液中离子的存在情况,分别取等量的试液装入5支试管里,做如下实验:
4
①测定溶液的pH,溶液呈强酸性;
②向溶液中加入足量稀硫酸和铜粉,振荡溶液充分反应,产生某种无色气体1.12L(标准状况),该气体遇到
空气立即变红棕色气体;
③向溶液中滴加过量氢氧化钠溶液,过滤、洗涤、灼烧、称重,得固体质量为3.2g;
④向溶液中加入过量浓氢氧化钠溶液,加热,收集到气体1.12L(标准状况);
⑤向溶液中加入足量氯化钡溶液,过滤、洗涤、干燥、称重,得固体2.33g;
回答下列问题:
(1)请写出铝元素在元素周期表中的位置___________。
(2)由实验①和②可知,该溶液中一定不存在的离子是___________,写出实验②中反应生成无色气体的离
子方程式___________。
(3)实验④中收集到气体的电子式为:___________,该反应的离子方程式为:___________。
(4)根据以上实验,你认为该溶液中是否一定存在Cl-?___________(填“是”或者“否”);若存在 ,1
份溶液中其物质的量的范围为___________,如何用实验方法证明其存在___________(用简明的文字表述操
作方法、现象以及结论;若不存在 ,后面两空不用填写)
7.(2022·广东省深圳市第七高级中学高一月考)(1)有一种“地康法”制取氯气的反应原理如下所示:
①反应I的离子方程式为________________________________。
②反应II属于____________反应。(填四种基本反应类型之一)
(2)有A、B、C、D四种可溶性盐,它们的阳离子分别是Ba2+、Ag+、Na+、Cu2+中的某一种,阴离子分别
是NO -、SO 2-、Cl-、CO2-中的一种(离子在物质中不重复出现)。
3 4 3
①若把四种盐分别溶于盛有蒸馏水的四支试管中,只有C盐的溶液呈蓝色;②若向四支试管中分别加入盐酸,B盐的溶液有沉淀生成,D盐的溶液有无色无味的气体逸出。
请回答下列问题:
①A的化学式为__________,B的化学式为__________ ,C的化学式为____________。
②写出D与足量CHCOOH溶液反应的离子方程式_______________________。
3
③写出A溶液中阴离子的检验方法_____________________________________。
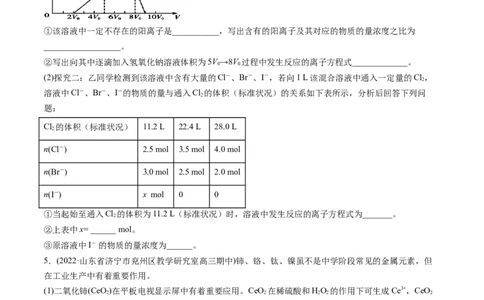
8.(2022·浙江省宁波市高三选考模拟)由五种元素组成的化合物X,某学习小组按如图流程进行探究实验。
已知:化合物X难溶于水;气体体积均在标准状况下测定,气体A能使品红溶液褪色,气体E在标况下的
密度为0.76g/L,固体C呈紫红色。
请回答:
(1)写出气体E的结构式______________;溶液B中含有的溶质(除了HSO )有______________(用化学式表
2 4
示)。
(2)化合物X含有的元素有Cu、H、______________(写出另外三种元素)。写出步骤1反应的化学方程式
___。
(3)一定条件下,往溶液B中通入气体A和E,可制备化合物X,写出该反应的离子方程式
_________________________。
(4)气体E可将Fe O 还原得到黑色固体(不含Fe O),请设计实验验证黑色固体的成分
2 3 3 4
_______________________________________________。