文档内容
专题 03 离子反应
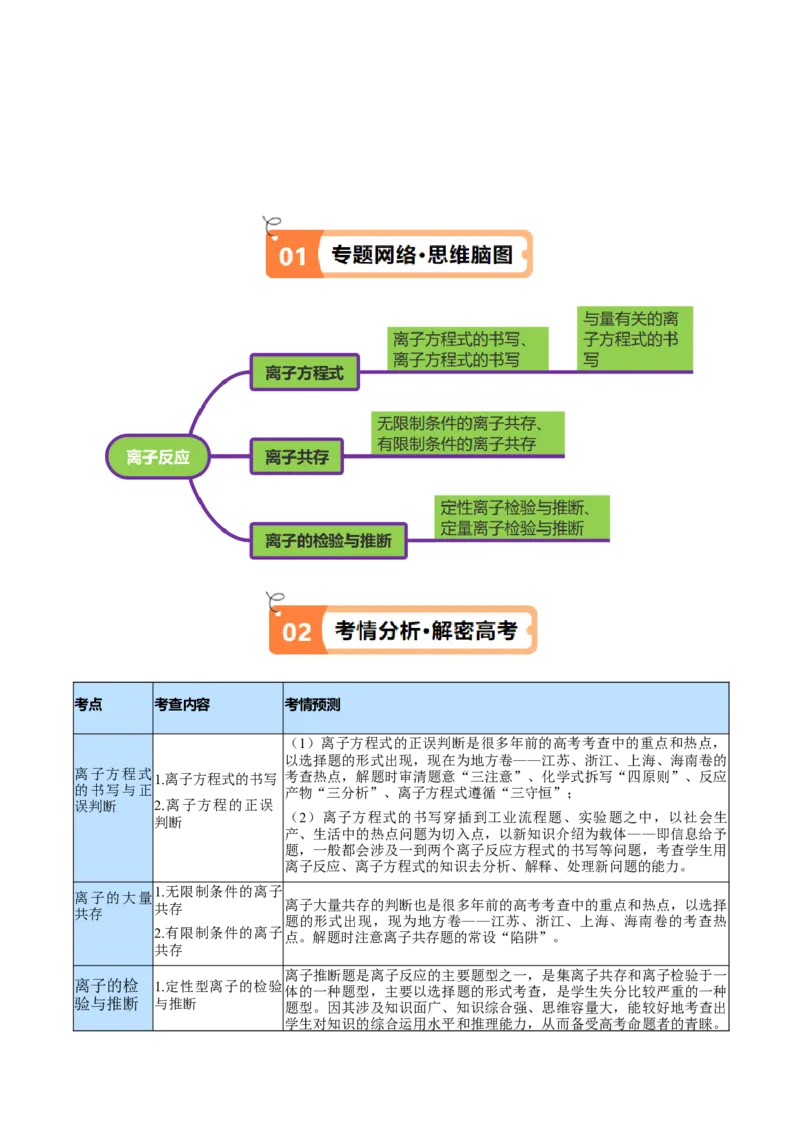
01专题网络·思维脑图
02考情分析·解密高考
03高频考点·以考定法
考点一 离子方程式的书 考点二 离子的大量共存 考点三 离子的检验与推断
写与正误判断 【高考解密】 【高考解密】
【高考解密】 命题点01 无附加条件的离子 命题点01 定量型离子检验与推
命题点01 离子方程式的正误 共存 断
判断 命题点02 有附加条件的离子 命题点02 定量型离子检验与推
命题点02 信息型离子方程式 共存 断
的书写 【技巧解密】 【技巧解密】
【技巧解密】 【考向预测】 【考向预测】
【考向预测】
04核心素养·微专题
微专题 多种方法突破与量有关的离子方程式的书写考点 考查内容 考情预测
(1)离子方程式的正误判断是很多年前的高考考查中的重点和热点,
以选择题的形式出现,现在为地方卷——江苏、浙江、上海、海南卷的
离子方程式 1.离子方程式的书写 考查热点,解题时审清题意“三注意”、化学式拆写“四原则”、反应
的书写与正 产物“三分析”、离子方程式遵循“三守恒”;
误判断 2.离子方程的正误
(2)离子方程式的书写穿插到工业流程题、实验题之中,以社会生
判断
产、生活中的热点问题为切入点,以新知识介绍为载体——即信息给予
题,一般都会涉及一到两个离子反应方程式的书写等问题,考查学生用
离子反应、离子方程式的知识去分析、解释、处理新问题的能力。
1.无限制条件的离子
离子的大量
共存 离子大量共存的判断也是很多年前的高考考查中的重点和热点,以选择
共存
题的形式出现,现为地方卷——江苏、浙江、上海、海南卷的考查热
2.有限制条件的离子点。解题时注意离子共存题的常设“陷阱”。
共存
离子推断题是离子反应的主要题型之一,是集离子共存和离子检验于一
离子的检 1.定性型离子的检验
体的一种题型,主要以选择题的形式考查,是学生失分比较严重的一种
验与推断 与推断 题型。因其涉及知识面广、知识综合强、思维容量大,能较好地考查出
学生对知识的综合运用水平和推理能力,从而备受高考命题者的青睐。2.定量型离子的检验
解题时应用离子共存和离子检验知识解答。
与推断
考点一 离子方程式的书写与正误判断
命题点01 离子方程式的正误判断
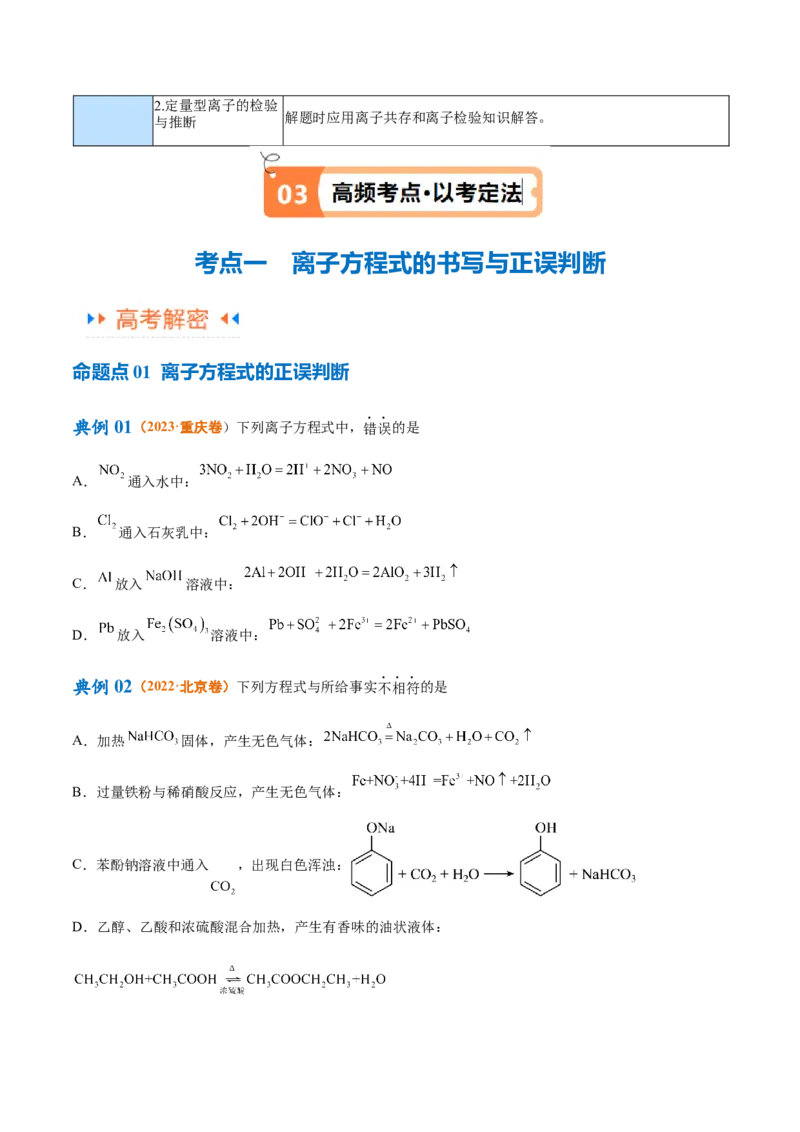
典例01(2023·重庆卷)下列离子方程式中,错误的是
A. 通入水中:
B. 通入石灰乳中:
C. 放入 溶液中:
D. 放入 溶液中:
典例02(2022·北京卷)下列方程式与所给事实不相符的是
A.加热 固体,产生无色气体:
B.过量铁粉与稀硝酸反应,产生无色气体:
C.苯酚钠溶液中通入 ,出现白色浑浊:
D.乙醇、乙酸和浓硫酸混合加热,产生有香味的油状液体:典例03(2021·湖北卷)对于下列实验,不能正确描述其反应的离子方程式是
A.向氢氧化钡溶液中加入盐酸:H++OH-=H O
2
B.向硝酸银溶液中滴加少量碘化钾溶液:Ag++I-=AgI↓
C.向烧碱溶液中加入一小段铝片:2Al+2OH-+6H O=2[Al(OH) ]-+3H ↑
2 4 2
D.向次氯酸钙溶液中通入少量二氧化碳气体:ClO-+CO +H O=HClO+HCO
2 2
命题点02 信息型离子方程式的书写
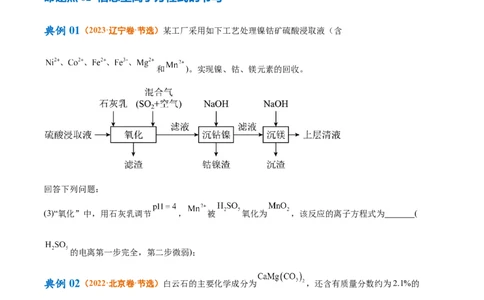
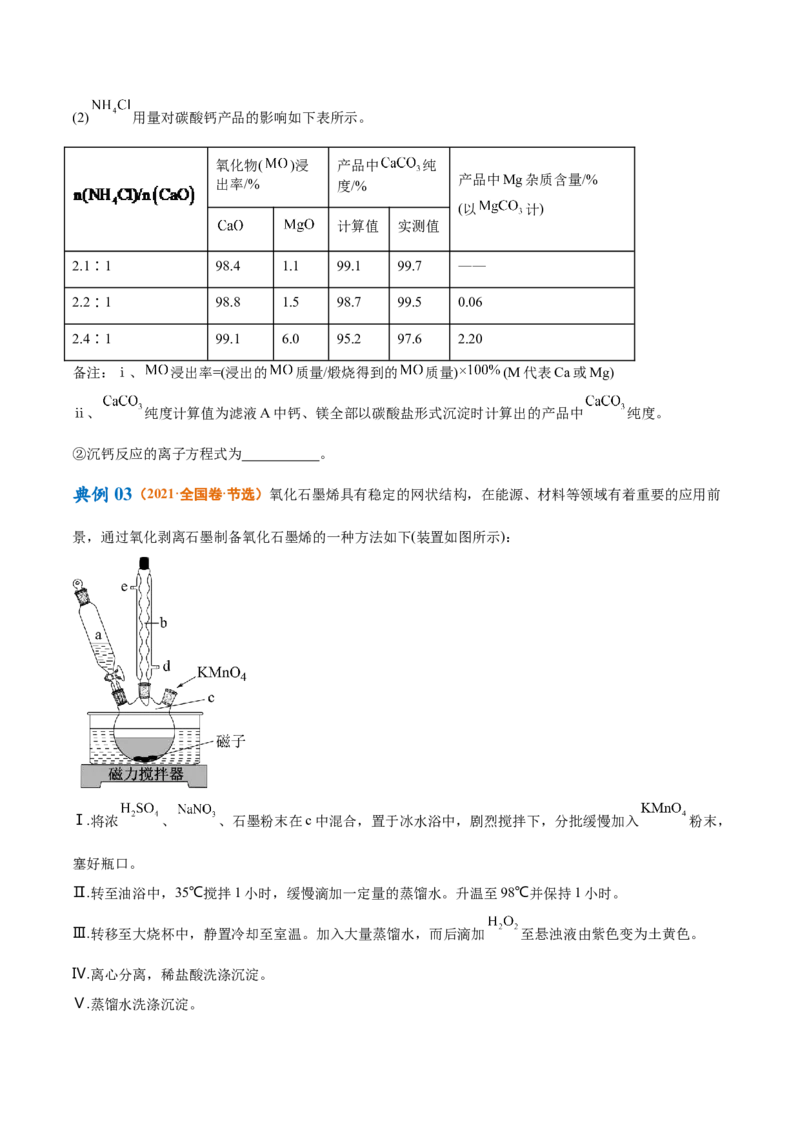
典例01(2023·辽宁卷·节选)某工厂采用如下工艺处理镍钴矿硫酸浸取液(含
和 )。实现镍、钴、镁元素的回收。
回答下列问题:
(3)“氧化”中,用石灰乳调节 , 被 氧化为 ,该反应的离子方程式为 (
的电离第一步完全,第二步微弱);
典例02(2022·北京卷·节选)白云石的主要化学成分为 ,还含有质量分数约为2.1%的
Fe O 和1.0%的SiO。利用白云石制备高纯度的碳酸钙和氧化镁,流程示意图如下。
2 3 2(2) 用量对碳酸钙产品的影响如下表所示。
氧化物( )浸 产品中 纯
产品中Mg杂质含量/%
出率/% 度/%
(以 计)
计算值 实测值
2.1∶1 98.4 1.1 99.1 99.7 ——
2.2∶1 98.8 1.5 98.7 99.5 0.06
2.4∶1 99.1 6.0 95.2 97.6 2.20
备注:ⅰ、 浸出率=(浸出的 质量/煅烧得到的 质量) (M代表Ca或Mg)
ⅱ、 纯度计算值为滤液A中钙、镁全部以碳酸盐形式沉淀时计算出的产品中 纯度。
②沉钙反应的离子方程式为 。
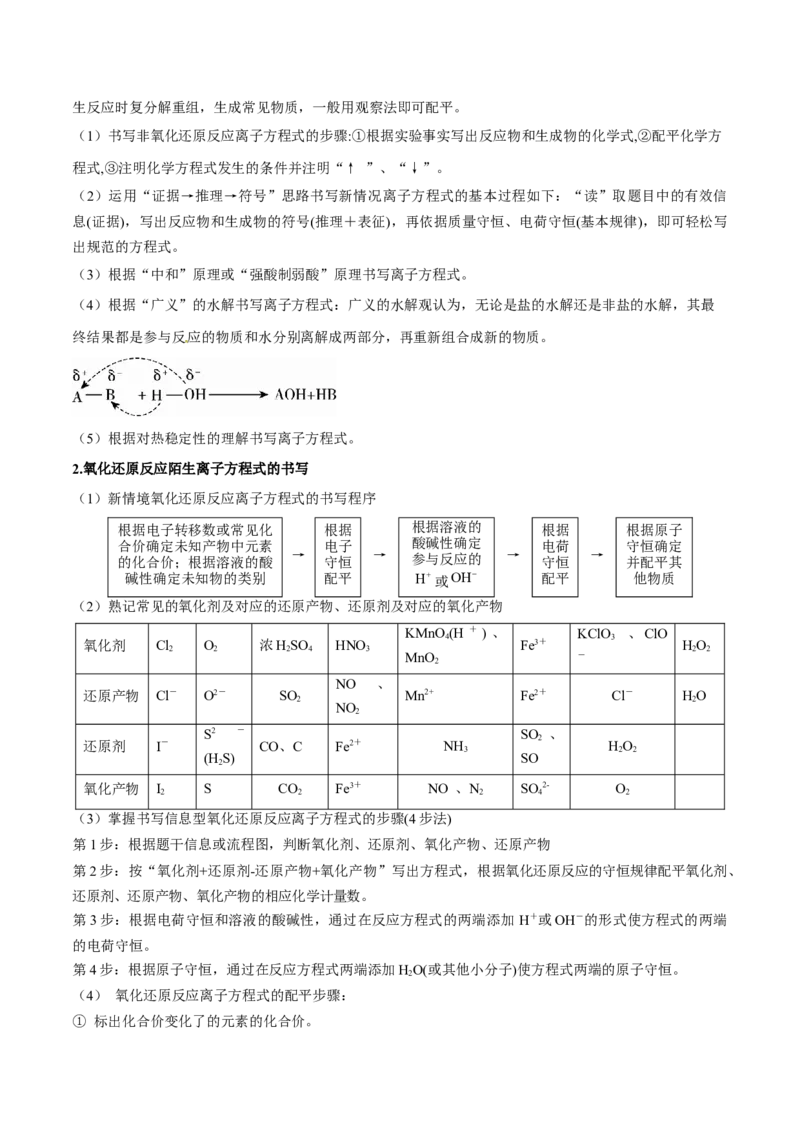
典例03(2021·全国卷·节选)氧化石墨烯具有稳定的网状结构,在能源、材料等领域有着重要的应用前
景,通过氧化剥离石墨制备氧化石墨烯的一种方法如下(装置如图所示):
Ⅰ.将浓 、 、石墨粉末在c中混合,置于冰水浴中,剧烈搅拌下,分批缓慢加入 粉末,
塞好瓶口。
Ⅱ.转至油浴中,35℃搅拌1小时,缓慢滴加一定量的蒸馏水。升温至98℃并保持1小时。
Ⅲ.转移至大烧杯中,静置冷却至室温。加入大量蒸馏水,而后滴加 至悬浊液由紫色变为土黄色。
Ⅳ.离心分离,稀盐酸洗涤沉淀。
Ⅴ.蒸馏水洗涤沉淀。Ⅵ.冷冻干燥,得到土黄色的氧化石墨烯。
回答下列问题:
(4)步骤Ⅲ中, 的作用是 (以离子方程式表示)。
一、离子方程式的正误判断
1、判断离子方程式正误的四个关键点
注意反应环境
审清题意“三注意” 注意操作顺序
注意反应物之间量的关系
易溶强电解质拆,弱电解质、难溶物不拆
微溶物清拆浊不拆
化学式拆写“四原则”
单质、氧化物不拆
浓硫酸不拆,浓盐酸、浓硝酸、稀硫酸拆
分析量不同时的产物
反应产物“三分析” 分析是否漏掉同步反应
分析变价元素的产物
原子是否守恒
方程式遵循“三守恒” 电荷是否守恒
电子转移是否守恒
2.判断离子方程式正误的基本方法
二、信息给予型离子方程式的书写
1.非氧化还原反应陌生离子方程式的书写
新情境下非氧化还原类离子方程式的书写,因没有涉及元素化合物的变化,故组成物质的各元素在发生反应时复分解重组,生成常见物质,一般用观察法即可配平。
(1)书写非氧化还原反应离子方程式的步骤:①根据实验事实写出反应物和生成物的化学式,②配平化学方
程式,③注明化学方程式发生的条件并注明“↑ ”、“↓”。
(2)运用“证据→推理→符号”思路书写新情况离子方程式的基本过程如下:“读”取题目中的有效信
息(证据),写出反应物和生成物的符号(推理+表征),再依据质量守恒、电荷守恒(基本规律),即可轻松写
出规范的方程式。源:学科网ZXXK]
(3)根据“中和”原理或“强酸制弱酸”原理书写离子方程式。
(4)根据“广义”的水解书写离子方程式:广义的水解观认为,无论是盐的水解还是非盐的水解,其最
终结果都是参与反应的物质和水分别离解成两部分,再重新组合成新的物质。
(5)根据对热稳定性的理解书写离子方程式。
2.氧化还原反应陌生离子方程式的书写
(1)新情境氧化还原反应离子方程式的书写程序
根据电子转移数或常见化 根据 根据溶液的 根据 根据原子
合价确定未知产物中元素 电子 酸碱性确定 电荷 守恒确定
→ → → →
的化合价;根据溶液的酸 守恒 参与反应的 守恒 并配平其
碱性确定未知物的类别 配平 H或OH 配平 他物质
(2)熟记常见的氧化剂及对应的还原产物、还原剂及对应的氧化产物
KMnO (H + ) 、 KClO 、ClO
4 3
氧化剂 Cl O 浓HSO HNO Fe3+ HO
2 2 2 4 3 2 2
MnO -
2
NO 、
还原产物 Cl- O2- SO Mn2+ Fe2+ Cl- HO
2 2
NO
2
S2 - SO 、
2
还原剂 I- CO、C Fe2+ NH HO
3 2 2
(H S) SO
2
氧化产物 I S CO Fe3+ NO 、N SO 2- O
2 2 2 4 2
(3)掌握书写信息型氧化还原反应离子方程式的步骤(4步法)
第1步:根据题干信息或流程图,判断氧化剂、还原剂、氧化产物、还原产物
第2步:按“氧化剂+还原剂-还原产物+氧化产物”写出方程式,根据氧化还原反应的守恒规律配平氧化剂、
还原剂、还原产物、氧化产物的相应化学计量数。
第3步:根据电荷守恒和溶液的酸碱性,通过在反应方程式的两端添加 H+或OH-的形式使方程式的两端
的电荷守恒。
第4步:根据原子守恒,通过在反应方程式两端添加HO(或其他小分子)使方程式两端的原子守恒。
2
(4) 氧化还原反应离子方程式的配平步骤:
① 标出化合价变化了的元素的化合价。② 列变化:分别标出化合价升高数和化合价降低数
③ 根据化合价升降总数相等确定发生氧化还原反应的物质的化学计量数。
④ 利用元素守恒,观察配平其他物质
(5)“补缺”的技巧
缺项离子方程式的配平:
配平离子方程式时,有时要用H+、OH-、HO来使化学方程式两边电荷及原子守恒,总的原则是酸性溶液
2
中不能出现OH-,碱性溶液中不能出现H+,具体方法如下:
酸性环境 碱性环境
反应物中少氧 左边加HO,右边加H+ 左边加OH-,右边加HO
2 2
反应物中多氧 左边加H+,右边加HO 左边加HO,右边加OH-
2 2
注:绝不可能出现的情况:H+→OH- 或者OH-→H+。
考向01 离子方程式的正误判断
1.(2023·四川资阳·统考一模)下列反应的离子方程式正确的是
A.铜与稀硝酸反应:
B.铅酸蓄电池放电时的负极反应:
C.用 溶液吸收少量 :
D.明矾溶液与过量氨水混合:
2.(2023·浙江宁波·统考模拟预测)下列过程中对应的离子方程式正确的是
A.向苯酚钠溶液中通入少量 :
B.酚酞滴入碳酸钠溶液中变红:
C.同浓度同体积明矾 溶液与 溶液混合:
D.用醋酸和淀粉 溶液检验加碘盐中的 :3.(2024·广西北海·统考一模)下列过程中的化学反应,相应的离子方程式正确的是
A. 在碱性环境中被空气氧化:
B.氢氧化铁加入氢碘酸溶液中:
C.用铁作阳极电解氯化镁溶液:
D.碳酸钙加入乙酸溶液中:
4.(2023·四川绵阳·统考一模)下列化学用语表达正确,且与所给事实相符的是
A.滴加酚酞的苏打水呈红色:CO +2H O=3HCO+2OH-
2 2 3
B.铁在潮湿空气中生成红褐色的铁锈,其负极的电极反应:Fe-3e-=Fe3+
C.用醋酸和淀粉-KI溶液检验加碘食盐中的IO :IO +5I-+6H+=3I +3H O
2 2
D.硫化钠溶液久置后出现浑浊:2NaS+O+2H O=2S↓+4NaOH
2 2 2
5.(2023·四川雅安·统考模拟预测)下列化学用语对事实的表述正确的是
A.氢氧化镁固体溶于盐酸:
B.水溶液中HCO 的电离方程式:
2 3
C.NaHS的水解反应:
D.钠跟水反应的离子方程式:
考向02 信息型离子方程式的书写
1.(2023·福建福州·统考模拟预测)用含 的溶液吸收工业尾气中的 和NO,获得 和
产品的工艺流程如下:下列说法错误的是
A.装置Ⅰ加入NaOH溶液是为了吸收
B.装置Ⅱ中反应后溶液pH减小
C.装置Ⅲ中阴极反应式为
D.装置Ⅳ中反应的条件是高温、高压、催化剂
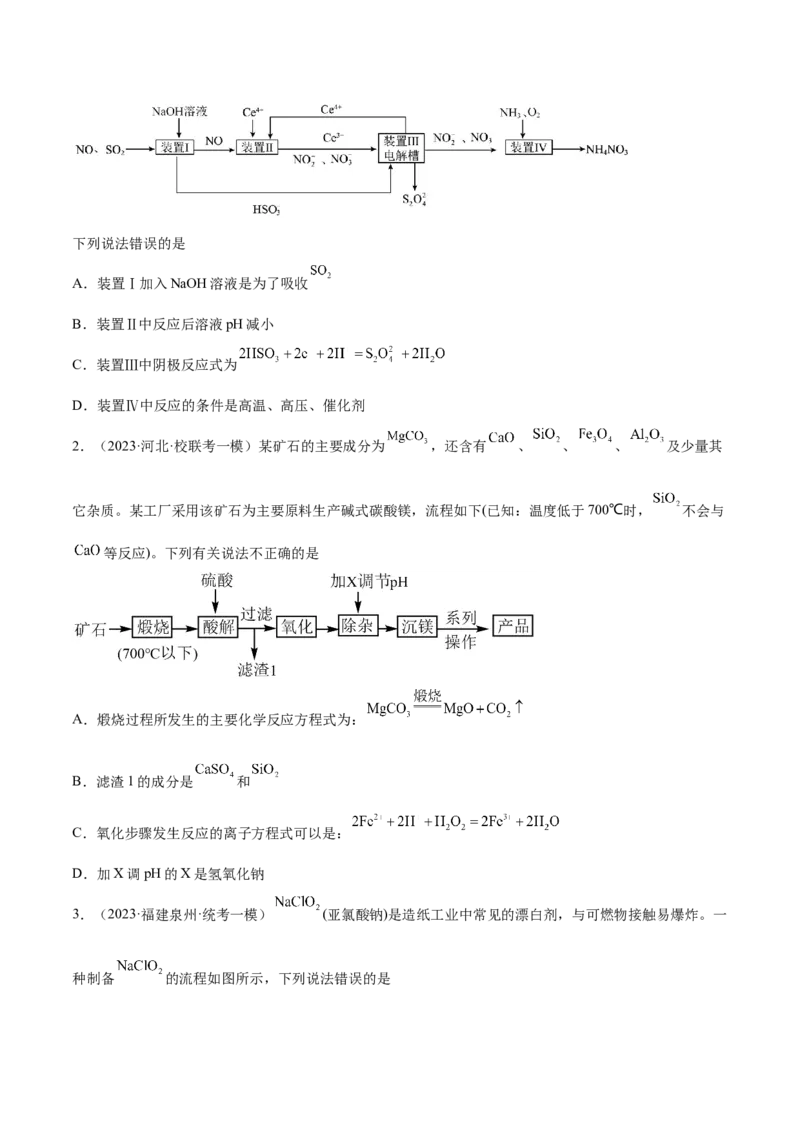
2.(2023·河北·校联考一模)某矿石的主要成分为 ,还含有 、 、 、 及少量其
它杂质。某工厂采用该矿石为主要原料生产碱式碳酸镁,流程如下(已知:温度低于700℃时, 不会与
等反应)。下列有关说法不正确的是
A.煅烧过程所发生的主要化学反应方程式为:
B.滤渣1的成分是 和
C.氧化步骤发生反应的离子方程式可以是:
D.加X调pH的X是氢氧化钠
3.(2023·福建泉州·统考一模) (亚氯酸钠)是造纸工业中常见的漂白剂,与可燃物接触易爆炸。一
种制备 的流程如图所示,下列说法错误的是A. 的漂白原理与 相似
B.气体1、气体2分别是 、
C.反应3的离子方程式:
D.“分离”操作过程包括结晶、过滤、乙醇洗涤等
4.(2023·辽宁鞍山·鞍山一中校考模拟预测)实验室可通过下列方法制备亚硫酸氢钠晶体,已知:
①反应Ⅰ和反应Ⅱ始终在恒温40℃的容器中进行
②实验过程中隔绝氧气
③ : ; ; ; ;
下列说法正确的是
A.反应Ⅰ的离子方程式为
B.在反应Ⅱ发生的过程中会产生大量的气体
C.反应I、II结束后,反应Ⅱ所得溶液中水的电离程度强于反应Ⅰ所得溶液中水的电离程度
D.亚硫酸氢钠溶液中:
5.(2023·湖南岳阳·统考三模)以黄铁矿(主要成分是FeS,含少量SiO)和软锰矿(主要成分是MnO ,含
2 2 2
少量Fe O、Al O)为原料制备MnSO ·H O的工艺流程如下。下列说法正确的是
2 3 2 3 4 2A.酸浸和沉锰操作均应在较高温度下进行
B.滤渣1的成分中含有S和SiO
2
C.调pH的目的只为除去溶液中的Fe3+
D.沉锰操作中主要反应的离子方程式是 2HCO +Mn2+ = MnCO ↓ +CO ↑+ H O
3 2 2
考点二 离子的大量共存
命题点01 无限制离子的大量共存
典例01(2022·天津卷)25℃时,下列各组离子中可以在水溶液中大量共存的是
A. 、 、 、 B. 、 、 、
C. 、 、 、 D. 、 、 、
典例02(2021·湖南卷)对下列粒子组在溶液中能否大量共存的判断和分析均正确的是
粒子组 判断和分析
不能大量共存,因发生反应:
A 、 、 、
不能大量共存,因发生反应:
B 、 、 、
C 、 、 、 能大量共存,粒子间不反应
D 、 、 、 能大量共存,粒子间不反应命题点02 有限制离子的大量共存
典例01(2021·重庆卷)25°时, 下列各组离子在指定溶液中一定能大量共存的是
A.1.0 mol·L-1氯化钡溶液中: Mg2+、K+、Br-、
B.1.0 mol·L-1硫酸中: A13+、 Na+、Cl-、
C.pH=1l 的氨水中: Fe2+、 Na+、 、ClO-
D.pH=1的硝酸中: Fe3+、K+、I-、
典例02(2021·福建卷)室温下,下列各组离子一定能与指定溶液共存的是
A. 的 溶液: 、 、 、
B. 的 溶液: 、 、 、
C. 的 溶液: 、 、 、
D. 的 溶液: 、 、 、
1.正确判断离子大量共存的前提——常见离子的性质
颜色 MnO(紫红)、Cu2+(蓝)、Fe2+(浅绿)、Fe3+(黄)
氧化性 ClO-、MnO、NO(H+)、Fe3+、Cr O
2
还原性 S2-(HS-)、SO(HSO)、I-、Br-、Fe2+
水解显酸性 Al3+、Mg2+、NH、Cu2+、Fe2+、Fe3+、Zn2+
水解显碱性 AlO、S2-、SO、CO、SiO、ClO-、CHCOO-
3
两性离子 HCO、HS-、HSO、HPO、HPO
2
注:“两性离子”指既能与酸反应又能与碱反应的离子,一般为多元弱酸的酸式酸根离子。
2.突破离子共存判断中的常设“陷阱”
条件 常见表述 误点点拨类型
“无色”
Cu2+、Fe2+、Fe3+、MnO-
等有色离子不能大量存在
4
“pH=1”或“pH=13” 溶液显酸性或碱性
“因发生氧化还原反应而不能 注意是能发生氧化还原反应的离子不能大量共存,并不
大量共存” 是其他离子反应,同时要注意溶液酸碱性的影响
“透明” “透明”也可“有色”
“与Al反应放出H” 溶液既可能显酸性也可能显碱性
2
“由水电离出的 c(H+)=1×10-12
溶液既可能显酸性也可能显碱性
mol·L-1”的溶液
“通入足量的NH ” 与NH ·HO反应的离子不能大量存在
3 3 2
含有大量Fe3+的溶液 应是酸性溶液并具有强氧化性
含有大量AlO-
、S2-的溶液 应是碱性溶液
2
含有大量NO-
的溶液 隐含H+与还原性离子不能同时大量存在
3
(1)“一定大量共存”
题干
(2)“可能大量共存” 审清关键字词,仔细分析判断
要求
(3)“不能大量共存”
3.离子不能大量共存的原因
(1)离子之间相互结合生成难溶物质。如
Ca2+和CO2-
生成CaCO
,H+和SiO2-
生成HSiO,Cu2+和OH-生成
3 3 3 2 3
Cu(OH) 等。
2
(2)离子之间相互结合生成气态物质。如H+和S2-生成HS,H+和HCO-
生成CO 等。
2 3 2
(3)离子之间相互结合生成弱电解质。如H+与CHCOO-、OH-、PO3-
等分别结合生成弱电解质CHCOOH、
3 4 3
HO、HPO 等。
2 3 4
(4)离子之间彼此促进水解。如Al3+、Fe3+分别与AlO- 、HCO- 、CO2-
、S2-等发生相互促进的水解反应生成
2 3 3
沉淀或气体。
(5)离子之间发生氧化还原反应。如Fe2+、S2-、I-、SO2- 分别与NO-
(H+)、ClO-因发生氧化还原反应而不能大
3 3
量共存;Fe3+与S2-、I-等因发生氧化还原反应而不能大量共存。
(6)离子之间能发生络合反应。如Fe3+和SCN-不能大量共存。
4.离子大量共存的解题思维模型5.审离子共存题目中的5大易忽视点
(1)注意判断离子共存的情况:“能、不能”,“一定、可能、一定不能”。
(2)注意题干中提示的溶液酸碱性:酸性溶液应考虑H+的存在,碱性溶液应考虑OH-的存在。
(3)注意题干中提示的溶液颜色:溶液无色时,有色离子不能存在。
(4)注意正确理解“透明溶液”,如NaCl溶液、KOH溶液为无色透明溶液,CuSO 溶液、FeCl 溶液是有色
4 3
透明溶液,不能认为“有色”就不透明。
(5)注意题干中提示的水的电离程度:当由水电离出的c(H+)或c(OH-)小于1×10-7 mol·L-1时,溶液可能为
酸性溶液或碱性溶液;当由水电离出的c(H+)或c(OH-)大于1×10-7 mol·L-1 时,溶液可能为弱酸盐溶液
或弱碱盐溶液。
考向01 无限制条件的离子大量共存
1.(2023·广东汕头·统考二模)理解与辨析是化学学科的关键能力,下列离子在溶液中能共存的是
A.S2-、Na+、H+、 B.Fe2+、 、H+、
C. 、 、OH-、Mg2+ D. 、Al3+、Cl-、Ca2+
2.(2023·天津·校联考一模)下列各组离子,能在溶液中大量共存的是
A. 、 、 、 B. 、 、 、
C. 、 、 、 D. 、 、 、
3.(2023上·上海静安·高三校考开学考试)在强酸性条件下因发生氧化还原反应不能大量共存的是
A.Mg2+、Na+、SO 、Cl- B.K+、CO 、Cl-、NO
C.Na+、Cl-、NO 、Fe2+ D.NH 、OH-、SO 、NO
4.(2023上·湖北武汉·高三统考开学考试)下列各组粒子在溶液中能大量共存的是A. 、 、 、 B. 、 、 、
C. 、 、 、 D. 、 、 、
5.(2023下·湖北黄冈·高三统考开学考试)在无色透明溶液中,不能大量共存的离子组是
A.Cu2+、Na+、SO 、Cl- B.K+、Na+、HCO 、NO
C.OH-、HCO 、Ca2+、Na+ D.Ba2+、Na+、OH-、NO
考向02 有限制条件的离子大量共存
1.(2023·湖北武汉·华中师大一附中校考模拟预测)向下列溶液中逐渐通入 至过量,最终体系中无沉
淀的是
A. B.
C. D.
2.(2023·重庆九龙坡·重庆市育才中学校考模拟预测)25℃时,下列各组离子在指定溶液中一定能大量共
存的是
A.pH=1的溶液中:Na+、NH 、[Ag(NH)]+、NO
3 2
B.麦芽糖溶液中:MnO 、Na+、SO 、H+
C.澄清透明的溶液中:Cu2+、Al3+、SO 、NO
D.能使甲基橙变为红色的溶液中:Fe2+、K+、Cl-、NO
3.(2023·青海海东·统考三模)下列各组离子在指定溶液中能大量共存的是
A.0.1mol·L-1NaHCO 溶液中:H+、Mg2+、Cl-、
3
B.0.1mol·L-1FeCl 溶液中:Fe2+、 、I-、
3
C.0.1mol·L-1HCl溶液中:Fe2+、 、Br-、D.0.1mol·L-1NaOH溶液中:K+、Ba2+、 、Br-
4.(2023·重庆沙坪坝·重庆一中校考模拟预测)常温下,下列各组离子在指定溶液中一定能大量共存的是
A.使甲基橙试液变红的溶液:
B.通入足量 的溶液:
C.通入足量 的溶液:
D.水电离的 的溶液:
5.(2023·河北邢台·邢台市第二中学校联考三模)下列各组离子在指定溶液中能大量共存的是
A. 的 溶液中: 、 、 、
B.使pH试纸显红色的溶液中: 、 、 、
C.含有KSCN的溶液中: 、 、 、
D. 的溶液中: 、 、 、
考点三 离子的检验与推断
命题点01 定性型离子检验与推断
典例01(2022·全国卷)某白色粉末样品,可能含有 、 、 和 。取少量样
品进行如下实验:
①溶于水,得到无色透明溶液
②向①的溶液中滴加过量稀盐酸,溶液变浑浊,有刺激性气体逸出。离心分离。
③取②的上层清液,向其中滴加 溶液有沉淀生成。
该样品中确定存在的是A. B. C. D.
典例02(2020·全国卷)某白色固体混合物由NaCl、KCl、MgSO 、CaCO 中的两种组成,进行如下实验:
4 3
① 混合物溶于水,得到澄清透明溶液;② 做焰色反应,通过钴玻璃可观察到紫色;③ 向溶液中加碱,
产生白色沉淀。根据实验现象可判断其组成为
A.KCl、NaCl B.KCl、MgSO
4
C.KCl、CaCO D.MgSO 、NaCl
3 4
命题点02 定量型离子检验与推断
典例01(2016·浙江卷)某固体可能含有NH +、Cu2+、Na+、Cl-、CO2-、SO 2-中的几种离子,取等质量的
4 3 4
两份该固体,进行如下实验(不考虑盐类的水解及水的电离);(1)一份固体溶于水得无色透明溶液,
加入足量BaCl 溶液,得沉淀6.63g,在沉淀中加入过量稀盐酸,仍有4.66g沉淀。
2
(2)另一份固体与过量NaOH固体混合后充分加热,产生使湿润的红色石蕊试纸变蓝色的气体0.672L
(标准状况)。
下列说法正确的是
A.该固体中一定含有NH +、CO2-、SO 2-、Na+ B.该固体中一定没有Cu2+、Cl-、Na+
4 3 4
C.该固体中只含有NH +、CO2-、SO 2-、Cl- D.根据以上实验,无法确定该固体中有Na+
4 3 4
典例02(2013·上海卷)某溶液可能含有Cl-、SO 2-、CO2-、NH +、Fe3+、Al3+和K+。取该溶液100mL,
4 3 4
加入过量NaOH溶液,加热,得到0.02mol气体,同时产生红褐色沉淀;过滤,洗涤,灼烧,得到1.6g
固体;向上述滤液中加足量BaCl 溶液,得到4.66g不溶于盐酸的沉淀。由此可知原溶液中
2
A.至少存在5种离子
B.Cl-一定存在,且c(Cl-)≥0.4mol/L
C.SO 2-、NH +、一定存在,Cl-可能不存在
4 4
D.CO2-、Al3+一定不存在,K+可能存在
3
一、离子检验
1.常见离子检验的特征反应及现象
1)常见阳离子的检验。(1)常规检验法。
①用NaOH溶液能检验出Cu2+、Fe3+、Fe2+、Al3+、NH。
离子 实验现象
Cu2+ 产生蓝色沉淀
Fe3+ 产生红褐色沉淀
Fe2+ 先产生白色沉淀,迅速变灰绿色,最后变红褐色沉淀
Al3+ 先生成白色胶状沉淀,继续加入NaOH溶液,白色胶状沉淀又逐渐溶解
NH 共热,产生使湿润的红色石蕊试纸变蓝的刺激性气体
②焰色反应:用焰色反应可检验出溶液中的K+(透过蓝色钴玻璃观察焰色为浅紫色)和Na+(焰色为黄色)。
(2)特殊检验法。
离子 检验试剂 实验现象
Fe3+ KSCN溶液或碘化钾淀粉溶液 溶液变红色或溶液变蓝色
酸性高锰酸钾溶液或KSCN溶液和少量 溶液紫色褪去或溶液先无变化,后变红
Fe2+
新制氯水(稀硝酸) 色
2)常见阴离子的检验
(1)OH-:滴入石蕊试液或酚酞试液,溶液变蓝色或红色。
(2)利用盐酸和其他试剂检验。
离子 检验方法
SO 先加入稀盐酸,无现象,再加入BaCl 溶液,生成白色沉淀
2
加入BaCl 溶液,产生白色沉淀,再加入稀盐酸,产生使品红褪色的无色、有刺
2
SO
激性气味的气体
①加入BaCl 溶液,产生白色沉淀,再加入稀盐酸,产生无色无味的气体;
2
CO
②加入稀盐酸,产生使澄清石灰水变浑浊的无色无味的气体
(3)利用HNO 酸化的AgNO 溶液检验
3 3
离子 实验现象
Cl- 生成不溶于稀硝酸的白色沉淀
Br- 生成不溶于稀硝酸的浅黄色沉淀
I- 生成不溶于稀硝酸的黄色沉淀
(4) I-:滴入淀粉溶液和氯水,溶液变蓝色或滴入氯水和CCl ,溶液分层,CCl 层显紫色。
4 4
2.离子检验实验设计题常用的答题模板
(1)实验操作:取少量或适量行测液(固体溶解后再取少量或适量行测液)于一洁净试管中,加入······试剂,
再加入······试剂(有必要时可以加热,如NH +的检验)。
4
(2)现象描述:如“溶液由······变为······”,“产生······气体”,“产生······色沉淀”,“若有······生成”,
“若没有······生成”。
(3)得出结论:如“说明溶液中含有······离子”,“若·····说明·····,若·····说明·····”。二、离子推断
1.解答离子推断题的“四项基本原则”
(1)肯定性原则:根据实验现象推出溶液中肯定存在或肯定不存在的离子(记住几种常见的有色离子:Fe2+、
Fe3+、Cu2+、MnO- 、CrO2- 、CrO2-
等)。
4 4 2 7
(2)互斥性原则:在肯定某些离子存在的同时,结合离子共存规律,否定一些离子的存在(要注意题目中的隐含条
件,如:酸性、碱性、指示剂的颜色变化、与铝反应产生H2、水的电离情况等)。
(3)电中性原则:溶液呈电中性,一定既有阳离子,又有阴离子,且溶液中正电荷总数与负电荷总数相等(这一原
则可帮助我们确定一些隐含的离子)。
(4)进出性原则:通常是在实验过程中使用,是指在实验过程中反应生成的离子或引入的离子对后续实验的干扰。
2.离子推断常见解题思路
离子推断题将离子共存、离子检验设定在一个可能的离子组中,要求通过多重推断,确定某些离子肯定
存在,某些离子肯定不存在,某些离子不能确定是否存在,有的最后还设置一个探究问题或者一个计算题。其
一般解题思路如下所示:
→→
3.推断时注意事项
(1)注意有颜色的离子与溶液的颜色是否一致。
(2)根据某现象推出含有的某种离子,该离子是否为前面的操作引入的。
(3)注意离子共存问题
①离子是否能存在于溶液中,要特别注意溶液的性质(如酸碱性、氧化性、还原性)与离子的性质。
②推断结果中的离子是否能共存于同一溶液中。
③离子是否会隐蔽转化,如Al3+遇到过量的强碱转化为AlO,AlO遇到过量的强酸转化为Al3+。
(4)电荷守恒法确定离子(定量推断最后一种离子存在的方法)
如果多种离子可共存,且确定存在的离子的物质的量已知,只有一种离子不能确定是否存在,此时可以用
电荷守恒法来确定最后一种离子是否存在,即根据阳离子所带正电荷总数等于阴离子所带负电荷总数来确定
最后一种离子是否存在。
考向01 定性型离子检验与推断
1.(2023·河南·校联考三模)某白色粉末样品。可能含有KNO、KI、KHSO 和KHCO 中的一种或几种。
3 4 3
取少量该样品进行如下实验:①溶于水,得到无色透明溶液;②向①的溶液中滴加过量BaCl 溶液,溶液变浑浊;③取②的上层清液,
2
向其中滴加FeCl 溶液,有无色气体产生。
2
该样品中确定存在的是
A.KNO、KI B.KI、KHSO C.KHSO、KHCO D.KNO、KHSO
3 4 4 3 3 4
2.(2023·河南濮阳·统考一模)有一包固体粉末,由NaOH、NaSO 、MgCl 、CaCO 、Ba( NO )、FeSO
2 3 2 3 3 2 4
中的几种组成,取少量样品进行如下实验:
①将样品加入水中,得到白色不溶物a和无色溶液
②向①中加入足量稀盐酸,产生气体,仍存在不溶物
该固体粉末一定含有的是
A.CaCO 、Ba( NO ) B.CaCO 、NaSO
3 3 2 3 2 3
C.NaSO 、Ba( NO ) D.CaCO 、NaSO 、Ba( NO )
2 3 3 2 3 2 3 3 2
3.(2023·吉林白山·校考模拟预测)某固体混合物X可能是由NaSiO、Fe、NaCO、MgCl 中的两种或
2 3 2 3 2
两种以上的物质组成。某兴趣小组为探究该固体混合物的组成,设计实验方案如图所示(所加试剂均过量)
下列说法不正确的是
A.气体A是CO、H 的混合物
2 2
B.沉淀A是HSiO
2 3
C.根据白色沉淀C是AgCl可知,白色沉淀B一定不是纯净物
D.该固体混合物一定含有Fe、NaCO、NaSiO
2 3 2 3
4.(2023·浙江宁波·校联考模拟预测)含固体混合物 、 、 、 、 、
、 、 、 中的两种或两种以上化合物,溶于水发生了化学反应,且得到澄清溶液,
推测可能存在的物质不合理的是
A. 、 B. 、 、C. 、 D. 、
5.(2023·海南省直辖县级单位·嘉积中学校考三模)某化学兴趣小组对混合的两种白色粉末或晶体进行如
下实验:
①取一烧杯溶解该混合物,溶液无色透明;②向该溶液中加入Ba(OH) 溶液后生成白色沉淀,加入足量稀
2
盐酸后沉淀部分溶解,同时有使澄清石灰水变浑浊的气体生成。
下列物质组中符合上述现象的是
A.NaCO、NaSO B.NaCO、NaNO
2 3 2 4 2 3 3
C.NaCl、NaCO D.NaSO 、NaOH
2 3 2 4
考向02 定量型离子检验与推断
1.(2023·上海金山·统考二模)溶液A中含有如下离子中的若干种:Na+、NH 、Mg2+、SO 、SO 、
Cl-、OH-。为确定溶液中所含离子,现取该溶液进行有关实验,实验结果如下:
下列说法正确的是
A.气体E能使湿润的蓝色石蕊试纸先变红后褪色
B.若向沉淀B中加入足量稀硝酸,最终得到4.66 g沉淀
C.滤液C中大量存在的离子有NH 、Ba2+、Cl-、OH-
D.溶液A中可能有Na+,无Cl-
2.(2023·安徽黄山·统考三模)某工业废水中可能含有K+、Ag+、Mg2+、Cu2+、Al3+、NH 、Cl-、CO 、
NO 、SO 、I-中的几种,且各离子物质的量浓度均为0.2mol/L(忽略水的电离及离子的水解),欲探究废
水的组成,进行了如下实验:
I.取该无色溶液5mL,滴加一滴氨水有沉淀生成,且离子种类增加
II.用铂丝蘸取溶液,在火焰上灼烧,透过蓝色钴玻璃观察,无紫色火焰III.另取溶液加入过量盐酸,有无色气体生成,该无色气体遇到空气变为红棕色
IV.向III中所得溶液中加入BaCl 溶液,有白色沉淀生成。
2
下列推断不正确的是
A.溶液中一定不含的阳离子是K+、NH 、Cu2+、Ag+
B.III中加入盐酸生成无色气体的离子方程式为:8H++6I-+2NO =3I +2NO↑+4HO
2 2
C.原溶液除H+和OH-外只含有Mg2+、Al3+、NO 、SO 、I-
D.另取100mL原溶液,加入足量的NaOH溶液,充分反应后过滤、洗涤、灼烧沉淀至恒重,得到固体质
量0.8g
3.(2023·内蒙古赤峰·统考一模)某无色透明溶液中可能含有
中的几种、取 100mL溶液,向其中加入少量溴水,溶液仍呈无色,继续滴加足量盐酸和Ba(NO ) 混合,
3 2
产生沉淀,沉淀经洗涤、高温干燥后质量为4.66g。滤液加足量NaOH、加热、生成气体在标准状况下体积
为 1120mL。以下推测正确的是
A.原溶液中肯定存在 B.原溶液中一定不含
C.原溶液中可能存在 Na⁺、 D.另取试液滴加足量盐酸、BaCl 溶液,即可确定离子组成
2
4.(2023·辽宁·校联考模拟预测)常温下, 溶液中可能含有下列离子中的若干种: 、 、
、 、 、 。现对X溶液进行如下实验,其现象和结果如图:
下列说法正确的是A.X溶液的
B.X溶液中一定含有 、 、 ,不能确定是否含有
C.X溶液中一定含有 ,且 为
D.向滤液中通入足量的 气体,可得白色沉淀,将沉淀过滤、洗涤、灼烧至恒重,可得固体
5.(2023·山东青岛·统考一模)实验室中利用氧化铜和氧化铁混合物进行如图实验。下列说法错误的是
A.“3.04g固体”一定是铁铜混合物
B.“溶液2”中溶质的物质的量为0.1mol
C.混合物中含氧元素的物质的量为0.06mol
D.反应②能生成0.04gH
2
微专题 多种方法突破与量有关的离子方程式的书写
命题点01 连续反应型离子方程式的书写
典例(2021·全国卷)下列过程中的化学反应,相应的离子方程式正确的是
A.用碳酸钠溶液处理水垢中的硫酸钙:
B.过量铁粉加入稀硝酸中:C.硫酸铝溶液中滴加少量氢氧化钾溶液:
D.氯化铜溶液中通入硫化氢:
命题点02 竞争反应型离子方程式的书写
典例01(2020·全国卷)对于下列实验,能正确描述其反应的离子方程式是
A.用NaSO 溶液吸收少量Cl:
2 3 2
B.向CaCl 溶液中通入CO:
2 2
C.向HO 溶液中滴加少量FeCl :
2 2 3
D.同浓度同体积NH HSO 溶液与NaOH溶液混合:
4 4
典例02(2014·全国·高考真题)下列离子方程式错误的是
A.向Ba(OH) 溶液中滴加稀硫酸:Ba2++2OH-+2H++ SO 2-=BaS0 ↓+2HO
2 4 4 2
B.酸性介质中KMnO 氧化 HO:2MnO -+5HO+6H+= 2Mn2++5O↑+ 8HO
4 2 2 4 2 2 2 2
C.等物质的量的MgCl 、Ba(OH) 和 HCl 溶液混合:Mg2++2OH-= Mg(OH) ↓
2 2 2
D.铅酸蓄电池充电时的正极反应:PbSO + 2HO-2e- = PbO +4H++SO 2-
4 2 2 4
命题点03 配比反应型离子方程式的书写
典例(2007·海南卷)能正确表示下列反应的离子方程式是
A.碳酸氢钙溶液和氢氧化钠溶液混合 +OH-= +H O
2
B.醋酸钠溶液和盐酸混合CHCOONa+H+ = CHCOOH + Na+
3 3
C.少量金属钠放入冷水中Na+ 2H O=Na++2OH-+H ↑
2 2
D.硫酸铜溶液和氢氧化钡溶液混合Cu2+ + +Ba2+ + 2OH-= Cu(OH) ↓+ BaSO↓
2 4一、与量有关的离子方程式的类型
1.连续反应型
指反应生成的离子因又能跟剩余(过量)的反应物继续反应而跟用量有关。
①CO 与碱溶液[Ca(OH) 、NaOH、氨水]或盐溶液[Ca(ClO) 、NaAlO 、NaSiO]反应
2 2 2 2 2 3
CO 与碱或盐溶液反应时:CO 少量时生成CO,过量时生成HCO
2 2
CO(少量)+2NH •H O===(NH )CO+HO
2 3 2 4 2 3 2
CO 与氨水的反应
2
CO(过量)+NH •H O===NH HCO
2 3 2 4 3
SO (少量)+2NaOH===NaSO +HO
2 2 3 2
SO 与NaOH溶液的反应
2
SO (过量)+NaOH===NaHSO
2 3
Ca(ClO) +HO+CO(少量)===CaCO ↓+2HClO
2 2 2 3
CO 与Ca(ClO) 溶液反应
2 2
Ca(ClO) +2HO+2CO(过量)===Ca(HCO )+2HClO
2 2 2 3 2
少量CO 与NaClO溶液反应 NaClO+HO+CO(少量)===NaHCO +HClO
2 2 2 3
少量CO 与 ONa溶液反应 ONa+CO 2 +H 2 O OH+NaHCO 3
2
【易错提醒】因酸性: H
2
CO
3
>HClO> OH>HCO,当CO
2
与NaClO溶液、 ONa溶液反应时,
无论CO 少量还是过量均生成HCO。
2
②SO 与盐溶液[NaClO、Ca(ClO) 、NaS]反应——氧化还原反应并非强酸制取弱酸
2 2 2
a.向NaClO溶液中通入SO 气体
2
SO 气体与少量NaClO溶液反应 SO +ClO-(少量)+HO===Cl-+SO+2H+
2 2 2
生成的H+能与ClO-继续反应 H++ClO-===HClO
SO 气体与过量NaClO溶液反应 SO +3ClO-(过量)+HO===Cl-+SO+2HClO
2 2 2
b.向NaS溶液中通入SO 气体
2 2
少量SO 气体与NaS溶液反应 SO (少量)+2NaS+2HO===3S↓+4NaOH
2 2 2 2 2
生成的NaOH能与SO 继续反应 SO (过量)+NaOH===NaHSO
2 2 3
过量SO 气体与NaS溶液反应 5SO +2NaS+2HO===3S↓+4NaHSO
2 2 2 2 2 3
③多元弱酸(HS、HPO )与碱溶液的反应——多元弱酸分步电离
2 3 4
HS+NaOH(少量)===NaHS+HO
2 2
NaOH溶液与HS溶液反应
2
HS+2NaOH(过量)===NaS+2HO
2 2 2
④多元弱酸的正盐[Na CO、NaSO 、NaS]与强酸的反应——注意互滴实验
2 3 2 3 2
少量HCl溶液与NaCO 溶液反应 NaCO+HCl(少量)===NaHCO +NaCl
2 3 2 3 3
过量HCl溶液与NaCO 溶液反应 NaCO+2HCl(过量)===2NaCl+HO+CO↑
2 3 2 3 2 2
⑤与“铝”有关的离子反应
a.向AlCl 溶液中滴入NaOH溶液
3少量NaOH溶液与AlCl 溶液反应 AlCl +3NaOH(少量)===Al(OH) ↓+3NaCl
3 3 3
过量NaOH溶液与AlCl 溶液反应 AlCl +4NaOH(过量)===NaAlO+3NaCl+2HO
3 3 2 2
b.向NaAlO 溶液中滴入稀盐酸
2
少量稀盐酸与NaAlO 溶液反应 NaAlO +HCl(少量)+HO===Al(OH) ↓+NaCl
2 2 2 3
过量稀盐酸与NaAlO 溶液反应 NaAlO +4HCl(过量)===NaCl+AlCl +2HO
2 2 3 2
⑥与氨水有关的络合反应
a.向AgNO 溶液中滴入氨水
3
少量氨水与AgNO 溶液反应 AgNO+NH ·H O(少量)===AgOH↓(白色)+NH NO
3 3 3 2 4 3
过量氨水与AgNO 溶液反应 AgNO+2NH ·H O(过量)===[Ag(NH )]NO +2HO
3 3 3 2 3 2 3 2
b.向CuSO 溶液中滴入氨水
4
少量氨水与CuSO 溶液反应 CuSO +2NH ·H O===Cu(OH) ↓+(NH )SO
4 4 3 2 2 4 2 4
过量氨水与CuSO 溶液反应 CuSO +4NH ·H O===[Cu(NH)]SO +4HO
4 4 3 2 3 4 4 2
⑦Fe与稀硝酸的反应
少量Fe与稀硝酸反应 Fe(少量)+4HNO(稀)===Fe(NO )+NO↑+2HO
3 3 3 2
过量Fe与稀硝酸反应 3Fe(过量)+8HNO(稀)===3Fe(NO )+2NO↑+4HO
3 3 2 2
⑧NaS溶液与FeCl 溶液的反应
2 3
少量NaS溶液与FeCl 溶液反应 NaS(少量)+2FeCl ===2NaCl+2FeCl +S↓
2 3 2 3 2
生成的FeCl 能与NaS继续反应 NaS+FeCl ===2NaCl+FeS↓
2 2 2 2
过量NaS溶液与FeCl 溶液反应 3NaS(过量)+2FeCl ===6NaCl+2FeS↓+S↓
2 3 2 3
⑨氯水、溴水、碘水与NaSO 溶液的反应
2 3
氯水与少量NaSO 溶液反应 NaSO (少量)+Cl+HO===2NaCl+HSO
2 3 2 3 2 2 2 4
生成的HSO 能与NaSO 继续反应 HSO +NaSO ===NaSO +HO+SO ↑
2 4 2 3 2 4 2 3 2 4 2 2
氯水与过量NaSO 溶液反应 2NaSO (过量)+Cl===2NaCl+NaSO +SO ↑
2 3 2 3 2 2 4 2
⑩Cl 与NaCO 溶液的反应
2 2 3
** 错误的表达式 **Cl+HO HCl+HClO
2 2
** 错误的表达式 **NaCO+HCl(少量)===NaHCO +
2 3 3
NaCl
少量Cl 与NaCO 溶液反应 ** 错误的表达式 **NaCO+HClO===NaHCO +NaClO
2 2 3 2 3 3
** 错误的表达式 **+** 错误的表达式 **+** 错误的
表达式 **得:
Cl(少量)+2NaCO+HO===2NaHCO +NaCl+NaClO
2 2 3 2 3
过量Cl 与NaCO 溶液反应 ** 错误的表达式 **Cl+HO HCl+HClO
2 2 3 2 2** 错误的表达式 **NaCO+2HCl(过量)===2NaCl+HO
2 3 2
+CO↑
2
** 错误的表达式 **+** 错误的表达式 **得:
2Cl(过量)+NaCO+HO===2NaCl+CO↑+2HClO
2 2 3 2 2
2.离子配比型
当一种反应物中有两种或两种以上组成离子参与反应时,因其组成比例不协调(一般为复盐或酸式盐),
当一种组成离子恰好完全反应时,另一种组成离子不能恰好完全反应(有剩余或不足),因而跟用量有关。
①NaHCO 溶液与Ca(OH) 、Ba(OH) 溶液的反应
3 2 2
反应的本质是因为阴离子可以反应 HCO -+OH-===CO+HO
3 2
少量NaHCO 溶液与Ca(OH) 溶液反应 Ca(OH) +NaHCO (少量)===HO+CaCO ↓+NaOH
3 2 2 3 2 3
过量NaHCO 溶液与Ca(OH) 溶液反应 Ca(OH) +2NaHCO (过量)===2HO+CaCO ↓+NaCO
3 2 2 3 2 3 2 3
②NaOH溶液与Ca(HCO )、Ba(HCO ) 溶液的反应
3 2 3 2
少量NaOH溶液与Ba(HCO ) 溶液反应 Ba(HCO )+NaOH(少量)===BaCO ↓+NaHCO +HO
3 2 3 2 3 3 2
过量NaOH溶液与Ba(HCO ) 溶液反应 Ba(HCO )+2NaOH(过量)===BaCO↓+NaCO+2HO
3 2 3 2 3 2 3 2
Ca(OH) 溶液与过量Ca(HCO ) 溶液 Ca(OH) +Ca(HCO )===2HO+2CaCO ↓
2 3 2 2 3 2 2 3
NaOH溶液与过量NaHCO 溶液 NaHCO +NaOH===Na CO+HO
3 3 2 3 2
【易错提醒】Ca(OH) 溶液与Ca(HCO ) 溶液则无少量、过量,同理NaOH溶液与NaHCO 溶液则无少量、
2 3 2 3
过量
③Ba(OH) 与NaHSO 溶液的反应
2 4
少量NaHSO 溶液与Ba(OH) 溶液反应 Ba(OH) +NaHSO(少量)===HO+BaSO↓+NaOH
4 2 2 4 2 4
过量NaHSO 溶液与Ba(OH) 溶液反应 Ba(OH) +2NaHSO(过量)===2HO+BaSO↓+NaSO
4 2 2 4 2 4 2 4
④明矾溶液与Ba(OH) 溶液的反应
2
Al3+沉淀完全(沉淀的物质的量最大) 2KAl(SO )+3Ba(OH) ===2Al(OH) ↓+3BaSO↓+KSO
4 2 2 3 4 2 4
SO沉淀完全(沉淀的质量最大) KAl(SO )+2Ba(OH) ===2BaSO↓+KAlO+2HO
4 2 2 4 2 2
3.先后反应型
一种反应物的两种或两种以上的组成离子,都能跟另一种反应物的组成离子反应,但因反应次序不同而跟
用量有关。又可称为竞争型,
①氧化还原反应与非氧化还原反应的竞争,一般是氧化还原反应优先。
②氧化还原反应中氧化性(还原性)强的优先,如还原性I->Fe2+>Br-,则与Cl 反应的顺序为I->Fe2+>Br
2
-。
③非氧化还原反应中性质强者优先,如向含 OH-、CO、AlO 的溶液中滴加盐酸,反应顺序为 OH-
>AlO>CO。
a.FeBr 溶液与氯气的反应——还原性:Fe2+>Br-
2少量Cl 与FeBr 溶液反应 3Cl(少量)+6FeBr ===2FeCl +4FeBr
2 2 2 2 3 3
过量Cl 与FeBr 溶液反应 3Cl(过量)+2FeBr ===2FeCl +2Br
2 2 2 2 3 2
n(FeBr):n(Cl )==1:1时 6Cl+6FeBr ===4FeCl +3Br +2FeBr
2 2 2 2 3 2 3
b.FeI 溶液与氯气反应——还原性:I->Fe2+
2
少量Cl 与FeI 溶液反应 Cl(少量)+FeI===FeCl +I
2 2 2 2 2 2
过量Cl 与FeI 溶液反应 3Cl(过量)+2FeI===2FeCl +2I
2 2 2 2 3 2
n(FeI ):n(Cl )==4:5时 5Cl+4FeI===4I+2FeCl +2FeCl
2 2 2 2 2 3 2
二、“少定多变”法突破与量有关的离子方程式的书写
1.“少定多变”法突破与量有关的离子方程式的书写原则
(1)“少定”就是把相对量较少的物质定为“1 mol”,若少量物质有两种或两种以上离子参加反应,则参加反
应的离子的物质的量之比与原物质组成比相符。
(2)“多变”就是过量的反应物,其离子的化学计量数根据反应实际需求量来确定,不受化学式中的比例制
约,是可变的。
2.应用
(1)过量与少量型。
书写原则是“以少定多”,即先根据题给条件判断“少量物质”,以“少量物质”的计量数(充分反应)确定所
需“过量物质”的计量数。如少量NaHCO 与足量Ca(OH) 溶液的反应:
3 2
“少定”——即定HCO的物质的量为1 mol,
“多变”——1 mol HCO能与1 mol OH-发生反应,得到1 mol H O和1 mol CO,1 mol CO再与 1 mol
2
Ca2+结合生成CaCO 沉淀。
3
离子方程式为HCO+Ca2++OH-===CaCO ↓+HO。
3 2
(2)定量型。
首先根据题给条件中反应物的物质的量,结合“以少定多”的原则及离子反应的顺序,逐步写出各步反应的
离子方程式,然后把各步离子方程式相加即可得到总反应的离子方程式。如明矾与含等物质的量的Ba(OH)2
的溶液反应的离子方程式书写方法为
三、分步书写法突破连续型离子方程式的书写
如向 AlCl 溶液中加入过量 NaOH 溶液,可按照反应顺序分别写出两步反应:Al3++3OH-
3
===Al(OH) ↓,Al(OH) +OH-===AlO+2HO,相加可得:Al3++4OH-===AlO+2HO。
3 3 2 2四、假设定序法突破竞争型离子反应方程式的书写
如Cl 与FeBr 溶液反应,Cl 既可以氧化Fe2+也可以氧化Br-,在不明确离子反应的先后顺序时,可假
2 2 2
设Cl 先与Br-反应,则生成的溴单质可以氧化Fe2+生成Fe3+,这样即可确定Cl 先与Fe2+反应,后与Br-
2 2
反应,然后再根据量的关系书写即可。
考向01 连续反应型离子方程式的书写
1.(2023·黑龙江大庆·大庆市东风中学校考模拟预测)物质的用量可能影响反应的产物,下列离子方程式
正确的是
A.向 Fe(NO ) 溶液中加入少量的 HI 溶液:
3 3
B.足量 NaOH 溶液与 HC O 溶液反应:
2 2 4
C.向 CuSO 溶液中加入过量氨水:
4
D.向 Mg(HCO ) 溶液中加入过量的 NaOH 溶液:
3 2
2.(2023·河南·校联考模拟预测)下列离子方程式书写正确的是
A. 与稀盐酸反应:
B.氢氧化钡溶液与碳酸钠反应:
C.向 溶液中滴加少量 溶液:
D. 通入 中:
3.(2023·广西南宁·南宁三中校考二模)下列离子方程式正确的是
A.食醋除水垢中的碳酸钙:CO +2CH COOH=CH COO-+CO ↑+H O
3 3 2 2
B.向HO 溶液中加入少量MnO :HO+MnO+2H+=Mn2++O ↑+2H O
2 2 2 2 2 2 2 2
C.向AlCl 溶液中加入过量NaOH溶液:Al3++3OH-=Al(OH) ↓
3 3
D.用过量氨水吸收废气中的SO :2NH •H O+SO =2NH +SO +H O
2 3 2 2 2
4.(2023·广东汕头·统考三模)硫及其化合物在生活中应用广泛,下列有关离子方程式书写正确的是A.往亚硫酸中逐步通入 气体:
B.往 溶液中滴加盐酸:
C.往 溶液中通入过量 :
D.实验室利用 制备 :
5.(2023·江西·江西师大附中校联考模拟预测)下列离子方程式符合题意且正确的是
A.在 溶液中滴加少量NaClO溶液:
B.在磁性氧化铁粉末中加入足量的稀硝酸:
C.在 溶液中加入过量NaOH溶液:
D.向含双氧水和氨气的混合液中加入铜粉得到深蓝色溶液:
考向02 竞争反应型离子方程式的书写
1.(2023·黑龙江大庆·大庆市东风中学校考模拟预测)物质的用量可能影响反应的产物,下列离子方程式
正确的是
A.向 Fe(NO ) 溶液中加入少量的 HI 溶液:
3 3
B.足量 NaOH 溶液与 HC O 溶液反应:
2 2 4
C.向 CuSO 溶液中加入过量氨水:
4
D.向 Mg(HCO ) 溶液中加入过量的 NaOH 溶液:
3 2
2.(2023·四川巴中·统考模拟预测)下列离子方程式符合所给事实的是
A.将少量SO 通入NaClO溶液:SO +H O+2ClO-=SO +2HClO
2 2 2B.铁片上镀铜的总反应(铜作阳极,硫酸铜溶液作电镀液):Cu(阳极) Cu(阴极)
C.泡沫灭火器的原理:2Al3++3CO +3H O=2Al(OH) ↓+3CO ↑
2 3 2
D.同浓度同体积NH HSO 溶液与NaOH溶液混合:NH +OH-=NH•H O
4 4 3 2
3.(2023·四川绵阳·四川省绵阳南山中学校考模拟预测)能正确表示下列反应的离子方程式的是
A.将 加入足量的稀盐酸中:
B. 溶液中滴加稀氨水:
C. 与稀硝酸反应:
D.同浓度同体积的 溶液与 溶液混合:
4.(2022·浙江·校联考模拟预测)下列有关离子方程式书写正确的是
A.硫酸铵和硫酸铁混合液与过量NaOH溶液混合:
B.碳酸氢钙溶液与氢氧化钙溶液混合:
C.苯酚钠溶液中通入少量 气体:2 2
D.氯气通入70℃的浓氢氧化钠溶液中:
5.(2023·广西南宁·南宁三中校联考模拟预测)下列指定反应的离子方程式正确的是
A.碘化亚铁溶液通入少量的氯气:2Fe2++2I-+2Cl=2Fe3++I +4Cl-
2 2
B.用HO 从酸化的海带灰浸出液中制取碘:2I-+H O+2H+=I +2H O
2 2 2 2 2 2
C.Fe(OH) 胶体的制备:Fe3++3NH•H O=Fe(OH) (胶体)+3NH
3 3 2 3
D.等物质的量的NaHCO 溶液与Ca(OH) 溶液混合:2HCO +Ca2++2OH-=CaCO ↓+CO
3 2 3
考向03 配比反应型离子方程式的书写1.(2023·陕西商洛·陕西省山阳中学校考一模)下列反应的离子方程式书写正确的是
A.金属Na与 溶液反应:
B. 溶于过量HI溶液:
C.澄清石灰水与过量小苏打溶液混合:
D.草酸( )与酸性 溶液反应:
2.(2024·广西·校联考一模)下列离子方程式书写正确的是
A.铁与足量的稀硝酸反应:Fe+2H+=Fe2++H ↑
2
B.醋酸溶液与碳酸氢钠溶液反应:HCO +H+=CO ↑+H O
2 2
C.氢氧化钡溶液中滴入稀硫酸:Ba2++OH-+SO +H+=BaSO ↓+H O
4 2
D.氯化铝溶液中滴入过量氨水:Al3++3NH•H O=Al(OH) ↓+3NH
3 2 3
3.(2023·河北保定·统考二模)下列反应的离子方程式书写错误的是
A.向酸性 溶液中滴加 溶液,溶液褪色:
B.将 溶液加入到石灰乳中得到氢氧化镁:
C.泡沬灭火器的反应原理:
D.在 溶液中加入过量的 溶液:
4.(2023·四川乐山·统考三模)下列方程式符合所给事实的是
A.用Ca(ClO) 溶液吸收废气中的SO :Ca(ClO) +SO+H O=2HClO+CaSO ↓
2 2 2 2 2 3
B.用盐酸和淀粉一KI溶液检验盐中有KIO : +5I-+6H+=3I +3H O
3 2 2
C.向NaHSO 溶液中加入Ba(OH) 至溶液为中性:H++OH-+Ba2++ =H O+BaSO↓
4 2 2 4D.用酸性KMnO 溶液滴定双氧水:2 +H O+6H+=2Mn2++3O ↑+4H O
4 2 2 2 2
5.(2023·湖北武汉·华中师大一附中校考模拟预测)下列离子方程式书写正确的是
A.向 溶液中通入 :
B. 溶液与过量NaOH溶液反应:
C.漂白粉溶液吸收少量 气体:
D.向 中加入 酸化的 溶液: