文档内容
专题验收评价
专题 04 氧化还原反应
内容概览
A·常考题不丢分
【考点一 氧化还原反应的基本概念】
【考点二 氧化还原反应的基本规律】
【考点三 氧化还原反应方程式的配平与计算】
【微专题 “陌生情境下”方程式的书写】
B·综合素养拿高分/拓展培优拿高分
C·挑战真题争满分
【考点一 氧化还原反应的基本概念】
1.(2023·浙江金华·模拟预测)关于反应2MnSO +5Na SO+8H O=2NaMnO +4Na SO +8H SO ,下列说法
4 2 2 8 2 4 2 4 2 4
正确的是
A.NaSO 中S元素化合价为+7价 B.MnSO 是氧化剂
2 2 8 4
C.生成1molNaMnO 时转移5mol电子 D.MnO 的氧化性弱于Mn2+
4
【答案】C
【解析】A.NaSO 中存在一个过氧键,即有2个氧显-1价,其余的氧显-2价,根据化合物的化合价为
2 2 8
0,可得硫元素为+ 6价,A错误;B.在该反应中锰元素由+2价升高为+7价,则硫酸锰为还原剂,B错误;
C.在该反应中锰元素由+2价升高为+7价,则生成1molNaMnO 时转移5mol电子,C正确;D.在该反应
4
中高锰酸根是氧化产物,其中锰元素的化合价为+7价,锰离子是还原剂,其中锰元素的化合价为+2价,
一般同种元素中元素的化合价越高氧化性越强(氯的含氧酸除外),D错误;故选C。
2.(2023·浙江金华·校联考模拟预测)加热硅与Ca(OH) 、NaOH的混合粉末可获得氢气
2
Si+Ca(OH) +2NaOH NaSiO+CaO+2H ↑,下列说法正确的是
2 2 3 2
A.NaSiO 是还原产物 B.可推知该反应为吸热反应
2 3
C.氧化剂与还原剂的物质的量之比为2∶1 D.该反应为置换反应
【答案】C【解析】A.反应Si+Ca(OH) +2NaOH NaSiO+CaO+2H ↑中Si元素化合价由0价上升到+4价,NaSiO
2 2 3 2 2 3
是氧化产物,故A错误;B.该反应需要加热,但吸热反应不一定需要加热,则不能推知该反应为吸热反
应,故B错误;C.反应Si+Ca(OH) +2NaOH NaSiO+CaO+2H ↑过程中Ca(OH) 先分解产生CaO和
2 2 3 2 2
HO,Si、NaOH和HO反应生成NaSiO 和H,其中Si元素化合价由0价上升到+4价,H元素由+1价下
2 2 2 3 2
降到0价,Si是还原剂,HO是氧化剂,氧化剂与还原剂的物质的量之比为2∶1,故C正确;D.置换反
2
应是单质与化合物反应生成另外的单质和化合物的化学反应,可表示为a+bc=b+ac或ab+c=ac+b,该反应
不是置换反应,故D错误;故选C。
3.(2023·山东济宁·统考三模)中华古诗文华丽优美且富含哲理,下列叙述不涉及氧化还原反应的是
A.落红不是无情物,化作春泥更护花 B.白日登山望烽火,黄昏饮马傍交河
C.欲渡黄河冰塞川,将登太行雪满山 D.蜡烛有心还惜别,替人垂泪到天明
【答案】C
【解析】A.涉及植物体的腐烂、分解,转化成二氧化碳、水和无机盐,存在元素化合价变化,与氧化还
原反应有关,选项A不符合;B.白日登山望烽火,黄昏饮马傍交河中白日登山望烽火包含着物质燃烧,
与氧化还原反应有关,选项B不符合;C.水的三态变化过程中没有新物质生成,属于物理变化,与氧化
还原反应无关,选项C符合;D.蜡烛燃烧包含氧化还原反应,选项D不符合;答案选C。
4.(2023·山东潍坊·统考三模)下列古诗词中不涉及氧化还原反应的是
A.美人首饰候王印,尽是沙中浪底来
B.人间巧艺夺天工,炼药燃灯清昼同
C.投泥泼水愈光明,烁玉流金见精悍
D.蜡烛有心还惜别,替人垂泪到天明
【答案】A
【解析】A.美人首饰候王印,尽是沙中浪底来涉及金属单质与杂质的分离属于物理变化,A正确;B.人
间巧艺夺天工,炼药燃灯清昼同涉及燃料的燃烧属于氧化还原反应,B错误;C.投泥泼水愈光明,烁玉
流金见精悍涉及冶炼矿石,融化铁水属于氧化还原反应,C错误;D.蜡烛有心还惜别,替人垂泪到天明
涉及烃类的燃烧属于氧化还原反应,D错误;故选A。
5.(2023·广东汕头·统考三模)研究 的综合利用对构建低碳环保社会有重要意义。下列有关 的应
用中涉及氧化还原反应的是
A.利用 生产纯碱 B.利用 制甲酸
C.利用干冰灭火 D.利用 制碳酸饮料
【答案】B
【解析】A.利用 生产纯碱涉及的方程式为:NH +H O+CO=NHHCO ,该反应中各元素化合价不变,
3 2 2 4 3
故不涉及氧化还原反应,故A项错误;B.利用 制甲酸的过程中二氧化碳生成了甲酸,化合价发生改
变,故该过程涉及氧化还原反应,故B项正确;C.干冰灭火的原因有两点,首先干冰升华吸热将温度降低至可燃物着火点以下,其次二氧化碳不支持燃烧,不涉及氧化还原反应,故C项错误;D.利用 制
碳酸饮料是利用二氧化碳与水反应生成碳酸:CO+H O=HCO,不涉及氧化还原反应,故D项错误。故答
2 2 2 3
案选B。
【考点二 氧化还原反应的基本规律】
1.(2023·辽宁·校联考三模)一种以镍电极废料(含 以及少量 , 和不溶性杂质)为原料制备
的过程可表示为:
“酸浸”后溶液中的金属离子除 外还有少量的 和 等。下列说法错误的是
A.氧化性:
B.氧化过程的离子方程式:
C.除杂过程仅为过滤操作
D.工业上可电解碱性 悬浊液制备 ,加入一定量的 有助于提高生产效率
【答案】C
【分析】镍电极废料(含Ni以及少量Al O、Fe O 和不溶性杂质)经过稀硫酸“酸浸”后,得到Ni2+和少量
2 3 2 3
的 Al3+ 和 Fe2+ 等,调节pH,将 Al3+ 和 Fe2+ 转化为沉淀,再过滤除去不溶性杂质,则滤液中含有 Ni2+
, Ni2+ 经过KClO的氧化,得到NiOOH。
【解析】A.“酸浸”后溶液中的金属离子除 Ni2+ 外还有少量的 Al3+ 和 Fe2+ 等,则发生反应:
Ni+2Fe3+=2Fe2++Ni2+,则氧化性: Fe3+>Ni2+ ,A项正确;B.Ni2+ 经过KClO的氧化,得到NiOOH,反应
的离子方程式为2Ni2++ClO−+4OH−=2NiOOH+Cl−+H O,B项正确;C.除杂过程包括:调节pH,将 Al3+
2
和 Fe2+ 转化为沉淀,再过滤除去不溶性杂质,C项错误;D.电解碱性 Ni(OH) 悬浊液制备NiOOH,阳
2
极反应为: Ni(OH) −e−+OH−=NiOOH +H O ,若加入一定量的KCl,氯离子在阳极上失电子生成氯气,
2 2
氯气在碱性条件下生成 ClO− , ClO− 将 Ni(OH) 氧化为NiOOH,有助于提高生产效率,D项正确;故选
2
C。
2.(2023·海南·海南中学校联考一模) 是一种常用的消毒剂,可通过反应
制取,下列有关说法正确的是
A.还原性:
B.每消耗 ,转移 电子
C.氧化剂与还原剂的物质的量之比为2∶1
D.若该反应通过原电池来实现,则 是负极产物
【答案】C
【解析】A. 反应中,SO 是还原剂、ClO 是还原产物,还原性
2 2,故A错误;B.SO 中S元素化合价由+4升高为+6,每消耗 ,转移 电子,故B
2
错误;C.NaClO 中Cl元素化合价降低,NaClO 是氧化剂,SO 中S元素化合价升高,SO 是还原剂,氧
3 3 2 2
化剂与还原剂的物质的量之比为2∶1,故C正确;D.若该反应通过原电池来实现,负极发生氧化反应,
正极发生还原反应,则 是正极产物,故D错误;选C。
3.(2023·山东日照·校联考二模)钒元素在酸性溶液中有多种存在形式,其中 为蓝色, 为淡黄
色,已知能发生如下反应:
Ⅰ.
Ⅱ.
下列说法错误的是
A.酸性条件下的氧化性:
B.反应Ⅱ中氧化产物和还原产物物质的量之比为
C.向 溶液中滴加酸性 溶液,溶液颜色由蓝色变为淡黄色
D.向含 的酸性溶液中滴加 溶液充分反应,转移 电子
【答案】D
【解析】A.氧化剂氧化性大于氧化产物,由Ⅰ可知,氧化性 ,由Ⅱ可知,氧化性
;故酸性条件下的氧化性: ,A正确;
B.反应Ⅱ中 发生氧化反应得到氧化产物 , 发生还原反应得到还原产物 ,由化学方程
式可知,氧化产物和还原产物物质的量之比为 ,B正确;C.向 溶液中滴加酸性 溶液,
被高锰酸钾氧化为 ,故溶液颜色由蓝色变为淡黄色,C正确;D.向含 的酸性溶液中
滴加 溶液充分反应,由于碘离子还原性大于亚铁离子,故碘离子完全和 反应生成碘单质,
转移 电子,D错误;故选D。
4.(2023上·江西抚州·高三临川一中校考期中)在复杂的体系中,确认化学反应先后顺序有利于解决问题,
下列化学反应先后顺序判断不正确的是
A.在含Ba(OH) 、KOH的混合溶液中缓慢通入CO:Ba(OH) 、KOH、KCO、BaCO
2 2 2 2 3 3
B.在含 、Al3+、H+的溶液中逐滴加入KOH溶液:H+、Al3+、 、Al(OH)
3
C.在含 、OH-、 的溶液中逐滴加入盐酸:OH-、 、 、 、Al(OH)
3
D.在含等物质的量的S2-、 、I-、Cl-、Br-的溶液中加入氯水: 、S2-、I-、Br-、Cl-
【答案】D
【解析】A.在含Ba(OH) 、KOH的混合溶液中缓慢通入CO,若先跟KOH反应,则生成的KCO 还会与
2 2 2 3
Ba(OH) 反应,重新生成BaCO ,所以Ba(OH) 先与CO 反应,KOH次之,因为Ba(HCO ) 能与KCO 反
2 3 2 2 3 2 2 3
应,所以KCO 先与CO 反应,BaCO 最后与CO 反应,A正确;B.因为一水合氨、Al(OH) 都能与H+反
2 3 2 3 2 3应,所以H+最先与KOH反应,一水合氨能与Al3+反应,则Al3+比 先与KOH反应,最后是Al(OH) 与
3
KOH反应,B正确;C.因为 、Al(OH) 都能与OH-反应,所以OH-最先与盐酸反应, 与 能
3
发生反应,则 与盐酸反应排在第二位, 与盐酸反应排在第三位, 能与Al3+反应,则 与
盐酸反应排在第四位,最后是Al(OH) 与盐酸反应,C正确;D.因为硫酸能与S2-反应,所以S2-最先与氯
3
水反应,I、Br 都能将 氧化,则 排在第二位,然后依次是I-、Br-、Cl-,D不正确;故选D。
2 2
5.(2023上·黑龙江大庆·高三铁人中学校考)在复杂的体系中,确认化学反应先后顺序有利于解决问题,
下列化学反应先后顺序判断不正确的是
A.在含Ba(OH) 、KOH的混合溶液中缓慢通入CO: Ba(OH) 、KOH、KCO、BaCO
2 2 2 2 3 3
B.在含 、Al3+、H+的溶液中逐滴加入KOH溶液:H+、Al3+、 、Al(OH)
3
C.在含 、OH-、 的溶液中逐滴加入盐酸: 、Al(OH) 、OH-、
3
D.在含等物质的量的Fe2+、Ag+、Cu2+、H+的溶液中加入锌粉:Ag+、Cu2+、H+、Fe2+
【答案】C
【解析】A.在含Ba(OH) 、KOH的混合溶液中缓慢通入CO,CO 先与Ba(OH) 反应生成BaCO 沉淀,然
2 2 2 2 3
后KOH与CO 反应生成KCO,再发生KCO 和CO 反应生成KHCO ,最后BaCO 和CO 反应生成
2 2 3 2 3 2 3 3 2
Ba(HCO ),故A正确;B.在含 、Al3+、H+的溶液中逐滴加入KOH溶液,H+先和KOH反应生成水,
3 2
然后发生Al3+和KOH反应生成氢氧化铝沉淀,再发生 和KOH反应生成氨水,最后Al(OH) 和KOH反
3
应生成偏铝酸钾,故B正确;C.在含 、OH-、 的溶液中逐滴加入盐酸,H+先和OH-反应生成水,
然后 和H+反应生成氢氧化铝沉淀,再发生 和H+反应生成二氧化碳,最后Al(OH) 和H+反应生成
3
铝离子,故C错误;D.氧化性:Ag+>Cu2+>H+> Fe2+,在含等物质的量的Fe2+、Ag+、Cu2+、H+的溶液中加
入锌粉,反应顺序为Ag+、Cu2+、H+、Fe2+,故D正确;选C。
【考点三 氧化还原反应方程式的配平与计算】
1.(2024·广西北海·统考一模·节选)硫酸铈铵 微溶于水,不溶于乙醇,溶于无机酸,
可用作分析试剂、氧化剂。某工厂用碳酸铈 矿石制备硫酸铈铵的工艺流程如图:
已知:① 。
②硫酸铈铵的熔点为 ,沸点为 。
回答下列问题:
(4)步骤二中, 与 反应生成 的化学方程式为 。【答案】(4)
【解析】(4) 与 反应生成 ,反应中Ce化合价由+3变为+4、过氧化
氢中氧化合价由-1变为-2,结合电子守恒、质量守恒可知,化学方程式为
;
2.(2023·黑龙江大庆·统考一模·节选)高铁酸钾 是新型多功能水处理剂,其生产工艺如图所示:
已知:① 与 溶液反应的产物与反应温度有关,温度较低时产物为 和 ;温度较
高时产物为 和 。
②同一条件下,溶液的碱性越强,高铁酸盐的稳定性越高。
回答下列问题:
(1)写出 与 溶液在较高温度下反应的离子方程式: 。
【答案】(1)
【解析】(1) 与NaOH溶液在较高温度下反应,产物为NaCl、 和 ,反应中部分氯化合价
由0变为-1、部分由0变为+5,根据电子守恒可知,离子方程式 ;
3.(2023·江苏南通·统考模拟预测·节选)碳酸铈 是一种稀土材料,工业上常以氟碳铈矿(主
要成分为CeFCO、SiO)为原料制备碳酸铈,其工艺流程如图所示:
3 2
已知:①“酸浸”后铈元素主要以 存在
②硫脲( )是一种常见的还原剂,易被氧化为 。
(2)“还原”时的产物为 沉淀,该反应的离子方程式为 。
(3)“沉淀”时的离子方程式为 。
【答案】(2)【解析】(2)(CeF )2+发生还原反应产物为 NaCe(SO ) , 被氧化成(SCN H),根据电
2 4 2 2 3 2
子守恒可得化学方程式
;
故答案为: ;
4.(2023·陕西渭南·统考一模·节选)草酸钻可用于指示剂和催化剂。工业上用水钻矿(主要成分为 ,
含少量 、 、MnO、MgO、CaO、 等)制取 的工艺流程如图所示:
(6) ( )热分解质量变化过程如图2所示。其中600℃以前是隔绝空气加热,
600℃以后在空气中加热。A、B、C均为纯净物。
①用化学方程式表示A点到B点的物质变化 。
②C点所示产物的化学式是 。
【答案】(6) Co+2CO Co O
2 2 3
【解析】(6)① 属于变价金属元素的结晶水合物,600℃前后分解反应原理不同。600℃前
隔绝空气加热的分解产物A、B中Co的化合价均为+2价。600℃后在空气中加热固体质量增加,只能是与
空气中的氧气反应,Co应升价。 受热分解生成A、B要经过失水与分解两个过程,设A、B
的摩尔质量分别为M 、M ,根据Co元素守恒 ,则M =147g/mol,MB为59.0
A B Ag/mol,故A、B分别为无水物 与Co,A点到B点的化学方程式为: Co+2CO ;
2
②600℃后在空气中加热,Co被空气中的氧气氧化,固体质量增加,类比Fe,Co有+2、+3价,可能生成
Co O,也可能生成Co O,设C的化学式为Co O, x : y=( ): [ + ] =2: 3,C点所示产物的
2 3 3 4 x y
化学式是Co O。
2 3
5.(2023·河南郑州·郑州外国语学校校考模拟预测·节选)锰酸锂离子蓄电池是第二代锂离子动力电池。
一种以软锰矿浆(主要成分为MnO ,含少量Fe O、FeO、Al O、SiO 等杂质)为原料制备锰酸锂的流程如
2 2 3 2 3 2
图所示。
(5)为测定锰酸锂的纯度,取2.00g产品置于锥形瓶中,向其中加入2.68gNa C O 和足量硫酸,充分反应后,
2 2 4
用0.100mol•L-1KMnO 标准溶液滴定未反应完的HC O,到达滴定终点时消耗KMnO 标准溶液20.00mL。
4 2 2 4 4
已知:LiMn O Mn2+,则该产品中锰酸锂的质量分数是 。[M(LiMn O)=181g•mol-1,
2 4 2 4
M(Na C O)=134g•mol-1]
2 2 4
【答案】(5)90.5%
【解析】(5)KMnO 标准溶液滴定未反应完的HC O,化学方程式为
4 2 2 4
,可知剩余的
,据此可知与LiMn O 反应的HC O 含量为
2 4 2 2 4
,LiMn O 参与反应的化学方程式为
2 4
,则
,故该产品中锰酸锂的质量分数是 。
【微专题 “陌生情境下”方程式的书写】
1.(2023·新疆乌鲁木齐·统考一模·节选)下图是氮在生态系统中的循环。细菌和电催化可促使含氮物质
进行氧化还原反应。(6)由于过度的人为干预,水体中的硝酸盐水平正在增加。硝酸盐转化为无害氮的反硝化作用,可以通过电
催化法来实现,写出在中性介质中硝酸盐转化为氮气的阴极电极反应式 。
【答案】(6)2NO +10e- + 6H O = N↑ + 12OH-
2 2
【解析】(6)在中性介质中 在阴极得电子生成氮气,阴极电极反应式2NO +10e- + 6H O = N↑ +
2 2
12OH-。
2.(2023·四川绵阳·统考一模·节选)电解锌的生产过程中产生大量富钴渣,主要含金属Zn、Cd及CoO、
MnO和FeO。采用以下工艺可利用富钴渣生产高纯锌:
回答下列问题:
(2)加入HO 后生成FeOOH的化学方程式为 。
2 2
(4)“除锰钴”中,生成MnO 的离子方程式为 。
2
(6)“电解”可通过如图装置实现。电解时,钛合金上的电极反应式为 。
【答案】(2)2FeSO +H O+2H O=2FeOOH↓+2H SO
4 2 2 2 2 4
(4)3Mn2++2MnO +2H O=5MnO ↓+4H+
2 2
(6)ZnO +2e-+2H O=Zn+4OH-
2
【分析】富钴渣主要含金属Zn、Cd及CoO、MnO和FeO,加入硫酸酸浸,溶解,加入过氧化氢把Fe2+氧
化成Fe3+,pH调整到5生成FeOOH沉淀,过滤后加入高锰酸钾生成MnO 和CoOOH沉淀过滤,加入Zn
2除去溶液中的Cd2+,过滤,加入氢氧化钠,把锌溶解生成NaZnO,电解生成单质Zn,反应方程式为
2 2
2NaZnO+2H O=4NaOH+2Zn+O 。
2 2 2 2
【解析】(2)加入HO 后,Fe2+被氧化生成FeOOH的化学方程式为
2 2
2FeSO +H O+2H O=2FeOOH↓+2H SO ;故答案为:2FeSO +H O+2H O=2FeOOH↓+2H SO 。
4 2 2 2 2 4 4 2 2 2 2 4
(4)“除锰钴”中,高锰酸钾和Mn2+反应生成MnO ,离子方程式为3Mn2++2MnO
2
+2H O=5MnO ↓+4H+;故答案为:3Mn2++2MnO +2H O=5MnO ↓+4H+。
2 2 2 2
(6)电解池中钛合金为阴极,发生还原反应,电极反应式为ZnO +2e-+2H O=Zn+4OH-;故答案为:ZnO
2
+2e-+2H O=Zn+4OH-。
2
3.(2023·湖南常德·常德市一中校考模拟预测·节选)铋(Bi)的化合物广泛应用于电子、医药等领域。由辉
铋矿(主要成分为BiS,含FeS、CuO、SiO 等杂质)制备NaBiO 的工艺流程如下:
2 3 2 2 3
已知: i. Bi3+易水解。 难溶于冷水。
ⅱii.“氧化浸取”时,铋元素转化为Bi3+,硫元素转化为硫单质。
回答下列问题:
(4)“转化”时,生成NaBiO 的离子方程式为 。
3
(5)已知酸性环境下,NaBiO 可以将Mn2+氧化成 ( 被还原成Bi3+)。请设计一个原电池装置来证明
3
这一点,在下图中的两个方框内标出两烧杯溶液中溶质的化学式,并写出正极的电极反应式:
。(左侧烧杯中已经加入了硫酸)
【答案】(4)
(5)NaBiO,MnSO ; (或)
3 4
【分析】向辉铋矿(主要成分为BiS,含FeS、CuO、SiO 等杂质)加盐酸、双氧水进行氧化浸取,BiS、
2 3 2 2 2 3
FeS、CuO转化为可溶性的盐和硫单质;由于 为不溶于水和盐酸的酸性氧化物,过滤则滤渣1的主要
2
成分为S和 ;调节滤液pH值使 转化成 沉淀;再次过滤除去铁离子,向滤液中加过滤量
氨除铜;再次用盐酸溶解固体,用NaOH、NaClO沉淀铋,使其转化为 沉淀,最后经系列操作得到
。据此分析可得:
【解析】(4)“转化”时NaOH、NaClO与 发生氧化还原反应生成难溶于冷水的 ,故答案为:;
(5)酸性环境下,NaBiO 可以将 氧化成 ( 被还原成Bi3+), 为电源正极反应物;
3
为电源负极反应物,由于电子由右经导线流向左,所以左、右两方框内的物质分别为NaBiO、
3
MnSO ;正极发生还原反应,即在酸性条件下 得到电子被还原为 ,故答案为:NaBiO,
4 3
MnSO ; (或) 。
4
4.(2023·内蒙古赤峰·统考一模·节选)随着新能源汽车的发展,钾电池成为近些年来研究的热点、锂电
池中一些金属的回收利用也是未来发展的一大方向。SiCl 是生产多晶硅的副产物。可以利用SiCl 对废弃
4 4
的钾电池正极材料LiCoO 进行氯化处理、进而回收Li、Co等金属,工艺路线如图所示:
2
(3)“850℃煅烧”时的化学方程式为 。
(4)利用碳酸锂( )与 按n(Li):n(Co)=1:1的比例配合,然后在空气中于700℃烧结可合成锂电
池正极材料 反应方程式为 。
(5)海水中有丰富的锂资源,我国科学家研发出利用太阳能从海水中提取金属锂的技术,提取原理如图所示。
金属锂在电极 (填“A”或“B”)上生成,阳极产生两种气体单质、电极反应式是 。
【答案】(2)SiCl +3H O=HSiO↓+4HCl
4 2 2 3
(3) 6Co(OH) +O 2Co O+6H O
2 2 3 4 2
(4)
(5)A 2Cl--2e-=Cl↑、2HO-4e-= O ↑+4H+
2 2 2
【分析】“500℃焙烧”的烧渣是LiCl、CoCl 和SiO 的混合物,水浸除去SiO,滤液1中加氢氧化钠生成
2 2 2
Co(OH) 沉淀,过滤,“850℃煅烧”时Co(OH) 和氧气反应生成Co O,滤液2加碳酸钠生成 沉淀。
2 2 3 4
【解析】(2)SiCl 发生水解生成硅酸沉淀和氯化氢,产生烟雾,反应的化学方程式为
4
SiCl +3H O=HSiO↓+4HCl;
4 2 2 3
(3)“850℃煅烧”时Co(OH) 和氧气反应生成Co O 和水,反应的化学方程式为6Co(OH) +O
2 3 4 2 22Co O+6H O;
3 4 2
(4)利用碳酸锂( )与 按n(Li):n(Co)=1:1的比例配合,然后在空气中于700℃烧结可合成
锂电池正极材料 ,Co元素化合价由+2升高为+3,所以氧气参加反应,根据得失电子守恒,反应方
程式为 ;
(5)根据电子流向,可知A是阴极、B是阳极,Li+得电子发生还原反应生成金属Li,金属锂在电极A上
生成;海水中含有氯离子和氢氧根离子,阳极上氯离子和氢氧根离子放电生成氯气和氧气,电极反应式是
2Cl--2e-=Cl↑、2HO-4e-= O ↑+4H+。
2 2 2
5.(2023·云南昆明·统考二模·节选)NiSO 主要用于电镀工业,作为电镀镍和化学镍的主要原料,也用于
4
生产其他镍盐(如氧化镍、硫酸镍铵、碳酸镍等),从矿渣[含NiFe O(铁酸镍)、NiO、FeO、CaO、SiO 等]
2 4 2
中回收NiSO 的工艺流程如图:
4
已知(NH )SO 在350℃分解生成NH 和HSO ,回答下列问题:
4 2 4 3 2 4
(2)矿渣中部分FeO焙烧时与HSO 反应生成Fe (SO ) 的化学方程式为 。
2 4 2 4 3
(5)以Fe、Ni为电极制取NaFeO 的原理如图所示。通电后,在铁电极附近生成紫红色的FeO ,若pH过
2 4
高
①电解时阳极的电极反应式为 ,离子交换膜(b)为 (填“阴”或“阳”)离子交换
膜。
②向铁电极区出现的红褐色物质中加入少量的NaClO溶液,沉淀溶解。该反应的离子方程式为
。
【答案】(2)4FeO+6H SO +O =2Fe (SO )+6H O
2 4 2 2 4 3 2
(5)Fe﹣6e﹣+8OH-=FeO +4H O 阴 2Fe(OH) +3ClO﹣+4OH﹣=2 FeO +3Cl﹣+5H O
2 3 2
【分析】某矿渣的主要成分是NiFe O(铁酸镍)、NiO、FeO、CaO、SiO 等,加入硫酸铵研磨后,600℃焙
2 4 2烧,已知:(NH )SO 在350℃以上会分解生成NH 和HSO NiFe O 在焙烧过程中生成NiSO 、Fe (SO ),
4 2 4 3 2 4. 2 4 4 2 4 3
在90℃的热水中浸泡过滤得到浸出液,加入NaF除去钙离子,过滤得到滤液加入萃取剂得到无机相和有机
相,无机相通过一系列操作得到硫酸镍,有机相循环使用,以此解答该题;
【解析】(2)矿渣中部分FeO焙烧时与HSO 反应生成Fe (SO ) 的化学方程式:
2 4 2 4 3
4FeO+6HSO +O =2Fe (SO )+6H O;
2 4 2 2 4 3 2
(5)①电解池中阳极发生氧化反应,依据题意可知铁在阳极失去电子,电极反应式为:Fe﹣6e﹣+8OH-
=FeO +4H O,离子交换膜(b))为阴离子交换膜;
2
②向铁电极区出现的红褐色物质中加入少量的NaClO溶液,沉淀溶解:2Fe(OH) +3ClO﹣+4OH﹣=2 FeO
3
+3Cl﹣+5H O;
2
1.(2024·广西·校联考一模)高铁酸钾(K FeO)是一种新型、高效、无毒的水处理剂。工业上,利用廉价
2 4
的铁黄(FeOOH)等为原料制备高铁酸钾。工艺流程如图:
下列说法错误的是
A.高铁酸钾在水处理过程中涉及氧化还原反应和盐类水解反应
B.制备NaFeO 反应中氧化剂和还原剂的物质的量之比为2∶3
2 4
C.根据流程可以判断相同温度下KFeO 的溶解度小于NaFeO
2 4 2 4
D.若通过电解法以铁为原料制备高铁酸钾,铁棒应该做阳极
【答案】B
【分析】铁黄和次氯酸钠反应生成高铁酸钠,2FeOOH+3NaClO+4NaOH=2Na FeO+3NaCl+3HO,高铁酸
2 4 2
钠在溶液中溶解度大于高铁酸钾,加入KOH,高铁酸钠在溶液中转化成高铁酸钾。
【解析】A.KFeO 具有强氧化性,可用于消毒杀菌,被还原为Fe3+,Fe3+发生盐类的水解生成Fe(OH) ,
2 4 3
具有吸附性,可用于吸附水中的悬浮杂质,故A正确;B.制备NaFeO 反应
2 4
2FeOOH+3NaClO+4NaOH=2Na FeO+3NaCl+3HO,氯元素化合价降低,NaClO是氧化剂,铁元素化合价
2 4 2
升高,FeOOH是还原剂,氧化剂和还原剂的物质的量之比为3∶2,故B错误;C.向高铁酸钠溶液加入浓
KOH能生成高铁酸钾沉淀,可知相同温度下KFeO 的溶解度小于NaFeO,故C正确;D.若通过电解法
2 4 2 4
以铁为原料制备高铁酸钾,铁元素化合价升高,在阳极反应,则铁棒应该做阳极,故D正确;故选B。
2.(2023·河北邢台·统考模拟预测)在分析化学上,测定含 酸性溶液中钛元素的含量通常涉及两个
反应:
I.用 粉还原 得到 ;II.用 溶液滴定,反应的离子方程式为。
下列说法错误的是
A.还原性:
B.反应I中氧化产物和还原产物的物质的量之比为
C.反应II的滴定实验可选用 溶液作指示剂
D.反应I中生成 时消耗的 和反应Ⅱ中消耗 时生成的 的量相同
【答案】B
【解析】A.根据反应I中 作还原剂,则还原性 ,再结合反应II可知还原性: ,
A项正确;B.根据电子守恒可知,反应I中氧化产物和还原产物的物质的量之比为 ,B项错误;C.
Fe3+和SCN-反应能生成红色物质,所以反应II的滴定实验可选用 溶液作指示剂,C项正确;D.书
写并配平反应的离子方程式可知 ,结合反应II分析可知D项正确;
故选B。
3.(2023·广东茂名·高三校联考)混合体系中,确认化学反应的先后顺序有利于问题的解决,下列反应先
后顺序判断正确的是
A.等物质的量的Fe3+、Cu2+、H+的溶液中加入Fe:Fe3+、H+、Cu2+
B.等物质的量的Ca(OH) 、NaOH的溶液中通入CO:Ca(OH) 、NaOH、CaCO 、NaCO
2 2 2 3 2 3
C.等物质的量的FeBr 、FeI 的溶液中缓慢通入Cl:Fe2+、I-、Br-
2 2 2
D.等物质的量的Al3+、H+、NH 溶液中,逐滴加入NaOH溶液:H+、Al3+、NH 、Al(OH)
3
【答案】D
【解析】A. 离子的氧化性顺序是:Fe3+>Cu2+>H+,在含等物质的量的Fe3+、Cu2+、H+的溶液中加入Fe,
Fe先和氧化性强的离子发生反应,则反应先后顺序为Fe3+、Cu2+、H+,故A错误;B. 在含等物质的量的
Ca(OH) 、NaOH的溶液中通入CO,CO 先是和Ca(OH) 发生反应生成碳酸钙沉淀和水,其次是氢氧化钠,
2 2 2 2
再是和碳酸钠之间发生反应,最后和碳酸钙发生反应,故B错误;C. 离子的还原性顺序为I->Fe2+>Br-,
在含等物质的量的FeBr 、FeI 的溶液中缓慢通入Cl,氯气具有氧化性,先和还原性强的离子反应,反应
2 2 2
先后顺序为I-、Fe2+、Br-,故C错误;D. 含等物质的量的Al3+、H+、NH 溶液中,逐滴加入NaOH溶
液,OH-先和H+反应生成水,再和Al3+反应生成Al(OH) 沉淀,然后和NH 反应生成一水合氨,最后和
3
Al(OH) 反应生成偏铝酸根离子和水,反应的先后顺序为H+、Al3+、NH 、Al(OH) ,故D正确;答案选D
3 3
。
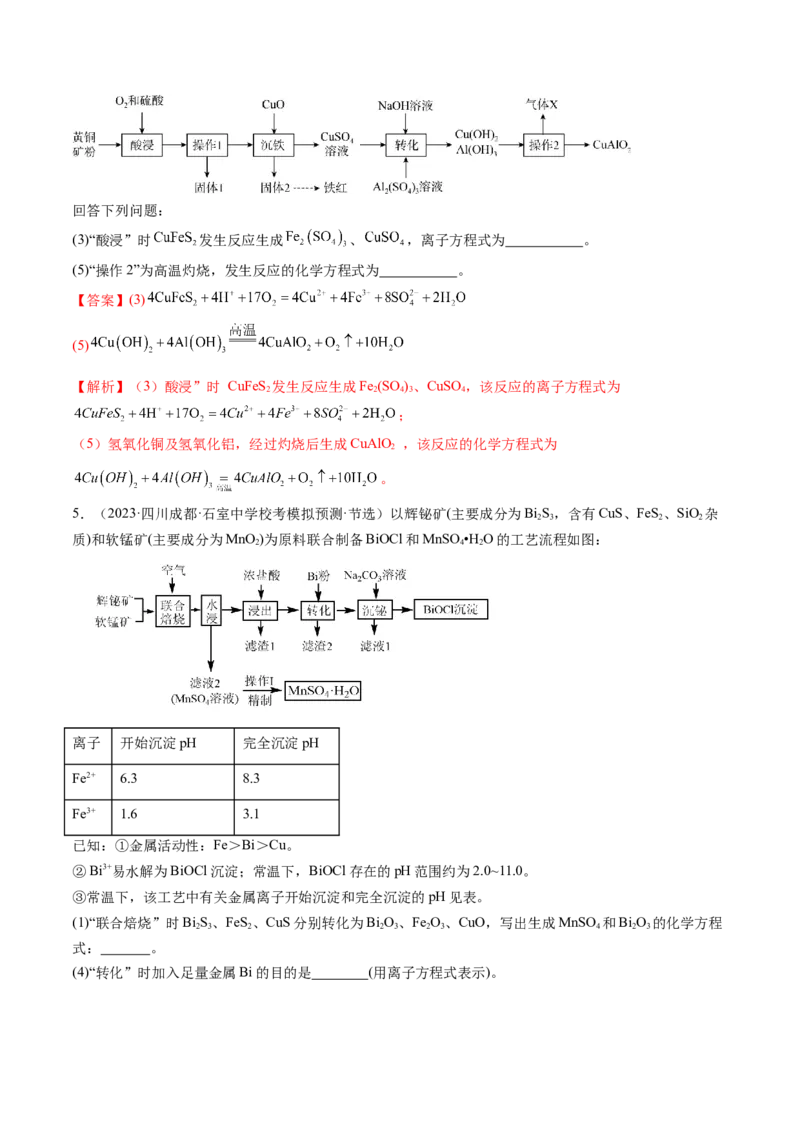
4.(2023·海南省直辖县级单位·统考模拟预测·节选)以黄铜矿(主要成分是 ,含 杂质)为原料
制备高纯度铁红和化工产生 ,流程如下:回答下列问题:
(3)“酸浸”时 发生反应生成 、 ,离子方程式为 。
(5)“操作2”为高温灼烧,发生反应的化学方程式为 。
【答案】(3)
(5)
【解析】(3)酸浸”时 CuFeS 发生反应生成Fe (SO )、CuSO ,该反应的离子方程式为
2 2 4 3 4
;
(5)氢氧化铜及氢氧化铝,经过灼烧后生成CuAlO ,该反应的化学方程式为
2
。
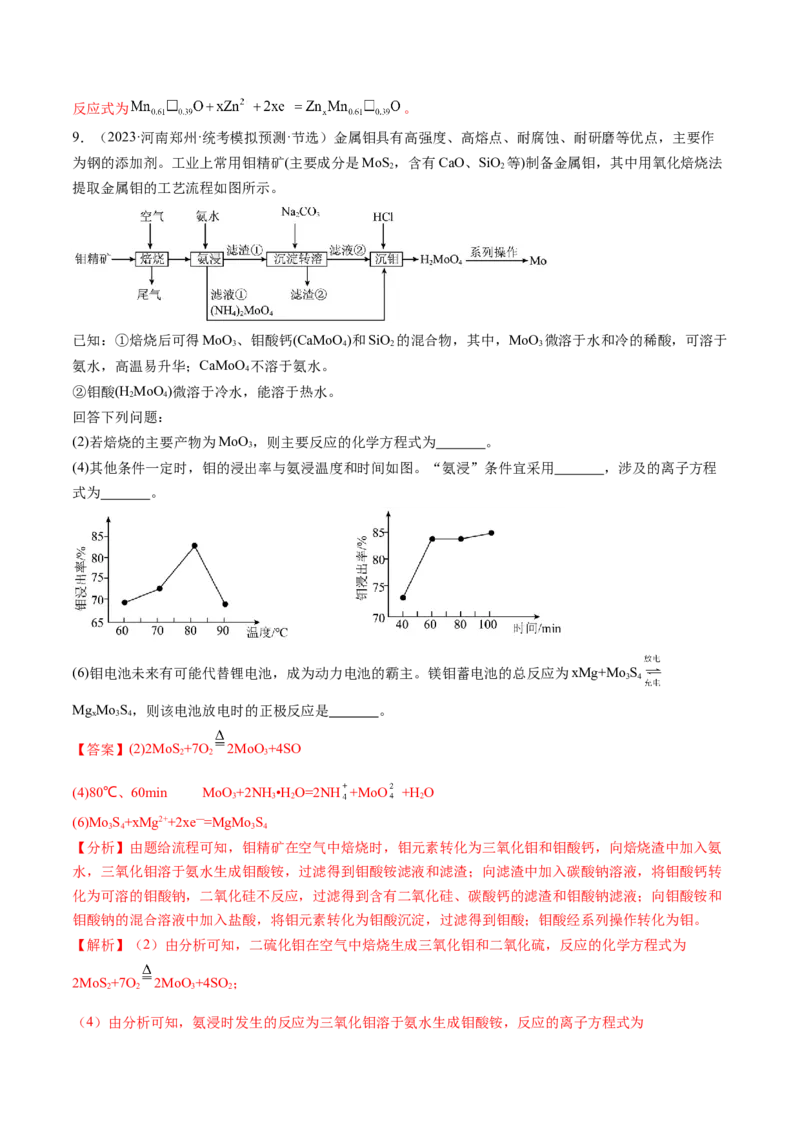
5.(2023·四川成都·石室中学校考模拟预测·节选)以辉铋矿(主要成分为BiS,含有CuS、FeS、SiO 杂
2 3 2 2
质)和软锰矿(主要成分为MnO )为原料联合制备BiOCl和MnSO •H O的工艺流程如图:
2 4 2
离子 开始沉淀pH 完全沉淀pH
Fe2+ 6.3 8.3
Fe3+ 1.6 3.1
已知:①金属活动性:Fe>Bi>Cu。
②Bi3+易水解为BiOCl沉淀;常温下,BiOCl存在的pH范围约为2.0~11.0。
③常温下,该工艺中有关金属离子开始沉淀和完全沉淀的pH见表。
(1)“联合焙烧”时BiS、FeS、CuS分别转化为BiO、Fe O、CuO,写出生成MnSO 和BiO 的化学方程
2 3 2 2 3 2 3 4 2 3
式: 。
(4)“转化”时加入足量金属Bi的目的是 (用离子方程式表示)。【答案】(1)2Bi S+6MnO+9O 2BiO+6MnSO
2 3 2 2 2 3 4
(4)Bi+3Fe3+=Bi3++3Fe2+、2Bi+3Cu2+=3Cu+2Bi3+
【分析】辉铋矿(主要成分为BiS,含有CuS、FeS、SiO 杂质)和软锰矿(主要成分为MnO )通入空气联合
2 3 2 2 2
焙烧,得到BiO、Fe O、CuO、SiO 和MnSO ,水浸得到滤液2为MnSO 溶液,通过精制得到
2 3 2 3 2 4 4
MnSO •H O,不溶性固体用浓盐酸浸出,二氧化硅不溶得到滤渣1为二氧化硅,滤液含有Cu2+、Bi3+、
4 2
Fe3+,加铋粉,按信息①,发生反应:Bi+3Fe3+=Bi3++3Fe2+、2Bi+3Cu2+=3Cu+2Bi3+,置换出铜,则滤渣2为
铜,滤液含有Bi3+、 Fe2+,加碳酸钠溶液沉铋、即调节pH得到BiOCl沉淀。
【解析】(1)“联合焙烧”时BiS、MnO 和O 在高温下反应生成MnSO 和BiO,化学方程式:
2 3 2 2 4 2 3
2BiS+6MnO+9O 2BiO+6MnSO 。
2 3 2 2 2 3 4
(4)按信息①金属活动性:Fe>Bi>Cu,结合Fe、Cu均能与铁离子反应可知,Bi 能与铁离子反应,则
“转化”时加入足量金属Bi的目的是:Bi+3Fe3+=Bi3++3Fe2+、2Bi+3Cu2+=3Cu+2Bi3+。
6.(2023·江苏盐城·盐城中学校考二模·节选)氧化铈(CeO)是一种应用非常广泛的稀土氧化物。现以氟碳
2
铈矿(含CeFCO、BaO、SiO 等)为原料制备氧化铈,其工艺流程如图所示:
3 2
已知:①稀土离子易与 形成复盐沉淀,Ce3+和 发生反应:
Ce (SO )+Na SO +nH O=Ce (SO )·Na SO ·nH O↓;
2 4 3 2 4 2 2 4 3 2 4 2
②硫脲: 具有还原性,酸性条件下易被氧化为(SCN H);
2 3 2
③Ce3+在空气中易被氧化为Ce4+,两者均能形成氢氧化物沉淀;
④Ce (CO) 为白色粉末,难溶于水。
2 3 3
回答下列问题:
(2)在另一种生产工艺中,在氟碳铈矿矿石粉中加入碳酸氢钠同时通入氧气焙烧,焙烧得到NaF和CeO 两
2
种固体以及两种高温下的气态物质,请写出焙烧过程中相应的化学方程式 。
(3)加入硫脲的目的是将 还原为Ce3+,反应的离子方程式为 。
【答案】(2)4CeFCO +4NaHCO+O 4NaF+4CeO +8CO +2H O
3 3 2 2 2 2
(3)2 +2 =2Ce3++(SCNH)+2HF+2F-
2 3 2【分析】氟碳铈矿(含CeFCO、BaO、SiO 等)在空气中焙烧,Ce3+在空气中氧化为Ce4+,加稀硫酸浸取,
3 2
Ce4+进入溶液,SiO 不反应,BaO与硫酸反应生成BaSO 沉淀,过滤分离,滤渣A为SiO、BaSO;含
2 4 2 4
滤液中加入硫脲将Ce4+还原为Ce3+,Ce (SO ) 与NaSO 形成复盐沉淀B为Ce (SO )•Na SO •nH O,
2 4 3 2 4 2 4 3 2 4 2
过滤分离。复盐沉淀加入NaOH,再加入稀盐酸,Ce3+被转移到溶液中,加入碳酸氢铵使Ce3+沉淀为
Ce (CO),最后灼烧分解生成CeO。
2 3 3 2
【解析】(2)在氟碳铈矿矿石粉(CeFCO)中加入碳酸氢钠同时通入氧气焙烧,焙烧得到NaF和CeO 两种
3 2
固体以及两种高温下的气态物质,根据质量守恒得到两种高温气体为二氧化碳和水蒸气,则焙烧过程中反
应的化学方程式为4CeFCO+4NaHCO+O 4NaF+4CeO +8CO +2H O。
3 3 2 2 2 2
(3)根据信息硫脲( )具有还原性,酸性条件下易被氧化为(SCN H),则加入硫脲的目的
2 3 2
是将 还原为Ce3+,反应的离子方程式为2 +2 =2Ce3++(SCNH)+2HF+2F-。
2 3 2
7.(2023·辽宁鞍山·统考一模·节选)废旧铅蓄电池拆解获得铅膏(主要由PbSO 、PbO 、PbO形成的悬浊
4 2
液),对其回收利用可减少环境污染。流程如下:
(1)“还原”步骤PbO 发生反应的化学方程式为 。
2
(2)利用选出的脱硫试剂写出“脱硫”步骤的离子方程式
(3)“酸浸”步骤HBF 是一种强酸,该步骤PbO发生反应的离子方程式为 。
4
(4)若电解时阳极有微量PbO 生成,写出生成PbO 的电极反应式 。
2 2
【答案】(1)
(2)
(3)
(4)
【分析】由流程可知,铅膏中PbO 在还原步骤中被SO 还原为PbSO ,再利用沉淀转化原理转化为
2 2 4
PbCO3,加入强酸HBF 后,PbCO 和PbO均溶解出 ,最后用电解原理得到单质Pb。
4 3
【解析】(1)为提高“还原”步骤的反应速率,可采取的具体措施有适当升温或充分搅拌等;PbO 在还
2
原步骤中被SO 还原为PbSO ,化学方程式为: ;故答案为:适当升温或充分搅拌等;
2 4
;
(2)该步骤的离子方程式为; ;故答案为:;
(3)HBF 溶解PbO的离子方程式为: ;故答案为: ;
4
(4)若电解时阳极有微量PbO 生成,则电极反应式为: ;故答案为:防止氢
2
离子在 Pb2+之前放电; 。
8.(2023·安徽芜湖·安徽师范大学附属中学校考模拟预测)菱锰矿的主要成分为MnCO ,主要杂质为
3
SiO、CaCO 、Al O、FeCO、NiS。已知K [Al(OH) ]=4×10-33。利用菱锰矿制晶体MnO的流程如下:
2 3 2 3 3 sp 3
(1)氧化过滤时体系溶液的pH=3,此时发生反应的离子方程式为 。
(4)沉锰时发生反应的离子方程式为 ;
(5)通过Zn2+在MnO晶体(正极)中嵌入和脱嵌,实现电极材料充放电的原理如图所示。
代表电池 (填“充电”或“放电”)过程,该过程的电极反应式为 。
【答案】(1)MnO +2Fe2++4H O=2Fe(OH) ↓+Mn2++2H+
2 2 3
(4)Mn2++2 =MnCO↓+H O+CO↑
3 2 2
(5)放电 Mn □ O+xZn2++2xe-=ZnMn □ O
0.61 0.39 x 0.61 0.39
【分析】菱锰矿的主要成分为 ,主要杂质为 、 、 、 、 ,用硫酸溶解,
碳酸锰和硫酸反应生成硫酸锰、碳酸钙和硫酸反应生成硫酸钙沉淀、氧化铝和硫酸反应生成硫酸铝、碳酸
亚铁和和硫酸反应生成硫酸亚铁,二氧化硅和硫酸不反应,过滤出二氧化硅、硫酸钙沉淀,滤液中含有
Mn2+、Al3+、Fe2+,用二氧化锰氧化Fe2+生成Fe(OH) 沉淀除铁,过滤出氢氧化铁沉淀,滤液中加氢氧化钙
3
调节pH=5生成Al(OH) 沉淀除铝,滤液中加SDD除 ,过滤,滤液加碳酸氢铵生成碳酸锰沉淀,灼烧
3
碳酸锰得到MnO晶体。
【解析】(1)氧化过滤时体系溶液的pH=3,目的是氧化Fe2+生成Fe(OH) 沉淀,此时发生反应的离子方
3
程式为 。
(4)沉锰时碳酸氢铵和硫酸锰反应生成碳酸锰沉淀、硫酸铵、二氧化碳,发生反应的离子方程式为
;
(5)电池放电时,阳离子向正极移动, 嵌入 晶体,②代表电池放电过程,该过程的电极反应式为 。
9.(2023·河南郑州·统考模拟预测·节选)金属钼具有高强度、高熔点、耐腐蚀、耐研磨等优点,主要作
为钢的添加剂。工业上常用钼精矿(主要成分是MoS ,含有CaO、SiO 等)制备金属钼,其中用氧化焙烧法
2 2
提取金属钼的工艺流程如图所示。
已知:①焙烧后可得MoO 、钼酸钙(CaMoO )和SiO 的混合物,其中,MoO 微溶于水和冷的稀酸,可溶于
3 4 2 3
氨水,高温易升华;CaMoO 不溶于氨水。
4
②钼酸(H MoO )微溶于冷水,能溶于热水。
2 4
回答下列问题:
(2)若焙烧的主要产物为MoO ,则主要反应的化学方程式为 。
3
(4)其他条件一定时,钼的浸出率与氨浸温度和时间如图。“氨浸”条件宜采用 ,涉及的离子方程
式为 。
(6)钼电池未来有可能代替锂电池,成为动力电池的霸主。镁钼蓄电池的总反应为xMg+Mo S
3 4
MgMoS,则该电池放电时的正极反应是 。
x 3 4
【答案】(2)2MoS +7O 2MoO +4SO
2 2 3
(4)80℃、60min MoO +2NH•H O=2NH +MoO +H O
3 3 2 2
(6)Mo S+xMg2++2xe—=MgMo S
3 4 3 4
【分析】由题给流程可知,钼精矿在空气中焙烧时,钼元素转化为三氧化钼和钼酸钙,向焙烧渣中加入氨
水,三氧化钼溶于氨水生成钼酸铵,过滤得到钼酸铵滤液和滤渣;向滤渣中加入碳酸钠溶液,将钼酸钙转
化为可溶的钼酸钠,二氧化硅不反应,过滤得到含有二氧化硅、碳酸钙的滤渣和钼酸钠滤液;向钼酸铵和
钼酸钠的混合溶液中加入盐酸,将钼元素转化为钼酸沉淀,过滤得到钼酸;钼酸经系列操作转化为钼。
【解析】(2)由分析可知,二硫化钼在空气中焙烧生成三氧化钼和二氧化硫,反应的化学方程式为
2MoS +7O 2MoO +4SO;
2 2 3 2
(4)由分析可知,氨浸时发生的反应为三氧化钼溶于氨水生成钼酸铵,反应的离子方程式为MoO +2NH•H O=2NH +MoO +H O;由图可知,氨浸温度为80℃、时间为60min时,钼的浸出率最高,
3 3 2 2
则氨浸宜采用的条件为80℃、60min,故答案为:80℃、60min;MoO +2NH•H O=2NH +MoO +H O;
3 3 2 2
(6)由镁钼蓄电池的总反应可知,四硫化三钼为蓄电池的正极,镁离子作用下,四硫化三钼在正极得到
电子发生还原反应生成MgMoS,电极反应式为MoS+xMg2++2xe—=MgMo S,故答案为:MoS+xMg2+
x 3 4 3 4 3 4 3 4
+2xe—=MgMo S。
3 4
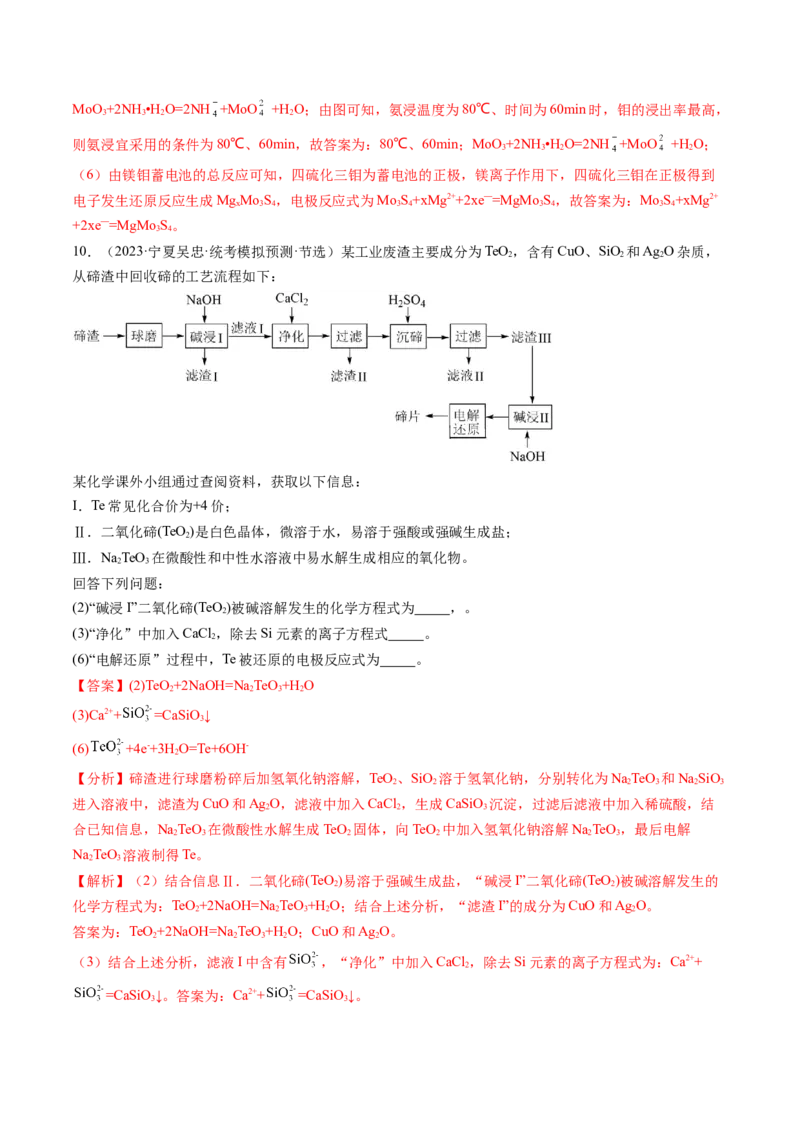
10.(2023·宁夏吴忠·统考模拟预测·节选)某工业废渣主要成分为TeO ,含有CuO、SiO 和Ag O杂质,
2 2 2
从碲渣中回收碲的工艺流程如下:
某化学课外小组通过查阅资料,获取以下信息:
I.Te常见化合价为+4价;
Ⅱ.二氧化碲(TeO )是白色晶体,微溶于水,易溶于强酸或强碱生成盐;
2
Ⅲ.NaTeO 在微酸性和中性水溶液中易水解生成相应的氧化物。
2 3
回答下列问题:
(2)“碱浸I”二氧化碲(TeO )被碱溶解发生的化学方程式为 ,。
2
(3)“净化”中加入CaCl ,除去Si元素的离子方程式 。
2
(6)“电解还原”过程中,Te被还原的电极反应式为 。
【答案】(2)TeO +2NaOH=Na TeO +H O
2 2 3 2
(3)Ca2++ =CaSiO ↓
3
(6) +4e-+3H O=Te+6OH-
2
【分析】碲渣进行球磨粉碎后加氢氧化钠溶解,TeO 、SiO 溶于氢氧化钠,分别转化为NaTeO 和NaSiO
2 2 2 3 2 3
进入溶液中,滤渣为CuO和Ag O,滤液中加入CaCl ,生成CaSiO 沉淀,过滤后滤液中加入稀硫酸,结
2 2 3
合已知信息,NaTeO 在微酸性水解生成TeO 固体,向TeO 中加入氢氧化钠溶解NaTeO ,最后电解
2 3 2 2 2 3
NaTeO 溶液制得Te。
2 3
【解析】(2)结合信息Ⅱ.二氧化碲(TeO )易溶于强碱生成盐,“碱浸I”二氧化碲(TeO )被碱溶解发生的
2 2
化学方程式为:TeO +2NaOH=Na TeO +H O;结合上述分析,“滤渣I”的成分为CuO和Ag O。
2 2 3 2 2
答案为:TeO +2NaOH=Na TeO +H O;CuO和Ag O。
2 2 3 2 2
(3)结合上述分析,滤液I中含有 ,“净化”中加入CaCl ,除去Si元素的离子方程式为:Ca2++
2
=CaSiO ↓。答案为:Ca2++ =CaSiO ↓。
3 3(6)电解时, 在阴极放电生成Te,其电极反应式为: +4e-+3H O=Te+6OH-。
2
答案为: +4e-+3H O=Te+6OH-。
2
1.(2023·福建·统考高考真题)稀有气体氙的氟化物 与 溶液反应剧烈,与水反应则较为温和,
反应式如下:
与水反应 与 溶液反应
i. ii.
iv.
iii.
下列说法错误的是
A. 具有平面三角形结构 B. 的还原性比 强
C.反应i~iv中有3个氧化还原反应 D.反应iv每生成 ,转移 电子
【答案】A
【解析】A.Xe原子以sp3杂化轨道成键, 分子为三角锥形分子,A错误;B.由iii、iv两组实验对
比可知,在氢氧化钠溶液中, 可以发生还原反应,而在水中则发生非氧化还原反应,故可知: 的
还原性比 强,B正确;C.I、iii、iv三组化学反应均为氧化还原反应,C正确;D.分析iv可知,每
生成一个 ,整个反应转移6个电子,故每生成 ,转移 电子,D正确;故选A。
2.(2022·浙江·统考高考真题)关于反应 ,下列说法正确的是
A. 发生还原反应
B. 既是氧化剂又是还原剂
C.氧化产物与还原产物的物质的量之比为2∶1
D. 发生反应,转移 电子
【答案】B
【分析】NaSO+H SO =Na SO +S ↓+SO ↑ +H O,该反应的本质是硫代硫酸根离子在酸性条件下发生歧化
2 2 3 2 4 2 4 2 2
反应生成硫和二氧化硫,化合价发生变化的只有S元素一种,硫酸的作用是提供酸性环境。
【解析】A.HSO 转化为硫酸钠和水,其中所含元素的化合价均未发生变化,故其没有发生还原反应,A
2 4
说法不正确;B.NaSO 中的S的化合价为+2,其发生歧化反应生成S(0价)和SO (+4价),故其既是氧化
2 2 3 2剂又是还原剂,B说法正确;C.该反应的氧化产物是SO ,还原产物为S,氧化产物与还原产物的物质的
2
量之比为1:1,C说法不正确;D.根据其中S元素的化合价变化情况可知,1mol Na SO 发生反应,要转
2 2 3
移2 mol电子,D说法不正确。综上所述,本题选B。
3.(2022·浙江·统考高考真题)关于反应4CO+SiH 4CO+2HO+SiO,下列说法正确的是
2 4 2 2
A.CO是氧化产物 B.SiH 发生还原反应
4
C.氧化剂与还原剂的物质的量之比为1∶4 D.生成1molSiO 时,转移8mol电子
2
【答案】D
【解析】A.根据反应方程式,碳元素的化合价由+4价降为+2价,故CO为还原产物,A错误;B.硅元
素化合价由-4价升为+4价,故SiH 发生氧化反应,B错误;C.反应中氧化剂为二氧化碳,还原剂为
4
SiH ,,则氧化剂与还原剂的物质的量之比为4:1,C错误;D.根据反应方程式可知,Si元素的化合价
4
由-4价升高至+4价,因此生成1molSiO 时,转移8mol电子,D正确;答案选D。
2
4.(2021·海南·统考高考真题)依据下列实验和现象,得出结论正确的是
选项 实验 现象 结论
点燃无色气体 ,将生成的气体通入澄 澄清石灰水先浑浊后澄
A 为
清石灰水 清
25℃时,向无色的 溶液中滴加1~2滴
B 溶液仍为无色 溶液的
酚酞试液
在淀粉和 的混合溶液中滴加 溶
C 液。[已知: 、 分别与卤素 溶液仍为蓝色 氧化性:
单质、卤素离子性质相似]
溶液由无色变为蓝色并 反应中 既作氧化剂
D 在稀 中加入少量
有红色固体生成 又作还原剂
【答案】D
【解析】A.无色气体甲烷在空气中燃烧生成二氧化碳和水,将生成的气体通入澄清石灰水,澄清石灰水
也会先浑浊后澄清,则无色气体X不一定为一氧化碳,故A错误;B.若无色Y溶液的pH在7—8之间,
向溶液中滴加1~2滴酚酞试液,溶液也为无色,则溶液仍为无色不能判断得到溶液pH小于7,故B错误;
C.若向淀粉和碘的混合溶液中滴加不足量的硫氰化钾溶液,碘未完全反应,溶液也呈蓝色,则溶液仍为
蓝色不能判断硫氰气和碘的氧化性强弱,故C错误;D.在稀硫酸中加入少量氧化亚铜固体,溶液由无色
变为蓝色并有红色固体生成说明氧化亚铜在稀硫酸溶液中反应生成硫酸铜和铜,则反应中氧化亚铜既作氧
化剂又作还原剂,故D正确;故选D。
5.(2022·浙江·高考真题)关于反应4CO+SiH 4CO+2HO+SiO,下列说法正确的是
2 4 2 2A.CO是氧化产物 B.SiH 发生还原反应
4
C.氧化剂与还原剂的物质的量之比为1∶4 D.生成1molSiO 时,转移8mol电子
2
【答案】D
【解析】A.根据反应方程式,碳元素的化合价由+4价降为+2价,故CO为还原产物,A错误;B.硅元
素化合价由-4价升为+4价,故SiH 发生氧化反应,B错误;C.反应中氧化剂为二氧化碳,还原剂为
4
SiH,,则氧化剂与还原剂的物质的量之比为4:1,C错误;D.根据反应方程式可知,Si元素的化合价
4
由-4价升高至+4价,因此生成1molSiO 时,转移8mol电子,D正确;答案选D。
2
6.(2023·辽宁·统考高考真题)某无隔膜流动海水电解法制 的装置如下图所示,其中高选择性催化剂
可抑制 产生。下列说法正确的是
A.b端电势高于a端电势 B.理论上转移 生成
C.电解后海水 下降 D.阳极发生:
【答案】D
【分析】根据图示,钛网上海水中Cl-、HO发生失电子的氧化反应生成HClO、O,钛网为阳极,电极反
2 2
应式为Cl-+H O-2e-=HClO+H+,钛箔上生成H,钛箔上生成H 的电极反应为2H++2e-=H ↑,钛箔为阴极,
2 2 2 2
高选择性催化剂PRT可抑制O 产生,电解的主要总反应为H++Cl-+H O HClO+H↑,以此解题。
2 2 2
【解析】A.由分析可知,a为正极,b电极为负极,则a端电势高于b端电势,A错误;B.右侧电极上产
生氢气的电极方程式为:2H++2e-=H ↑,则理论上转移 生成 ,B错误;C.由分析可知,电解
2
的主要总反应为H++Cl-+H O HClO+H↑,电解后海水中H+浓度减小,pH上升,C错误;D.由图可知,
2 2
阳极上的电极反应为: ,D正确;故选D。
7.(2022·浙江·统考高考真题)通过电解废旧锂电池中的 可获得难溶性的 和 ,电解
示意图如下(其中滤布的作用是阻挡固体颗粒,但离子可自由通过。电解过程中溶液的体积变化忽略不计)。
下列说法不正确的是A.电极A为阴极,发生还原反应
B.电极B的电极反应:
C.电解一段时间后溶液中 浓度保持不变
D.电解结束,可通过调节 除去 ,再加入 溶液以获得
【答案】C
【解析】A.由电解示意图可知,电极B上Mn2+转化为了MnO ,锰元素化合价升高,失电子,则电极B
2
为阳极,电极A为阴极,得电子,发生还原反应,A正确;B.由电解示意图可知,电极B上Mn2+失电子
转化为了MnO ,电极反应式为:2HO+Mn2+-2e-=MnO+4H+,B正确;C.电极A为阴极, LiMn O 得电
2 2 2 2 4
子,电极反应式为:2LiMn O+6e-+16H+=2Li++4Mn2++8H O,依据得失电子守恒,电解池总反应为:
2 4 2
2LiMn O+4H+=2Li++Mn2++3MnO+2H O,反应生成了Mn2+,Mn2+浓度增大,C错误;D.电解池总反应为:
2 4 2 2
2LiMn O+4H+=2Li++Mn2++3MnO+2H O,电解结束后,可通过调节溶液pH将锰离子转化为沉淀除去,然
2 4 2 2
后再加入碳酸钠溶液,从而获得碳酸锂,D正确;答案选C。
8.(2021·重庆·统考高考真题)CO 电化学传感器是将环境中CO 浓度转变为电信号的装置,工作原理如
2 2
图所示,其中YSZ是固体电解质,当传感器在一定温度下工作时,在熔融LiCO 和YSZ之间的界面X会
2 3
生成固体LiO。下列说法错误的是
2
A.CO 迁移方向为界面X →电极b
B.电极a上消耗的O 和电极b上产生的CO 的物质的量之比为1:1
2 2
C.电极b为负极,发生的电极反应为2CO -4e-=O ↑+2CO ↑
2 2
D.电池总反应为LiCO=Li O+CO↑
2 3 2 2
【答案】B
【分析】根据图示可知在电极a上O 得到电子变为O2-,所以a电极为负极;在电极b上熔融LiCO 失去
2 2 3
电子变为CO、O,所以金属电极b为正极,然后根据同种电荷相互排斥,一致电荷相互吸引的原则分析
2 2判断。
【解析】A.根据图示可知:电极a上O 得到电子变为O2-,所以a电极为正极;在电极b上熔融LiCO 失
2 2 3
去电子变为CO、O,所以金属电极b为负极。CO 会向负极区移动,故CO 迁移方向为界面X →电极
2 2
b,A正确;B.在电极a上发生反应:O+4e-=2O2-,在电极b上发生反应:2CO -4e-= O ↑+2CO ↑,在同
2 2 2
一闭合回路中电子转移数目相等,可知电极a上消耗的O 和电极b上产生的CO 的物质的量之比为1:2,
2 2
B错误;C.电极b为负极,失去电子发生氧化反应 ,则负极的电极反应为2CO -4e-=O ↑+ 2CO↑,C正
2 2
确;D.负极上熔融的LiCO 失去电子被氧化产生O、CO 气体,反应式为LiCO(熔融)=2Li++ ;
2 3 2 2 2 3
2CO -4e-=O ↑+2CO ↑,正极上发生反应:O+4e-=2O2-,根据在同一闭合回路中电子转移数目相等,将正、
2 2 2
负极电极式叠加,可得总反应方程式为:LiCO=Li O+CO↑,D正确;故合理选项是B。
2 3 2 2
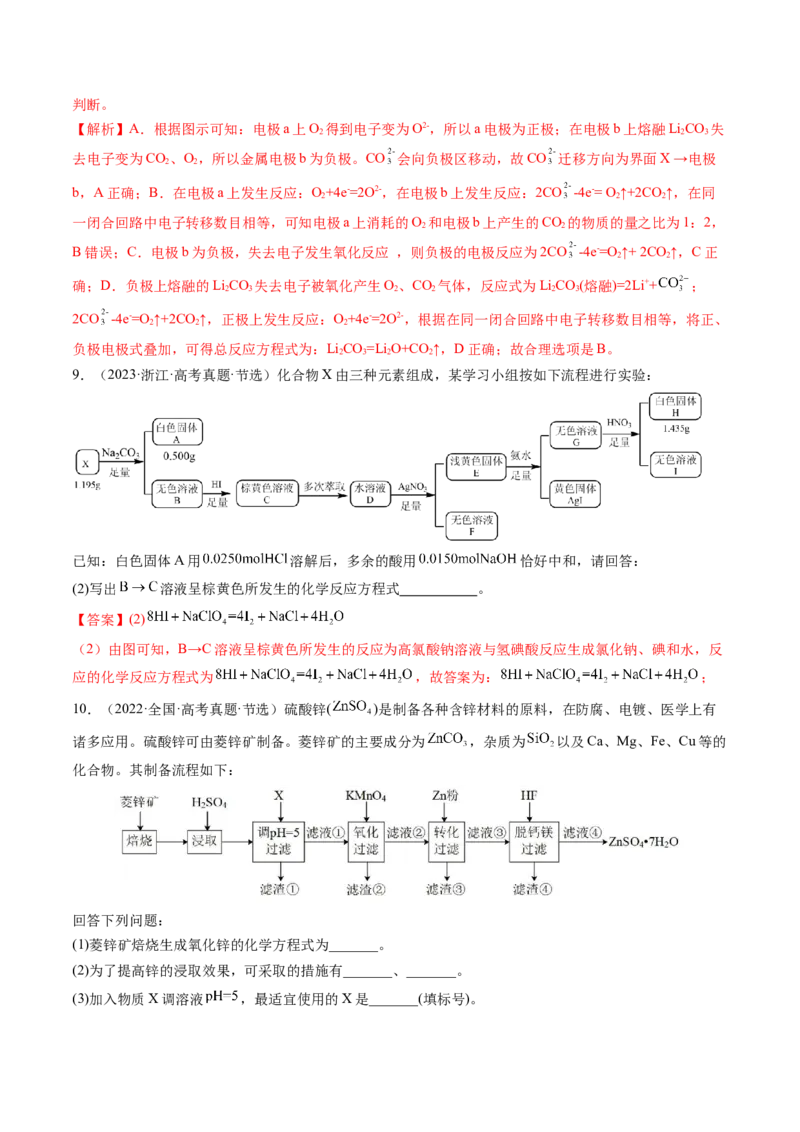
9.(2023·浙江·高考真题·节选)化合物X由三种元素组成,某学习小组按如下流程进行实验:
已知:白色固体A用 溶解后,多余的酸用 恰好中和,请回答:
(2)写出 溶液呈棕黄色所发生的化学反应方程式 。
【答案】(2)
(2)由图可知,B→C溶液呈棕黄色所发生的反应为高氯酸钠溶液与氢碘酸反应生成氯化钠、碘和水,反
应的化学反应方程式为 ,故答案为: ;
10.(2022·全国·高考真题·节选)硫酸锌( )是制备各种含锌材料的原料,在防腐、电镀、医学上有
诸多应用。硫酸锌可由菱锌矿制备。菱锌矿的主要成分为 ,杂质为 以及Ca、Mg、Fe、Cu等的
化合物。其制备流程如下:
回答下列问题:
(1)菱锌矿焙烧生成氧化锌的化学方程式为_______。
(2)为了提高锌的浸取效果,可采取的措施有_______、_______。
(3)加入物质X调溶液 ,最适宜使用的X是_______(填标号)。A. B. C.
滤渣①的主要成分是_______、_______、_______。
(4)向 的滤液①中分批加入适量 溶液充分反应后过滤,滤渣②中有 ,该步反应的离
子方程式为_______。
(5)滤液②中加入锌粉的目的是_______。
(6)滤渣④与浓 反应可以释放HF并循环利用,同时得到的副产物是_______、_______。
【答案】(1)ZnCO ZnO+CO ↑
3 2
(2)3Fe2++ +7H O=3Fe(OH) ↓+MnO↓+5H+
2 3 2
【解析】由题干信息,菱锌矿的主要成分为ZnCO ,杂质为SiO 以及Ca、Mg、Fe、Cu等的化合物,结合
3 2
流程图分析,菱锌矿焙烧,主要发生反应ZnCO ZnO+CO ↑,再加入HSO 酸浸,得到含Zn2+、Ca2+、
3 2 2 4
Mg2+、Fe2+、Fe3+、Cu2+的溶液,加入物质X调节pH=5,结合表格数据,过滤得到Fe(OH) 、CaSO、SiO
3 4 2
的滤渣①,滤液①中主要含有Zn2+、Cu2+、Mg2+、Ca2+、Fe2+,再向滤液①中加入KMnO 溶液氧化Fe2+,过
4
滤得到Fe(OH) 和MnO 的滤渣②,滤液②中加入锌粉,发生反应Zn+Cu2+=Zn2+=Cu,过滤后得到滤渣③为
3 2
Cu,再向滤液③中加入HF脱钙镁,过滤得到滤渣④为CaF 、MgF ,滤液④为ZnSO 溶液,经一系列处理
2 2 4
得到ZnSO·7H O。
4 2
(1)由分析,焙烧时,生成ZnO的反应为:ZnCO ZnO+CO ↑;
3 2
(2)向80~90℃滤液①中加入KMnO 溶液,可氧化Fe2+,得到Fe(OH) 和MnO 的滤渣②,反应的离子方程
4 3 2
式为3Fe2++ +7H O=3Fe(OH) ↓+MnO↓+5H+。
2 3 2