文档内容
专题验收评价
专题 07 物质结构与元素周期律
内容概览
A·常考题不丢分
【考点一 原子结构与性质、元素周期律】
【考点二 考点二 分子结构与性质】
【考点三 晶体结构与性质】
【微专题 晶胞参数、坐标参数的分析与应用】
B·综合素养拿高分/拓展培优拿高分
C·挑战真题争满分
【考点一 原子结构与性质、元素周期律】
1.(2023·上海金山·统考二模)有关磷原子最外层电子的描述正确的是
A.有2种不同运动状态 B.有5种不同能量
C.有4种不同的伸展方向 D.只有1种自旋方向
2.(2023·山东菏泽·统考一模)某元素基态原子4s轨道上有2个电子,则该基态原子价电子排布可能是(
)
A.4s B. C. D.
3.(2023·山东滨州·统考一模)下列叙述正确的是
A.钠的焰色反应是电子由基态转化成激发态时释放能量产生的B.价电子排布为 的元素位于第五周期第ⅠA族,属于s区元素
C.各能层的s电子云轮廓图都是球形,但球的半径大小不同
D.乙醇比甲醚的沸点高是因为乙醇的相对分子质量大
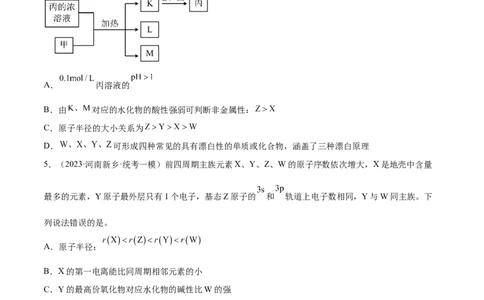
4.(2023·四川成都·石室中学校考一模)短周期主族元素W、X、Y、Z的原子序数依次增加,其中Y和
Z同主族。K、L、M均是由这些元素组成的二元化合物,甲、乙分别是X、Y的单质,甲是常见的固体,
乙是常见的气体,相关物质的转化关系如图所示。下列说法正确的是
A. 丙溶液的
B.由 对应的水化物的酸性强弱可判断非金属性:
C.原子半径的大小关系为
D. 可形成四种常见的具有漂白性的单质或化合物,涵盖了三种漂白原理
5.(2023·河南新乡·统考一模)前四周期主族元素X、Y、Z、W的原子序数依次增大,X是地壳中含量
最多的元素,Y原子最外层只有1个电子,基态Z原子的 和 轨道上电子数相同,Y与W同主族。下
列说法错误的是。
A.原子半径:
B.X的第一电离能比同周期相邻元素的小
C.Y的最高价氧化物对应水化物的碱性比W的强
D.Z单质形成的晶体属于共价晶体
【考点二 分子结构与性质】
1.(2023·海南省直辖县级单位·嘉积中学校联考二模) 是一种重要的化工产品,实验室可
利用 制取该配合物: 。下列叙述正确的是A. 和 均只含极性键
B.1mol 中含24mol配位键
C.该反应中 作还原剂
D. 中H—N—H的键角大于 中H—N—H的键角
2.(2023·浙江绍兴·统考模拟预测)古代陶器釉料中大多含有钴的化合物,下列说法不正确的是
A.CoO的熔点比CoS高
B. 中 中心原子的杂化方式是
C. 中 所含π键和σ键的比例为2:1
D. 中存在配位键、范德华力、非极性键
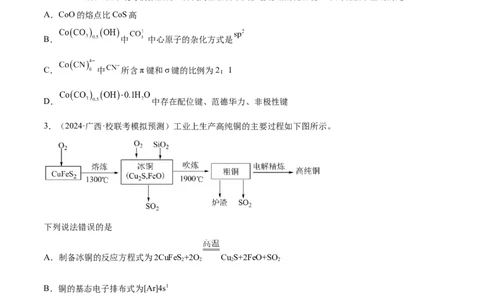
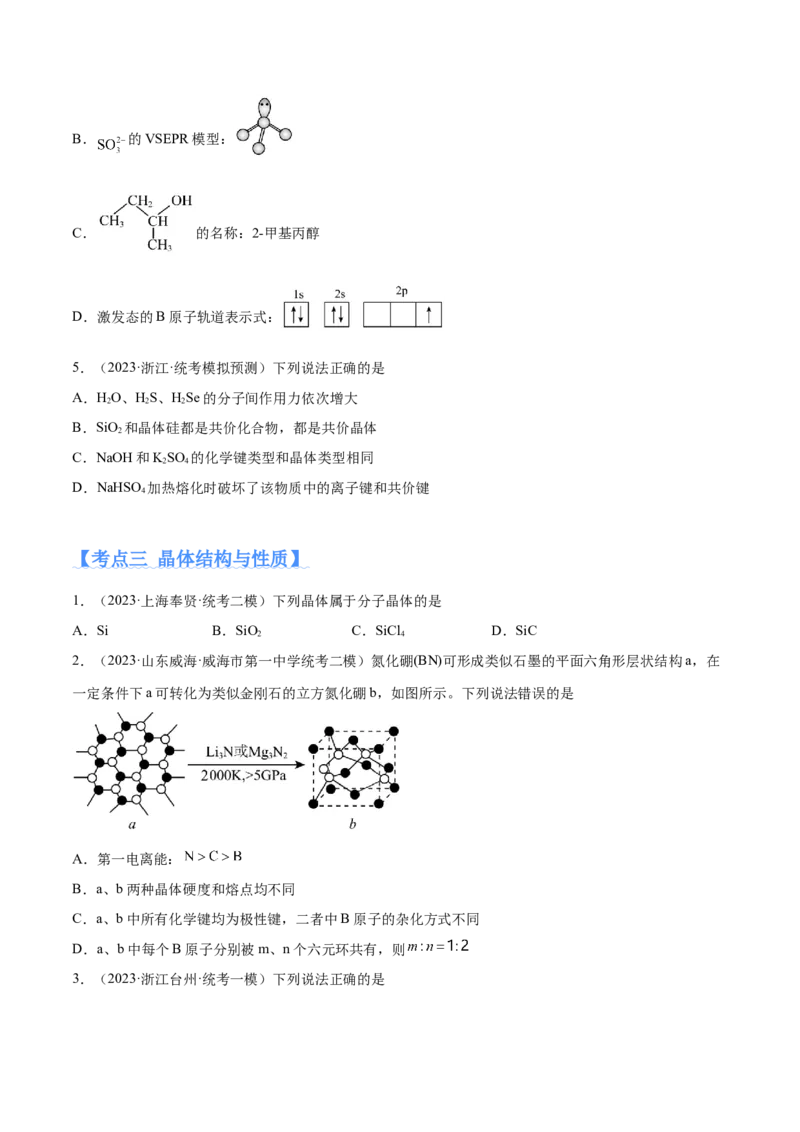
3.(2024·广西·校联考模拟预测)工业上生产高纯铜的主要过程如下图所示。
下列说法错误的是
A.制备冰铜的反应方程式为2CuFeS+2O Cu S+2FeO+SO
2 2 2 2
B.铜的基态电子排布式为[Ar]4s1
C.电解精炼铜阴极电极反应式为
D.生产粗铜过程中产生的SO 的价层电子对互斥模型为平面三角形
2
4.(2023·浙江·校联考一模)下列化学用语或表述正确的是
A.SiO 的结构式:O=Si=O
2B. 的VSEPR模型:
C. 的名称:2-甲基丙醇
D.激发态的B原子轨道表示式:
5.(2023·浙江·统考模拟预测)下列说法正确的是
A.HO、HS、HSe的分子间作用力依次增大
2 2 2
B.SiO 和晶体硅都是共价化合物,都是共价晶体
2
C.NaOH和KSO 的化学键类型和晶体类型相同
2 4
D.NaHSO 加热熔化时破坏了该物质中的离子键和共价键
4
【考点三 晶体结构与性质】
1.(2023·上海奉贤·统考二模)下列晶体属于分子晶体的是
A.Si B.SiO C.SiCl D.SiC
2 4
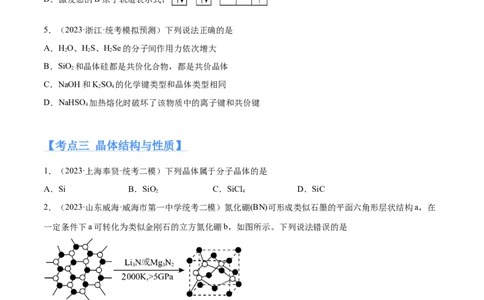
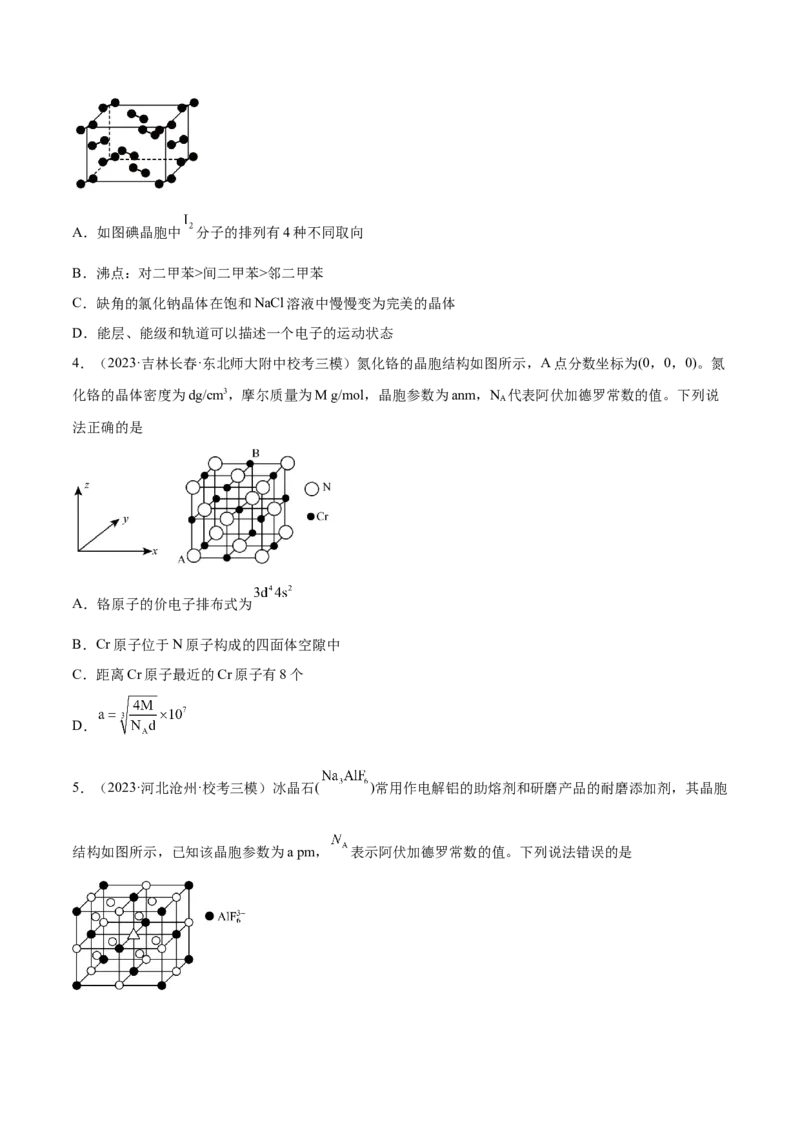
2.(2023·山东威海·威海市第一中学统考二模)氮化硼(BN)可形成类似石墨的平面六角形层状结构a,在
一定条件下a可转化为类似金刚石的立方氮化硼b,如图所示。下列说法错误的是
A.第一电离能:
B.a、b两种晶体硬度和熔点均不同
C.a、b中所有化学键均为极性键,二者中B原子的杂化方式不同
D.a、b中每个B原子分别被m、n个六元环共有,则
3.(2023·浙江台州·统考一模)下列说法正确的是A.如图碘晶胞中 分子的排列有4种不同取向
B.沸点:对二甲苯>间二甲苯>邻二甲苯
C.缺角的氯化钠晶体在饱和NaCl溶液中慢慢变为完美的晶体
D.能层、能级和轨道可以描述一个电子的运动状态
4.(2023·吉林长春·东北师大附中校考三模)氮化铬的晶胞结构如图所示,A点分数坐标为(0,0,0)。氮
化铬的晶体密度为dg/cm3,摩尔质量为M g/mol,晶胞参数为anm,N 代表阿伏加德罗常数的值。下列说
A
法正确的是
A.铬原子的价电子排布式为
B.Cr原子位于N原子构成的四面体空隙中
C.距离Cr原子最近的Cr原子有8个
D.
5.(2023·河北沧州·校考三模)冰晶石( )常用作电解铝的助熔剂和研磨产品的耐磨添加剂,其晶胞
结构如图所示,已知该晶胞参数为a pm, 表示阿伏加德罗常数的值。下列说法错误的是A. 中Al的配位数为6
B.图中△位置填充的是Na
C.晶胞中 形成的全部四面体空隙和 的比值为1∶1
D.该晶体的密度为 gcm-3
⋅
【微专题 晶胞参数、坐标参数的分析与应用】
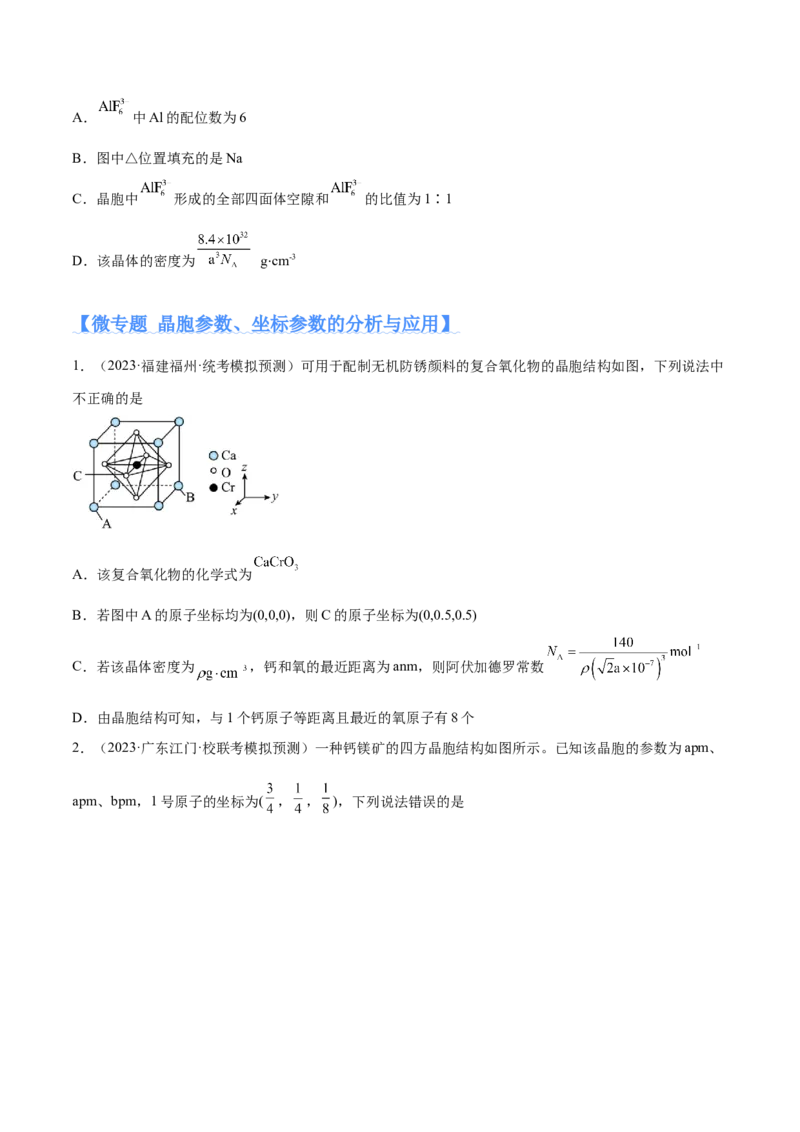
1.(2023·福建福州·统考模拟预测)可用于配制无机防锈颜料的复合氧化物的晶胞结构如图,下列说法中
不正确的是
A.该复合氧化物的化学式为
B.若图中A的原子坐标均为(0,0,0),则C的原子坐标为(0,0.5,0.5)
C.若该晶体密度为 ,钙和氧的最近距离为anm,则阿伏加德罗常数
D.由晶胞结构可知,与1个钙原子等距离且最近的氧原子有8个
2.(2023·广东江门·校联考模拟预测)一种钙镁矿的四方晶胞结构如图所示。已知该晶胞的参数为apm、
apm、bpm,1号原子的坐标为( , , ),下列说法错误的是A.2号原子的坐标为( , , )
B.距离硫原子最近的硫原子数目为4
C.硫原子的配位数为4
D.该晶体的密度为 g/cm3
3.(2023·辽宁·校联考二模)LiO具有反萤石结构,其立方晶胞结构如图所示(晶胞的边长为apm)下列说
2
法错误的是
A.字母B表示氧离子,配位数是8
B.若晶胞中M的坐标为(0,0,0),则P的坐标为( , , )
C.A处于B围成的正八面体空隙中
D.晶胞中A与B的最短距离为 cm
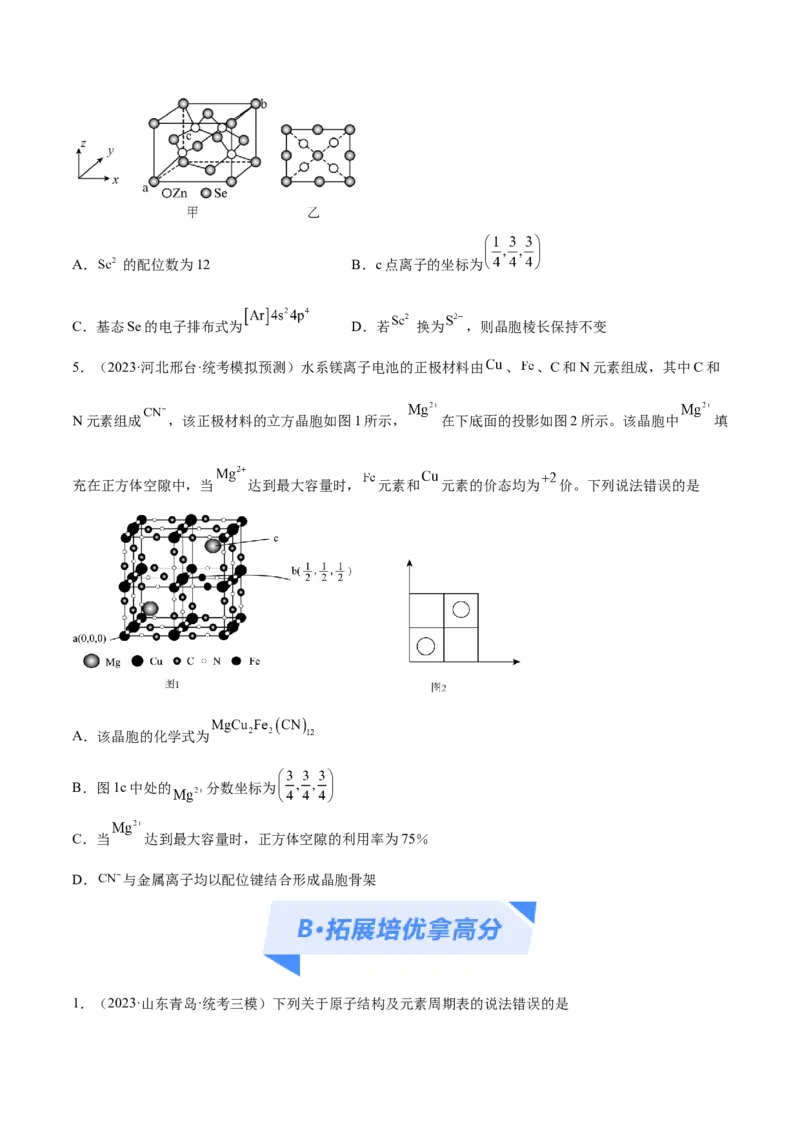
4.(2023下·湖北武汉·高三统考阶段练习)硒化锌是一种重要的半导体材料,图甲为其晶胞结构,图乙为
晶胞的俯视图。已知a点的坐标 ,b点的坐标 。下列说法正确的是A. 的配位数为12 B.c点离子的坐标为
C.基态Se的电子排布式为 D.若 换为 ,则晶胞棱长保持不变
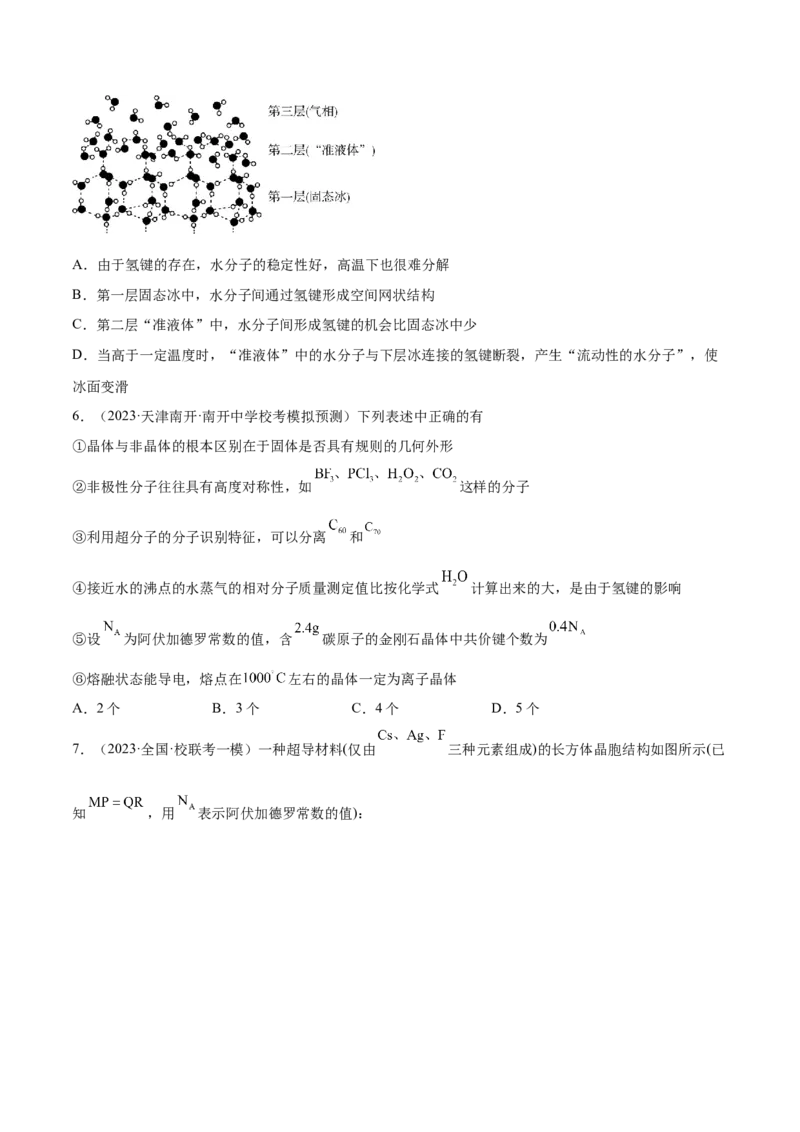
5.(2023·河北邢台·统考模拟预测)水系镁离子电池的正极材料由 、 、C和N元素组成,其中C和
N元素组成 ,该正极材料的立方晶胞如图1所示, 在下底面的投影如图2所示。该晶胞中 填
充在正方体空隙中,当 达到最大容量时, 元素和 元素的价态均为 价。下列说法错误的是
A.该晶胞的化学式为
B.图1c中处的 分数坐标为
C.当 达到最大容量时,正方体空隙的利用率为75%
D. 与金属离子均以配位键结合形成晶胞骨架
1.(2023·山东青岛·统考三模)下列关于原子结构及元素周期表的说法错误的是A.位于同一轨道内电子的运动状态也不相同
B.位于 d 区和 ds 区的元素都是金属元素
C.前四周期未成对电子数最多的元素位于ⅥB 族
D.基态原子最外层电子排布为ns1 的元素均在ⅠA 族或ⅠB 族
2.(2023·四川资阳·统考一模)W、X、Y、Z、Q是核电荷数依次增大的五种短周期元素。 的半径在
所有离子中最小,X、Y、Z同周期且相邻,Z、Q位于同一主族且Z的核电荷数是Q的一半。下列说法正
确的是
A.Z、Q元素的最高正价相同
B.W、X、Y、Z四种元素不能形成离子化合物
C.X、Q的最高价氧化物对应水化物的酸性:
D.X、Y、Z分别与W形成的简单化合物的沸点:
3.(2023·陕西渭南·统考模拟预测)短周期主族元素X、Y、Z、W的原子序数依次增大,W、X同主族,
Y、Z可形成阴离子 ,X、W可形成阴离子 。下列说法正确的是
A.非金属性: B.X、W具有相同的最高正价
C.原子半径: D.X、Z不可能形成化合物
4.(2023下·辽宁·高三校联考开学考试)2017年南京理工大学合成出下图的离子化合物,该物质由两种
阳离子和两种阴离子构成,其中有两种10电子离子和一种18电子离子。X、Y、Z、M均为短周期元素,
且均不在同一族。下列说法不正确的是
A.X与Y形成的化合物沸点高于Y同族元素与X形成的化合物
B.MY 均不含有非极性共价键
2
C.Y氢化物的稳定性一定比Z的强
D.在该盐中,存在极性共价键和非极性共价键
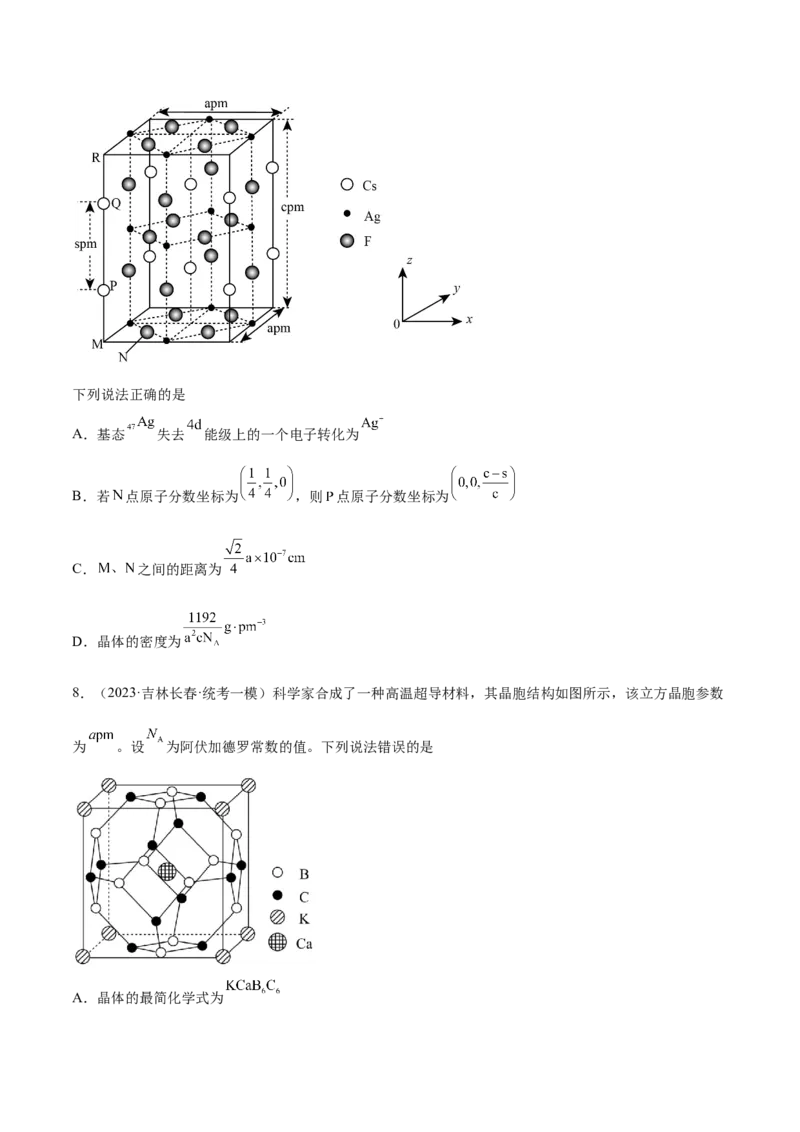
5.(2023·山东威海·统考二模)“冰面为什么滑?”,这与冰层表面的结构有关(如图)。下列有关说法错
误的是A.由于氢键的存在,水分子的稳定性好,高温下也很难分解
B.第一层固态冰中,水分子间通过氢键形成空间网状结构
C.第二层“准液体”中,水分子间形成氢键的机会比固态冰中少
D.当高于一定温度时,“准液体”中的水分子与下层冰连接的氢键断裂,产生“流动性的水分子”,使
冰面变滑
6.(2023·天津南开·南开中学校考模拟预测)下列表述中正确的有
①晶体与非晶体的根本区别在于固体是否具有规则的几何外形
②非极性分子往往具有高度对称性,如 这样的分子
③利用超分子的分子识别特征,可以分离 和
④接近水的沸点的水蒸气的相对分子质量测定值比按化学式 计算出来的大,是由于氢键的影响
⑤设 为阿伏加德罗常数的值,含 碳原子的金刚石晶体中共价键个数为
⑥熔融状态能导电,熔点在 左右的晶体一定为离子晶体
A.2个 B.3个 C.4个 D.5个
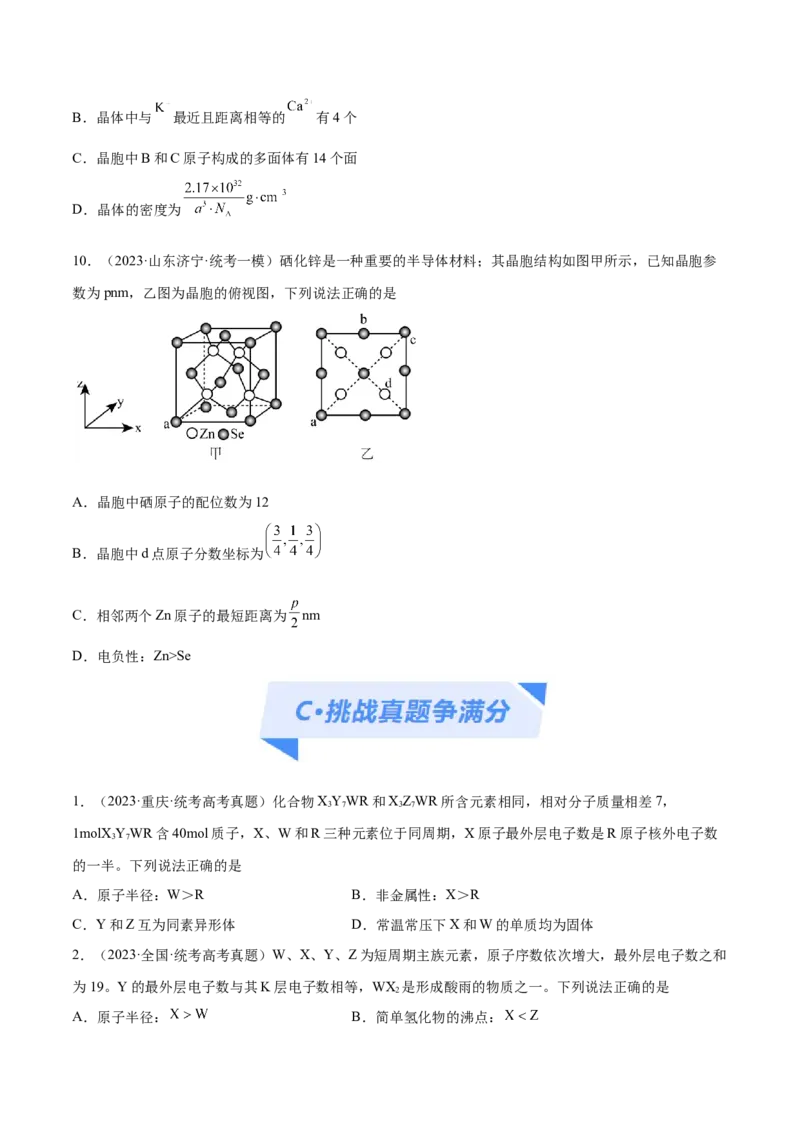
7.(2023·全国·校联考一模)一种超导材料(仅由 三种元素组成)的长方体晶胞结构如图所示(已
知 ,用 表示阿伏加德罗常数的值):下列说法正确的是
A.基态 失去 能级上的一个电子转化为
B.若 点原子分数坐标为 ,则 点原子分数坐标为
C. 之间的距离为
D.晶体的密度为
8.(2023·吉林长春·统考一模)科学家合成了一种高温超导材料,其晶胞结构如图所示,该立方晶胞参数
为 。设 为阿伏加德罗常数的值。下列说法错误的是
A.晶体的最简化学式为B.晶体中与 最近且距离相等的 有4个
C.晶胞中B和C原子构成的多面体有14个面
D.晶体的密度为
10.(2023·山东济宁·统考一模)硒化锌是一种重要的半导体材料;其晶胞结构如图甲所示,已知晶胞参
数为pnm,乙图为晶胞的俯视图,下列说法正确的是
A.晶胞中硒原子的配位数为12
B.晶胞中d点原子分数坐标为
C.相邻两个Zn原子的最短距离为 nm
D.电负性:Zn>Se
1.(2023·重庆·统考高考真题)化合物XYWR和XZWR所含元素相同,相对分子质量相差7,
3 7 3 7
1molX YWR含40mol质子,X、W和R三种元素位于同周期,X原子最外层电子数是R原子核外电子数
3 7
的一半。下列说法正确的是
A.原子半径:W>R B.非金属性:X>R
C.Y和Z互为同素异形体 D.常温常压下X和W的单质均为固体
2.(2023·全国·统考高考真题)W、X、Y、Z为短周期主族元素,原子序数依次增大,最外层电子数之和
为19。Y的最外层电子数与其K层电子数相等,WX 是形成酸雨的物质之一。下列说法正确的是
2
A.原子半径: B.简单氢化物的沸点:C. 与 可形成离子化合物 D. 的最高价含氧酸是弱酸
3.(2022·湖南·高考真题)科学家合成了一种新的共价化合物(结构如图所示),X、Y、Z、W为原子序数
依次增大的短周期元素,W的原子序数等于X与Y的原子序数之和。下列说法错误的是
A.原子半径: B.非金属性:
C.Z的单质具有较强的还原性 D.原子序数为82的元素与W位于同一主族
4.(2022·广东·高考真题)甲~戊均为短周期元素,在元素周期表中的相对位置如图所示。戊的最高价氧
化物对应的水化物为强酸。下列说法不正确的是
甲 乙
丙 丁 戊
A.原子半径:丁>戊>乙
B.非金属性:戊>丁>丙
C.甲的氢化物遇氯化氢一定有白烟产生
D.丙的最高价氧化物对应的水化物一定能与强碱反应
5.(2021·重庆·统考高考真题)元素X、Y和Z可形成化合物XYZ, X的原子序数是Z的原子序数的5
3 3 6
倍,1 mol X YZ 含42mol质子,下列叙述正确的是
3 3 6
A.X位于周期表的第二周期第VA族
B.Y的原子半径大于X的原子半径
C.Y的氧化物为无色气体
D.Z的单质与Cl 反应可生成共价化合物
2
6.(2023·辽宁·统考高考真题)下列化学用语或表述正确的是
A.BeCl 的空间结构:V形 B.P 中的共价键类型:非极性键
2 4
C.基态Ni原子价电子排布式:3d10 D.顺—2—丁烯的结构简式:
7.(2022·天津·统考高考真题)利用反应 可制备NH。下列叙述正确
2 4
的是A.NH 分子有孤电子对,可做配体
3
B.NaCl晶体可以导电
C.一个NH 分子中有4个σ键
2 4
D.NaClO和NaCl均为离子化合物,他们所含的化学键类型相同
8.(2022·北京·高考真题)已知: 。下列说法不正确的是
A. 分子的共价键是 键, 分子的共价键是 键
B.燃烧生成的 气体与空气中的水蒸气结合呈雾状
C.停止反应后,用蘸有浓氨水的玻璃棒靠近集气瓶口产生白烟
D.可通过原电池将 与 反应的化学能转化为电能
9.(2023·辽宁·统考高考真题)下列化学用语或表述正确的是
A.BeCl 的空间结构:V形 B.P 中的共价键类型:非极性键
2 4
C.基态Ni原子价电子排布式:3d10 D.顺—2—丁烯的结构简式:
10.(2022·天津·统考高考真题)一定条件下,石墨转化为金刚石吸收能量。下列关于石墨和金刚石的说
法正确的是
A.金刚石比石墨稳定
B.两物质的碳碳 键的键角相同
C.等质量的石墨和金刚石中,碳碳 键数目之比为4∶3
D.可以用X射线衍射仪鉴别金刚石和石墨