文档内容
专题 08 水溶液中的离子平衡
一、单选题
1.化学与生活密切相关,下列生活常识不能用对应的化学知识解释的是
选项 生活常识 化学知识
A 餐后要将洗浄的铁锅擦干 减缓铁的锈蚀
B 护肤品中添加丙三醇 丙三醇有吸水性
C 煮沸豆浆 主要将蛋白质转换为氨基酸
D 用热的纯碱溶液清洗油污 油脂在热的纯碱溶液中更易发生水解
A.A B.B C.C D.D
2.下列属于弱电解质的是
A.CHCOOH B.NaOH C.NaCl D.CHCHOH
3 3 2
3.下列物质的水溶液因水解呈酸性的是
A.NaCl B. C.HCOONa D.
4.下列物质的水溶液因水解而呈碱性的是
A.KCl B.AlCl C.CHCOONa D.Ba(OH)
3 3 2
5.纯净的氯化钠是不潮解的,但粗盐很容易潮解,这主要是因为其中含有杂质MgCl 的缘故。为得到纯
2
净的氯化钠,有人设计了一个实验:把买来的粗盐放入纯氯化钠饱和溶液一段时间,过滤,洗涤,可得纯
净的氯化钠晶体。则下列说法正确的是
A.设计实验的根据是NaCl的溶解平衡
B.设计实验的根据是MgCl 比NaCl易溶于水
2
C.在整个过程中NaCl饱和溶液浓度会变大(温度不变)
D.粗盐的晶粒大一些有利于提纯
6.某品牌牙膏的成分含水、丙三醇、二氧化硅、苯甲酸钠、十二烷基硫酸钠和氟化钠等。已知:牙釉质
中含有羟基磷酸钙 ,是牙齿的保护层。在牙齿表面存在平衡:下列说法不正确的是
A.若使牙膏呈弱酸性,更有利于保护牙釉质
B.丙三醇的俗称是甘油
C. 是摩擦剂,有助于去除牙齿表面的污垢
D.NaF能将 转化为更难溶的 ,减少龋齿的发生
7.下列物质溶于水后,溶液中仅含一种分子的是
A. B. C. D.
8.下列因素能影响水的电离平衡,且能使水的电离平衡向右移动的是
A.CHCOOH B. C.升高温度 D.X-
3 b
9.实验室用标准盐酸溶液测定某NaOH溶液的浓度,用酚酞作指示剂,下列操作中可能使测定结果偏高
的是
A.盛NaOH溶液的锥形瓶用蒸馏水清洗后没有再用NaOH溶液润洗
B.锥形瓶内溶液颜色变化由粉红色刚好变成无色,立即记下滴定管液面所在刻度
C.开始实验时酸式滴定管尖嘴部分有气泡,在滴定过程中气泡消失
D.滴定前仰视读数,滴定后俯视读数
10.下列说法中,正确的是
A.强电解质溶液的导电能力一定比弱电解质强
B.冰醋酸是弱电解质,但液态时不能导电
C.盐酸中加入固体NaCl,因Cl-浓度增大,所以溶液酸性减弱
D.硫酸钠是强电解质,硫酸钡是弱电解质
11.常温下,CHCOOH、HCOOH(甲酸)的电离常数数值分别为1.7×10-5、1.8×10-4,以下关于0.1mol/
3
LCH COOH溶液、0.1mol/LHCOOH溶液的说法正确的是
3
A.c(H+):CHCOOH>HCOOH
3
2B.等体积的两溶液中,分别加入过量的镁,产生氢气的体积:HCOOH>CHCOOH
3
C.HCOOH可能与NaOH发生反应:H++OH-=H O
2
D.将CHCOOH溶液稀释100倍过程中, 保持不变
3
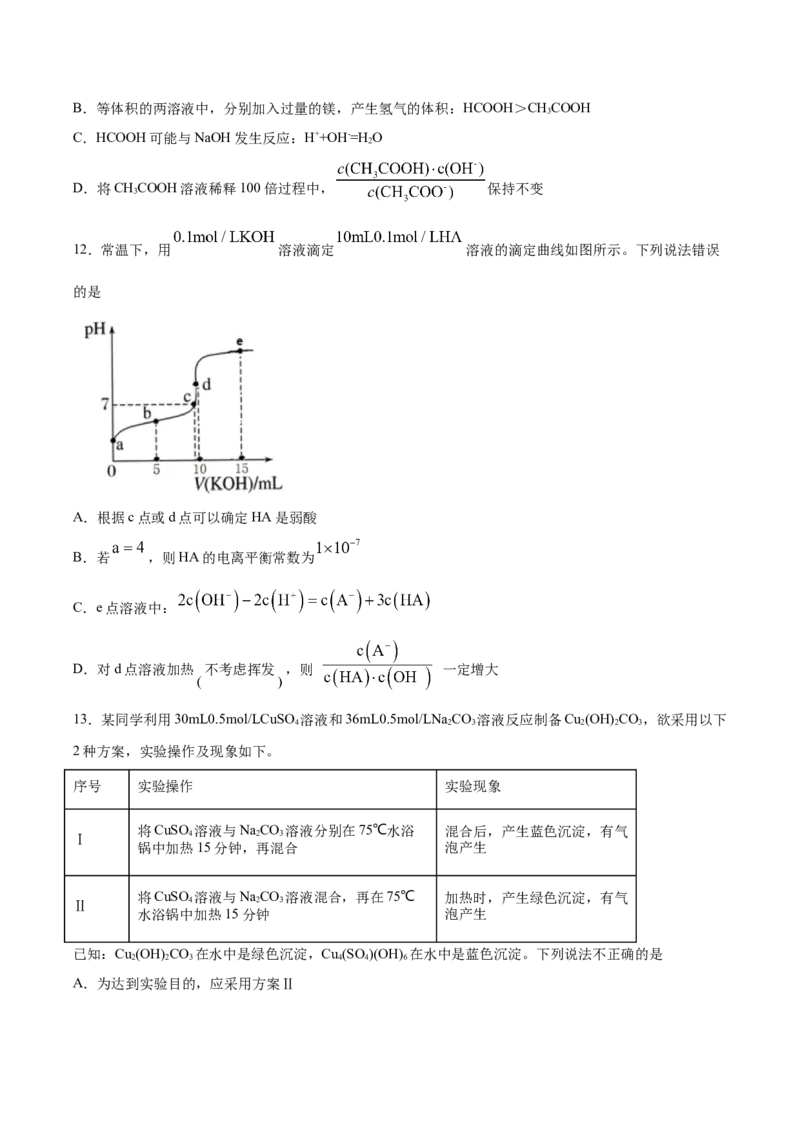
12.常温下,用 溶液滴定 溶液的滴定曲线如图所示。下列说法错误
的是
A.根据c点或d点可以确定HA是弱酸
B.若 ,则HA的电离平衡常数为
C.e点溶液中:
D.对d点溶液加热 不考虑挥发 ,则 一定增大
13.某同学利用30mL0.5mol/LCuSO 溶液和36mL0.5mol/LNa CO 溶液反应制备Cu (OH) CO,欲采用以下
4 2 3 2 2 3
2种方案,实验操作及现象如下。
序号 实验操作 实验现象
将CuSO 溶液与NaCO 溶液分别在75℃水浴 混合后,产生蓝色沉淀,有气
Ⅰ 4 2 3
锅中加热15分钟,再混合 泡产生
将CuSO 溶液与NaCO 溶液混合,再在75℃ 加热时,产生绿色沉淀,有气
Ⅱ 4 2 3
水浴锅中加热15分钟 泡产生
已知:Cu (OH) CO 在水中是绿色沉淀,Cu (SO )(OH) 在水中是蓝色沉淀。下列说法不正确的是
2 2 3 4 4 6
A.为达到实验目的,应采用方案ⅡB.方案I中,混合前存在平衡:Cu2++2H O Cu(OH) +2H+
2 2
C.制备原理是:2Cu2++2CO +H O Cu (OH) CO↓+CO ↑
2 2 2 3 2
D.对比Ⅰ、Ⅱ可知,II中CO 水解程度较大
14.由于血液中存在如下平衡过程: 、 、
,使血液的pH维持在7.35~7.45.如超出这个范围会造成酸中毒(pH过
低)或碱中毒(pH过高),急性中毒时需静脉注射 或 进行治疗。下列叙述正确的是
A.血液中 浓度过高会导致酸中毒,使血液中 的值增大
B.治疗碱中毒时,患者需降低呼吸频率,以增加血液中 浓度
C.急性酸中毒时,救治方式是静脉注射 溶液
D.酸或碱中毒时,会导致血液中的酶发生水解
15.25℃时,下列说法不正确的是
A.0.010mol/L 溶液的 ,可推知HCN为弱酸
B.0.10mol/L 溶液中, 是 的三倍
C.纯水中加入少量 固体,水的电离度增大
D.氨水的pH不一定比NaOH溶液的pH小
16.下列说法正确的是
A.在相同温度下,物质的量浓度相等的氨水、 溶液, 相等
B.中和 和体积均相等的盐酸、 溶液,所需 的物质的量相同
C.室温下 的 溶液和 的 溶液中,
4D.浓度和体积都相等的盐酸和醋酸溶液分别与足量的 完全反应,盐酸产生的 多
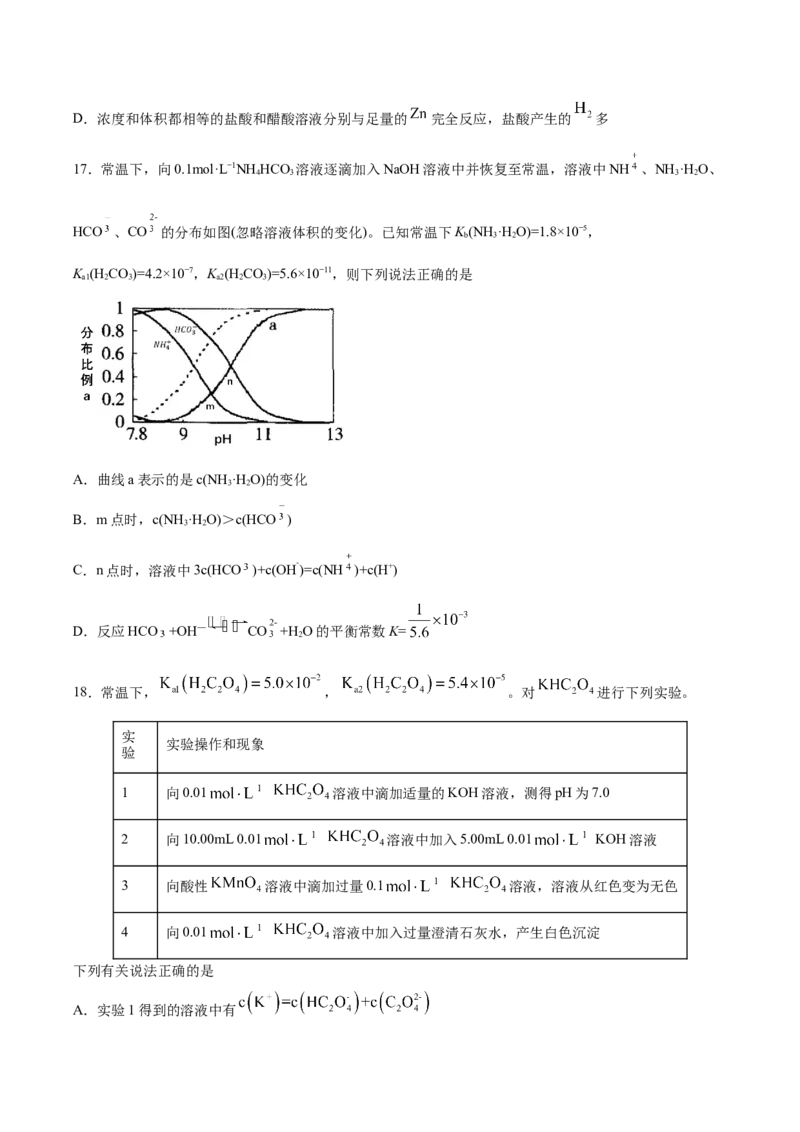
17.常温下,向0.1mol·L−1NH HCO 溶液逐滴加入NaOH溶液中并恢复至常温,溶液中NH 、NH ·H O、
4 3 3 2
HCO 、CO 的分布如图(忽略溶液体积的变化)。已知常温下K (NH ·H O)=1.8×10−5,
b 3 2
K (H CO)=4.2×10−7,K (H CO)=5.6×10−11,则下列说法正确的是
a1 2 3 a2 2 3
A.曲线a表示的是c(NH ·H O)的变化
3 2
B.m点时,c(NH ·H O)>c(HCO )
3 2
C.n点时,溶液中3c(HCO )+c(OH⁻)=c(NH )+c(H+)
D.反应HCO +OH— CO +H O的平衡常数K=
2
18.常温下, , 。对 进行下列实验。
实
实验操作和现象
验
1 向0.01 溶液中滴加适量的KOH溶液,测得pH为7.0
2 向10.00mL 0.01 溶液中加入5.00mL 0.01 KOH溶液
3 向酸性 溶液中滴加过量0.1 溶液,溶液从红色变为无色
4 向0.01 溶液中加入过量澄清石灰水,产生白色沉淀
下列有关说法正确的是
A.实验1得到的溶液中有B.实验2得到的溶液中有
C.实验3中反应的离子方程式为
D.实验4反应后静置的上层清液中有
19.25℃时,将SO 通入蒸馏水中模拟酸雨形成过程,实验数据如图。已知HSO 的K =10-2,K =10-7。
2 2 3 a1 a2
下列说法不正确的是
A.在50s~300s时间段,pH下降的原因是二氧化硫与水反应生成了亚硫酸
B.在300s未通O 时,溶液中c(HSO )=10-5.46mol•L-1
2 2 3
C.在400s时,溶液中c(HSO )+c(SO )+ c(SO )+c(H SO )≈10-6.75 mol•L-1
2 3
D.在600s时,溶液中c(H+)约为c(SO )的2倍
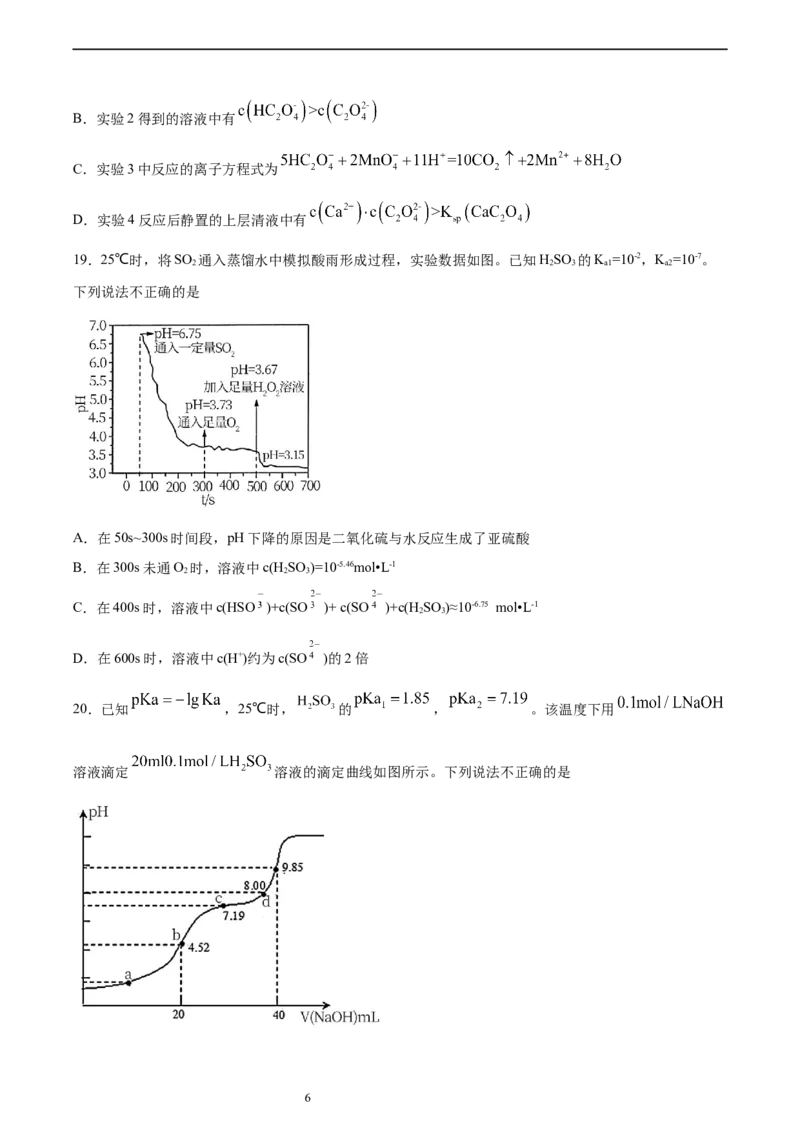
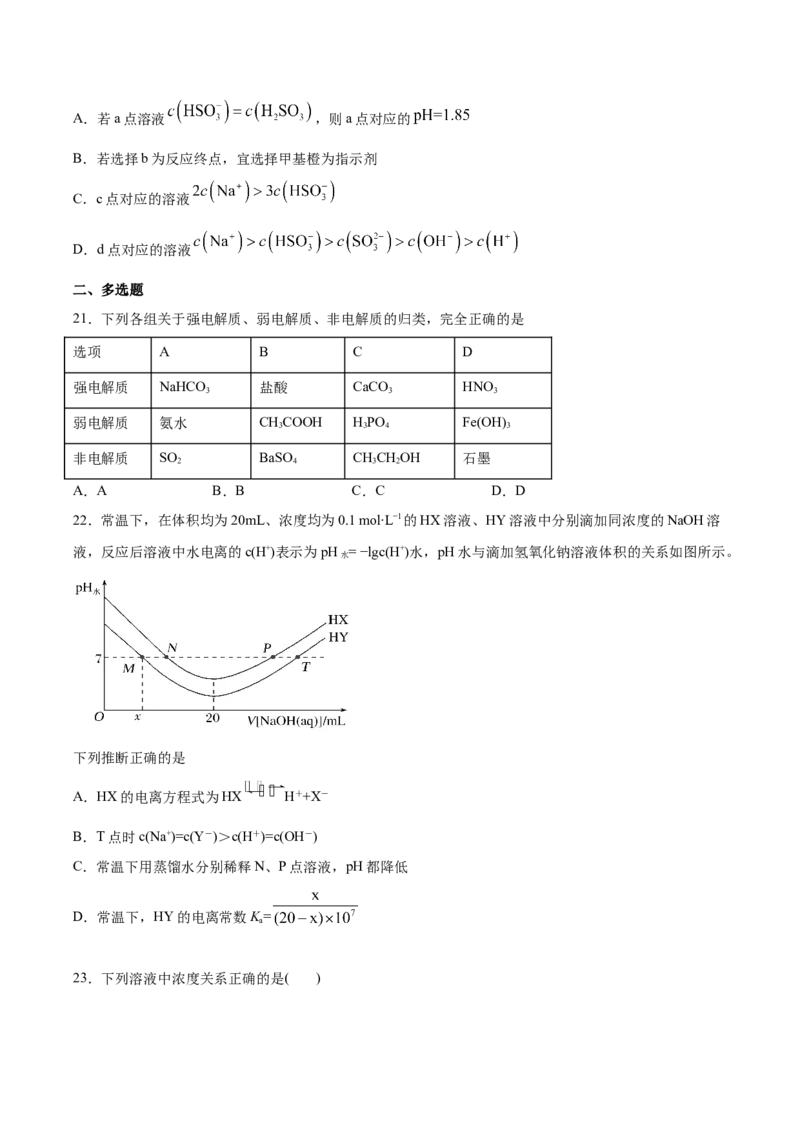
20.已知 ,25℃时, 的 , 。该温度下用
溶液滴定 溶液的滴定曲线如图所示。下列说法不正确的是
6A.若a点溶液 ,则a点对应的
B.若选择b为反应终点,宜选择甲基橙为指示剂
C.c点对应的溶液
D.d点对应的溶液
二、多选题
21.下列各组关于强电解质、弱电解质、非电解质的归类,完全正确的是
选项 A B C D
强电解质 NaHCO 盐酸 CaCO HNO
3 3 3
弱电解质 氨水 CHCOOH HPO Fe(OH)
3 3 4 3
非电解质 SO BaSO CHCHOH 石墨
2 4 3 2
A.A B.B C.C D.D
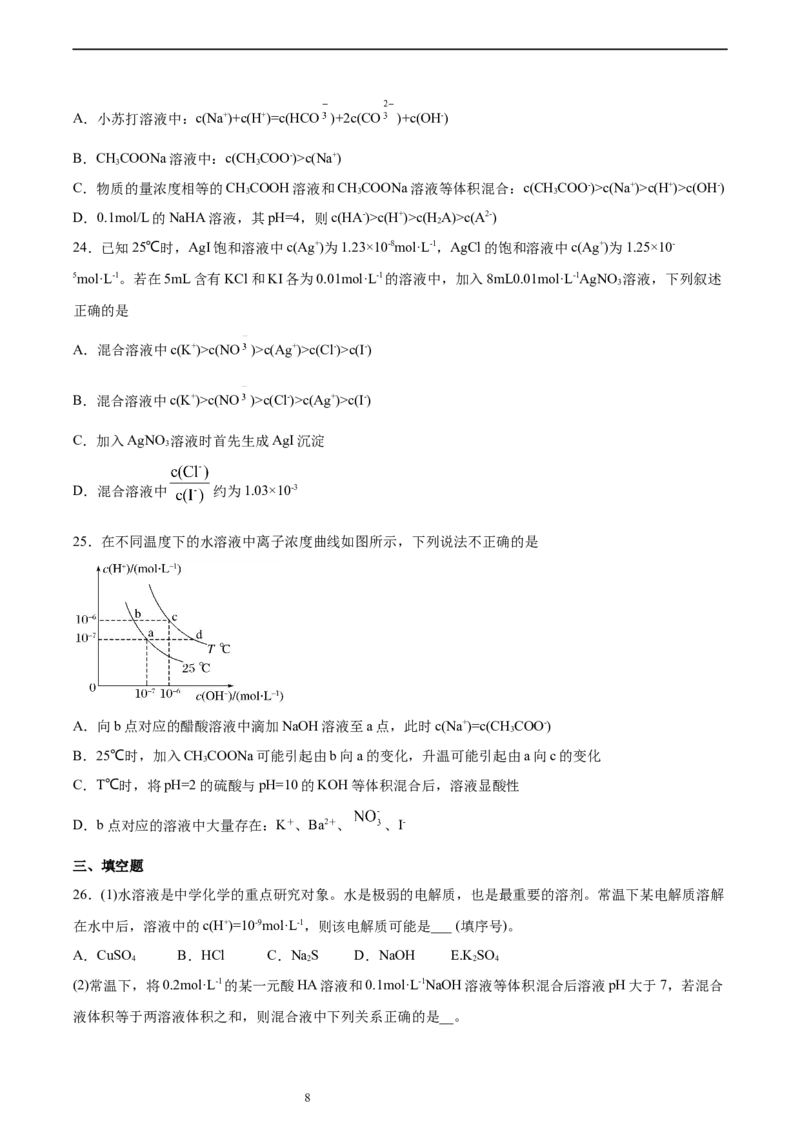
22.常温下,在体积均为20mL、浓度均为0.1 mol∙L−1的HX溶液、HY溶液中分别滴加同浓度的NaOH溶
液,反应后溶液中水电离的c(H+)表示为pH = −lgc(H+)水,pH水与滴加氢氧化钠溶液体积的关系如图所示。
水
下列推断正确的是
A.HX的电离方程式为HX H++X-
B.T点时c(Na+)=c(Y-)>c(H+)=c(OH-)
C.常温下用蒸馏水分别稀释N、P点溶液,pH都降低
D.常温下,HY的电离常数K=
a
23.下列溶液中浓度关系正确的是( )A.小苏打溶液中:c(Na+)+c(H+)=c(HCO )+2c(CO )+c(OH-)
B.CHCOONa溶液中:c(CHCOO-)>c(Na+)
3 3
C.物质的量浓度相等的CHCOOH溶液和CHCOONa溶液等体积混合:c(CHCOO-)>c(Na+)>c(H+)>c(OH-)
3 3 3
D.0.1mol/L的NaHA溶液,其pH=4,则c(HA-)>c(H+)>c(H A)>c(A2-)
2
24.已知25℃时,AgI饱和溶液中c(Ag+)为1.23×10-8mol·L-1,AgCl的饱和溶液中c(Ag+)为1.25×10-
5mol·L-1。若在5mL含有KCl和KI各为0.01mol·L-1的溶液中,加入8mL0.01mol·L-1AgNO 溶液,下列叙述
3
正确的是
A.混合溶液中c(K+)>c(NO )>c(Ag+)>c(Cl-)>c(I-)
B.混合溶液中c(K+)>c(NO )>c(Cl-)>c(Ag+)>c(I-)
C.加入AgNO 溶液时首先生成AgI沉淀
3
D.混合溶液中 约为1.03×10-3
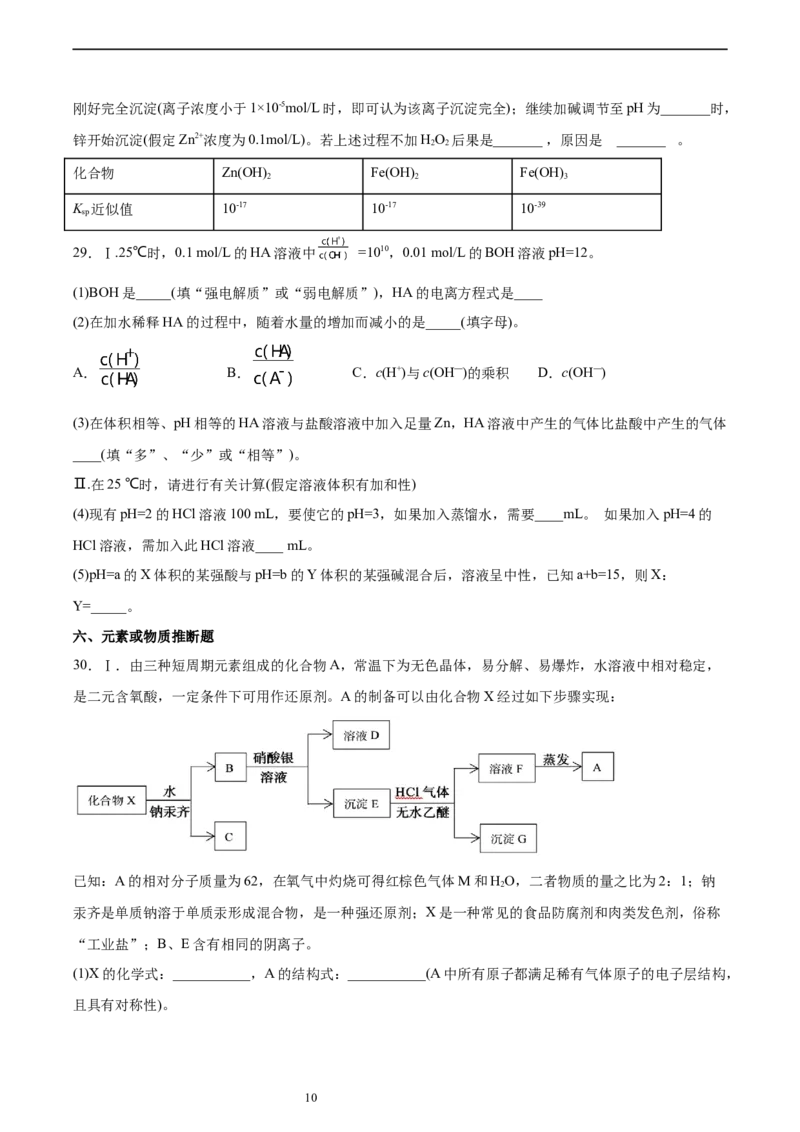
25.在不同温度下的水溶液中离子浓度曲线如图所示,下列说法不正确的是
A.向b点对应的醋酸溶液中滴加NaOH溶液至a点,此时c(Na+)=c(CH COO-)
3
B.25℃时,加入CHCOONa可能引起由b向a的变化,升温可能引起由a向c的变化
3
C.T℃时,将pH=2的硫酸与pH=10的KOH等体积混合后,溶液显酸性
D.b点对应的溶液中大量存在:K+、Ba2+、 、I-
三、填空题
26.(1)水溶液是中学化学的重点研究对象。水是极弱的电解质,也是最重要的溶剂。常温下某电解质溶解
在水中后,溶液中的c(H+)=10-9mol·L-1,则该电解质可能是___ (填序号)。
A.CuSO B.HCl C.NaS D.NaOH E.K SO
4 2 2 4
(2)常温下,将0.2mol·L-1的某一元酸HA溶液和0.1mol·L-1NaOH溶液等体积混合后溶液pH大于7,若混合
液体积等于两溶液体积之和,则混合液中下列关系正确的是__。
8A.c(HA)c( )>c( )>c(OH-)>c(H+),D错误;
故选D。
21.C
【详解】
A.氨水是混合物,既不是电解质也不是非电解质,故A错误;
B.盐酸为混合物,既不是电解质也不是非电解质,BaSO 是盐,属于强电解质,故B错误;
4
C.CaCO 是强电解质,HPO 是弱电解质,CHCHOH属于非电解质,故C正确;
3 3 4 3 2
D.HNO 是强电解质,Fe(OH) 是弱碱,部分电离属于弱电解质,石墨是单质,既不是电解质也不是非电
3 3
解质,故D错误;
故选C。
22.AD
【分析】向HX溶液、HY溶液中分别滴加同浓度的NaOH溶液,酸性不断减弱,水电离出的氢离子浓度增大,pH
不断减小,当pH 减小到pH =7时,溶液呈中性,再继续滴加NaOH溶液至反应完全,水电离程度最大,
水 水 水
继续滴加NaOH溶液,水电离程度减小,减小不断增强。
【详解】
A.根据图中信息,加入20mLNaOH溶液时,溶液中溶质为NaX,其pH <7,说明促进了水的电离,即
水
HX为弱酸,因此HX的电离方程式为HX H++X-,故A正确;
B.加入20mLNaOH溶液的点为碱性,而T点在碱性NaY基础上还加入了NaOH溶液,说明T点溶液显碱
性,因此T点时c(Na+)>c(Y-)>c(OH-)>c(H+),故B错误;
C.根据图中信息N点呈中性,因此常温下用蒸馏水稀释N点,pH值不变,P点溶液呈碱性,常温下用蒸
馏水稀释P点,碱性减弱,pH值降低,故C错误;
D.常温下,加入xmLNaOH溶液时,HY的电离常数 ,故D正
确。
综上所述,答案为AD。
23.AC
【详解】
A.小苏打溶液中满足电荷守恒:c(Na+)+c(H+)=c(HCO )+2c(CO )+c(OH-),A正确;
B.CHCOONa溶液中醋酸根水解:c(CHCOO-)<c(Na+),B错误;
3 3
C.物质的量浓度相等的CHCOOH溶液和CHCOONa溶液等体积混合,溶液显酸性,醋酸的电离常数大
3 3
于醋酸根离子的水解程度:c(CHCOO-)>c(Na+)>c(H+)>c(OH-),C正确;
3
D.0.1mol/L的NaHA溶液,其pH=4,说明HA-的电离常数大于其水解程度,则c(HA-)>c(H+)>c(A2-)>
c(HA),D错误;
2
答案选AC。
24.BC
【详解】
AB.KCl和KI混合溶液中加入AgNO 溶液,因为K (AgI)< K (AgCl),先生成AgI,再生成AgCl,KI+
3 sp sp
AgNO= AgI↓+KNO ,n(KI)= 0.01mol·L-1 5 10-3L=5.0 10-5mol,消耗n(AgNO)= 5.0 10-5mol,KCl+
3 3 3
10AgNO= AgCl↓+KNO ,过量的AgNO 为0.01mol·L-1 8 10-3L-5.0 10-5mol=3.0 10-5mol,而KCl为
3 3 3
0.01mol·L-1 5 10-3L=5.0 10-5mol,则KCl过量,生成AgCl为3.0 10-5mol,由此得出反应后溶液中的溶
质为KNO、KCl,生成AgI、AgCl沉淀,离子浓度顺序为c(K+)>c(NO )>c(Cl-)>c(Ag+)>c(I-),故A错误,
3
B正确;
C.因为K (AgI)< K (AgCl),加入AgNO 溶液时首先生成AgI沉淀,故C正确;
sp sp 3
D.混合溶液中 1.03×106,故D错误;
答案选BC。
25.CD
【详解】
A.向b点对应的醋酸溶液中滴加NaOH溶液至a点,因为a点溶液呈中性,根据电荷守恒规律,所以
c(Na+)=c(CH COO-),故A正确;
3
B.25℃时,加入CHCOONa属于强碱弱酸盐,会发生水解使溶液显碱性,使得c(OH-)离子浓度增大,可
3
能引起由b向a的变化,升温溶液中的c(OH-)和c(H+)同时同等程度的增大,所以可能引起a向c的变化,
故B正确;
C.由图像知 T℃时Kw=10-12,将pH=2的硫酸与pH=10的KOH等体积混合后,溶液显中性,故C错误;
D.由图像知b点对应的溶液呈酸性,溶液中NO -、I-在酸性条件下发生氧化还原反应,因此 K+、Ba2+、
3
NO -、I-不能大量存在,故D错误;
3
答案:CD。
26.CD D Cu2++2H O Cu(OH) +2H+ΔH>0,加热促进了Cu2+水解,生成了更多的难溶物
2 2
Cu(OH) H SO
2 2 4
【详解】
(1)常温下,纯水中c(H+)=10-7mol•L-1,加入某物质后,溶液中c(H+)=10-9mol•L-1,说明溶液呈碱性,则加入
的物质是碱或强碱弱酸盐,故答案为:CD;
(2)混合溶液中溶质为等物质的量浓度的HA和NaA,混合溶液的pH>7,溶液呈碱性,说明NaA水解程度
大于HA电离程度,
A.NaA的水解程度大于HA电离程度,则c(HA)>c(A-),故A错误;
B.NaA的水解程度大于HA电离程度,则c(HA)>c(A-),且溶液体积是原来的二倍,则c(HA)小于 0.1m
ol/L,故B错误;C.根据物料守恒得2c(Na+)=c(HA)+c(A-),故C错误;
D.根据物料守恒得2c(Na+)=c(HA)+c(A-)、电荷守恒得c(Na+)+c(H+)=c(OH-)+c(A-),所以存在
2c(OH-)=2c(H+)+[c(HA)-c(A-)],故D正确;
故答案为:D;
(3)硫酸铜溶液中,铜离子水解生成氢氧化铜和硫酸,使得溶液变浑浊,则原因是:Cu2++2H O
2
Cu(OH) +2H+ΔH>0,加热促进了Cu2+水解,生成了更多的难溶物Cu(OH) ,溶液呈酸性,可以加入HSO
2 2 2 4
溶液来抑制水解。
27.MgCl 溶液 样品质量和加入足量MgCl 溶液后生成的沉淀质量 烧杯、玻璃棒、胶头滴管、
2 2
1000mL容量瓶 检漏、润洗 甲基橙或酚酞 96% cdf
【详解】
(1)含有少量NaSO 的NaOH样品中NaOH的含量进行测定,甲同学运用沉淀法测定样品中NaOH的含量,
2 4
溶解后加入氯化镁溶液完全沉淀氢氧根离子,过滤、洗涤、称量沉淀质量和样品质量得到质量分数;故答
案为:氯化镁溶液;样品质量和加入足量MgCl 溶液后生成的沉淀质量;
2
(2)①用分析天平准确称取该样品5.0000g,全部溶于水配制成1000.00mL溶液。配制该溶液所需要的主要
玻璃仪器为烧杯、玻璃棒、胶头滴管、1000mL容量瓶。
②滴定管在使用前应先检漏、洗涤、用待装液润洗、正式装液,排除气泡并调节液面,滴定管在使用前除
洗涤外,还应检漏、润洗;故答案为:检漏、润洗;
④由于石蕊变色时不容易判断,一般不选作指示剂,反应是用强酸滴定强碱,则上述中和滴定中应选用的
指示剂是甲基橙或酚酞。
⑤氢氧化钠溶液的浓度为:[0.1000mol/L×0.024L]/0.02L=0.1200mol/L,样品中含有的氢氧化钠的物质的量
为:0.1200mol/L×1L=0.12mol,氢氧化钠的质量为:40g/mol×0.12mol=4.800g,故样品中,NaOH的质量百
分含量为: ×100%=96%,故答案为:96%;
⑥a.滴定前用蒸馏水冲洗锥形瓶,对实验无影响;
b.碱式滴定管使用前未润洗,使待测液的体积偏小,则消耗的标准液偏小,所以会导致最终滴定结果偏低;
c.滴定过程中不慎将滴酸溶液滴在锥形瓶外,导致消耗标准液体积增加,所以会导致最终滴定结果偏高;
d.酸式滴定管中滴定前有气泡,滴定后气泡消失,导致消耗标准液体积增加,所以会导致最终滴定结果偏
高;
e.滴定前仰视读数,滴定后俯视读数,导致消耗的标准液偏小,所以会导致最终滴定结果偏低;
12f.酸式滴定管在使用前没有标准液润洗,标准液被稀释,消耗标准液的体积偏大,所以会导致最终滴定结
果偏高;
故选cdf。
28.Fe3+ 2.7 6 Zn2+与Fe2+分离不开 Zn(OH) 和Fe(OH) 的K 相近
2 2 sp
【详解】
加稀硫酸和HO 溶解时,发生反应Fe+2H+=Fe2++H ↑、2Fe2++H O+2H+=2Fe3++2H O,铁变为Fe3+;Fe3+刚
2 2 2 2 2 2
好完全沉淀时,c(OH-)= mol/L= mol/L,pH为-lg ≈2.7;继续加碱,锌开始
沉淀(假定Zn2+浓度为0.1mol/L)时,c(OH-)= mol/L=10-8mol/L,调节至pH为-lg =6。若上述过程
不加HO,则Fe被稀硫酸转化为Fe2+,其氢氧化物的K 与Zn(OH) 相近,则加碱后会同时发生沉淀,所
2 2 sp 2
以后果是Zn2+与Fe2+分离不开,原因是Zn(OH) 和Fe(OH) 的K 相近。答案为:Fe3+;2.7;6;Zn2+与
2 2 sp
Fe2+分离不开;Zn(OH) 和Fe(OH) 的K 相近。
2 2 sp
29.强电解质 HA⇌H++A— B 多 900 1 000 10∶1
【详解】
(1)由0.01 mol/L的BOH溶液pH=12可知,BOH在溶液中完全电离,属于强电解质;由0.1 mol/L的HA溶
液中 =1010可得:c(H+)= mol/L=10—2 mol/L,则HA在溶液中部分电离,属于弱酸,电离
方程式为HA⇌H++A—,故答案为:强电解质;HA⇌H++A—;
(2) A.由HA的电离常数可得 = ,在加水稀释HA的过程中,c(A—)减小,电离常数K 不变,
a
则 的值增大,故不符合题意;
B.由HA的电离常数可得 = ,在加水稀释HA的过程中,c(H+)减小,电离常数K 不变,
a则 的值减小, 故符合题意;
C.水的离子积常数为温度函数,温度不变,水的离子积常数不变,c(H+)与c(OH—)的乘积为水的离子积常
数,则在加水稀释HA的过程中,c(H+)与c(OH—)的乘积不变,故不符合题意;D.水的离子积常数为温度
函数,温度不变,水的离子积常数不变,c(H+)与c(OH—)的乘积为水的离子积常数,在加水稀释HA的过程
中,c(H+)减小,则c(OH—)增大,故不符合题意;
B符合题意,故答案为:B;
(3) 体积相等、pH相等的HA溶液与盐酸溶液中,HA的物质的量大于HCl,则与足量Zn反应时,HA溶
液中产生的氢气比盐酸中产生的氢气多,故答案为:多;
(4)设稀释盐酸加入蒸馏水的体积为VmL,由稀释前后,盐酸溶液中氢离子的物质的量不变可得:10—2
mol/L×0.1L=10—3mol/L×(0.1+0.001V)L,解得V=900;设加入pH=4的盐酸溶液的体积为VmL,由题意可得:
=10—3mol/L,解得V=1000,故答案为:900;1000;
(5) pH=a的X体积的某强酸与pH=b的Y体积的某强碱混合后,溶液呈中性可知,酸溶液中的氢离子的物
质的量等于碱溶液中的氢氧根离子的物质的量,则10—amol/L×XL=10—14+bmol/L×YL, = =10,故
答案为:10:1。
30.NaNO H-O-N=N-O-H N O +H O HN O +OH- 2NaNO +4Na+2H O=Na NO+4NaOH
2 2 2 2 2 2 2 2 2
X装置可排除装置内空气的干扰,可通过关闭活塞K 实现铜丝与硝酸的分离,从而控制反应的进行
1
ClNO + H O = H+ + Cl-+ HNO(写成NO↑ + NO ↑也可以)
2 2 2
【分析】
A的相对分子质量为62,在氧气中灼烧可得红棕色气体M和HO,M为NO ,二者物质的量之比为2:
2 2
1,根据原子守恒可得A为的分子式为HNO,结构式为H-O-N=N-O-H;X是一种常见的食品防腐剂和肉
2 2 2
类发色剂,俗称“工业盐”,故X为NaNO ,钠汞齐是一种强还原剂,将X还原为B(NaNO),同时
2 2 2 2
生成C(NaOH),B与AgNO 反应生成沉淀E(Ag NO)和D(NaNO ),E与HCl气体在无水乙醚的
3 2 2 2 3
环境中反应生成G(AgCl)和HNO 的溶液,蒸干后得到HNO。
2 2 2 2 2 2
【详解】
14Ⅰ.(1)根据分析,X的化学式为NaNO ;A的结构式为H-O-N=N-O-H;
2
(2)根据分析,B为NaNO,NO 水解导致溶液显碱性,NO +H O HN O +OH-;
2 2 2 2 2 2 2
(3)根据分析,C是NaOH,NaNO 与钠汞齐的反应为2NaNO +4Na+2H O=Na NO+4NaOH;
2 2 2 2 2 2
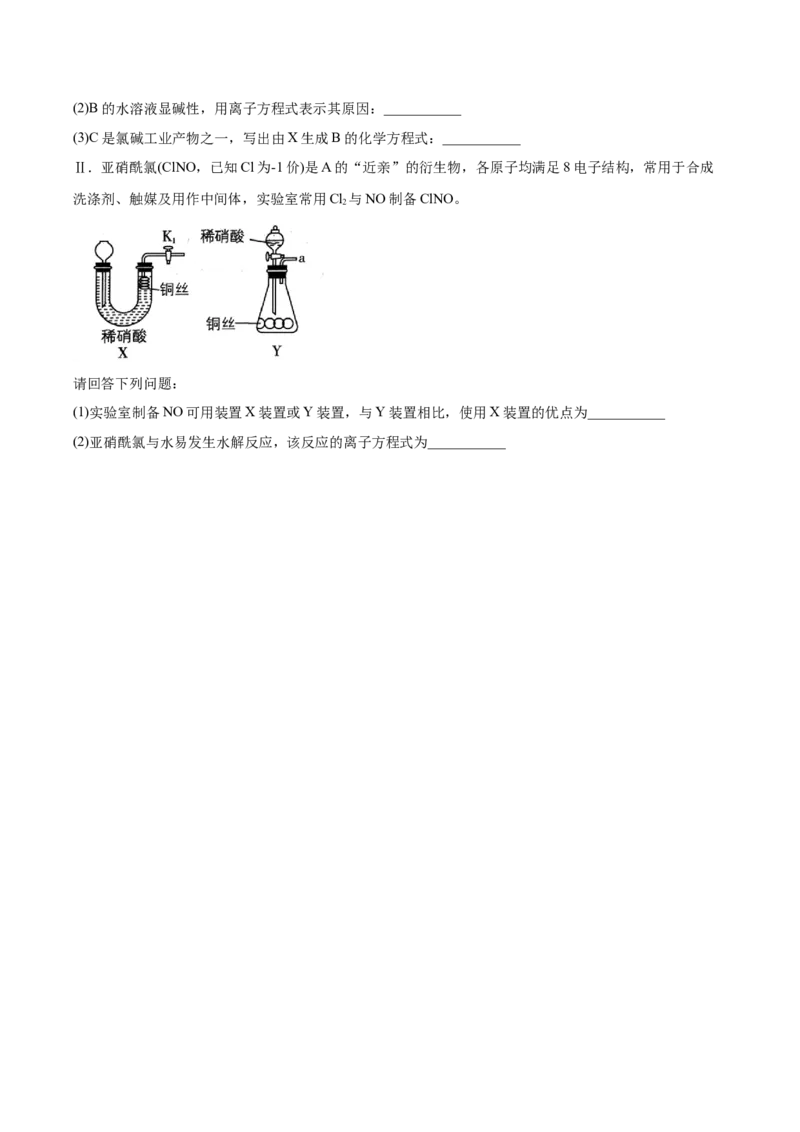
Ⅱ.(1)X装置中充满硝酸,装置中没有空气,关闭活塞K,右侧生成的气体压力增大,可将液体压入左侧
1
长颈漏斗,实现铜丝与硝酸的分离,从而控制反应的进行;
(2) 亚硝酰氯(ClNO)与水易发生水解反应,根据水解的原理生成HCl和HNO,离子方程式为ClNO +
2
HO = H+ + Cl-+ HNO。
2 2