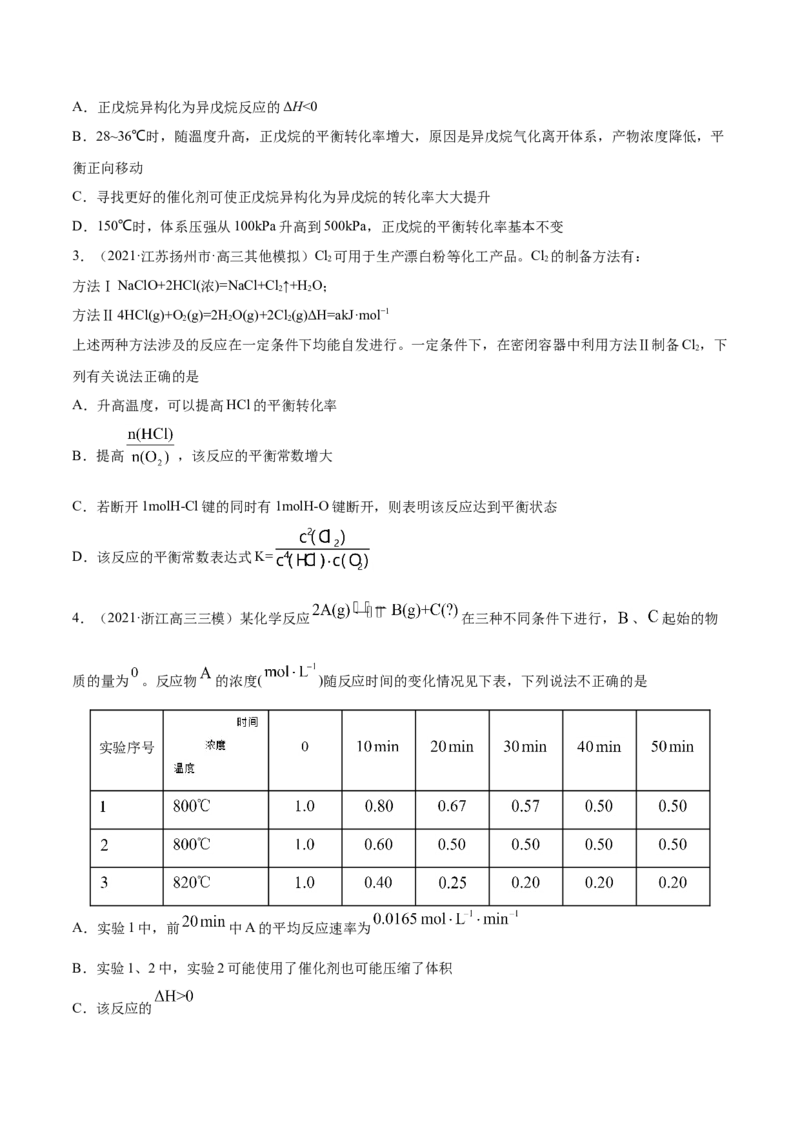文档内容
专题 09 反应速率、化学平衡
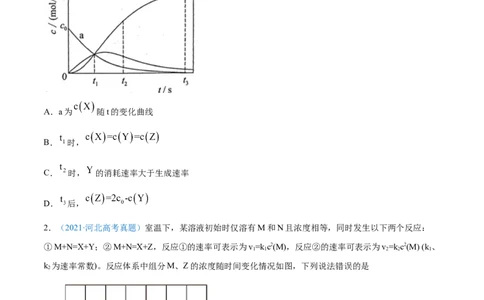
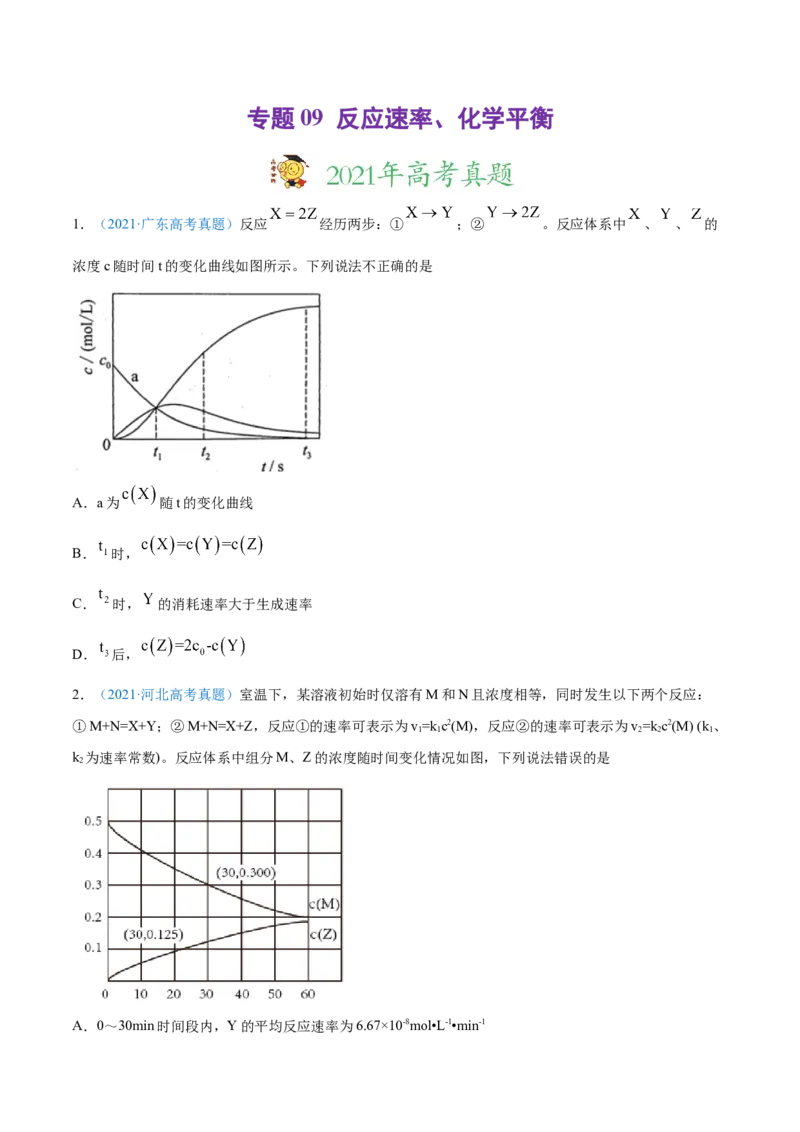
1.(2021·广东高考真题)反应 经历两步:① ;② 。反应体系中 、 、 的
浓度c随时间t的变化曲线如图所示。下列说法不正确的是
A.a为 随t的变化曲线
B. 时,
C. 时, 的消耗速率大于生成速率
D. 后,
2.(2021·河北高考真题)室温下,某溶液初始时仅溶有M和N且浓度相等,同时发生以下两个反应:
①M+N=X+Y;②M+N=X+Z,反应①的速率可表示为v=kc2(M),反应②的速率可表示为v=kc2(M) (k 、
1 1 2 2 1
k 为速率常数)。反应体系中组分M、Z的浓度随时间变化情况如图,下列说法错误的是
2
A.0~30min时间段内,Y的平均反应速率为6.67×10-8mol•L-1•min-1B.反应开始后,体系中Y和Z的浓度之比保持不变
C.如果反应能进行到底,反应结束时62.5%的M转化为Z
D.反应①的活化能比反应②的活化能大
3.(2021·浙江高考真题)相同温度和压强下,关于物质熵的大小比较,合理的是
A.
B.
C.
D.
4.(2021·浙江高考真题)一定温度下:在 的四氯化碳溶液( )中发生分解反应:
。在不同时刻测量放出的 体积,换算成 浓度如下表:
0 600 1200 1710 2220 2820 x
1.40 0.96 0.66 0.48 0.35 0.24 0.12
下列说法正确的是
A. ,生成 的平均速率为
B.反应 时,放出的 体积为 (标准状况)
C.反应达到平衡时,
D.推测上表中的x为3930
5.(2021·浙江高考真题)取50 mL过氧化氢水溶液,在少量I- 存在下分解:2HO=2H O+O↑。在一定温
2 2 2 2
度下,测得O 的放出量,转换成HO 浓度(c)如下表:
2 2 2
t/min 0 20 40 60 80
c/(mol·L-1) 0.80 0.40 0.20 0.10 0.050
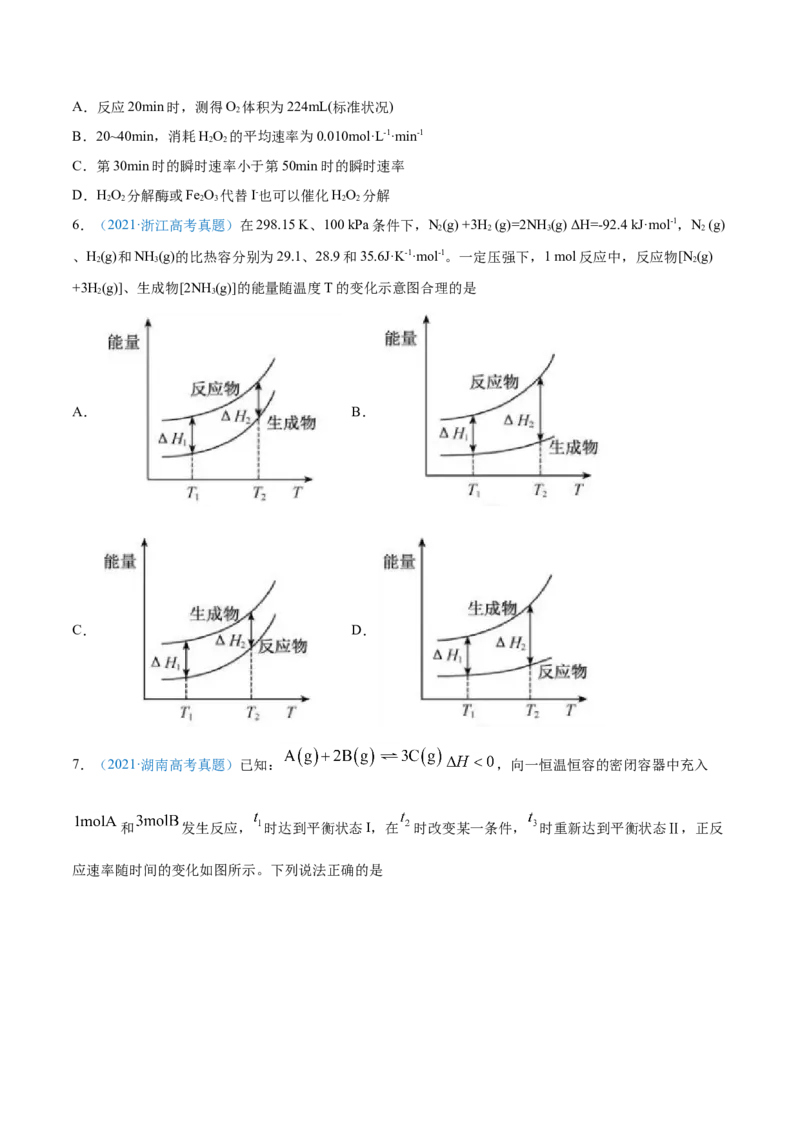
下列说法不正确的是A.反应20min时,测得O 体积为224mL(标准状况)
2
B.20~40min,消耗HO 的平均速率为0.010mol·L-1·min-1
2 2
C.第30min时的瞬时速率小于第50min时的瞬时速率
D.HO 分解酶或Fe O 代替I-也可以催化HO 分解
2 2 2 3 2 2
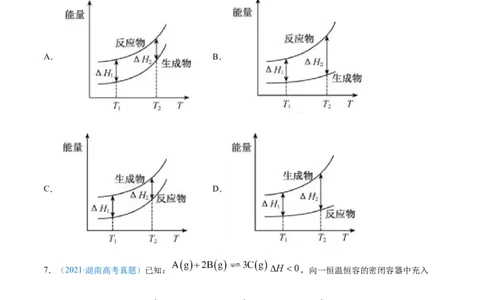
6.(2021·浙江高考真题)在298.15 K、100 kPa条件下,N(g) +3H (g)=2NH (g) ΔH=-92.4 kJ·mol-1,N (g)
2 2 3 2
、H(g)和NH (g)的比热容分别为29.1、28.9和35.6J·K-1·mol-1。一定压强下,1 mol反应中,反应物[N (g)
2 3 2
+3H (g)]、生成物[2NH (g)]的能量随温度T的变化示意图合理的是
2 3
A. B.
C. D.
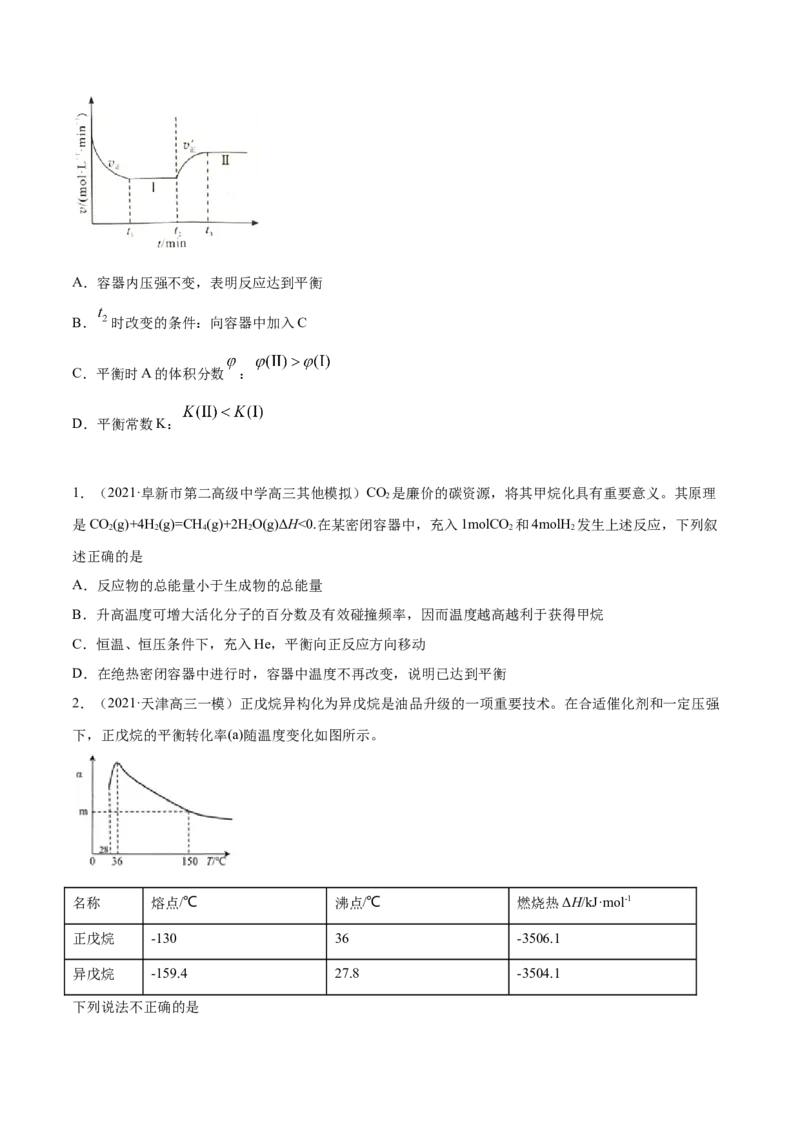
7.(2021·湖南高考真题)已知: ,向一恒温恒容的密闭容器中充入
和 发生反应, 时达到平衡状态I,在 时改变某一条件, 时重新达到平衡状态Ⅱ,正反
应速率随时间的变化如图所示。下列说法正确的是A.容器内压强不变,表明反应达到平衡
B. 时改变的条件:向容器中加入C
C.平衡时A的体积分数 :
D.平衡常数K:
1.(2021·阜新市第二高级中学高三其他模拟)CO 是廉价的碳资源,将其甲烷化具有重要意义。其原理
2
是CO(g)+4H(g)=CH (g)+2HO(g)ΔH<0.在某密闭容器中,充入1molCO 和4molH 发生上述反应,下列叙
2 2 4 2 2 2
述正确的是
A.反应物的总能量小于生成物的总能量
B.升高温度可增大活化分子的百分数及有效碰撞频率,因而温度越高越利于获得甲烷
C.恒温、恒压条件下,充入He,平衡向正反应方向移动
D.在绝热密闭容器中进行时,容器中温度不再改变,说明已达到平衡
2.(2021·天津高三一模)正戊烷异构化为异戊烷是油品升级的一项重要技术。在合适催化剂和一定压强
下,正戊烷的平衡转化率(a)随温度变化如图所示。
名称 熔点/℃ 沸点/℃ 燃烧热ΔH/kJ·mol-1
正戊烷 -130 36 -3506.1
异戊烷 -159.4 27.8 -3504.1
下列说法不正确的是A.正戊烷异构化为异戊烷反应的ΔH<0
B.28~36℃时,随溫度升高,正戊烷的平衡转化率增大,原因是异戊烷气化离开体系,产物浓度降低,平
衡正向移动
C.寻找更好的催化剂可使正戊烷异构化为异戊烷的转化率大大提升
D.150℃时,体系压强从100kPa升高到500kPa,正戊烷的平衡转化率基本不变
3.(2021·江苏扬州市·高三其他模拟)Cl 可用于生产漂白粉等化工产品。Cl 的制备方法有:
2 2
方法ⅠNaClO+2HCl(浓)=NaCl+Cl ↑+H O;
2 2
方法Ⅱ4HCl(g)+O (g)=2HO(g)+2Cl (g)ΔH=akJ·mol−1
2 2 2
上述两种方法涉及的反应在一定条件下均能自发进行。一定条件下,在密闭容器中利用方法Ⅱ制备Cl,下
2
列有关说法正确的是
A.升高温度,可以提高HCl的平衡转化率
B.提高 ,该反应的平衡常数增大
C.若断开1molH-Cl键的同时有1molH-O键断开,则表明该反应达到平衡状态
D.该反应的平衡常数表达式K=
4.(2021·浙江高三三模)某化学反应 在三种不同条件下进行, 、 起始的物
质的量为 。反应物 的浓度( )随反应时间的变化情况见下表,下列说法不正确的是
实验序号
A.实验1中,前 中A的平均反应速率为
B.实验1、2中,实验2可能使用了催化剂也可能压缩了体积
C.该反应的D.实验3中,在 时加入一定量的C物质,平衡可能不移动
5.(2021·天津南开中学高三二模)利用传感技术可以探究压强对2NO (g) NO(g)化学 平衡移动的
2 2 4
影响。在室温、100kPa条件下,往针中筒充入一定体积的NO 气体后密封并保持活塞位置不变。分别在
2
t、 t 时刻迅速移动活塞并保持活塞位置不变,测定针筒内气体压强变化如图所示。下列说法正确的是
1 2
A.B点处NO 的转化率为3%
2
B.E点到H点的过程中,NO 的物质的量先增大后减小
2
C.E、H两点对应的正反应速率大小为v =v
H E
D.B、H两点气体的平均相对分子质量大小为M =M
B H
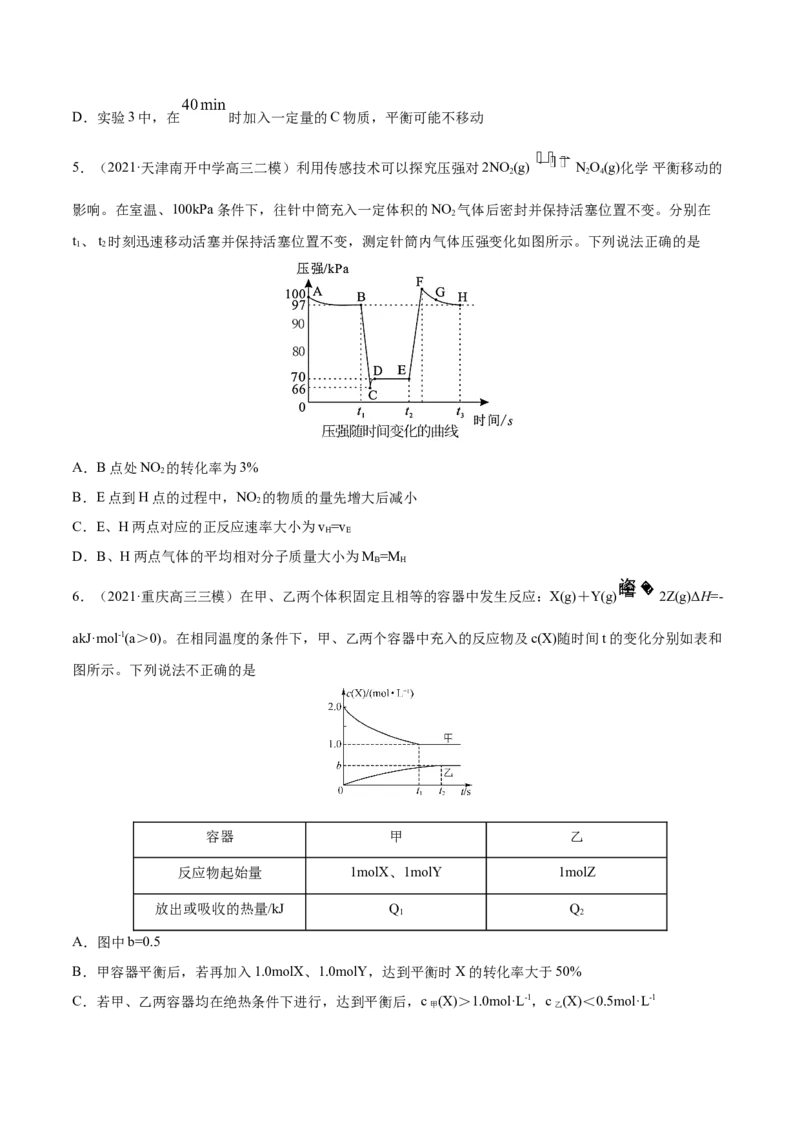
6.(2021·重庆高三三模)在甲、乙两个体积固定且相等的容器中发生反应:X(g)+Y(g) 2Z(g)ΔH=-
akJ·mol-1(a>0)。在相同温度的条件下,甲、乙两个容器中充入的反应物及c(X)随时间t的变化分别如表和
图所示。下列说法不正确的是
容器 甲 乙
反应物起始量 1molX、1molY 1molZ
放出或吸收的热量/kJ Q Q
1 2
A.图中b=0.5
B.甲容器平衡后,若再加入1.0molX、1.0molY,达到平衡时X的转化率大于50%
C.若甲、乙两容器均在绝热条件下进行,达到平衡后,c (X)>1.0mol·L-1,c (X)<0.5mol·L-1
甲 乙D.放出或吸收的热量关系为Q=2Q =0.5a
1 2
7.(2021·河北唐山市·高三三模)工业上利用 对烟道气进行脱硝(除氮氧化物)的 技术具有效率
高、性能可靠的优势。 技术的原理为 和 在催化剂( )表面转化为 和 ,反应进
程中的相对能量变化如图所示。下列说法正确的是
A.总反应方程式为
B. 是脱硝反应的催化剂
C.升高温度,脱硝反应的正反应速率的增大程度大于其逆反应速率的增大程度
D.决定反应速率的步骤是“ 的转化”
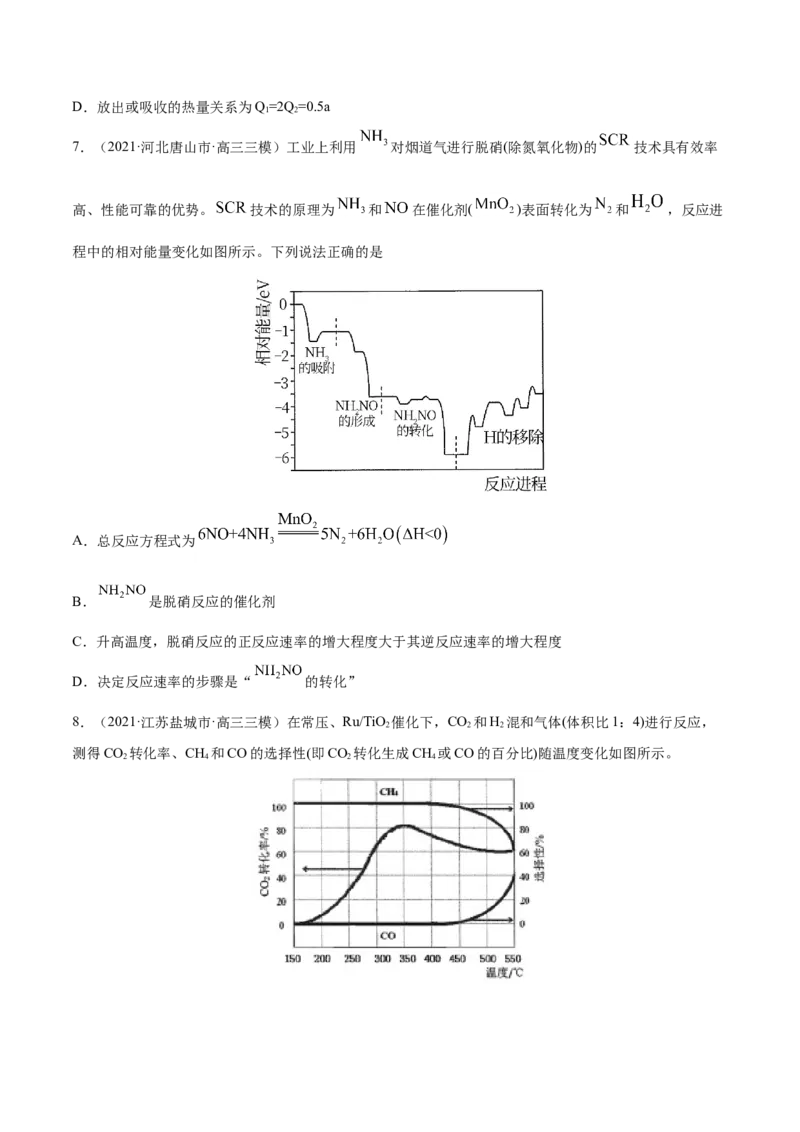
8.(2021·江苏盐城市·高三三模)在常压、Ru/TiO 催化下,CO 和H 混和气体(体积比1:4)进行反应,
2 2 2
测得CO 转化率、CH 和CO的选择性(即CO 转化生成CH 或CO的百分比)随温度变化如图所示。
2 4 2 4反应I:CO(g)+4H(g) CH(g)+2HO(g) H
2 2 4 2 1
△
反应Ⅱ:CO(g)+H(g) CO(g)+HO(g) H
2 2 2 2
△
下列说法正确的是
A. H、 H 都小于零
1 2
B.改△变压△强,对CO产量没有影响
C.反应I的平衡常数可表示为K=
D.为提高CH 选择性,可采用控制反应温度、调节压强等措施
4
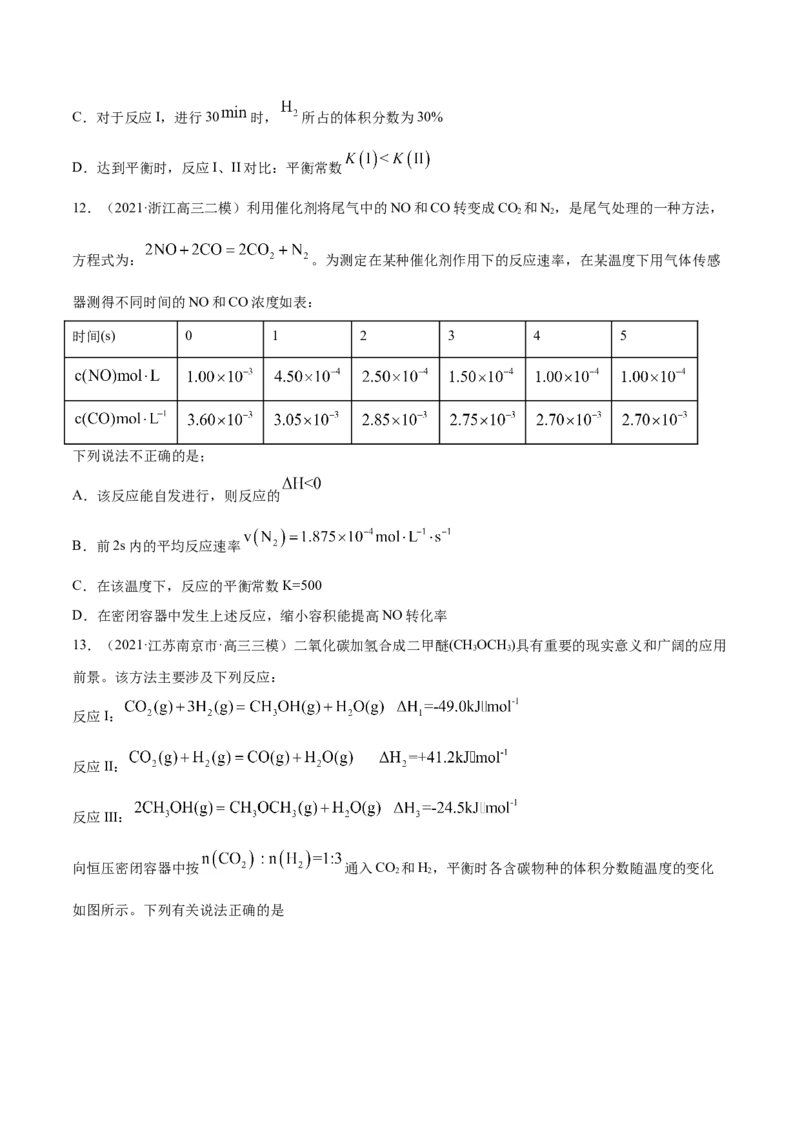
9.(2021·辽宁沈阳市·高三三模)乙基叔丁基酸(以 表示)是一种性能优良的高辛烷值汽油调和剂,
用乙醇与异丁烯(以 表示)在催化剂 催化下合成 ,反应为
。向刚性恒容容器中按物质的量之比1:1充入乙醇和异丁烯,在温度
为378 K与388 K时异丁烯的转化率随时间变化如图所示。下列说法中正确的是
A.正反应为吸热反应
B.A、M、B三点,逆反应速率最大的点A
C.388 K时,容器内起始总压为 ,则
D.容器内起始总压为 ,M点时
10.(2021·辽宁沈阳市·高三三模)我国科学家用 催化剂电催化还原 制甲酸的机理如图1所示,
反应历程如图2所示,其中吸附在催化剂表面的原子用*标注。下列说法中错误的是A.使用 催化剂能够降低反应的活化能
B.制甲酸的决速步骤为
C.电催化还原 制甲酸的副反应
D.催化剂 活性位点在催化过程中的作用是活化水分子
11.(2021·河北唐山市·高三三模)温度 °C,反应 中所有物
质均为气态。在起始温度、体积相同( °C、2L密闭容器)时,发生反应的部分数据见下表:
反应条件 反应时间
0 2 6 0 0
10 4.5
反应Ⅰ:
恒温恒容
20 1
30 1
反应Ⅱ:
0 0 0 2 2
绝热恒容
下列说法正确的是
A.对反应I,前10 内的平均反应速率
B.在其他条件不变的情况下,若30 时只向容器中再充入1 和1 ,则平衡
正向移动C.对于反应I,进行30 时, 所占的体积分数为30%
D.达到平衡时,反应I、II对比:平衡常数
12.(2021·浙江高三二模)利用催化剂将尾气中的NO和CO转变成CO 和N,是尾气处理的一种方法,
2 2
方程式为: 。为测定在某种催化剂作用下的反应速率,在某温度下用气体传感
器测得不同时间的NO和CO浓度如表:
时间(s) 0 1 2 3 4 5
下列说法不正确的是;
A.该反应能自发进行,则反应的
B.前2s内的平均反应速率
C.在该温度下,反应的平衡常数K=500
D.在密闭容器中发生上述反应,缩小容积能提高NO转化率
13.(2021·江苏南京市·高三三模)二氧化碳加氢合成二甲醚(CHOCH )具有重要的现实意义和广阔的应用
3 3
前景。该方法主要涉及下列反应:
反应I:
反应II:
反应III:
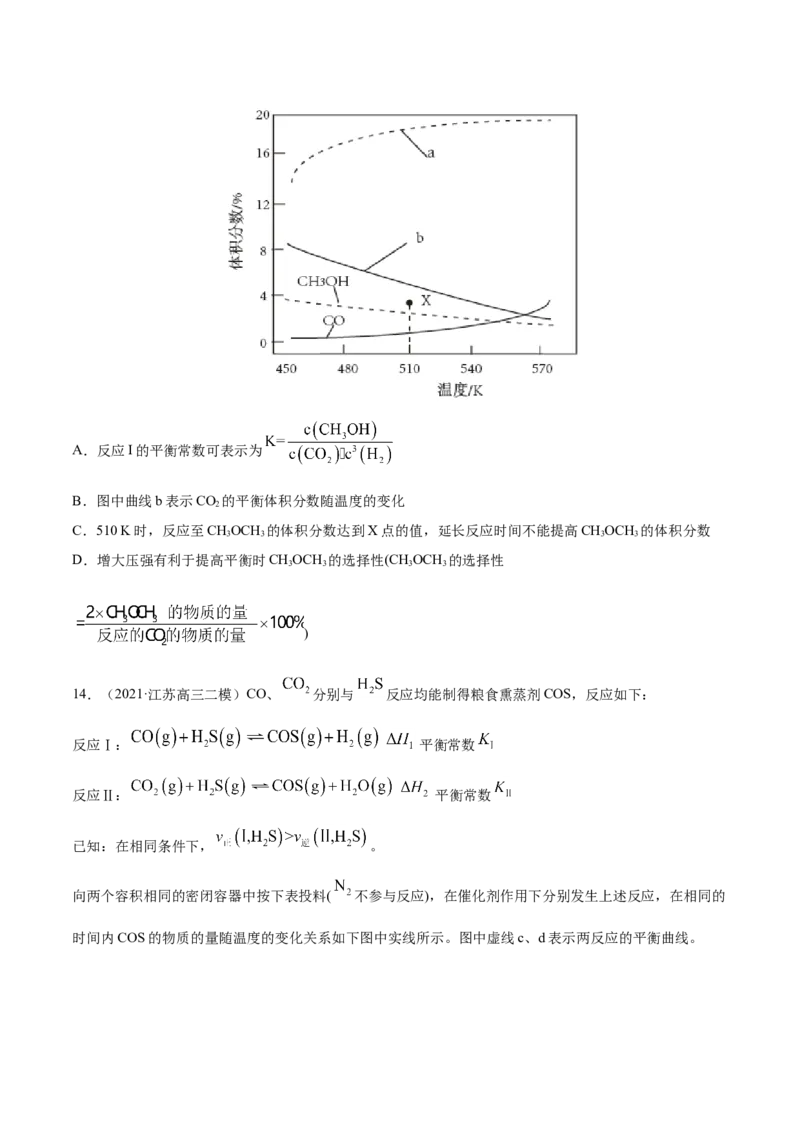
向恒压密闭容器中按 通入CO 和H,平衡时各含碳物种的体积分数随温度的变化
2 2
如图所示。下列有关说法正确的是A.反应I的平衡常数可表示为
B.图中曲线b表示CO 的平衡体积分数随温度的变化
2
C.510 K时,反应至CHOCH 的体积分数达到X点的值,延长反应时间不能提高CHOCH 的体积分数
3 3 3 3
D.增大压强有利于提高平衡时CHOCH 的选择性(CHOCH 的选择性
3 3 3 3
)
14.(2021·江苏高三二模)CO、 分别与 反应均能制得粮食熏蒸剂COS,反应如下:
反应Ⅰ: 平衡常数
反应Ⅱ: 平衡常数
已知:在相同条件下, 。
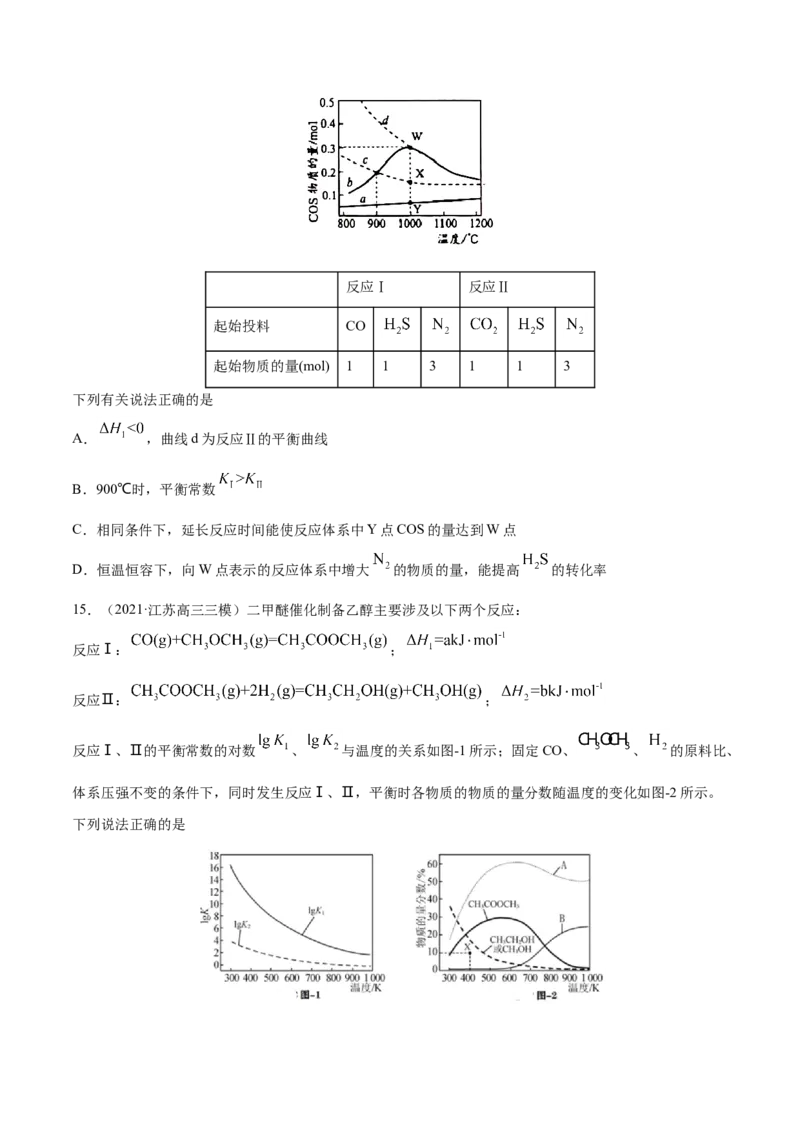
向两个容积相同的密闭容器中按下表投料( 不参与反应),在催化剂作用下分别发生上述反应,在相同的
时间内COS的物质的量随温度的变化关系如下图中实线所示。图中虚线c、d表示两反应的平衡曲线。反应Ⅰ 反应Ⅱ
起始投料 CO
起始物质的量(mol) 1 1 3 1 1 3
下列有关说法正确的是
A. ,曲线d为反应Ⅱ的平衡曲线
B.900℃时,平衡常数
C.相同条件下,延长反应时间能使反应体系中Y点COS的量达到W点
D.恒温恒容下,向W点表示的反应体系中增大 的物质的量,能提高 的转化率
15.(2021·江苏高三三模)二甲醚催化制备乙醇主要涉及以下两个反应:
反应Ⅰ: ;
反应Ⅱ: ;
反应Ⅰ、Ⅱ的平衡常数的对数 、 与温度的关系如图-1所示;固定CO、 、 的原料比、
体系压强不变的条件下,同时发生反应Ⅰ、Ⅱ,平衡时各物质的物质的量分数随温度的变化如图-2所示。
下列说法正确的是A.
B.测得X点 的物质的量分数是10%,则X点反应Ⅱ有:v <v
正 逆
C.由 的曲线知,600K后升高温度对反应Ⅰ的影响程度大于反应Ⅱ
D.曲线B表示 的物质的量分数随温度的变化
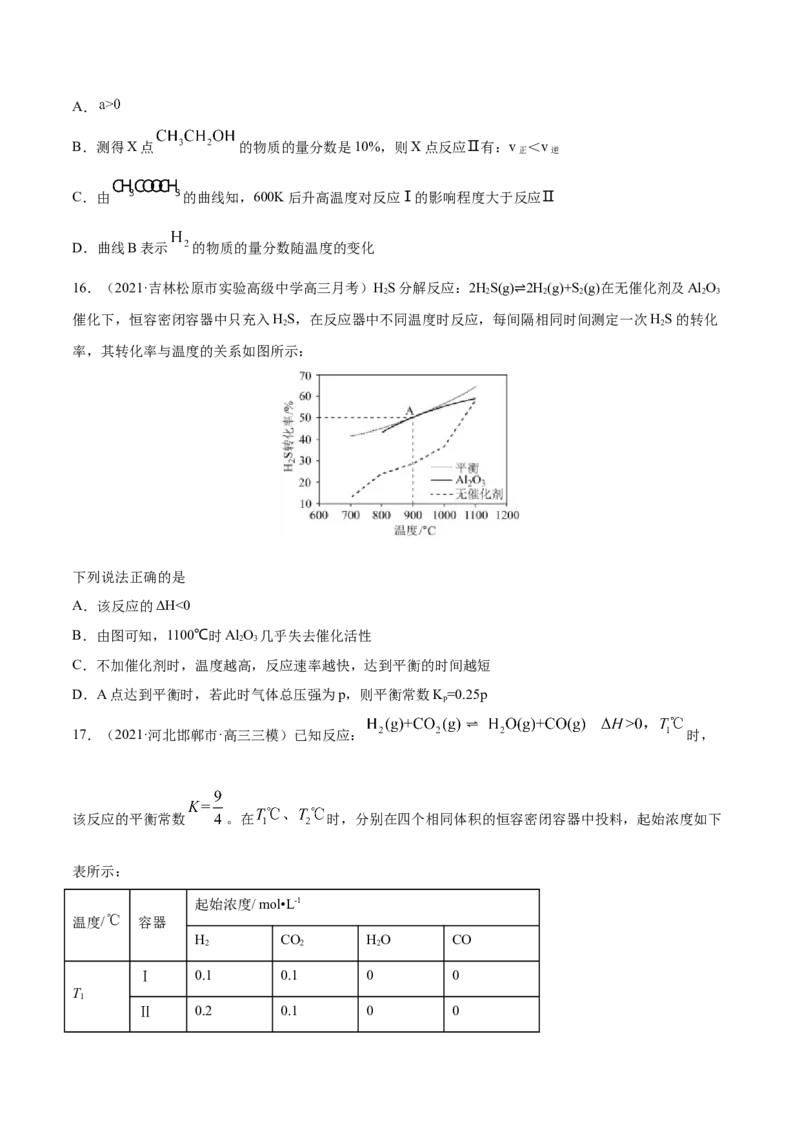
16.(2021·吉林松原市实验高级中学高三月考)HS分解反应:2HS(g) 2H(g)+S (g)在无催化剂及Al O
2 2 2 2 2 3
催化下,恒容密闭容器中只充入HS,在反应器中不同温度时反应,每间⇌隔相同时间测定一次HS的转化
2 2
率,其转化率与温度的关系如图所示:
下列说法正确的是
A.该反应的ΔH<0
B.由图可知,1100℃时Al O 几乎失去催化活性
2 3
C.不加催化剂时,温度越高,反应速率越快,达到平衡的时间越短
D.A点达到平衡时,若此时气体总压强为p,则平衡常数K=0.25p
p
17.(2021·河北邯郸市·高三三模)已知反应: 时,
该反应的平衡常数 。在 时,分别在四个相同体积的恒容密闭容器中投料,起始浓度如下
表所示:
起始浓度/ mol•L-1
温度/ 容器
H CO HO CO
2 2 2
Ⅰ 0.1 0.1 0 0
T
1
Ⅱ 0.2 0.1 0 0Ⅲ 0.1 0.2 0.1 0.1
T Ⅳ 0.04 0.04 0.06 0.06
2
下列判断正确的是
A.若容器Ⅰ 达到平衡,则 内,v(CO)=0.012mol•L-1•min-1
B. CO 的平衡转化率:容器Ⅰ>容器Ⅱ
2
C.容器Ⅲ中反应向正反应方向进行
D.若容器Ⅳ中反应向正反应方向进行,则T<T
2 1
18.(2021·天津高三二模)CH—CO 催化重整可以得到合成气(CO和H),有利于减小温室效应,其主要
4 2 2
反应为CH(g)+CO (g) 2CO(g)+2H(g) H=+247kJ·mol-1,同时存在以下反应:
4 2 2
积碳反应:CH
4
(g) C(⇌s)+2H
2
(g) H
1
>0△
消碳反应:CO
2
(g)+⇌C(s) 2CO(g△) H
2
>0
积碳会影响催化剂的活性⇌,一定时△间内积碳量和反应温度的关系如图。一定温度下,在体积为2L的密闭
容器中加入2molCH 、1molCO 以及催化剂进行该反应,达平衡时CO 的转化率为50%,下列说法正确的
4 2 2
是
A.该温度下催化重整反应的平衡常数为
B.高压利于提高CH 的平衡转化率并减少积碳
4
C.增大CH 与CO 的物质的量之比有助于减少积碳
4 2
D.温度高于600℃,积碳反应的速率减慢,消碳反应的速率加快,积碳量减少
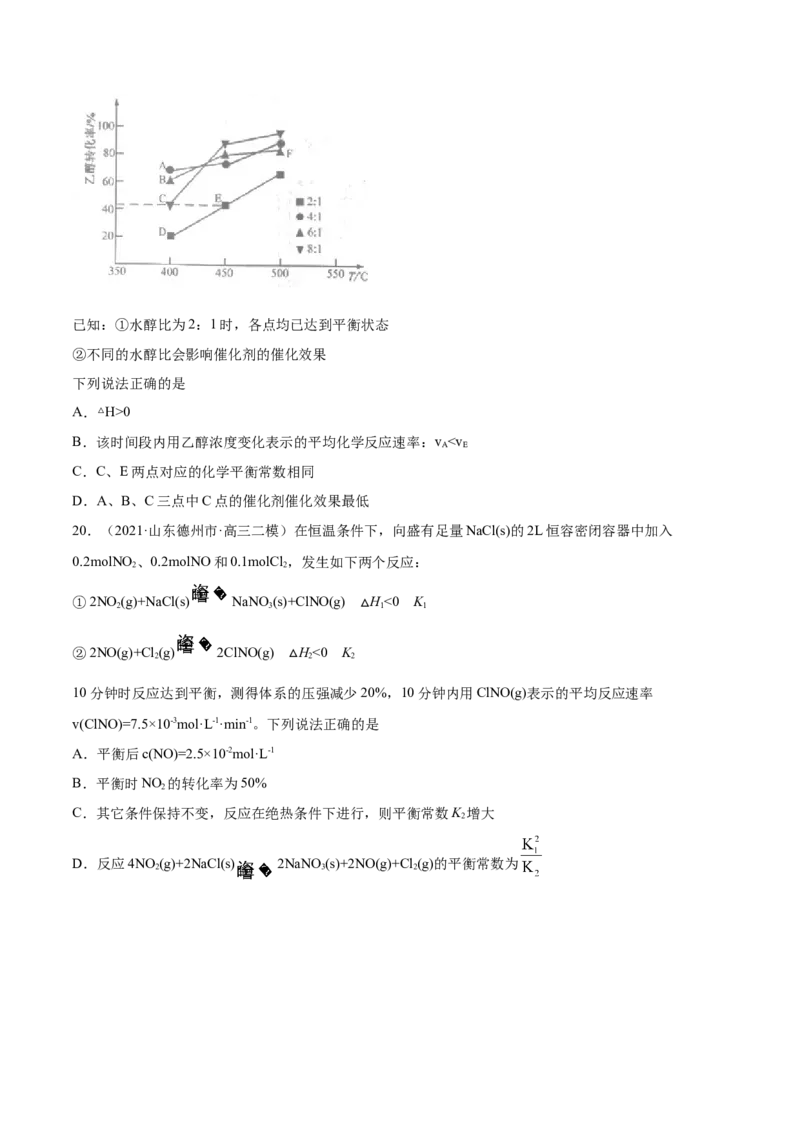
19.(2021·山东烟台市·高三二模)在体积相同的密闭容器中分别加入一定量的催化剂、1 molC HOH(g)
2 5
和不同量的HO(g),发生反应C HOH(g)+3H O(g) 2CO(g)+6H(g) H,测得相同时间内不同水醇比下
2 2 5 2 2 2
△
乙醇转化率随温度变化的关系如图所示。已知:①水醇比为2:1时,各点均已达到平衡状态
②不同的水醇比会影响催化剂的催化效果
下列说法正确的是
A.△H>0
B.该时间段内用乙醇浓度变化表示的平均化学反应速率:v