文档内容
1.二氯化二硫(S Cl)在工业上用于橡胶的硫化,还可以作为贵金属的萃取剂。可由硫和氯气在100~110 ℃直
2 2
接化合而成。实验室用以下装置制备SCl 并对尾气进行回收利用。已知SCl 的熔点:-77 ℃,沸点:137 ℃,
2 2 2 2
SCl 遇水剧烈反应。
2 2
(1)S Cl 遇水会生成黄色单质、一种能使品红溶液褪色的气体化合物及酸雾,写出该反应的化学方程式
2 2
__________________________________。
(2)B中所装试剂名称为__________________________。
(3)A、B装置中的空气可以通过控制K、K 来去除,具体方法为_________。
2 3
(4)装置E的作用是____________________________________________,写出E中发生的氧化还原反应的化
学方程式_________________________。
(5)实验时,D装置开始需要油浴加热一段时间,之后停止加热,仅需通入氯气即可。生成二氯化二硫的反应为
________ (填“放热”或“吸热”)反应。
(6)该装置由于存在系统缺陷,使制得的二氯化二硫可能不纯,现需对该装置进行改进,则改进的方法为
____________________________________。
【答案】2SCl+2H O=SO ↑+3S↓+4HCl 浓硫酸 关闭K 打开K,当B装置上方充满黄绿色气体时,关闭
2 2 2 2 2 3
K 打开K 吸收多余的氯气及氯化氢气体并获得漂白粉或漂粉精,防止污染环境 2Ca(OH) + 2Cl =
3 2 2 2
CaCl + Ca(ClO) +2H O 放热 在D与E之间加一个装有无水氯化钙或五氧化二磷或硅胶干燥管(或装
2 2 2
有浓硫酸的洗气瓶)
【解析】(1)SCl 遇水会生成黄色单质S、一种能使品红褪色的气体SO 及HCl,结合电子守恒、原子守恒可得
2 2 2
此反应的化学方程式2SCl+2H O=SO ↑+3S↑+4HCl;
2 2 2 2
故答案为:2SCl+2H O=SO ↑+3S↑+4HCl。
2 2 2 2
(2)A中所制得氯气中含有水蒸汽,利用B中所装浓硫酸干燥氯气,防止SCl 水解,
2 2
故答案为:浓硫酸。
(3)装置内空气中有氧气,加热硫时要氧化硫,故通入N 的目的是排尽装置中的空气,防止硫加热时与氧气
2反应;关闭K 打开K,当B装置上方充满黄绿色气体时,关闭K 打开K,通过上述操作可将A、B装置中的
2 3 3 2
空气去除;
故答案为:关闭K 打开K,当B装置上方充满黄绿色气体时,关闭K 打开K。
2 3 3 2
2.磺酰氯(SO Cl)主要用作氯化剂或氯磺化剂,也用于制造医药品、染料、表面活性剂等,熔、沸点分别为-
2 2
54.1℃和69.2℃。
(1)SO Cl 中S的化合价为______,SO Cl 在潮湿空气中发生剧烈反应,散发出具有刺激性和腐蚀性的“发
2 2 2 2
烟”,该反应的化学方程式为____________________。
(2)拟用干燥的SO 和Cl 通入如图装置(省略夹持装置)制取磺酰氯。
2 2
①仪器A的名称为___________,通水方向为___________(填 “a→b”或“b→a”),装置B的作用是
___________。
②反应装置中的活性炭的作用可能为:______________。
③若SO 和Cl 未经干燥,就通入装置中,也散发出具有刺激性和腐蚀性的“发烟”,该反应的化学方程式为
2 2
_________。
④滴定法测定磺酰氯的纯度:取1.800g产品,加入到100mL0.5000mol·L−1NaOH溶液中加热充分水解,冷却后加蒸馏水准确稀释至250mL,取25mL溶液于锥形瓶中,滴加2滴甲基橙,用0.1000mol·L−1标准HCl溶液
滴定至终点,重复实验三次取平均值,消耗10.00mL。 达到滴定终点的现象为___________,产品的纯度为
_________。
【答案】+6 SO Cl+2HO=2HCl↑+HSO 球形冷凝管 a→b 吸收多余SO 和Cl,防止污染空气,防
2 2 2 2 4 2 2
止空气中水蒸气进入三颈烧瓶,使SO Cl 发生水解反应而变质 催化剂 SO +Cl+2HO=2HCl+
2 2 2 2 2
HSO 滴定终点现象是滴加最后一滴HCl标准液,锥形瓶中溶液由黄色变为橙色,且30s内不恢复
2 4
75.00%
③SO 以还原性为主,Cl 具有强氧化性,在有水的情况下,发生SO +Cl+2HO=2HCl+HSO ;
2 2 2 2 2 2 4
④磺酰氯在氢氧化钠溶液中转化成NaCl和NaSO ,用盐酸滴定的是过量的NaOH,甲基橙作指示剂,因此滴
2 4
定终点现象是滴加最后一滴HCl标准液,锥形瓶中溶液由黄色变为橙色,且30s内不恢复;发生的反应是
SO Cl+2HO=2HCl↑+HSO 、H++OH-=H O,因此n(SO Cl)=
2 2 2 2 4 2 2 2
=1×10-2mol,m(SOCl)=1×10-2mol×135g·mol-
2 2
1=1.35g,则产品的纯度为1.35g/1.800g×100%=75.00%。
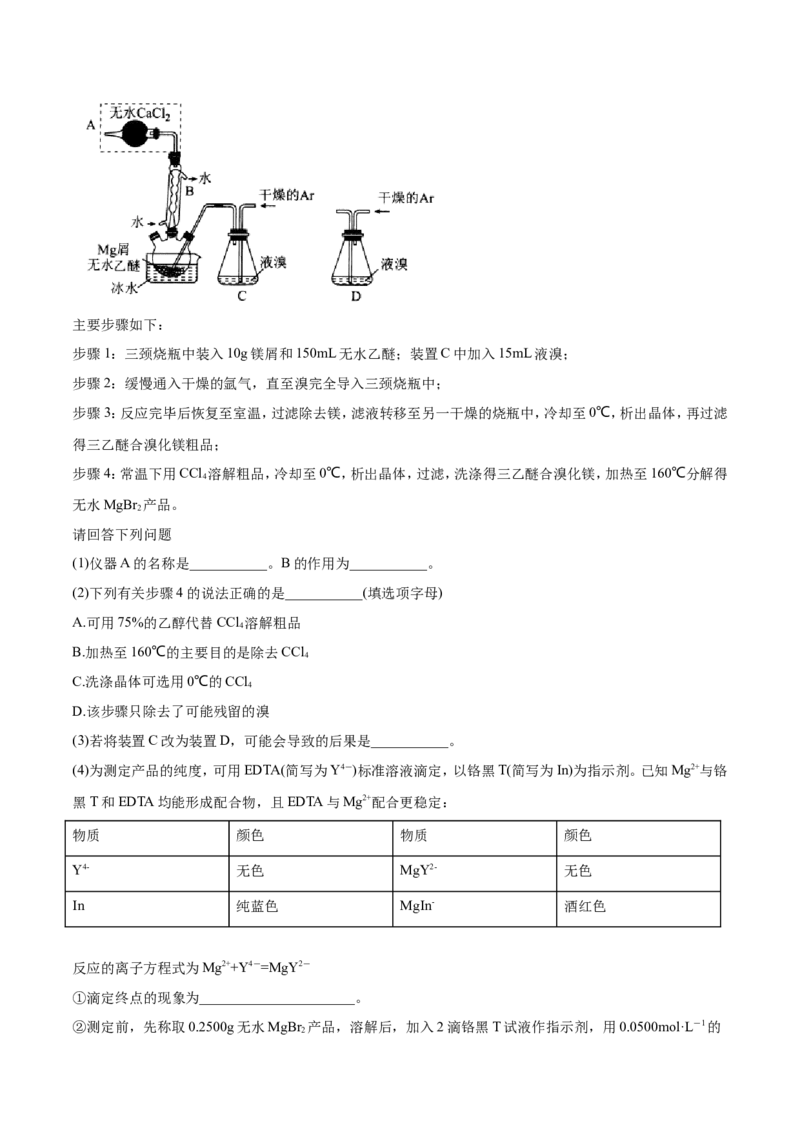
3.I.无水MgBr 可用作催化剂,实验室采用镁屑与液溴为原料制备无水MgBr ,装置如图所示(夹持装置省略)。
2 2
已知:①Mg和Br 反应剧烈放热;MgBr 具有强吸水性
2 2
②MgBr +3C HOC H MgBr ·3C HOC H。
2 2 5 2 5 2 2 5 2 5主要步骤如下:
步骤1:三颈烧瓶中装入10g镁屑和150mL无水乙醚;装置C中加入15mL液溴;
步骤2:缓慢通入干燥的氩气,直至溴完全导入三颈烧瓶中;
步骤3:反应完毕后恢复至室温,过滤除去镁,滤液转移至另一干燥的烧瓶中,冷却至0℃,析出晶体,再过滤
得三乙醚合溴化镁粗品;
步骤4:常温下用CCl 溶解粗品,冷却至0℃,析岀晶体,过滤,洗涤得三乙醚合溴化镁,加热至160℃分解得
4
无水MgBr 产品。
2
请回答下列问题
(1)仪器A的名称是___________。B的作用为___________。
(2)下列有关步骤4的说法正确的是___________(填选项字母)
A.可用75%的乙醇代替CCl 溶解粗品
4
B.加热至160℃的主要目的是除去CCl
4
C.洗涤晶体可选用0℃的CCl
4
D.该步骤只除去了可能残留的溴
(3)若将装置C改为装置D,可能会导致的后果是___________。
(4)为测定产品的纯度,可用EDTA(简写为Y4-)标准溶液滴定,以铬黑T(简写为In)为指示剂。已知Mg2+与铬
黑T和EDTA均能形成配合物,且EDTA与Mg2+配合更稳定:
物质 颜色 物质 颜色
Y4- 无色 MgY2- 无色
In 纯蓝色 MgIn- 酒红色
反应的离子方程式为Mg2++Y4-=MgY2-
①滴定终点的现象为______________________。
②测定前,先称取0.2500g无水MgBr 产品,溶解后,加入2滴铬黑T试液作指示剂,用0.0500mol·L-1的
2EDTA标准溶液滴定至终点,消耗EDTA标准溶液25.00mL,则测得无水MgBr 产品的纯度是
2
______________________(用质量分数表示)。
Ⅱ.化合物MgAl (OH) (H O) 可作环保型阻燃材料,受热时按如下化学方程式分解:
5 3 19 2 4
2MgAl (OH) (H O) ===27HO+10MgO+3Al O。
5 3 19 2 4 2 2 3
(5)写出该化合物作阻燃剂的两条依据:______________________。
(6)MgO可溶于NH Cl的水溶液,用离子方程式表示其原理:______________________。
4
【答案】干燥管 冷凝回流溴和乙醚 C 会将液溴快速压入三颈烧瓶,反应过快大量放热而存在安全隐
患 滴入最后一滴EDTA标准液时,溶液由酒红色变为纯蓝色,且半分钟内保持不变 92% 分解反应
是吸热反应,使环境温度降低;生成的氧化镁、氧化铝附着表面隔绝空气;水蒸气稀释空气
[来源:学科网]
②设样品中MgBr 的物质的量为xmol
2
Mg2++Y4-=MgY2-
1 1
X 0.05mol·L-1 0.025L
X=0.00125mol
MgBr 产品的纯度是
2
(5) 2Mg Al (OH) (H O) ===27HO+10MgO+3Al O,反应是吸热反应,使环境温度降低;生成的氧化镁、氧化
5 3 19 2 4 2 2 3
铝附着表面隔绝空气;水蒸气稀释空气,所以MgAl (OH) (H O) 作阻燃剂;(6)MgO与NH Cl溶液反应生成
5 3 19 2 4 4
氯化镁、氨水,反应离子方程式是 。
4.FeCl 是一种常用的还原剂、媒染剂。某化学小组同学在实验室里用如下两种方法来制备无水FeCl 。有关
2 2物质的性质如下:
C 6 H 5 Cl(氯苯) C 6 H 4 Cl 2 (二氯苯) [来 FeCl 3 FeCl 2
源:Z*xx*k.Com]
不溶于C HCl、C HCl、苯,易溶于乙
溶解性 不溶于水,易溶于苯、乙醇 6 5 6 4 2
醇,易吸水
熔点/℃ -45 53 易升华
沸点/℃ 132 173 — —
请回答下列问题:
(1)利用反应2FeCl + C HCl→2FeCl + C HCl+HCl制取无水FeCl 并测定FeCl 的转化率。按上图装置,在三
3 6 5 2 6 4 2 2 3
颈烧瓶中放入32.5g无水氯化铁和过量的氯苯。打开K、K,关闭K,通一段时间H 后关闭K,控制三颈烧
1 2 3 2 2
瓶内反应温度在128-139℃,反应一段时间。反应完成后打开K 再通氢气一段时间。
2
①仪器a的名称是________,装置B中盛装的试剂是________。
②反应后再通入H 的目的是________________________。
2
③冷却实验装置,将三颈烧瓶内物质倒出,经过滤、用苯洗涤、干燥后,得到粗产品,回收滤液中C HCl的操
6 5
作方法是________________。
④反应后将锥形瓶中溶液配成250mL溶液,取25.00mL所配溶液,用0.4mol·L-1NaOH溶液滴定,消耗NaOH
溶液23.60mL,则氯化铁的转化率为________。
(2)打开K、K,关闭K,通氢气与氯化铁反应制取无水FeCl 。
1 3 2 2
①写出反应的化学方程式________________________________。
②实验制得FeCl 后并防止氧化的操作是________________________________。
2
③请指出该制备方法的缺点________________________________________。
【答案】球形冷凝管 无水CaCl(或硅胶、PO) 将反应器中的HCl气体全部排入到锥形瓶内,使其被
2 2 5
充分吸收 蒸馏滤液,并收集132 的馏分 94.4% H +2FeCl 2FeCl + 2HCl 先熄灭酒精灯,再继
2 3 2
续通入氢气一段时间 氯化铁易升华,转化率低;导管易堵塞③由题中表格所给数据可知,C HCl的沸点为132 ,C HCl 的沸点为173 ,利用沸点不同回收滤液中
6 5 6 4 2
C HCl可采用蒸馏法,即蒸馏滤液,收集132 的馏分,
6 5
故答案为:蒸馏滤液,并收集132 的馏分;
④NaOH与HCl按1:1完全反应,则标准NaOH溶液滴定的盐酸的物质的量 = 0.4 mol·L-1×23.60×10-3 L =
9.44×10-3 mol,则锥形瓶中盐酸的物质的量= ×9.44×10-3 mol = 9.44×10-2 mol,再根据已知关系式2FeCl
3
1HCl可知,消耗的FeCl 的物质的量 = 2×9.44×10-2 mol = 0.1888 mol,故FeCl 的转化率 =
3 3
×100% = ×100% = 94.4%,
故答案为:94.4%;
(2)①氢气与氯化铁反应时,氢气作为还原剂,还原氯化铁为氯化亚铁,其反应的方程式可表示为:H+2FeCl
2 3
2FeCl + 2HCl,
2
故答案为:H+2FeCl 2FeCl + 2HCl;
2 3 2
②实验通过氢气与FeCl 反应制得FeCl 后,为防止FeCl 被氧化,先熄灭酒精灯,再继续通入氢气一段时间,
3 2 2
以排尽装置中的空气,
故答案为:先熄灭酒精灯,继续通入氢气一段时间;
③根据表中数据可知,因氯化亚铁易升华,则用加热的方法制备氯化亚铁,会导致转化率降低,且导管易堵塞,
故答案为:氯化铁易升华,转化率低;导管易堵塞。5.亚氯酸钠(NaClO)是一种高效的漂白剂和消毒剂,它在酸性条件下生成NaCl并放出ClO ,ClO 有类似Cl
2 2 2 2
的性质。某兴趣小组探究亚氯酸钠的制备与性质。
Ⅰ.制备亚氯酸钠
关闭止水夹②,打开止水夹①,从进气口通入足量ClO ,充分反应。
2
(1)仪器a的名称为______________,仪器b的作用是______________。
(2)装置A中生成NaClO 的离子方程式为____________________________。
2
(3)若从装置A反应后的溶液中获得NaClO 晶体,则主要操作有减压蒸发浓缩、_____、_____、洗涤、干燥等。
2
Ⅱ.探究亚氯酸钠的性质
停止通ClO 气体,再通入空气一段时间后,关闭止水夹①,打开止水夹②,向A中滴入稀硫酸。
2
(4)开始时A中反应缓慢,稍后产生气体的速率急剧加快,请解释可能的原因___________。
(5)B中现象为_________________ 。产生该现象的离子方程式为___________________。
(6)实验完成后,为防止装置中滞留的有毒气体污染空气,可以进行的操作是:再次打开止水夹①,
__________________________________。
【答案】烧瓶(圆底烧瓶) 防止倒吸 2ClO +2OH-+HO =2ClO -+HO+O↑ 降温结晶 过滤
2 2 2 2 2 2
NaClO 与HSO 反应生成的Cl-对反应起催化作用 溶液变蓝色 2ClO +10I-+8H+=2Cl-+5I +4H O 从
2 2 4 2 2 2
进气口通入一段时间的空气
【解析】 ( 1 )根据仪器a的特点,仪器a为圆底烧瓶,仪器b为干燥管,因此仪器b的作用是防止倒吸;
(2 )根据实验步骤,装置A中加入NaOH、HO 和ClO ,产物是NaClO ,Cl的化合价降低,即ClO 作氧化剂,
2 2 2 2 2
HO 作还原剂, HO 的氧化产物是O,因此有ClO + H O+OH-→ClO - +O ↑ + H O,根据化合价升降法进行
2 2 2 2 2 2 2 2 2 2 2
配平,得出仪器A中发生离子反应方程式为2ClO + 2OH- +H O=2ClO - +H O+O↑;
2 2 2 2 2 26.氧化镁在医药、建筑等行业应用广泛。硫酸镁还原热解制备高纯氧化镁是一种新的探索。以菱镁矿(主要成
分为MgCO ,另含少量杂质FeCO 和SiO 等)为原料制备高纯氧化镁的实验流程如下:
3 3 2
(1)酸溶时,MgCO 与稀硫酸反应的离子方程式为_____________________________。
3
(2)滤渣1的化学式为__________________。
(3)写出流程中“氧化”的离子方程式为______________________________________。
(4)调节pH时,使用pH试纸的具体操作是取一小块pH试纸放在洁净的玻璃片上,
_______________________________________________________;滤渣2中除了过量的MgO外,还含有的物
质是____________。
(5)高温煅烧过程中,同时存在以下反应:2MgSO +C 2MgO+2SO ↑+CO↑;MgSO +C MgO
4 2 2 4
+SO ↑+CO↑;MgSO +3C高温 MgO+S↑+3CO↑。利用下图装置对煅烧产生的气体进行连续分别吸收或收
2 4
集(其中S蒸气在A管中沉积)。
①D中收集的气体是_________________(填化学式)。
②B中盛放的溶液是__________________(填下列选项的字母编号)。
a.NaOH溶液 b.NaCO 溶液 c.稀硝酸 d.酸性KMnO 溶液
2 3 4【答案】MgCO +2H+=Mg2++CO↑+HO SiO 2Fe2++2H++H O=2Fe3++2H O 用洁净干燥的玻璃棒蘸取
3 2 2 2 2 2 2
待测溶液点在试纸的中部,再与比色卡对照得出读数 Fe(OH) CO d
3
(5)根据方程式可知煅烧得到的气体主要有SO 、CO、CO、S,产生的气体进行分步吸收或收集,所以通过A
2 2
使硫蒸气冷凝下来,再通过B装置高锰酸钾溶液吸收二氧化硫,通过C中的氢氧化钠溶液吸收二氧化碳,最
后剩余一氧化碳气体在D中收集;
①CO难溶于水,D中收集的气体可以是CO;
②装置B吸收二氧化硫,由于二氧化碳、二氧化硫均与氢氧化钠溶液、碳酸钠溶液反应,稀硝酸能把二氧化硫
氧化,但同时生成NO气体,所以B中盛放的溶液选择KMnO 溶液吸收二氧化硫,故答案为d。
4
7.制备纯净的液态无水四氯化锡的反应为Sn+2Cl SnCl , Sn也可以与HC1反应生成SnCl(SnCl 易挥
2 4 2 4
发形成气体,极易发生水解,水解生成SnO ·xH 0)。已知:
2 2
摩尔质量(g/
物质 mol) 熔点(℃) 沸点(℃)
Sn 119 231 2260
SnCl 190 246 623
2
SnCl 261 -30 114
4
[来源:学科网ZXXK]
制备装置如图所示:回答下列问题:
(1) Sn在元素周期表中的位罝为____________________________。
(2) Ⅱ、Ⅲ中的试剂分別为_______、__________;Ⅶ的作用是____________________、_____________。
(3)实验所得SnCl 因溶解了Cl 而略显黄色,提纯SnCl 的方法是____________(填序号)。
4 2 4
a.用NaOH溶液洗涤再蒸馏 b.升华 c.重结晶 d.蒸馏 e.过滤
(4)写出I中反应的化学方程式:_____________________________________。
(5)加热Sn粒之前要先让氯气充满整套装置,其目的是_________________。
(6)写出SnCl 水解的化学方程式:________________________________________。
4
【答案】第5周期IVA族 饱和食盐水 浓硫酸 吸收尾气中的氯气,防止污染空气 防止空气中
的水蒸气进入装置VI而使SnCl 水解 d MnO +4HCl(浓) MnCl +Cl↑+2H O 排除装置内的空气
4 2 2 2 2
和水蒸汽 SnCl +(x+2)H O==SnO·xH O↓+4HCl↑
4 2 2 2
(3)SnCl 和Cl 的沸点不同,当液态的SnCl 中溶有液态的Cl 时,可以根据两者的沸点不同,利用蒸馏法将
4 2 4 2
两者分离,故答案选d。
因此,本题正确答案为:d;(4)I中二氧化锰与浓盐酸反应产生氯气,对应的化学方程式为: MnO +4HCl(浓)
2
MnCl +Cl↑+2H O。
2 2 2
因此,本题正确答案为:MnO +4HCl(浓) MnCl +Cl↑+2H O;
2 2 2 2
(5)加热Sn前先通氯气的作用是排除装置中少量的空气和水,防止生成的SnCl 发生水解。
4
因此,本题正确答案为:排除装置内的空气和水蒸气;
(6)SnCl 发生水解时可以考虑先生成HCl和Sn(OH),然后Sn(OH) 分解并生成SnO ·xH O,对应的方程式
4 4 4 2 2
为:SnCl +(x+2)H O=SnO ·xH O↓+4HCl↑。
4 2 2 2
因此,本题正确答案为:SnCl +(x+2)H O=SnO ·xH O↓+4HCl↑。
4 2 2 2
8.甲、乙实验小组设计如下实验装置分别制备SnCl 和漂白粉。
4
(1)已知:a.金属锡熔点231 ℃,化学活泼性与铁相似;
b.干燥的氯气与熔融金属锡反应生成SnCl ,SnCl 的沸点114 ℃;
4 4
c.SnCl 、SnCl 均易水解,易溶于有机溶剂,且Sn2+易被氧化。根据图甲装置回答:
2 4
①试管Ⅱ中的试剂是____________________,Ⅲ中的试剂是________________________。
②Ⅵ处装置最好选用________(填字母)。
③Ⅰ处装置中反应的离子方程式是____________________________________________。
④实验结束后,欲回收利用装置Ⅰ中未反应完的MnO ,需要的玻璃仪器有______________。
2
(2)已知:①Cl 与潮湿的消石灰反应是放热反应;②温度较高时Cl 与潮湿Ca(OH) 的反应为6Cl+
2 2 2 2
6Ca(OH) =Ca(ClO)+5CaCl +6HO。
2 3 2 2 2
根据图乙装置回答:此实验所得Ca(ClO) 产率较低的理由是
2
①________________________________________________________________________;②________________________________________________________________________。
【答案】饱和食盐水 浓HSO C MnO +4H++2Cl- Mn2++Cl↑+2HO 普通漏斗、玻璃棒、烧杯
2 4 2 2 2
B、C之间缺少吸收HCl的装置,2HCl+Ca(OH) ===CaCl +2HO Cl 与消石灰反应为放热反应,温度升高,
2 2 2 2
部分Ca(OH) 转化为Ca(ClO )
2 3 2
9.在工业中利用镁制取硅:2Mg+SiO 2MgO+Si,同时有副反应发生:2Mg+Si MgSi,MgSi遇
2 2 2
盐酸迅速反应生成SiH(硅烷),SiH 在常温下是一种不稳定、易分解的气体。如图是进行Mg与SiO 反应的实
4 4 2
验装置:
(1)由于氧气的存在对该实验有较大影响,实验中应通入气体X作为保护气,试管中的固体药品可选用
________(填字母)。
a.石灰石 b.锌粒 c.纯碱
(2)实验开始时,必须先通入X气体,再加热反应物,其理由是____________________,当反应开始后,移走
酒精灯反应能继续进行,其原因是_____________。
(3)反应结束后,待冷却至常温时,往反应后的混合物中加入稀盐酸。可观察到闪亮的火星,产生此现象的原
因用化学方程式表示为____________________。
【答案】b 让氢气排尽装置内的空气,避免空气中的成分对实验的影响 该反应为放热反应,可利用自身放出的热量维持反应进行 MgSi+4HCl===2MgCl +SiH↑、SiH+2O===SiO +2HO
2 2 4 4 2 2 2
10.氰化钠是一种剧毒物质,工业上常用硫代硫酸钠溶液处理废水中的氰化钠。硫代硫酸钠的工业制备原理
为:2NaS+Na CO+4SO===3Na SO+CO 。某化学兴趣小组拟用该原理在实验室制备硫代硫酸钠,并检测
2 2 3 2 2 2 3 2
氰化钠废水处理排放情况。
I.实验室通过如图所示装置制备NaSO
2 2 3
(1)实验中要控制SO 生成速率,可采取的措施有_____________(写出一条)。
2
(2)b装置的作用是_____________ 。
(3)反应开始后,c 中先有淡黄色浑浊产生,后又变为澄清,此浑浊物为__________(填化学式)。
(4)实验结束后,在e处最好连接盛__________(填“NaOH 溶液”、“水”、“CCl ”中的一种) 的注射器,接
4
下来的操作为______________,最后拆除装置。
II.氰化钠废水处理
(5)已知: a.废水中氰化钠的最高排放标准为0.50mg/L;
b.Ag++2CN-==[Ag(CN) ]-,Ag++I-=AgI↓,AgI 呈黄色,且CN-优先与Ag+反应。
2
实验如下: 取20.00mL处理后的氰化钠废水于锥形瓶中,并滴加几滴KI溶液作指示剂,用1.00×10-4mol/L的
标准AgNO 溶液滴定,消耗AgNO 溶液的体积为1.50mL。
3 3①滴定时1.00×10-4mol/L的标准AgNO 溶液应用________(填仪器名称) 盛装; 滴定终点时的现象是
3
______________。
②处理后的废水是否达到排放标准_______(填“是”或“否”)。
【答案】控制反应温度或调节酸的滴加速度安全瓶,防止倒吸SNaOH溶液打开K 关闭K 酸式滴定管滴入最
1 2
后一滴硝酸银溶液,出现黄色沉淀,且半分钟内沉淀不消失否
(3)二氧化硫与硫化钠在溶液中反应得到S,硫与亚硫酸钠反应得到NaSO,c中先有浑浊产生,后又变澄清,
2 2 3
此浑浊物为S,故答案为:S;
(4)实验结束后,装置b中还有残留的二氧化硫,为防止污染空气,应用氢氧化钠溶液吸收,氢氧化钠和二氧化
硫反应生成亚硫酸钠和水,再关闭K 打开K,防止拆除装置时污染空气,故答案为:NaOH溶液;关闭K 打
2 1 2
开K;
1
【实验二】(5)①硝酸银溶液显酸性,应该用酸式滴定管盛装;Ag+与CN-反应生成[Ag(CN) ]-,当CN-反应结束
2
时,滴入最后一滴硝酸银溶液,Ag+与I-生成AgI黄色沉淀半分钟内沉淀不消失,说明反应到达滴定终点,故
答案为:酸式滴定管;滴入最后一滴硝酸银溶液,出现淡黄色沉淀,半分钟内沉淀不消失;
②消耗AgNO 的物质的量为1.5×10-3L×0.0001mol/L=1.50×10-7mol,根据方程式Ag++2CN-=[Ag(CN) ]-,处理
3 2
的废水中氰化钠的质量为1.50×10-7mol×2×49g/mol=1.47×10-5g,废水中氰化钠的含量为
=0.735mg/L>0.50mg/L,处理后的废水未达到达到排放标准,故答案为:否。
11.高铁酸钾(K FeO)为紫黑色粉末,是一种新型高效消毒剂。KFeO 易溶于水,微溶于浓KOH溶液,在0
2 4 2 4
℃~5 ℃的强碱性溶液中较稳定。一般制备方法是先用Cl 与KOH溶液在20 ℃以下反应生成KClO(在较高
2
温度下则生成KClO),KClO再与KOH、Fe(NO ) 溶液反应即可制得KFeO。实验装置如图所示:
3 3 3 2 4回答下列问题:
(1)制备KClO。
①仪器a的名称是________________;装置B吸收的气体是________。
②装置C中三颈烧瓶置于冰水浴中的目的是______________;装置D的作用是_____________。
(2)制备KFeO。
2 4
①装置C中得到足量KClO后,将三颈烧瓶上的导管取下,加入KOH溶液、Fe(NO ) 溶液,水浴控制反应温
3 3
度,搅拌,当溶液变为紫红色,该反应的离子方程式为________________________________。
②向装置C中加入饱和________溶液,析出紫黑色晶体,过滤。
(3)测定KFeO 纯度。测定KFeO 的纯度可用滴定法,滴定时有关反应的离子方程式为:
2 4 2 4
a.FeO 2-+CrO -+2H O═CrO 2-+Fe(OH) ↓+OH-
4 2 2 4 3
b.2CrO 2-+2H+═Cr O2-+H O
4 2 7 2
c.Cr O2-+6Fe2++14H+═2Cr3++6Fe3++7H O
2 7 2
称取2.0g制备的KFeO 样品溶于适量KOH溶液中,加入足量的KCrO ,充分反应后过滤,滤液在250mL容
2 4 2
量瓶中定容.取25.00mL加入稀硫酸酸化,用0.10 mol•L-1的(NH )Fe(SO ) 标准溶液滴定至终点,重复操作2
4 2 4 2
次,平均消耗(NH )Fe(SO ) 溶液的体积为24.00mL,则该KFeO 样品的纯度为________。
4 2 4 2 2 4
【答案】分液漏斗HCl防止Cl 与KOH反应生成KClO 吸收多余的Cl,防止污染空气3ClO-+2Fe3++10OH-
2 3 2
=2FeO 2- +3Cl-+5H OKOH79.2%
4 2
(2)①足量KClO中依次加入KOH溶液、Fe(NO ) 溶液,发生氧化还原反应生成KFeO、KCl和水等,反应的
3 3 2 4
离子方程式为3ClO-+2Fe3++10OH-═2FeO 2-+3Cl-+5H O,故答案为:3ClO-+2Fe3++10OH-═2FeO 2-+3Cl-+5H O;
4 2 4 2
②KFeO 易溶于水、微溶于浓KOH溶液,所以向装置C中加入饱和KOH溶液,析出紫黑色晶体,过滤,故答
2 4案为:KOH;
(3)根据反应FeO2-+CrO -+2H O═CrO 2-+Fe(OH) ↓+OH-、2CrO2-+2H+═Cr O2-+H O和 Cr O2-+6Fe2+
4 2 2 4 3 4 2 7 2 2 7
+14H+═6Fe3++2Cr3++7H O,可得关系式2FeO2-~Cr O2-~6Fe2+,根据题意可知,(NH )Fe(SO ) 的物质的量为
2 4 2 7 4 2 4 2
0.024L×0.1000 mol/L=0.0024mol,所以高铁酸钾的质量为0.0024mol× × ×198g/mol=1.584g,所以
KFeO 样品的纯度为 ×100%=79.2%,故答案为:79.2%。
2 4
12.工业上,向500℃~600℃的铁屑中通入氯气生产无水氯化铁;向炽热铁屑中通入氯化氢气体生产无水氯
化亚铁。现用如图所示的装置模拟上述过程进行试验。
回答下列问题:
(1)制取无水氯化铁实验中,仪器甲的名称为_______________,进行实验时,应先点燃___________(选填A
或C)处酒精灯。
(2)制取无水氯化铁的实验中,A中反应的离子方程式为_______________________,装置B中加入的试剂是
____________________。
(3)制取的无水氯化铁中混有少量氯化亚铁,其原因是__________________(化学方程式表示)。为除去氯气
中混有的少量HCl,可以在装置A、B间加入装有_______________的洗气瓶。
(4)工业上常用石灰乳吸收制氯气的尾气制得漂白粉,漂白粉的有效成分是_____________(填化学式)。长
期露置于空气中的漂白粉,加稀盐酸后产生的气体是_____________(填数字代号)。
① O ② Cl ③ CO ④ HClO
2 2 2
(5)制取无水氯化亚铁实验中,装置A用来制取HCl气体,其化学方程式为:NaCl + HSO (浓)
2 4
NaHSO + HCl↑,通过装置C后尾气的成分是_________________。若仍用D的装置进行尾气处理,存在的主
4要问题是_________________________________________。
(6)制取无水氯化亚铁实验中,若操作不当,制得的FeCl 会含有少量FeCl ,检验FeCl 常用的试剂是
2 3 3
________________。(填化学式)欲制得纯净的FeCl ,在实验操作中应先__________________________,再
2
___________________________。
【答案】 分液漏斗 A MnO +4H++2Cl- Mn2++Cl↑+2HO 浓硫酸 Fe+2HCl FeCl +H 饱和食
2 2 2 2 2
盐水 Ca(ClO) ③ 氯化氢、氢气 发生倒吸、可燃性气体H 不能被吸收 KSCN溶液 点燃A处的酒精
2 2
灯 点燃C处的酒精灯
氢气;氯化氢易溶于水,氢气难溶于水,若仍用D的装置进行尾气处理,存在的主要问题是发生倒吸、可燃性
气体H 不能被吸收;(6)Fe3+遇KSCN溶液变血红色,检验FeCl 常用的试剂是KSCN溶液;加热条件下铁能
2 3
被氧气氧化为+3价,所以欲制得纯净的FeCl ,在实验操作中应先点燃A处的酒精灯制取氯化氢,用氯化氢
2
排出装置中的空气后再点燃C处的酒精灯。
13.亚硝酰氯(NOCl,熔点:-64.5 ℃,沸点:-5.5 ℃)是一种黄色气体,遇水易水解。可用于合成清洁剂、触
媒剂及中间体等。实验室可由氯气与一氧化氮在常温常压下合成。
(1)甲组的同学拟制备原料气NO和Cl,制备装置如图所示:
2
为制备纯净干燥的气体,补充下表中缺少的药品。装置Ⅰ
装置Ⅱ
烧瓶中 分液漏斗中
[来源:Zxxk.Com][来源:学科网]
制备纯净的Cl MnO ①________ ②________
2 2
制备纯净的NO Cu ③________ ④________
(2)乙组同学利用甲组制得的NO和Cl 制备NOCl,装置如图所示:
2
①装置连接顺序为a→________________(按气流自左向右方向,用小写字母表示)。
②装置Ⅳ、Ⅴ除可进一步干燥NO、Cl 外,另一个作用是____________________。
2
③装置Ⅶ的作用是________________________________________________________。
④装置Ⅷ中吸收尾气时,NOCl发生反应的化学方程式为______________________。
(3)丙组同学查阅资料,查得王水是浓硝酸与浓盐酸的混酸,一定条件下混酸可生成亚硝酰氯和氯气,该反应
的化学方程式为_______________________________________。
【答案】浓盐酸饱和食盐水稀硝酸水e→f(或f→e)→c→b→d通过观察气泡调节气体的流速防止水蒸气进入
反应器NOCl+2NaOH===NaCl+NaNO +HOHNO (浓)+3HCl(浓)===NOCl↑+Cl↑+2HO
2 2 3 2 2
因此①接口顺序为a→e→f(或f→e) →c→b→d,②通过观察洗气瓶中的气泡的快慢,调节NO、Cl 气体的流
2
速,以达到最佳反应比,提高原料的利用率,减少有害气体的排放,③装置Ⅶ中装有的无水CaCl ,是防止水
2
蒸气进入装置Ⅸ中使生成的NOCl变质,④NOCl遇水反应生成HCl和HNO,再与NaOH反应,所以反应的
2
化学方程式为:NOCl+2NaOH NaCl+NaNO+H O。
2 2
(3)由题中叙述可知,反应物为浓硝酸和浓盐酸,生成物为亚硝酰氯和氯气,所以可写出反应的化学方程式为HNO(浓)+3HCl(浓) NOCl↑+Cl ↑+2H O。
3 2 2
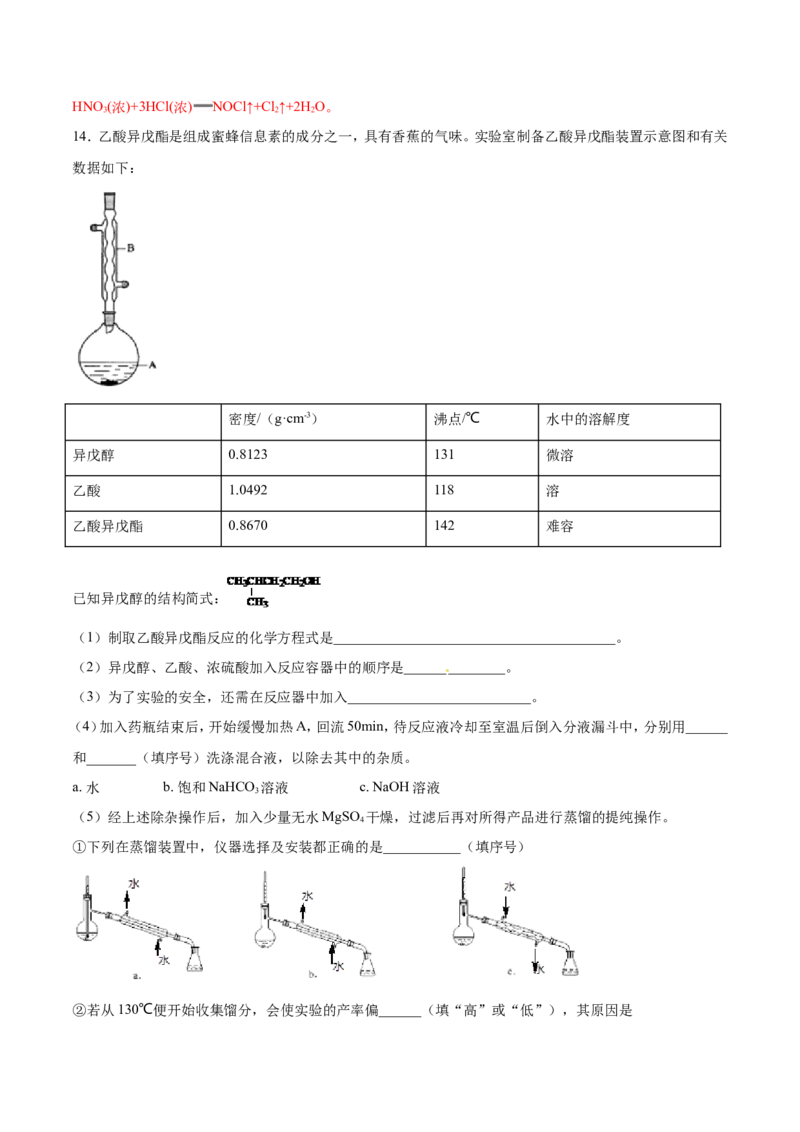
14.乙酸异戊酯是组成蜜蜂信息素的成分之一,具有香蕉的气味。实验室制备乙酸异戊酯装置示意图和有关
数据如下:
密度/(g·cm-3) 沸点/℃ 水中的溶解度
异戊醇 0.8123 131 微溶
乙酸 1.0492 118 溶
乙酸异戊酯 0.8670 142 难容
已知异戊醇的结构简式:
(1)制取乙酸异戊酯反应的化学方程式是________________________________________。
(2)异戊醇、乙酸、浓硫酸加入反应容器中的顺序是______________。
(3)为了实验的安全,还需在反应器中加入__________________________。
(4)加入药瓶结束后,开始缓慢加热A,回流50min,待反应液冷却至室温后倒入分液漏斗中,分别用______
和_______(填序号)洗涤混合液,以除去其中的杂质。
a. 水 b. 饱和NaHCO 溶液 c. NaOH溶液
3
(5)经上述除杂操作后,加入少量无水MgSO 干燥,过滤后再对所得产品进行蒸馏的提纯操作。
4
①下列在蒸馏装置中,仪器选择及安装都正确的是___________(填序号)
②若从130℃便开始收集馏分,会使实验的产率偏______(填“高”或“低”),其原因是___________________________________________。
(6)为提高异戊醇的转化率可采取的措施是___________________________________。
【答案】CHCOOH+ +H O 异戊醇、乙酸、浓硫酸 碎瓷片
3 2
a b b 高 产品中会收集到异戊醇 加入过量的乙酸或及时分离出反应产物
【解析】(1)已知异戊醇的结构简式: ,制取乙酸异戊酯反应的化学方程式是CHCOOH+
3
+H O;
2
15.氢化钙(CaH)固体是登山运动员常用的能源提供剂。氢化钙要密封保存,一旦接触到水就发生反应生成
2
氢氧化钙和氢气。氢化钙通常用氢气与金属钙加热制取,下图是模拟制取装置。
(1)装置B的作用是___________________;装置D的作用是_______________________;
(2)利用实验装置进行实验,实验步骤如下:检查装置气密性后装入药品;打开分液漏斗活塞,________(请
按正确的顺序填入下列步骤的序号)。
①加热反应一段时间 ②收集气体并检验其纯度 ③关闭分液漏斗活塞 ④停止加热,充分冷却
(3)为了确认进入装置C的氢气已经干燥,应在B、C之间再接一装置,该装置中加入的试剂是______。(4)甲同学设计一个实验,测定上述实验中得到的氢化钙的纯度。请完善下列实验步骤。①样品称量②加入
________溶液(填化学式),搅拌、过滤③________(填操作名称)④_______(填操作名称)⑤称量碳酸钙
(5)乙同学利用如图装置测定上述实验中得到的氢化钙的纯度。他称取46 mg 所制得的氢化钙样品,记录开
始时注射器活塞停留在10.00mL刻度处,反应结束后充分冷却,活塞最终停留在57.04mL刻度处。(上述气体
体积均在标准状况下测定)试通过计算求样品中氢化钙的纯度:__________________________。
【答案】除去氢气中的水蒸气 防止空气中的水蒸气进入C装置 ②①④③ 无水硫酸铜(或其他合
理答案) NaCO(KCO 或其他合理答案) 洗涤 烘干(干燥) 91.3%
2 3 2 3
(3)检验是否干燥用无水硫酸铜,因为无水硫酸铜遇水变蓝色现象很明显,故为了确认进入装置C的氢气已
经干燥,应在B、C之间再接一装置,该装置中加入的试剂是无水硫酸铜;
本题答案为:无水硫酸铜。
(4)从最终称量碳酸钙可以知道,应加入碳酸钠溶液,使CaH 反应的同时得到碳酸钙沉淀,然后经过滤、洗涤、
2
烘干、称量,确定纯度;
本题答案为:NaCO、洗涤、烘干。
2 3
(5)由注射器D开始时活塞停留在10mL刻度处,反应结束后充分冷却,活塞最终停留57.04mL刻度处,可以知
道生成氢气:57.04mL-10mL=47.04mL,所以氢气的质量为: 2g/mol=0.0042g=4.2mg,设混合物中
氢化钙的质量为x,生成氢气质量为y,则钙的质量为46mg-x,钙与水反应生成氢气质量为4.2mg-y,CaH 2HO===Ca(OH) 2H ,
2 2 2 2
42 4
X y 有42:4=x:y---①
Ca 2HO=== Ca(OH) H ,
2 2 2
40 2
46-x 4.2-y 有40:2=(46-x):(4.2-y)---②
联立①②解得x=42mg,y=4mg。所以样品中氢化钙的纯度为: 100 =91.3 ;
本题答案为:91.3
16.在梨、香蕉等水果中存在着乙酸正丁酯。实验室制备乙酸正丁酯的反应、装置示意图和有关数据如下:
水中溶解性 密度(g·cm-3) 沸点 相对分子质量
乙酸 溶于水 1.049 2 118 60
正丁醇 微溶于水 0.809 8 117.7 74
乙酸正丁酯 微溶于水 0.882 4 126.5 116
实验步骤:
Ⅰ.乙酸正丁酯的制备在A中加入7.4 g正丁醇、6.0 g乙酸,再加入数滴浓硫酸,摇匀,放入1~2颗沸石。按图安装带分水器的回流
反应装置,并在分水器中预先加入水,使水面略低于分水器的支管口,通入冷凝水,缓慢加热A。在反应过程
中,通过分水器下部的旋塞分出生成的水,保持分水器中水层液面的高度不变,使油层尽量回到圆底烧瓶中。
反应达到终点后,停止加热,记录分出水的体积。
Ⅱ.产品的精制
把分水器中的酯层和A中反应液倒入分液漏斗中,分别用少量水、饱和碳酸钠溶液和水洗涤,分出的产物加
入少量无水硫酸镁固体,静置后过滤,将产物常压蒸馏,收集124-126 ℃的馏分,得到5.8 g产品。请回答下列
问题:
(1)冷水应从冷凝管的________(填“a”或“b”)口通入。
(2)产品的精制过程中,第一次水洗的目的是________________,第二次水洗的目的是________________,洗
涤完成后将有机层从分液漏斗的________(填“上口”或“下口”)转移到锥形瓶中。
(3)本实验提高产品产率的方法是_________________________________________。
(4)判断反应终点的依据是_______________________________________________。
(5)该实验过程中,生成乙酸正丁酯的产率是_______________________________。
【答案】a 除去大部分乙酸,正丁醇和硫酸 除去残留的钠盐 上口 使用分水器分离酯化反应
生成的水,使平衡正向移动 分水器中的水层不再增加 50%
(4)反应到平衡后,各物质物质的量不会改变,所以当分水器中的水层不再增加,说明反应到终点。
(5)根据方程式分析,7.4g正丁醇和6.0g乙酸完全反应生成乙酸正丁酯的质量为11.6g,所以产率为
5.8g÷11.6g×100%= 50%。
17.氯化苄(C HCHCl)为无色液体,是一种重要的有机化工原料。现在实验室模拟工业上用甲苯与干燥氯气
6 5 2
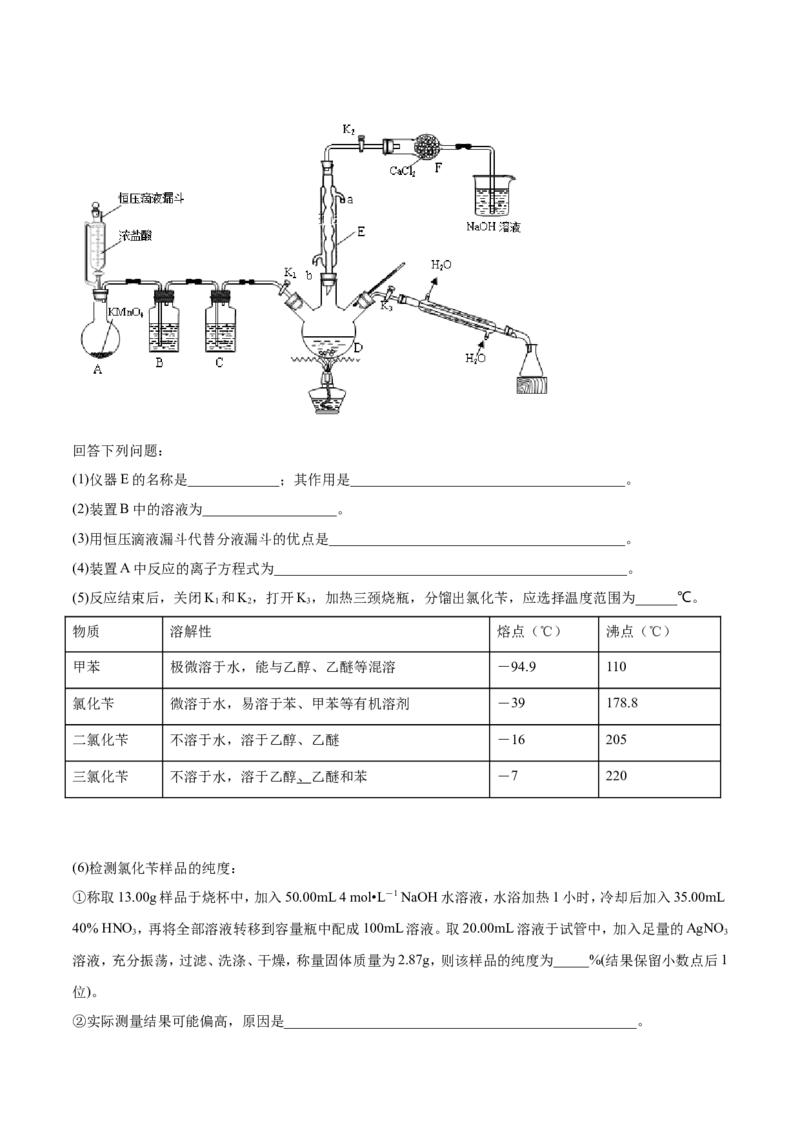
在光照条件下加热反应合成氯化苄、分离出氯化苄并检验样品的纯度,其装置(夹持装置略去)如图所示:回答下列问题:
(1)仪器E的名称是_____________;其作用是_______________________________________。
(2)装置B中的溶液为___________________。
(3)用恒压滴液漏斗代替分液漏斗的优点是__________________________________________。
(4)装置A中反应的离子方程式为__________________________________________________。
(5)反应结束后,关闭K 和K,打开K,加热三颈烧瓶,分馏出氯化苄,应选择温度范围为______℃。
1 2 3
物质 溶解性 熔点(℃) 沸点(℃)
甲苯 极微溶于水,能与乙醇、乙醚等混溶 -94.9 110
氯化苄 微溶于水,易溶于苯、甲苯等有机溶剂 -39 178.8
二氯化苄 不溶于水,溶于乙醇、乙醚 -16 205
三氯化苄 不溶于水,溶于乙醇、乙醚和苯 -7 220
(6)检测氯化苄样品的纯度:
①称取13.00g样品于烧杯中,加入50.00mL 4 mol•L-1 NaOH水溶液,水浴加热1小时,冷却后加入35.00mL
40% HNO ,再将全部溶液转移到容量瓶中配成100mL溶液。取20.00mL溶液于试管中,加入足量的AgNO
3 3
溶液,充分振荡,过滤、洗涤、干燥,称量固体质量为2.87g,则该样品的纯度为_____%(结果保留小数点后1
位)。
②实际测量结果可能偏高,原因是__________________________________________________。【答案】球形冷凝管 导出Cl、HCl气体,冷凝回流甲苯 饱和食盐水 使漏斗与烧瓶内压强一致,液
2
体顺利流下 2MnO -+10Cl-+16H+=2Mn2++5Cl↑+8H O 178.8-205 97. 3 样品混有二氯化苄、三氯化
4 2 2
苄等杂质
126.5g 143.5g
xg 2.87
x=12.65g
样品纯度为 97.3%,
二氯化苄、三氯化苄中氯元素的质量分数大于氯化苄,样品若混有二氯化苄、三氯化苄等杂质会使测量结果
偏高。
18.硼位于ⅢA族,三卤化硼是物质结构化学的研究热点,也是重要的化工原料。三氯化硼(BCl )可用于制取
3
乙硼烷(B H),也可作有机合成的催化剂。
2 6
[查阅资料] ①BCl 的熔点为-107.3 ℃,沸点为12.5 ℃;②2B+6HCl 2BCl ↑+3H↑;③硼与铝的性质
3 3 2
相似,也能与氢氧化钠溶液反应。
[设计实验] 某同学设计如图所示装置制备三氯化硼:
请回答下列问题:(1)常温下,可用高锰酸钾与浓盐酸发生的反应可替代A装置中的反应,请写出高锰酸钾与浓盐酸反应的离
子方程式:_______________________________________________。
(2)E装置的作用是________________________________。如果拆去B装置,可能的后果是
______________________________________________________________________。
(3)三氯化硼遇水剧烈反应生成硼酸(H BO)和白雾,写出该反应的化学方程式
3 3
______________________________________________________。实验室保存三氯化硼的注意事项是
___________________________________。
(4)实验中可以用一个盛装____________________(填试剂名称)的干燥管代替F和G装置,使实验更简便。
(5)为了顺利完成实验,正确的操作是_____(填序号)。
①先点燃A处酒精灯,后点燃D处酒精灯 ②同时点燃A、D处酒精灯 ③先点燃D处酒精灯,后点燃A
处酒精灯
(6)请你补充完整下面的简易实验,以验证制得的产品中是否含有硼粉:取少量样品于试管中,滴加浓
________________(填化学式)溶液,若有气泡产生,则样品中含有硼粉;若无气泡产生,则样品中无硼粉。
【答案】2MnO -+10Cl-+16H+ = 2Mn2++8HO+5Cl↑ 冷却和收集三氯化硼 硼粉与HCl反应生成的
4 2 2
氢气与氯气混合,加热时易发生爆炸 BCl +3HO=HBO+3HCl↑ 隔绝空气,密封保存 碱石灰
3 2 3 3
① NaOH
(3)三氯化硼遇水剧烈反应生成硼酸(H BO)和白雾,该反应的化学方程式是BCl +3HO=HBO+3HCl↑;因
3 3 3 2 3 3
此在实验室保存三氯化硼的注意事项要隔绝空气,密封保存,防止受潮水解;
(4)为防止BCl 水解在E与G之间连接一个盛有浓硫酸的装置;G装置中NaOH溶液吸收多余的Cl,防止
3 2
污染大气;在实验中也可以用一个盛装碱石灰的干燥管代替F和G装置,碱石灰既能吸收HO(g)又能吸收
2
Cl,使实验更简便;
2
(5)①先点燃A处酒精灯,待整套装置中都充满Cl 后再点燃D处酒精灯,使之发生反应,正确;②若先点燃
2
D处酒精灯,这时B就与装置中的空气发生反应得到B O,再点燃A处酒精灯产生的BCl 产率和纯度降低,
2 3 3
错误;③同时点燃A、D处酒精灯也会导致产生B O,影响制备BCl ;答案选①。
2 3 3
(6)由于B的性质与Al相似,既能与强酸反应,也能与强碱反应放出氢气,所以取少量样品于试管中,滴加浓NaOH溶液,若有气泡产生,则样品中含有硼粉。
19.铝氢化钠(NaAlH )是有机合成的重要还原剂,其合成线路如下图所示:
4
(1)制备无水AlCl 实验装置如下,已知AlCl 易升华(178℃),在潮湿空气中易水解。
3 3
实验时应先点燃________(填“A”或“D”)处酒精灯。装置F的作用是________________________。
(2)制取铝氢化钠的化学方程式是___________________________________。
(3)铝氢化钠样品性质探究和纯度测定。已知铝氢化钠样品中仅含有少量杂质NaH,NaH也会与水反应。
①铝氢化钠与水反应的化学方程式为__________________;
②取少量上述样品,滴加足量的水,向反应后的溶液中逐滴滴加盐酸并振荡,直至盐酸过量。滴加盐酸过程中
可观察到的现象是__________________。
③称取1.56g上述样品与水完全反应后,测得气体在标准状况下的体积为2240mL,样品中铝氢化钠的质量
分数为_________%(结果保留两位有效数字)。若实验室用如下两种装置分别测定生成气体的体积(其他操作
一致),用甲装置测得铝氢化钠的含量________________乙装置。(填“大于”、“小于”或“等于”)。
【答案】A 吸收未反应的氯气,防止空气中的水蒸气进入装置或防止AlCl 水解
3
AlCl +4NaH=NaAlH +3NaCl NaAlH +4H O = NaAl(OH) +4H ↑(或 NaAlH +2H O = NaAlO +4H ↑) 开
3 4 4 2 4 2 4 2 2 2
始没有沉淀,后产生白色沉淀,最终白色沉淀完全溶解(现象不全面不得分) 69 大于②NaH与水反应生成了NaOH和H,铝氢化钠与水反应生成了偏铝酸钠和H,向反应后的溶液中逐滴滴加
2 2
盐酸并振荡,盐酸先与氢氧化钠溶液发生中和,开始没有沉淀,然后盐酸与偏铝酸钠溶液反应生成氢氧化铝
白色沉淀,继续滴加盐酸,氢氧化铝与盐酸反应,白色沉淀完全溶解,故答案为:开始没有沉淀,后产生白色
沉淀,最终白色沉淀完全溶解。
③由于两种物质均能与水反应生成氢气,因此可以通过测量氢气的体积计算纯度。设样品中铝氢化钠的物质
的量是xmol,NaH是ymol,则54x+24y=1.56、4x+y=2.24L/22.4L/mol,解得x=0.02,所以样品中铝氢化钠
的质量分数为0.02mol×54g/mol÷1.56g×100%=69%;
利用甲装置进行反应时,产生的氢气与装置内的气体都进入量气管中,测量出氢气的体积偏大,测得铝氢化
钠的含量偏高,乙装置中外接一个橡皮管,平衡大气压,避免了装置内的气体对氢气体积测定的影响,故答案
为:69,大于。
20.叠氮化钠(NaN )是汽车安全气囊最理想的气体发生剂原料。工业水合肼法制备叠氮化钠的工艺流程如
3
图所示:
已知:NaN 能与AgNO 反应生成白色难溶于水的AgN ;部分相关物质的物理性质如下表:
3 3 3
熔点℃ 沸点℃ 溶解性
CHOH −97 64.7 与水互溶
3
水合肼
−51.7 118.5 与水、醇互溶,不溶于乙醚和氯仿
(N H•H O)
2 4 2
亚硝酸甲酯 −17 −12 溶于乙醇、乙醚(CHONO)
3
请回答:
(1)步骤Ⅰ中NaNO 与稀硫酸发生副反应生成两种气体(其中一种气体在空气中可以转化为产物中的另一
2
种气体)的离子方程式为_________________________;步骤Ⅱ中生成NaN 的化学方程式为
3
______________________。
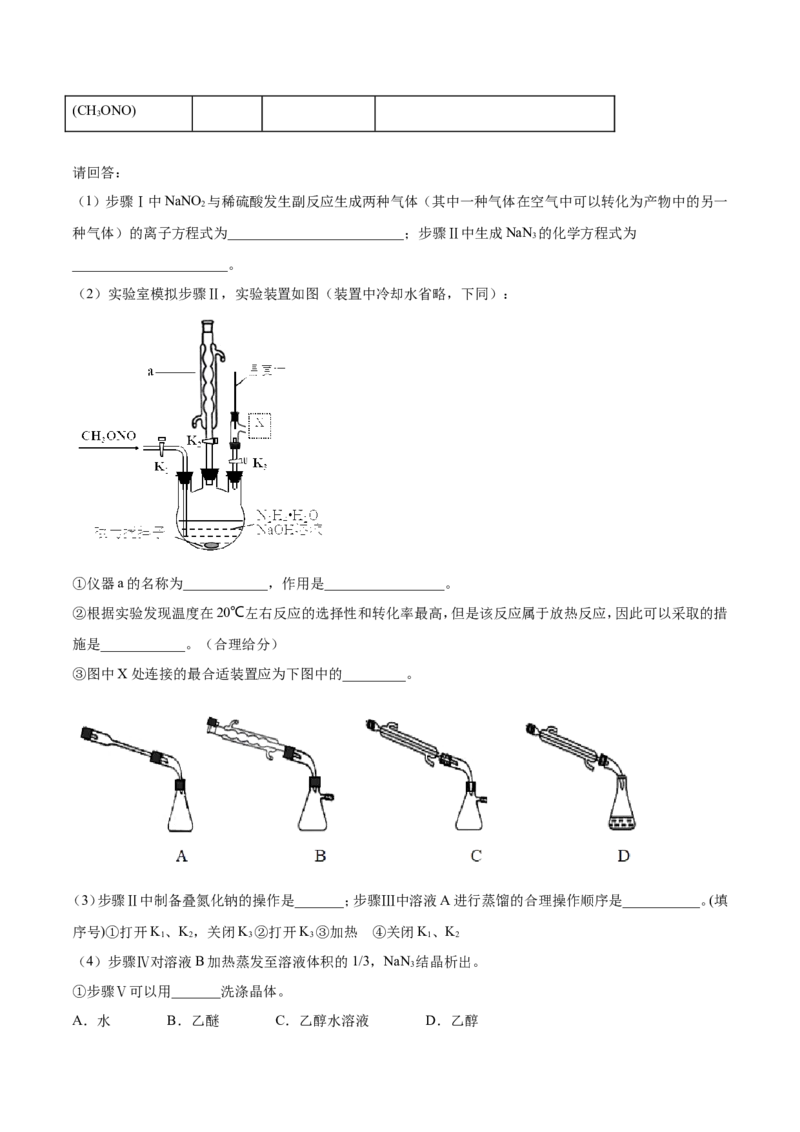
(2)实验室模拟步骤Ⅱ,实验装置如图(装置中冷却水省略,下同):
①仪器a的名称为____________,作用是_________________。
②根据实验发现温度在20℃左右反应的选择性和转化率最高,但是该反应属于放热反应,因此可以采取的措
施是____________。(合理给分)
③图中X处连接的最合适装置应为下图中的_________。
(3)步骤Ⅱ中制备叠氮化钠的操作是_______;步骤Ⅲ中溶液A进行蒸馏的合理操作顺序是___________。(填
序号)①打开K、K,关闭K ②打开K ③加热 ④关闭K、K
1 2 3 3 1 2
(4)步骤Ⅳ对溶液B加热蒸发至溶液体积的1/3,NaN 结晶析出。
3
①步骤Ⅴ可以用_______洗涤晶体。
A.水 B.乙醚 C.乙醇水溶液 D.乙醇②沉淀滴定法测定产品纯度,是以淡黄色KCrO 溶液作指示剂,将AgNO 标准溶液滴入样品溶液,至少量
2 4 3
Ag CrO 出现(即析出橘红色沉淀),达到滴定终点。AgNO 溶液要装在棕色的酸式滴定管里进行滴定,理由
2 4 3
是__________。下列操作合理的是______。
A.滴定管管尖不可接触锥形瓶内壁
B.滴定时滴液速度应先快后慢,接近终点时一滴一摇
C.滴定过程中可用蒸馏水将锥形瓶壁上粘附的溶液冲下
D.若未等滴定管液面稳定就读数,会导致测定结果偏高
E.若发现AgNO 溶液滴加过量,可回滴样品溶液,至红色褪去
3
【答案】2NO ‾ + 2H+ = NO↑+ NO↑+ H OCH ONO + N H + NaOH =(箭头也行)NaN + CHOH + 2H O或
2 2 2 3 2 4 3 3 2
CHONO + N H∙HO + NaOH =(箭头也行)NaN + CHOH + 2H O球形冷凝管冷凝回流,平衡气压20℃冷水
3 2 4 2 3 3 2
浴 或 缓慢通入气体等C①④②③ 或 ②④③DAgNO 溶液显酸性,且见光易分解BCD
3
【解析】 (1) 步骤Ⅰ中NaNO 与稀硫酸发生副反应生成两种气体,其中一种气体在空气中可以转化为产物中
2
的另一种气体,说明两种气体分别为一氧化氮和二氧化氮,则离子方程式为: 2NO ‾ + 2H+ = NO↑+ NO↑+
2 2
HO; 步骤Ⅱ中CHONO在氢氧化钠和肼反应生成NaN ,从后面的流程分析,产物还有甲醇,反应方程式为:
2 3 3
CHONO + N H + NaOH =NaN + CHOH + 2H O或 CHONO + N H∙HO + NaOH =NaN + CHOH + 2H O。
3 2 4 3 3 2 3 2 4 2 3 3 2
(2) ①仪器a为球形冷凝管。该冷凝管的作用为冷凝回流,平衡气压。②实验发现温度在20℃左右反应的选择
性和转化率最高,但是该反应属于放热反应,所以要控制反应的温度尽量在20℃左右,或使反应慢慢进行,
减少因反应放热温度的升高,故答案为: 20℃冷水浴或缓慢通入气体等。③X应连接冷凝管且应为直形冷凝
管,不能用球形冷凝管,避免产物的残留,故选C。(3)步骤Ⅱ中制备叠氮化钠的操作打开K 通入亚硝酸甲酯,
1
打开K 与大气相通,并使由于反应热而变成气体的反应物冷凝成液体流回烧瓶,同时要关闭K,故选①;步
2 3
骤Ⅲ中溶液A进行蒸馏的合理操作为关闭K、K,打开K,对烧瓶进行加热,顺序是④②③ 或 ②④③。(4)
1 2 3
①根据亚硝酸甲酯的物理性质中能溶于乙醇、乙醚,水合肼与水或醇互溶,不溶于乙醚和氯仿,所以应选项乙
醇对产品进行洗涤,故选D。 ②AgNO 溶液显酸性,且见光易分解,所以选择使用棕色的酸式滴定管。A.在
3
滴定终点是,滴定管管尖可接触锥形瓶内壁,可使滴定管流出的液体充分反应,故错误;B.滴定时滴液速度
应先快后慢,接近终点时一滴一摇,保证准确控制滴定终点,故正确;C.滴定过程中可用蒸馏水将锥形瓶壁
上粘附的溶液冲下,使溶液间充分反应,准确确定滴定终点,故正确;D.若未等滴定管液面稳定就读数,滴定
终点读数变大,则滴定消耗的体积变大,会导致测定结果偏高,故正确;E.若发现AgNO 溶液滴加过量,不可
3
回滴样品溶液,滴定的数据错误,实验作废,故错误。故选BCD。
21.作为工业生产的催化剂和制备纳米MgO的材料,草酸镁(MgC O·2H O)有着广阔的应用和发展前景。回
2 4 2
答下列问题:(1)MgC O·2H O的制备
2 4 2
已知氯化镁、草酸铵、草酸镁在水中的溶解度如下表:
氯化镁 草酸铵 草酸镁
20℃ 54.6g 4.45g
70℃ 61.0g 22.4g 微溶
100℃ 73.3g 34.7g
实验方法:(i)加热煮沸蒸馏水,取300mL冷却至70℃,加140g MgCl ·6H O,此制MgCl 溶液;
2 2 2
(ii)按照图示装置装好药品,连接好装置;
(iii)在磁力加热搅拌的情况下,缓缓滴入饱和(NH )C O 溶液,并水浴加热,直至不再产生白色沉淀为止;
4 2 2 4
(iv)分离沉淀、洗涤,得MgC O·2H O晶体。
2 4 2
①装置中仪器甲的名称是_____,其冷水进水口为_____填“a”或“b”)。
②仪器乙中c部位的作用是____________________。
③检验产品洗涤干净的方法是________________。
(2)MgC O·2H O分解产物的探究
2 4 2
利用下图所示装置探究MgC O·2H O分解产物CO、CO 等的性质。
2 4 2 2①A中发生反应的化学方程式为______________________。
②装置B中盛装的药品是_____,装置C的作用是______,装置D中的试剂是______,装置G中的现象是
____________________。
【答案】 球形冷凝管 a 保持漏斗内部压强与反应器内的压强相等,使乙中液体顺利流下 取洗涤后溶液,
滴加稀HNO 酸化的AgNO 溶液,若无白色沉淀,则洗涤干净 MgC O·2H O =MgO+CO ↑+CO↑+2H O 无
3 3 2 4 2 2 2
水CuSO 检验产物CO (浓)NaOH溶液 黑色固体变红
4 2
【解析】(1)由题中信息可知,该实验用氯化镁溶液与草酸铵溶液通过复分解反应制备草酸镁。
①装置中仪器甲的名称是球形冷凝管,为保证其冷凝效果,其冷水进水口为a。
②仪器乙为滴液漏斗,其中c部位的作用是保持漏斗内部压强与反应器内的压强相等,使乙中液体顺利流下。
③产品表面会吸附氯化铵,Cl-较易检验,所以,检验产品洗涤干净的方法就是检验洗涤液中是否还有Cl-,具
体操作是:取洗涤后溶液,滴加稀HNO 酸化的AgNO 溶液,若无白色沉淀,则洗涤干净。
3 3
22.氮化铝(AlN)是一种性能优异的新型材料,在许多领域有广泛应用,前景广阔。某化学小组模拟工业制氮化
铝原理,欲在实验室制备氮化铝并检验其纯度。
查阅资料:①实验室用饱和NaNO 与NH Cl溶液共热制N:NaNO +NHCl NaCl+N↑+2H O。
2 4 2 2 4 2 2
②工业制氮化铝:Al O+3C+N 2AlN+3CO,氮化铝在高温下能水解。
2 3 2
③AlN与NaOH饱和溶液反应:AlN+NaOH+H O NaAlO +NH↑。
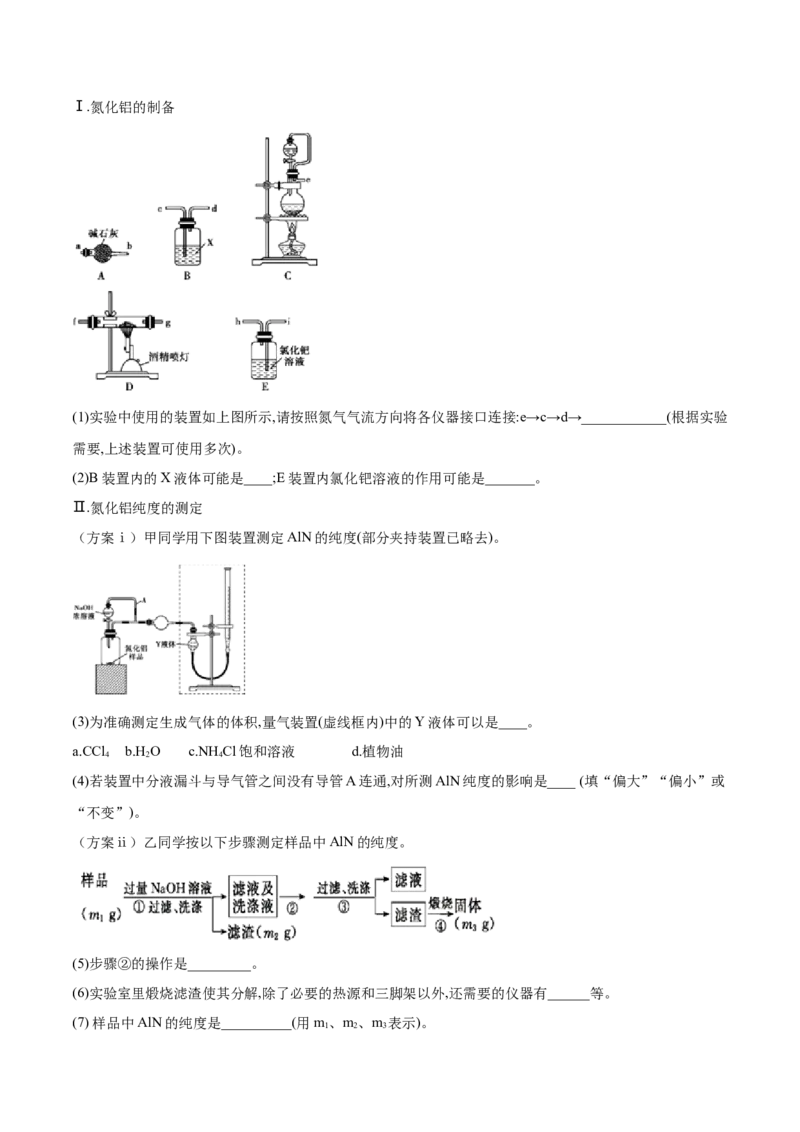
2 2 3Ⅰ.氮化铝的制备
(1)实验中使用的装置如上图所示,请按照氮气气流方向将各仪器接口连接:e→c→d→____________(根据实验
需要,上述装置可使用多次)。
(2)B装置内的X液体可能是____;E装置内氯化钯溶液的作用可能是_______。
Ⅱ.氮化铝纯度的测定
(方案ⅰ)甲同学用下图装置测定AlN的纯度(部分夹持装置已略去)。
(3)为准确测定生成气体的体积,量气装置(虚线框内)中的Y液体可以是____。
a.CCl b.H O c.NH Cl饱和溶液 d.植物油
4 2 4
(4)若装置中分液漏斗与导气管之间没有导管A连通,对所测AlN纯度的影响是____ (填“偏大”“偏小”或
“不变”)。
(方案ⅱ)乙同学按以下步骤测定样品中AlN的纯度。
(5)步骤②的操作是_________。
(6)实验室里煅烧滤渣使其分解,除了必要的热源和三脚架以外,还需要的仪器有______等。
(7) 样品中AlN的纯度是__________(用m、m、m 表示)。
1 2 3【答案】a→b→f(g)→g(f)→a(c)→b(d)→I浓硫酸吸收CO,防止污染ad偏大通入过量CO 气体坩埚、泥三角、坩
2
埚钳 ×100%
(3) AlN+NaOH+H O= NaAlO +NH↑,量气装置中收集的气体为氨气。a.氨气是极性分子,难溶于CCl ,可以
2 2 3 4
选用;b.氨气极易溶于水,不能选用;c.氨气在NH Cl饱和溶液中溶解度仍然很大,不能选用;d.氨气难溶于植
4
物油,可以选用;故选ad;
(4)若装置中分液漏斗与导气管之间没有导管A连通,,应用氢氧化钠溶液体积的影响会使得测得的氨气的
体积偏大,所测AlN纯度偏大,故答案为:偏大;
(5)根据流程图,滤液即洗涤液中含有NaAlO ,经过步骤②得到沉淀为氢氧化铝,因此步骤②是通入过量CO
2 2
气体,故答案为:通入过量CO 气体;
2
(6)实验室里煅烧滤渣氢氧化铝使其分解,除了必要的热源和三脚架以外,还需要的仪器有坩埚、泥三角、坩
埚钳,故答案为:坩埚、泥三角、坩埚钳;
(7)根据Al O+3C+N 2AlN+3CO,AlN+NaOH+H O= NaAlO +NH↑,样品的主要成分为Al O、C和 AlN,
2 3 2 2 2 3 2 3
滤渣为C,最终的固体为Al O, 样品中AlN的纯度为
2 3
×100%,故答案为: ×100%。
23.二氯二氢硅(SiHC1 )常作于外延法工艺中重要的硅源。易燃、有毒,与水接触易水解,沸点8.2℃。在铜催
2 2化作用下,HCl 与硅在250-260℃反应可以制得SiHCl.
2 2
(1) 利用浓硫酸、浓盐酸为原料,选用A 装置制取HC1,利用了浓硫酸的_______性。
(2)D 装置中生成 二氯二氢硅的化学方程式为___________________。
(3) 按照气体从左到右方向,制取SiHCl 的装置连接次序为
2 2
a→___→___→f→g→___→___→____→_____(填仪器接口的字母,其中装置C 用到2 次).其中装置B 的作用
是____;前面装置C 中装的药品为______,后面装置C的作用为____________。
(4)新的制取SiHCl 方法是: 往硅粉中先通入Cl 在300-350℃反应生成SiCl ,然后再与HCl 在250-260℃反应,
2 2 2 4
可以大大提高产率。如果通入气体次序相反,产率会降低,其原因是__________(用化学方程式表示).
【答案】 吸水 Si+2HCl SiHCl; d e b c d e 收集 SiHCl 无水 CaCl 除去多余 HCl,以免
2 2 2 2 2
污染环境,同时吸收空气中的水,以免与 SiHCl 反应 SiHCl+2Cl SiCl +2HCl
2 2 2 2 2 4
【解析】(1)利用浓硫酸、浓盐酸为原料,浓硫酸有吸水性,使浓盐酸更易挥发出HCl,故答案为:吸水;
(2)D装置中生成二氯二氢硅的化学方程式为Si+2HCl SiHCl,故答案为:Si+2HCl
2 2
SiHCl;
2 224.氢化铝锂(IiAlH)是有机合成中的重要还原剂。某课题组设计实验制备氢化铝锂并测定其纯度。已知: 氢
4
化铝锂、氢化锂遇水都剧烈反应,并产生同一种气体。
回答下列问题:
I.制备氢化锂(IiH)
选择图1中的装置制备氢化锂(必要时可重复使用):
(1)装置D中NaOH溶液的作用是________________________________________。
(2)装置的连接顺序(从左至石)为A→__________________________________。
(3)检验好装置的气密性,点燃酒精灯前需进行的实验操作是____________________________________。
II.制备氢化铝理
1947 年,Schlesinger、Bond 和Finholt首次制得氢化铝理,其方法是使氢化锂与无水三氯化铝按定比例在乙醚
中混合,搅拌,充分反应后,经一系列操作得到LiAlH 晶体。
4
(4)将乙醚换为去离子水是否可行,请简述理出:____________________________________。
(5)氢化锂与无水三氯化铝反应的化学方程式为___________________________________。
III.测定氢化铝锂产品(不含氢化锂)的纯度。(6)按图2装配仪器、检查装置气密性并装好约品(Y形管中的蒸馏水足量,为了避免氢化铝锂遇水发生爆炸,
蒸馏水中需掺入四氢呋喃作稀释剂),启动反应的操作是_________________。读数之前,上下移功量气管在
右侧的容器,使量气管左、右两侧的液面在同一水平而上,其目的是___________________________。
(7)标准状况下,反应前量气管读数为VmL,反应完毕并冷却之后,量气管读数为VmL。该样品的纯度为
1 2
_____________________(用含a、V、V 的代数式表示)。若起始读数时俯视刻度线,测得的结果将
1 2
___________(填“偏高”“偏低”或“无影响”)。
【答案】 除去H 中混有的HS DBCBE 打开装置A中分液漏斗的活塞和玻璃塞,一段时间后,用小试管在
2 2
装置E的水槽中收集气体并验纯 不可行,因为氢化铝锂、氢化锂遇水都剧烈反应
4LiH+ AlCl ==LiAlH + 3LiC1 倾斜Y形管,将蒸馏水注入ag产品中 使量气管内气体的压强与大气压强相
3 4
等 {[19(V –V)]/448a}% 偏高
2 1
锂遇水发生爆炸,蒸馏水中需掺入四氢呋喃作稀释剂,启动反应的操作是倾斜Y形管,将蒸馏水注入ag产品
中;读数之前,上下移功量气管在右侧的容器,使量气管左、右两侧的液面在同一水平而上,其目的是使量气
管内气体的压强与大气压强相等;(7)根据反应 LiAlH +2H O==4H ↑+ LiAlO 可知,样品的纯度为
4 2 2 2(V V )103L 1
2 1 38g/mol 19V V ;若起始读数时俯视刻度线,测得体积读数偏
22.4L/mol 4 100% 2 1 %
ag 448a
大,测定结果将偏高。
25.2017年10月27日,世界工生组织国际癌症研究机构将三氯乙醛划为2A类致癌物,但它可用于生产氯霉
素、合霉素等。某探究小组模拟备三氯乙醛自实验装置如图所示(夹持、加热装置均略去)。
已知:C HOH+4Cl =CCl CHO+5HCl,副反应是C HOH+HCl=C HCl+H 0。
2 5 2 3 2 5 2 5 2
容下列问题:
(1)写出装置A中发生反应的化学方程式:__________________。
(2)仪器b中冷凝水从________(填“p”或“q”,下同 )口进,______口出。
(3)进入装置D的是纯净、干燥的Cl,则装置B中的试剂为_____,装置C中的试剂为____。若撤去装置B,
2
对实验的影响是____________________。
(4)实验时发现D中导管口处气泡速率过快,合理的解决方法是__________________。
(5)已知:CCl CHO +OH-=CHCl +HC00-; HC00-+I =H++2I-+CO ↑ I+2S O2-=2I-+S O2-
3 3 2 2 2 2 3 4 6
称取0.40g产品,配成待测溶液,加入20.00mL0.100mol/L碘标准溶液,再加入适量NaC0 溶液,反应完全后,
2 3
加盐酸调节溶液的pH,并立即用0.020mol/L的NaSO 溶液滴定至终点。重复上述操作3次,平均消耗
2 2 3
NaSO 溶液20.00mL。滴定时所用指示剂是_______,达到滴定终点的现象是______,测得产品的纯度为
2 2 3
____________________。
【答案】 MnO +4HCl(浓) MnCl +Cl↑+2H O p q 饱和食盐水 浓HSO 氯化氢杂质与乙醇反应,生
2 2 2 2 2 4
成氯乙烷,导致三氯乙醛的纯度降低 停止对A加热(或控制滴加1盐酸量等合理答案) 淀粉溶液 蓝色变
为无色,且半分钟内不变色 66.4% (或66.375%)
【解析】(1)二氧化锰与浓盐酸加热反应生成氯气;正确答案:MnO +4HCl(浓) MnCl + Cl ↑+2H O。
2 2 2 2
(2)为保证冷凝效果,采用逆流原理,仪器b中冷凝水从p口进,q口出;正确答案:p、q。
(3)氯气含有氯化氢和水蒸气,因此混合气体先通过饱和食盐水,除去氯化氢,然后再通过浓硫酸,吸收水蒸气,最后的得到纯净的氯气;若没有装置B,氯化氢会与乙醇反应生成氯代烃,发生了副反应,影响三氯乙醛
的纯度;正确答案:饱和食盐水;浓HSO ;氯化氢杂质与乙醇反应,生成氯乙烷,导致三氯乙醛的纯度降低。
2 4
点睛:(5)进行计算时,加入20.00mL0.100mol/L碘标准溶液一部分来氧化溶液中HC00-,剩余的碘,用
0.020mol/L的NaSO 溶液进行滴定,这样产生的差值即为氧化HC00-消耗碘的量,再根据方程式进行后续计
2 2 3
算。