文档内容
专题 16 物质结构与性质综合题
(本卷共20小题,满分100分,考试用时75分钟)
可能用到的相对原子质量:H 1 Li 7 B 11 C 12 N 14 O 16 Na 23 Mg 24 Al 27 S 32 Cl 35.5
第I卷 (选择题共50分)
一、选择题:本题共10个小题,每小题3分,共30分,在每小题给出的四个选项中,只有一项是符
合题目要求的。
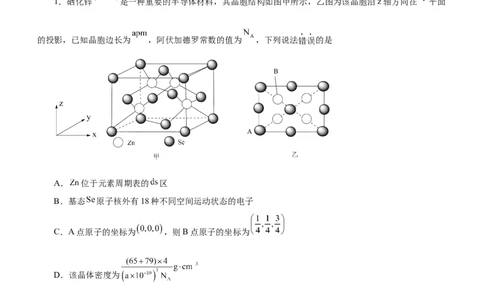
1.硒化锌 是一种重要的半导体材料,其晶胞结构如图甲所示,乙图为该晶胞沿z轴方向在 平面
的投影,已知晶胞边长为 ,阿伏加德罗常数的值为 ,下列说法错误的是
A. 位于元素周期表的 区
B.基态 原子核外有18种不同空间运动状态的电子
C.A点原子的坐标为 ,则B点原子的坐标为
D.该晶体密度为
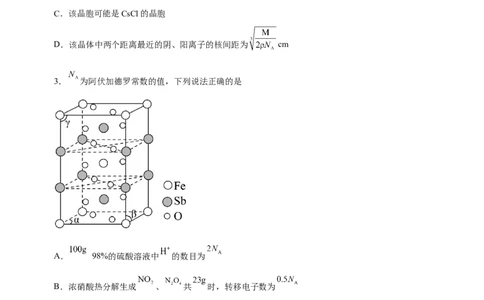
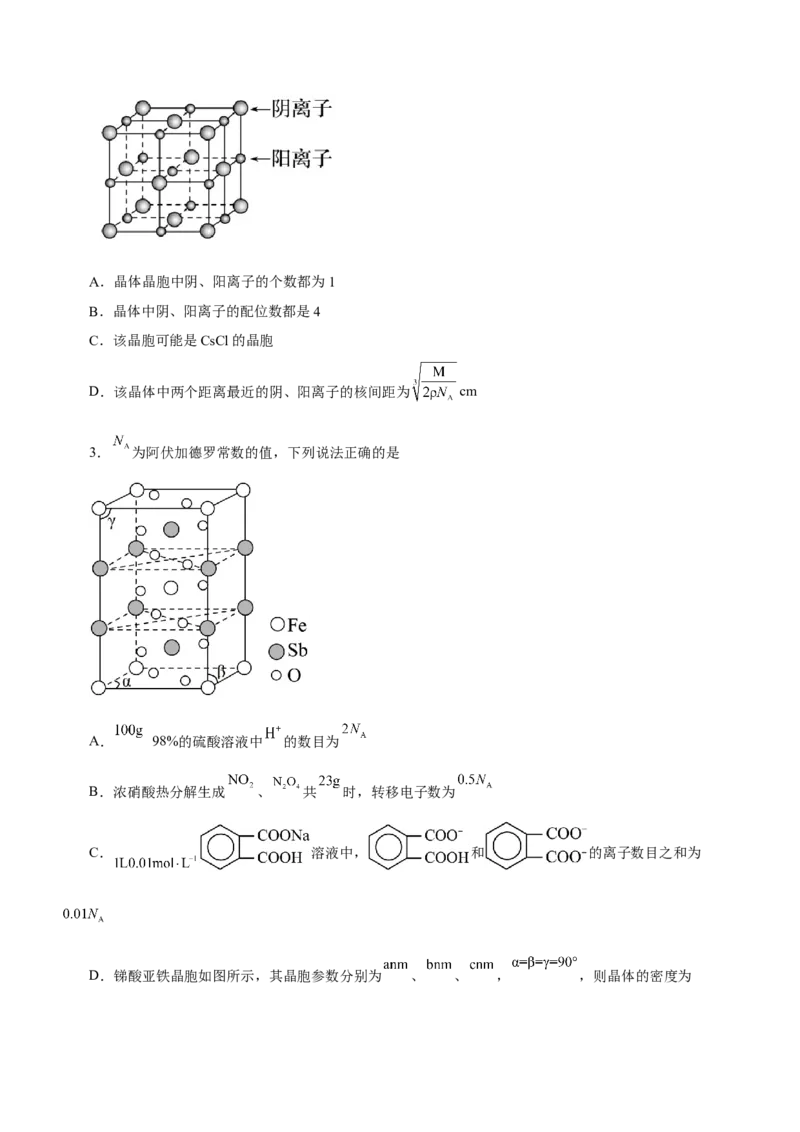
2.已知某离子晶体的晶胞示意图如图所示,其摩尔质量为Mg·mol-1,阿伏加德罗常数的值为N ,晶体的
A
密度为ρg·cm-3,下列说法中正确的是A.晶体晶胞中阴、阳离子的个数都为1
B.晶体中阴、阳离子的配位数都是4
C.该晶胞可能是CsCl的晶胞
D.该晶体中两个距离最近的阴、阳离子的核间距为 cm
3. 为阿伏加德罗常数的值,下列说法正确的是
A. 98%的硫酸溶液中 的数目为
B.浓硝酸热分解生成 、 共 时,转移电子数为
C. 溶液中, 和 的离子数目之和为
D.锑酸亚铁晶胞如图所示,其晶胞参数分别为 、 、 , ,则晶体的密度为4.氮、氧分别是空气中和地壳中含量最多的两种元素。下列说法正确的是
A.电负性:N>O B.活泼性:
C.第一电离能:N>O D.熔沸点:
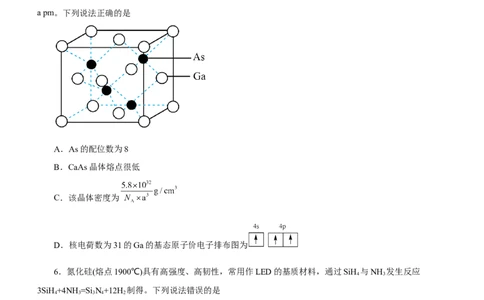
5.第二代半导体材料的代表物质GaAs,其晶胞结构如图所示,阿伏加德罗常数的值为 ,晶胞边长为
a pm。下列说法正确的是
A.As的配位数为8
B.CaAs晶体熔点很低
C.该晶体密度为
D.核电荷数为31的Ga的基态原子价电子排布图为
6.氮化硅(熔点1900℃)具有高强度、高韧性,常用作LED的基质材料,通过SiH 与NH 发生反应
4 3
3SiH+4NH=Si N+12H 制得。下列说法错误的是
4 3 3 4 2
A.键角:SiH>NH B.SiH 稳定性强于NH ,可证明非金属性N>Si
4 3 4 3
C.Si N 属于共价晶体 D.SiH 为由极性键构成的非极性分子
3 4 4
17.我国科学家成功创制了一种碳家族单晶新材料——单层聚合碳60,结构中每个C 与周围6个C 通
60 60
过碳碳共价键相连。下列有关说法错误的是
A.金刚石和C 均为分子晶体 B.C 中的12C中子数为6
60 60
C.石墨与单层聚合C 不属于同位素 D.单层聚合C 中存在非极性键
60 60
8.下列说法不正确的是A.石墨晶体中存在共价键与分子间作用力,属于混合型晶体
B.纯金属中加入其它元素会改变规则的层状排列,能增大金属硬度
C.液晶是液体和晶体聚集而成的一种特殊的混合物
D.NaCl和SiC晶体熔化时,克服粒子间作用力的类型不相同
9.下列关于CO 的说法不正确的是
2
A.CO 是由极性键形成的非极性分子 B.CO 分子中σ键与π键的数目比为1∶1
2 2
C.干冰中一个CO 分子周围有8个紧邻分子 D.CO 的大量排放可能引起温室效应
2 2
10.下列叙述中正确的是
A.NH 、CO、CO 都是极性分子 B.CH、CCl 均为含极性键的非极性分子
3 2 4 4
C.CS、HO、C H 都是直线型分子 D.HF、HCl、HBr、HI的稳定性依次增强
2 2 2 2
二、选择题:本题共5个小题,每小题4分,共20分。在每小题给出的四个选项中,只有一项或两项是
符合题目要求的。若正确答案只包括一个选项,多选时,该小题得0分;若正确答案包括两个选项,只选一个
且正确的得2分,选两个且都正确的得4分,但只要选错一个,该小题得0分。
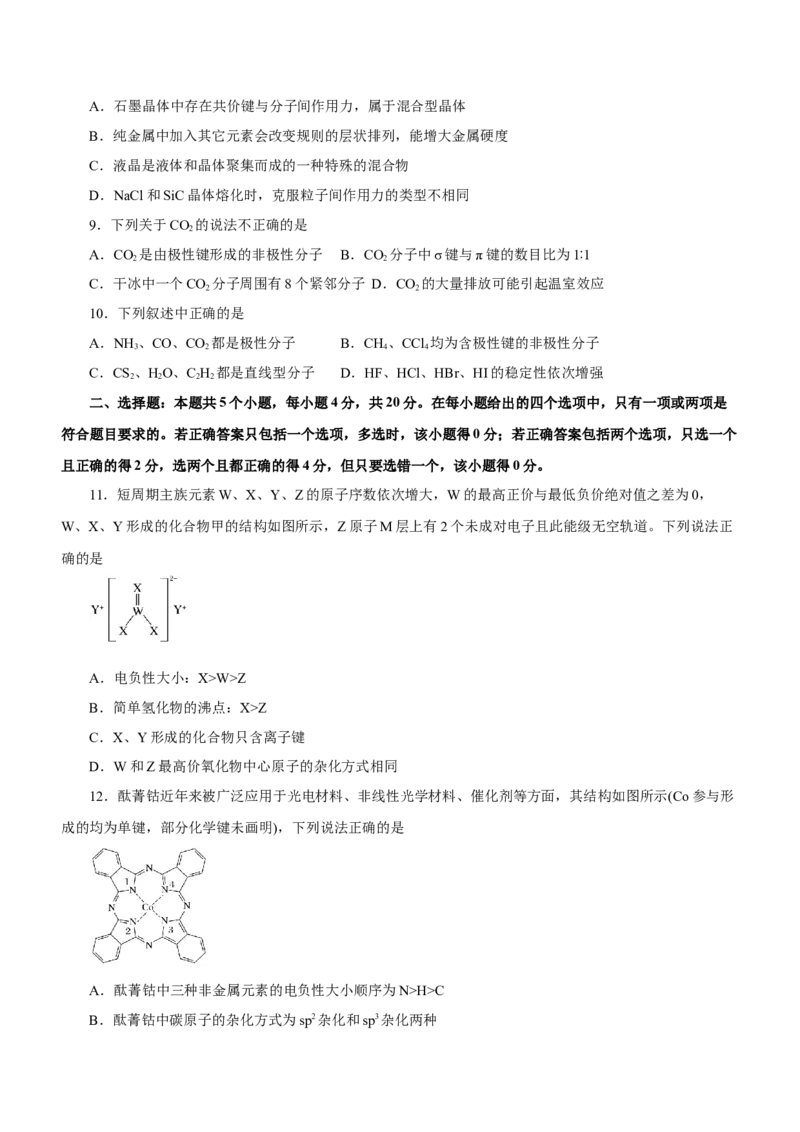
11.短周期主族元素W、X、Y、Z的原子序数依次增大,W的最高正价与最低负价绝对值之差为0,
W、X、Y形成的化合物甲的结构如图所示,Z原子M层上有2个未成对电子且此能级无空轨道。下列说法正
确的是
A.电负性大小:X>W>Z
B.简单氢化物的沸点:X>Z
C.X、Y形成的化合物只含离子键
D.W和Z最高价氧化物中心原子的杂化方式相同
12.酞菁钴近年来被广泛应用于光电材料、非线性光学材料、催化剂等方面,其结构如图所示(Co参与形
成的均为单键,部分化学键未画明),下列说法正确的是
A.酞菁钴中三种非金属元素的电负性大小顺序为N>H>C
B.酞菁钴中碳原子的杂化方式为sp2杂化和sp3杂化两种C.Co(Ⅱ)与4个氮原子之间通过配位键结合
D.2号和4号N原子分别与周围3个原子形成的空间结构为平面三角形
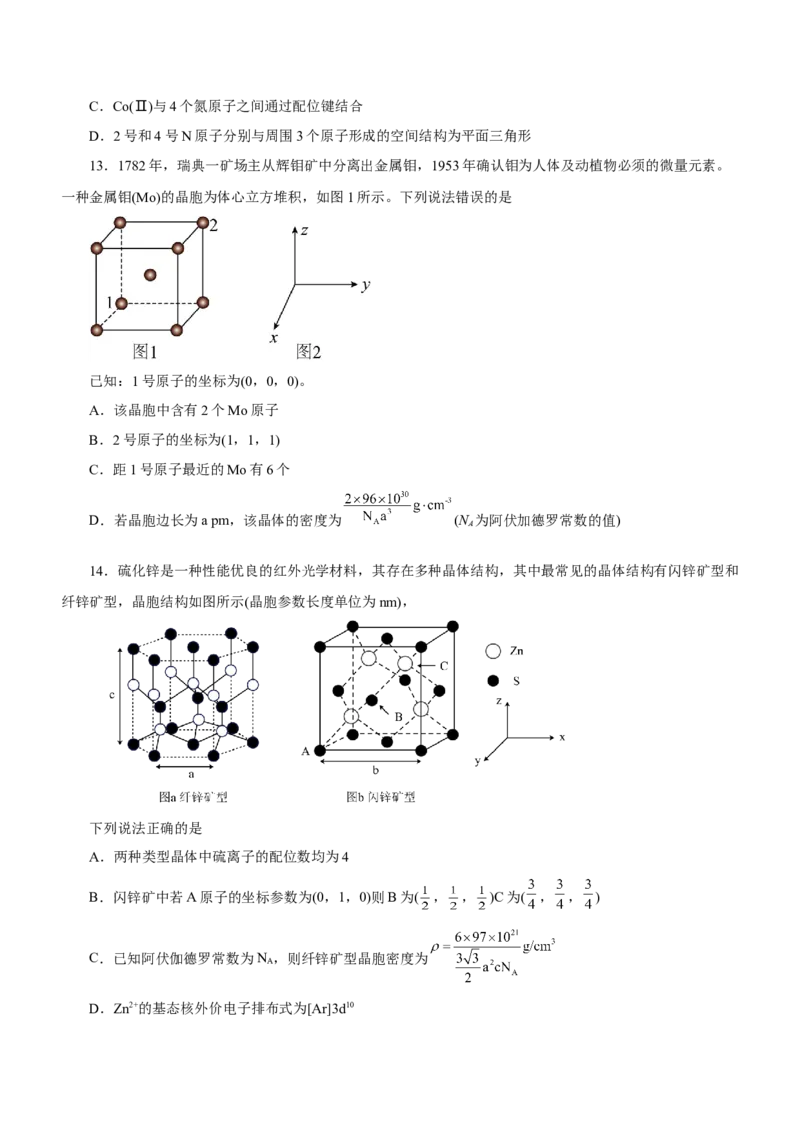
13.1782年,瑞典一矿场主从辉钼矿中分离出金属钼,1953年确认钼为人体及动植物必须的微量元素。
一种金属钼(Mo)的晶胞为体心立方堆积,如图1所示。下列说法错误的是
已知:1号原子的坐标为(0,0,0)。
A.该晶胞中含有2个Mo原子
B.2号原子的坐标为(1,1,1)
C.距1号原子最近的Mo有6个
D.若晶胞边长为a pm,该晶体的密度为 (N 为阿伏加德罗常数的值)
A
14.硫化锌是一种性能优良的红外光学材料,其存在多种晶体结构,其中最常见的晶体结构有闪锌矿型和
纤锌矿型,晶胞结构如图所示(晶胞参数长度单位为nm),
下列说法正确的是
A.两种类型晶体中硫离子的配位数均为4
B.闪锌矿中若A原子的坐标参数为(0,1,0)则B为( , , )C为( , , )
C.已知阿伏伽德罗常数为N ,则纤锌矿型晶胞密度为
A
D.Zn2+的基态核外价电子排布式为[Ar]3d1015. 能与悬浮在大气中的海盐粒子作用,反应为 (CINO各原子均达到8
电子稳定结构)。下列说法正确的是
A. 晶体属于分子晶体 B.ClNO的结构式为
C.NaCl晶胞中 的配位数为6 D. 是由极性键构成的非极性分子
第II卷 (非选择题共50分)
三、非选择题:本题共5个小题,共50分。
16.(10分)Wilson病是一种先天性铜代谢障碍性疾病,D-青霉胺具有排铜作用,用以治疗或控制
Wilson病症。D-青霉胺结构简式如图:
回答下列问题:
(1)写出Cu的简化电子排布式_______。
(2)已知气态基态原子得到一个电子形成气态基态负一价离子所产生的能量变化称为该元素原子的第一电
子亲合能(吸收能量为负值,释放能量为正值),试解释碳原子第一电子亲合能较大的原因_______。 第一电子
亲合能可能为正值或负值,而第二电子亲合能均为负值,原因是_______。
(3)D-青霉胺中,硫原子的VSEPR模型为_______,碳原子的杂化方式为_______。
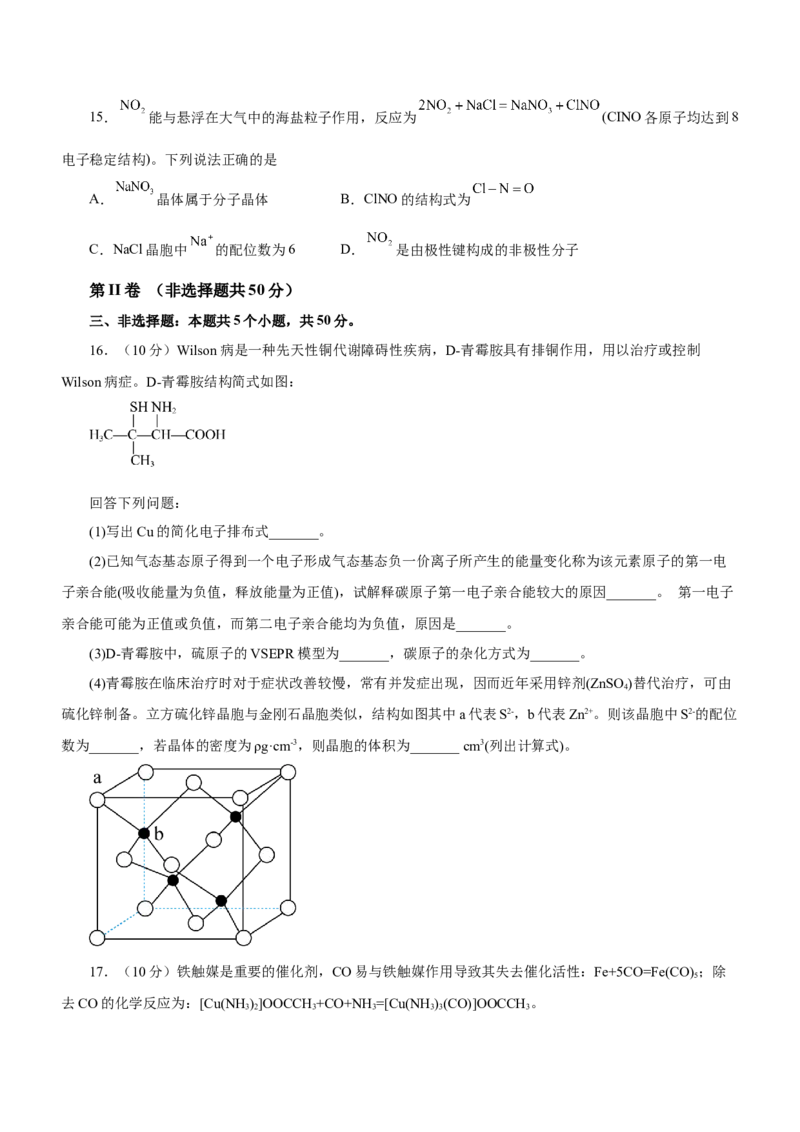
(4)青霉胺在临床治疗时对于症状改善较慢,常有并发症出现,因而近年采用锌剂(ZnSO)替代治疗,可由
4
硫化锌制备。立方硫化锌晶胞与金刚石晶胞类似,结构如图其中a代表S2-,b代表Zn2+。则该晶胞中S2-的配位
数为_______,若晶体的密度为ρg·cm-3,则晶胞的体积为_______ cm3(列出计算式)。
17.(10分)铁触媒是重要的催化剂,CO易与铁触媒作用导致其失去催化活性:Fe+5CO=Fe(CO) ;除
5
去CO的化学反应为:[Cu(NH )]OOCCH +CO+NH=[Cu(NH)(CO)]OOCCH 。
3 2 3 3 3 3 3(1)Fe(CO) 又名羰基铁,常温下为黄色油状液体,则Fe(CO) 的晶体类型是____。
5 5
(2)NH 的空间构型为____,NH 极易溶于水,除了因为NH 是极性分子外还因为____。
3 3 3
(3)配合物[Cu(NH )]OOCCH 中碳原子的杂化类型是____,配位体中提供孤对电子的原子是____。
3 2 3
(4)用[Cu(NH )]OOCCH 除去CO的反应中,肯定有形成____。
3 2 3
a.离子键 b.配位键 c.非极性键 d.σ键
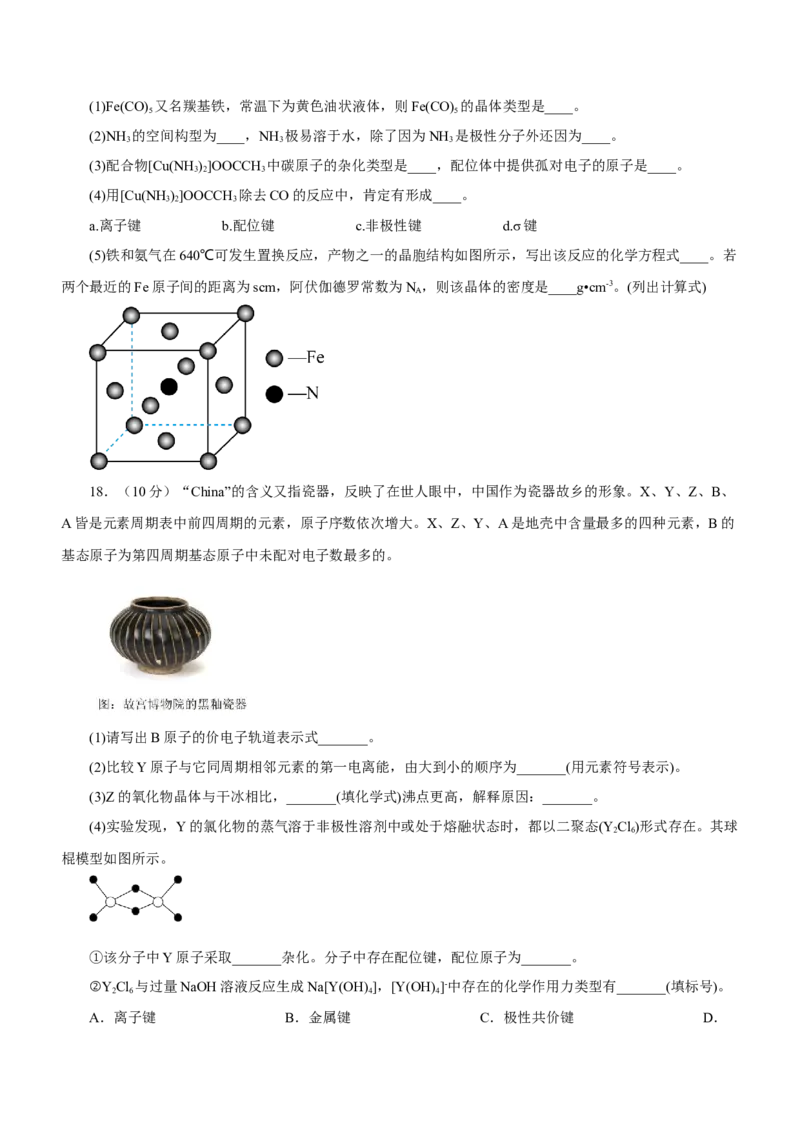
(5)铁和氨气在640℃可发生置换反应,产物之一的晶胞结构如图所示,写出该反应的化学方程式____。若
两个最近的Fe原子间的距离为scm,阿伏伽德罗常数为N ,则该晶体的密度是____g•cm-3。(列出计算式)
A
18.(10分)“China”的含义又指瓷器,反映了在世人眼中,中国作为瓷器故乡的形象。X、Y、Z、B、
A皆是元素周期表中前四周期的元素,原子序数依次增大。X、Z、Y、A是地壳中含量最多的四种元素,B的
基态原子为第四周期基态原子中未配对电子数最多的。
(1)请写出B原子的价电子轨道表示式_______。
(2)比较Y原子与它同周期相邻元素的第一电离能,由大到小的顺序为_______(用元素符号表示)。
(3)Z的氧化物晶体与干冰相比,_______(填化学式)沸点更高,解释原因:_______。
(4)实验发现,Y的氯化物的蒸气溶于非极性溶剂中或处于熔融状态时,都以二聚态(Y Cl)形式存在。其球
2 6
棍模型如图所示。
①该分子中Y原子采取_______杂化。分子中存在配位键,配位原子为_______。
②Y Cl 与过量NaOH溶液反应生成Na[Y(OH) ],[Y(OH) ]-中存在的化学作用力类型有_______(填标号)。
2 6 4 4
A.离子键 B.金属键 C.极性共价键 D.非极性共价键 E.配位键 F.σ键 G.π键
H.氢键
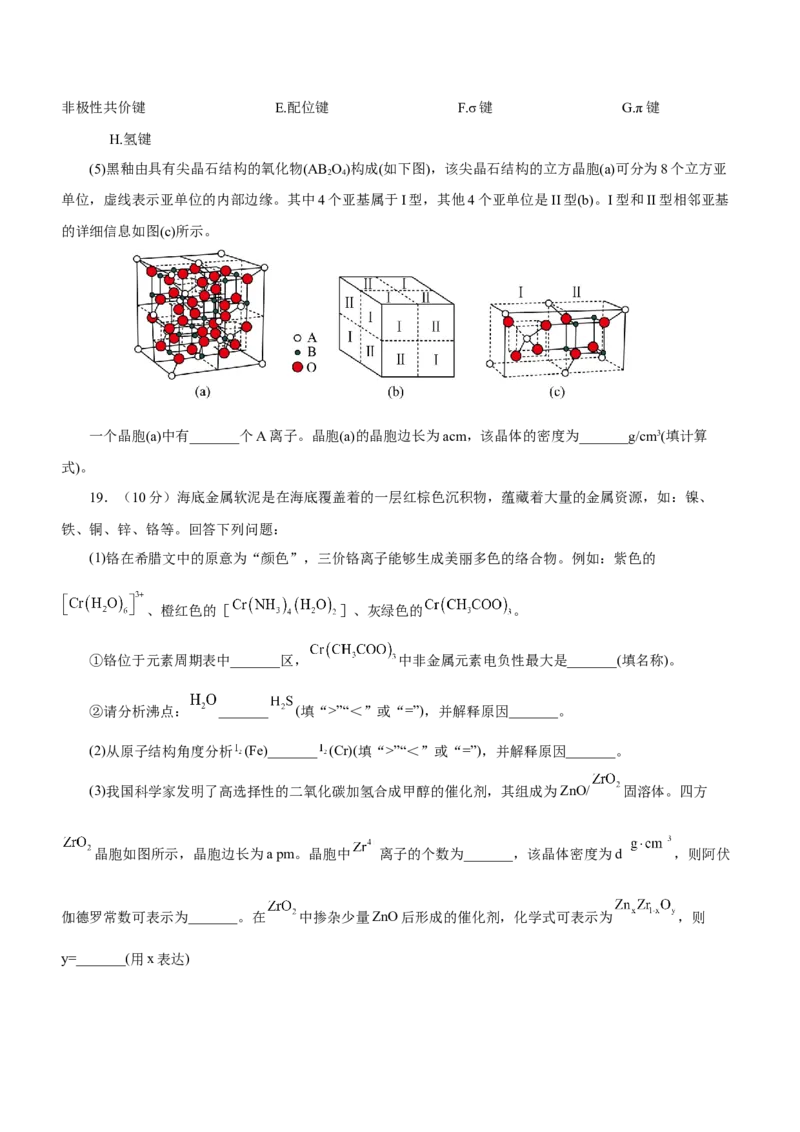
(5)黑釉由具有尖晶石结构的氧化物(AB O)构成(如下图),该尖晶石结构的立方晶胞(a)可分为8个立方亚
2 4
单位,虚线表示亚单位的内部边缘。其中4个亚基属于I型,其他4个亚单位是II型(b)。I型和II型相邻亚基
的详细信息如图(c)所示。
一个晶胞(a)中有_______个A离子。晶胞(a)的晶胞边长为acm,该晶体的密度为_______g/cm3(填计算
式)。
19.(10分)海底金属软泥是在海底覆盖着的一层红棕色沉积物,蕴藏着大量的金属资源,如:镍、
铁、铜、锌、铬等。回答下列问题:
(1)铬在希腊文中的原意为“颜色”,三价铬离子能够生成美丽多色的络合物。例如:紫色的
、橙红色的[ ]、灰绿色的 。
①铬位于元素周期表中_______区, 中非金属元素电负性最大是_______(填名称)。
②请分析沸点: _______ (填“>”“<”或“=”),并解释原因_______。
(2)从原子结构角度分析 (Fe)_______ (Cr)(填“>”“<”或“=”),并解释原因_______。
(3)我国科学家发明了高选择性的二氧化碳加氢合成甲醇的催化剂,其组成为ZnO/ 固溶体。四方
晶胞如图所示,晶胞边长为a pm。晶胞中 离子的个数为_______,该晶体密度为d ,则阿伏
伽德罗常数可表示为_______。在 中掺杂少量ZnO后形成的催化剂,化学式可表示为 ,则
y=_______(用x表达)20.(10分)秦始皇帝陵博物院首次在兵马俑的彩绘中发现了古人人工合成的“中国蓝”“中国紫”颜
料。人们对这些颜料的研究发现,其成分主要是钡和铜的硅酸盐(BaCuSi O)。
x y
回答下列问题:
(1)基态铜原子的电子排布式为____。“中国蓝”的发色中心是以Cu2+为中心的配位化合物,形成该配位
键,Cu2+提供____,若“中国蓝”的化学组成中x:y=1:3,则其化学式为____。
(2)“中国蓝”“中国紫”中存在SiO 四面体结构,其中Si原子采取的杂化类型为___。与SiO 不同,
CO 的立体构型为____。
(3)C和Si同主族,但CO 与SiO 的熔沸点差异很大,这是因为CO 是____晶体,而SiO 是___晶体。
2 2 2 2
(4)MgO的熔沸点____BaO(填“>”“<”“=”),原因是____。
(5)立方CuO晶胞结构如图所示。晶胞参数为a pm,N 代表阿伏加德罗常数的值。则两个距离最近Cu2+之
A
间的距离为____pm(用代数式表示),其晶体密度为____(用代数式表示)。