文档内容
专题 17 有机推断与合成路线
1.有机化合物的组成与结构:(1)能根据有机化合物的元素含量、相对分子质量确定有机化合物的分子式;
(2)了解常见有机化合物的结构;了解有机化合物分子中的官能团,能正确地表示它们的结构;(3)了解确定有
机化合物结构的化学方法和物理方法(如质谱、红外光谱、核磁共振氢谱等);(4)能正确书写有机化合物的同分
异构体(不包括手性异构体);(5)能够正确命名简单的有机化合物;(6)了解有机分子中官能团之间的相互影响。
2.烃及其衍生物的性质与应用:(1)掌握烷、烯、炔和芳香烃的结构与性质;(2)掌握卤代烃、醇、酚、
醛、羧酸、酯的结构与性质,以及它们之间的相互转化;(3)了解烃类及衍生物的重要应用以及烃的衍生物的
合成方法;(4)根据信息能设计有机化合物的合成路线。
3.糖类、氨基酸和蛋白质:(1)了解糖类、氨基酸和蛋白质的组成、结构特点、主要化学性质及应用;(2)
了解糖类、氨基酸和蛋白质在生命过程中的作用。4.合成高分子:(1)了解合成高分子的组成与结构特点;能依
据简单合成高分子的结构分析其链节和单体;(2)了解加聚反应和缩聚反应的含义;(3)了解合成高分子在高新
技术领域的应用以及在发展经济、提高生活质量方面中的贡献。
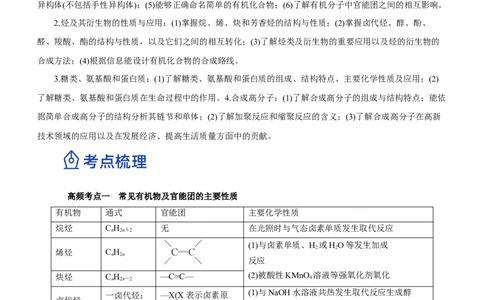
高频考点一 常见有机物及官能团的主要性质
有机物 通式 官能团 主要化学性质
烷烃 C H 无 在光照时与气态卤素单质发生取代反应
n 2n+2
(1)与卤素单质、H 或HO等发生加成
2 2
烯烃 C H
n 2n
反应
炔烃 C n H 2n-2 —C≡C— (2)被酸性KMnO 4 溶液等强氧化剂氧化
一卤代烃: —X(X表示卤素原
(1)与NaOH水溶液共热发生取代反应生成醇
卤代烃
R—X 子)
(2)与NaOH醇溶液共热发生消去反应
(1)与活泼金属反应产生H
2
(2)与卤化氢或浓氢卤酸反应生成卤代烃
(3)脱水反应:乙醇
一元醇:R
醇 醇羟基—OH
—OH
(4)催化氧化为醛或酮
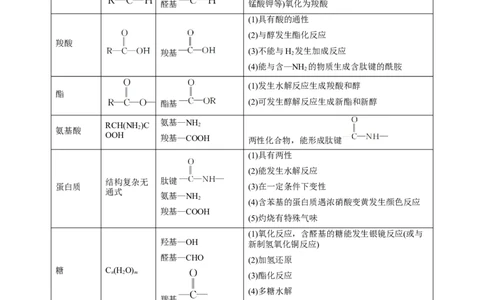
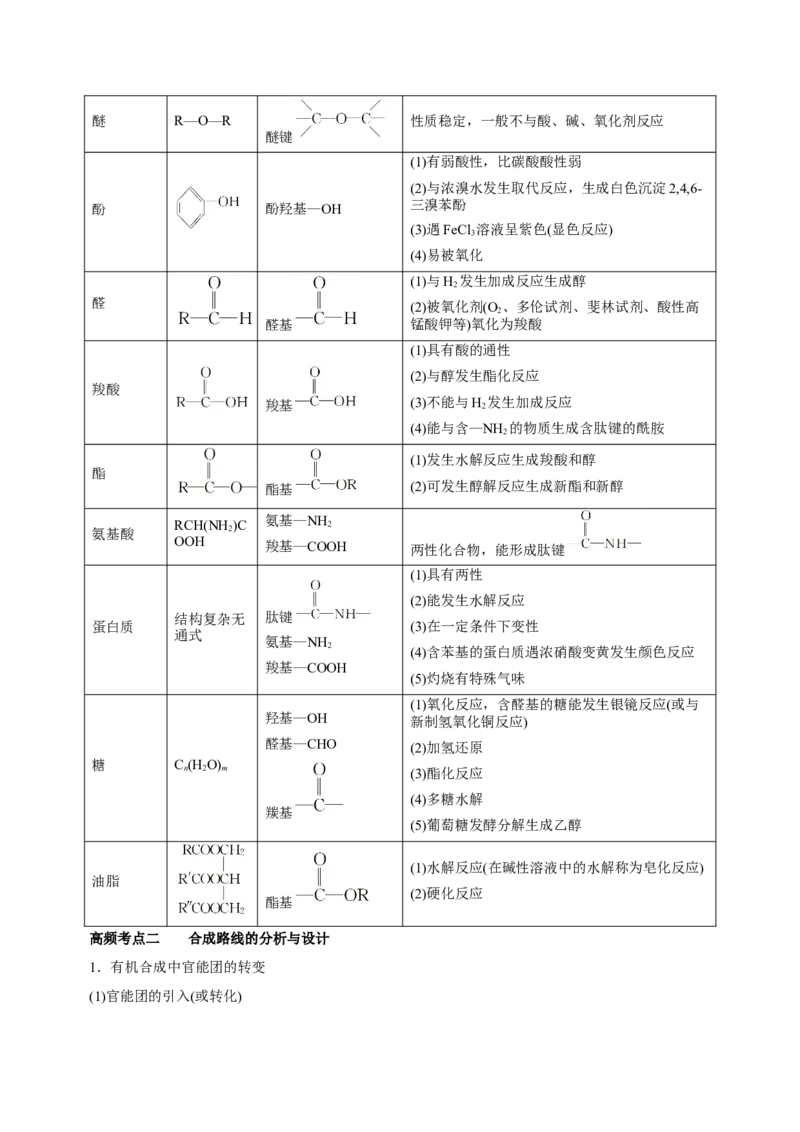
(5)与羧酸或无机含氧酸反应生成酯醚 R—O—R 性质稳定,一般不与酸、碱、氧化剂反应
醚键
(1)有弱酸性,比碳酸酸性弱
(2)与浓溴水发生取代反应,生成白色沉淀2,4,6-
酚 酚羟基—OH 三溴苯酚
(3)遇FeCl 溶液呈紫色(显色反应)
3
(4)易被氧化
(1)与H 发生加成反应生成醇
2
醛 (2)被氧化剂(O 、多伦试剂、斐林试剂、酸性高
2
醛基 锰酸钾等)氧化为羧酸
(1)具有酸的通性
(2)与醇发生酯化反应
羧酸
羧基 (3)不能与H 2 发生加成反应
(4)能与含—NH 的物质生成含肽键的酰胺
2
(1)发生水解反应生成羧酸和醇
酯
酯基 (2)可发生醇解反应生成新酯和新醇
氨基—NH
RCH(NH )C 2
氨基酸 2
OOH
羧基—COOH 两性化合物,能形成肽键
(1)具有两性
(2)能发生水解反应
结构复杂无 肽键
蛋白质 (3)在一定条件下变性
通式
氨基—NH
2 (4)含苯基的蛋白质遇浓硝酸变黄发生颜色反应
羧基—COOH
(5)灼烧有特殊气味
(1)氧化反应,含醛基的糖能发生银镜反应(或与
羟基—OH 新制氢氧化铜反应)
醛基—CHO (2)加氢还原
糖 C (H O)
n 2 m (3)酯化反应
(4)多糖水解
羰基
(5)葡萄糖发酵分解生成乙醇
(1)水解反应(在碱性溶液中的水解称为皂化反应)
油脂
(2)硬化反应
酯基
高频考点二 合成路线的分析与设计
1.有机合成中官能团的转变
(1)官能团的引入(或转化)—OH
+HO;R—X+HO;R—CHO+H;RCOR′+H;R
2 2 2 2
—COOR′+HO;多糖水解
2
—X 烷烃+X;烯(炔)烃+X 或HX;R—OH+HX
2 2
官能团
R—OH和R—X的消去;炔烃不完全加成
的引入
—CHO 某些醇氧化;烯烃氧化;炔烃水化;糖类水解
R—CHO+O;苯的同系物被强氧化剂氧化;羧酸盐酸化;R—
—COOH 2
COOR′+HO
2
—COO— 酯化反应
(2)官能团的消除
①消除双键:加成反应。
②消除羟基:消去、氧化、酯化反应。
③消除醛基:还原和氧化反应。
(3)官能团的保护
被保护的
被保护的官能团性质 保护方法
官能团
①用NaOH溶液先转化为酚钠,后酸化重新转化为酚:
易被氧气、臭氧、双氧水、
酚羟基
酸性高锰酸钾溶液氧化
②用碘甲烷先转化为苯甲醚,后用氢碘酸酸化重新转化
为酚:
易被氧气、臭氧、双氧水、
氨基 先用盐酸转化为盐,后用NaOH溶液重新转化为氨基
酸性高锰酸钾溶液氧化
易与卤素单质加成,易被氧
用氯化氢先通过加成转化为氯代物,后用NaOH醇溶液
碳碳双键 气、臭氧、双氧水、酸性高
通过消去反应重新转化为碳碳双键
锰酸钾溶液氧化
乙醇(或乙二醇)加成保护: ――――→
醛基 易被氧化
―――→
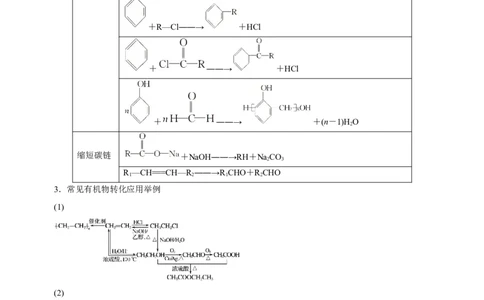
2.增长碳链或缩短碳链的方法
举例
2CH≡CH―→CH===CH—C≡CH
2
2R—Cl――→R—R+2NaCl
增长碳链
CHCHO―――――→
3R—Cl――→R—CN――→R—COOH
CHCHO――→ ――→
3
nCH===CH ――→CH —CH
2 2 2 2
nCH===CH—CH===CH ――→
2 2
CH —CH===CH—CH
2 2
2CHCHO――――→
3
+R—Cl――→ +HCl
+ ――→ +HCl
+ ――→ +(n-1)H O
2
缩短碳链 +NaOH――→RH+NaCO
2 3
R —CH===CH—R ――→R CHO+R CHO
1 2 1 2
3.常见有机物转化应用举例
(1)
(2)
(3)(4)CH CHO―――――→ ――→
3
4.有机合成路线设计的几种常见类型
根据目标分子与原料分子在碳骨架和官能团两方面变化的特点,我们将合成路线的设计分为
(1)以熟悉官能团的转化为主型
如:以CH===CHCH 为主要原料(无机试剂任用)设计CHCH(OH)COOH的合成路线流程图(须注明反应条
2 3 3
件)。
CH===CHCH――→ ―――→ ――→ ――→
2 3
――→
(2)以分子骨架变化为主型
如:请以苯甲醛和乙醇为原料设计苯乙酸乙酯( )的合成路线流程图(注明反
应条件)。
提示:R—Br+NaCN―→R—CN+NaBr
――――→ ――→ ――→ ――→
―――――→
(3)陌生官能团兼有骨架显著变化型(常为考查的重点)
要注意模仿题干中的变化,找到相似点,完成陌生官能团及骨架的变化。如:模仿――→ ――→ ――→ ――→
香兰素 A B C
――→
D 多巴胺
设计以苯甲醇、硝基甲烷为主要原料制备苯乙胺( )的合成路线流程图。
关键是找到原流程中与新合成路线中的相似点。(碳架的变化、官能团的变化;硝基引入及转化为氨基的
过程)
――→ ――→ ――→ ――→
――→
高频考点二 有机合成与推断
1.根据反应条件推断反应物或生成物
(1)“光照”为烷烃的卤代反应。
(2)“NaOH水溶液、加热”为R—X的水解反应,或酯( )的水解反应。
(3)“NaOH醇溶液、加热”为R—X的消去反应。
(4)“HNO (浓HSO )”为苯环上的硝化反应。
3 2 4
(5)“浓HSO 、加热”为R—OH的消去或酯化反应。
2 4
(6)“浓HSO 、170 ℃”是乙醇消去反应的条件。
2 4
2.根据有机反应的特殊现象推断有机物的官能团(1)使溴水褪色,则表示该物质中可能含有碳碳双键、碳碳三键或醛基。
(2)使酸性KMnO 溶液褪色,则该物质中可能含有碳碳双键、碳碳三键、醛基或苯的同系物(侧链烃基中与
4
苯环直接相连的碳原子上必须含有氢原子)。
(3)遇FeCl 溶液显紫色或加入浓溴水出现白色沉淀,表示该物质分子中含有酚羟基。
3
(4)加入新制Cu(OH) 悬浊液并加热,有砖红色沉淀生成(或加入银氨溶液并水浴加热有银镜出现),表示该
2
物质中含有—CHO。
(5)加入金属钠,有H 产生,表示该物质分子中可能有—OH 或—COOH。
2
(6)加入NaHCO 溶液有气体放出,表示该物质分子中含有—COOH。
3
3.以特征产物为突破口来推断碳架结构和官能团的位置
(1)醇的氧化产物与结构的关系
(2)由消去反应的产物可确定“—OH”或“—X”的位置。
(3)由取代产物的种类或氢原子环境可确定碳架结构。有机物取代产物越少或相同环境的氢原子数越多,
说明该有机物结构的对称性越高,因此可由取代产物的种类或氢原子环境联想到该有机物碳架结构的对称性而
快速进行解题。
(4)由加氢后的碳架结构可确定碳碳双键或碳碳三键的位置。
(5)由有机物发生酯化反应能生成环酯或高聚酯,可确定该有机物是含羟基的羧酸;根据酯的结构,可确
定 —OH与—COOH的相对位置。
4.根据关键数据推断官能团的数目
(1)—CHO ;
(2)2—OH(醇、酚、羧酸)――→H;
2
(3)2—COOH――→CO,—COOH――→CO;
2 2
(4) ――→ ――→ —C≡C— ――→ ;
(5)RCHOH――――→CHCOOCH R。
2 3 2
(M) (M+42)
r r5.根据新信息类推
高考常见的新信息反应总结如下
(1)丙烯αH被取代的反应:CH—CH===CH +Cl Cl—CH —CH===CH +HCl。
3 2 2――→ 2 2
(2)共轭二烯烃的1,4加成反应:
①CH===CH—CH===CH +Br ―→ ;
2 2 2
② 。
(3)烯烃被O 氧化:R—CH===CH ――→R—CHO+HCHO。
3 2
(4)苯环侧链的烃基(与苯环相连的碳原子上含有氢原子)被酸性KMnO 溶液氧化:
4
――→ 。
(5)苯环上的硝基被还原: ――→ 。
(6)醛、酮的加成反应(加长碳链,—CN水解得—COOH):
①CHCHO+HCN―→ ;
3
② +HCN――→ ;
③CH CHO+NH ――→
3 3
(作用:制备胺);
④CH CHO+CHOH――→
3 3
(作用:制半缩醛)。(7)羟醛缩合: + ――→ 。
(8)醛或酮与格氏试剂(R′MgX)发生加成反应,所得产物经水解可得醇:
+R′MgX―→ ――→ 。
(9)羧酸分子中的αH被取代的反应:
RCHCOOH+Cl――→ +HCl。
2 2
(10)羧酸用LiAlH 还原时,可生成相应的醇:
4
RCOOH――→RCHOH。
2
(11)酯交换反应(酯的醇解):
R COOR +R OH―→R COOR +R OH。
1 2 3 1 3 2
题型一 有机推断综合
例1. (2022·北京卷)碘番酸可用于X射线的口服造影液,其合成路线如图所示。
已知:R-COOH+R’-COOH +H O
2
(1)A可发生银镜反应,其官能团为___________。
(2)B无支链,B的名称为___________;B的一种同分异构体中只有一种环境氢,其结构简式为
___________。(3)E是芳香族化合物, 的方程式为___________。
(4)G中有乙基,则G的结构简式为___________。
(5)碘番酸中的碘在苯环不相邻的碳原了上,碘番酸的相对分了质量为571,J的相对分了质量为193。
则碘番酸的结构简式为___________。
(6)通过滴定法来确定口服造影液中碘番酸的质量分数。
第一步 取 样品,加入过量 粉, 溶液后加热,将I元素全部转为 ,冷却,洗涤。
第二步 调节溶液 ,用 溶液滴定至终点,用去 。已知口服造影液中无其他含
的
碘物质,则碘番酸 质量分数为___________。
【变式探究】(2022·山东卷)支气管扩张药物特布他林(H)的一种合成路线如下:
已知:
Ⅰ.
Ⅱ.、
Ⅲ.
回答下列问题:
(1)A→B反应条件为_______;B中含氧官能团有_______种。
(2)B→C反应类型为_______,该反应的目的是_______。
(3)D结构简式为_______;E→F的化学方程式为_______。(4)H的同分异构体中,仅含有 、 和苯环结构的有_______种。
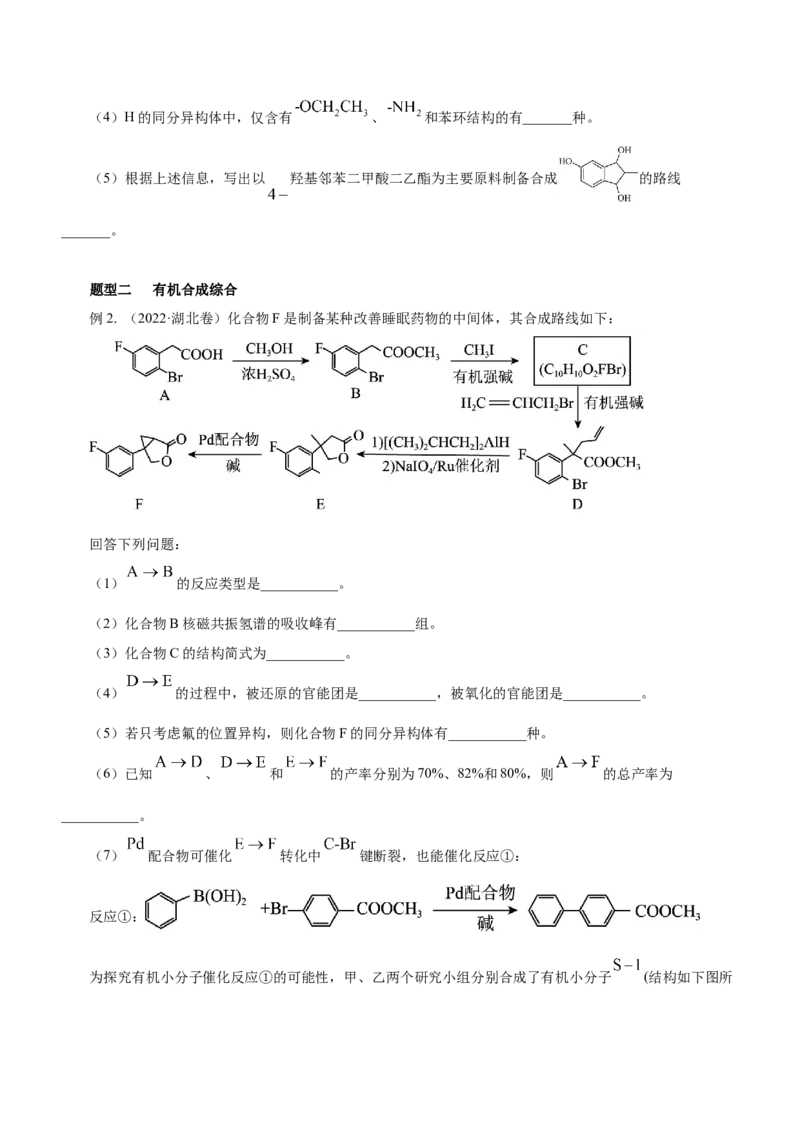
(5)根据上述信息,写出以 羟基邻苯二甲酸二乙酯为主要原料制备合成 的路线
_______。
题型二 有机合成综合
例2. (2022·湖北卷)化合物F是制备某种改善睡眠药物的中间体,其合成路线如下:
回答下列问题:
(1) 的反应类型是___________。
(2)化合物B核磁共振氢谱的吸收峰有___________组。
(3)化合物C的结构简式为___________。
(4) 的过程中,被还原的官能团是___________,被氧化的官能团是___________。
(5)若只考虑氟的位置异构,则化合物F的同分异构体有___________种。
(6)已知 、 和 的产率分别为70%、82%和80%,则 的总产率为
___________。
(7) 配合物可催化 转化中 键断裂,也能催化反应①:
反应①:
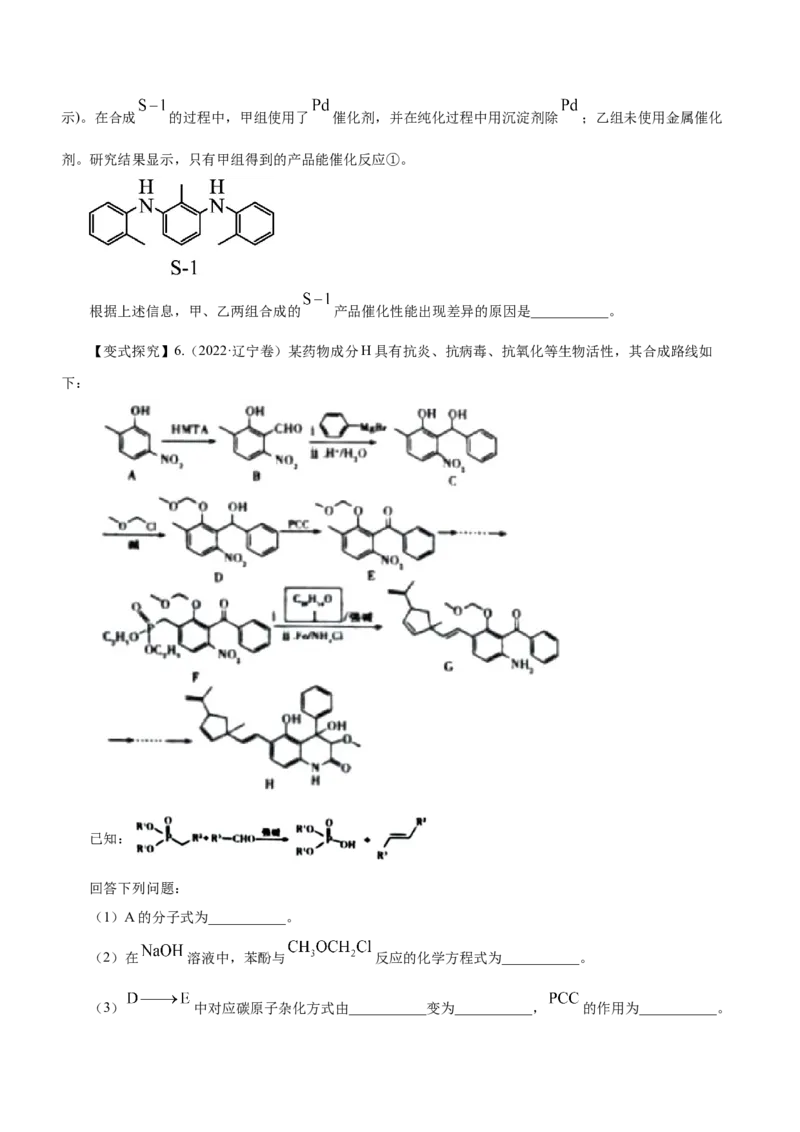
为探究有机小分子催化反应①的可能性,甲、乙两个研究小组分别合成了有机小分子 (结构如下图所示)。在合成 的过程中,甲组使用了 催化剂,并在纯化过程中用沉淀剂除 ;乙组未使用金属催化
剂。研究结果显示,只有甲组得到的产品能催化反应①。
根据上述信息,甲、乙两组合成的 产品催化性能出现差异的原因是___________。
【变式探究】6.(2022·辽宁卷)某药物成分H具有抗炎、抗病毒、抗氧化等生物活性,其合成路线如
下:
已知:
回答下列问题:
(1)A的分子式为___________。
(2)在 溶液中,苯酚与 反应的化学方程式为___________。
(3) 中对应碳原子杂化方式由___________变为___________, 的作用为___________。(4) 中步骤ⅱ实现了由___________到___________的转化(填官能团名称)。
(5)I的结构简式为___________。
(6)化合物I的同分异构体满足以下条件的有___________种(不考虑立体异构);
i.含苯环且苯环上只有一个取代基
ii.红外光谱无醚键吸收峰
其中,苯环侧链上有3种不同化学环境的氢原子,且个数比为6∶2∶1的结构简式为___________(任写一
种)。
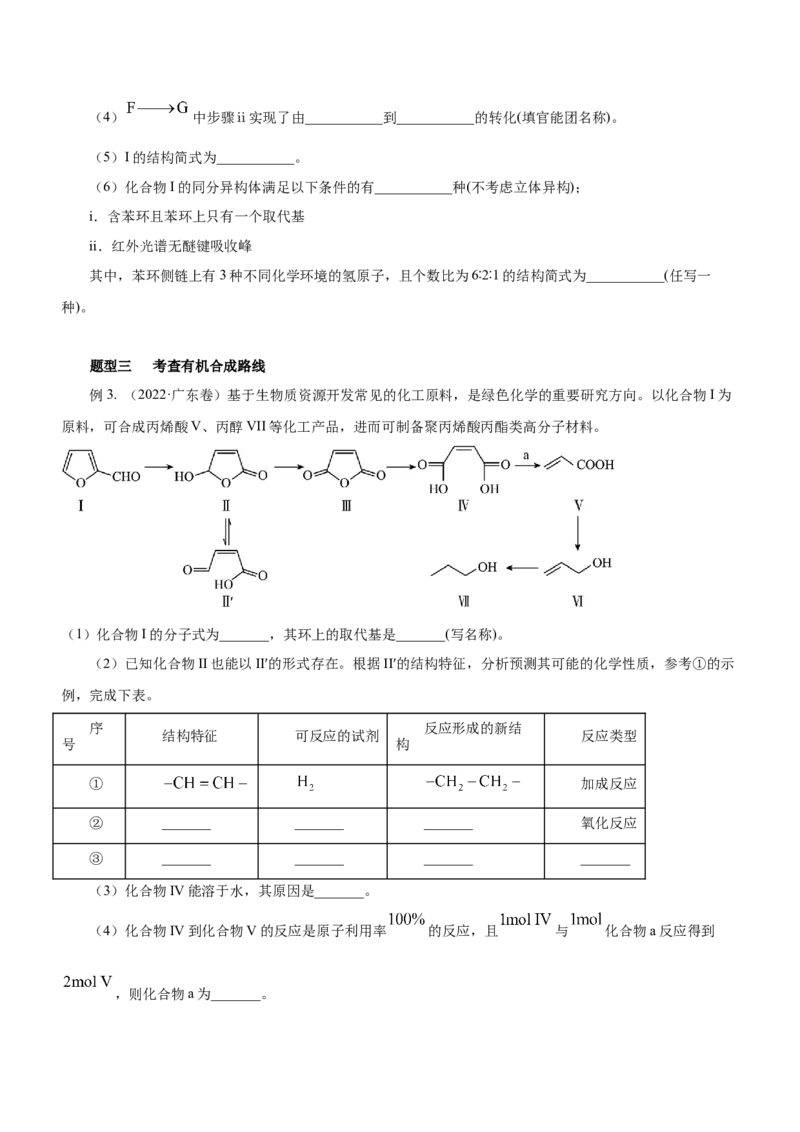
题型三 考查有机合成路线
例3. (2022·广东卷)基于生物质资源开发常见的化工原料,是绿色化学的重要研究方向。以化合物I为
原料,可合成丙烯酸V、丙醇VII等化工产品,进而可制备聚丙烯酸丙酯类高分子材料。
(1)化合物I的分子式为_______,其环上的取代基是_______(写名称)。
(2)已知化合物II也能以II′的形式存在。根据II′的结构特征,分析预测其可能的化学性质,参考①的示
例,完成下表。
序 反应形成的新结
结构特征 可反应的试剂 反应类型
号 构
① 加成反应
② _______ _______ _______ 氧化反应
③ _______ _______ _______ _______
(3)化合物IV能溶于水,其原因是_______。
(4)化合物IV到化合物V的反应是原子利用率 的反应,且 与 化合物a反应得到
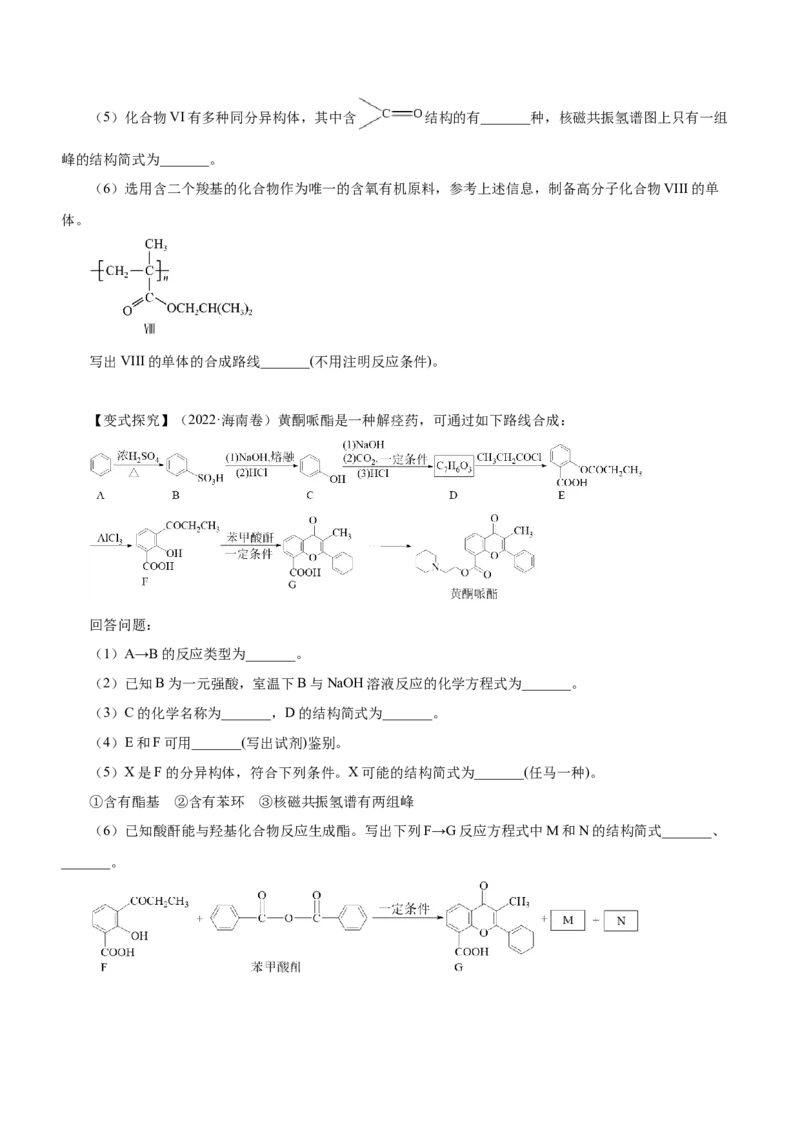
,则化合物a为_______。(5)化合物VI有多种同分异构体,其中含 结构的有_______种,核磁共振氢谱图上只有一组
峰的结构简式为_______。
(6)选用含二个羧基的化合物作为唯一的含氧有机原料,参考上述信息,制备高分子化合物VIII的单
体。
写出VIII的单体的合成路线_______(不用注明反应条件)。
【变式探究】(2022·海南卷)黄酮哌酯是一种解痉药,可通过如下路线合成:
回答问题:
(1)A→B的反应类型为_______。
(2)已知B为一元强酸,室温下B与NaOH溶液反应的化学方程式为_______。
(3)C的化学名称为_______,D的结构简式为_______。
(4)E和F可用_______(写出试剂)鉴别。
(5)X是F的分异构体,符合下列条件。X可能的结构简式为_______(任马一种)。
①含有酯基 ②含有苯环 ③核磁共振氢谱有两组峰
(6)已知酸酐能与羟基化合物反应生成酯。写出下列F→G反应方程式中M和N的结构简式_______、
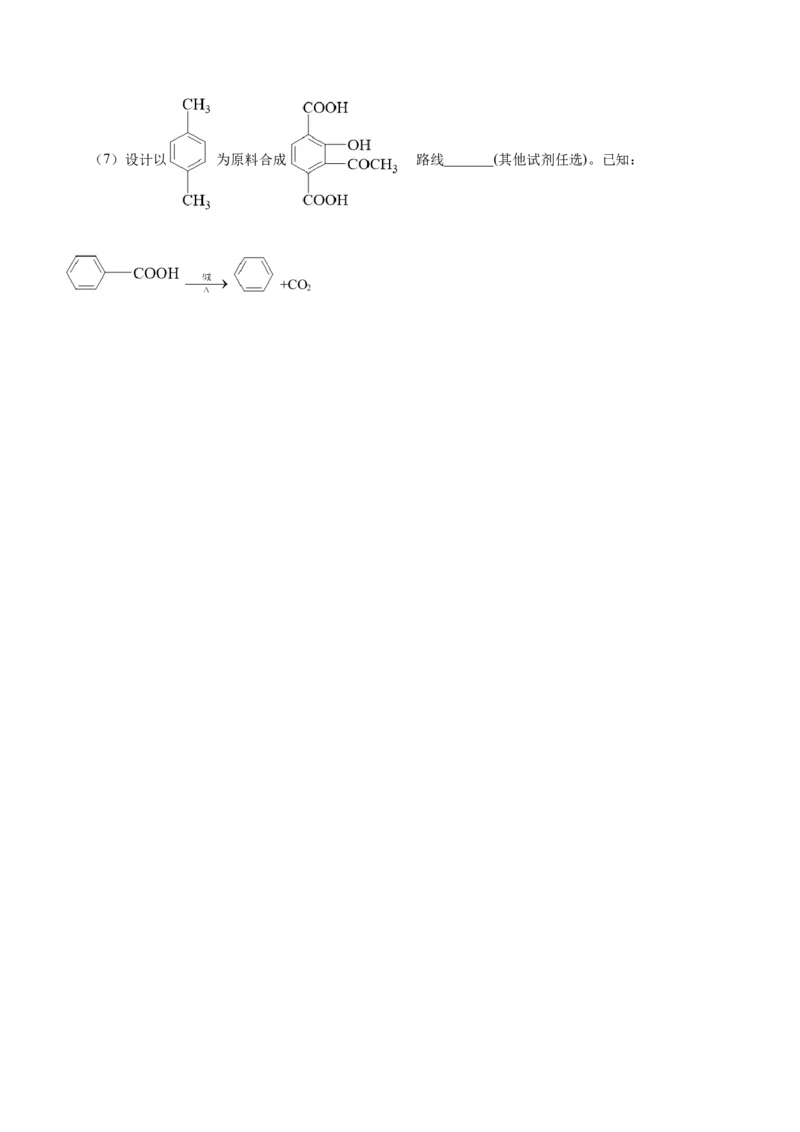
_______。(7)设计以 为原料合成 路线_______(其他试剂任选)。已知:
的
+CO
2