文档内容
专题 17 有机推断与合成路线
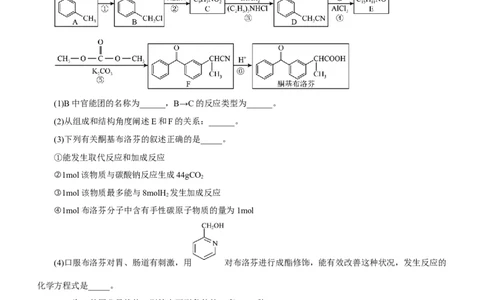
1.酮基布洛芬是一种常用的解热镇痛药,通过抑制前列腺素的生成可达到缓解疼痛的作用,并有解热、
抗炎的作用,尤其对近期新型冠状病毒感染引起的发热症状有很好的治疗作用。其合成路线如图所示:
(1)B中官能团的名称为______,B→C的反应类型为______。
(2)从组成和结构角度阐述E和F的关系:______。
(3)下列有关酮基布洛芬的叙述正确的是_____。
①能发生取代反应和加成反应
②1mol该物质与碳酸钠反应生成44gCO
2
③1mol该物质最多能与8molH 发生加成反应
2
④1mol布洛芬分子中含有手性碳原子物质的量为1mol
(4)口服布洛芬对胃、肠道有刺激,用 对布洛芬进行成酯修饰,能有效改善这种状况,发生反应的
化学方程式是_____。
(5)H为C的同分异构体,则符合下列条件的H有_____种。
①除苯环外不含其他环状结构;②含有硝基,且直接连在苯环上;③苯环上只有两个取代基。
(6) 请写出用乙烯和碳酸二甲酯( )为原料(无机试剂和有机溶剂任选,合成路线流程
图示例见本题题干),设计制备异丁酸的一种合成路线流程图______。
【答案】(1) 羧基、碳氯键 取代反应 (2)同系物 (3)①④(4) + → +H O (5)6
2
(5) C H CHCHCl CHCHCN (CH)CHCN (CH)CHCOOH
2 4 3 2 3 2 3 2 3 2
【分析】对比A、B结构可知,A 转化为B发生取代反应,Cl取代了甲基上的 H,故此步反应条件应为
Cl、光照;B转化为C的过程中,H、O个数均没有改变,多了1个C和1个N,少了一个 Cl,故可知C结
2
构 ,此步发生取代反应,-CN取代了-Cl;同理,E 结构为: ;D 转化为 E发生取
代反应,苯环取代了-Cl;E 转化为F发生取代反应-CH 取代了E中-CH-上的H;F转化为酮基布洛芬步骤中
3 2
在H+条件下可以将-CN变为-COOH,据此分析解题。
【解析】(1)B中官能团的名称为羧基、碳氯键,据分析可知B→C的反应类型为取代反应;(2)E和
F两者结构相似,相差一个-CH,两者的关系为同系物;(3)酮基布洛芬的结构简式为:
2
。①由于含有甲基与羧基能发生取代反应,苯环可发生加成反应,正确;②羧基可与碳酸钠反应,1mol该物
质消耗0.5mol碳酸钠,生成0.5mol二氧化碳,反应生成22gCO,错误;③该物质含有2个苯环,两个苯环消
2
耗6mol H,氢气可以酮羰基中的碳氧双键加成,不能与羧基、酯基中的碳氧双键加成,1mol该物质最多能与
2
7molH 发生加成反应,错误;④1mol布洛芬分子中含有手性碳原子物质的量为1mol
2
,正确;故选①④;(4) 与 发生酯化反应: +(6) → +H O;(5)C的结构为 ,符合条件①除苯环外不含其他环状
2
结构;②含有硝基,且直接连在苯环上;③苯环上只有两个取代基,除去-NO ,则另一个取代基为-C H,-
2 3 3
C H 的同分异构体分别为: 、这两种取代基均有有邻间对三种位置,共3×2=6种;
3 3
(6)异丁酸的结构为:(CH)CHCOOH,原料为乙烯,反应过程中C原子个数增加,原料有
3 2
,根据题干逆推,想要获得-COOH,参照F转化为酮基布洛芬步骤在酸性条件下将-CN
转化为-COOH,可得合成路线:C H CHCHCl CHCHCN (CH)CHCN
2 4 3 2 3 2 3 2
(CH)CHCOOH。
3 2
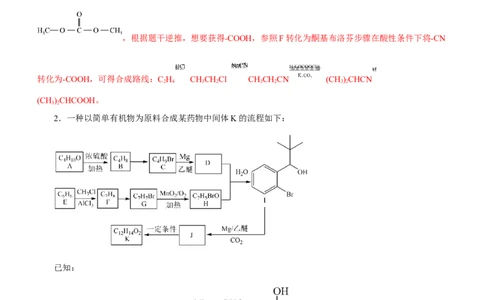
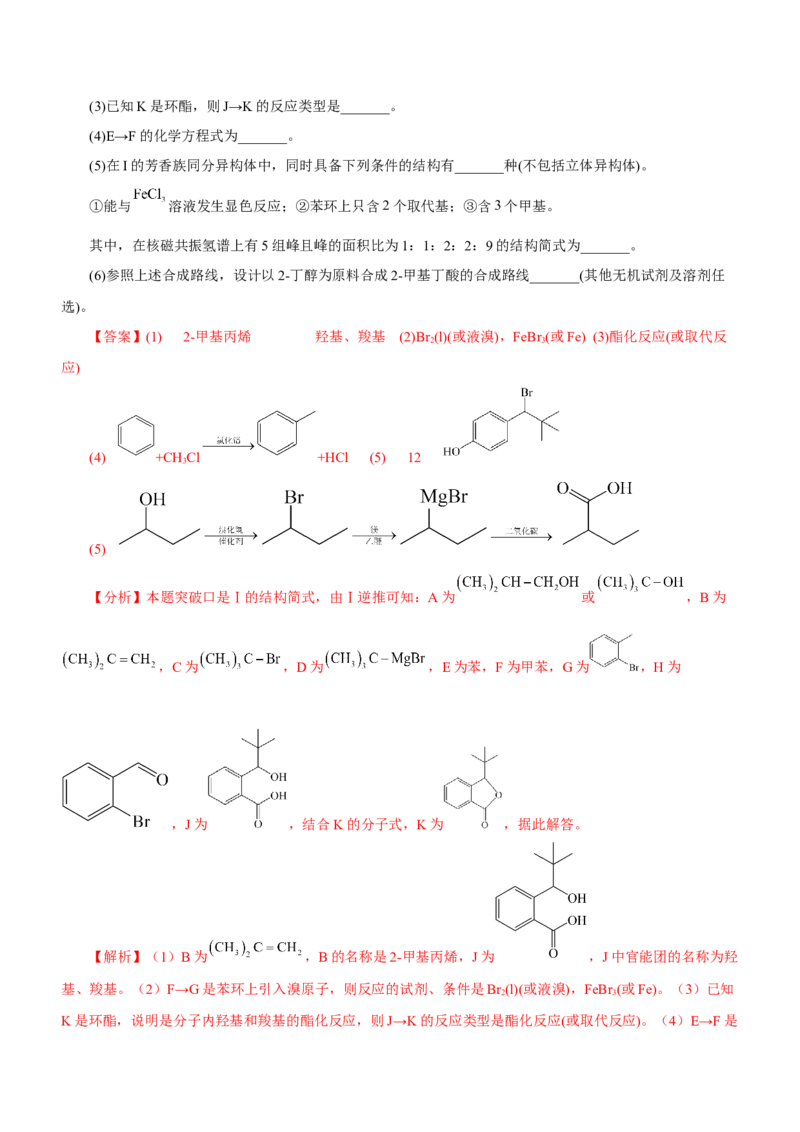
2.一种以简单有机物为原料合成某药物中间体K的流程如下:
已知:
回答下列问题:
(1)B的名称是_______(用系统命名法命名),J中官能团的名称为_______。
(2)F→G的试剂、条件是_______。(3)已知K是环酯,则J→K的反应类型是_______。
(4)E→F的化学方程式为_______。
(5)在I的芳香族同分异构体中,同时具备下列条件的结构有_______种(不包括立体异构体)。
①能与 溶液发生显色反应;②苯环上只含2个取代基;③含3个甲基。
其中,在核磁共振氢谱上有5组峰且峰的面积比为1:1:2:2:9的结构简式为_______。
(6)参照上述合成路线,设计以2-丁醇为原料合成2-甲基丁酸的合成路线_______(其他无机试剂及溶剂任
选)。
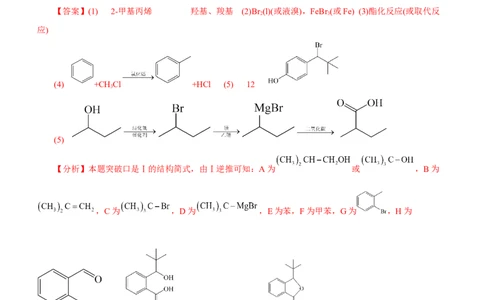
【答案】(1) 2-甲基丙烯 羟基、羧基 (2)Br (l)(或液溴),FeBr (或Fe) (3)酯化反应(或取代反
2 3
应)
(4) +CH Cl +HCl (5) 12
3
(5)
【分析】本题突破口是Ⅰ的结构简式,由Ⅰ逆推可知:A为 或 ,B为
,C为 ,D为 ,E为苯,F为甲苯,G为 ,H为
,J为 ,结合K的分子式,K为 ,据此解答。
【解析】(1)B为 ,B的名称是2-甲基丙烯,J为 ,J中官能团的名称为羟
基、羧基。(2)F→G是苯环上引入溴原子,则反应的试剂、条件是Br (l)(或液溴),FeBr (或Fe)。(3)已知
2 3
K是环酯,说明是分子内羟基和羧基的酯化反应,则J→K的反应类型是酯化反应(或取代反应)。(4)E→F是苯环上引入甲基,则反应的化学方程式为 +CH Cl +HCl。(5)①能与 溶液发
3
生显色反应;②苯环上只含2个取代基;③含3个甲基,说明苯环上含1个羟基、1个溴戊基。含3个甲基的
溴戊基有4种: 、 、 、 (—R表示苯基),溴戊基与羟基位于
邻、间、对三种,共12种同分异构体,其中,在核磁共振氢谱上有5组峰且峰的面积比为1:1:2:2:9的
结构简式为 。(6)2-丁醇首先和溴化氢发生取代反应生成2-溴丁烷,然后2-溴丁烷转化
为 ,最后 和二氧化碳反应转化为 ,则合成2-甲基丁酸的合成路线为
。
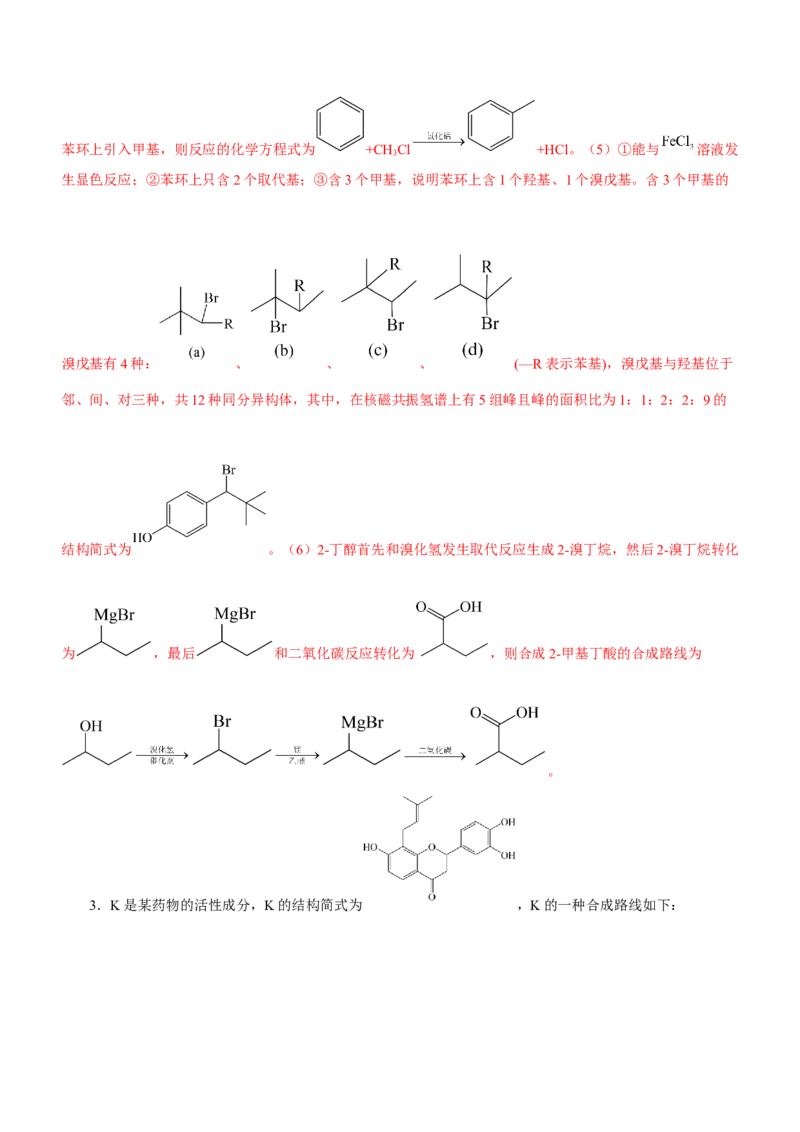
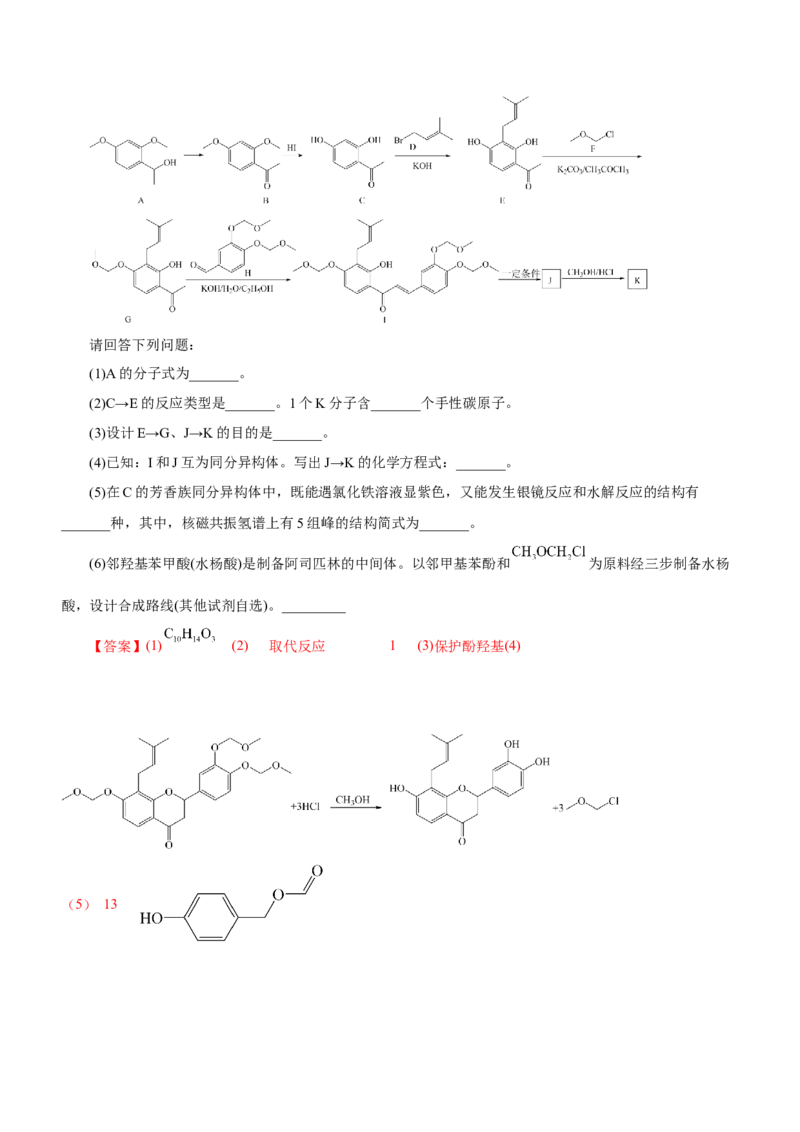
3.K是某药物的活性成分,K的结构简式为 ,K的一种合成路线如下:请回答下列问题:
(1)A的分子式为_______。
(2)C→E的反应类型是_______。1个K分子含_______个手性碳原子。
(3)设计E→G、J→K的目的是_______。
(4)已知:I和J互为同分异构体。写出J→K的化学方程式:_______。
(5)在C的芳香族同分异构体中,既能遇氯化铁溶液显紫色,又能发生银镜反应和水解反应的结构有
_______种,其中,核磁共振氢谱上有5组峰的结构简式为_______。
(6)邻羟基苯甲酸(水杨酸)是制备阿司匹林的中间体。以邻甲基苯酚和 为原料经三步制备水杨
酸,设计合成路线(其他试剂自选)。_________
【答案】(1) (2) 取代反应 1 (3)保护酚羟基(4)
(5) 13(6)
【解析】(1)根据A分子的结构简式,A的分子式为: 。(2)C→E中,溴和苯环上的氢结合
生成溴化氢,发生取代反应;根据K的结构简式,1个K分子含1个手性碳原子。(3)E→G将酚羟基转化成
醚键,J→K将醚键转化成酚羟基,此设计是为了保护酚羟基。(4)I和J互为同分异构体,再结合K的结构
简式,可知I→J是碳碳双键和酚羟基的加成反应,形成六元环;J→K是苯环上醚键与氯化氢反应,恢复酚羟
基,化学方程式如下: 。(5)同分异构体含
有酚羟基、甲酸酯基,分两种情况讨论:第一种情况是苯环上有2个取代基: 、 ,有3种同
分异构体;第二种情况是苯环上有3个取代基: 、 、 ,有10种同分异构体,故符合条件的
同分异构体有13种。核磁共振氢谱上有5组峰的结构简式为 。(6)根据信息,先
保护羟基,后氧化甲基,最后恢复羟基,合成路线为:
。
4.布洛芬是一种常用的解热镇痛药,通过抑制前列腺素的生成可达到缓解疼痛的作用,并有解热、抗炎
的作用,尤其对近期新型冠状病毒感染引起的发热症状有很好的治疗作用。以有机物A为原料制备布洛芬(H)
的一种合成路线如图所示:回答下列问题:
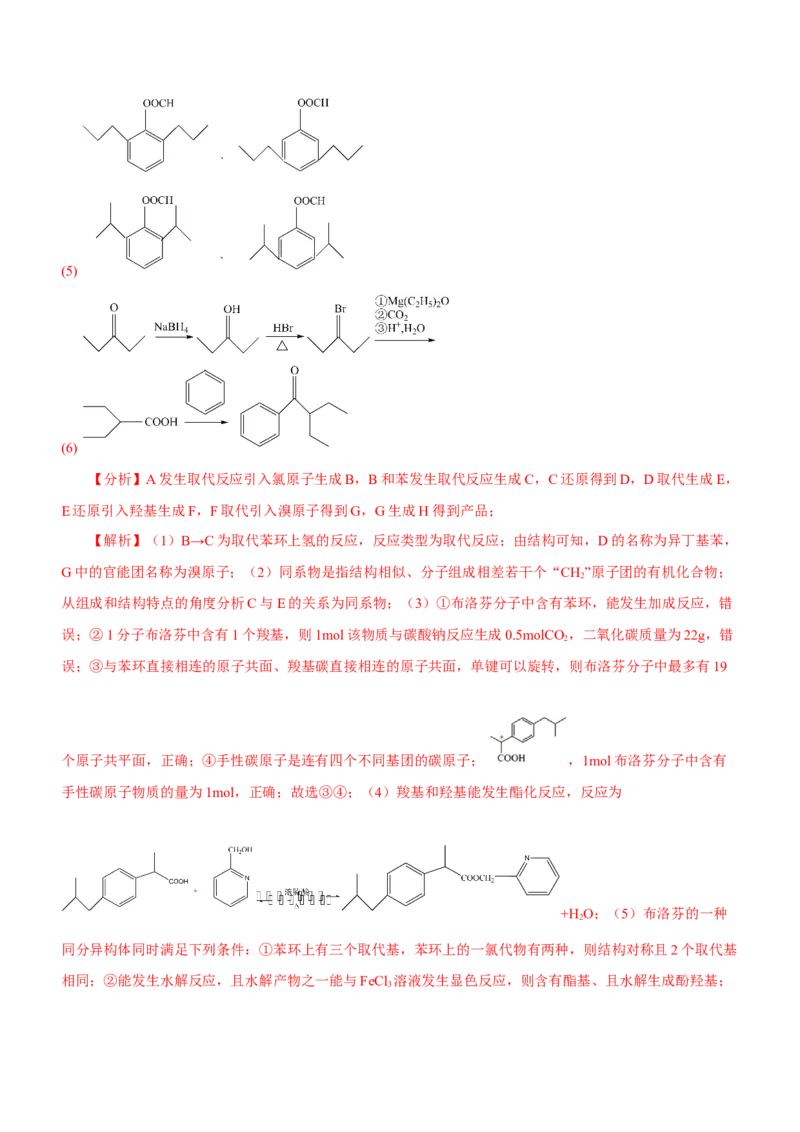
(1)B→C的反应类型为_______,D的名称为_______,G中的官能团名称为_______。
(2)从组成和结构特点的角度分析C与E的关系为_______。
(3)下列有关布洛芬的叙述正确的是_______。
①能发生取代反应,不能发生加成反应
②1 该物质与碳酸钠反应生成44g
③布洛芬分子中最多有19个原子共平面
④1 布洛芬分子中含有手性碳原子物质的量为1
(4)口服布洛芬对胃、肠道有刺激,用 对布洛芬进行成酯修饰,能有效改善这种状况,发生反应
的化学方程式是_______。
(5)布洛芬的一种同分异构体同时满足下列条件,写出该同分异构体的结构简_______。
①苯环上有三个取代基,苯环上的一氯代物有两种
②能发生水解反应,且水解产物之一能与 溶液发生显色反应
③能发生银镜反应
(6) 请写出以 和 为原料制备 的合成路线流程图(无机试剂和有机溶剂任选,合
成路线流程图示例见本题题干)_______。
【答案】(1) 取代反应 异丁基苯 溴原子 (2)互为同系物 (3)③④
(4) +H O
2(5)
(6)
【分析】A发生取代反应引入氯原子生成B,B和苯发生取代反应生成C,C还原得到D,D取代生成E,
E还原引入羟基生成F,F取代引入溴原子得到G,G生成H得到产品;
【解析】(1)B→C为取代苯环上氢的反应,反应类型为取代反应;由结构可知,D的名称为异丁基苯,
G中的官能团名称为溴原子;(2)同系物是指结构相似、分子组成相差若干个“CH”原子团的有机化合物;
2
从组成和结构特点的角度分析C与E的关系为同系物;(3)①布洛芬分子中含有苯环,能发生加成反应,错
误;②1分子布洛芬中含有1个羧基,则1mol该物质与碳酸钠反应生成0.5molCO,二氧化碳质量为22g,错
2
误;③与苯环直接相连的原子共面、羧基碳直接相连的原子共面,单键可以旋转,则布洛芬分子中最多有19
个原子共平面,正确;④手性碳原子是连有四个不同基团的碳原子; ,1mol布洛芬分子中含有
手性碳原子物质的量为1mol,正确;故选③④;(4)羧基和羟基能发生酯化反应,反应为
+H O;(5)布洛芬的一种
2
同分异构体同时满足下列条件:①苯环上有三个取代基,苯环上的一氯代物有两种,则结构对称且2个取代基
相同;②能发生水解反应,且水解产物之一能与FeCl 溶液发生显色反应,则含有酯基、且水解生成酚羟基;
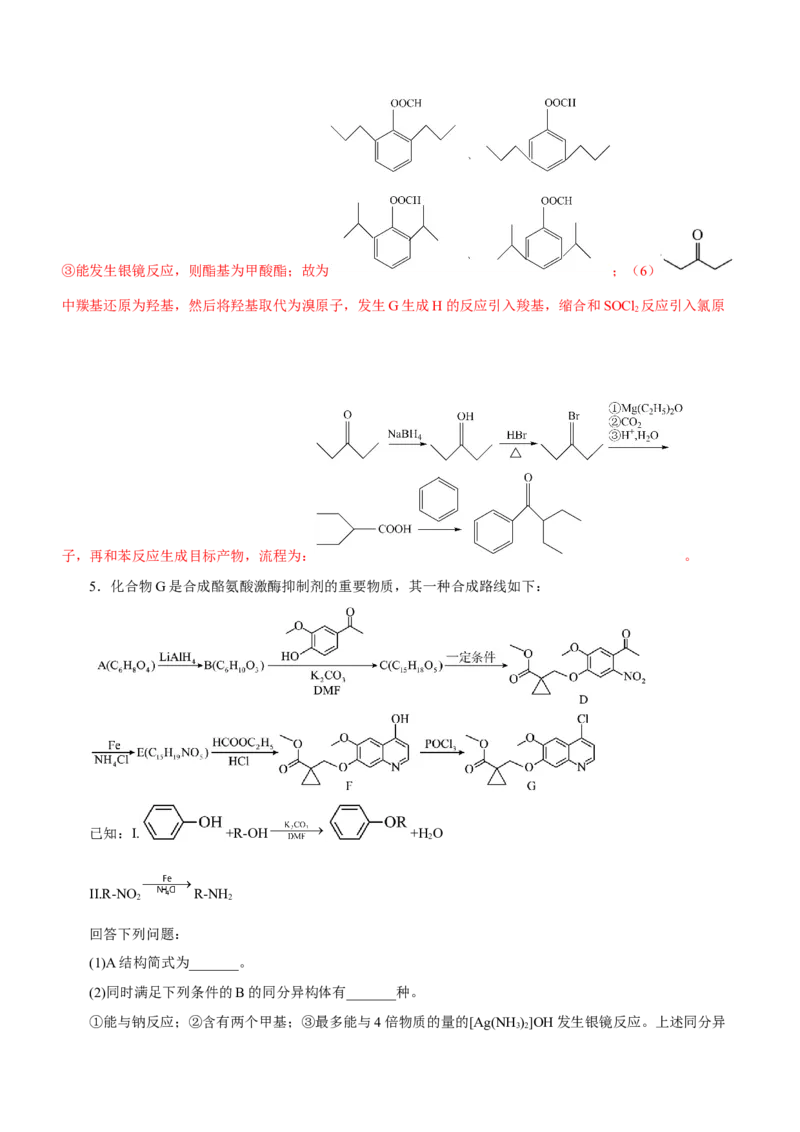
3③能发生银镜反应,则酯基为甲酸酯;故为 ;(6)
中羰基还原为羟基,然后将羟基取代为溴原子,发生G生成H的反应引入羧基,缩合和SOCl 反应引入氯原
2
子,再和苯反应生成目标产物,流程为: 。
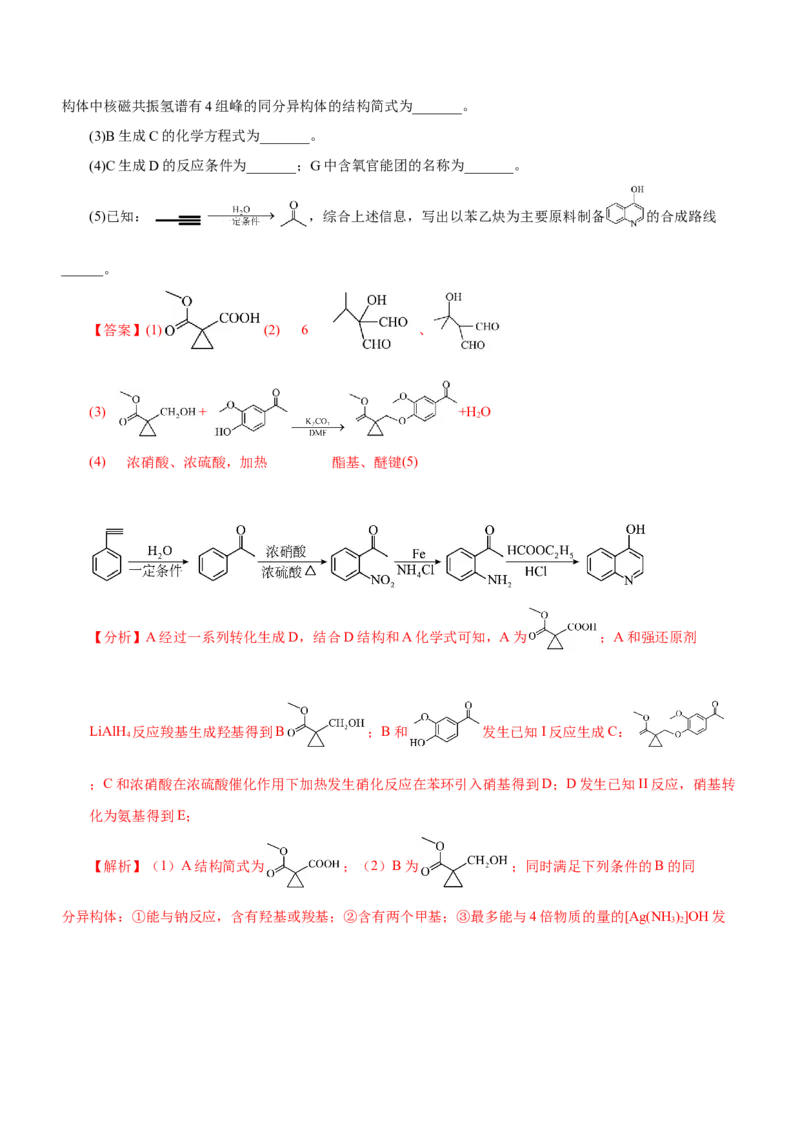
5.化合物G是合成酪氨酸激酶抑制剂的重要物质,其一种合成路线如下:
已知:I. +R-OH +H O
2
II.R-NO R-NH
2 2
回答下列问题:
(1)A结构简式为_______。
(2)同时满足下列条件的B的同分异构体有_______种。
①能与钠反应;②含有两个甲基;③最多能与4倍物质的量的[Ag(NH)]OH发生银镜反应。上述同分异
3 2构体中核磁共振氢谱有4组峰的同分异构体的结构简式为_______。
(3)B生成C的化学方程式为_______。
(4)C生成D的反应条件为_______;G中含氧官能团的名称为_______。
(5)已知: ,综合上述信息,写出以苯乙炔为主要原料制备 的合成路线
______。
【答案】(1) (2) 6 、
(3) + +H O
2
(4) 浓硝酸、浓硫酸,加热 酯基、醚键(5)
【分析】A经过一系列转化生成D,结合D结构和A化学式可知,A为 ;A和强还原剂
LiAlH 反应羧基生成羟基得到B ;B和 发生已知I反应生成C:
4
;C和浓硝酸在浓硫酸催化作用下加热发生硝化反应在苯环引入硝基得到D;D发生已知II反应,硝基转
化为氨基得到E;
【解析】(1)A结构简式为 ;(2)B为 ;同时满足下列条件的B的同
分异构体:①能与钠反应,含有羟基或羧基;②含有两个甲基;③最多能与4倍物质的量的[Ag(NH)]OH发
3 2生银镜反应,则含有2个醛基,而与钠反应的只能为羟基;结构可以为: 、 、
、 、 、 共6钟;上述同分异构体中核磁共振氢谱有4
组峰的同分异构体的结构简式为 、 ;(3)由分析可知,B生成C的化学方程式为
+ +H O;(4)C和浓硝酸在浓硫酸催化作用下加热发生硝
2
化反应在苯环引入硝基得到D,故反应条件为:浓硝酸、浓硫酸,加热;由G结构可知,G中含氧官能团的名
称为酯基、醚键;(5)苯乙炔和水在一定条件下生成酮羰基,再发生C生成D的反应引入硝基,硝基还原为
氨基,发生E生成F的反应得到产物,反应为:
。
6.褪黑素是由松果体产生的一种胺类激素,在调节昼夜节律及睡眠-觉醒方面发挥重要作用。某研究小组
以乙炔为原料,设计合成路线如下(部分反应条件已省略):已知:
①褪黑素结构为:
②
③无水乙酸钠在碱石灰作用下发生反应:
回答下列问题:
(1)A的名称为_______;B→C的反应类型为_______。
(2)D中所含官能团的名称为_______;E的结构简式为_______。
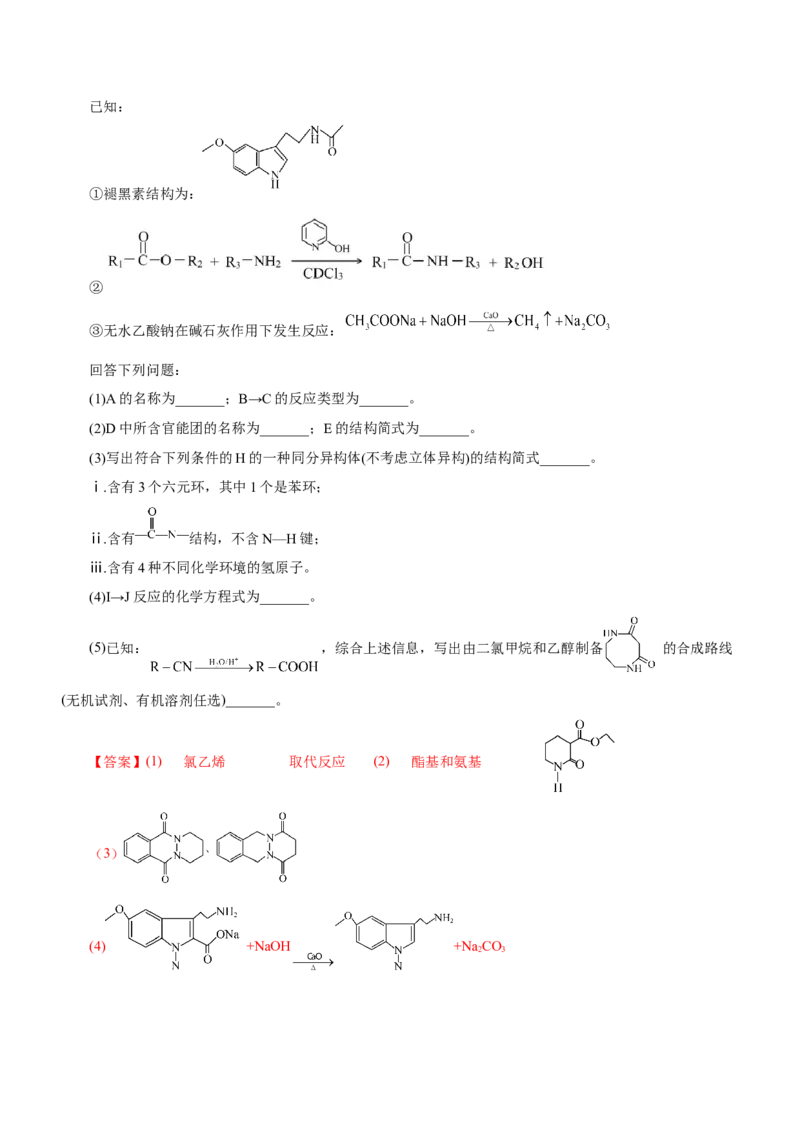
(3)写出符合下列条件的H的一种同分异构体(不考虑立体异构)的结构简式_______。
ⅰ.含有3个六元环,其中1个是苯环;
ⅱ.含有 结构,不含N—H键;
ⅲ.含有4种不同化学环境的氢原子。
(4)I→J反应的化学方程式为_______。
(5)已知: ,综合上述信息,写出由二氯甲烷和乙醇制备 的合成路线
(无机试剂、有机溶剂任选)_______。
【答案】(1) 氯乙烯 取代反应 (2) 酯基和氨基
(3)
(4) +NaOH +Na CO
2 3(5)
【分析】HC≡CH和HCl在HgCl 催化下生成A结合A的分子式可知,A为CH=CHCl,A和NaCN发生
2 2
取代反应生成B,结合B的分子式可知,B为CH=CHCN,B和M发生加成反应生成D,根据D的结构简式
2
及M的分子式知,M为 ,C和氢气发生加成反应生成D,D比C多4个氢原子,则C
中-C≡N完全和氢气发生加成反应,则D为 ,D发生取代反应生成E,E发生水解反应然后酸
化得到F,根据F的结构简式及E的分子式知,E为 , H发生水解反应生成I,根据I的化学式
知,I为 ,I和碱石灰反应生成J,J发生取代反应生成褪黑素,则J为 ;
(5)以二氯甲烷和乙醇为原料合成有机物 ,二氯甲烷和NaCN发生取代反应生成NCCH CN,
2
NCCH CN和氢气发生加成反应生成HNCH CHCHNH ,NCCH CN发生水解反应生成HOOCCH COOH,
2 2 2 2 2 2 2 2
CHCHOH和HOOCCH COOH发生转化反应得到CHCHOOCCH COOCH CH,
3 2 2 3 2 2 2 3
CHCHOOCCH COOCH CH 和HNCH CHCHNH 发生取代反应得到目标产物,据此分析解题。
3 2 2 2 3 2 2 2 2 2
【解析】(1)由分析可知,A的结构简式为:CH=CHCl,则名称为氯乙烯,B→C即CH=CHCl+NaCN
2 2
CH=CHCN+NaCl,该反应的反应类型为取代反应,故答案为:氯乙烯;取代反应;(2)由分析可知,
2D的结构简式为: ,故D中所含官能团的名称为酯基和氨基,E的结构简式为 ;
(3)H的同分异构体符合下列条件:ⅰ.含有3个六元环,其中1个是苯环;ⅱ.含有 结构,不含N—H
键;ⅲ.含有4种不同化学环境的氢原子,结构对称,符合条件的结构简式有 ;(4)由
分析可知,I的结构简式为: ,J的结构简式为: ,结合已知信息③可知,
I→J反应的化学方程式为 +NaOH +Na CO;(5)以二氯甲烷和乙醇为
2 3
原料合成有机物 ,二氯甲烷和NaCN发生取代反应生成NCCH CN,NCCH CN和氢气发生加成反应生
2 2
成HNCH CHCHNH ,NCCH CN发生水解反应生成HOOCCH COOH,CHCHOH和HOOCCH COOH发生
2 2 2 2 2 2 2 3 2 2
转化反应得到CHCHOOCCH COOCH CH,CHCHOOCCH COOCH CH 和HNCH CHCHNH 发生取代反
3 2 2 2 3 3 2 2 2 3 2 2 2 2 2
应得到目标产物,由此确定合成路线如下:
。
7.2022年1月1日,曾经的天价抗癌药泊马度胺(K)被正式纳入国家医保目录,为癌症患者带来了希望。其合成路线如下(部分条件已省略):
已知:① ,Boc O的结构简式为 ,
2
可用—Boc代表
②
③ ,Fe的产物为Fe2+
回答下列问题:
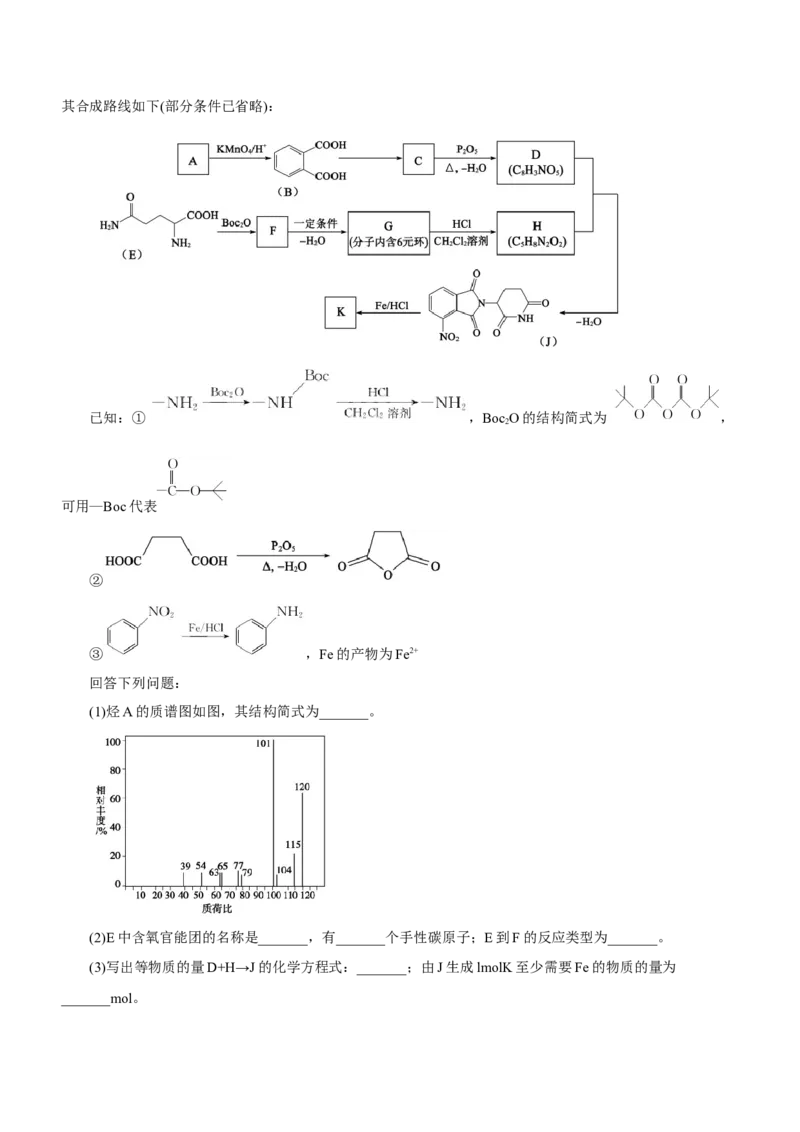
(1)烃A的质谱图如图,其结构简式为_______。
(2)E中含氧官能团的名称是_______,有_______个手性碳原子;E到F的反应类型为_______。
(3)写出等物质的量D+H→J的化学方程式:_______;由J生成lmolK至少需要Fe的物质的量为
_______mol。(4)满足下列要求的B的芳香族同分异构体共有_______种;其中核磁共振氢谱中4个峰的分子结构简式为
_______。
①能发生银镜反应;②与NaHCO 反应有气体产生
3
(5)如下流程可制备化合物M( ):
则:试剂b为_______。
【答案】(1) (2) 羧基、羰基 1 取代反应
(4) + → +H O 3 (4) 13
2
(5)
【分析】A可以被酸性高锰酸钾溶液氧化成 ,且A的相对分子质量是106,可以推知A为
,D和H发生脱水的聚合反应生成 ,结合D、H的分子式可知,D为 ,H
为 ,C发生信息②的反应生成D,则C为 ,E通过信息①的反应生成F,F脱水生成G,G发生信息①的反应生成 ,可以推知G为 ,F为 以此
解答
【解析】(1)由分析可知,A的结构简式为 。(2)由E的结构简式可知,E中含氧官能团的
名称是羧基、羰基;连接四个不同原子或基团的碳原子,称为手性碳原子,E中有1个手性碳原子,由分析可
知,E到F的反应类型为取代反应。(3)D和H发生脱水的聚合反应生成 ,反应方程式
为: + → +H O;由信息③可知,把J中的硝基转化为氨基过程
2
中,N元素化合价由+3价下降到-3价,产物Fe以Fe2+形式存在,由J生成1molK至少需要Fe物质的量为
3mol。(4)B的芳香族同分异构体,满足条件①能发生银镜反应,说明其中含有醛基或甲酸酯结构;②与
NaHCO 反应有气体产生,说明其中含有-COOH;苯环上取代基可能的组合为-COOH、-OOCH,-COOH、-
3
OH、-CHO,满足条件的同分异构体共有13种,其中核磁共振氢谱中4个峰的分子结构简式为 。(5)
路线I中反应中的氨基和羧基也可能发生脱水缩合反应导致有副产物产生,结合信息①可以先将
中的氨基转化为 后在和 反应,最后再将 转化为氨基即可。
8.有机物G能用于合成多种药物和农药,下面是G的一种合成路线如图:已知:
① (苯胺,呈碱性,易被氧化)
②苯胺和甲基吡啶( )互为同分异构体,并具有芳香性
回答下列问题:
(1)A的名称为_____;C中官能团的名称为_____。
(2)③的化学方程式为_____,反应类型为_____。
(3)E的结构简式为_____,1molE在反应⑤过程中最多消耗_____molNaOH。
(4)G的芳香性同系物M的分子式为C H ON,满足下列条件的M有_____种,写出其中一种同分异构体
11 13 4
的结构简式:_____。
①分子结构中含一个六元环,且环上一氯代物只有一种
②1mol该物质与足量NaHCO 反应生成2molCO
3 2
③磁共振氢谱有4组峰,峰面积之比为6∶4∶2∶1
(6) 已知:苯环上有烷烃基时,新引入的取代基连在苯环的邻、对位:苯环上有羧基时,新引入的取代基
连在苯环的间位。根据题中的信息,设计以甲苯为原料合成有机物 的流程图(无机试剂任
选)______。
【答案】(1) 3-甲基苯酚 羧基和酯基(2) +HNO
3+H O 取代反应 (3) 3
2
(4) 4
(5)
【分析】由题干流程图可知,A和乙酰氯反应生成 和HCl,则A为 ,C(
硝化反应生成D( ),D在Fe/ HCl条件下还原为E,由已知信息①可知E为
,E先在NaOH溶液中水解再酸化得到F ,据此分析解答。
【解析】(1)由分析可知A为 ,其名称为3-甲基苯酚;由C的结构式可知,含有官能团的名称
为羧基和酯基;(2)过程③是 硝化反应生成D,其化学方程式为 +HNO
3+H O,其反应类型为取代反应;(3)由分析可知E的结构简式为
2
;E中存在羧基和酯基,并且酯基水解后生成乙酸和酚羟基,所以1molE在反应⑤过程中
最多消耗3mol NaOH;(4)M的分子式为C H ON, 1mol该物质与足量NaHCO 反应生成2molCO ,表明
11 13 4 3 2
该物质含有两个羧基,磁共振氢谱有4组峰,峰面积之比为6∶4∶2∶1,表明该物质有四种环境的H,个数比为
6∶4∶2∶1,并且该分子结构中含一个六元环,且环上一氯代物只有一种,则满足条件的M有4种,分别为
、 、 、 ;
(5) 和浓硝酸在浓硫酸、加热条件下发生取代反应生成 , 被酸性高锰酸钾氧化
为 , 被Fe和HCl还原为 ,则合成路线为
。
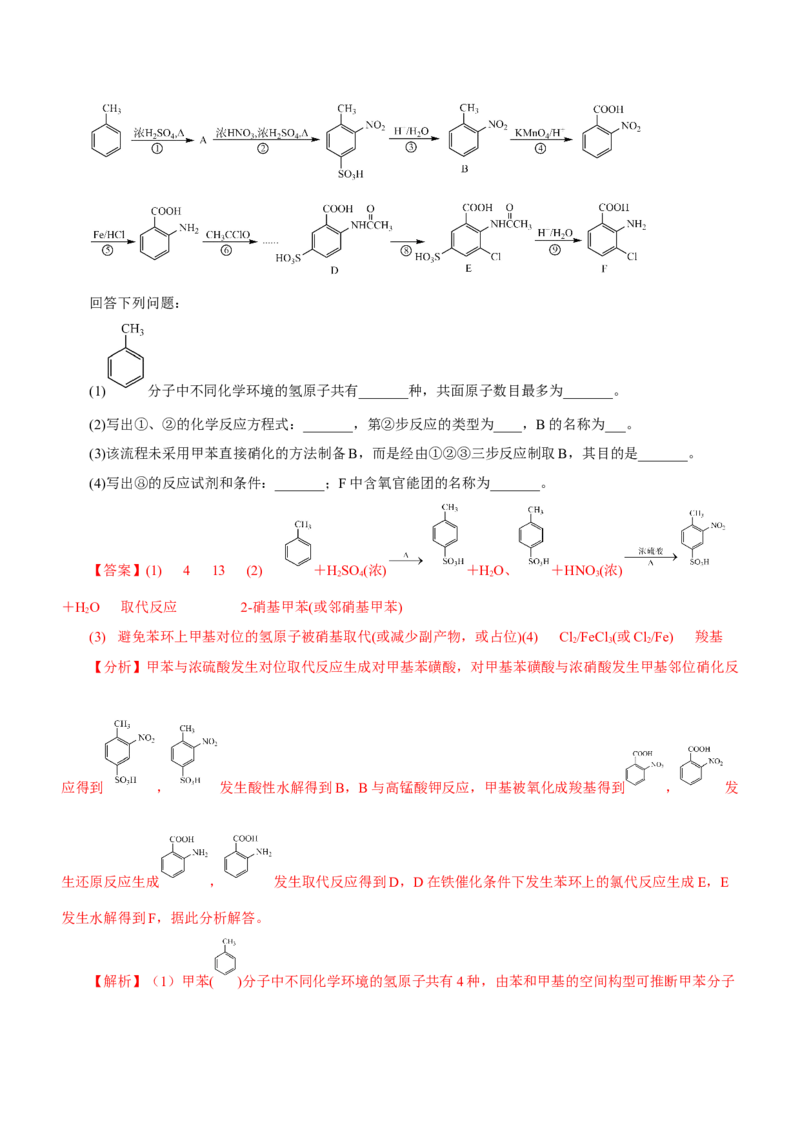
9.2-氨基-3-氯苯甲酸(F)是重要的医药中间体,其制备流程图如下:
已知:回答下列问题:
(1) 分子中不同化学环境的氢原子共有_______种,共面原子数目最多为_______。
(2)写出①、②的化学反应方程式:_______,第②步反应的类型为____,B的名称为___。
(3)该流程未采用甲苯直接硝化的方法制备B,而是经由①②③三步反应制取B,其目的是_______。
(4)写出⑧的反应试剂和条件:_______;F中含氧官能团的名称为_______。
【答案】(1) 4 13 (2) +HSO (浓) +HO、 +HNO(浓)
2 4 2 3
+HO 取代反应 2-硝基甲苯(或邻硝基甲苯)
2
(3) 避免苯环上甲基对位的氢原子被硝基取代(或减少副产物,或占位)(4) Cl/FeCl (或Cl/Fe) 羧基
2 3 2
【分析】甲苯与浓硫酸发生对位取代反应生成对甲基苯磺酸,对甲基苯磺酸与浓硝酸发生甲基邻位硝化反
应得到 , 发生酸性水解得到B,B与高锰酸钾反应,甲基被氧化成羧基得到 , 发
生还原反应生成 , 发生取代反应得到D,D在铁催化条件下发生苯环上的氯代反应生成E,E
发生水解得到F,据此分析解答。
【解析】(1)甲苯( )分子中不同化学环境的氢原子共有4种,由苯和甲基的空间构型可推断甲苯分子中共面原子数目最多为13个。故答案为:4;13;(2)反应①为 与浓硫酸反应,结合 的结构可知
该步反应为甲基对位氢被磺酸基取代,反应方程式为: +HSO (浓) +HO;反应②为 与
2 4 2
浓硝酸的硝化反应得到 ,反应方程式为: +HNO(浓) +HO,该反应为硝化反
3 2
应也属于取代反应,由B的结构可知其名称为2-硝基甲苯(或邻硝基甲苯),故答案为: +HSO (浓)
2 4
+HO、 +HNO(浓) +HO;取代反应;2-硝基甲苯(或邻硝基甲苯);(3)由①②③
2 3 2
三步反应制取B的信息可知,若甲苯直接硝化,甲苯中甲基的邻位和对位均可发生硝化反应,有副产物生
成。(4)由D( )和F( )的结构简式可推知E中含有氯原子,苯环上引入氯原子的方法是在
Fe或FeCl 作催化剂的条件下与Cl 发生取代反应;F( )的含氧官能团为羧基。
3 2
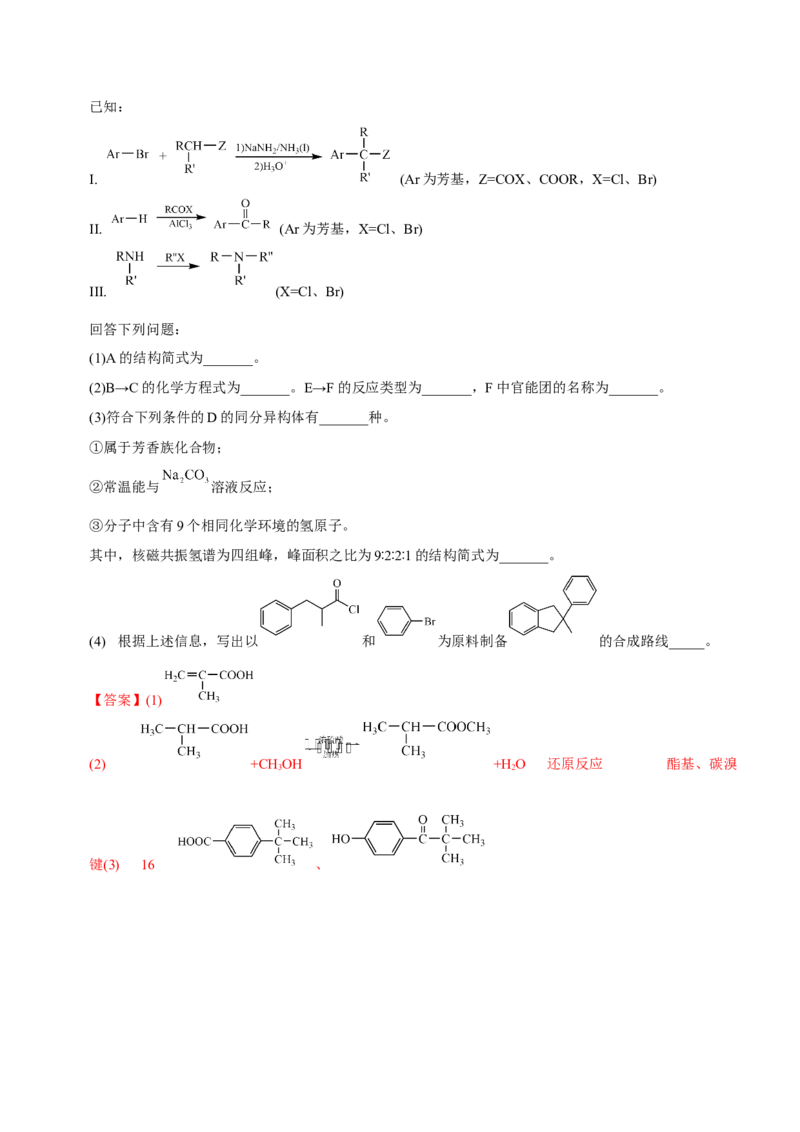
10.抗炎药物洛索洛芬钠中间体H的一种合成路线如下:已知:
I. (Ar为芳基,Z=COX、COOR,X=Cl、Br)
II. (Ar为芳基,X=Cl、Br)
III. (X=Cl、Br)
回答下列问题:
(1)A的结构简式为_______。
(2)B→C的化学方程式为_______。E→F的反应类型为_______,F中官能团的名称为_______。
(3)符合下列条件的D的同分异构体有_______种。
①属于芳香族化合物;
②常温能与 溶液反应;
③分子中含有9个相同化学环境的氢原子。
其中,核磁共振氢谱为四组峰,峰面积之比为9∶2∶2∶1的结构简式为_______。
(4) 根据上述信息,写出以 和 为原料制备 的合成路线_____。
【答案】(1)
(2) +CH OH +H O 还原反应 酯基、碳溴
3 2
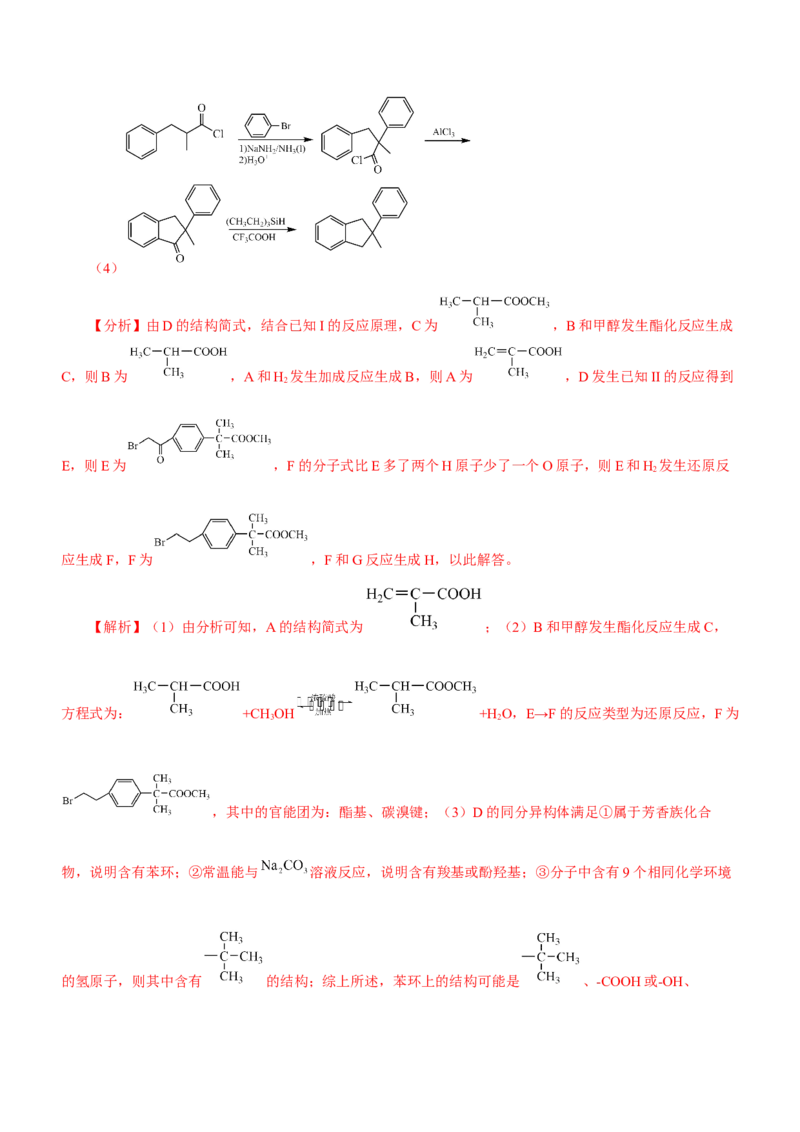
键(3) 16 、(4)
【分析】由D的结构简式,结合已知I的反应原理,C为 ,B和甲醇发生酯化反应生成
C,则B为 ,A和H 发生加成反应生成B,则A为 ,D发生已知II的反应得到
2
E,则E为 ,F的分子式比E多了两个H原子少了一个O原子,则E和H 发生还原反
2
应生成F,F为 ,F和G反应生成H,以此解答。
【解析】(1)由分析可知,A的结构简式为 ;(2)B和甲醇发生酯化反应生成C,
方程式为: +CH OH +H O,E→F的反应类型为还原反应,F为
3 2
,其中的官能团为:酯基、碳溴键;(3)D的同分异构体满足①属于芳香族化合
物,说明含有苯环;②常温能与 溶液反应,说明含有羧基或酚羟基;③分子中含有9个相同化学环境
的氢原子,则其中含有 的结构;综上所述,苯环上的结构可能是 、-COOH或-OH、或-OH、-CHO、 ,符合条件的D的同分异构体有16种,其中核磁共振氢谱为四组峰,
峰面积之比为9∶2∶2∶1的结构简式是对称的结构,可以是 、 ;(4)
和 发生已知I的反应生成 , 发生已知II的反应生成
, 发生加成反应得到 ,合成路线为:
。
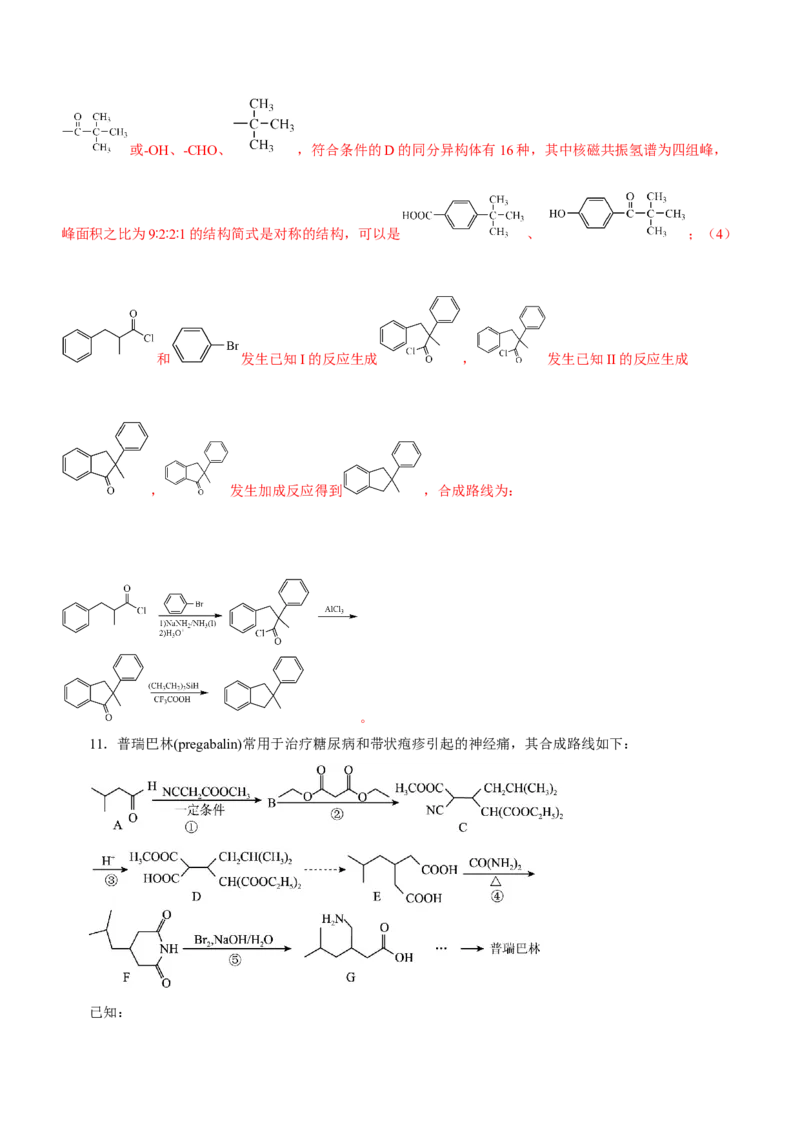
11.普瑞巴林(pregabalin)常用于治疗糖尿病和带状疱疹引起的神经痛,其合成路线如下:
已知:i.R CHO+R -CHCOOR +H O
1 2 2 2
ii.RCOOH+CO(NH ) RCONH +NH↑+CO ↑
2 2 2 3 2
回答下列问题:
(1)A的化学名称为_______。
(2)B的结构简式为_______。
(3)反应②的反应类型是_______。
(4)D中有_______个手性碳原子。
(5)写出反应④的化学方程式_______。
(6)H是G的同系物,其碳原子数比G少四个,则H可能的结构(不考虑立体异构)有_______种,其中-NH
2
在链端的有_______(写结构简式)。
【答案】(1)3-甲基丁醛或异戊醛 (2) (3)加成反应 (4)2
(5) +CO(NH) +CO ↑+NH ↑+H O
2 2 2 3 2
(6) 5 、
【分析】根据A的结构简式,A属于醛,按照系统命名的原则,该有机物A的名称为3-甲基丁醛;对比B
和C的结构简式,C中不含有碳碳双键,B→C的反应类型为加成反应,以此解题。
【解析】(1)根据A的结构简式,A属于醛,按照系统命名的原则,该有机物A的名称为3-甲基丁醛;
(2)对比A和C的结构简式,A与NCCH COOCH 发生已知(i)的反应,NCCH COOCH 中的亚甲基上C与醛
2 3 2 3
基上的碳原子以碳碳双键相连,同时生成水,则B的结构简式为 ;(3)对比B和C的结构
简式,C中不含有碳碳双键,B→C的反应类型为加成反应。(4)根据手性碳原子的定义,有机物D中含有的
手性碳原子有2个,即 ;(5)根据已知ii可知,反应④的反应方程式为+CO(NH) +CO ↑+NH ↑+H O;(6)H是G的同系物,碳原子比G少四个,即H中有四个碳原
2 2 2 3 2
子,与G具有相同的官能团,H中应含有氨基和羧基,H可能的结构简式为 ,结构简式还可
能是 ,结构简式还可能是 ,还可能是 ,有1种结构,还
可能是 ,共有5种;其中-NH 在链端的有: 、 。
2
12.有机物H是一种合成镇痛药的主要成分。某小组设计如图的合成路线:
已知:① (X为卤素原子,R为H或烃基,下同)
②
(1)A的化学名称为___________。
(2)B→C的反应类型为___________。
(3)D中含氧官能团的名称为___________。
(4)G与足量氢氧化钠溶液反应的化学方程式为___________。
(5)M是E的同分异构体,同时满足下列条件的M的结构有___________种(不考虑立体异构)。
①结构中含有氨基和羧基,只有1个苯环,无其他环状结构。
②核磁共振氢谱中有4组吸收峰,且峰面积之比为6∶2∶2∶1.(6)参照上述合成路线和信息,以 和有机化合物A为原料(无机试剂任选),设计制备 的合
成路线___________。
【答案】(1)对甲基苯酚 (2)加成反应 (3)酚羟基、酮羰基(4) +2NaOH→
+2H O (5)4
2
(6)
【分析】由A的分子式、C的结构简式,推知A为 ,A与 发生取代反应生成B,
B与HCHO发生加成反应生成C,故B为 ,由分子式可知,C中羟基被氯原子取代生成D,D中氯原子
被-CN取代生成E,E与CHCHO发生信息Ⅱ的反应生成F,F中-CN转化为-COOH而生成G,结合G的结构
3
简式,推知D为 、E为 、F为 ,G分子内脱去2个氢原子成环生成H;(6)
发生G→H的转化生成 , 发生消去反应生成 , 与
在催化剂条件下生成 ,据此分析解题。
【解析】(1)由分析可知,A的结构简式为 ,A的化学名称为对甲基苯酚;(2)由分析可
知,B→C是 与HCHO发生加成反应生成C即 ;(3)由分析可知,D为 ,D中所含官能团有碳氯键、酚羟基、酮羰基,其中含氧官能团为:酚羟基和酮羰基;(4)G与足量氢氧化钠反应的
化学方程式为 +2NaOH→ +2H O;(5)M是E( )的同分异构体,同时满
2
足下列条件的M的结构:①结构中含有氨基和羧基,只有1个苯环,无其他环状结构,说明存在1个三键或2
个双键,②核磁共振氢谱中有4组吸收峰,且峰面积之比为6:2:2:1,说明存在对称结构,且有2个化学环
境相同的甲基,-NH 、-C≡CCOOH处于对位,2个甲基均与-NH 或-C≡CCOOH相邻,-COOH、-C≡CNH 处于
2 2 2
对位,2个甲基均与-COOH或-C≡CNH 相邻,符合条件的同分异构体共有4种;(6) 发生G→H的转
2
化生成 , 发生消去反应生成 , 与 在催化剂条件下生成
,故该合成路线为: 。
13.化合物H是用于治疗慢性阻塞性肺病奥达特罗的合成中间体,其合成路线如下:
已知:Ⅰ. 代表
Ⅱ.
回答下列问题:
(1)A的名称为_______;B中官能团的名称为_______;(2)D→E的反应类型为_______,反应⑤条件中 的作用是_______;
(3)有机物M的分子式为 ,则M→H的反应方程式为_______;
(4)有机物N是反应②过程中的副产物,其分子式为 ,则N的结构简式为;_______;
(5)设计以苯酚和光气(COCl )为原料合成 的合成路线。______
2
【答案】(1) 对苯二酚(或1,4-苯二酚) 羟基(酚羟基)、羰基(酮基)(2) 还原反应 与生成
的HCl反应,促进平衡正向移动,提高原料利用率 (3) +NaOH
+NaBr+H O (4) (或写成: )
2
(5)
【分析】根据A生成B的反应条件可知该反应与信息Ⅱ类似,根据B的结构简式可知A应为 ;有机
物M的分子式为C H ONBr,而G的分子式为C H ONBr,可知G生成M的过程中发生了酮羰基与氢气的
17 16 4 17 14 4加成,所以M为 。
【解析】(1)A的结构简式为 ,有两个处于对位的酚羟基,所以名称为对苯二酚(或1,4-苯二
酚);根据B的结构简式可知其官能团为酚羟基、羰基;(2)对比D和E的结构简式可知D中硝基变为氨
基,应为还原反应;根据E和F的结构简式可知E生成F的过程为取代反应,反应过程中会有HCl生成,碳酸
钾可以与生成的HCl反应,促进平衡正向移动,提高原料利用率;(3)M的结构简式为
,该反应的化学方程式为 +NaOH
+NaBr+H O;(4)根据B、C的结构简式可知该过程中B中的一个酚羟基上的氢原子被取代,根据反应机理
2
和副产物的分子式可知,副产物应是两个酚羟基上的氢原子都被取代,所以N为 (或写成:
);(5)苯酚为 ,类比C生成F的过程可知由苯酚和光气(COCl )为原料
2合成 的路线为
。
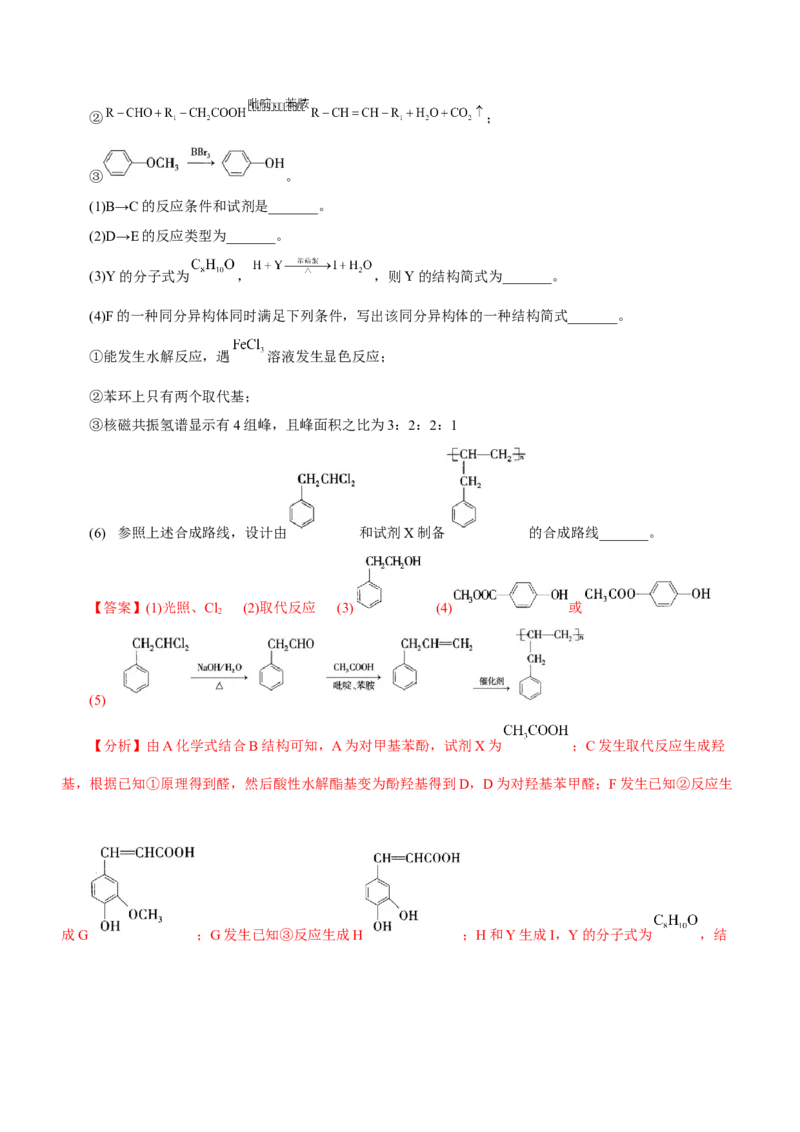
14.苯乙烯(A)是一种重要化工原料,以苯乙烯为原料可以制备一系列化工产品,如图所示。
请回答下列问题:
(1)E中所含官能团的名称是_______,B→C的反应类型是_______。
(2)在溴的四氯化碳溶液中加入过量的A,观察到的现象是_______。
(3)D→E的副产物是 ,生成1 mol E至少需要_______g 。
(4)在浓硫酸作用下,E与足量 反应的化学方程式为_______。
(5)下列说法正确的是_______(填标号)。
a.A能发生加成反应
b.C、D、E中均只有一种官能团
c.F能使溴的四氯化碳溶液褪色
(6)F的同分异构体中,含六元环的结构有_______(不包括立体异构体和F本身)种。
【答案】(1) 羟基 取代反应 (2)溴的四氯化碳溶液褪色 (3)120
(4) (5)ab (6)4
【分析】A是苯乙烯,和氢气加成生成环烷烃F;A和溴加成生成卤代烃B,B发生苯环上的取代反应生
成C,C和氢气加成生成D,D发生水解生成醇E。【解析】(1)E中官能团的为羟基, 为苯环上的H原子被Br原子取代,反应类型为取代反应;
(2)A中含有碳碳双键,加入过量的溴的四氯化碳溶液,A和溴发生加成反应,所以溴的四氯化碳溶液褪
色;(3) 是卤代烃发生的水解反应,1molD中含有3molBr原子,水解消耗3mol的 ,质量为
120g;(4)在浓硫酸作用下,E与足量 发生酯化反应,化学方程式为:
;(5)a.A中含有苯环和碳碳双键,能
发生加成反应,a正确;b.C和D中只含有溴原子,E中只含有羟基,均只有一种官能团,b正确;c.F中没
有碳碳双键,不能使溴的四氯化碳溶液褪色;故选ab。(6)F为 ,含六元环的结构有:
, , 和 ,共4种。
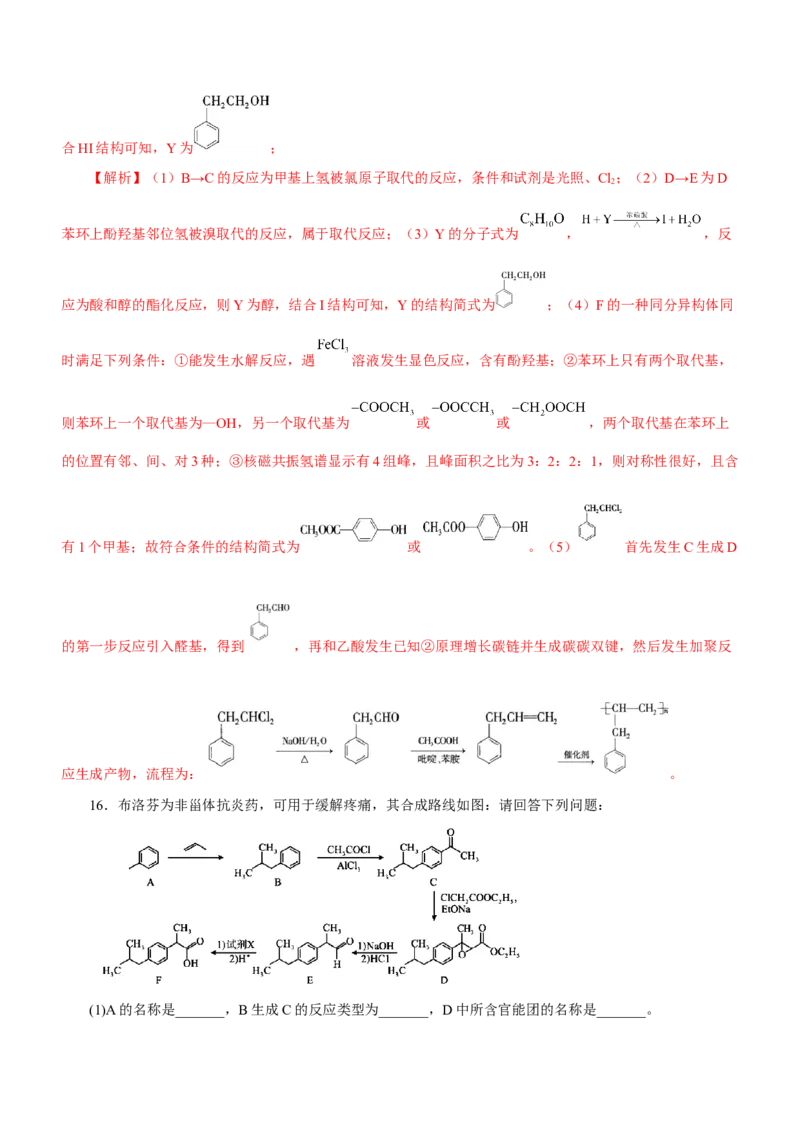
15.由芳香化合物A制备药物中间体Ⅰ的一种合成路线如下:
已知:①同一碳原子上连两个羟基不稳定,发生反应: +H O;
2② ;
③ 。
(1)B→C的反应条件和试剂是_______。
(2)D→E的反应类型为_______。
(3)Y的分子式为 , ,则Y的结构简式为_______。
(4)F的一种同分异构体同时满足下列条件,写出该同分异构体的一种结构简式_______。
①能发生水解反应,遇 溶液发生显色反应;
②苯环上只有两个取代基;
③核磁共振氢谱显示有4组峰,且峰面积之比为3:2:2:1
(6) 参照上述合成路线,设计由 和试剂X制备 的合成路线_______。
【答案】(1)光照、Cl (2)取代反应 (3) (4) 或
2
(5)
【分析】由A化学式结合B结构可知,A为对甲基苯酚,试剂X为 ;C发生取代反应生成羟
基,根据已知①原理得到醛,然后酸性水解酯基变为酚羟基得到D,D为对羟基苯甲醛;F发生已知②反应生
成G ;G发生已知③反应生成H ;H和Y生成I,Y的分子式为 ,结合HI结构可知,Y为 ;
【解析】(1)B→C的反应为甲基上氢被氯原子取代的反应,条件和试剂是光照、Cl;(2)D→E为D
2
苯环上酚羟基邻位氢被溴取代的反应,属于取代反应;(3)Y的分子式为 , ,反
应为酸和醇的酯化反应,则Y为醇,结合I结构可知,Y的结构简式为 ;(4)F的一种同分异构体同
时满足下列条件:①能发生水解反应,遇 溶液发生显色反应,含有酚羟基;②苯环上只有两个取代基,
则苯环上一个取代基为—OH,另一个取代基为 或 或 ,两个取代基在苯环上
的位置有邻、间、对3种;③核磁共振氢谱显示有4组峰,且峰面积之比为3:2:2:1,则对称性很好,且含
有1个甲基;故符合条件的结构简式为 或 。(5) 首先发生C生成D
的第一步反应引入醛基,得到 ,再和乙酸发生已知②原理增长碳链并生成碳碳双键,然后发生加聚反
应生成产物,流程为: 。
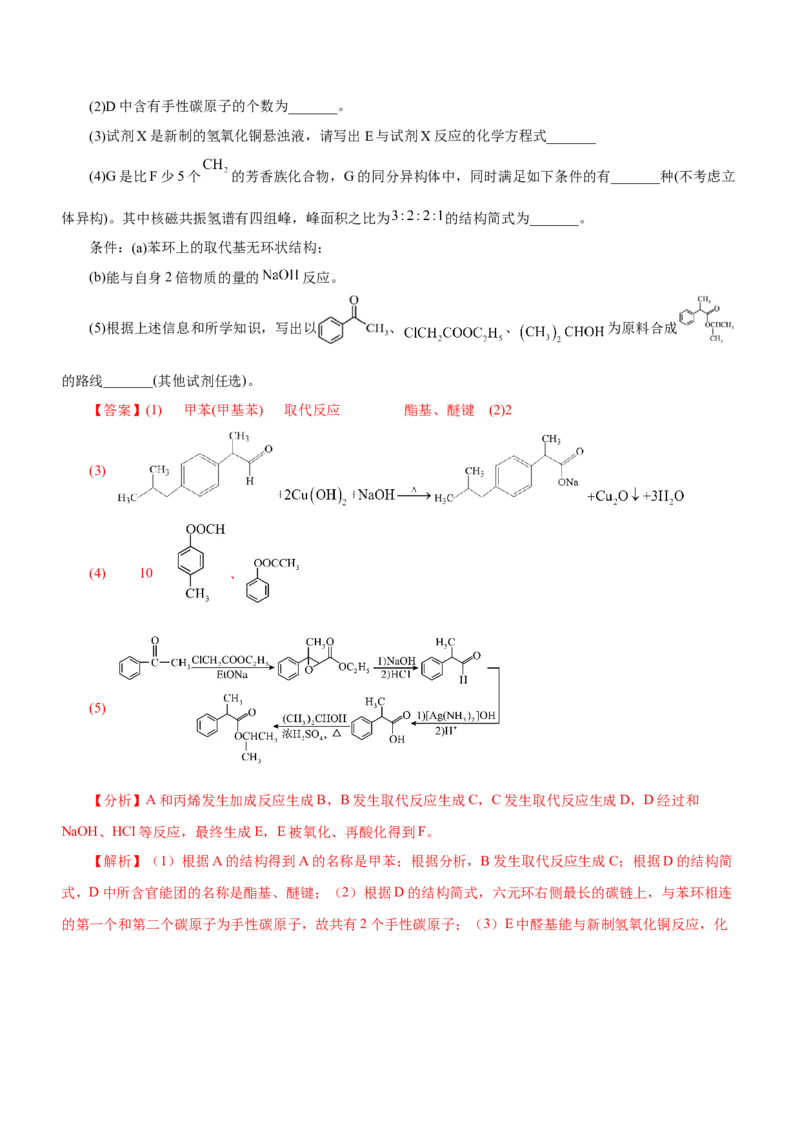
16.布洛芬为非甾体抗炎药,可用于缓解疼痛,其合成路线如图:请回答下列问题:
(1)A的名称是_______,B生成C的反应类型为_______,D中所含官能团的名称是_______。(2)D中含有手性碳原子的个数为_______。
(3)试剂X是新制的氢氧化铜悬浊液,请写出E与试剂X反应的化学方程式_______
(4)G是比F少5个 的芳香族化合物,G的同分异构体中,同时满足如下条件的有_______种(不考虑立
体异构)。其中核磁共振氢谱有四组峰,峰面积之比为 的结构简式为_______。
条件:(a)苯环上的取代基无环状结构;
(b)能与自身2倍物质的量的 反应。
(5)根据上述信息和所学知识,写出以 、 、 为原料合成
的路线_______(其他试剂任选)。
【答案】(1) 甲苯(甲基苯) 取代反应 酯基、醚键 (2)2
(3)
(4) 10 、
(5)
【分析】A和丙烯发生加成反应生成B,B发生取代反应生成C,C发生取代反应生成D,D经过和
NaOH、HCl等反应,最终生成E,E被氧化、再酸化得到F。
【解析】(1)根据A的结构得到A的名称是甲苯;根据分析,B发生取代反应生成C;根据D的结构简
式,D中所含官能团的名称是酯基、醚键;(2)根据D的结构简式,六元环右侧最长的碳链上,与苯环相连
的第一个和第二个碳原子为手性碳原子,故共有2个手性碳原子;(3)E中醛基能与新制氢氧化铜反应,化学方程式为; ;
(4)G是比F少5个CH 的芳香族化合物,则G含有8个碳原子,F为酸,根据苯环上的取代基无环状结构;
2
能与自身2倍物质的量的NaOH反应,说明G的同分异构体中含有酚酸酯和甲基,或者是两个酚羟基和一个
−CH=CH,或者是−OOCCH ;当是酚酸酯和甲基时,有邻、间、对三种;当是两个酚羟基和一个−CH=CH
2 3 2
时,两个酚羟基在邻位,有2种结构,当两个酚羟基在间位,有3种结构,当两个酚羟基在对位,有1种结
构;当是−OOCCH 时,有1种结构,因此G的同分异构体中,同时满足条件的有10种;其中核磁共振氢谱有
3
四组峰,峰面积之比为3:2:2:1的结构简式为 、 ;(5) 与ClCH COOC H 在
2 2 5
EtONa作用下反应生成 , 在第一步NaOH,第二步HCl作用下生成
, 在银氨溶液作用下反应、再酸化生成 , 和(CH)CHOH在浓硫酸作用下发生
3 2
酯化反应生成 ,其合成路线为: 。
1. (2022·湖南卷)物质J是一种具有生物活性的化合物。该化合物的合成路线如下:已知:① + ;
②
回答下列问题:
(1)A中官能团的名称为_______、_______;
(2)F→G、G→H的反应类型分别是_______、_______;
(3)B的结构简式为_______;
(4)C→D反应方程式为_______;
(5) 是一种重要的化工原料,其同分异构体中能够发生银镜反应的有_______种(考虑立体异
构),其中核磁共振氢谱有3组峰,且峰面积之比为 的结构简式为_______;
(6)Ⅰ中的手性碳原子个数为_______(连四个不同的原子或原子团的碳原子称为手性碳原子);
(7)参照上述合成路线,以 和 为原料,设计合成 的路线_______(无机试剂任
选)。【答案】(1)醚键 醛基 (2)取代反应 加成反应 (3)
(4) (5)5
(6)1 (7)
【解析】A( )和 反应生成B(C H O),根据“已知①”可以推出
12 14 4
B的结构简式为 ;B和HCOONH 发生反应得到C(C H O),C又转化为D
4 12 16 4
(C O O),根据“已知②”可推出C的结构简式为 ,D的结构简式为
12 14 3
;D和HOCH CHOH反应生成E( );E在一定条件下转化为F( );
2 2
F和CHI在碱的作用下反应得到G(C H O),G和 反应得到H( ),对比F和H
3 15 18 5的结构简式可得知G的结构简式为 ;H再转化为I( );I最终转化为J(
)。
(1)A的结构简式为 ,其官能团为醚键和醛基。
(2)由分析可知,G的结构简式为 ,对比F和G的结构简式可知F→G的反应为取代反
应;G→H反应中, 的碳碳双键变为碳碳单键,则该反应为加成反应。
(3)由分析可知,B的结构简式为 。
(4)由分析可知,C、D的结构简式分别为C的结构简式为 、 ,则C→D的
化学方程式为 。
(5) 的同分异构体能发生银镜反应,说明该物质含有醛基,根据分子式C HO可得知,该物质
4 6
还含有碳碳双键或者三元环,还要分析顺反异构,则符合条件的同分异构体有5种,它们分别是
CH=CHCHCHO、 (与后者互为顺反异构体)、 (与前者互为顺反异构体)、 和
2 2
,其中核磁共振氢谱有3组峰,且峰面积之比为4:1:1的结构简式是 。
(6)连四个不同的原子或原子团的碳原子成为手性碳原子,则I中手性碳原子的个数为1,是连有甲基的
碳原子。(7)结合G→I的转化过程可知,可先将 转化为 ,再使 和 反应生成
,并最终转化为 ;综上所述,合成路线为:
。
2.(2022·江苏卷)化合物G可用于药用多肽的结构修饰,其人工合成路线如下:
(1)A分子中碳原子的杂化轨道类型为_______。
(2)B→C的反应类型为_______。
(3)D的一种同分异构体同时满足下列条件,写出该同分异构体的结构简式:_______。
①分子中含有4种不同化学环境的氢原子;②碱性条件水解,酸化后得2种产物,其中一种含苯环且有2
种含氧官能团,2种产物均能被银氨溶液氧化。
(4)F的分子式为 ,其结构简式为_______。
(5)已知: (R和 表示烃基或氢, 表示烃基);
写出以 和 为原料制备 的合成路线流程图(无机试剂和有机溶剂任用,合成路线流程图示例见本题题干)_______。
【答案】(1)sp2和sp3
(2)取代反应 (3)
(4) (5)
【解析】A( )和CHI发生取代反应生成B( );B和SOCl 发
3 2
生取代反应生成C( );C和CHOH发生取代反应生成D( );D
3
和NH OH发生反应生成E( );E经过还原反应转化为F,F再转化为G,其中F和
2
G的分子式都是C H NO ,则F为 ,F和G互为手性异构体。
12 17 2
(1)A分子中,苯环上的碳原子和双肩上的碳原子为sp2杂化,亚甲基上的碳原子为sp3杂化,即A分子
中碳原子的杂化轨道类型为sp2和sp3。(2)B→C的反应中,B中的羟基被氯原子代替,该反应为取代反应。
(3)D的分子式为C H O,其一种同分异构体在碱性条件水解,酸化后得2种产物,其中一种含苯环
12 14 3
且有2种含氧官能团,2种产物均能被银氨溶液氧化,说明该同分异构体为酯,且水解产物都含有醛基,则水
解产物中,有一种是甲酸,另外一种含有羟基和醛基,该同分异构体属于甲酸酯;同时,该同分异构体分子中
含有4种不同化学环境的氢原子,则该同分异构体的结构简式为 。
(4)由分析可知,F的结构简式为 。
(5)根据已知的第一个反应可知, 与CHMgBr反应生成 , 再被氧化为
3
,根据已知的第二个反应可知, 可以转化为 ,根据流程图中D→E的反应可知, 和
NH OH反应生成 ;综上所述, 的合成路线为:
2
。
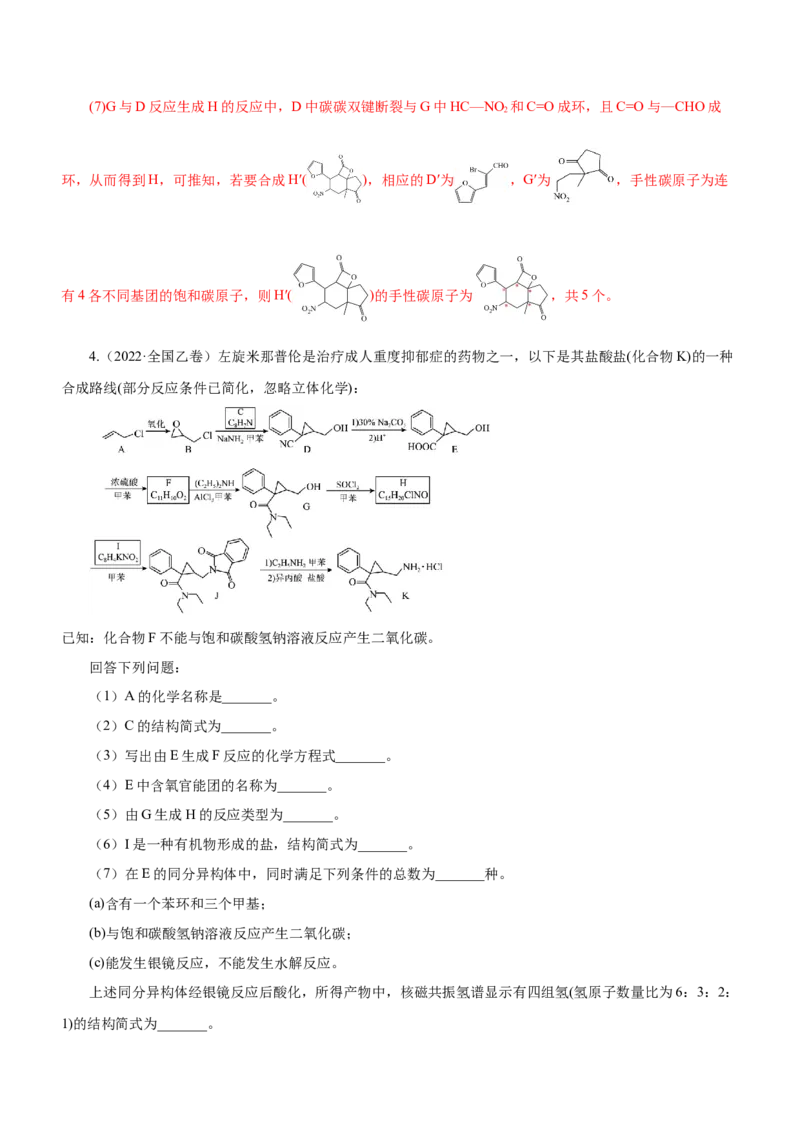
3.(2022·全国甲卷)用N-杂环卡其碱(NHC base)作为催化剂,可合成多环化合物。下面是一种多环化合
物H的合成路线(无需考虑部分中间体的立体化学)。回答下列问题:
(1)A的化学名称为_______。
(2)反应②涉及两步反应,已知第一步反应类型为加成反应,第二步的反应类型为_______。
(3)写出C与 / 反应产物的结构简式_______。
(4)E的结构简式为_______。
(5)H中含氧官能团的名称是_______。
(6)化合物X是C的同分异构体,可发生银镜反应,与酸性高锰酸钾反应后可以得到对苯二甲酸,写出X
的结构简式_______。
(7)如果要合成H的类似物H′( ),参照上述合成路线,写出相应的D′和G′的结构简式
_______、_______。H′分子中有_______个手性碳(碳原子上连有4个不同的原子或基团时,该碳称为手性碳)。
【答案】(1)苯甲醇 (2)消去反应
(3) (4) (5)硝基、酯基和羰基
(6) (7) 5
【解析】由合成路线,A的分子式为C HO,在Cu作催化剂的条件下发生催化氧化生成B,B的结构简
7 8
式为 ,则A为 ,B与CHCHO发生加成反应生成 , 再发生消去反应反应生成
3C,C的结构简式为 ,C与Br /CCl 发生加成反应得到 , 再在碱性条件下发生消
2 4
去反应生成D,D为 ,B与E在强碱的环境下还原得到F,E的分子式为C HO,F的结构简式为
5 6 2
,可推知E为 ,F与 生成G,G与D反应生成H,据此分析解答。
(1)由分析可知,A的结构简式为 ,其化学名称为苯甲醇;
(2)由B、C的结构简式,结合反应条件,可知B( )先与CHCHO发生碳氧双键的加成反应生成
3
, 再发生消去反应生成C( ),故第二步的反应类型为消去反应;
(3)根据分析可知,C与Br /CCl 发生加成反应得到 ;
2 4
(4)由分析,E的结构简式为 ;
(5)H的结构简式为 ,可其分子中含有的含有官能团为硝基、酯基和羰基;
(6)C的结构简式为 ,分子式为C HO,其同分异构体X可发生银镜反应,说明含有醛基,又与
9 8
酸性高锰酸钾反应后可得到对苯二甲酸,则X的取代基处于苯环的对位,满足条件的X的结构简式为:
;(7)G与D反应生成H的反应中,D中碳碳双键断裂与G中HC—NO 和C=O成环,且C=O与—CHO成
2
环,从而得到H,可推知,若要合成H′( ),相应的D′为 ,G′为 ,手性碳原子为连
有4各不同基团的饱和碳原子,则H′( )的手性碳原子为 ,共5个。
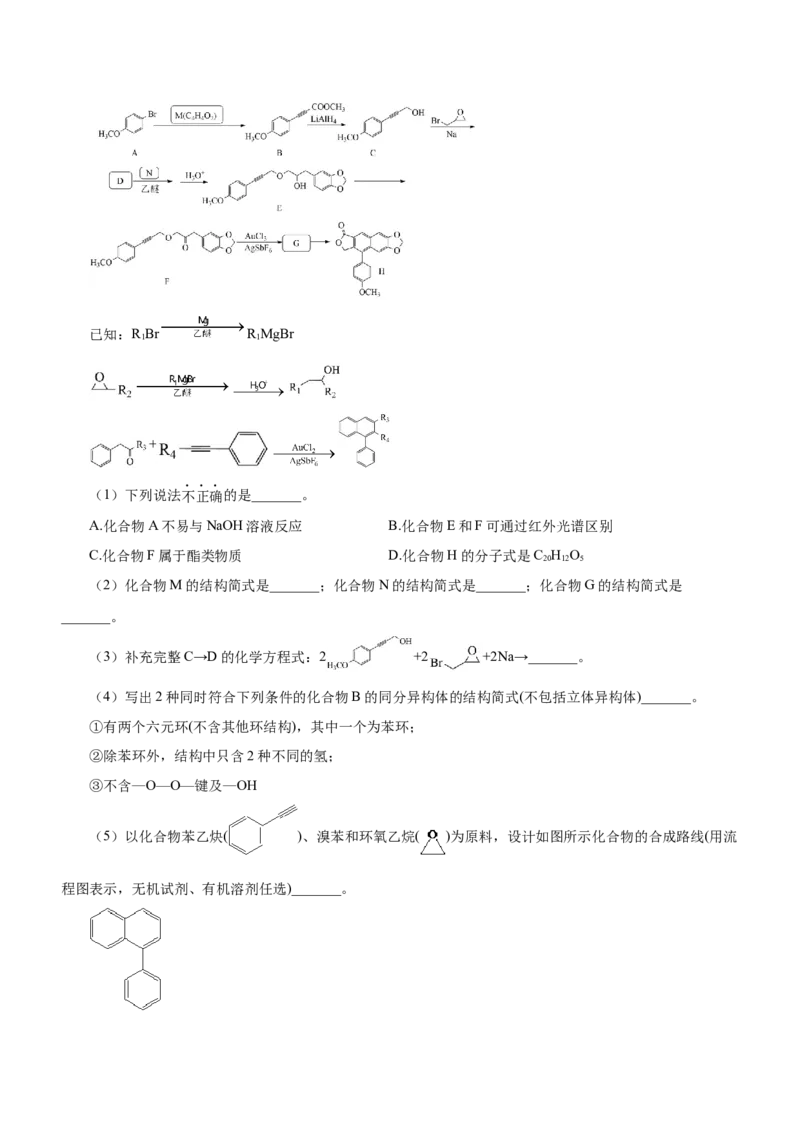
4.(2022·全国乙卷)左旋米那普伦是治疗成人重度抑郁症的药物之一,以下是其盐酸盐(化合物K)的一种
合成路线(部分反应条件已简化,忽略立体化学):
已知:化合物F不能与饱和碳酸氢钠溶液反应产生二氧化碳。
回答下列问题:
(1)A的化学名称是_______。
(2)C的结构简式为_______。
(3)写出由E生成F反应的化学方程式_______。
(4)E中含氧官能团的名称为_______。
(5)由G生成H的反应类型为_______。
(6)I是一种有机物形成的盐,结构简式为_______。
(7)在E的同分异构体中,同时满足下列条件的总数为_______种。
(a)含有一个苯环和三个甲基;
(b)与饱和碳酸氢钠溶液反应产生二氧化碳;
(c)能发生银镜反应,不能发生水解反应。
上述同分异构体经银镜反应后酸化,所得产物中,核磁共振氢谱显示有四组氢(氢原子数量比为6:3:2:
1)的结构简式为_______。【答案】(1)3-氯丙烯 (2) (3) +H O
2
(4)羟基、羧基 (5)取代反应
(6) (7)10 、
【解析】
【分析】A发生氧化反应生成B,B与C在NaNH 、甲苯条件下反应生成D,对比B、D的结构简式,结
2
合C的分子式C HN,可推知C的结构简式为 ;D与30%Na CO 反应后再酸化生成E,E在浓硫
8 7 2 3
酸、甲苯条件下反应生成F,F不能与饱和NaHCO 溶液反应产生CO,F中不含羧基,F的分子式为
3 2
C H O,F在E的基础上脱去1个HO分子,说明E发生分子内酯化生成F,则F的结构简式为 ;
11 10 2 2
F与(C H)NH在AlCl 、甲苯条件下反应生成G,G与SOCl 、甲苯反应生成H,H的分子式为C H ClNO,H
2 5 2 3 2 15 20
与I反应生成J,结合G、J的结构简式知,H的结构简式为 ;I的分子式为C HKNO,I是一种有
8 4 2
机物形成的盐,则I的结构简式为 ;据此作答。
(1)A的结构简式为CH=CHCHCl,属于氯代烯烃,其化学名称为3-氯丙烯。
2 2
(2)根据分析,C的结构简式为 。
(3)E的结构简式为 ,F的结构简式为 ,E生成F的化学方程式为+H O。
2
(4)E的结构简式为 ,其中含氧官能团的名称为(醇)羟基、羧基。
(5)G的结构简式为 ,H的结构简式为 ,G与SOCl 发生取代反应生成H。
2
(6)根据分析,I的结构简式为 。
(7)E的结构简式为 ,E的分子式为C H O,不饱和度为6;E的同分异构体与饱和
11 12 3
NaHCO 溶液反应产生CO,结合分子式中O原子的个数,说明含1个羧基,能发生银镜反应、不能发生水解
3 2
反应说明还含1个醛基;若3个甲基在苯环上的位置为 时,羧基、醛基在苯环上有3种位置;若3个甲
基在苯环上的位置为 时,羧基、醛基在苯环上有6种位置;若3个甲基在苯环上的位置为 时,羧
基、醛基在苯环上有1种位置;故符合题意的同分异构体共有3+6+1=10种;上述同分异构体经银镜反应后酸
化所得产物中核磁共振氢谱显示有4组氢且氢原子数量比为6:3:2:1的结构简式为 、
。
5.(2022·浙江卷)化合物H是一种具有多种生物活性的天然化合物。某课题组设计的合成路线如图(部分
反应条件已省略):已知:R Br R MgBr
1 1
+
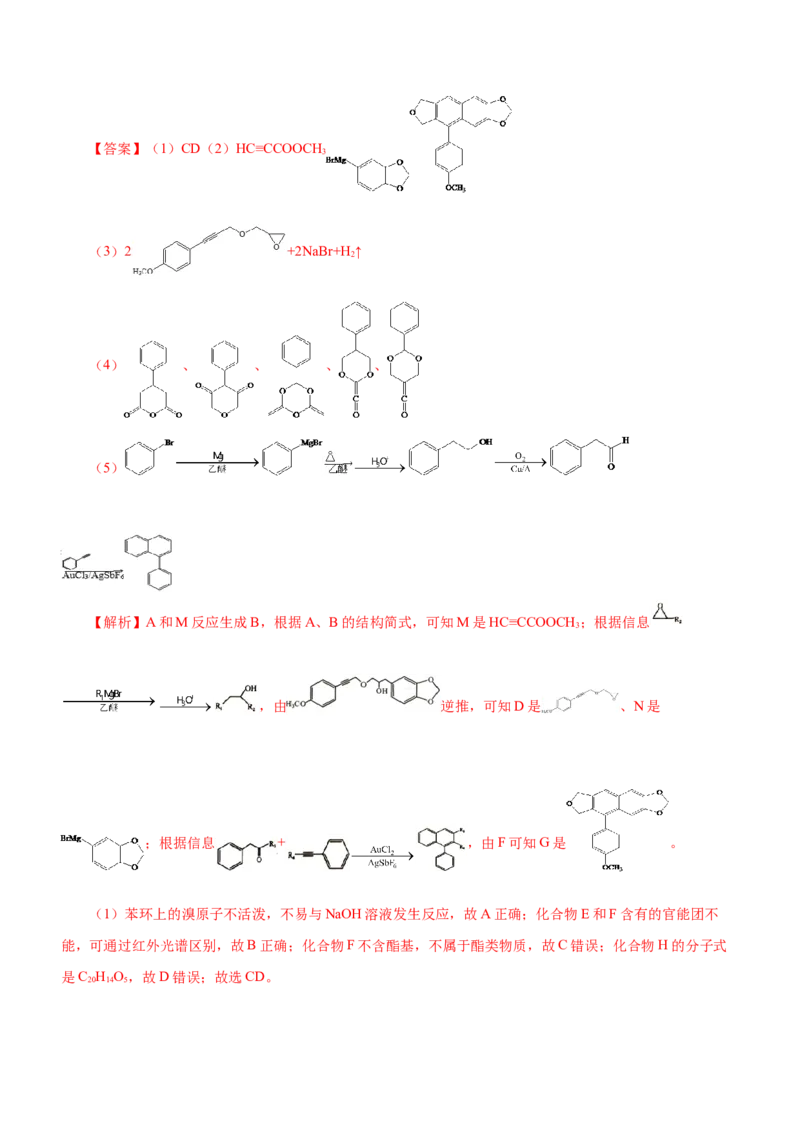
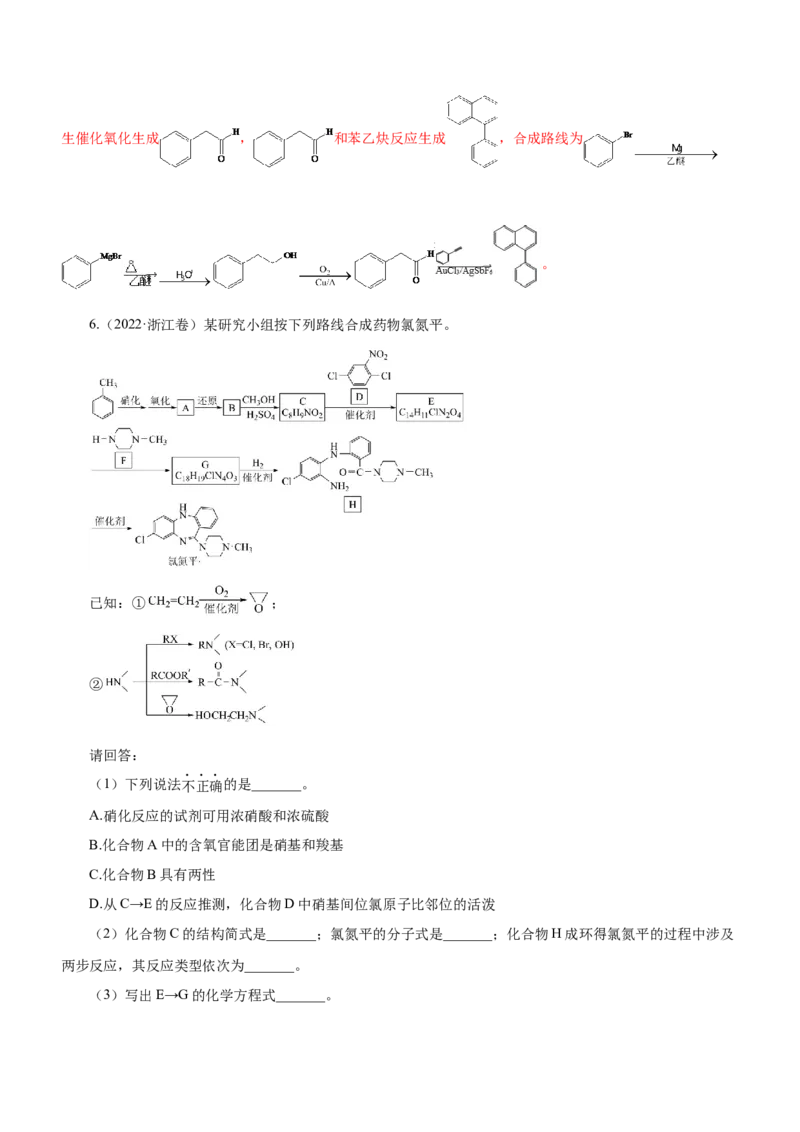
(1)下列说法不正确的是_______。
A.化合物A不易与NaOH溶液反应 B.化合物E和F可通过红外光谱区别
C.化合物F属于酯类物质 D.化合物H的分子式是C H O
20 12 5
(2)化合物M的结构简式是_______;化合物N的结构简式是_______;化合物G的结构简式是
_______。
(3)补充完整C→D的化学方程式:2 +2 +2Na→_______。
(4)写出2种同时符合下列条件的化合物B的同分异构体的结构简式(不包括立体异构体)_______。
①有两个六元环(不含其他环结构),其中一个为苯环;
②除苯环外,结构中只含2种不同的氢;
③不含—O—O—键及—OH
(5)以化合物苯乙炔( )、溴苯和环氧乙烷( )为原料,设计如图所示化合物的合成路线(用流
程图表示,无机试剂、有机溶剂任选)_______。【答案】(1)CD(2)HC≡CCOOCH
3
(3)2 +2NaBr+H ↑
2
(4) 、 、 、 、
(5)
【解析】A和M反应生成B,根据A、B的结构简式,可知M是HC≡CCOOCH ;根据信息
3
,由 逆推,可知D是 、N是
;根据信息 + ,由F可知G是 。
(1)苯环上的溴原子不活泼,不易与NaOH溶液发生反应,故A正确;化合物E和F含有的官能团不
能,可通过红外光谱区别,故B正确;化合物F不含酯基,不属于酯类物质,故C错误;化合物H的分子式
是C H O,故D错误;故选CD。
20 14 5(2)A和M反应生成B,根据A、B的结构简式,可知M是HC≡CCOOCH ;根据信息
3
,由 逆推,可知D是 、N是
;根据信息 + ,由F可知G是 。
(3)根据信息 ,由 逆推,可知D是
,C→D的方程式是2 +2 +2Na→2 +2NaBr+H ↑;
2
(4)①有两个六元环(不含其他环结构),其中一个为苯环;
②除苯环外,结构中只含2种不同的氢,说明结构对称;
③不含—O—O—键及—OH,符合条件的 的同分异构体有 、 、
、 、 。
(5)溴苯和镁、乙醚反应生成 , 和环氧乙烷反应生成 , 发生催化氧化生成 , 和苯乙炔反应生成 ,合成路线为
。
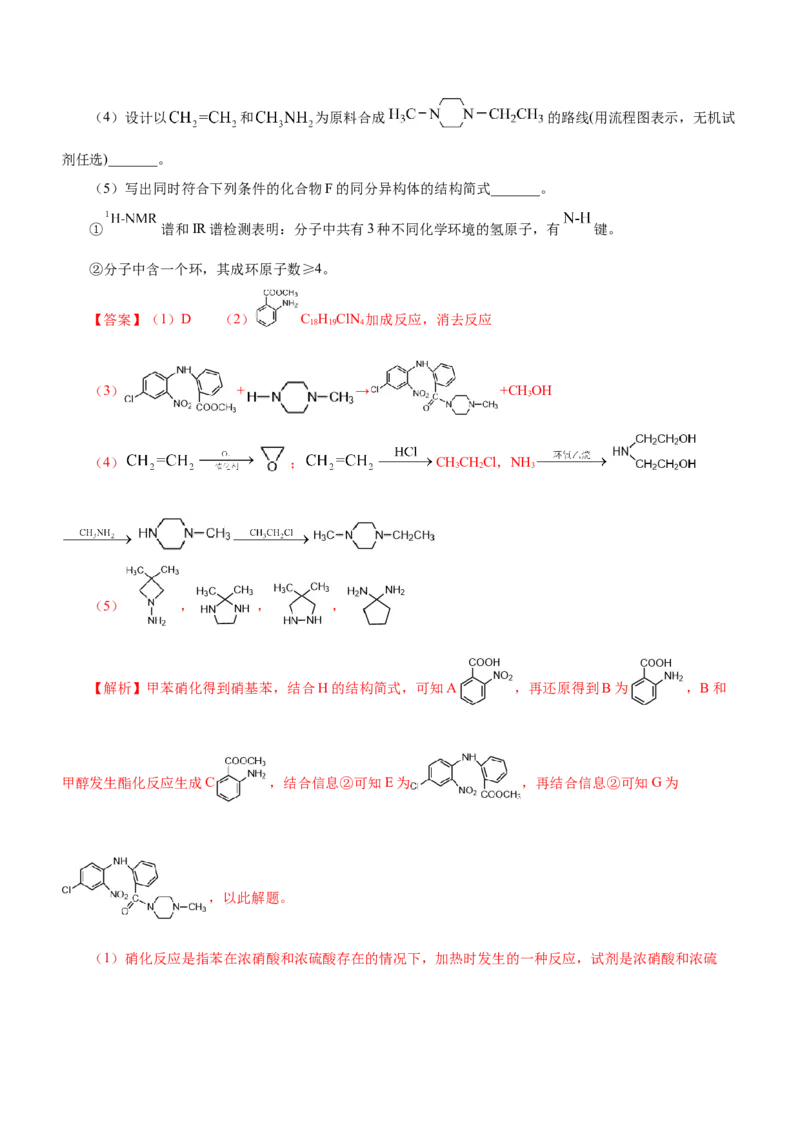
6.(2022·浙江卷)某研究小组按下列路线合成药物氯氮平。
已知:① ;
②
请回答:
(1)下列说法不正确的是_______。
A.硝化反应的试剂可用浓硝酸和浓硫酸
B.化合物A中的含氧官能团是硝基和羧基
C.化合物B具有两性
D.从C→E的反应推测,化合物D中硝基间位氯原子比邻位的活泼
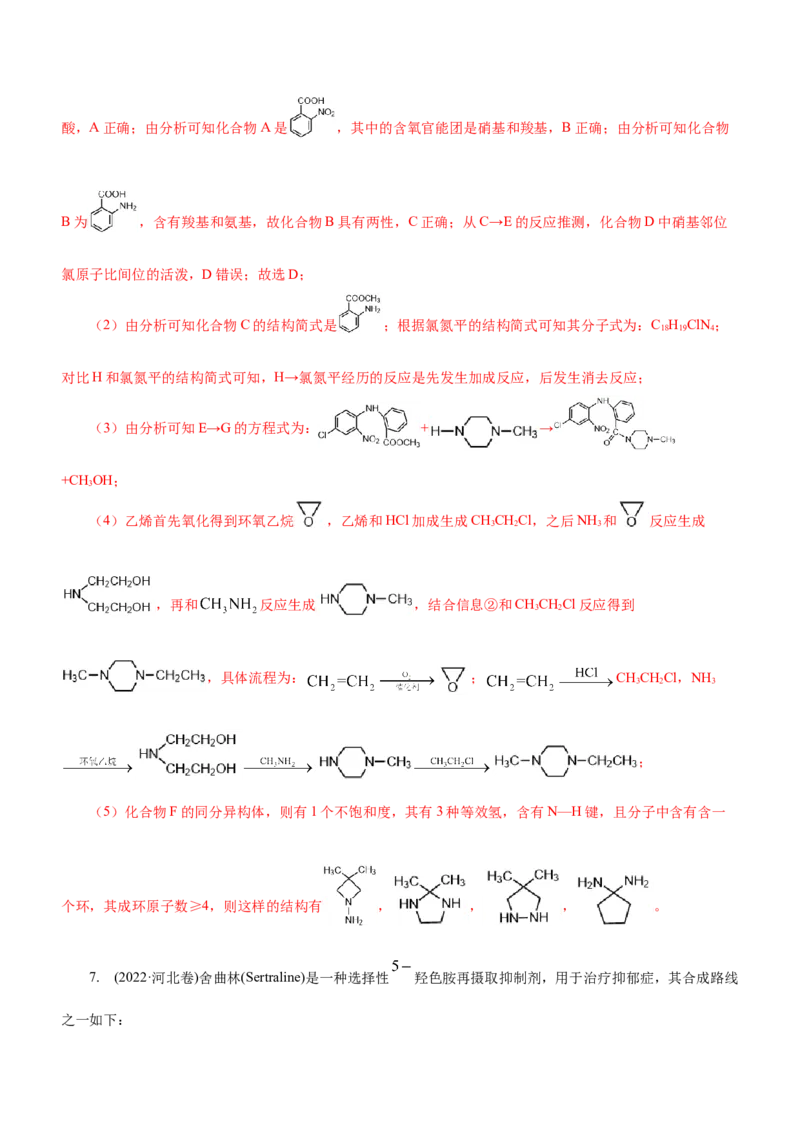
(2)化合物C的结构简式是_______;氯氮平的分子式是_______;化合物H成环得氯氮平的过程中涉及
两步反应,其反应类型依次为_______。
(3)写出E→G的化学方程式_______。(4)设计以 和 为原料合成 的路线(用流程图表示,无机试
剂任选)_______。
(5)写出同时符合下列条件的化合物F的同分异构体的结构简式_______。
① 谱和IR谱检测表明:分子中共有3种不同化学环境的氢原子,有 键。
②分子中含一个环,其成环原子数≥4。
【答案】(1)D (2) C H ClN 加成反应,消去反应
18 19 4
(3) + → +CH OH
3
(4) ; CHCHCl,NH
3 2 3
(5) , , ,
【解析】甲苯硝化得到硝基苯,结合H的结构简式,可知A ,再还原得到B为 ,B和
甲醇发生酯化反应生成C ,结合信息②可知E为 ,再结合信息②可知G为
,以此解题。
(1)硝化反应是指苯在浓硝酸和浓硫酸存在的情况下,加热时发生的一种反应,试剂是浓硝酸和浓硫酸,A正确;由分析可知化合物A是 ,其中的含氧官能团是硝基和羧基,B正确;由分析可知化合物
B为 ,含有羧基和氨基,故化合物B具有两性,C正确;从C→E的反应推测,化合物D中硝基邻位
氯原子比间位的活泼,D错误;故选D;
(2)由分析可知化合物C的结构简式是 ;根据氯氮平的结构简式可知其分子式为:C H ClN ;
18 19 4
对比H和氯氮平的结构简式可知,H→氯氮平经历的反应是先发生加成反应,后发生消去反应;
(3)由分析可知E→G的方程式为: + →
+CH OH;
3
(4)乙烯首先氧化得到环氧乙烷 ,乙烯和HCl加成生成CHCHCl,之后NH 和 反应生成
3 2 3
,再和 反应生成 ,结合信息②和CHCHCl反应得到
3 2
,具体流程为: ; CHCHCl,NH
3 2 3
;
(5)化合物F的同分异构体,则有1个不饱和度,其有3种等效氢,含有N—H键,且分子中含有含一
个环,其成环原子数≥4,则这样的结构有 , , , 。
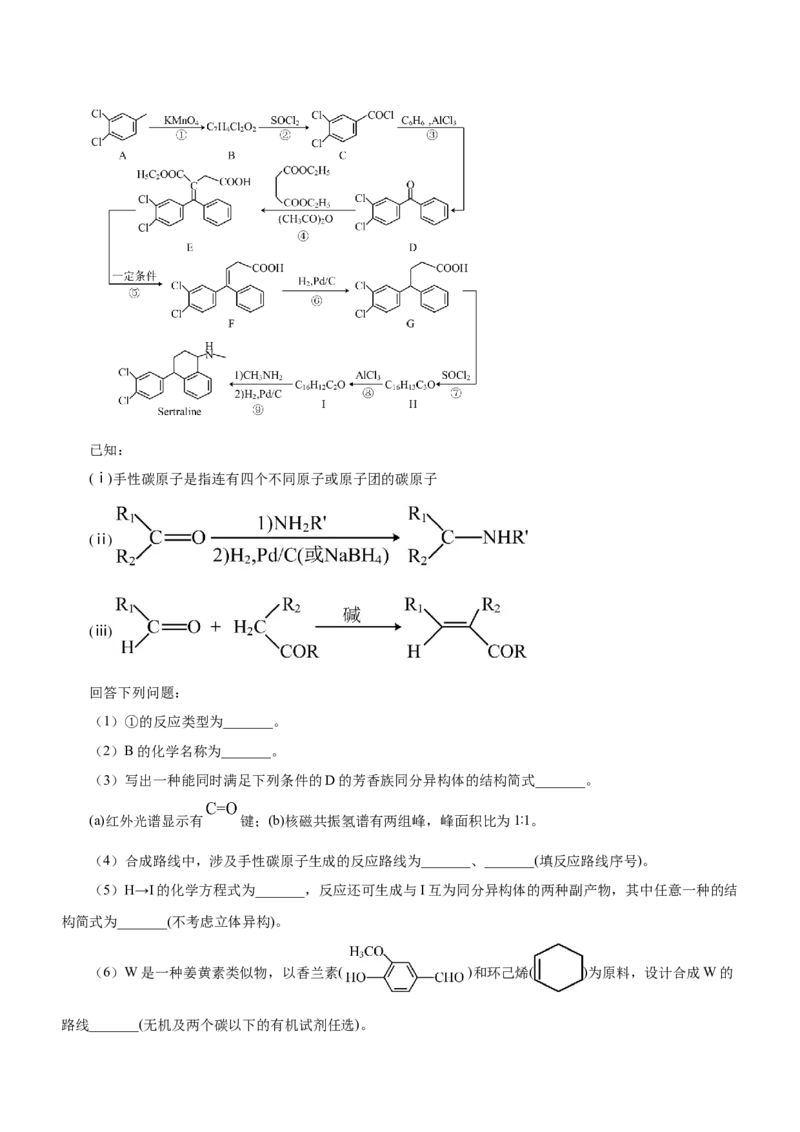
7. (2022·河北卷)舍曲林(Sertraline)是一种选择性 羟色胺再摄取抑制剂,用于治疗抑郁症,其合成路线
之一如下:已知:
(ⅰ)手性碳原子是指连有四个不同原子或原子团的碳原子
(ⅱ)
(ⅲ)
回答下列问题:
(1)①的反应类型为_______。
(2)B的化学名称为_______。
(3)写出一种能同时满足下列条件的D的芳香族同分异构体的结构简式_______。
(a)红外光谱显示有 键;(b)核磁共振氢谱有两组峰,峰面积比为1∶1。
(4)合成路线中,涉及手性碳原子生成的反应路线为_______、_______(填反应路线序号)。
(5)H→I的化学方程式为_______,反应还可生成与I互为同分异构体的两种副产物,其中任意一种的结
构简式为_______(不考虑立体异构)。
(6)W是一种姜黄素类似物,以香兰素( )和环己烯( )为原料,设计合成W的
路线_______(无机及两个碳以下的有机试剂任选)。【答案】(1)氧化反应 (2)3,4-二氯苯甲酸 (3) (4) ⑥ ⑨
(5)
和
(6)
【解析】A在KMnO 作用下,甲基被氧化为羧基,得到B ,B中羧基上的-OH被
4
SOCl 中的Cl取代得到C,C中的Cl原子与苯环上的H原子在AlCl 环境发生消去反应得到D,D中羰基在
2 3
和乙酸酐共同作用下生成碳碳双键得到E,E在一定条件下脱去酯基生成F,F中的碳碳双键加氢
得到G,G与SOCl 反应得到H ,H脱去HCl得到I ,I中的羰基发生已知(ⅱ)的
2
反应得到目标产物舍曲林。
(1)据分析,①是 中的甲基被KMnO 氧化为羧基,反应类型是氧化反应。
4
(2)据分析,B的结构简式是 ,名称是3,4-二氯苯甲酸。(3)从D的结构简式可知,其分子式为C HClO,能满足核磁共振氢谱两组峰,且峰面积比为1:1的
13 8 2
结构应是高度对称结构,又含有C=O,则该芳香族同分异构体的结构简式为: 。
(4)手性碳原子指连接四个不同原子或原子团的碳,题给合成路线中涉及手性碳原子的物质是G(
)、H( )、I( )和Sertraline(
),则涉及手性碳原子生成的反应路线是G和Sertraline的生成,即路线⑥和⑨。
(5)据分析,H→I是H中的碳基上的Cl与苯环消去HCl,形成一个环,化学方程式为:
;当该碳基上的Cl与苯环上的其它氢原子消去,
则得到I的同分异构体,有 和 。
(6)根据题给信息(ⅲ),目标物资W可由2个 与1个 合成,故设计合成路线如下:
。