文档内容
专题 22 晶体结构与性质
(建议完成时间:45分钟 实际完成时间:_______分钟)
目 录
考点一 晶体与晶胞
考点二 常见晶体的结构与性质
考点三 晶体中原子坐标
考点一 晶体与晶胞
1.(2023·天津南开·南开中学校考模拟预测)下列表述中正确的有
①晶体与非晶体的根本区别在于固体是否具有规则的几何外形
②非极性分子往往具有高度对称性,如 这样的分子
③利用超分子的分子识别特征,可以分离 和
④接近水的沸点的水蒸气的相对分子质量测定值比按化学式 计算出来的大,是由于氢键的影响
⑤设 为阿伏加德罗常数的值,含 碳原子的金刚石晶体中共价键个数为
⑥熔融状态能导电,熔点在 左右的晶体一定为离子晶体
A.2个 B.3个 C.4个 D.5个
【答案】B
【解析】①晶体与非晶体的根本区别在于晶体有自范性,与是否有规则的几何外形无关,如:玻璃,故①
错误;②PCl 为三角锥形分子,HO 为书页形分子,PCl 、HO 分子的正负电荷重心不重合,为极性分子,
3 2 2 3 2 2
故②错误;③C 和C 的混合物加入一种空腔大小适合C 的“杯酚”中可进行分离,这是利用超分子的
60 70 60
分子识别特征,故③正确;④接近水的沸点的水蒸气的相对分子质量测定值比用化学式HO计算出来的相
2
对分子质量大一些,其主要原因是接近水的沸点的水蒸气中水分子间因氢键而形成了“缔合分子”,故④
正确;⑤金刚石中每个C原子形成4个共价键,每个共价键被2个C原子共用,所以每个C原子占有的共
价键个数为4× =2,2.4g金刚石中n(C)= =0.2mol,则碳原子个数为0.2mol×2N /mol=0.4N ,故
A A
⑤正确;⑥熔融状态能导电,熔点在1000℃左右的晶体可能是金属晶体,故⑥错误;故选:B。
2.(2023·山东泰安·统考三模)磷元素有白磷、红磷、黑磷等常见的单质,其中黑磷晶体是一种比石墨烯
更优秀的新型材料,其晶体有与石墨类似的层状结构,如图所示。下列有关说法中错误的是
1
原创精品资源学科网独家享有版权,侵权必究!A.黑磷中磷原子采取 杂化
B.白磷、红磷、黑磷互为同素异形体
C.黑磷能导电,黑磷属于混合型晶体
D.白磷是非极性分子,白磷难溶于水、易溶于
【答案】A
【解析】A.由图可知,黑磷中磷原子形成3个共价键,且存在1对孤电子对,采取 杂化,A错误;
B.同素异形体是同种元素组成的不同单质;白磷、红磷、黑磷互为同素异形体,B正确;C.黑磷晶体有
与石墨类似的层状结构,能导电,属于混合型晶体,C正确;D.白磷分子为四面体结构,是非极性分子,
根据相似相溶原理可知,白磷难溶于水、易溶于 ,D正确;故选A。
3.(2023·辽宁鞍山·统考一模)氮化硼(BN)晶体有多种结构。六方相氨化硼是通常存在的稳定相,与石墨
相似,具有层状结构,可作高温润滑剂;立方相氮化硼是超硬材料,有优异的耐磨性。它们的晶体结构如
图所示,关于这两种晶体的说法正确的是
A.两种晶体中B原子的杂化方式均为sp2
B.两种晶体中B-N键键长相等
C.六方相氮化硼层间共价键键能较小,所以可做高温润滑剂
D.每个立方氮化硼晶胞中含有4个B原子和4个N原子
【答案】D
【解析】A.立方氮化硼中硼原子形成4个共价键,所以立方氮化硼中硼原子采用的是sp3杂化,选项A错
误;B.六方相氨化硼具有层状结构,立方相氮化硼形成正四面体结构,两种晶体中B-N键键长不相等,
选项B错误;C.六方相氮化硼层间作用力为范德华力,相对较小,所以可做高温润滑剂,选项C错误;
D.根据立方氨化硼的晶胞示意图,每个晶胞中B原子个数是8 +6 =4,N原子个数为4,选项D正
确;答案选D。
4.(2023·湖北荆州·沙市中学校考模拟预测)快离子导体是一类具有优良导电能力的固体电解质。图
1(Li SBF )和图2是潜在的快离子导体材料的结构示意图。温度升高时,NaCl晶体出现缺陷,晶体的导电
3 4
性增强。该晶体导电时,③迁移的途径有两条:
途径1:在平面内挤过2、3号氯离子之间的狭缝(距离为x)迁移到空位。
途径2:挤过由1、2、3号氯离子形成的三角形通道(如图3,小圆的半径为y)迁移到空位。
已知:氯化钠晶胞参数a=564pm,r(Na+)=95pm,r(Cl-)=185pm, =1.4, =1.7。下列说法不正确的是
A.第二周期元素中第一电离能介于B和F之间的元素有4种
B.图1所示晶体中,每个Li+与4个呈四面体结构的离子相邻
C.氯化钠晶体中,Na+填充在氯离子形成的正八面体空隙中
D.温度升高时,NaCl晶体出现缺陷,晶体的导电性增强,该晶体导电时,③迁移的途径可能性更大的是
途径1
【答案】D
【解析】A.第二周期元素第一电离能从左向右呈增大趋势,由于Be的2s轨道全满,N的2p轨道半满,
结构稳定,造成Be和N比同周期相邻元素的第一电离能高,因此第一电离能介于B和F之间的有Be、
C、N、O共4种,A正确;B.由图1所示晶体结构可知,Li+位于棱心,正四面体结构的离子在体心,则
每个Li+与4个呈四面体结构的离子相邻,B正确;C. NaCl晶胞中Na+周围有3个Cl-,则在NaCl晶体
中,Na+周围等距离最近有6个C1-,6个C1-构成正八面体结构,即Na+填充在C1-堆积而成的八面体空隙
中,C正确;D.该三角形为等边三角形,边长等于图2中面对角线长度,故三角形边长=
,即 ,r(Cl-)=185pm,解得x=24.8pm;内部虚线部分
三角形的顶角为120°、两腰长为r(Cl )+y、底长为282 pm,边角关系有 [ r(Cl )+y]=282 pm,解得
y= 47.2pm;由于挤过由1、2、 3号氯离子形成的三角形通道y的值大于挤过2、3号氯离子之间的狭缝x
值,所以Na+如果能挤过,那么挤过由1、2、 3号氯离子形成的三角形通道相对容易些,即迁移可能性更
大的途径是途径2,D错误;故选D。
5.(2023·广东广州·统考三模)研究者利用冷冻透射电子显微镜,在石墨烯膜上直接观察到了自然环境下
生成的二维晶体,其结构如图所示。下列说法正确的是A.石墨烯属于烯烃,可发生加成反应
B.石墨烯中碳原子的杂化轨道类型为sp2
C.二维晶体的化学式为CaCl
2
D.二维晶体中Ca和Cl的配位数均为6
【答案】B
【解析】A.石墨烯属于碳单质,不含有H元素,不属于烯烃,不能发生加成反应,故A错误;B.石墨
烯为平面结构,C的价层电子对数为3,故碳原子的杂化轨道类型为sp2,故B正确;C.每个Ca周围距离
最近的Cl有3个,每个Cl周围距离最近的Ca有3个,故二维晶体的化学式为CaCl,故C错误;D.由C
分析知,二维晶体中Ca和Cl的配位数均为3,故D错误;故选B。
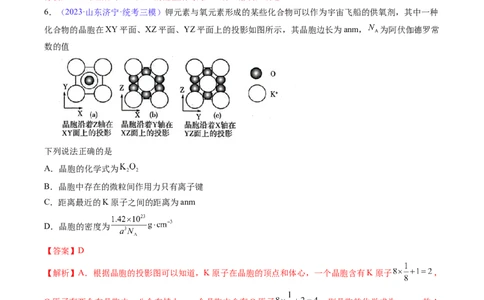
6.(2023·山东济宁·统考三模)钾元素与氧元素形成的某些化合物可以作为宇宙飞船的供氧剂,其中一种
化合物的晶胞在XY平面、XZ平面、YZ平面上的投影如图所示,其晶胞边长为anm, 为阿伏伽德罗常
数的值
下列说法正确的是
A.晶胞的化学式为
B.晶胞中存在的微粒间作用力只有离子键
C.距离最近的K原子之间的距离为anm
D.晶胞的密度为
【答案】D
【解析】A.根据晶胞的投影图可以知道,K原子在晶胞的顶点和体心,一个晶胞含有K原子 ,
O原子有两个在晶胞内,八个在棱上,一个晶胞中含有O原子 ,则晶胞的化学式为 ,故A
错误;B.晶胞的化学式为 ,则晶胞中存在的微粒间作用力有离子键和共价键,故B错误;C.K原子
在晶胞的顶点和体心,则距离最近的K原子之间的距离为体对角线的一半即 anm,故C错误;D.根据
前面分析该晶胞中含有2个 ,则晶胞的密度为 ,故D正确。综上所述,
答案为D。考点二 常见晶体的结构与性质
1.(2023·浙江温州·乐清市知临中学校考二模)下列物质中可做耐高温材料的共价化合物的是
A. B. C.W D.
【答案】A
【解析】A. 为共价化合物,硬度大熔点高,是可做耐高温材料的共价化合物,故A正确;B.氧化
镁为离子化合物,故B错误;C.W为金属单质,故C错误;D.二氧化碳常温下为气体,不可做耐高温
材料,故D错误;故选A。
2.(2023·辽宁沈阳·沈阳二中校考模拟预测)下列关于化学与生活、科技的说法,错误的是
A.激光打印机墨粉中的炭黑属于混合型晶体
B.可用硝酸铵和水合碳酸钠作冷敷袋的生要物质
C.高压法聚乙烯结构中含有较多支链,较柔软,可生产食品包装袋等
D.当把常规晶体粉碎为纳米晶体时,其熔点会下降,主要原因是晶体的表面积增大
【答案】A
【解析】A.石墨属于典型的混合型晶体,而炭黑属于非晶体,选项A错误;B.硝酸铵和水合碳酸钠溶
解吸热,可用作冷敷袋的主要物质,选项B正确;C.高压法聚乙烯属于热塑性聚合物,结构中含有较多
支链,柔软且耐磨,可生产食品包装袋等,选项C正确;D.晶体的熔点受晶体的晶格形状的影响,将常
规晶体粉碎为纳米晶体,由于晶体表面积的增大,使得其熔点下降,选项D正确;故选A。
3.(2023·山东威海·威海市第一中学统考二模)氮化硼(BN)可形成类似石墨的平面六角形层状结构a,在
一定条件下a可转化为类似金刚石的立方氮化硼b,如图所示。下列说法错误的是
A.第一电离能:
B.a、b两种晶体硬度和熔点均不同
C.a、b中所有化学键均为极性键,二者中B原子的杂化方式不同
D.a、b中每个B原子分别被m、n个六元环共有,则
【答案】D
【解析】A.已知同一周期从左往右元素的第一电离能呈增大趋势,ⅡA与ⅢA、ⅤA与ⅥA反常,故第
一电离能: ,A正确;B.由题干信息可知,a类似石墨的平面六角形层状结构,b类似金刚石结
构,结构决定性质,故两种晶体硬度和熔点均不同,B正确;C.由题干信息可知,a类似石墨的平面六角
形层状结构,b类似金刚石结构,故a、b中所有化学键均为B-N极性键,a中B周围的价层电子对数为
3,采用sp2杂化,而b中B周围的价层电子对数为4,采用sp3杂化,即二者中B原子的杂化方式不同,C
正确;D.已知石墨中每个C被3个六元环共用,即a中每个B被3个六元环共用,而金刚石中每个C被12个六元环共用,即b中每个B被12个六元环共用,故a、b中每个B原子分别被m、n个六元环共有,
则 ,D错误;故答案为:D。
4.(2023·上海奉贤·统考二模)下列晶体属于分子晶体的是
A.Si B.SiO C.SiCl D.SiC
2 4
【答案】C
【解析】A.Si为共价晶体,A错误;B.SiO 为共价晶体,B错误;C.SiCl 为分子晶体,C正确;D.
2 4
SiC为共价晶体,D错误;故答案选C。
5.(2023·上海浦东新·统考二模)刚玉(主要成分为 )硬度仅次于金刚石,常用于高级研磨材料,它
A.是分子晶体 B.是共价化合物
C.可做铝热剂 D.熔融状态下能导电
【答案】D
【解析】A.刚玉(主要成分为 )硬度仅次于金刚石,所以不属于分子晶体,事实上氧化铝属于过渡晶
体,偏向共价晶体,A不符合题意;B.氧化铝中铝元素与氧元素之间为离子键,所以属于离子化合物,B
不符合题意;C.铝热剂是铝粉和难熔金属氧化物的混合物,所以氧化铝不能做铝热剂,C不符合题意;
D.氧化铝为离子化合物,熔融状态下可电离成铝离子和氧离子,可导电,D符合题意;故选D。
6.(2023·安徽淮南·统考一模)钙钛矿(CaTiO )型化合物是一类可用于生产太阳能电池、传感器、固体电
3
阻器等的功能材料,晶胞如图(a)所示,其中Ti的电负性为1.5,一种立方钙钛矿结构的金属卤化物光电材
料的组成为Pb2+、I-和有机碱离子,其晶胞如图(b)所示。下列有关说法正确的是
A.基态Ti原子的核外电子排布式为1s22s22p63s23p64s23d2
B.TiF 、TiCl 、 TiBr 、 TiI 熔点依次升高
4 4 4 4
C.用图(b) 晶胞中的金属卤化物光电材料制作的太阳能电池,在使用过程中产生单质铅和碘,会降低了器
件效率和使用寿命。
D.图(b)晶胞中Pb2+与图(a) 晶胞中Ca的空间位置相同
【答案】C
【解析】A.Ti是22号元素,故基态Ti原子的核外电子排布式为1s22s22p63s23p63d24s2,A错误;B.由于
F的电负性大于Cl、Br、I,Ti与F的电负性差值为2.5>1.7,TiF 为离子化合物,熔点最高,而Cl、Br、I
4
的电负性与Ti的差值均小于1.7,即其它三种均为共价化合物,为分子晶体,对于组成和结构相似的分子
晶体,随相对分子质量的增大,分子间作用力增大,熔点逐渐升高,且一般晶体的熔沸点:离子晶体大于
分子晶体,故TiCl 、 TiBr 、 TiI 、TiF 熔点依次升高,B错误;C.用图(b) 晶胞中的金属卤化物光电材
4 4 4 4料制作的太阳能电池,在使用过程中产生单质铅和碘,导致光电材料损坏,会降低了器件效率和使用寿命,
C正确;D.距离Pb2+最近的是处于面心的6个I-,Pb2+的配位数为6,图(a)中Ti的配位数也是6,图(a)和
图(b)可以看出Pb2+和Ti空间位置相同,D错误;故答案为:C。
考点三 晶体中原子坐标
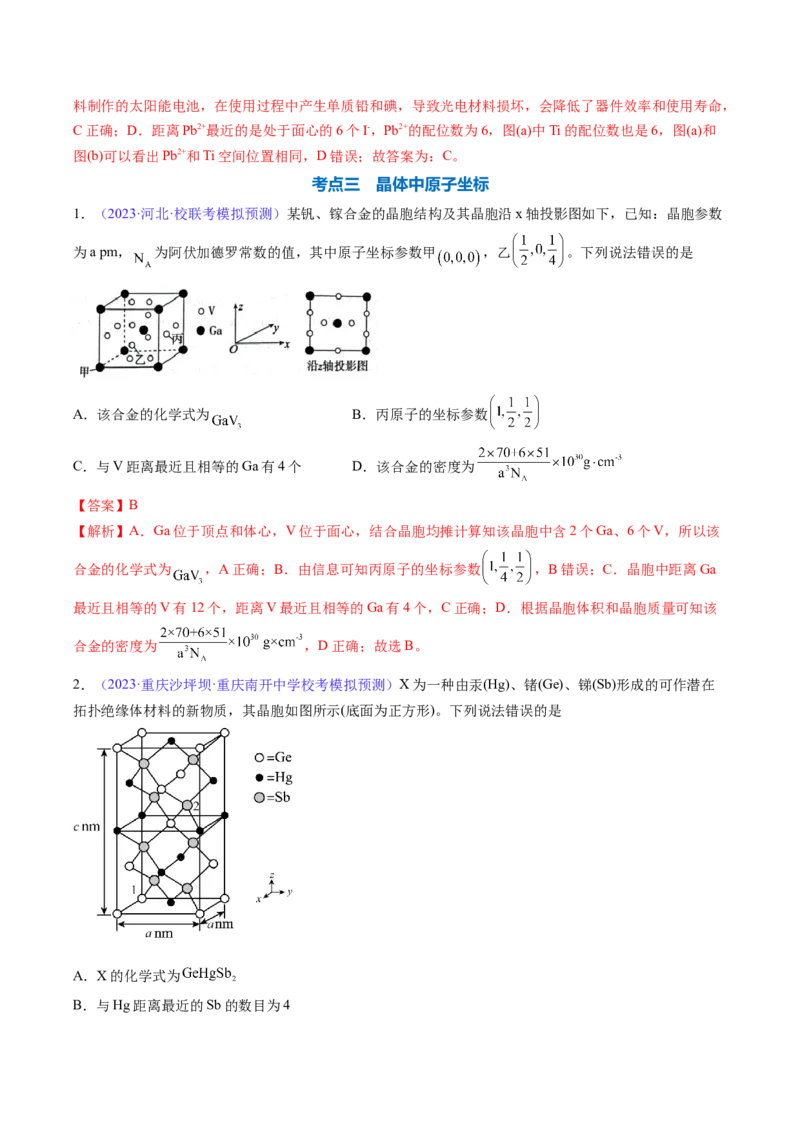
1.(2023·河北·校联考模拟预测)某钒、镓合金的晶胞结构及其晶胞沿x轴投影图如下,已知:晶胞参数
为a pm, 为阿伏加德罗常数的值,其中原子坐标参数甲 ,乙 。下列说法错误的是
A.该合金的化学式为 B.丙原子的坐标参数
C.与V距离最近且相等的Ga有4个 D.该合金的密度为
【答案】B
【解析】A.Ga位于顶点和体心,V位于面心,结合晶胞均摊计算知该晶胞中含2个Ga、6个V,所以该
合金的化学式为 ,A正确;B.由信息可知丙原子的坐标参数 ,B错误;C.晶胞中距离Ga
最近且相等的V有12个,距离V最近且相等的Ga有4个,C正确;D.根据晶胞体积和晶胞质量可知该
合金的密度为 ,D正确;故选B。
2.(2023·重庆沙坪坝·重庆南开中学校考模拟预测)X为一种由汞(Hg)、锗(Ge)、锑(Sb)形成的可作潜在
拓扑绝缘体材料的新物质,其晶胞如图所示(底面为正方形)。下列说法错误的是
A.X的化学式为
B.与Hg距离最近的Sb的数目为4C.若晶胞中原子1的坐标为 ,则原子2的坐标为
D.设X的最简式的分子量为 ,则X晶体的密度为
【答案】C
【解析】A.X中含Hg个数为 ,Ge个数为 ,Sb个数为8,则X的化学式
为 ,故A正确;B.以右侧面的Hg分析,与Hg距离最近的Sb的数目为4,故B正确;C.若晶
胞中原子1的坐标为 ,则原子2在上面那个立方体的体对角线的四分之一处,其z坐标为
,则其坐标为 ,故C错误;D.设X的最简式的分子量为 ,则X晶体的密度为
,故D正确。综上所述,答案为C。
3.(2023·重庆·校联考三模)纳米 可催化 的分解,其晶胞结构如图所示。关于 的说法正确
的是
A. 的配位数是4
B. 与 间最短距离为
C.若A离子的坐标为 ,则B原子的坐标为
D.若晶体密度为 ,则晶胞参数
【答案】C
【解析】A.根据晶胞图可知,Ce4+的配位数为8,故A错误;B.把晶胞平均分成8个小立方体,O2-位于
小立方体的中心,即Ce4+与O2-最短距离是体对角线的 ,最短距离是 nm,故B错误;C.若A的坐
标为(0, , ),A点位于面心,根据B选项分析,则B的坐标为( , , ),故C正确;D.Ce4+位于顶点和面心,个数为 =4,O2-位于晶胞内部,个数为8,化学式为CeO,则晶胞的质量为
2
g,根据密度的定义,晶胞的参数为 nm= nm,故D错误;
答案为C。
4.(2023·湖南·校联考模拟预测) 晶体是制备氟代硼铍酸钾晶体的原料之一,其晶胞结构与 类似,
下列说法中不正确的是
A.Be原子的配位数是12
B.若原子a、b的坐标分别为 、 ,则原子c的坐标为
C.沿晶胞面对角线投影,所得的投影结果是
D.设O与Be的最近距离为 ,用 表示阿伏加德罗常数的值,则 晶体的密度为
【答案】A
【解析】A.由晶胞结构可知Be位于O原子构成的四面体的体心,Be原子的配位数是4,A错误;B.由
的晶胞结构可知,每个Be处于晶胞体对角线的 处,结合原子a、b的坐标可知原子c的坐标为
,B正确;C.沿面对角线进行投影,可知所得的投影结果是 ,C正确;D.若
O与Be的最近距离为 ,则题中a、c之间的距离为 ,又因为a、c之间的距离为晶胞体对角线长的
,则晶胞体对角线长为 ,故晶胞棱长为 ,晶胞内Be的个数为4,O的个数为,则根据晶胞质量=晶胞密度×晶胞体积可得,晶胞密度为 ,D正
确;故选:A。
5.(2023·重庆沙坪坝·重庆一中校考模拟预测)氮化铬的晶胞结构如图所示, 点分数坐标为 。
氮化铬的晶体密度为 ,摩尔质量为 ,晶胞参数为 , 代表阿伏加德罗常数的值。
下列说法正确的是
A.铬原子的价电子排布图为:
B. 点的分数坐标为
C.距离 原子最近的 原子有8个
D.
【答案】D
【解析】A.Cr原子的价层电子排布式为3d54s1,其价电子排布图为 ,A错
误;B.A点分数坐标为(0,0,0),根据坐标系,B点位于棱心上,则B点分数坐标为( ,1,1),B错误;C.
以位于体心的Cr原子为例,距离 原子最近的 原子位于棱心,共有12个,C错误;D.该晶胞中,位
于顶点和面心的N原子个数为 ,位于体心和棱心的Cr原子个数为 ,则
,解得 nm,D正确;故选D。
6.(2023·福建宁德·统考一模)钛及其化合物在生产、生活中有着广泛的用途。回答下列问题:
(1)Ti(BH) 是一种储氢材料。BH 中B原子的杂化轨道类型为 ;Ti、B、H元素的电负性由大到小排列
4 3
顺序为 。
(2)已知Ti3+易形成多种配合物,[TiCl(H O) ]Cl ·H O是其中的一种。
2 5 2 2
①1mol该配合物中含有 molσ键。②Ti3+具有较强还原性的原因是 。
(3)研究表明,TiO 通过氮掺杂反应可生成TiO N,能使TiO 对可见光具有活性,反应如图所示。
2 2-x y 2
①上图TiO 晶胞中钛原子占据 个氧原子围成的八面体空隙。
2
②已知所有的Ti-O键键长为rpm,B点原子的分数坐标为( , , ),则A点原子的分数坐标为( ,
0, )。
③TiO N 晶体中x= 。
2-x y
【答案】(1)sp3 H>B>Ti
(2)18 Ti3+的价层电子排布为3d1很容易在失去一个电子达到3d轨道上全空的稳定结构
(3)6 +
【解析】(1)BH 中B原子价层电子对数为 ,B原子的杂化轨道类型为sp3;由上述离子中
元素价态可知B显+3价、H显-1价,可知H的电负性大于B,Ti为金属元素,电负性最小,元素的电负性
由大到小排列顺序为H>B>Ti;
(2)①1mol该配合物中共含6mol水,1mol水中含2molO-Hσ键,另外Ti与1个Cl离子和5个水分子形
成配位键,共形成6mol配位键,则1mol该配合物中含有18molσ键;②Ti3+的价层电子排布为3d1很容易
在失去一个电子达到3d轨道上全空的稳定结构,因此Ti3+具有较强还原性;
(3)①由图可知TiO 晶胞中钛原子位于6个氧原子围成的八面体空隙中;②由图可知A点x坐标与B点
2
相同为 ,A点y坐标为0,A点z坐标为B点坐标基础上增加一个Ti-O键长的相对长度,即为 + ;③
由晶胞结构可知Ti原子8个位于顶点,4个位于面上,1个位于体心,个数为: ,N原子
位于面心,个数为 ,O原子有1个在体内,7个在棱上,7个在面上,个数为:
,Ti:O:N=4: : =1: : ,结合化学式可知2-x= ,x= 。