文档内容
专题 23 化学反应的热效应
(建议完成时间:45分钟 实际完成时间:_______分钟)
目 录
考点一 焓变 热化学方程式
考点二 燃烧热 中和反应反应热和能源
考点三 盖斯定律 反应热计算
考点一 焓变 热化学方程式
1.(2023·天津·统考一模)胶状液氢(主要成分是 和 )有望用于未来的运载火箭和空间运输系统。实
验测得: 时, 完全燃烧生成液态水,放出 热量; 完全燃烧生成液态水和
,放出 的热量。下列热化学方程式的书写中正确的是
A.
B.
C.
D.
【答案】B
【解析】A.CH 燃烧为放热反应,ΔH<0,A项错误;B.1molCH 燃烧放出890.3kJ,反应放热且产生
4 4
HO(l),B项正确;C.CH 燃烧产生的HO(l),C项错误;D.ΔH单位错误应该为2H(g)+O(g)=2HO(l)
2 4 2 2 2 2
ΔH=−571.6kJ/mol,D项错误;故选B。
2.(2023·广东·深圳市光明区高级中学校联考模拟预测)已知:298K时,相关物质的相对能量如图所示。
下列说法错误的是。
A.CO燃烧的热化学方程式为2CO(g)+O(g) 2CO(g) ∆H=-566kJ∙mol-1
2 2
B.H 的燃烧热为∆H=-242kJ∙mol-1
2
1
原创精品资源学科网独家享有版权,侵权必究!C.C H 比C H 稳定
2 6 2 4
D.CO(g)+HO(g) CO(g)+H(g)是放热反应
2 2 2
【答案】B
【解析】A.CO燃烧的热化学方程式为2CO(g)+O(g) 2CO(g) ∆H=[(-393×2)-(-110×2+0)]
2 2
kJ∙mol-1=-566kJ∙mol-1,A正确;B.H 的燃烧热为∆H=[(-286)-(0+ ×0)] kJ∙mol-1=-286kJ∙mol-1,B错误;C.
2
C H 的能量为-84kJ∙mol-1,C H 的能量为52kJ∙mol-1,物质具有的能量越低,稳定性越强,则C H 比C H
2 6 2 4 2 6 2 4
稳定,C正确;D.CO(g)+HO(g) CO(g)+H(g) ∆H=[(-393+0)-(-110-242)] kJ∙mol-1=-41kJ∙mol-1,是放热反
2 2 2
应,D正确;故选B。
3.(2023·江西上饶·鄱阳一中校考一模)下列说法中正确的是
A.若 2NO (g) NO(g) ∆H =+56.9kJ·mol-1 ,则 置于密闭容器中充分反应吸收的热量为
2 2 4
56.9kJ
B.表示中和热的热化学方程式:
C.在稀溶液中,强酸与强碱反应的中和热为ΔH=-57.3kJ·mol-1,若将含有0.5mol H SO 的浓硫酸和含有
2 4
1molNaOH的溶液混合,放出的热量大于57.3kJ
D.H(g)的燃烧热是285.8kJ·mol-1,则2HO(g)=2H (g)+O(g) ∆H =+571.6kJ·mol-1
2 2 2 2
【答案】C
【解析】A.若 2NO (g) NO(g) ∆H =+56.9kJ·mol-1,将 置于密闭容器中,参加反应的NO
2 2 4 2
小于2mol,则充分反应吸收的热量小于56.9kJ,A不正确;B.表示中和热的热化学方程式中,H+和OH-
的状态都应为aq,而不是l,即为: ,B不正确;C.浓硫酸溶
于水时,会放出热量,若将含有0.5mol H SO 的浓硫酸和含有1molNaOH的溶液混合,放出的热量为中和
2 4
热与溶解热之和,应大于57.3kJ,C正确;D.H(g)的燃烧热是285.8kJ·mol-1,则2HO(l)=2H(g)+O(g)
2 2 2 2
∆H =+571.6kJ·mol-1,2HO(g)=2H (g)+O(g) ∆H<+571.6kJ·mol-1,D不正确;故选C。
2 2 2
4.(2023·河北·校联考二模)下图是用钌 基催化剂催化 和 的反应示意图,当反应生成
液态 时放出 的热量。下列说法错误的是
A.反应历程中存在极性键、非极性键的断裂与形成B.图示中物质I为该反应的催化剂,物质II、III为中间产物
C.使用催化剂可以降低反应的活化能,但无法改变反应的焓变
D.由题意知:
【答案】A
【解析】A.由反应示意图可知反应过程中不存在非极性键的形成,故A错误;B.物质I为反应起点存在
的物质,且在整个过程中量未发生改变,物质I为催化剂,物质II、III为中间过程出现的物质,为中间产
物,故B正确;C.催化剂通过降低反应的活化能加快反应速率,但不影响反应的焓变,故C正确;D.
生成 液态 时放出 的热量,该反应的热化学方程式为:
,则 ,故D正确;故选:A。
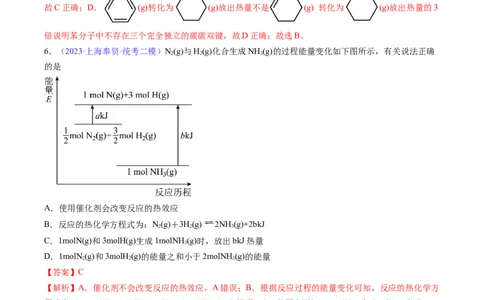
5.(2023·上海杨浦·统考二模)相关有机物分别与氢气发生反应生成1mol环己烷( )的能量变化
如图所示:
下列叙述错误的是
A. (g) (g)为吸热反应
B. (g) (g)
C.相同状况下,等质量的 和 完全燃烧, 放热少
D. ,可推测苯分子中不存在三个完全独立的碳碳双键
【答案】B
【解析】A.由图可知, (g)的能量小于 (g),则 (g) (g)的反应为吸热反应,故A正确;B.由图可知, (g)转化为 (g)和氢气的反应为放热反应,反应的热化
学方程式为 (g) (g) ,故B错误;C.由图可知,
(g)的能量小于 (g),则相同状况下,等质量的 和 完全燃烧, 放热少,
故C正确;D. (g)转化为 (g)放出热量不是 (g) 转化为 (g)放出热量的3
倍说明苯分子中不存在三个完全独立的碳碳双键,故D正确;故选B。
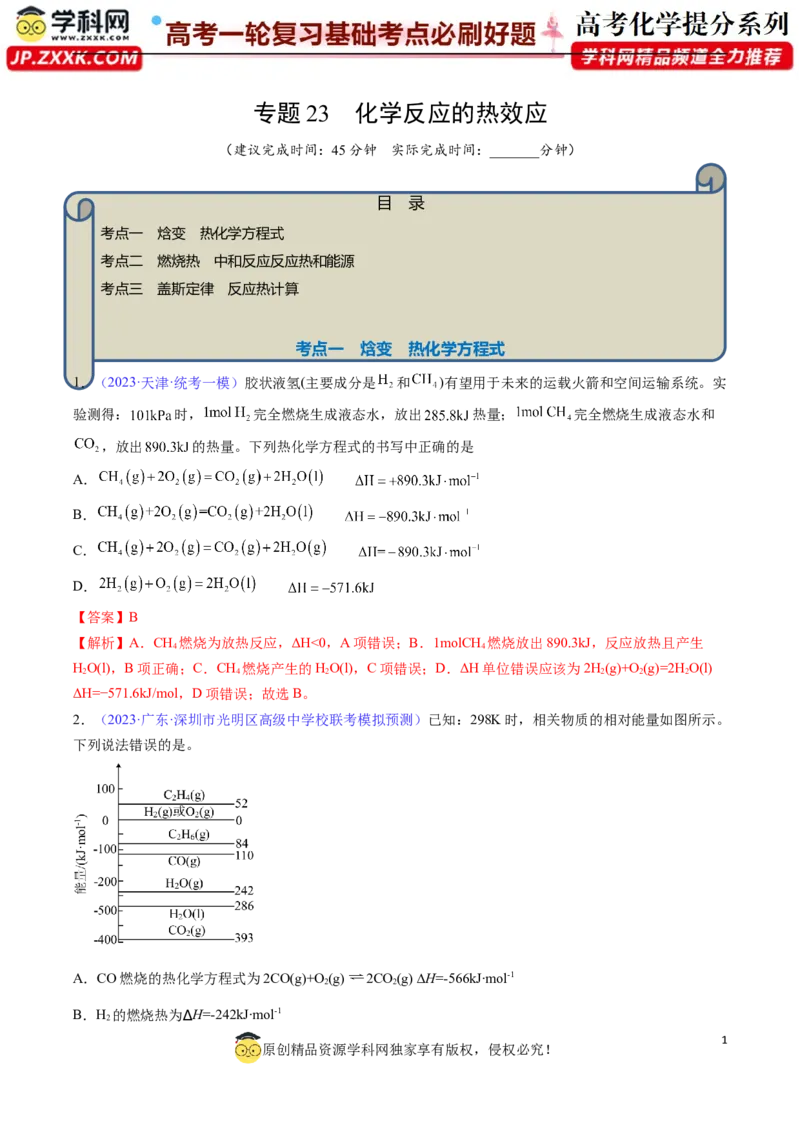
6.(2023·上海奉贤·统考二模)N(g)与H(g)化合生成NH (g)的过程能量变化如下图所示,有关说法正确
2 2 3
的是
A.使用催化剂会改变反应的热效应
B.反应的热化学方程式为:N(g)+3H(g) 2NH (g)+2bkJ
2 2 3
C.1molN(g)和3molH(g)生成1molNH (g)时,放出bkJ热量
3
D.1molN (g)和3molH (g)的能量之和小于2molNH (g)的能量
2 2 3
【答案】C
【解析】A.催化剂不会改变反应的热效应,A错误;B.根据反应过程的能量变化可知,反应的热化学方
程式为N(g)+3H(g)=2NH (g) ΔH=-2(b-a)kJ/mol,B错误;C.从图中可知,1molN(g)和3molH(g)生成
2 2 3
1molNH (g)时,放出bkJ热量,C正确;D.氮气和氢气反应生成氨气,这是一个放热反应,1molN (g)和
3 2
3molH (g)的能量之和大于2molNH (g)的能量,D错误;故答案选C。
2 3
7.(2023秋·广西南宁·高三南宁市武鸣区武鸣高级中学校考开学考试)Ni 可活化 C H 放出 CH,其反
2 6 4
应历程如下图所示:下列关于活化历程的说法错误的是
A.此反应的决速步骤:中间体 2→中间体3
B.涉及极性键的形成和非极性键的断裂
C.三种中间体比较,中间体2最稳定
D.3
【答案】D
【解析】A.反应的活化能越大,反应速率越慢,化学反应速率取决于最慢的一步反应,由图可知,中间
体2→中间体3能量差值最大,则该步反应的活化能最大,是化学反应的决速步骤,故A正确;B.由图可
知,反应过程涉及非极性键C―C键断裂和极性键C―H 键的形成,故 B 正确;C.物质的能量越低越稳
定,由图可知,中间体2的能量最低,则中间体2最稳定,故 C 正确;D.由图可知,镍和乙烷的反应为
反应物总能量大于生成物总能量的放热反应,反应的热化学方程式为
,故 D 错误;故选D。
8.(2023秋·湖南衡阳·高三衡阳市八中校考开学考试) 超干重整 的催化转化如图1所示,相关反
应的能量变化如图2所示:
下列说法不正确的是A.过程Ⅰ的热化学方程式为:
B.过程Ⅱ实现了含碳物质与含氢物质的分离
C.过程Ⅱ中 为催化剂,降低了反应的
D. 超干重整 的总反应为:
【答案】C
【解析】A.Ⅰ、 ,Ⅱ、
,根据盖斯定律,由Ⅰ 2-Ⅱ得到
,选项A正确;B.过程Ⅱ的反应第一步是
CO+CO+H +Fe O+CaO→H O+Fe+CaCO ,第二步反应:Fe+CaCO +稀有气体→稀有气体
2 2 3 4 2 3 3
+Fe+CaCO+CO,两步反应实现了含碳物质与含氢物质的分离,选项B正确;C.过程Ⅱ中 为
3
催化剂,改变反应速率不能改变反应的 ,选项C不正确;D.根据流程中物质的参与和生成情况,结
合反应过程中有催化剂和中间产物,总反应可表示为 ,选项D正确;答案选
C。
9.(2023秋·云南曲靖·高三宣威市第三中学校考开学考试)已知:CH(g)的燃烧热为-890.31kJ•mol-1,则
4
下列热化学方程式正确的是
A.CH(g)+2O(g)=CO (g)+2HO(l) △H=+890.31kJ•mol-1
4 2 2 2
B.CH(g)+2O(g)=CO +2H O(g) △H=-890.31kJ•mol-1
4 2 2 2
C.CH(g)+O(g)=CO(g)+2HO(l) △H=-890.31kJ•mol-1
4 2 2
D.CH(g)+2O(g)=CO (g)+2HO(l) △H=-890.31kJ•mol-1
4 2 2 2
【答案】D
【解析】CH(g)的燃烧热是1mol甲烷完全燃烧生成二氧化碳和液态水放出的能量,CH(g)的燃烧热
4 4
为-890.31kJ•mol-1,表示甲烷燃烧热的热化学方程式是CH(g)+2O(g)=CO (g)+2HO(l) △H=-890.31kJ•mo
4 2 2 2
l-1,故选D。
10.(2023秋·北京西城·高三北师大实验中学校考开学考试) (g)与 (g)在铁催化剂表面经历如下过程
生成 (g):下列说法不正确的是
A.Ⅰ过程中破坏的均为非极性键
B.Ⅰ过程吸收能量,Ⅱ过程放出能量
C.氨分解的热化学方程式为
D.使用催化剂可以降低反应的焓变,从而提高化学反应速率
【答案】D
【解析】A.Ⅰ过程中断裂 molN (g)和 molH (g)中的化学键得到1molN和3molH,N、H 中均为非极
2 2 2 2
性键,A项正确;B.Ⅰ过程断裂化学键、吸收能量,Ⅱ过程形成化学键、放出能量,B项正确;C.由图
可知, molN (g)和 molH (g)反应生成1molNH (g)放出1175kJ-1129kJ=46kJ的能量,合成氨的热化学方
2 2 3
程式为 N(g)+ H(g) NH (g) ∆H=-46kJ/mol,则氨分解的热化学方程式为2NH (g) N(g)
2 2 3 3 2
+3H (g) ∆H=+92kJ/mol,C项正确;D.使用催化剂不能改变反应的焓变,能降低反应的活化能,从而提
2
高化学反应速率,D项错误;答案选D。
考点二 燃烧热 中和反应反应热和能源
1.(2023·江苏连云港·连云港高中校考模拟预测) 的燃烧热为 。下列化学反应表示正
确的是
A.在空气中煅烧 的反应:
B.在弱碱性条件下,FeS与 反应:
C.FeS与 反应的离子方程式:
D. 的燃烧:
【答案】B
【解析】A.空气中煅烧 时,铁被氧气氧化生成Fe O,正确的方程式为:
2 3
,故A错误;B.FeS具有还原性, 具有氧化性,铁被氧化为+3价,
铬被还原为+3价,弱碱性条件下分别生成对应的氢氧化物,离子方程式为
,故B正确;C.FeS是难溶物,不能拆,正确的离子
方程式为: ,故C错误;D.HS的燃烧热表示1molH S完全燃烧生成液态水时释放
2 2
出的热量,选项中生成的水为气态水, >- ,故D错误;故选B。
2.(2023·重庆万州·重庆市万州第二高级中学校考模拟预测)分别向1 L 0.5 mol·L-1的Ba(OH) 溶液中加
2
入①浓硫酸;②稀硫酸;③稀硝酸,恰好完全反应时的热效应分别为ΔH、ΔH、ΔH,下列关系中正确的
1 2 3
是( )A.ΔH>ΔH >ΔH B.ΔH<ΔH <ΔH C.ΔH>ΔH =ΔH D.ΔH=ΔH<ΔH
1 2 3 1 2 3 1 2 3 1 2 3
【答案】B
【解析】强酸与强碱的稀溶液发生中和反应热效应表示为: ═ ,
分别向1L 0.5mol/L的 溶液中加入①浓硫酸②稀硫酸③稀硝酸,因浓硫酸溶于水放热,生成硫酸钡沉
淀会放出少量的热,则恰好完全反应时的放出的热量为:①>②>③,所以 ;所以B选项是正
确的。
3.(2023·江西上饶·鄱阳一中校考一模)已知在25℃时:①HF(aq)+OH-(aq)=F-(aq)+H O(l) △H=-67.7kJ•
2
mol-1②H+(aq)+OH-(aq)=H O(l) △H=-57.3kJ•mol-1③HCN(aq)+NaOH(aq)=NaCN(aq)+H O(l) △H=-12.1kJ•mo
2 2
l-1。下列说法正确的是
A.HF电离的热化学方程式为HF(aq) F-(aq)+H+(aq) △H>0
B.HCN在水溶液中电离的△H等于+45.2kJ•mol-1
C.在氢氧化钠溶液与盐酸溶液的反应中,盐酸的量一定,氢氧化钠溶液的量越多,中和反应反应热的绝
对值越大
D.稀硫酸与稀氢氧化钡溶液反应的热化学方程式:HSO (aq)+Ba(OH)(aq)=BaSO (s)+2HO(1) △H=-114.
2 4 2 4 2
6kJ•mol-1
【答案】B
【解析】A.根据盖斯定律,由①-②可得HF(aq)⇌F-(aq)+H+(aq)△H=(-67.7kJ•mol-1)-
(-57.3kJ•mol-1)=-10.4kJ•mol-1<0,A项错误;B.根据盖斯定律,由③-②可得HCN(aq)⇌CN-(aq)+H+
(aq)△H=(-12.1kJ•mol-1)-(-57.3kJ•mol-1)=+45.2kJ•mol-1kJ•mol-1,B项正确;C.中和反应反应热是指在稀溶液
中,强酸与强碱发生中和反应生成lmolHO时的反应热,与反应物的量无关,C项错误;D.由HSO (aq)
2 2 4
+Ba(OH) (aq)=BaSO (s)+2HO(l)可知反应生成2molH O同时生成BaSO 沉淀,因此反应放出热量
2 4 2 2 4
>114.6kJ•mol-1,D项错误;故选B。
4.(2023·江西吉安·吉安三中校考一模)下列热化学方程式正确的是
A.已知2C(s)+2O(g)=2CO (g) ΔH=akJ·mol-1,2C(s)+O(g)=2CO(g) ΔH=bkJ·mol-1,则a0,则石墨比金刚石稳定
C.已知NaOH(aq)+HCl(aq)=NaCl(aq)+H O(l) ΔH=-57.4kJ·mol-1,则20.0gNaOH固体与稀盐酸完全中和,
2
放出28.7kJ的热量
D.已知2C(s)+2O(g)=2CO (g) ΔH;2C(s)+O(g)=2CO(g) ΔH,则ΔH>ΔH
2 2 l 2 2 l 2
【答案】B
【解析】A.燃烧热是在25℃、101kP下用1mol可燃物完全燃烧生成稳定氧化来进行测定的,因为所给方
程式中水的状态不是液态,所以不能确定氢气的燃烧热数值,故A错误;B.物质的能量越低越稳定,因
为石墨转化为金刚石为吸热反应,可知石墨的能量低于金刚石的能量,所以石墨比金刚石稳定,故B正确;
C.中和热是指稀的强酸强碱溶液发生中和反应生成1mol水时放出的热量,而氢氧化钠固体溶于水时会放
出大量的热,所以20.0 g NaOH固体与稀盐酸完全中和时,放出的热量大于28.7 kJ,故C错误;
D.ΔH 为碳单质完全燃烧时的反应热,ΔH 为碳单质不完全燃烧时的反应热,燃烧反应为放热反应所以
1 2
ΔH均为负数,所以ΔH 小于ΔH,故D错误;故选:B。
1 2
7.(2023·辽宁·校联考模拟预测)下列有关及应热和热化学方程式的描述不正确的是
A.已知: ,则稀氨水和稀 溶液完全反应生成
时,放出热量少于
B.热化学方程式各物质前的化学计量数既可以是整数也可以是分数,既表示分子数也表示物质的量
C. ,20℃和25℃时, 的燃烧热不同
D.键能数值为平均值,用键能求出的反应热是估算值【答案】B
【解析】A.已知: ,由于氨水是弱碱,属于弱电解质,其在
水溶液中边反应边电离,电离是一个吸热过程,则稀氨水和稀 溶液完全反应生成 时,放
出热量少于 ,A正确;B.热化学方程式各物质前的化学计量数用于表示其物质的量,而不是其分
子数,故热化学方程式各物质前的化学计量数既可以是整数也可以是分数,B错误;C.燃烧热与外界的
压强和温度有关,相同质量的物质在不同温度下具有的总能量不同,故101kpa,20℃和25℃时,CH 的燃
4
烧热不同,C正确;D.化学反应的微观本质为旧化学键的断裂和新化学键的形成过程,可以用反应物的
总键能减去生成物的总键能来估算反应热,即键能数值为平均值,用键能求出的反应热是估算值,D正确;
故答案为:B。
8.(2023·山东菏泽·山东省鄄城县第一中学校考三模)已知 、 、 可作为燃料电池
的燃料,其相关热化学方程式如下。
①
②
③
④
下列说法正确的是
A.
B.反应③的
C.反应①中若生成 ,则
D.反应②中的 能表示甲烷的燃烧热
【答案】D
【解析】A.根据盖斯定律,方程式 ,所以 ,A错误;B.根据反应
③, ,B错误;C.反应①中若生成 ,从 变成 要吸收能量,使放出的能量减
小, 变大,则 ,C错误;D. 甲烷完全燃烧,生成 和 放出的热量为燃烧热,
则反应②中的 能表示甲烷的燃烧热,D正确;故选D。
考点三 盖斯定律 反应热计算
1.(2023·河北衡水·衡水市第二中学校考模拟预测)尿素是重要的化工原料,也常用作氮肥。以氨为原料
合成尿素的相关反应如下:
① ;②
;③;④ 。
下列叙述正确的是
A.反应①在较高温度下易自发进行
B.反应②的平衡常数
C.在恒容密闭容器中发生反应②,当气体摩尔质量不变时反应达到平衡
D.
【答案】D
【解析】A.反应①为放热的熵减反应,根据 反应可以自发进行,则在较低温度下易自发进行,
A错误;B.平衡常数等于平衡时生成物浓度系数次方之积与反应物浓度系数次方之积的比,纯固体和纯
液体不计入其中;反应②的平衡常数 ,B错误;C.在恒容密闭容器中发生反应②,反应中只有
水一种气体,其摩尔质量为定值,当气体摩尔质量不变时,不能说明反应达到平衡,C错误;D.由盖斯
定律可知,反应①+②-③得反应④ ,则 ,
D正确;故选D。
2.(2023·浙江绍兴·统考模拟预测)甲醇与水蒸气在催化剂作用下发生如下反应:
反应Ⅰ:CHOH(g) CO (g)+ 2H (g) ΔH
3 2 1
反应Ⅱ:CO (g)+ H O(g) CO (g)+ H (g) ΔH
2 2 2 2
根据能量变化示意图,下列说法正确的是
A.E-E >E-E
3 2 4 1
B.反应Ⅱ决定整个反应的速率
C.催化剂可以降低总反应的焓变
D.CHOH(g)+HO(g) CO(g)+3H(g) ΔH=ΔH -ΔH
3 2 2 2 1 2
【答案】A
【解析】A.由于绝对值 ,该值为负值,去掉绝对值后,E-E >E-E ,A选项正确;B.
3 2 4 1由图可知,反应I正反应的活化能为E-E ,反应Ⅱ的活化能为E-E ,反应I的活化能较大,则反应I的反
1 5 2 3
应速率慢于反应Ⅱ,反应I决定整个反应的速率,B选项错误;C.催化剂可改变反应的活化能,反应的焓
变由始态和终态决定,催化剂不改变焓变,C选项错误;D.根据盖斯定律,反应I+Ⅱ可得目标方程
CH
3
OH(g)+H
2
O(g)⇌CO
2
(g)+3H
2
(g) ΔH=ΔH
1
+ΔH
2
,D选项错误;答案选A。
3.(2023·上海普陀·统考二模)在生产、生活、科技中,氢能已获得越来越多的关注,是非常重要的能源。
已知:
下列推断正确的是
A.HO(l)吸收能量后,分子中氢氧键断裂而生成HO(g)
2 2
B.2H(g)+O(g)=2HO(g) =-484 kJ
2 2 2
C.若2H(g)+O(g)=2HO(g)+Q;2H(g)+O(l)=2H O(g)+Q;则Q>Q
2 2 2 1 2 2 2 2 1 2
D.将2 mol H O(g)分解成H(g)和O(g),吸收4×463 kJ的热量
2 2 2
【答案】C
【解析】A.HO(l)吸收能量后变为HO(g)是物理变化,分子中氢氧键不断裂,A错误;B.由题干转化历
2 2
程图可知,2H(g)+O(g)=2HO(g) =2×436kJ/mol+496kJ/mol-4×463kJ/mol=-484kJ/mol,B错误;C.
2 2 2
由于O(l)变为O(g)的过程需要吸收热量,故若2H(g)+O(g)=2HO(g)+Q;2H(g)+O(l)=2H O(g)+Q,
2 2 2 2 2 1 2 2 2 2
前者放出的热量大于后者即 Q>Q,C正确;D.由B项分析可知,将2 mol H O(g)分解成H(g)和
1 2 2 2
O(g),吸收484 kJ的热量,D错误;故答案为:C。
2
4.(2023·浙江金华·校联考模拟预测)某小组为测定NaCl晶体中离子键断裂时所需要的能量(△H),设计
4
了如图所示的转化关系,则△H 可表示为
4
A.△H+△H -△H-△H+△H B.△H+△H +△H -△H+△H
1 2 3 5 6 1 2 3 5 6
C.△H+△H +△H -△H-△H D.△H+△H -△H-△H-△H
1 2 3 5 6 3 5 1 2 6
【答案】A
【解析】由图可知,氯化钠和溴化钠固体通过过程1、2、6得到的微粒和通过过程3、4、5得到的微粒都
是Na+(g)、Br-(aq)、Na+(aq)、Cl-(aq),故两部分的反应热相同,△H+△H +△H =△H +△H +△H ,即
3 4 5 1 2 6
△H=△H +△H -△H-△H+△H ;故选A。
4 1 2 3 5 6
5.(2023·浙江·校联考三模)标准状态下,气态反应物、生成物及活化分子[A(B)表示“A+B→产物”的
活化分子]的相对能量如表所示:物质
相对能量/
91.3 33.2 -296.8 -395.7 0 142.7 237.2 -96.1
下列说法不正确的是
A.
B. 反应不能自发进行
C.相同条件下, 比 速率快
D.1mol (g)的总键能大于1mol NO(g)总键能
【答案】C
【解析】A. ΔH=生成物总能量-反应物总能量=91.3kJ/mol+
(-395.7kJ/mol)-[33.2kJ/mol+(-296.8kJ/mol)]=-40.8kJ/mol,故A正确;B. H=生成物
总能量-反应物总能量=+285.4kJ/mol>0,且 S<0,则任何温度下 H-T S>0,即反应
不能自发进行,故B正确;C.反应 的活化能=活化分子能量-反应物总
能量=-96.1kJ/mol-(-296.8kJ/mol+142.7kJ/mol)=58kJ/mol,反应 的活化
能为237.2kJ/mol-(91.3kJ/mol+142.7kJ/mol)=3.2kJ/mol<58kJ/mol,反应的活化能越高,反应速率越慢,
则相同条件下, 比 速率慢,故C错误;
D.反应 ΔH=生成物总能量-反应物总能量=2×33.2kJ/mol-2×91.3kJ/mol-0kJ/
mol=-116.2kJ/mol,为放热反应,焓变△H=反应物总键能-生成物总键能,则该反应反应物总键能<生成物
总键能,即1molNO(g)和0.5molO 总键能<1molNO (g)的总键能,所以1molNO (g)的总键能大于
2 2 2
1molNO(g)总键能,故D正确;故选:C。
6.(2023·浙江金华·浙江省丽水中学校联考一模)在标准状况下,1mol离子晶体完全分离成气态阳离子、
阴离子所吸收的能量可以用(U)来表示,LiO 是离子晶体,其(U)的实验值可通过玻恩—哈伯热力学循环图
2
计算得到
已知 ;
下列说法不正确的是A.U(LiO)=+2980kJ/mol B.O=O键能为498kJ/mol
2
C.ΔH=703kJ/mol D.Li第一电离能I=1040kJ/mol
2 1
【答案】D
【解析】A.从图分析,2mol气态锂离子和1mol气态氧离子生成氧化锂晶体放热为2980kJ,则
U(LiO)=+2980kJ/mol,A正确;B.从图分析,0.5mol氧气变成氧原子吸收249kJ的能量,故O=O键能为
2
498kJ/mol,B正确;C.已知 ; ,
根据盖斯定律分析,ΔH= =703kJ/mol
2
,C错误;D.从盖斯定律分析,有-598=-2980+249+703+318+ΔH,则ΔH=1040kJ/mol,则锂的第一电离
1 1
能为520kJ/mol ,D错误;故选D。
7.(2023·重庆九龙坡·统考二模)火箭发射时可以用液态肼作燃料, 作氧化剂。相关物质的能量转化
关系如下。已知 ,则
的反应热 为
A. B. C. D.
【答案】A
【解析】根据图示信息,可得已知反应:
可得目标方程式: ,所以
,故选A。
8.(2023·重庆·重庆南开中学校考三模)将2 mol 和3 mol 置于密闭容器中,在250℃下只发生如
下两个反应:
kJ/mol
kJ/mol
一段时间后, 和 恰好全部消耗,共放出303 kJ热量。
已知:部分化学键的键能如下表所示
化学键 (ClF中) ( 中)键能/(kJ/mol) 157 243 248 X
则X的值为
A.172 B.202 C.238 D.258
【答案】A
【分析】根据反应热与键能的关系△H=∑D(反应物)−∑D(生成物),可求出a,以及用x把b表示出
来,然后根据化学方程式的计算可解。
【解析】根据反应热与键能的关系△H=∑D(反应物)−∑D(生成物),由题意Cl+F═2ClF ΔH =
2 2 1
akJ/mol;Cl+3F═2ClF ΔH=bkJ/mol可知;ΔH=(243+157−2×248)kJ/mol=−96kJ/mol,ΔH=(243
2 2 3 2 1 2
+3×157−2×3x)kJ/mol=(714−6x)kJ/mol,即a=−96,b=714−6x,设参与Cl+F═2ClF ΔH1=akJ/mol
2 2
的氯气物质的量为m,则消耗的氟气也为m,剩下的氯气和氟气正好按Cl+3F═2ClF ΔH=bkJ/mol的系
2 2 3 2
数比反应,即 ,解之得,m=1.5mol,则有1.5mol×(−96kJ/mol)+0.5mol×(714−6x)kJ/mol=
303kJ,解之得x=172,故答案选A。