文档内容
专题 29 弱电解质的电离平衡
(建议完成时间:45分钟 实际完成时间:_______分钟)
目 录
考点一 弱电解质的电离平衡及影响因素
考点二 电离度、电离平衡常数及计算
考点一 弱电解质的电离平衡及影响因素
1.(2023·北京东城·统考二模) 时, 的电离常数 , 的电离常数 、
。下列说法不正确的是
A. 溶液和 溶液中离子种类相同
B. 时,反应 的
C. ,物质的量浓度相同的 溶液与 溶液的 :前者小于后者
D.向氯水中加入少量 固体, 增大
【答案】B
【解析】A.碳酸钠电离出钠离子和碳酸根离子,碳酸根离子水解生成碳酸氢根离子,碳酸氢根离子水解
生成碳酸分子,碳酸氢钠电离出钠离子和碳酸氢根离子,碳酸氢根离子电离出碳酸根离子和氢离子,碳酸
氢根离子水解生成碳酸分子和氢氧根离子,两种溶液中离子种类相同,A正确;B. 时,反应
的 ,B错误;C.从电离平衡
常数分析,次氯酸的电离平衡常数比碳酸氢根离子的电离平衡常数大,根据越弱越水解分析,碳酸根离子
水解程度大,溶液碱性强,pH大,C正确;D.氯水中含有盐酸和次氯酸,盐酸能和碳酸氢钠反应,使氯
气和水反应的平衡正向移动,次氯酸的浓度增大,D正确;故选B。
2.(2023·天津河东·统考二模)常温下,下列事实能说明某一元酸 是一元强酸的是
A. 溶液的
B. 溶液
C. 溶液比 硝酸导电能力弱
D. 溶液与 溶液混合
【答案】D
【解析】A. 溶液的 ,说明HX在水溶液中只能部分电离,属于一元弱酸,A不合题意;
B. 溶液 ,说明NaX是强碱弱酸盐,因为X-水解呈碱性,即HX为一元弱酸,B不
合题意;C. 溶液比 硝酸导电能力弱说明HX只能部分电离,属于一元弱酸,C
1
原创精品资源学科网独家享有版权,侵权必究!不合题意;D. 溶液与 溶液,二者前后完全反应生成NaX,混
合后溶液 即说明NaX为强酸强碱盐,即说明HX为一元强酸,D符合题意;故答案为:D。
3.(2023·四川南充·统考三模)如图所示,常温下,往甲室和乙室中分别加入等体积、浓度均为0.1mol/L
的CHCOONH 溶液(pH≈7)和CHCOOH溶液(pH≈3),中间用交换膜隔开(只有未电离的CHCOOH分子可
3 4 3 3
自由通过交换膜,且不考虑溶液体积的变化),达到平衡后,下列说法错误的是
A.常温下,K(CHCOOH)≈1.0×10-5
a 3
B.平衡后,甲、乙两室pH相等
C.平衡后,甲室中:c(NH )<c(CHCOO-)
3
D.平衡前,CHCOOH分子从乙室进入甲室
3
【答案】B
【分析】0.1mol/L CH COONH 溶液pH约为7,说明铵根离子和CHCOO-离子在溶液中的水解程度几乎相
3 4 3
等,溶液中CHCOOH和一水合氨的浓度约为10—7mol/L,由只有未电离的CHCOOH分子可自由通过交换
3 3
膜可知,甲室溶液中CHCOOH的浓度小于乙室,乙室中CHCOOH通过交换膜进入甲室,当两室溶液中
3 3
CHCOOH浓度相等时,乙室的电离和甲室的水解都达到平衡。
3
【解析】A.由0.1mol/LCH COOH溶液pH约为3可知,电离c(CHCOO-)≈c(H+)=10-3mol/L,常温下,
3 3
K(CHCOOH)≈ =1.0×10-5,故A正确;B.由分析可知,当两室溶液中HA
a 3
浓度相等时,乙室的电离和甲室的水解都达到平衡,由于甲室中的A—离子会抑制HA的电离,所以平衡后,
甲、乙两室的溶液pH不相等,故B错误;C.CHCOONH 溶液pH≈7,由电荷守恒:c(H+)+c(
3 4
)=c(OH-)+c(CH COO-),乙室中CHCOOH通过交换膜进入甲室使c(CHCOO-)增大,平衡后,甲室中:c(
3 3 3
)<c(CHCOO-),故C正确;D.由分析可知,只有未电离的CHCOOH分子可自由通过交换膜可知,
3 3
甲室溶液中CHCOOH的浓度小于乙室,乙室中CHCOOH通过交换膜进入甲室,故D正确;故选:B。
3 3
4.(2023·上海闵行·统考二模)室温下,甲、乙两烧杯均盛有20mLpH=4的醋酸溶液,向乙烧杯中加水稀
释至pH=5,对此时两烧杯中溶液描述正确的是
A.溶液体积:10V >V
甲 乙
B.水电离出的H+浓度:c(H+) =10c(H+)
甲 乙
C.若分别用pH=10的NaOH溶液恰好完全中和,所得溶液的pH:甲>乙
D.若分别与10mLpH=10的NaOH溶液反应,所得溶液的pH:甲>乙
【答案】C【解析】A.醋酸是弱酸,加水稀释,醋酸电离平衡正向移动,pH=4的醋酸溶液加水稀释10倍,稀释后
溶液pH<5,若使pH=5,需继续加水稀释,所以溶液体积:10V 乙,所以pH:甲>乙,故C正确;D.若分
别与10mLpH=10的NaOH溶液反应,剩余醋酸的物质的量相等,所得溶液的体积甲<乙,剩余醋酸的浓度
甲>乙,所得溶液的pH:甲<乙,故D错误;选C。
5.(2023秋·河北衡水·高三河北武强中学校考开学考试)在0.1 mol·L-1的HCN溶液中存在如下电离平衡:
HCN H++CN-。下列叙述正确的是
A.加入少量NaOH固体,平衡正向移动
B.加入少量NaCN固体,平衡正向移动
C.加水,平衡逆向移动
D.滴加少量0.1 mol·L-1HCl溶液, 溶液中c(H+)减小
【答案】A
【解析】A.加入NaOH固体,OH-与H+结合,促进平衡正向进行,A正确;B.加入NaCN固体,溶液中
CN-的浓度增大,促进平衡逆向进行,B错误;C.加水,促进电离,平衡正向进行,C错误;D.加入
HCl,溶液中H+浓度增大,平衡逆向进行,CN-浓度减小,D错误;故答案为:A。
6.(2023春·河南漯河·高三漯河高中校考开学考试)柠檬酸是天然防腐剂和食品添加剂,它是一种有机三
元酸,常温下可以与NaOH溶液反应生成柠檬酸钠(用NaY表示),下列说法正确的是
3
A.柠檬酸的电离方程式为HY 3H++Y3-
3
B.pH=2的HY溶液c(H+)=0.03mol•L-1
3
C.NaHY溶液加水稀释过程中, 保持不变
2
D.NaY溶液的pH随着c(Na Y)的增大而增大
3 3
【答案】D
【解析】A.柠檬酸属于三元弱酸,分步电离,电离方程式为
,A错误;B.pH=2的 溶液, 应为
,B错误;C.温度恒定, 的水解平衡常数不变, 为定值,加水稀释时,
减小, 应增大,C错误;D. 水解使溶液呈碱性,随 增大,溶液碱性越强,溶
液的pH增大,D正确;答案选D。
7.(2023春·广东·高三统考开学考试)下列关于 的配制及测定,说法正确的是
(1)室温下,取一定量冰醋酸,进行如下实验:
①将冰醋酸配制成 醋酸溶液;②取20mL①所配溶液,加入a mL NaOH溶液,充分反应后,测得溶液 ;③向②所得溶液中继续滴加稀盐酸,直至溶液中 。
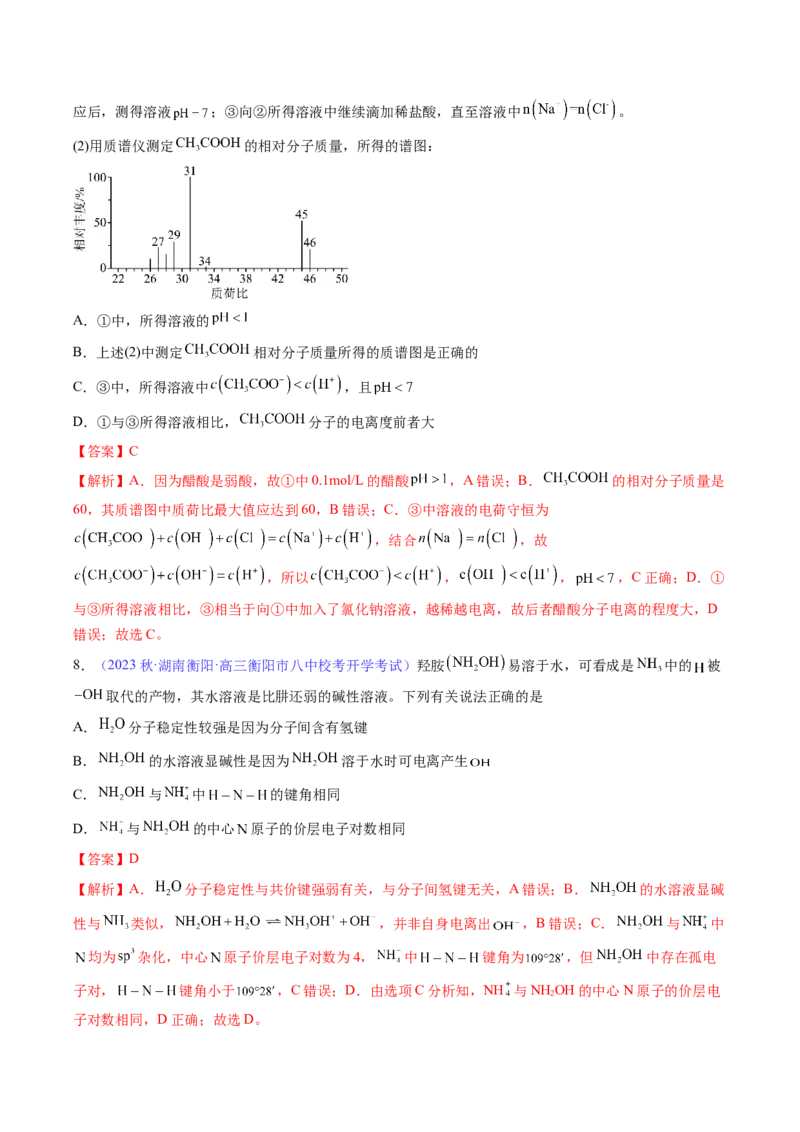
(2)用质谱仪测定 的相对分子质量,所得的谱图:
A.①中,所得溶液的
B.上述(2)中测定 相对分子质量所得的质谱图是正确的
C.③中,所得溶液中 ,且
D.①与③所得溶液相比, 分子的电离度前者大
【答案】C
【解析】A.因为醋酸是弱酸,故①中0.1mol/L的醋酸 ,A错误;B. 的相对分子质量是
60,其质谱图中质荷比最大值应达到60,B错误;C.③中溶液的电荷守恒为
,结合 ,故
,所以 , , ,C正确;D.①
与③所得溶液相比,③相当于向①中加入了氯化钠溶液,越稀越电离,故后者醋酸分子电离的程度大,D
错误;故选C。
8.(2023秋·湖南衡阳·高三衡阳市八中校考开学考试)羟胺 易溶于水,可看成是 中的 被
取代的产物,其水溶液是比肼还弱的碱性溶液。下列有关说法正确的是
A. 分子稳定性较强是因为分子间含有氢键
B. 的水溶液显碱性是因为 溶于水时可电离产生
C. 与 中 的键角相同
D. 与 的中心 原子的价层电子对数相同
【答案】D
【解析】A. 分子稳定性与共价键强弱有关,与分子间氢键无关,A错误;B. 的水溶液显碱
性与 类似, ,并非自身电离出 ,B错误;C. 与 中
均为 杂化,中心 原子价层电子对数为4, 中 键角为 ,但 中存在孤电
子对, 键角小于 ,C错误;D.由选项C分析知,NH 与NH OH的中心N原子的价层电
2
子对数相同,D正确;故选D。9.(2023·浙江·校联考一模)已知25℃时, 。某体系中,膜只允许未电离的HA自由通
过(如图所示)。
设溶液中 ,当达到平衡时,下列叙述正确的是
A.溶液Ⅰ和Ⅱ中的 不相等
B.溶液Ⅰ中
C.溶液Ⅱ中的HA的电离度为
D.溶液Ⅰ、Ⅱ中水电离出的 之比为
【答案】C
【解析】A.根据题意,未电离的HA可自由穿过隔膜,故溶液I和Ⅱ中的c(HA)相等,A错误;B.由图
可知溶液I本应显酸性,常温下溶液I的pH=7.0,则溶液I中c(H+)=c(OH-)=1×10-7mol/L,c(H+)<c(OH-)
+c(A-),B错误;C.常温下溶液Ⅱ的pH=3.0,溶液中c(H+)=0.001mol/L,K= =1.0×10-5,c
a 总
(HA)=c(HA)+c(A-),则 =1.0×10-5,解得 = ,C正确;D.溶液Ⅰ中水电离出的
c(H+)=10-7mol/L、Ⅱ中水电离出的c(H+)=c(OH-)= mol/L=10-11mol/L,溶液Ⅰ、Ⅱ中水电离出的c(H+)之
比=10-7mol/L:10-11mol/L=104:1,D错误;故答案为:C。
10.(2023秋·贵州贵阳·高三校联考开学考试)下列有关电解质溶液的说法错误的是
A.向0.1mol/L 溶液中加入少量水,溶液中 不变
B.将 溶液从20℃升温至30℃,溶液 增大
C.向盐酸中加入氨水至中性,溶液中
D.向AgCl、AgBr的饱和溶液中加入少量 溶液,溶液中 不变
【答案】B【解析】A.电离常数是温度函数,温度不变,电离常数不变,醋酸溶液加水稀释时,溶液中
= ,醋酸的电离常数不变,则溶液中 不变,故A正确;B.
醋酸钠在溶液中的水解反应是吸热反应,升高温度,水解平衡向正反应方向移动,水解常数K 增大,溶液
h
中 = ,则醋酸钠溶液从20℃升温至30℃时,溶液中 减小,
故B错误;C.向盐酸中加入氨水至中性时,溶液中氢离子浓度等于氢氧根离子浓度,由电荷守恒c(NH )
+c(H+)=c(Cl—)+ c(OH—)可知,溶液中 ,故C正确;D.向A氯化银、溴化银的饱和溶液中加入
少量硝酸银溶液,溶液中 = = ,溶度积是温度函数,温度不变,溶度积不
变,则溶液中 不变,故D正确;故选B。
考点二 电离度、电离平衡常数及计算
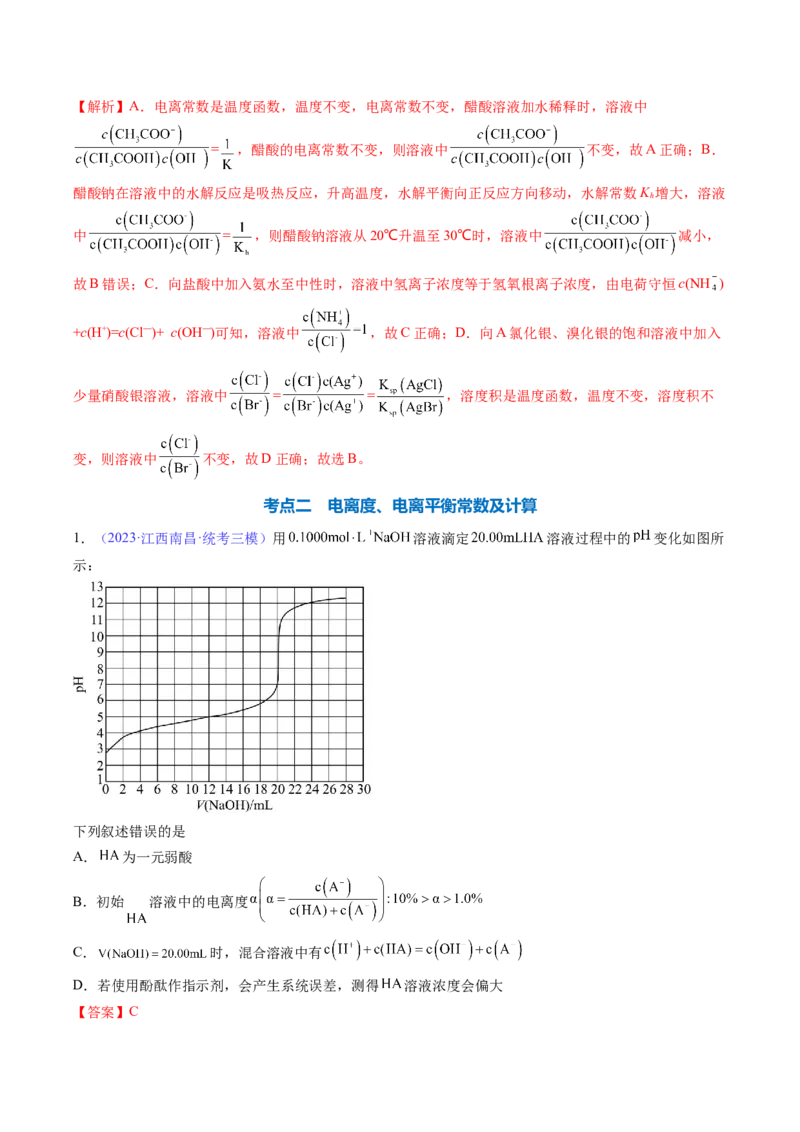
1.(2023·江西南昌·统考三模)用 溶液滴定 溶液过程中的 变化如图所
示:
下列叙述错误的是
A. 为一元弱酸
B.初始 溶液中的电离度
C. 时,混合溶液中有
D.若使用酚酞作指示剂,会产生系统误差,测得 溶液浓度会偏大
【答案】C【分析】滴定过程中溶液pH突变时, ,此时参与反应的 ,由此可知
HA的初始浓度为 。
【解析】A.初始溶液 ,说明HA未完全电离,因此 为一元弱酸,故A项正确;B.初始HA
溶液中 ,初始溶液中 稍大于 , ,
因此初始 溶液中的电离度 ,故B项正确;C. 时,溶
液中溶质为NaA,溶液中存在电荷守恒: ,物料守恒:
,因此 ,故C项错误;D.酚酞试液在溶液pH>10时变红,
由图可知当溶液pH>10时,所加NaOH溶液体积大于20mL,因此测得 溶液浓度会偏大,故D项正确;
综上所述,错误的是C项。
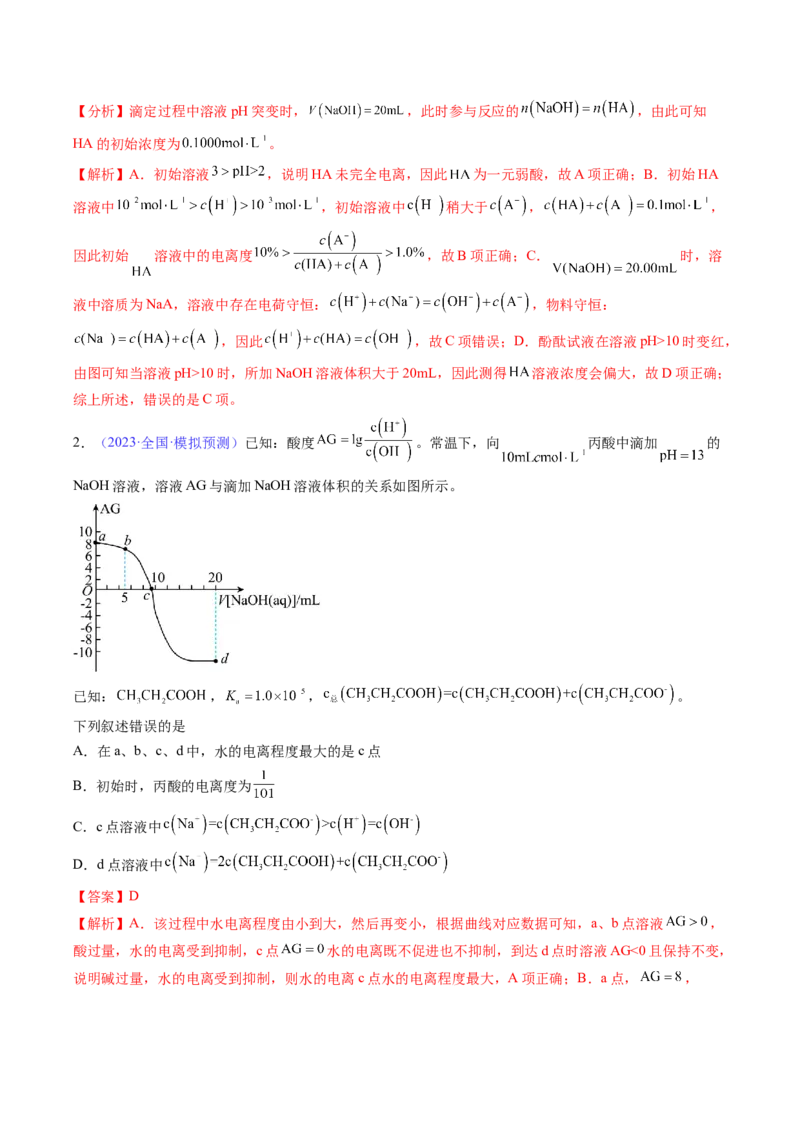
2.(2023·全国·模拟预测)已知:酸度 。常温下,向 丙酸中滴加 的
NaOH溶液,溶液AG与滴加NaOH溶液体积的关系如图所示。
已知: , , 。
下列叙述错误的是
A.在a、b、c、d中,水的电离程度最大的是c点
B.初始时,丙酸的电离度为
C.c点溶液中
D.d点溶液中
【答案】D
【解析】A.该过程中水电离程度由小到大,然后再变小,根据曲线对应数据可知,a、b点溶液 ,
酸过量,水的电离受到抑制,c点 水的电离既不促进也不抑制,到达d点时溶液AG<0且保持不变,
说明碱过量,水的电离受到抑制,则水的电离c点水的电离程度最大,A项正确;B.a点, ,,则 ,根据丙酸电离常数表达式可知,
,则 ,又
,则
,解得 ,B项正确;C.c点溶
液呈中性, ,根据电荷守恒 ,则
,因此 ,C项正确;D.若丙酸起
始浓度c=1 ,d点溶液中溶质为 和NaOH,此时二者浓度相等,则存在物料守恒
,D项错误;故答案为:D。
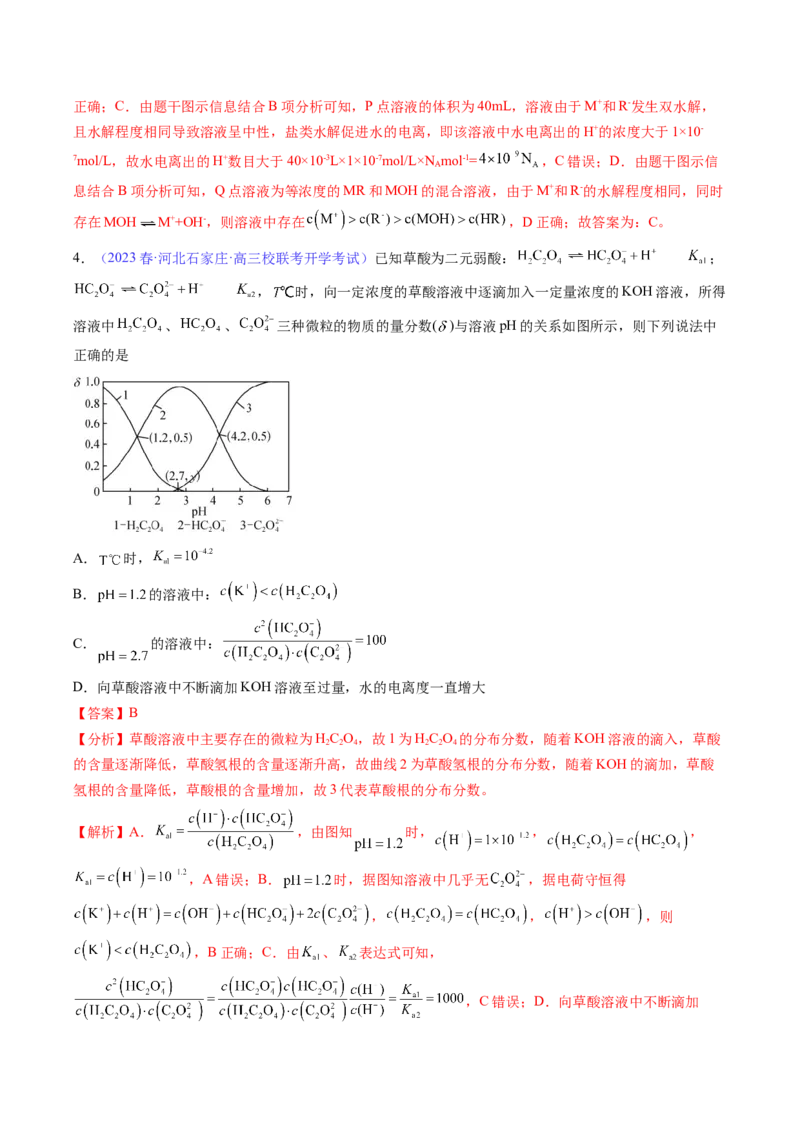
3.(2023春·河北沧州·高三校联考期中)25℃时,向20.0mL0.100mol/LHR溶液中滴加0.100mol/LMOH溶
液,混合溶液的pH与加入MOH溶液体积的变化关系如图所示。设N 为阿伏加德罗常数的值。下列说法
A
错误的是
A. 的电离常数的数量级为
B. 溶液的电离度大于
C.P点溶液中水电离出的H+数目为
D.Q点溶液中存在
【答案】C
【解析】A.由题干图示信息可知,0.100mol/L的HR溶液的pH为2.7,则HR的电离常数Ka=
≈ ,则其数量级为 ,A正确;B.由题干图示信息可知,加入20.00mLMOH溶液时溶液的pH
等于7,则说明M+和R-的水解程度相同,即MOH的电离平衡常数与HR的相等,则有
溶液中:c(M+)=c(OH-)= =10-2.7mol/L,则其电离度为: ≈2.0%,大于 ,B正确;C.由题干图示信息结合B项分析可知,P点溶液的体积为40mL,溶液由于M+和R-发生双水解,
且水解程度相同导致溶液呈中性,盐类水解促进水的电离,即该溶液中水电离出的H+的浓度大于1×10-
7mol/L,故水电离出的H+数目大于40×10-3L×1×10-7mol/L×N mol-1= ,C错误;D.由题干图示信
A
息结合B项分析可知,Q点溶液为等浓度的MR和MOH的混合溶液,由于M+和R-的水解程度相同,同时
存在MOH M++OH-,则溶液中存在 ,D正确;故答案为:C。
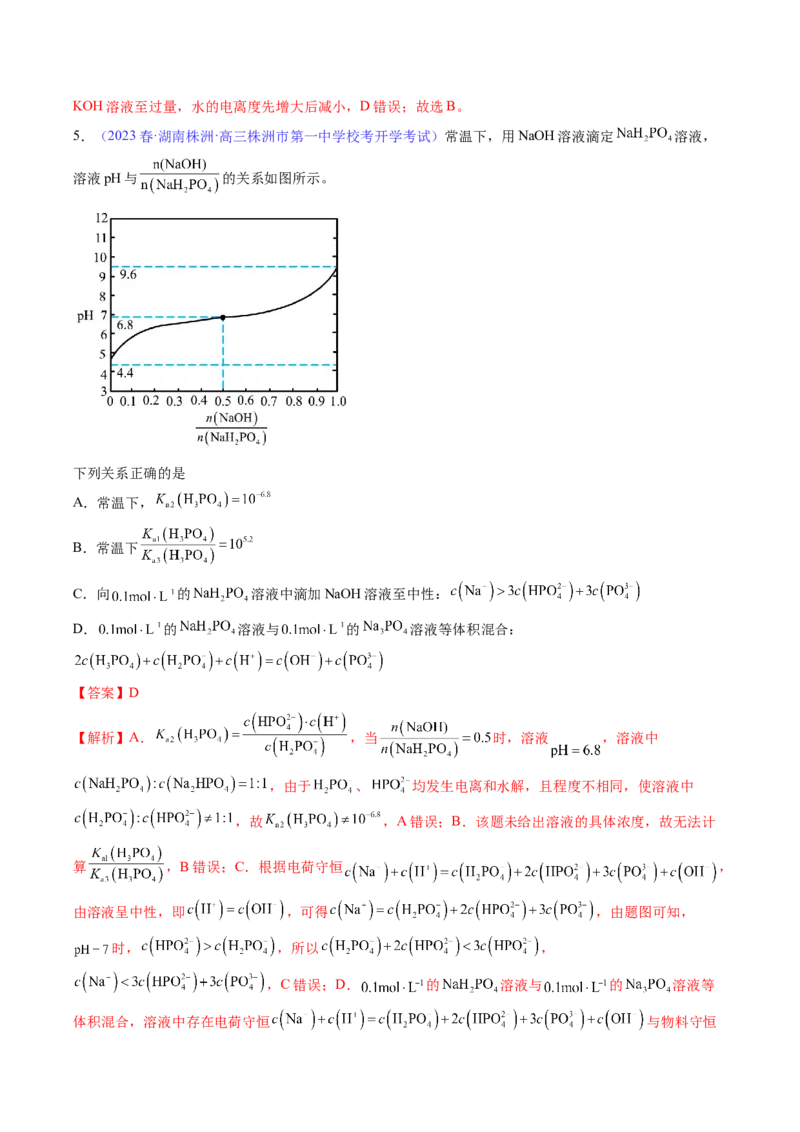
4.(2023春·河北石家庄·高三校联考开学考试)已知草酸为二元弱酸: ;
, 时,向一定浓度的草酸溶液中逐滴加入一定量浓度的KOH溶液,所得
溶液中 、 、 三种微粒的物质的量分数( )与溶液pH的关系如图所示,则下列说法中
正确的是
A. 时,
B. 的溶液中:
C. 的溶液中:
D.向草酸溶液中不断滴加KOH溶液至过量,水的电离度一直增大
【答案】B
【分析】草酸溶液中主要存在的微粒为HC O,故1为HC O 的分布分数,随着KOH溶液的滴入,草酸
2 2 4 2 2 4
的含量逐渐降低,草酸氢根的含量逐渐升高,故曲线2为草酸氢根的分布分数,随着KOH的滴加,草酸
氢根的含量降低,草酸根的含量增加,故3代表草酸根的分布分数。
【解析】A. ,由图知 时, , ,
,A错误;B. 时,据图知溶液中几乎无 ,据电荷守恒得
, , ,则
,B正确;C.由 、 表达式可知,
,C错误;D.向草酸溶液中不断滴加KOH溶液至过量,水的电离度先增大后减小,D错误;故选B。
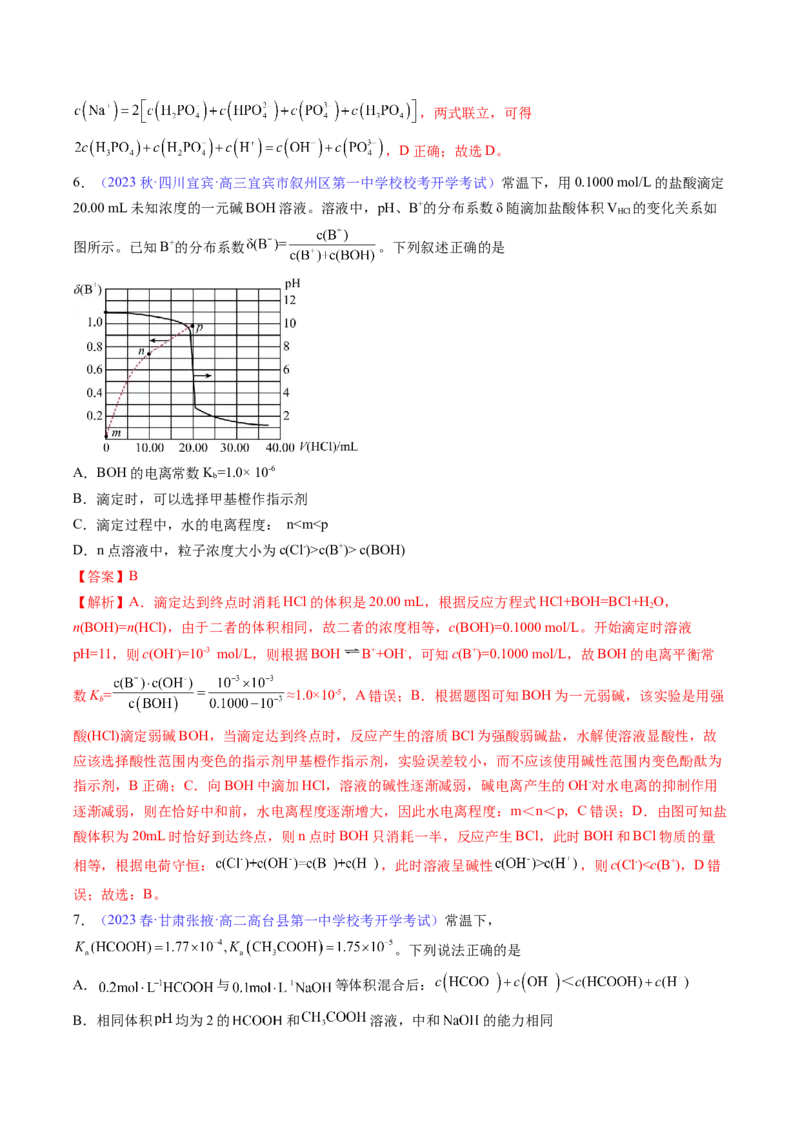
5.(2023春·湖南株洲·高三株洲市第一中学校考开学考试)常温下,用NaOH溶液滴定 溶液,
溶液pH与 的关系如图所示。
下列关系正确的是
A.常温下,
B.常温下
C.向 的 溶液中滴加NaOH溶液至中性:
D. 的 溶液与 的 溶液等体积混合:
【答案】D
【解析】A. ,当 时,溶液 ,溶液中
,由于 、 均发生电离和水解,且程度不相同,使溶液中
,故 ,A错误;B.该题未给出溶液的具体浓度,故无法计
算 ,B错误;C.根据电荷守恒 ,
由溶液呈中性,即 ,可得 ,由题图可知,
时, ,所以 ,
,C错误;D. 的 溶液与 的 溶液等
体积混合,溶液中存在电荷守恒 与物料守恒,两式联立,可得
,D正确;故选D。
6.(2023秋·四川宜宾·高三宜宾市叙州区第一中学校校考开学考试)常温下,用0.1000 mol/L的盐酸滴定
20.00 mL未知浓度的一元碱BOH溶液。溶液中,pH、B+的分布系数δ随滴加盐酸体积V 的变化关系如
HCl
图所示。已知B+的分布系数 。下列叙述正确的是
A.BOH的电离常数K=1.0× 10-6
b
B.滴定时,可以选择甲基橙作指示剂
C.滴定过程中,水的电离程度: nc(B+)> c(BOH)
【答案】B
【解析】A.滴定达到终点时消耗HCl的体积是20.00 mL,根据反应方程式HCl+BOH=BCl+H O,
2
n(BOH)=n(HCl),由于二者的体积相同,故二者的浓度相等,c(BOH)=0.1000 mol/L。开始滴定时溶液
pH=11,则c(OH-)=10-3 mol/L,则根据BOH B++OH-,可知c(B+)=0.1000 mol/L,故BOH的电离平衡常
数K = ≈1.0×10-5,A错误;B.根据题图可知BOH为一元弱碱,该实验是用强
b
酸(HCl)滴定弱碱BOH,当滴定达到终点时,反应产生的溶质BCl为强酸弱碱盐,水解使溶液显酸性,故
应该选择酸性范围内变色的指示剂甲基橙作指示剂,实验误差较小,而不应该使用碱性范围内变色酚酞为
指示剂,B正确;C.向BOH中滴加HCl,溶液的碱性逐渐减弱,碱电离产生的OH-对水电离的抑制作用
逐渐减弱,则在恰好中和前,水电离程度逐渐增大,因此水电离程度:m<n<p,C错误;D.由图可知盐
酸体积为20mL时恰好到达终点,则n点时BOH只消耗一半,反应产生BCl,此时BOH和BCl物质的量
相等,根据电荷守恒: ,此时溶液呈碱性 ,则c(Cl-)