文档内容
专题三 复杂离子方程式的书写 基础过关检测
考试时间:70分钟 卷面分值:100分
学校:___________姓名:___________班级:___________考号:___________
注意事项:
1.答题前,务必将自己的姓名、考号填写在答题卡规定的位置上。
2.答选择题时,必须使用2B铅笔将答题卡上对应题目的答案标号涂黑。如需改动,用
橡皮擦擦干净后,再选涂其它答案标号。
3.答非选择题时,必须将答案书写在专设答题页规定的位置上。
4.所有题目必须在答题卡上作答。在试题卷上答题无效。
5.考试结束后,只交试卷答题页。
可能用到的相对原子质量:H-1 C-12 N-14 O-16 Na-23 Mg-24 S-32 Cl-35.5
1.(模拟)硫化氢(H S)是一种有毒气体,高于200℃分解,脱除HS的方法很多,如
2 2
用NaCO 吸收,含HS的气体与饱和NaCO 溶液在吸收塔内逆流接触,生成两种酸
2 3 2 2 3
式盐。该反应的离子方程式为_______。
2.(2023秋·广东广州·高三广州市南武中学校考期末)黑木耳中含有丰富的人体所必
需的铁元素。某研究小组测定黑木耳中铁元素含量,实验方案如下。回答下列问题:
(2)测定黑木耳中铁元素含量(已知黑木耳提取液中铁元素以Fe2+和Fe3+的形式存在)
步骤一 取112g黑木耳,经灼烧、酸浸制得提取液,加入过量的铜粉
步骤二 过滤,向滤液中加入0.10mol/L酸性KCr O 溶液10mL时,恰好完全反应
2 2 7
①“步骤一”中加入过量铜粉的目的是_______。
②请补充完整步骤②中发生反应的离子反应方程式:_______。
______Fe2++_______ +_______=_______Fe3++_______Cr3++_______。
③实验测得黑木耳中铁元素的质量分数为_______。
3.(2021·浙江绍兴·校考模拟预测)NaCN属于剧毒化学品,应与酸类、氧化剂、食
用化学品分开存放。其阴离子 中各原子均满足8电子稳定结构,NaCN的电子式为
_______;强氧化剂NaClO会将 氧化,生成 、 和 等无毒无害物质,可用该反应处理含氰废水(破氰),该反应的离子方程式为_______。
4.(2022·陕西渭南·一模)元素化合物在化工生产和环境科学中有着重要的用途。
(1)向NH Al(SO ) 溶液中逐滴加入稀NaOH溶液至过量,反应的离子方程式依次为
4 4 2
____、____、____。
(2)自然界中Cr主要以+3价和+6价形式存在。 中的Cr能引起细胞的突变,可以
用亚硫酸钠在酸性条件下将 还原。写出该反应的离子方程式:____。
(3)常温下,氰化钠(NaCN)能与过氧化氢溶液反应生成一种酸式盐和一种能使湿润的红
色石蕊试纸变成蓝色的气体,大大降低其毒性。写出该反应的离子方程式:____。
(4)已知:CCl 与水不相溶且密度比水大,Cl 的CCl 溶液呈黄绿色,Br 的CCl 溶液呈
4 2 4 2 4
橙红色,且Br 易从水溶液中溶入CCl 中。Cl 既能氧化Br-,也能氧化Fe2+。
2 4 2
①取10mL0.1mol/LFeBr 溶液,向其中滴加几滴新制的氯水,振荡后溶液呈黄色。取
2
少量反应后的溶液加入KSCN溶液,溶液变为红色。另取少量反应后的溶液加入
CCl ,振荡后,下层为无色液体。以上实验结论表明还原性:Fe2+____Br- (填“>”或
4
“<”)。
②若在400mL0.1mol/LFeBr 溶液中通入标准状况下672mL的Cl,取少量反应后的溶
2 2
液加入CCl ,振荡后下层液体呈____色,写出该反应的离子方程式____。
4
5.(2022·上海青浦·统考二模)铋元素位于第六周期VA族,常用于治疗胃病的药物
中,也广泛用于合金制造、冶金工业、半导体工业、核工业中。
(5)铋酸钠(NaBiO)在酸性溶液中具有很强的氧化性,可用于测定钢铁试样中锰的含量。
3
完成并配平下列反应方程式,并用单线桥标出电子转移的方向和数目_______。
_______BiO +_______Mn+_______H+→_______Bi3++_______MnO +______
6.(2022·安徽淮北·统考一模)铬是人体必须的微量元素,在人体代谢中发挥着特殊
作用。回答下列问题:
(1)金属铬可以通过焦炭高温还原铬铁矿(FeCrO)制取,同时生成一种有毒的气体,该
2 4
反应的化学方程式为______。
(2)①取冶炼所得的金属铬溶解在盐酸中制取CrCl 溶液,其中混有FeCl 杂质,请完成
3 2
除杂方案:向溶液中加入足量NaOH溶液,过滤,向滤液中______,过滤,将固体溶
解在稀盐酸中(已知Cr(OH) 是两性氢氧化物)。
3
②由CrCl 溶液得到CrCl •6H O,除去其结晶水的操作是______。
3 3 2
(3)Cr3+在碱性条件下易被氧化成CrO ,写出向CrCl 溶液中加入氨水和过氧化氢发生
3
试卷第2页,共10页反应的离子方程式______。
(4)CrO 在酸性条件下可转化为Cr O ,Cr O 可以用来检验HO,原理是Cr O
2 2 2 2 2
+4H O+2H+ 2CrO(蓝色)+5H O。
2 2 5 2
①CrO 中铬元素为+6价,其中过氧键的数目为______。
5
②酸化重铬酸钾选用的酸为______(填标号)。
a.稀盐酸 b.稀硫酸 c.氢碘酸 d.磷酸
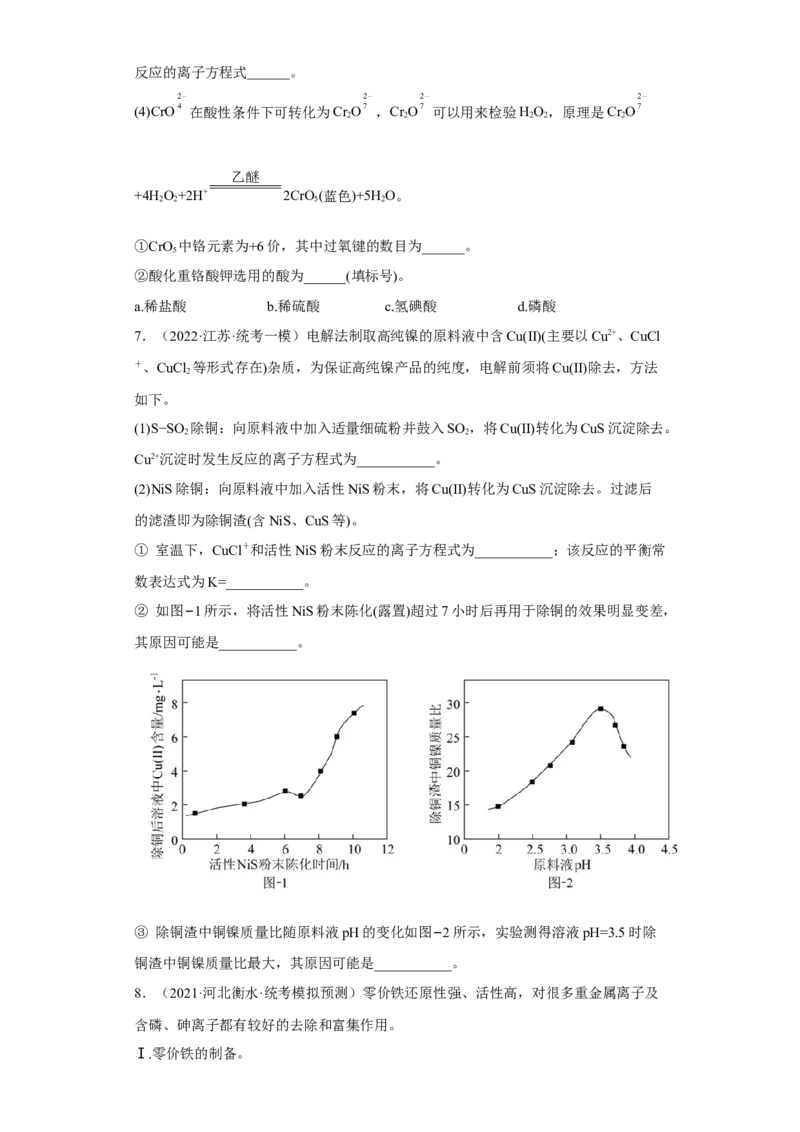
7.(2022·江苏·统考一模)电解法制取高纯镍的原料液中含Cu(II)(主要以Cu2+、CuCl
+、CuCl 等形式存在)杂质,为保证高纯镍产品的纯度,电解前须将Cu(II)除去,方法
2
如下。
(1)S−SO 除铜:向原料液中加入适量细硫粉并鼓入SO ,将Cu(II)转化为CuS沉淀除去。
2 2
Cu2+沉淀时发生反应的离子方程式为___________。
(2)NiS除铜:向原料液中加入活性NiS粉末,将Cu(II)转化为CuS沉淀除去。过滤后
的滤渣即为除铜渣(含NiS、CuS等)。
① 室温下,CuCl+和活性NiS粉末反应的离子方程式为___________;该反应的平衡常
数表达式为K=___________。
② 如图−1所示,将活性NiS粉末陈化(露置)超过7小时后再用于除铜的效果明显变差,
其原因可能是___________。
③ 除铜渣中铜镍质量比随原料液pH的变化如图−2所示,实验测得溶液pH=3.5时除
铜渣中铜镍质量比最大,其原因可能是___________。
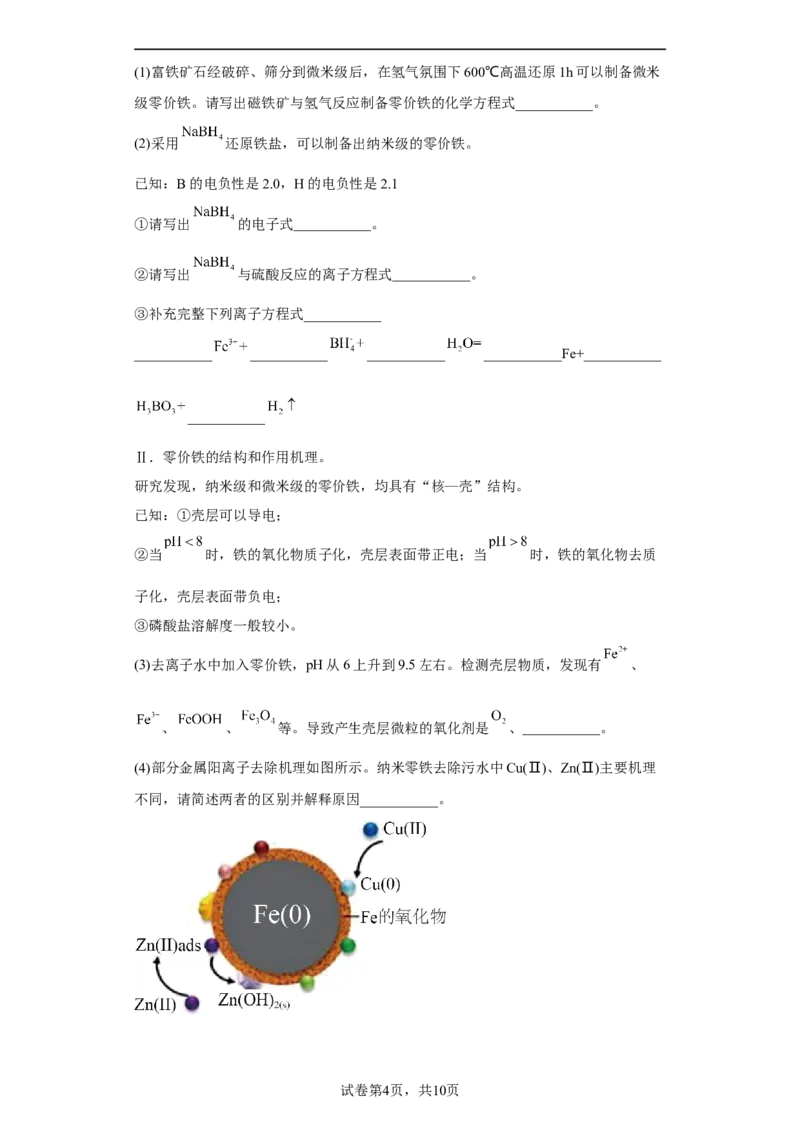
8.(2021·河北衡水·统考模拟预测)零价铁还原性强、活性高,对很多重金属离子及
含磷、砷离子都有较好的去除和富集作用。
Ⅰ.零价铁的制备。(1)富铁矿石经破碎、筛分到微米级后,在氢气氛围下600℃高温还原1h可以制备微米
级零价铁。请写出磁铁矿与氢气反应制备零价铁的化学方程式___________。
(2)采用 还原铁盐,可以制备出纳米级的零价铁。
已知:B的电负性是2.0,H的电负性是2.1
①请写出 的电子式___________。
②请写出 与硫酸反应的离子方程式___________。
③补充完整下列离子方程式___________
___________ ___________ ___________ ___________Fe+___________
___________
Ⅱ.零价铁的结构和作用机理。
研究发现,纳米级和微米级的零价铁,均具有“核—壳”结构。
已知:①壳层可以导电;
②当 时,铁的氧化物质子化,壳层表面带正电;当 时,铁的氧化物去质
子化,壳层表面带负电;
③磷酸盐溶解度一般较小。
(3)去离子水中加入零价铁,pH从6上升到9.5左右。检测壳层物质,发现有 、
、 、 等。导致产生壳层微粒的氧化剂是 、___________。
(4)部分金属阳离子去除机理如图所示。纳米零铁去除污水中Cu(Ⅱ)、Zn(Ⅱ)主要机理
不同,请简述两者的区别并解释原因___________。
试卷第4页,共10页(5)去除含磷( )微粒:
①控制pH___________8。
②通过形成___________(填化学式)进一步去除 。
(6)综上所述,零价铁去除重金属离子及含磷微粒的主要机理有___________。
9.(2021·河南信阳·统考一模)磷是重要的元素,能形成多种含氧酸和含氧酸盐。回
答下列问题:
Ⅰ. 亚磷酸(H PO )是二元酸,HPO 溶液存在电离平衡:HPO H+ + H PO 。亚磷
3 3 3 3 3 3 2
酸与足量NaOH溶液反应,生成水和NaHPO
2 3。
(1)写出亚磷酸钠(Na HPO )中磷的化合价___________。
2 3
(2)当亚磷酸与少量NaOH溶液反应的离子方程式为___________。
(3)亚磷酸具有强还原性,可使碘水褪色,该反应的化学方程式___________。
Ⅱ.已知:①次磷酸(H PO )是一种一元弱酸;
3 2
②常温下,电离平衡常数K(H PO )=5.9×10-2,K(CHCOOH)=1.8×10-5;
a 3 2 a 3
(4)下列说法正确的是___________。
A.次磷酸的电离方程式为:H
3
PO 2⇌H++H
2
PO
B.NaH PO 属于酸式盐
2 2
C.浓度均为0.1mol•L-1的次磷酸(H PO )与盐酸相比前者导电能力强
3 2
D.0.1mol•L-1NaH PO 溶液的pH比0.1mol•L-1CHCOONa溶液的pH小
2 2 3
(5)次磷酸钠NaH PO 具有强还原性,是一种很好的化学镀剂。如NaH PO 能将溶液中
2 2 2 2
的Ni2+还原为Ni,用于化学镀镍。酸性条件下镀镍溶液中发生如下反应:____
___________Ni2++___________H PO
2
+___________(___________)═___________Ni+___________H PO +_______(_________
2
__)请完成并配平上列的离子方程式。
Ⅲ.磷酸是三元弱酸(H PO )
3 4
(6)磷酸钙与焦炭、石英砂混合,在电炉中加热到1 500 ℃生成白磷,反应为:
2Ca (PO )+6SiO 6CaSiO +P O 10C+P O P+10CO
3 4 2 2 3 4 10 4 10 4
若反应生成31 g P,则反应过程中转移的电子数为___________(用N 表示阿伏加德罗
4 A常数的值)。
10.(2021·山东·模拟预测)(1)向盛有HO 溶液的试管中加入几滴酸化的FeCl 溶液,
2 2 2
溶液变成棕黄色,发生反应的离子方程式为___。
(2)双氧水浓度可在酸性条件下用KMnO 溶液测定,该反应的离子方程式为___。
4
(3)实验室中可用次氯酸钠溶液与氨反应制备联氨(N H),反应的化学方程式为___。
2 4
(4)在鼓泡反应器中通入含有SO 和NO的烟气,反应温度为323K,NaClO 溶液浓度为
2 2
5×10-3mol·L-1。反应一段时间后溶液中离子浓度的分析结果如表。
离子 SO SO NO
c/(mol·L-1) 8.35×10-4 6.87×10-6 1.5×10-4
离子 NO Cl-
c/(mol·L-1) 1.2×10-5 3.4×10-3
写出NaClO 溶液脱硝过程中主要反应的离子方程式___。
2
11.(2021·山东·模拟预测)(1)水中的溶解氧是水生生物生存不可缺少的条件。某课
外小组采用碘量法测定学校周边河水中的溶解氧。将水样与Mn(OH) 碱性悬浊液(含有
2
KI)混合,反应生成MnO(OH) ,实现氧的固定。“氧的固定”中发生反应的化学方程
2
式为___。
(2)+6价铬的化合物毒性较大,常用NaHSO 将废液中的 还原成Cr3+,反应的离
3
子方程式为___。
12.(2021·山东·模拟预测)碳酸锰主要用于制备软磁铁氧体,工业上以软锰矿(主要
成分为MnO )和黄铁矿(主要成分为FeS)为主要原料制备碳酸锰的一种工艺流程如图。
2 2
溶浸后的溶液中,阴离子只有 ,则生成 的离子方程式为___。
13.(2021·山东·模拟预测)实验室以锌灰(含ZnO、PbO、CuO、FeO、Fe O、SiO
2 3 2
等)为原料制备Zn(PO )·4H O的流程如图。
3 4 2 2
试卷第6页,共10页滴加KMnO 溶液后有MnO 生成,该反应的离子方程式为___。
4 2
14.(2021·山东·模拟预测)二氧化氯(ClO )是目前国际上公认的第四代高效、无毒的
2
消毒剂,是一种黄绿色的气体,易溶于水,沸点为11℃。
(1)用NH Cl、盐酸、NaClO(亚氯酸钠)为原料制备ClO 的流程如图所示:
4 2 2
①写出电解时发生反应的化学方程式:___。
②ClO 的消毒效率(以转移电子数目的多少为依据)是等物质的量的Cl 的___倍。
2 2
(2)产品中ClO 含量的测量:向锥形瓶中加入由适量碘化钾、3mL硫酸组成的混合溶液,
2
将上述反应过程中生成的一部分ClO 气体通入锥形瓶中充分反应。再加入几滴淀粉溶
2
液,用cmol/L硫代硫酸钠标准溶液滴定(I+2 =2I-+S ,通入的气体中不存在
2
能与I、 反应的成分),共用去VmL硫代硫酸钠溶液。
2
①请写出上述二氧化氯气体与碘化钾溶液反应的离子方程式:___。
②滴定终点的现象是___。
③测得通入ClO 的质量m(ClO )=___(用含c、V的代数式表示)。
2 2
15.(2017·云南玉溪·峨山彝族自治县第一中学校考模拟预测)(1)次氯酸盐是一些漂
白剂和消毒剂的有效成分。“84”消毒液的有效成分是次氯酸钠,制取该消毒液的化学
方程式为__。
(2)二氧化氯(ClO )是目前国际上公认的第四代高效、无毒的广谱消毒剂,它可由KClO
2 3
溶液在一定条件下与SO 反应制得。该反应的离子方程式为__。
2
(3)漂白剂亚氯酸钠(NaClO)在常温黑暗处可保存一年之久,但亚氯酸不稳定可分解,
2
反应的离子方程式为HClO→ClO ↑+H++Cl-+H O(未配平)。当1molHClO 发生分解反应
2 2 2 2
时,转移电子的物质的量是___mol。
(4)海水提溴过程中溴元素的变化如图所示:①过程Ⅰ,海水显碱性,调其pH<3.5后,再通入氯气。调海水pH可提高Cl 的利用率,
2
用平衡移动原理解释其原因:__。
②过程Ⅱ,用热空气将溴赶出,再用浓碳酸钠溶液吸收。完成并配平下列化学方程式:
___。
____Br +____Na CO=____NaBrO+____CO +____
2 2 3 3 2
(5)NaBrO 是一种分析试剂。向硫酸酸化的NaI溶液中逐滴加入NaBrO 溶液,当加入
3 3
2.6mol NaBrO 时,测得反应后溶液中溴和碘的存在形式及物质的量如表。则原溶液中
3
NaI的物质的量是___mol。
粒子 I 2 Br 2 IO
物质的量/mol 0.5 1.3 未知
16.(2021·浙江绍兴·统考二模)氧的常见氢化物有HO与HO。
2 2 2
(1)纯净HO 为浅蓝色粘稠液体,除相对分子质量的影响外,其沸点(423K)明显高于水
2 2
的原因为_______。
(2) H O 既有氧化性也有还原性,写出一个离子方程式其中HO 在反应中仅体现还原
2 2 2 2
性_______。
17.(2021·北京丰台·统考一模)锰广泛存在于自然界中,工业可用软锰矿(主要成分
是MnO )制备锰。
2
资料:①MnCO 难溶于水,可溶于稀酸。
3
②在Mn2+催化下,SO 在水溶液中被氧化成HSO 。
2 2 4
I.制备
(1)写出铝热法还原MnO 制备锰的化学方程式_______。
2
(2)工业上制备锰时,会产生大量废水和锰渣。锰渣煅烧会产生含高浓度SO 的烟气,
2
可用以下方法处理。
处理方法一:
①用软锰矿进行脱硫可生成硫酸锰,从而达到资源的循环使用。写出一定条件下利用
MnO 进行脱硫的化学方程式_______。
2
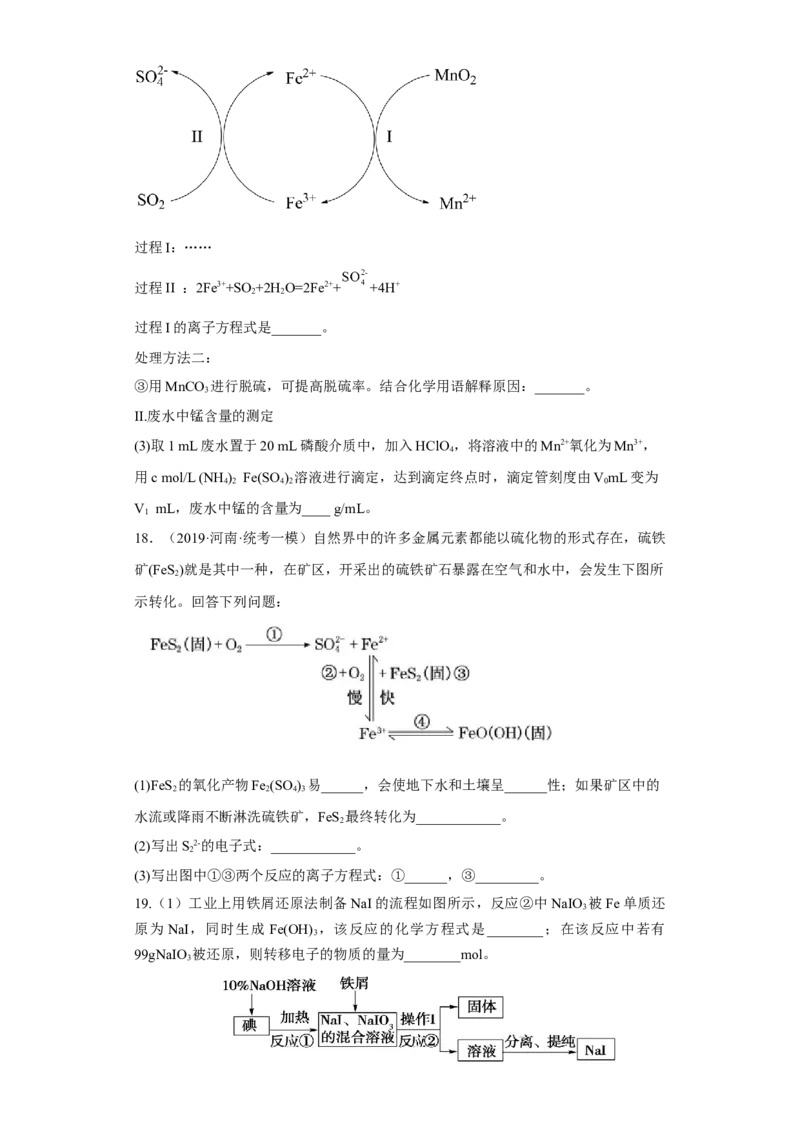
②研究表明,用Fe2+/Fe3+可强化脱硫效果,其过程如下所示:
试卷第8页,共10页过程I:……
过程II :2Fe3++SO+2H O=2Fe2++ +4H+
2 2
过程I的离子方程式是_______。
处理方法二:
③用MnCO 进行脱硫,可提高脱硫率。结合化学用语解释原因:_______。
3
II.废水中锰含量的测定
(3)取1 mL废水置于20 mL磷酸介质中,加入HClO,将溶液中的Mn2+氧化为Mn3+,
4
用c mol/L (NH) Fe(SO ) 溶液进行滴定,达到滴定终点时,滴定管刻度由VmL变为
4 2 4 2 0
V mL,废水中锰的含量为____ g/mL。
1
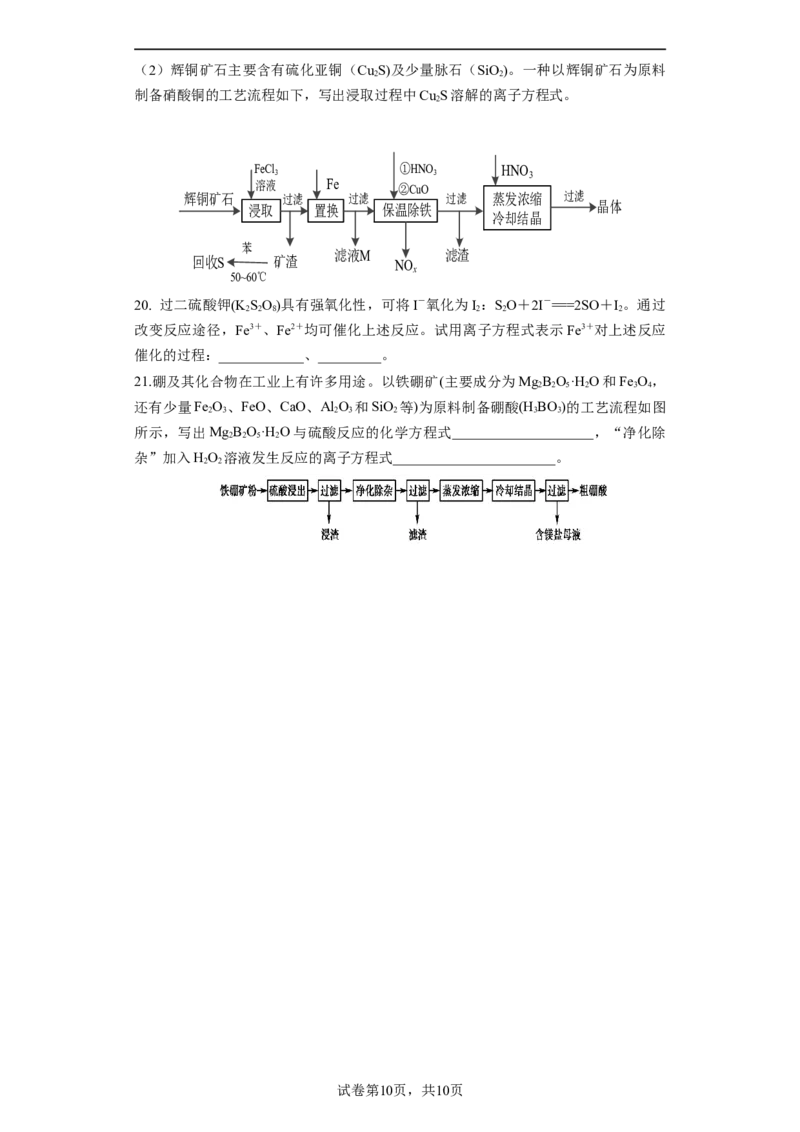
18.(2019·河南·统考一模)自然界中的许多金属元素都能以硫化物的形式存在,硫铁
矿(FeS )就是其中一种,在矿区,开采出的硫铁矿石暴露在空气和水中,会发生下图所
2
示转化。回答下列问题:
(1)FeS 的氧化产物Fe (SO ) 易______,会使地下水和土壤呈______性;如果矿区中的
2 2 4 3
水流或降雨不断淋洗硫铁矿,FeS 最终转化为____________。
2
(2)写出S2-的电子式:____________。
2
(3)写出图中①③两个反应的离子方程式:①______,③_________。
19.(1)工业上用铁屑还原法制备NaI的流程如图所示,反应②中NaIO 被Fe单质还
3
原为 NaI,同时生成 Fe(OH) ,该反应的化学方程式是________;在该反应中若有
3
99gNaIO 被还原,则转移电子的物质的量为________mol。
3(2)辉铜矿石主要含有硫化亚铜(Cu S)及少量脉石(SiO)。一种以辉铜矿石为原料
2 2
制备硝酸铜的工艺流程如下,写出浸取过程中Cu S溶解的离子方程式。
2
FeCl ①HNO HNO
3 3 3
溶液 Fe ②CuO
辉铜矿石 过滤 过滤 过滤 蒸发浓缩 过滤
浸取 置换 保温除铁 晶体
冷却结晶
苯
滤液M 滤渣
回收S 矿渣 NO
x
50~60℃
20. 过二硫酸钾(K SO)具有强氧化性,可将I-氧化为I :SO+2I-===2SO+I 。通过
2 2 8 2 2 2
改变反应途径,Fe3+、Fe2+均可催化上述反应。试用离子方程式表示Fe3+对上述反应
催化的过程:____________、_________。
21.硼及其化合物在工业上有许多用途。以铁硼矿(主要成分为MgB O·H O和Fe O ,
2 2 5 2 3 4
还有少量Fe O 、FeO、CaO、Al O 和SiO 等)为原料制备硼酸(H BO)的工艺流程如图
2 3 2 3 2 3 3
所示,写出MgB O·H O与硫酸反应的化学方程式____________________,“净化除
2 2 5 2
杂”加入HO 溶液发生反应的离子方程式_______________________。
2 2
试卷第10页,共10页