文档内容
热化学、化学反应速率与平衡的综合分析
1.题型特点
这类试题往往以化学反应速率、化学平衡知识为主题,借助图像、图表的手段,综合考查关联知识,
关联知识主要有:
(1)ΔH符号的判断、热化学方程式的书写、应用盖斯定律计算ΔH。
(2)化学反应速率的计算与比较,外因对化学反应速率的影响(浓度、压强、温度、催化剂)。
(3)平衡常数、转化率的计算,温度对平衡常数的影响;化学平衡状态的判断,用化学平衡的影响因素
进行分析和解释。
(4)在多层次曲线图中反映化学反应速率、化学平衡与温度、压强、浓度的关系。
2.解答化学平衡移动问题的步骤
(1)正确分析反应特点:包括反应物、生成物的状态,气体体积变化,反应的热效应。
(2)明确外界反应条件:恒温恒容、恒温恒压、反应温度是否变化、反应物投料比是否变化。
(3)结合图像或K与Q的关系、平衡移动原理等,判断平衡移动的方向或结果。
3.分析图表与作图时应注意的问题
(1)仔细分析并准确画出曲线的最高点、最低点、拐点和平衡点。
(2)找准纵坐标与横坐标的对应数据。
(3)描绘曲线时注意点与点之间的连接关系。
(4)分析表格数据时,找出数据大小的变化规律。
4.解答有关平衡常数的计算
(1)结合题意,运用“三段式”,分析计算、确定各物理量的变化。
(2)多重平衡体系的计算用好连续计算法(分设变量)、守恒法两种方法。
(3)多重平衡体系达到整体综合平衡后,每种平衡组分都只能有一个平衡浓度。
1.(2024·湖北,17)用BaCO 和焦炭为原料,经反应Ⅰ、Ⅱ得到BaC ,再制备乙炔是我国科研人员提出
3 2
的绿色环保新路线。
反应Ⅰ:BaCO (s)+C(s) BaO(s)+2CO(g)
3
反应Ⅱ:BaO(s)+3C(s) BaC (s)+CO(g)
2
回答下列问题:
(1)写出BaC 与水反应的化学方程式 。
2
p
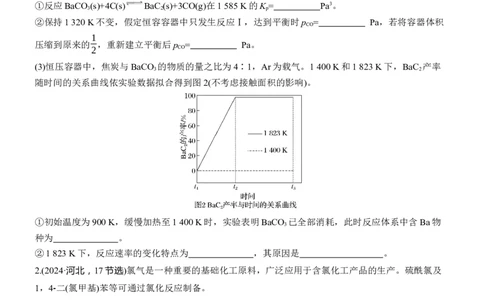
(2)已知K =(p )n、K=( CO )n(n是CO的化学计量系数)。反应Ⅰ、Ⅱ的lg K与温度的关系曲线见图
p CO 105Pa
1。①反应BaCO (s)+4C(s) BaC (s)+3CO(g)在1 585 K的K = Pa3。
3 2 p
②保持1 320 K不变,假定恒容容器中只发生反应Ⅰ,达到平衡时p = Pa,若将容器体积
CO
1
压缩到原来的 ,重新建立平衡后p = Pa。
2 CO
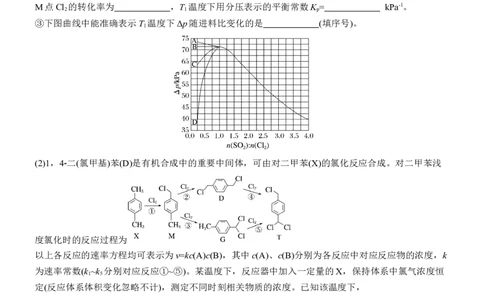
(3)恒压容器中,焦炭与BaCO 的物质的量之比为4∶1,Ar为载气。1 400 K和1 823 K下,BaC 产率
3 2
随时间的关系曲线依实验数据拟合得到图2(不考虑接触面积的影响)。
①初始温度为900 K,缓慢加热至1 400 K时,实验表明BaCO 已全部消耗,此时反应体系中含Ba物
3
种为 。
②1 823 K下,反应速率的变化特点为 ,其原因是 。
2.(2024·河北,17节选)氯气是一种重要的基础化工原料,广泛应用于含氯化工产品的生产。硫酰氯及
1,4⁃ 二(氯甲基)苯等可通过氯化反应制备。
(1)硫酰氯常用作氯化剂和氯磺化剂,工业上制备原理如下:SO (g)+Cl (g) SO Cl (g) ΔH=-67.59
2 2 2 2
kJ·mol-1。
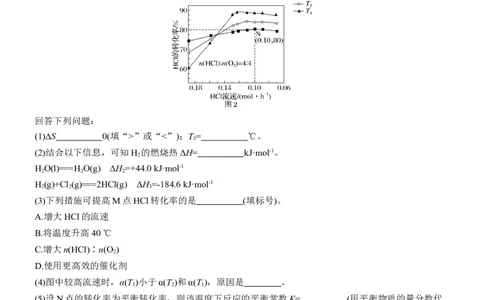
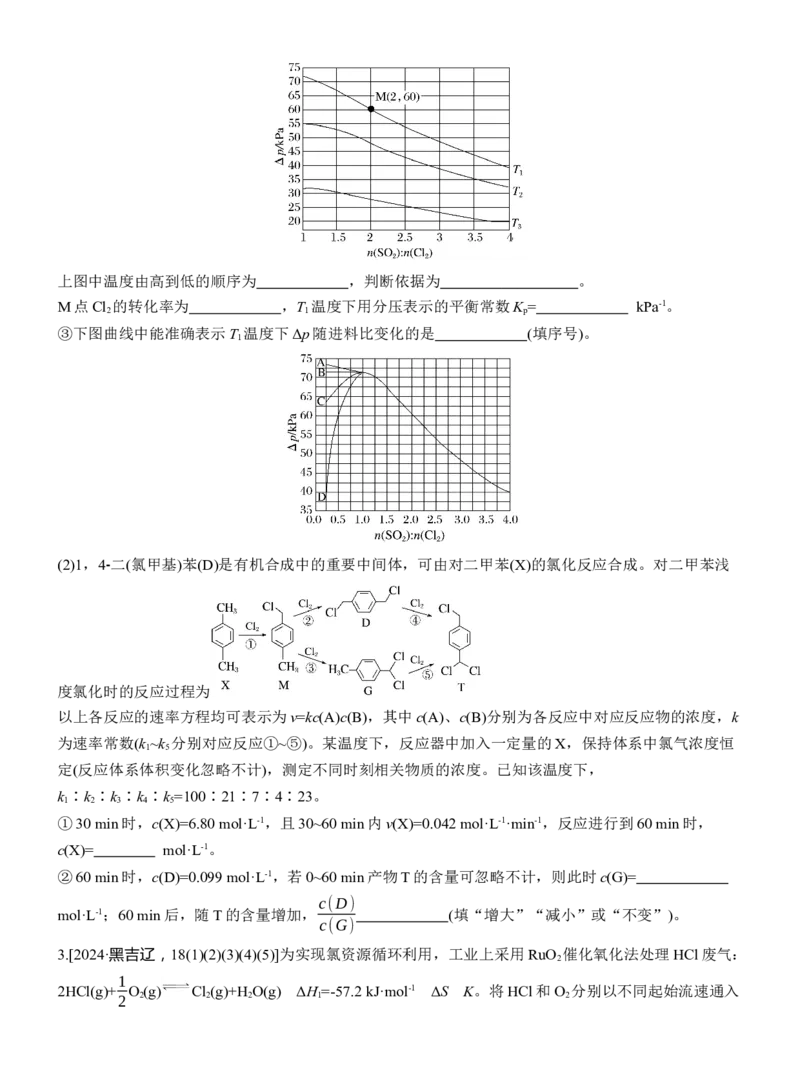
②恒容密闭容器中按不同进料比充入SO (g)和Cl (g),测定T 、T 、T 温度下体系达平衡时的
2 2 1 2 3
Δp(Δp=p -p,p 为体系初始压强,p =240 kPa,p为体系平衡压强),结果如图。
0 0 0上图中温度由高到低的顺序为 ,判断依据为 。
M点Cl 的转化率为 ,T 温度下用分压表示的平衡常数K = kPa-1。
2 1 p
③下图曲线中能准确表示T 温度下Δp随进料比变化的是 (填序号)。
1
(2)1,4⁃ 二(氯甲基)苯(D)是有机合成中的重要中间体,可由对二甲苯(X)的氯化反应合成。对二甲苯浅
度氯化时的反应过程为
以上各反应的速率方程均可表示为v=kc(A)c(B),其中c(A)、c(B)分别为各反应中对应反应物的浓度,k
为速率常数(k ~k 分别对应反应①~⑤)。某温度下,反应器中加入一定量的X,保持体系中氯气浓度恒
1 5
定(反应体系体积变化忽略不计),测定不同时刻相关物质的浓度。已知该温度下,
k ∶k ∶k ∶k ∶k =100∶21∶7∶4∶23。
1 2 3 4 5
①30 min时,c(X)=6.80 mol·L-1,且30~60 min内v(X)=0.042 mol·L-1·min-1,反应进行到60 min时,
c(X)= mol·L-1。
②60 min时,c(D)=0.099 mol·L-1,若0~60 min产物T的含量可忽略不计,则此时c(G)=
c(D)
mol·L-1;60 min后,随T的含量增加, (填“增大”“减小”或“不变”)。
c(G)
3.[2024·黑吉辽,18(1)(2)(3)(4)(5)]为实现氯资源循环利用,工业上采用RuO 催化氧化法处理HCl废气:
2
1
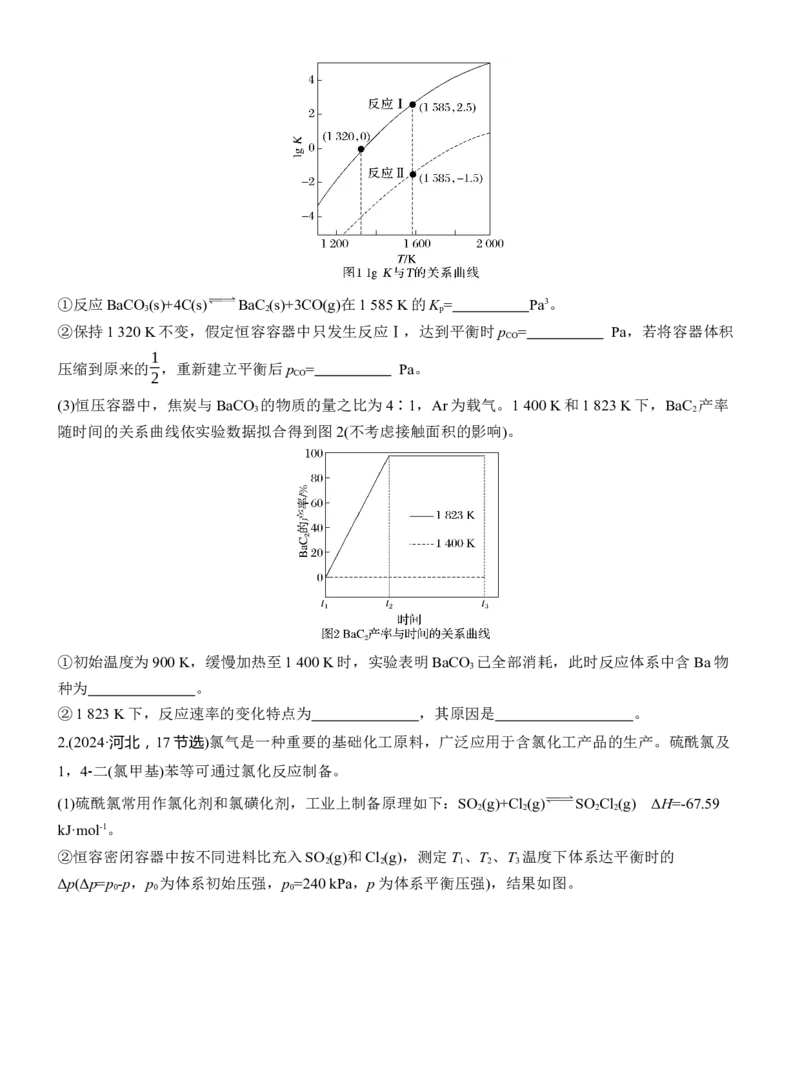
2HCl(g)+ O (g) Cl (g)+H O(g) ΔH =-57.2 kJ·mol-1 ΔS K。将HCl和O 分别以不同起始流速通入
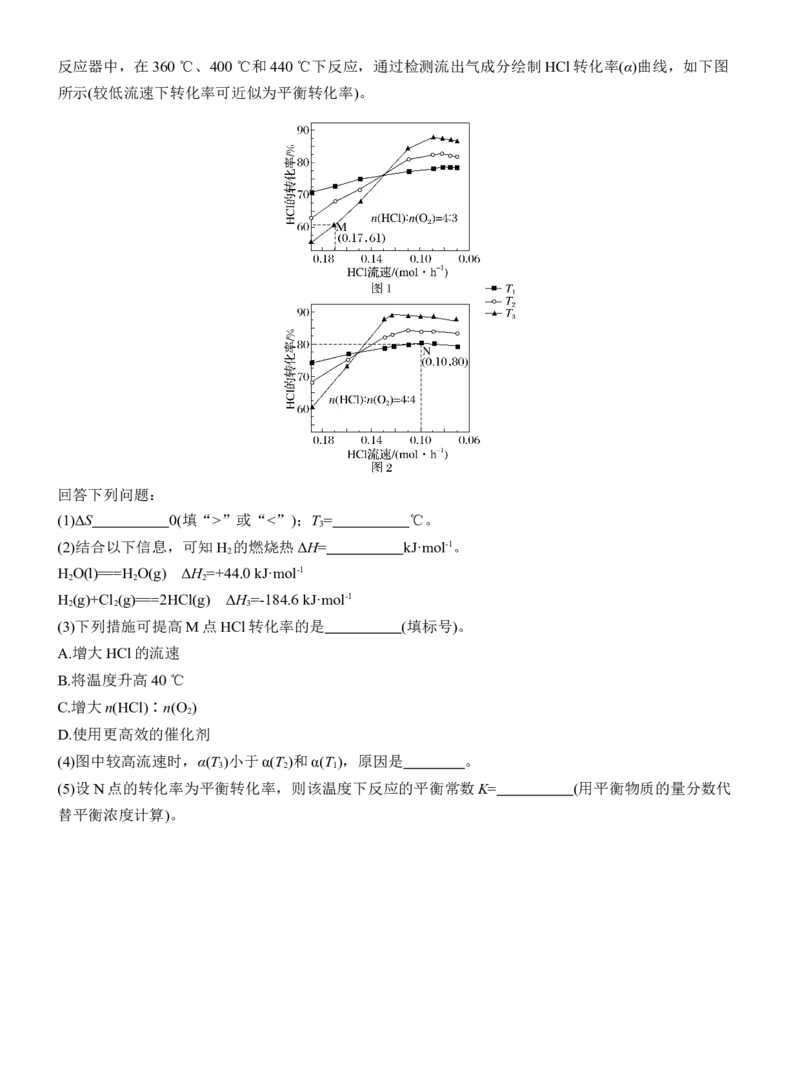
2 2 2 2 1 2反应器中,在360 ℃、400 ℃和440 ℃下反应,通过检测流出气成分绘制HCl转化率(α)曲线,如下图
所示(较低流速下转化率可近似为平衡转化率)。
回答下列问题:
(1)ΔS 0(填“>”或“<”);T = ℃。
3
(2)结合以下信息,可知H 的燃烧热ΔH= kJ·mol-1。
2
H O(l)===H O(g) ΔH =+44.0 kJ·mol-1
2 2 2
H (g)+Cl (g)===2HCl(g) ΔH =-184.6 kJ·mol-1
2 2 3
(3)下列措施可提高M点HCl转化率的是 (填标号)。
A.增大HCl的流速
B.将温度升高40 ℃
C.增大n(HCl)∶n(O )
2
D.使用更高效的催化剂
(4)图中较高流速时,α(T )小于α(T )和α(T ),原因是 。
3 2 1
(5)设N点的转化率为平衡转化率,则该温度下反应的平衡常数K= (用平衡物质的量分数代
替平衡浓度计算)。答案精析
精练高考真题
1.(1)BaC +2H O Ba(OH) +HC≡CH↑ (2)①1016 ②105 105 (3)①BaO ②速率不变至BaC 产率接近
2 2 2 2
p
100% 容器中只发生反应Ⅱ,反应条件恒温1 823 K、恒压,且该反应只有CO为气态,据K= CO 可知,
105Pa
CO的压强为定值,所以化学反应速率不变
解析 (1)Ba、Ca同主族,BaC 与CaC 结构相似,BaC 与水反应和CaC 与水反应相似,其反应的化学方
2 2 2 2
程式为BaC +2H O Ba(OH) +HC≡CH↑。(2)①反应Ⅰ+反应Ⅱ得BaCO (s)+4C(s) BaC (s)+3CO(g),则
2 2 2 3 2
p p
CO CO
其平衡常数K=K ×K =( )3;由图1可知,1 585 K时K =102.5,K =10-1.5,即( )3=102.5×10-
Ⅰ Ⅱ 105Pa Ⅰ Ⅱ 105Pa
1.5=10,所以p3 =10×(105 Pa)3=1016 Pa3,则K =p3 =1016 Pa3。②由图1可知,1 320 K时反应Ⅰ的
CO p CO
p 1
K =100=1,即K =( CO )2=1,所以p2 =(105 Pa)2,即p =105 Pa;若将容器体积压缩到原来的 ,由于
Ⅰ Ⅰ 105Pa CO CO 2
温度不变、平衡常数不变,重新建立平衡后p 不变,即p =105 Pa。(3)①由图2可知,1 400 K时,BaC
CO CO 2
的产率为0,即没有BaC 生成,又实验表明BaCO 已全部消耗,此时反应体系中含Ba物种只有BaO。
2 3
2.(1)②T >T >T 该反应是放热的、气体分子数减小的反应,恒容条件下,反应正向进行时,容器内压强
3 2 1
减小,从T 到T 平衡时Δp增大,说明反应正向进行程度逐渐增大,对应温度逐渐降低 75% 0.03 ③D
3 1
(2)①5.54 ②0.033 增大
解析 (1)②该反应的正反应为气体体积减小的反应,反应正向进行程度越大,Δp越大。由图可知,从T
3
到T ,Δp增大,说明反应正向进行程度逐渐增大,已知正反应为放热反应,则温度由T 到T 逐渐降低,
1 3 1
即T >T >T 。由图中M点可知,进料比为n(SO )∶n(Cl )=2,平衡时Δp=60 kPa,已知恒温恒容条件下,容
3 2 1 2 2
器内气体物质的量之比等于压强之比,可据此列出三段式:
SO (g)+Cl (g) SO Cl (g) Δp
2 2 2 2
起始压强/kPa 160 80
转化压强/kPa 60 60 60 60
平衡压强/kPa 100 20 60
60 kPa p(SO Cl ) 60 kPa
2 2
可计算得α(Cl )= ×100%=75%,K = = =0.03 kPa-1。③根据
2 80 kPa p p(SO )·p(Cl ) 100 kPa×20 kPa
2 2
“等效平衡”原理,该反应中SO 和Cl 的化学计量数之比为1∶1,则SO 和Cl 的进料比互为倒数(如2与
2 2 2 2
Δc(X)
0.5)时,Δp相等。(2)①根据v(X)= ,60 min时,c(X)=6.80 mol·L-1-v(X)·Δt=6.80 mol·L-1-0.042
Δt
v (D) k ·c(M) k
mol·L-1·min-1×30 min=5.54 mol·L-1。②由题给反应速率方程推知 生成 = 2 = 2 =3,又D、G的初
v (G) k ·c(M) k
生成 3 3v(D) Δc(D) 1
始浓度均为0,则 = ,则Δc(G)= ×Δc(D)=0.033 mol·L-1,即此时c(G)=0.033 mol·L-1。60 min
v(G) Δc(G) 3
v (D) k ·c(D) 4×0.099
消耗 4
后,D和G转化为T的速率比为 = = ,结合二者的生成速率可知,D生成的快
v (G) k ·c(G) 23×0.033
消耗 5
c(D)
而消耗的慢,G生成慢而消耗的快,则 增大。
c(G)
3.(1)< 360 (2)-285.8 (3)BD (4)反应未达平衡时,流速过快,反应物分子来不及在催化剂表面接触而
发生反应,导致转化率下降,同时,T 温度低,反应速率低,故单位时间内氯化氢的转化率低 (5)6
3
1
解析 (1)2HCl(g)+ O (g) Cl (g)+H O(g)反应后气体分子数目减小,该反应ΔS<0;该反应为放热反应,
2 2 2 2
由于在流速较低时的转化率视为平衡转化率,在流速低的时候,温度越高,HCl的转化率越小,由图像可
1
知,T 代表的温度为440 ℃,T 为360 ℃。(2)根据盖斯定律可得反应H (g)+ O (g)===H O(l)的
1 3 2 2 2 2
ΔH=ΔH +ΔH -ΔH =-57.2 kJ·mol-1-184.6 kJ·mol-1-44.0 kJ·mol-1=-285.8 kJ·mol-1,即氢气的燃烧热ΔH=-285.8
1 3 2
kJ·mol-1。(3)增大HCl的流速,由图像可知,HCl的转化率减小,A不符合题意;M点对应的温度为360
℃,由图像可知,温度升高40 ℃为400 ℃时,HCl的转化率增大,B符合题意;增大n(HCl)∶n(O ),HCl
2
的转化率减小,C不符合题意;M点时,反应未达到平衡,使用高效催化剂,可以增加该温度下的反应速
率,使单位时间内HCl的转化率增加,D符合题意。(5)由图像可知,N点HCl的平衡转化率为80%,设起
始n(HCl)=n(O )=4 mol,可列出三段式:
2
1
2HCl(g)+ O (g) Cl (g)+H O(g)
2 2 2 2
起始量/mol 4 4 0 0
变化量/mol 3.2 0.8 1.6 1.6
平衡量/mol 0.8 3.2 1.6 1.6
1.6 1.6
×
7.2 7.2
则K= =6。
1
0.8 3.2
( ) 2×( )2
7.2 7.2