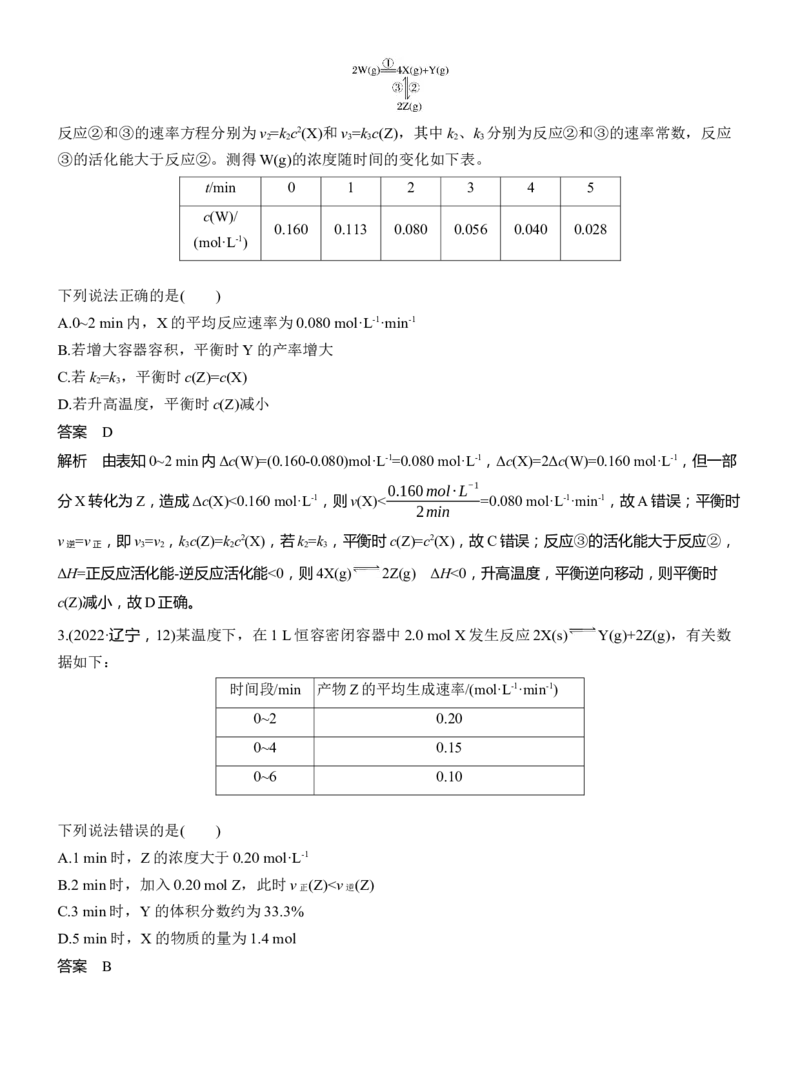文档内容
化学反应速率与平衡图像、图表分析
1.化学平衡与平衡转化率
(1)转化率和平衡转化率
转化率有未达到平衡的转化率和平衡转化率,在审题的时候一定要注意转化率是否为平衡转化率。
(2)转化率与温度的关系
可逆反应
的焓变ΔH
升高温度
吸热反应,
ΔH>0
未达到平衡的转化率增大
平衡转化率增大
放热反应,
ΔH<0
未达到平衡的转化率增大
平衡转化率减小
(3)增大反应物的浓度与平衡转化率的关系(其中A、B、C均为气体)
可逆
反应
改变
条件
平衡移
动方向
反应物平
衡转化率
备注
A+B
C
增大A
的浓度正向
移动
α(A)减小
α(B)增大
-
A
B+C
增大A
的浓度
正向
移动
α(A)
减小
反应物平
衡转化率
实际是考
虑压强的
影响
2A
B+C
增大A
的浓度
正向
移动
α(A)
不变
3A
B+C
增大A
的浓度
正向
移动
α(A)
增大(4)如果两气体物质的投料比按照化学计量数投料,那么无论是否达到化学平衡,两者的转化率一直相
等。
2.化学平衡常数、平衡移动方向与反应速率的关系
aA(g)+bB(g) cC(g)+dD(g)
cc (C)·cd (D) cc (C)·cd (D)
K= Q=
ca (A)·cb (B) ca (A)·cb (B)
平衡时浓度 某时刻浓度
{
=Q,反应处于化学平衡状态,v =v
正 逆
K Q,平衡向正反应方向移动,v >v
正 逆
3.化学反应速率与平衡图像分析思路
例1 (2023·河南安阳一中模拟预测) (环戊二烯)容易发生聚合反应生成二聚体,该反应为可逆反
应。不同温度下,溶液中环戊二烯浓度与反应时间的关系如图所示,下列说法不正确的是( )
A.T v (Z),B
正 逆
错误;反应生成的Y与Z的物质的量之比恒等于1∶2,反应体系中只有Y和Z为气体,同温同压下,体
V(Y) 1
积之比等于物质的量之比, = ,故Y的体积分数始终约为33.3%,C正确;由B项分析可知5 min
V(Z) 2
时反应处于平衡状态,此时生成的Z为0.6 mol,则X的转化量为0.6 mol,初始X的物质的量为2.0 mol,
剩余X的物质的量为1.4 mol,D正确。
考向二 化学反应速率与平衡图像分析
4.(2024·黑吉辽,10)异山梨醇是一种由生物质制备的高附加值化学品,150 ℃时其制备过程及相关物质
浓度随时间变化如图所示,15 h后异山梨醇浓度不再变化。下列说法错误的是( )
A.3 h时,反应②正、逆反应速率相等
B.该温度下的平衡常数:①>②
C.0~3 h平均速率(异山梨醇)=0.014 mol·kg-1·h-1
D.反应②加入催化剂不改变其平衡转化率
答案 A
解析 由图可知,3 h后异山梨醇浓度继续增大,15 h后异山梨醇浓度才不再变化,所以3 h时,反应②未
达到平衡状态,即正、逆反应速率不相等,故A错误;图像显示该温度下,15 h后所有物质浓度都不再变
化,且此时山梨醇转化完全,即反应充分,而1,4⁃失水山梨醇仍有剩余,即反应②正向进行程度小于反
应①,所以该温度下的平衡常数:①>②,故B正确;在0~3 h内异山梨醇的浓度变化量为0.042 mol·kg-1,0.042mol·kg-1
所以平均速率(异山梨醇)= =0.014 mol·kg-1·h-1,故C正确;催化剂只能改变化学反应速率,
3 h
不能改变物质平衡转化率,故D正确。
5.(2024·湖南,14)恒压下,向某密闭容器中充入一定量的CH OH(g)和CO(g),发生如下反应:
3
主反应:CH OH(g)+CO(g)===CH COOH(g) ΔH
3 3 1
副反应:CH OH(g)+CH COOH(g)===CH COOCH (g)+H O(g) ΔH
3 3 3 3 2 2
在不同温度下,反应达到平衡时,测得两种含碳产物的分布分数δ[δ(CH COOH)=
3
n(CH COOH)
3 ]随投料比x(物质的量之比)的变化关系如图所示,下列说法正确的
n(CH COOH)+n(CH COOCH )
3 3 3
是( )
n(CH OH)
A.投料比x代表 3
n(CO)
B.曲线c代表乙酸的分布分数
C.ΔH <0,ΔH >0
1 2
D.L、M、N三点的平衡常数:K(L)=K(M)>K(N)
答案 D
解析 图中曲线表示的是两种含碳产物的分布分数即δ(CH COOH)、δ(CH COOCH ),结合主、副反应可
3 3 3
n(CO)
知,x代表 ,曲线a或曲线b表示CH COOH分布分数,曲线c或曲线d表示CH COOCH 分
n(CH OH) 3 3 3
3
n(CO)
布分数,故A、B错误;曲线a或曲线b表示δ(CH COOH),由图像可知,当 相同时,
3 n(CH OH)
3
T >T ,T 时δ(CH COOH)大于T 时,说明升高温度主反应的平衡正向移动,故ΔH >0;同理,T 时
2 1 2 3 1 1 1
δ(CH COOCH )大于T 时,说明升高温度副反应的平衡逆向移动,故ΔH <0,C错误;L、M、N三点对应
3 3 2 2
副反应ΔH <0,且T >T =T ,升高温度平衡逆向移动,故K(L)=K(M)>K(N),D正确。
2 N M L
6.(2023·辽宁,12)一定条件下,酸性KMnO 溶液与H C O 发生反应,Mn(Ⅱ)起催化作用,过程中不同
4 2 2 4
价态含Mn粒子的浓度随时间变化如图所示。下列说法正确的是( )A.Mn(Ⅲ)不能氧化H C O
2 2 4
B.随着反应物浓度的减小,反应速率逐渐减小
C.该条件下,Mn(Ⅱ)和Mn(Ⅶ)不能大量共存
D.总反应为:2MnO-
+5C
O2-
+16H+===2Mn2++10CO ↑+8H O
4 2 4 2 2
答案 C
解析 由图像可知,随着时间的推移Mn(Ⅲ)的浓度先增大后减小,说明开始反应生成Mn(Ⅲ),后Mn(Ⅲ)
被消耗生成Mn(Ⅱ),Mn(Ⅲ)能氧化H C O ,A项错误;随着反应物浓度的减小,到大约13 min时开始生
2 2 4
成Mn(Ⅱ),Mn(Ⅱ)对反应起催化作用,13 min后反应速率会增大,B项错误;由图像可知,Mn(Ⅶ)的浓度
为0后才开始生成Mn(Ⅱ),该条件下Mn(Ⅱ)和Mn(Ⅶ)不能大量共存,C项正确;H C O 为弱酸,在离子
2 2 4
方程式中不拆成离子,总反应为2MnO-
+5H C O +6H+===2Mn2++10CO ↑+8H O,D项错误。
4 2 2 4 2 2
7.(2023·湖南,13)向一恒容密闭容器中加入1 mol CH 和一定量的H O,发生反应:CH (g)+H O(g)
4 2 4 2
n(CH )
CO(g)+3H (g)。CH 的平衡转化率按不同投料比x[x= 4 ]随温度的变化曲线如图所示。下列说法错
2 4 n(H O)
2
误的是( )
A.x v ,故B错误;由图像可知,x一定时,温度升高CH 的平衡转化
b正 c正 4
率增大,说明正反应为吸热反应,温度升高平衡正向移动,K增大,温度相同,K不变,则点a、b、c对应的平衡常数:K0
B.气体的总物质的量:n0.75,即平衡常数K>12,故C错误;根据图像可知,甲容
2
器达到平衡的时间短,温度高,所以达到平衡的速率相对乙容器的快,即v >v ,故D错误。
a正 b正
题型突破练 [分值:50 分]
(选择题1~10题,每小题5分,共50分)
1.(2024·安徽皖江名校联盟二模)汽车尾气的排放会对环境造成污染。利用高效催化剂处理汽车尾气中的NO
与CO的反应为2NO(g)+2CO(g) N (g)+2CO (g) ΔH<0。一定温度下,在1 L恒容密闭容器中加入1
2 2
mol CO和1 mol NO发生上述反应,部分物质的体积分数(φ)随时间(t)的变化如图所示。下列说法正确的是(
)A.曲线Ⅱ表示的是φ(CO )随时间的变化
2
B.t min时,反应达到化学平衡状态
2
C.增大压强,该平衡右移,平衡常数增大
0.8
D.0~t min内的平均反应速率为v(NO)= mol·L-1·min-1
4 t
4
答案 D
解析 因为初始投料中n(CO)与n(NO)之比等于化学方程式中对应的化学计量数之比,反应至t min时达平
4
衡,φ(CO)=φ(NO)=0.125,其中一生成物的体积分数为0.25,另一生成物的体积分数为0.5,按生成物的化
学计量数可知,平衡时φ(N )=0.25、φ(CO )=0.5,故曲线Ⅱ表示的是φ(N )随时间的变化,A项错误;t min
2 2 2 2
后,φ还在变化,反应没有达到化学平衡状态,B项错误;增大压强,该平衡右移,平衡常数不变,C项
0.8
错误;计算可得0~t min内,Δn(NO)=0.8 mol,故v(NO)= mol·L-1·min-1,D项正确。
4 t
4
2.(2021·浙江1月选考,19)取50 mL过氧化氢水溶液,在少量I-存在下分解:2H O ===2H O+O ↑。在一定
2 2 2 2
温度下,测得O 的放出量,转换成H O 浓度(c)如下表:
2 2 2
t/min 0 20 40 60 80
c/(mol·L-1) 0.80 0.40 0.20 0.10 0.050
下列说法不正确的是( )
A.反应20 min时,测得O 体积为224 mL(标准状况)
2
B.20~40 min,消耗H O 的平均速率为0.010 mol·L-1·min-1
2 2
C.第30 min时的瞬时速率小于第50 min时的瞬时速率
D.H O 分解酶或Fe O 代替I-也可以催化H O 分解
2 2 2 3 2 2
答案 C
解析 反应的H O 的物质的量为0.05 L×(0.80 mol·L-1-0.40 mol·L-1)=0.02 mol,根据2H O ===2H O+O ↑,
2 2 2 2 2 2
可知生成的O 为0.01 mol,在标准状况下是224 mL,A正确;20~40 min,消耗H O 的平均速率为
2 2 2
0.40mol·L-1-0.20 mol·L-1
=0.010 mol·L-1·min-1,B正确;在相同条件下,浓度越大,反应速率越大,第
20min
30 min时H O 的浓度大于第50 min时H O 的浓度,因此第30 min时的瞬时速率大于第50 min时的瞬时速
2 2 2 2
率,C错误;H O 在分解酶或Fe O 作催化剂的条件下也可以分解,D正确。
2 2 2 33.(2024·南宁高三第一次适应性测试)一定温度下向容器中加入M发生反应如下:①M―→P,②M―→Q,
③P Q。反应体系中M、P、Q的浓度随时间t的变化曲线如图所示。下列说法正确的是( )
A.反应①的活化能大于反应②
B.t s时,反应③已达平衡
1
C.该温度下,反应③的平衡常数小于1
D.t s时,c(Q)=c -c(P)
2 0
答案 D
解析 由图可知,M同时生成P和Q时,生成物中P多Q少,说明反应①容易发生,活化能较反应②的低,
A错误;t s后,P浓度在减少,Q浓度在增加,反应③并未达到平衡,B错误;反应③的平衡常数K=
1
c(Q)
,由图知,平衡时,Q的浓度大于P的浓度,故K>1,C错误;t s时,根据反应可知,M完全转化
c(P) 2
为P和Q,P转化为Q,所以c(Q)=c -c(P),D正确。
0
4.(2024·长春模拟)一定条件下,反应H (g)+Br (g) 2HBr(g)的速率方程为v=kcα(H )·cβ(Br )·cγ(HBr),某温
2 2 2 2
度下,该反应在不同浓度下的反应速率如下表:
c(H)/ c(Br )/ c(HBr)/
2 2
反应速率
(mol·L-1) (mol·L-1) (mol·L-1)
0.1 0.1 2 v
0.1 0.4 2 8v
0.2 0.4 2 16v
0.4 0.1 4 2v
0.2 0.1 c 4v
根据表中的测定结果,下列结论错误的是( )
A.α的值为1
B.表中c的值为2
C.反应体系的三种物质中,Br (g)的浓度对反应速率影响最大
2
D.在反应体系中保持其他物质浓度不变,增大HBr(g)浓度,会使反应速率降低
答案 B
解析 将表中数据代入速率方程可得到①v=k×0.1α×0.1β×2γ,②8v=k×0.1α×0.4β×2γ,③16v=k×0.2α×0.4β×2γ,
3
④2v=k×0.4α×0.1β×4γ,⑤4v=k×0.2α×0.1β×cγ,解得α=1,β= ,γ=-1,c=1,A正确,B错误;由于α=1,β=
23
,γ=-1,故反应体系的三种物质中,Br (g)的浓度对反应速率影响最大,C正确;在反应体系中保持其他
2 2
物质浓度不变,增大HBr(g)浓度,由于γ=-1,cγ(HBr)减小,会使反应速率降低,D正确。
5.(2024·江西赣州二模)甲烷水蒸气重整制合成气[CH (g)+H O(g) CO(g)+3H (g) ΔH]是利用甲烷资源的
4 2 2
途径之一,其他条件相同时,在不同催化剂(Ⅰ、Ⅱ、Ⅲ)作用下,反应相同时间后,CH 的转化率随反应
4
温度的变化如图所示。下列说法错误的是( )
A.该反应ΔH>0
B.平衡常数:K=K 0,故A正确;
平衡常数只受温度影响,温度相同,对于同一反应的平衡常数也相同,该反应的正反应为吸热反应,升高
温度K增大,则K=K Ⅱ>Ⅲ,故C
a b c
错误;增大压强,平衡向气体分子数减小的方向移动,即平衡逆向移动,说明v 增大倍数小于v 增大倍
正 逆
数,故D正确。
6.(2024·安徽示范高中皖北协作区高三联考)一定条件下可合成乙烯:6H (g)+2CO (g) CH ==CH (g)
2 2 2 2
+4H O(g),已知温度对CO 的平衡转化率和催化剂催化效率的影响如图所示,下列说法正确的是( )
2 2
A.温度不变,若增大压强,v >v ,平衡常数增大
正 逆
B.升高温度,平衡向逆反应方向移动,催化剂的催化效率降低
C.温度不变,若恒压下向平衡体系中充入惰性气体,平衡不移动
D.若投料比n(H )∶n(CO )=3∶1,则图中 M点乙烯的体积分数约为7.7%
2 2
答案 D解析 平衡常数只与温度有关,温度不变,平衡常数不变,故A错误;升高温度,CO 的平衡转化率降低,
2
可知平衡向逆反应方向移动,根据图示,催化剂的催化效率先升高后降低,故B错误;温度不变,若恒压
下向平衡体系中充入惰性气体,体积增大,相当于减压,平衡逆向移动,故C错误;若投料比
n(H )∶n(CO )=3∶1,图中 M点CO 的平衡转化率为50%,则
2 2 2
6H (g)+2CO (g) CH ==CH (g)+4H O(g)
2 2 2 2 2
初始/mol 3a a 0 0
转化/mol 1.5a 0.5a 0.25a a
平衡/mol 1.5a 0.5a 0.25a a
0.25a
乙烯的体积分数为 ×100%≈7.7%,故D正确。
3.25a
E
7.(2024·江西上饶二模)已知阿伦尼乌斯公式是反应速率常数随温度变化关系的经验公式,可写作Rln k=- a
T
+C(k为反应速率常数,E 为反应活化能,R和C为大于0的常数),为探究m、n两种催化剂对某反应的催
a
化效能,进行了实验探究,依据实验数据获得曲线如图所示。下列说法正确的是( )
A.在m催化剂作用下,该反应的活化能E=9.6×104 J·mol-1
a
B.对该反应催化效能较高的催化剂是m
C.不改变其他条件,升高温度,会降低反应的活化能
D.可以根据该图像判断升高温度时平衡移动的方向
答案 A
E
解析 将(7.2,56.2)和(7.5,27.4)代入Rln k=- a+C中,计算可知E=9.6×104 J·mol-1,故A正确;对比图中
T a
直线m和n的斜率绝对值的大小可知,使用催化剂n时对应的E 较小,则对该反应催化效能较高的催化剂
a
是n,故B错误;图中m、n均为直线,斜率不发生变化,因此不改变其他条件,只升高温度,反应的活
化能不变,故C错误;阿伦尼乌斯公式表示反应速率常数随温度的变化关系,无法根据该图像判断升高温
度时平衡移动的方向,故D错误。
8.利用环戊二烯( )加氢制备环戊烯( ),按n(H )∶n(C H )=1∶1加入恒压密闭容器中,若仅发生如
2 5 6
下反应:
①实验测得环戊二烯转化率(曲线b)和环戊烯选择性(曲线a)随温度变化曲线如图(已知:选择性=转化为目标
产物的反应物在总转化量中的占比)。下列说法错误的是( )
A.70 ℃时,H 的转化率为87.4%
2
B.由图可知,反应的活化能:①<②
n(H )
2
C.相同条件下,若增大 , 选择性增大
n(C H )
5 6
D.升高温度, 生成速率增大, 生成速率减小
答案 D
解析 由图可知,70 ℃时,环戊二烯的转化率为92%,环戊烯的选择性为95%,设起始投入H 的量为1
2
mol,则H 的转化量n(H )=n(环戊烯)=1 mol×92%×95%=0.874 mol,H 的转化率为87.4%,A正确;由图可
2 2 2
知,环戊烯选择性较高,相同时间内,反应①的速率较快,说明反应的活化能:①<②,B正确;相同条
n(H )
2
件下,若增大 ,相当于增大H 的物质的量,反应①中环戊二烯转化率增大,环戊烯选择性增大,
n(C H ) 2
5 6
C正确;升高温度, 生成速率增大, 生成速率也增大,D错误。
9.(2024·广东汕头高三一模)氮氧化物的排放是导致酸雨的原因之一。某研究小组利用反应探究NO的转化:
2NO(g)+2CO(g) N (g)+2CO (g) ΔH<0,向体积均为1 L的两个密闭容器中分别加入2 mol CO(g)和2
2 2
mol NO(g),探究绝热恒容和恒温恒容条件下压强随时间的变化曲线,如图所示,下列有关说法错误的是(
)
A.乙为恒温恒容条件下发生的反应
4
B.甲容器中NO的平衡转化率为 ×100%
15
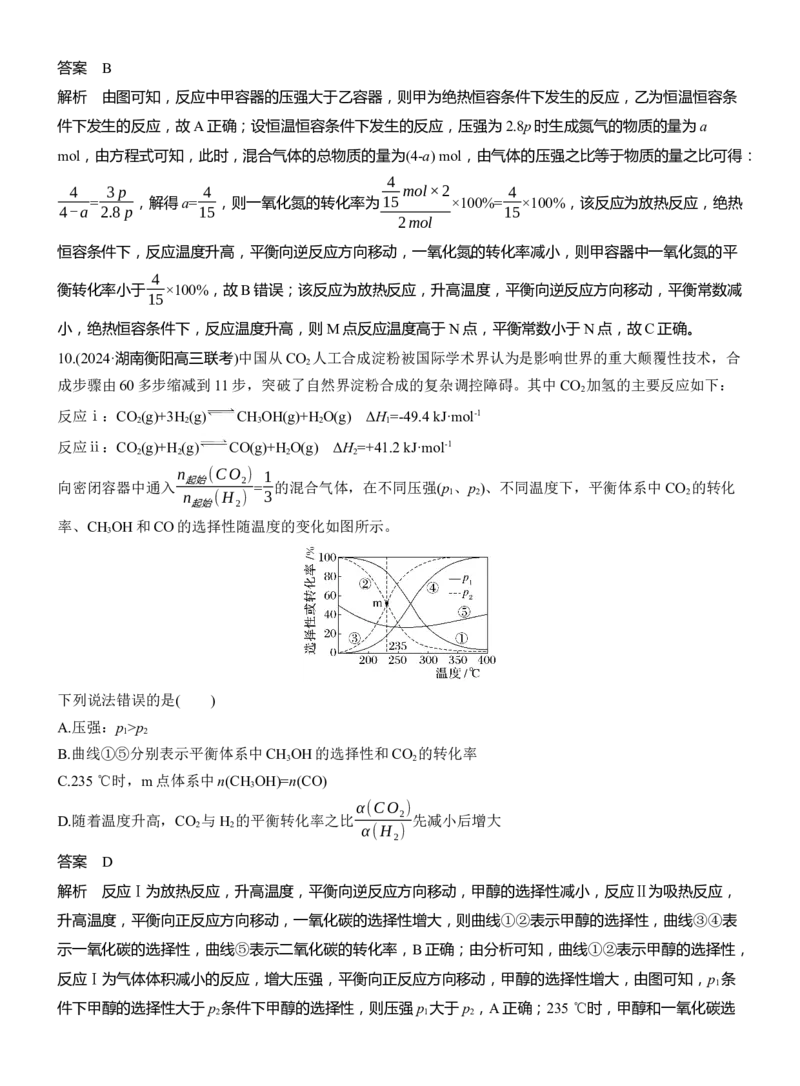
C.反应平衡常数:Mp
1 2
B.曲线①⑤分别表示平衡体系中CH OH的选择性和CO 的转化率
3 2
C.235 ℃时,m点体系中n(CH OH)=n(CO)
3
α(CO )
D.随着温度升高,CO 与H 的平衡转化率之比 2 先减小后增大
2 2 α(H )
2
答案 D
解析 反应Ⅰ为放热反应,升高温度,平衡向逆反应方向移动,甲醇的选择性减小,反应Ⅱ为吸热反应,
升高温度,平衡向正反应方向移动,一氧化碳的选择性增大,则曲线①②表示甲醇的选择性,曲线③④表
示一氧化碳的选择性,曲线⑤表示二氧化碳的转化率,B正确;由分析可知,曲线①②表示甲醇的选择性,
反应Ⅰ为气体体积减小的反应,增大压强,平衡向正反应方向移动,甲醇的选择性增大,由图可知,p 条
1
件下甲醇的选择性大于p 条件下甲醇的选择性,则压强p 大于p ,A正确;235 ℃时,甲醇和一氧化碳选
2 1 2择性相同,两个反应分别生成甲醇和一氧化碳的量相同,故m点体系中n(CH OH)=n(CO),C正确;随着
3
温度升高,反应ⅰ平衡逆向移动,反应ⅱ平衡正向移动,反应ⅱ中二氧化碳和氢气化学计量数之比是
1∶1,氢气消耗少于反应ⅰ,故反应ⅱ进行程度越大,氢气转化率越低且二氧化碳转化率越高,故CO 与
2
H 的平衡转化率之比增大,D错误。
2