文档内容
专题五 能力提升检测卷
1.下列化学用语书写正确的是
A.中子数为8的碳原子: B.钙离子的结构示意图:
C.HCN的电子式: D.二氧化硅的结构式:
2.镅( Am)用于高铁车厢的烟雾传感器。下列关于 Am的说法不正确的是
A.中子数为146 B.质量数为241 C.质子数为95 D.电子数为146
3.我国科学家通过测量 中 和 两种核素的比例来确定“北京人”年龄,这种测量方法叫铝铍
测年法。关于 和 的说法不正确的是
A. 和 化学性质完全不同 B. 的原子核内中子数比质子数多
C.可用质谱法区分 和 D. 和 的质子数和中子数都不相同
4.(Te)与氧元素同族,在元素周期表中与硒(Se)相邻,位于硒(Se)的下方。含元素碲(Te)的几种物质存在如
图所示转化关系。下列说法错误的是
A.反应①利用了 的还原性
B.碲(Te)位于元素周期表中第五周期第ⅥA族
C.反应③利用了 的氧化性
D.HTeO 转化为HTeO 发生了氧化还原反应
2 2 5 2 4 9
5.医学界通过用放射性 标记的 ,发现一种 的羧酸衍生物在特定条件下可通过断裂 杀死细胞,从而抑制艾滋病病毒 。下列说法正确的是
A. 原子与 中普通碳原子的化学性质相同
B. 与 为同一种核素
C. 是一种新型的化合物
D. 与 互为同位素
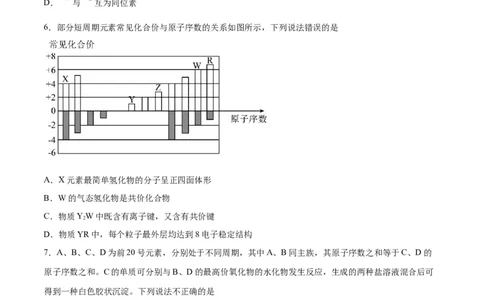
6.部分短周期元素常见化合价与原子序数的关系如图所示,下列说法错误的是
A.X元素最简单氢化物的分子呈正四面体形
B.W的气态氢化物是共价化合物
C.物质YW中既含有离子键,又含有共价键
2
D.物质YR中,每个粒子最外层均达到8电子稳定结构
7.A、B、C、D为前20号元素,分别处于不同周期,其中A、B同主族,其原子序数之和等于C、D的
原子序数之和。C的单质可分别与B、D的最高价氧化物的水化物发生反应,生成的两种盐溶液混合后可
得到一种白色胶状沉淀。下列说法不正确的是
A.简单离子的半径 B.氧化物的熔点:
C.化合物 中含有离子键和共价键 D.化合物 与水反应可生成两种碱
8.短周期元素X、Y、Z、M、W、Q、R的原子半径及主要化合价如下:
元素代号 X Y Z M W Q R
原子半径/nm 0.186 0.143 0.104 0.099 0.070 0.066 0.032
主要化合价 +1 +3 +6,-2 +7,-1 +5,-3 -2 +1下列说法错误的是
A.Z在周期表中的位置是第三周期、VIA族
B.由X、Y、Z、Q四种元素形成的简单离子半径由小到大的顺序是:
C.W和R,Q和R均能形成含有非极性共价键的18e-化合物
D.由Z、W、Q、R四种元素形成的一种离子化合物,其水溶液显强酸性,1 mol该化合物的晶体中所含
的离子数是3N
A
9.元素在周期表中的位置,反映了元素的原子结构和元素性质。下列说法正确的是
A.同周期IA族元素的金属性比IIA族元素的金属性强
B.主族元素的最高正价等于该元素原子的最外层电子数
C.核外电子排布相同的微粒化学性质也相同
D.在金属元素与非金属元素的交界处寻找优良的催化剂
10.X、Y、Z、W为短周期元素,如下表所示,其中W原子的最外层电子数是其内层电子的 。下列说
法不正确的是
X Y
Z W
A.X元素的氢化物分子间可以形成氢键
B.Y元素的两种同素异形体常温下都是气体
C.阴离子半径从大到小的顺序为W>Z>Y>X
D.最高价氧化物对应水化物的酸性:W>Z
11.X、Y、Z、W、Q为短周期主族元素,原子序数依次增大且原子序数总和等于49。它们的化合物在常
温下有如下转化关系:已知:乙、戊分子都含有10个电子。甲为三元化合物,其他化合物均为二元化合
物。下列说法正确的是
A.原子半径从大到小顺序:W>Z>YB.简单氢化物的稳定性:Q>W>Z>Y
C.最高价氧化物对应水化物的酸性:Q>W
D.化合物WQ 中含极性键、非极性键和离子键
2 2
12.X、Y、Z、M是四种短周期主族元素,其中X、Y位于同一主族,Y与M、X与Z位于同一周期。X
原子的最外层电子数是其电子层数的3倍,Z原子的核外电子数比X原子的少1。M是同周期主族元素中
原子半径最大的。下列说法正确的是
A.X、Y、Z的最简单氢化物中,Z的热稳定性最强
B.X、M组成的常见物质中阳离子与阴离子之比一定是2∶1
C.氧化物对应水化物酸性Y强于Z
D.四种元素简单离子的半径大小为Y>X>Z>M
13.X、Y、Z、W是四种短周期元素,原子序数依次增大。X元素原子的最外层电子数是Y元素原子最外
层电子数的3倍,Y、Z元素的原子序数之比为4:5,X、W元素形成的一种阴离子的结构如图所示。下
列说法正确的是
A.该阴离子中X元素均显-1价
B.简单离子半径:X<Y
C.最高价氧化物对应水化物的酸性:W<Z
D.X、Y形成化合物的熔点高于X、W形成化合物的熔点
14.R、X、Y、Z四种短周期主族元素,其原子半径与原子序数关系如图所示。已知:它们的原子序数之
和等于51,R的原子序数与Z的最子外层电子数均为7。下列叙述错误的是A.最简单氢化物的稳定性:Y< Z
B.同浓度的最简单氢化物水溶液的pH:R> Z> Y
C.化合物XY 中含两种化学键
2 2
D.等浓度的X、Z最高价氧化物对应的水化物的稀溶液中,水的电离程度相同
15.由下列实验及相应事实推理所得的结论,不能用元素周期律解释的是
实验 事实 结论
A 将体积相同的 和 分别投入冷水 与 反应更剧烈 金属性:
B 将足量硫酸与 溶液混合 生成 非金属性:
C 分别加热 气体和 气体 气体更易分解 稳定性:
D 工业上用焦炭还原石英砂制得粗硅 非金属性:
16.已知W、X、Y、Z是原子序数依次增大的前20号元素,其中X为地壳中含量最多的金属元素,化合
物M由W、Y、Z三种元素组成,将M进行下列实验:
①取适量M,加水完全溶解,无气体产生;进行焰色反应,透过蓝色钴玻璃观察到火焰呈紫色;
②取1.685g M溶于水,加入含HCl 0.02000 mol的盐酸恰好中和;中和后的溶液与硝酸酸化的过量AgNO
3
溶液反应,得到4.305g白色沉淀。则下列说法不正确的是
A.简单离子半径大小:Y > Z > W > X
B.元素X分别与W、Y之间形成的化合物均为离子化合物
C.元素X、Y、Z最高价氧化物的水化物之间可以相互反应D.简单氢化物的沸点:Z > W > Y
17.原子序数依次增大的短周期主族元素X、Y、Z、W,其中X与Z同族,其中Y、Z、W构成的某种离
子化合物结构如图所示。下列叙述中正确的是
A.简单氢化物的稳定性: B.原子半径大小关系是:
C.Z与Y形成的化合物可能含有非极性键 D.W的氧化物的水化物是一种强酸
18.短周期主族元素W、X、Y、Z、Q 原子序数依次增大,形成的化合物是一种重要的食品添加剂,结构
如下图。Z核外最外层电子数与X 核外电子总数相等。W的原子半径在周期表中最小。下列有关叙述正确
的是
A.原子半径大小:Y>Z>Q
B.该化合物中Y 原子不满足8 电子稳定结构
C.该化合物中,W、X、Y、Z、Q 之间均为共价键
D.Q元素对应的单质能与水反应,也能与乙醇反应
19.现有A、B、C、D、E、F六种短周期主族元素,原子序数依次增大。已知A的气态氢化物能与其最
高价氧化物的水化物反应得到一种离子化合物,B的一种单质具有杀菌消毒的作用,C+和D3+的电子层结
构相同,E的主族序数是其周期序数的2倍。
(1)F在元素周期表中的位置是 。
(2)上述元素形成的简单离子中,半径最大的是 (填离子符号)。
(3)由上述元素中的一种或几种组成的物质甲可以发生如下反应:
①若丙具有漂白性,则甲和水反应的离子方程式为 。
②若乙的水溶液是强碱性溶液,物质丙为B的一种单质,则甲中含有的化学键的类型为 ,D的单
质与乙的水溶液反应的离子方程式为 。③若甲为D和E形成的二元化合物,物质丙是气体,则丙的结构式为 ;物质乙为白色沉淀,
其化学式为 。
20.下列表格是元素周期表的一部分。请按要求填空(用化学用语填写)
(1)元素①和⑥形成的化合物中存在的化学键类型为 。
(2)用化学方程式表示④的简单氢化物的工业制法 。
(3)写出由③④⑥形成的化合物的电子式 。
(4)列举元素⑨形成的氧化物的一种用途 ,元素 在周期表中的位置 。
(5)①⑤⑦⑧的简单离子半径由大到小的顺序为 。⑪
(6)写出⑧ 的最高价氧化物的水化物发生反应的化学方程式为 。
⑫
(7)X是由①④⑤⑧⑩形成的复盐,向含0.01 mol X的溶液中加入0.024 mol ,生成沉淀的物质的
量的总和为 。
21.R、W、X、Y、M是原子序数依次增大的五种主族元素。R最常见同位素的原子核中不含中子。W与
X可形成两种稳定的化合物:WX和WX。工业革命以来,人类使用的化石燃料在燃烧过程中将大量WX
2 2
排入大气,在一定程度导致地球表面平均温度升高。Y与X是同一主族的元素,且在元素周期表中与X相
邻。
(1)W的原子结构示意图是 。
(2)WX 的电子式是 。
2
(3)R X、R Y中,稳定性较高的是 (填化学式),请从原子结构的角度解释其原因: 。
2 2
(4)Se与Y是同一主族的元素,且在元素周期表中与Y相邻。
①根据元素周期律,下列推断正确的是 (填字母序号)。
a.Se的最高正化合价为+7价
b.HSe的还原性比HY强
2 2
c.HSeO 的酸性比HYO 强
2 3 2 4
d.SeO 在一定条件下可与NaOH溶液反应
2
②室温下向SeO 固体表面吹入NH ,可得到两种单质和HO,该反应的化学方程式为 。
2 3 2(5)科研人员从矿石中分离出一种氧化物,化学式可表示为MO。为确定M元素的种类,进行了一系列
2 3
实验,结果如下:
①M的相对原子质量介于K和Rb(铷)之间;
②0.01 mol M O 在碱性溶液中与Zn充分反应可得到M的简单氢化物,反应完全时,被MO 氧化的Zn为
2 3 2 3
0.06 mol;
综合以上信息推断,M可能位于元素周期表第 族。
22.原子序数依次增大的X、Y、Z、W、M五种短周期主族元素中,X、Y两元素间能形成原子个数比分
别为1:1和1:2的固态化合物A和B,Y是短周期元素中失电子能力最强的元素,W、M的最高价氧化 物
对应的水化物化学式分别为HWO、HMO ,Z的单质能与盐酸反应。
3 4 4
(1)根据上述条件不能确定的元素是 (填代号),A的电子式为 ,举例说明Y、Z的金属性相对
强弱: (写出一个即可)。
(2)W能形成多种含氧酸及应的盐,其中NaH WO 能与盐酸反应但不能与NaOH溶液反应,则下列说法中
2 2
正确的是 (填字母)
A H WO 是三元酸
3 2
B H WO 是一元弱酸
3 2
C NaH WO 是酸式盐
2 2
D NaHWO 不可能被硝酸氧化
2 2
(3)X、M形成的一种化合物MX 是一种优良的水处理剂,某自来水化验室利用下列方法裣测处理后的 水
2
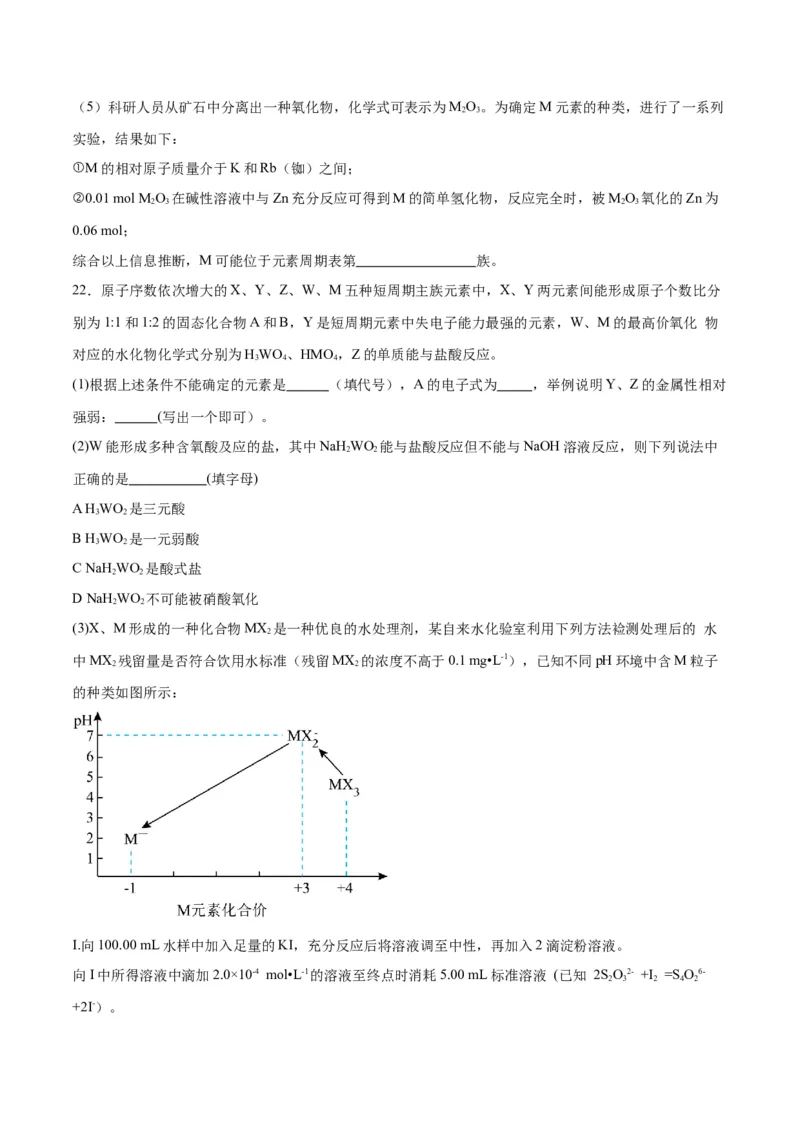
中MX 残留量是否符合饮用水标准(残留MX 的浓度不高于0.1 mg•L-1),已知不同pH环境中含M粒子
2 2
的种类如图所示:
I.向100.00 mL水样中加入足量的KI,充分反应后将溶液调至中性,再加入2滴淀粉溶液。
向I中所得溶液中滴加2.0×10-4 mol•L-1的溶液至终点时消耗5.00 mL标准溶液 (已知 2SO2- +I =S O6-
2 3 2 4 2
+2I-)。①则该水样中残留的的浓度为 mg•L-1。
②若再向II中所得溶液中加硫酸调节水样pH至1〜3,溶液又会呈蓝色,其原因是 (用离子方程式表
示)。