文档内容
专题十二 化学反应原理 专题检测
(7 小题,共100分)
1.(2022·河南郑州·三模)(14分)“水煤气(CO和H )”是化学工业常用的原料气,
2
在某工业上应用原理如下:
主反应:CO(g)+H O(g) CO (g)+H (g)ΔH=﹣41.03kJ•mol﹣1
2 2 2
副反应:CO(g)+2H (g)⇌CH OH(g)ΔH=﹣116kJ•mol﹣1
2 3
(1)写出CO
2
加氢制CH
3
OH⇌的热化学方程式 。
(2)在压强为81kPa的恒压体系中充入一定量含CO、H 、H O、N 的混合气体,充分反
2 2 2
应后,在T℃下,反应达到平衡后,测得混合气体各组分的物质的量分别为
0.6molCO、3molH 、1.6molH O、1molN 、1.6molCO 和0.3molCH OH。
2 2 2 2 3
①T℃时,副反应的标准平衡常数K = (保留三位有效数字)(已知:分压=总
p
压×该组分物质的量分数,对于反应dD(g)+eE(g) gG(g)+hH(g),KΘ=
⇌
其中pΘ=100kPa,p 、p 、p 、p 为各组分的平衡分压)。
G H D E
②平衡时CO的转化率为 。
③为同时提高CO的平衡转化率和CH OH的平衡产率,应选择的反应条件为
3
(填标号)。
A.低温、高压
B.高温、低压
C.低温、低压
D.高温、高压
(3)若其他条件一定,向原料气中加入N 稀释气体并保持总压强不变,测得CO的平衡
2
百分含量增大,原因是 。
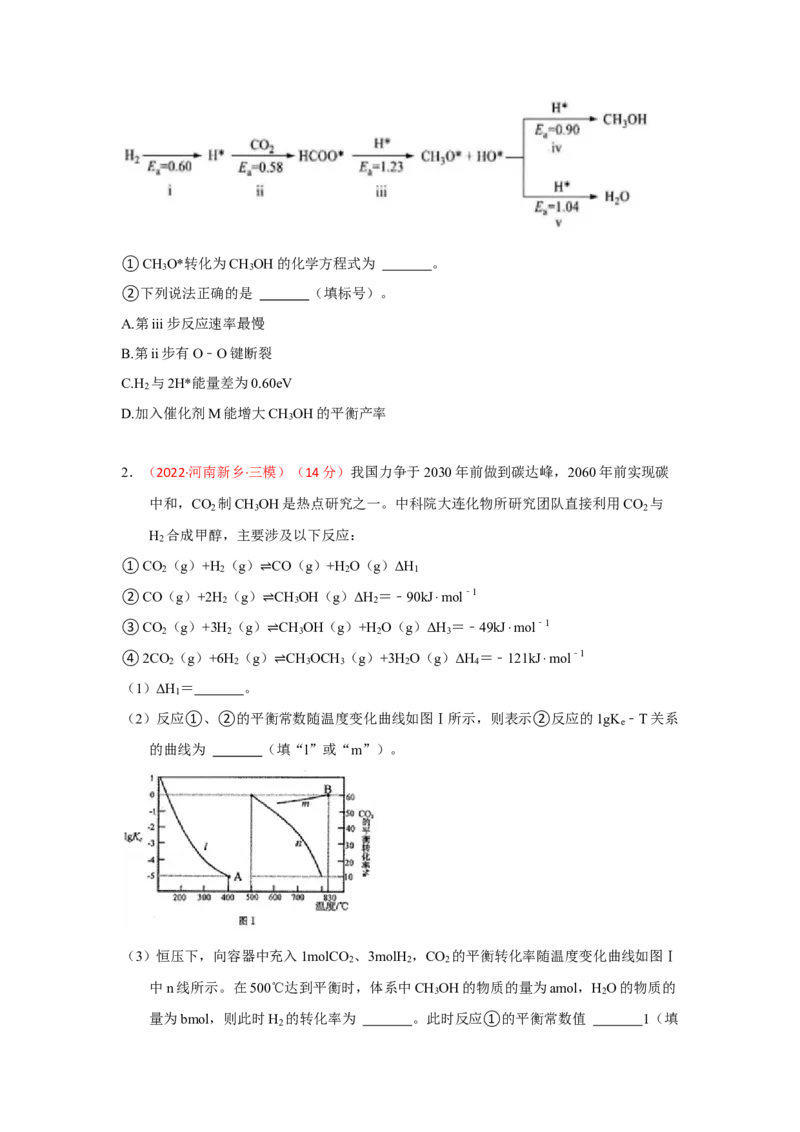
(4)利用M催化CO 加氢制CH OH的反应历程如图,其中吸附在催化剂表面的物种用*
2 3
表示,Ea表示活化能,单位为eV。①CH O*转化为CH OH的化学方程式为 。
3 3
②下列说法正确的是 (填标号)。
A.第iii步反应速率最慢
B.第ii步有O﹣O键断裂
C.H 与2H*能量差为0.60eV
2
D.加入催化剂M能增大CH OH的平衡产率
3
2.(2022·河南新乡·三模)(14分)我国力争于2030年前做到碳达峰,2060年前实现碳
中和,CO 制CH OH是热点研究之一。中科院大连化物所研究团队直接利用CO 与
2 3 2
H 合成甲醇,主要涉及以下反应:
2
①CO (g)+H (g) CO(g)+H O(g)ΔH
2 2 2 1
②CO(g)+2H
2
(g)⇌CH
3
OH(g)ΔH
2
=﹣90kJ⋅mol﹣1
③CO
2
(g)+3H
2
(g)⇌ CH
3
OH(g)+H
2
O(g)ΔH
3
=﹣49kJ⋅mol﹣1
④2CO
2
(g)+6H
2
(g)⇌ CH
3
OCH
3
(g)+3H
2
O(g)ΔH
4
=﹣121kJ⋅mol﹣1
(1)ΔH 1 = 。 ⇌
(2)反应①、②的平衡常数随温度变化曲线如图Ⅰ所示,则表示②反应的1gK ﹣T关系
e
的曲线为 (填“l”或“m”)。
(3)恒压下,向容器中充入1molCO 、3molH ,CO 的平衡转化率随温度变化曲线如图Ⅰ
2 2 2
中n线所示。在500℃达到平衡时,体系中CH OH的物质的量为amol,H O的物质的
3 2
量为bmol,则此时H 的转化率为 。此时反应①的平衡常数值 1(填
2“大于”、“小于”或“等于。)
(4)有同学认为在400℃以后反应②在该体系中可以忽略,其依据是 。
(5)500℃以后CO 的平衡转化率随温度变化的可能原因是 。
2
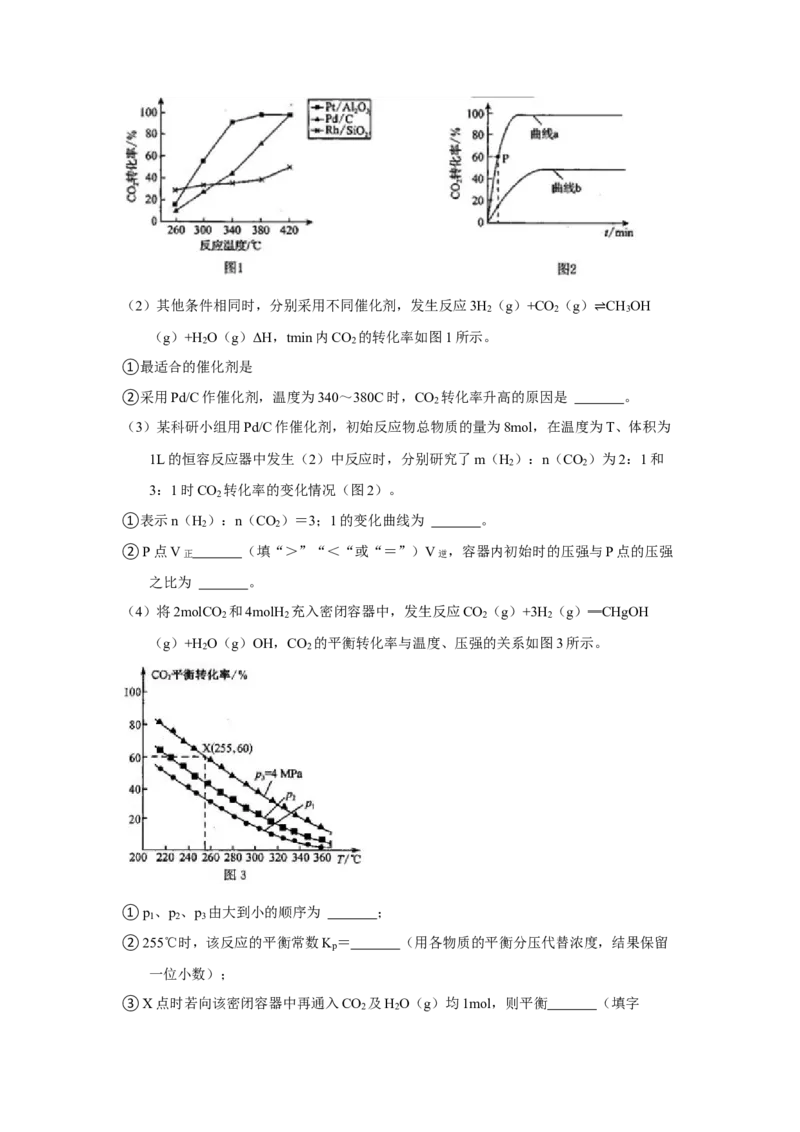
(6)恒压下将CO 和H 按体积比1:3混合,在不同催化剂作用下发生反应。在相同时间
2 2
段内CH OH的选择性和产率随温度的变化如图Ⅱ所示。其中CH OH的选择性=
3 3
×100%。
则合成甲醇的适宜条件是 (填标号)。
A.230℃
B.210℃
C.CZT催化剂
D.CZ(Zr﹣1)T催化剂
(7)BASF高压法制备CH COOH时的钴碘催化循环法如图Ⅲ所示,该循环的总反应为
3
。
3.(广东省珠海市2022届高三上学期摸底测试)(14分)中科院天津工业生物所利用光
伏发电,将电解水获得的H 与CO 反应合成甲醇,再由甲醇经若干酶促反应合成淀
2 2
粉,首次在实验室实现二氧化碳到淀粉的从头合成。回答下列问题:
(1)该研究成果的重大意义是 。(答出一点即可)
(2)已知:在一定温度和压强下,由最稳定单质生成1mol化合物的焓变称为该物质的摩
尔生成焓。某些化合物的摩尔生成焓如表所示。
化合物 CO (g) CH OH(g) H O(g)
2 3 2
摩尔生成焓/(kJ•mol﹣1) ﹣395 ﹣200 ﹣242
反应Ⅰ:CO (g)+3H (g) CH OH(g)+H O(g) ΔH
2 2 3 2 1
⇌反应Ⅱ:CO (g)+H (g) CO(g)+H O(g) ΔH
2 2 2 2
①反应Ⅰ的焓变ΔH = ⇌ kJ•mol﹣1。
1
②保持温度T不变,在一刚性密闭容器中,充入一定量的CO 和H ,同时发生反应Ⅰ和
2 2
Ⅱ,起始及达平衡时,容器内各气体的物质的量如表所示。
CO H CH OH CO H O
2 2 3 2
起始量/mol 4.0 8.0 0 0 0
平衡量/mol n 3.0
1
已知起始时总压强为1.5pkPa,平衡时体系总压强为pkPa,则表中n = ,反应Ⅰ的
1
平衡常数K = 。(含p的式子表示)
p
(3)取物质的量浓度为amol•L﹣1的甲醇,选择不同的工程酶组块作为催化剂反应10h,
测得实验数据如表所示。
实验序号 温度/K 不同工程酶的组块 淀粉/(g•L﹣1)
1 T agp﹣M 0.21
1 1
2 T agp﹣M 0.38
1 2
3 T agp﹣M 1.82
2 2
4 T agp﹣M 1.24
2 3
①根据表中数据选取最佳的反应条件 。
②已知温度升高,反应生成的淀粉量先增加后急剧减少,其可能原因是 。
③实验4可用淀粉的质量浓度表示反应速率为 g•L﹣1•h﹣1。淀粉的产率为
。(用含a的式子表示)
4.(广东省汕头市2022届高三下学期第一次模拟)(14分)甲醇(CH OH)是一种可再
3
生能源,具有广阔的开发和应用前景,Pt/Al O 、Pd/C、Rh/SiO 都可以用作合成
2 3 2
CH OH的催化剂:3H (g)+CO (g) CH OH(g)+H O(g)ΔH。回答下列问
3 2 2 3 2
题: ⇌
(1)已知:iH (g)+CO (g) CO(g)+H O(g)ΔH =+41kJ•mol﹣1;
2 2 2 1
ii.2H (g)+CO(g) CH OH(⇌g)ΔH =﹣90kJ•mol﹣1
2 3 2
3H (g)+CO (g) ⇌CH OH(g)+H O(g)的ΔH= kJ•mol﹣1。
2 2 3 2
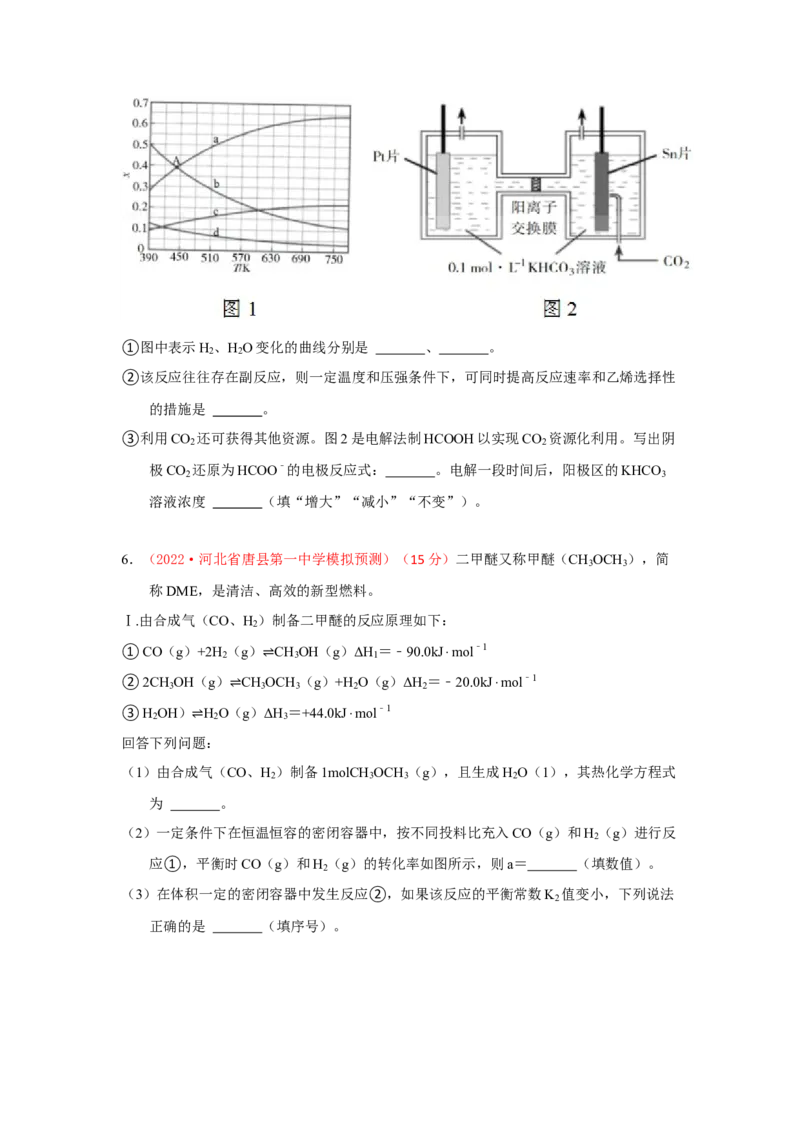
⇌(2)其他条件相同时,分别采用不同催化剂,发生反应3H (g)+CO (g) CH OH
2 2 3
(g)+H O(g)ΔH,tmin内CO 的转化率如图1所示。 ⇌
2 2
①最适合的催化剂是
②采用Pd/C作催化剂,温度为340~380C时,CO 转化率升高的原因是 。
2
(3)某科研小组用Pd/C作催化剂,初始反应物总物质的量为8mol,在温度为T、体积为
1L的恒容反应器中发生(2)中反应时,分别研究了m(H ):n(CO )为2:1和
2 2
3:1时CO 转化率的变化情况(图2)。
2
①表示n(H ):n(CO )=3;1的变化曲线为 。
2 2
②P点V正 (填“>”“<“或“=”)V逆 ,容器内初始时的压强与P点的压强
之比为 。
(4)将2molCO 和4molH 充入密闭容器中,发生反应CO (g)+3H (g)═CHgOH
2 2 2 2
(g)+H O(g)OH,CO 的平衡转化率与温度、压强的关系如图3所示。
2 2
①p 、p 、p 由大到小的顺序为 ;
1 2 3
②255℃时,该反应的平衡常数K = (用各物质的平衡分压代替浓度,结果保留
p
一位小数);
③X点时若向该密闭容器中再通入CO 及H O(g)均1mol,则平衡 (填字
2 2母)。
A.正向移动
B.逆向移动
C.不移动
5.(2022·河南开封·三模)(14分)乙烯是重要的化工原料,目前主要通过石油炼化制
备。随着化石燃料资源日益减少,科研工作者正在探索和研发制备乙烯(C H )的新
2 4
方法。
Ⅰ.甲烷直接脱氢制备乙烯
(1)已知燃烧热:H 为285.8kJ/mol,CH 为890.3kJ/mol,C H 为1411.0kJ/mol。则由甲
2 4 2 4
烷直接脱氢制备乙烯的热化学方程式是 。k正 、k逆 均是与温度有关的常数,
当升高温度时,k正 增大的倍数 k逆 增大的倍数(填“>”、“=”或
“<”,下同);
(2)T ℃时,向初始压强100kPa的恒容密闭反应器中充入1molCH ,发生(1)中反应,
0 4
测得平衡混合气体中H 的体积分数为40.0%。则:
2
①在该温度下,其压强平衡常数K = 。(分压=总压×物质的量分数)
p
②若向该反应器中通入高温水蒸气(不参加反应,高于T ℃),则C H 的产率将增大,
0 2 4
其理由是 。
③实际制备C H 时,通常存在副反应2CH (g)═C H (g)+H (g)。若在T ℃时,H
2 4 4 2 6 2 0 2
的体积分数为45%,C H 20%,其余为C H 和CH ,则体系中CH 的体积分数是
2 4 2 6 4 4
。
Ⅱ.CO 催化加氢合成乙烯:2CO +6H ═C H +4H O
2 2 2 2 4 2
(3)理论计算表明,压强为0.1MPa,原料初始组成n(CO ):n(H )=1:3,反应达
2 2
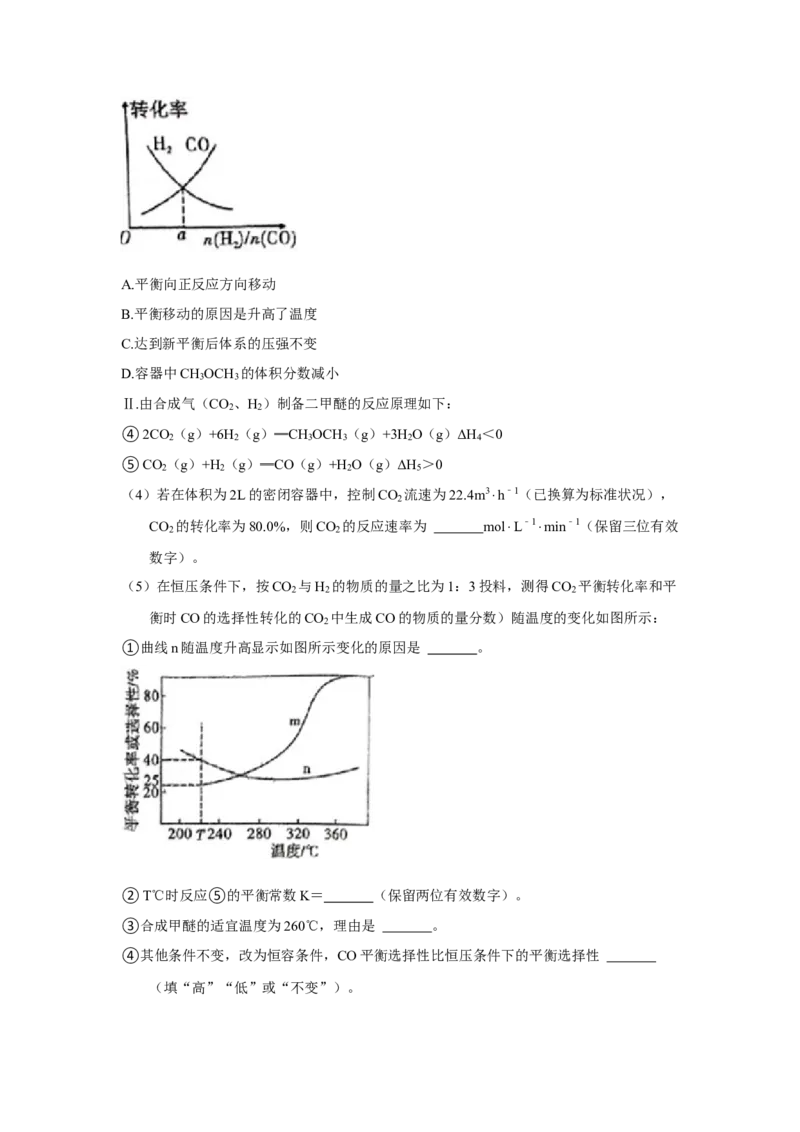
到平衡时四种组分的物质的量分数x随温度T的变化如图1所示。①图中表示H 、H O变化的曲线分别是 、 。
2 2
②该反应往往存在副反应,则一定温度和压强条件下,可同时提高反应速率和乙烯选择性
的措施是 。
③利用CO 还可获得其他资源。图2是电解法制HCOOH以实现CO 资源化利用。写出阴
2 2
极CO 还原为HCOO﹣的电极反应式: 。电解一段时间后,阳极区的KHCO
2 3
溶液浓度 (填“增大”“减小”“不变”)。
6.(2022·河北省唐县第一中学模拟预测)(15分)二甲醚又称甲醚(CH OCH ),简
3 3
称DME,是清洁、高效的新型燃料。
Ⅰ.由合成气(CO、H )制备二甲醚的反应原理如下:
2
①CO(g)+2H
2
(g) CH
3
OH(g)ΔH
1
=﹣90.0kJ⋅mol﹣1
②2CH
3
OH(g) CH
3
⇌OCH
3
(g)+H
2
O(g)ΔH
2
=﹣20.0kJ⋅mol﹣1
③H
2
OH) H
2
O(⇌g)ΔH
3
=+44.0kJ⋅mol﹣1
回答下列问题⇌:
(1)由合成气(CO、H )制备1molCH OCH (g),且生成H O(1),其热化学方程式
2 3 3 2
为 。
(2)一定条件下在恒温恒容的密闭容器中,按不同投料比充入CO(g)和H (g)进行反
2
应①,平衡时CO(g)和H (g)的转化率如图所示,则a= (填数值)。
2
(3)在体积一定的密闭容器中发生反应②,如果该反应的平衡常数K 值变小,下列说法
2
正确的是 (填序号)。A.平衡向正反应方向移动
B.平衡移动的原因是升高了温度
C.达到新平衡后体系的压强不变
D.容器中CH OCH 的体积分数减小
3 3
Ⅱ.由合成气(CO 、H )制备二甲醚的反应原理如下:
2 2
④2CO (g)+6H (g)═CH OCH (g)+3H O(g)ΔH <0
2 2 3 3 2 4
⑤CO (g)+H (g)═CO(g)+H O(g)ΔH >0
2 2 2 5
(4)若在体积为2L的密闭容器中,控制CO
2
流速为22.4m3⋅h﹣1(已换算为标准状况),
CO
2
的转化率为80.0%,则CO
2
的反应速率为 mol⋅L﹣1⋅min﹣1(保留三位有效
数字)。
(5)在恒压条件下,按CO 与H 的物质的量之比为1:3投料,测得CO 平衡转化率和平
2 2 2
衡时CO的选择性转化的CO 中生成CO的物质的量分数)随温度的变化如图所示:
2
①曲线n随温度升高显示如图所示变化的原因是 。
②T℃时反应⑤的平衡常数K= (保留两位有效数字)。
③合成甲醚的适宜温度为260℃,理由是 。
④其他条件不变,改为恒容条件,CO平衡选择性比恒压条件下的平衡选择性
(填“高”“低”或“不变”)。7.(2022·广东·执信中学模拟预测)(15分)我国正式公布实现碳达峰、碳中和的时
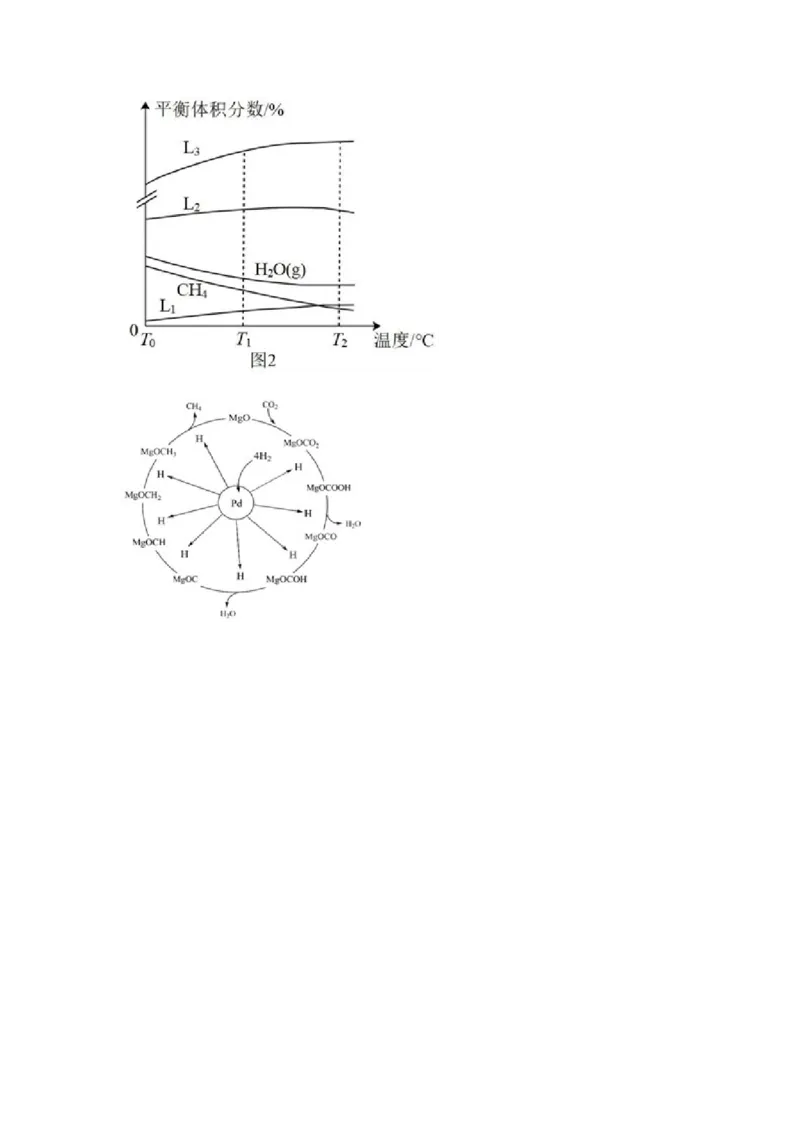
间和目标后,使含碳化合物的综合利用更受关注和重视。回答下列问题:
(1)一定条件下,Pd﹣Mg/SiO 催化剂可使CO 甲烷化从而变废为宝,其反应机理如图1
2 2
所示,该反应的化学方程式为 ,反应过程中碳元素的化合价为﹣2价的中间
体是 。
(2)二氧化碳与氢气重整体系中涉及的主要反应如下:
Ⅰ.CO (g)+4H (g) CH (g)+2H O(g)ΔH=﹣165kJ•mol﹣1
2 2 4 2
Ⅱ.CO (g)+H (g) ⇌CO(g)+H O(g)ΔH=+41kJ•mol﹣1
2 2 2
①二氧化碳与甲烷反应⇌生成一氧化碳和氢气的热化学方程式为 ;恒温恒容密闭容
器中进行该反应,下列事实能说明反应达到平衡状态的是 (填选项字母)。
A.CO 与CH 的有效碰撞几率不变
2 4
B.相同时间内形成C﹣H键和H﹣H键的数目相等
C.混合气体的密度不再改变
D.氢原子数不再改变
②一定温度下,向10L恒容密闭容器中充入1molCO 和1molH ,发生反应Ⅰ和反应Ⅱ,
2 2
5min末达到平衡时测得CO 的转化率为50%,CH 与CO的分压之比为1:4,H O
2 4 2
(g)的分压为p 。则0~5min内,平均反应速率v(H )= mol•L﹣1•min﹣1;
0 2
反应Ⅱ的平衡常数K = (K 是用分压表示的平衡常数)。
p p
③向恒容密闭容器中以物质的量之比为1:4充入CO 和H ,发生反应Ⅰ和反应Ⅱ,实验
2 2
测得平衡体系中各组分的体积分数与温度的关系如图2所示。其中表示H 的体积分数
2
与温度关系的曲线为 (填“L ”、“L ”或“L ”);T ℃之后,H O(g)
1 2 3 1 2
平衡体积分数随温度的变化程度小于CH 平衡体积分数随温度的变化程度,原因为
4
;T ℃时CO的平衡分压 (填“>”“<”或“=”)T ℃时CO的平衡分
1 2
压,理由为 。