文档内容
专题突破(三) 以金属及其化合物为主体的化工流程
化学工艺流程题是高考热点题型之一,大多以金属及其化合物的性质与转化为主体,此
类试题源于化工生产实际,以解决化学实际问题为线索进行设问,使问题情境更加真实。此
类试题的情境新颖,信息容量大,涉及化学基础知识、实验基本操作和技能等,要求考生在复
杂情境中对必备知识和关键能力进行综合运用,体现“高考命题应坚持理论联系实际的原
则,使用贴近时代、贴近社会、贴近生活素材,选取日常生活、工业生产、国家发展、社会进步
中的实际问题,考查学生运用知识、能力和素养解决实际问题的能力,让学生充分感受到课
堂所学内容中蕴含的应用价值”的指导思想。
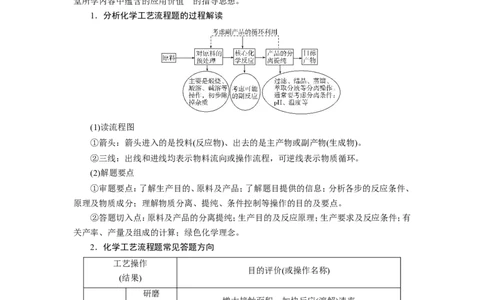
1.分析化学工艺流程题的过程解读
(1)读流程图
①箭头:箭头进入的是投料(反应物)、出去的是主产物或副产物(生成物)。
②三线:出线和进线均表示物料流向或操作流程,可逆线表示物质循环。
(2)解题要点
①审题要点:了解生产目的、原料及产品;了解题目提供的信息;分析各步的反应条件、
原理及物质成分;理解物质分离、提纯、条件控制等操作的目的及要点。
②答题切入点:原料及产品的分离提纯;生产目的及反应原理;生产要求及反应条件;有
关产率、产量及组成的计算;绿色化学理念。
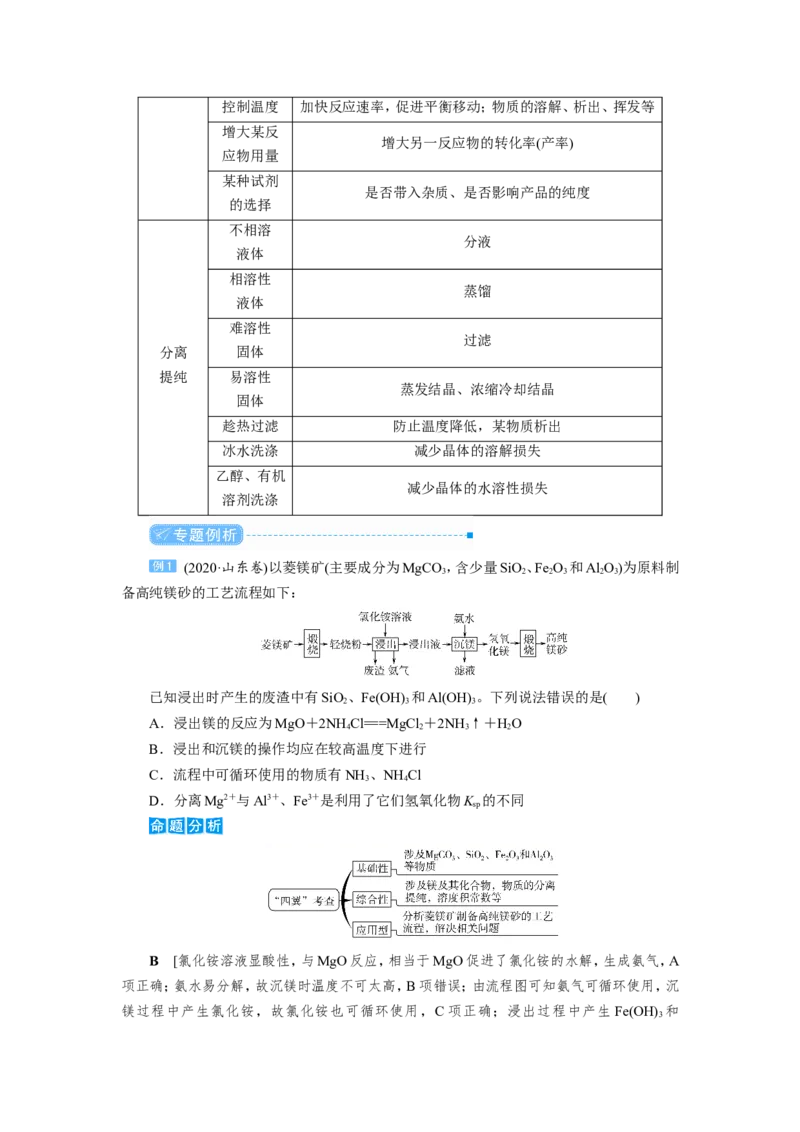
2.化学工艺流程题常见答题方向
工艺操作
目的评价(或操作名称)
(结果)
研磨
增大接触面积,加快反应(溶解)速率
(粉碎)
煅烧
方法 矿物分解、燃烧,转化为易溶于酸、碱的物质
(焙烧)
措施
水浸 利用水溶性把物质进行分离
酸浸 利用物质与酸(碱)反应除掉杂质或把目标物质转化为可溶
(碱浸) 性离子
控制 调节溶
某些金属离子的沉淀,控制物质的溶解
条件 液pH控制温度 加快反应速率,促进平衡移动;物质的溶解、析出、挥发等
增大某反
增大另一反应物的转化率(产率)
应物用量
某种试剂
是否带入杂质、是否影响产品的纯度
的选择
不相溶
分液
液体
相溶性
蒸馏
液体
难溶性
过滤
分离 固体
提纯 易溶性
蒸发结晶、浓缩冷却结晶
固体
趁热过滤 防止温度降低,某物质析出
冰水洗涤 减少晶体的溶解损失
乙醇、有机
减少晶体的水溶性损失
溶剂洗涤
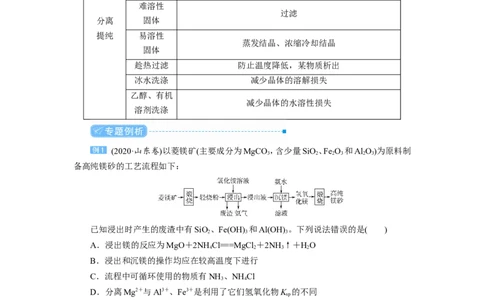
(2020·山东卷)以菱镁矿(主要成分为MgCO ,含少量SiO、Fe O 和Al O)为原料制
3 2 2 3 2 3
备高纯镁砂的工艺流程如下:
已知浸出时产生的废渣中有SiO、Fe(OH) 和Al(OH) 。下列说法错误的是( )
2 3 3
A.浸出镁的反应为MgO+2NH Cl===MgCl +2NH ↑+HO
4 2 3 2
B.浸出和沉镁的操作均应在较高温度下进行
C.流程中可循环使用的物质有NH 、NH Cl
3 4
D.分离Mg2+与Al3+、Fe3+是利用了它们氢氧化物K 的不同
sp
B [氯化铵溶液显酸性,与MgO反应,相当于MgO促进了氯化铵的水解,生成氨气,A
项正确;氨水易分解,故沉镁时温度不可太高,B项错误;由流程图可知氨气可循环使用,沉
镁过程中产生氯化铵,故氯化铵也可循环使用,C项正确;浸出过程中产生Fe(OH) 和
3Al(OH) ,沉镁过程中加氨水调节pH产生Mg(OH) ,利用三种离子氢氧化物K 的不同,使其
3 2 sp
先后沉淀而分离,D项正确。]
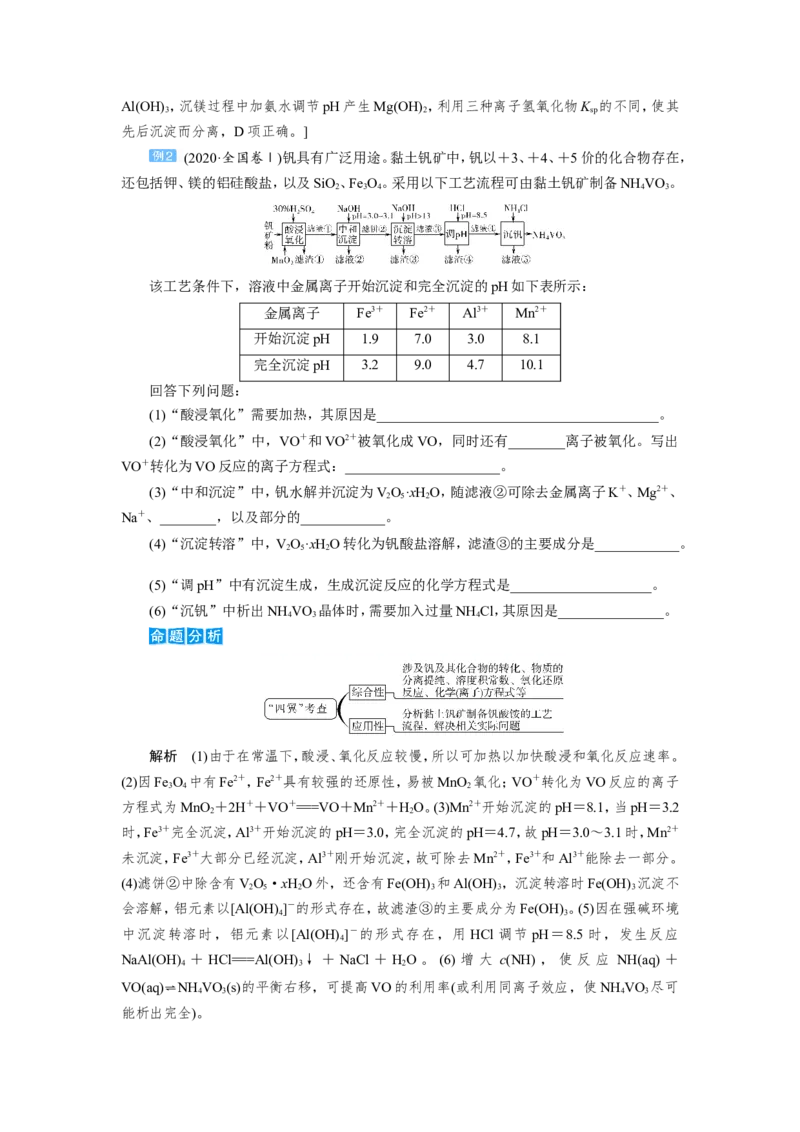
(2020·全国卷Ⅰ)钒具有广泛用途。黏土钒矿中,钒以+3、+4、+5价的化合物存在,
还包括钾、镁的铝硅酸盐,以及SiO、Fe O。采用以下工艺流程可由黏土钒矿制备NH VO 。
2 3 4 4 3
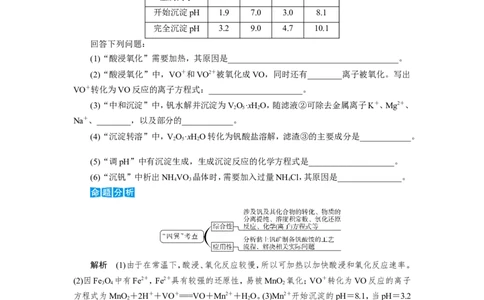
该工艺条件下,溶液中金属离子开始沉淀和完全沉淀的pH如下表所示:
金属离子 Fe3+ Fe2+ Al3+ Mn2+
开始沉淀pH 1.9 7.0 3.0 8.1
完全沉淀pH 3.2 9.0 4.7 10.1
回答下列问题:
(1)“酸浸氧化”需要加热,其原因是________________________________________。
(2)“酸浸氧化”中,VO+和VO2+被氧化成VO,同时还有________离子被氧化。写出
VO+转化为VO反应的离子方程式:______________________。
(3)“中和沉淀”中,钒水解并沉淀为VO·xHO,随滤液②可除去金属离子K+、Mg2+、
2 5 2
Na+、________,以及部分的____________。
(4)“沉淀转溶”中,VO·xHO转化为钒酸盐溶解,滤渣③的主要成分是____________。
2 5 2
(5)“调pH”中有沉淀生成,生成沉淀反应的化学方程式是____________________。
(6)“沉钒”中析出NH VO 晶体时,需要加入过量NH Cl,其原因是_______________。
4 3 4
解析 (1)由于在常温下,酸浸、氧化反应较慢,所以可加热以加快酸浸和氧化反应速率。
(2)因Fe O 中有Fe2+,Fe2+具有较强的还原性,易被MnO 氧化;VO+转化为VO反应的离子
3 4 2
方程式为MnO +2H++VO+===VO+Mn2++HO。(3)Mn2+开始沉淀的pH=8.1,当pH=3.2
2 2
时,Fe3+完全沉淀,Al3+开始沉淀的pH=3.0,完全沉淀的pH=4.7,故pH=3.0~3.1时,Mn2+
未沉淀,Fe3+大部分已经沉淀,Al3+刚开始沉淀,故可除去Mn2+,Fe3+和Al3+能除去一部分。
(4)滤饼②中除含有VO·xHO外,还含有Fe(OH) 和Al(OH) ,沉淀转溶时Fe(OH) 沉淀不
2 5 2 3 3 3
会溶解,铝元素以[Al(OH) ]-的形式存在,故滤渣③的主要成分为Fe(OH) 。(5)因在强碱环境
4 3
中沉淀转溶时,铝元素以[Al(OH) ]-的形式存在,用 HCl 调节 pH=8.5 时,发生反应
4
NaAl(OH) + HCl===Al(OH) ↓ + NaCl + HO 。 (6) 增 大 c(NH) , 使 反 应 NH(aq) +
4 3 2
VO(aq)⇌NH
4
VO
3
(s)的平衡右移,可提高VO的利用率(或利用同离子效应,使NH
4
VO
3
尽可
能析出完全)。答案 (1)加快酸浸和氧化反应速率(促进氧化完全)
(2)Fe2+ VO++MnO +2H+===VO+Mn2++HO
2 2
(3)Mn2+ Al3+和Fe3+
(4)Fe(OH)
3
(5)NaAl(OH) +HCl===Al(OH) ↓+NaCl+HO
4 3 2
(6)利用同离子效应,促进NH VO 尽可能析出完全
4 3
1.(2021·北京首都师大附中检测)工业上应用两矿法浸出软锰矿(主要成分MnO )和方铅
2
矿(主要成分PbS、FeS),制备PbSO 和MnO,转化流程如下。
2 4 3 4
已知:PbCl
2
微溶于水,溶液中存在可逆反应:PbCl
2
+2Cl- ⇌PbCl。
下列说法正确的是( )
A.Ⅰ中可使用浓盐酸代替稀盐酸和NaCl的混合溶液
B.Ⅱ中生成的沉淀Y是Fe(OH)
2
C.Ⅳ中试剂X可能作氧化剂
D.Ⅴ中发生反应:Pb2++SO=== PbSO
4
C [Ⅰ中可使用浓盐酸代替稀盐酸和NaCl的混合溶液,在70 ℃时可与软锰矿中MnO
2
反应生成Cl ,A错误;MnO 、FeS 和盐酸发生反应:3MnO +2FeS +12HCl===3MnCl +
2 2 2 2 2 2
2FeCl +4S+6HO,步骤Ⅱ调节pH使Fe3+转化为沉淀,故沉淀Y是Fe(OH) ,B错误;Ⅳ中
3 2 3
溶液加入试剂X和氨水,Mn2+被氧化生成MnO,则试剂X可能作氧化剂,C正确;PbCl 微
3 4 2
溶于水,溶液中存在可逆反应:PbCl +2Cl-===PbCl,Ⅴ中加入稀硫酸,发生反应:PbCl+
2
SO===PbSO+4Cl-,D错误。]
4
2.(2020·山东师大附中三模)以铜银合金(含少量铁)废料为原料回收银和铜的工艺流程
如下,下列说法正确的是( )A.粗铜溶于过量稀硝酸,过滤、低温干燥得纯铜
B.电解时用粗银作阴极,硝酸银溶液为电解质溶液
C.用稀硫酸处理渣料时主要发生了氧化还原反应
D.从滤液B中可以提取绿矾(FeSO ·7H O)
4 2
D [Cu可溶于过量稀硝酸,故粗铜溶于过量稀硝酸,过滤、低温干燥不能得到纯铜,A
项错误;电解粗银时,用粗银作阳极,纯银作阴极,硝酸银溶液为电解质溶液,B项错误;铜银
合金(含少量铁)在高温下与空气中O 反应生成CuO、Fe O ,用稀硫酸处理渣料时,生成
2 3 4
CuSO 、FeSO 和Fe (SO ),发生非氧化还原反应,C项错误;滤液A中含有CuSO 、FeSO 和
4 4 2 4 3 4 4
Fe (SO ) ,加入适量铁粉过滤,滤液 B 中含有 FeSO ,故从滤液 B 中可以提取绿矾
2 4 3 4
(FeSO ·7HO),D项正确。]
4 2
3.(2021·江西南昌二中检测)明矾[KAl(SO)·12H O]是一种重要的化工产品,在生产、生
4 2 2
活中都有广泛的用途。某工厂计划利用炼铝厂的废料铝灰(含Al、Al O 、少量SiO 和
2 3 2
FeO·xFe O)为原料生产明矾产品,设计的生产工艺流程如下:
2 3
已知:K [Fe(OH) ]=1.0×10-36
sp 3
请回答下列问题:
(1)检验滤液A中是否存在Fe2+,可用K[Fe(CN) ]溶液,请写出其检验的离子反应方程
3 6
式________________________________________________________________________。
(2)沉淀器中加入KMnO 溶液的作用是_________________________________________;
4
有人认为该生产流程较为复杂,可以用溶液______________________________(填化学
式)
代替KMnO 溶液而使操作Ⅰ和操作Ⅱ过程得到优化。
4
(3)操作Ⅲ是________、________(填操作名称)、过滤、洗涤;在洗涤晶体时采用的洗涤剂
最合适的是________(填正确答案标号)。
A.稀硫酸 B.蒸馏水 C.70%酒精
(4)明矾可作净水剂,其净水原理是_______________________________________(用离
子方程式表示)。
(5)在沉淀器中调pH=3,请计算说明Fe3+是否完全沉淀_________________________。
(当Fe3+离子浓度小于或等于1.0×10-5 mol/L时,可以认为溶液中无该离子)。
解析 (2)铝灰含Al、Al O、少量SiO 和FeO·xFe O,加入稀硫酸浸出,滤液A中含有
2 3 2 2 3
Al3+、Fe2+、Fe3+;沉淀器中加入KMnO 溶液,将Fe2+氧化为Fe3+,并调节pH=3,转化为
4Fe(OH) 沉淀。原流程中为了除去Fe2+,加入KMnO 引入了MnO,后又加入MnSO ,过于复
3 4 4
杂,用HO 不引入新杂质。
2 2
答案 (1)2[Fe(CN) ]3-+3Fe2+===Fe [Fe(CN) ]↓
6 3 6 2
(2)将Fe2+氧化成Fe3+ HO
2 2
(3)蒸发浓缩 冷却结晶 C
(4)Al3++3H
2
O⇌Al(OH)
3
(胶体)+3H+
(5)由K [Fe(OH) ]=c3(OH-)·c(Fe3+)=1.0×10-36可计算c(Fe3+)=1.0×10-3 mol·L-1>
sp 3
1.0×10-5 mol·L-1,所以Fe3+没有沉淀完全
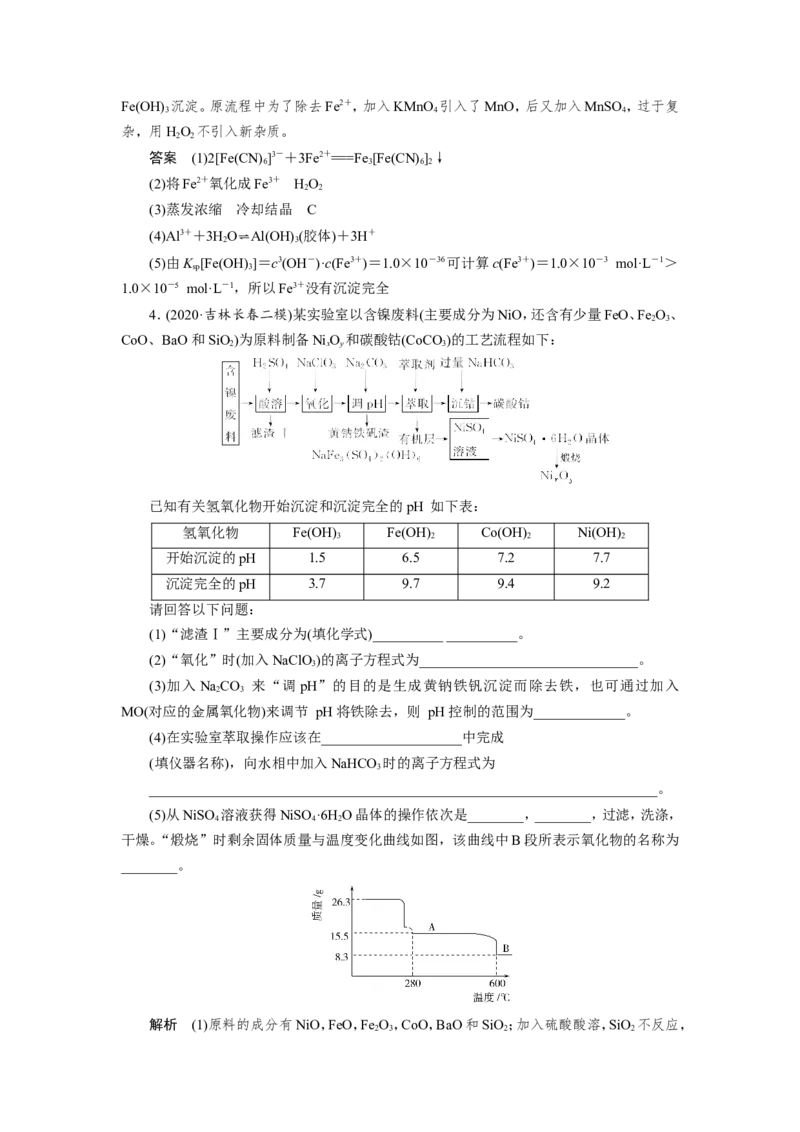
4.(2020·吉林长春二模)某实验室以含镍废料(主要成分为NiO,还含有少量FeO、Fe O、
2 3
CoO、BaO 和SiO)为原料制备NiO 和碳酸钴(CoCO)的工艺流程如下:
2 x y 3
已知有关氢氧化物开始沉淀和沉淀完全的pH 如下表:
氢氧化物 Fe(OH) Fe(OH) Co(OH) Ni(OH)
3 2 2 2
开始沉淀的pH 1.5 6.5 7.2 7.7
沉淀完全的pH 3.7 9.7 9.4 9.2
请回答以下问题:
(1)“滤渣Ⅰ”主要成分为(填化学式)__________ __________。
(2)“氧化”时(加入NaClO)的离子方程式为_______________________________。
3
(3)加入NaCO 来“调pH”的目的是生成黄钠铁钒沉淀而除去铁,也可通过加入
2 3
MO(对应的金属氧化物)来调节 pH 将铁除去,则 pH 控制的范围为_____________。
(4)在实验室萃取操作应该在____________________中完成
(填仪器名称),向水相中加入NaHCO 时的离子方程式为
3
________________________________________________________________________。
(5)从NiSO 溶液获得NiSO ·6H O晶体的操作依次是________,________,过滤,洗涤,
4 4 2
干燥。“煅烧”时剩余固体质量与温度变化曲线如图,该曲线中B段所表示氧化物的名称为
________。
解析 (1)原料的成分有NiO,FeO,Fe O,CoO,BaO和SiO;加入硫酸酸溶,SiO 不反应,
2 3 2 2所以会出现在滤渣中,BaO会最终变成BaSO 沉淀,所以也会出现在滤渣中;
4
(2)氧化步骤的目的是将二价铁转变成三价铁,便于在后续步骤中沉淀法除去,所以离子
方程式为6H++ClO+6Fe2+===6Fe3++Cl-+3HO;
2
(3)加入NaCO 这一步是为了除去铁,同时也要避免其他元素的损耗,所以选择的pH区
2 3
间为3.7~7.2;
(4)萃取最关键的仪器是分液漏斗;加入碳酸氢钠后,产物之一是CoCO 沉淀,考虑到
3
NaHCO 是过量的,所以最终的离子方程式为2HCO+Co2+===CoCO ↓+HO+CO↑;
3 3 2 2
(5)由溶液获取结晶的常规操作是:蒸发浓缩,冷却结晶,过滤洗涤干燥;硫酸镍晶体的摩
尔质量是263 g/mol,所以26.3 g即为0.1 mol;280 ℃开始,固体的质量减少,这个时期是因为
结晶水丢失导致的,所以A段对应的物质就是0.1 mol的NiSO ;温度到600 ℃,固体的质量
4
再次下降,得到最终的镍的氧化物;根据原子守恒,8.3 g氧化物中Ni的质量为5.9 g,那么O
的质量为2.4 g即0.15 mol,所以固体氧化物中n(Ni)∶n(O)=2∶3,所以固体氧化物即三氧
化二镍。
答案 (1)BaSO 和SiO
4 2
(2)6H++ClO+6Fe2+===6Fe3++Cl-+3HO
2
(3)3.7