文档内容
章末综合检测(六) 化学反应与能量
一、选择题:本题包括10小题,每小题只有一个选项最符合题意。
1.(2021·山西太原调研)在25 ℃ 101 kPa时,下列关于反应热的说法不正确的是( )
A.1 mol 钠与2 mol 钠完全燃烧时,燃烧热相同
B.CO(g)的燃烧热 ΔH=-283.0 kJ/mol,则 2CO(g)+O(g)===2CO (g)的 ΔH=-
2 2
(2×283.0)kJ/mol
C.在稀溶液中:H+(aq)+OH-(aq)===H O(l) ΔH=-57.3 kJ/mol,若将含1 mol HNO 的
2 3
稀溶液与含1 mol Ba(OH) 的稀溶液混合,放出的热量为57.3 kJ
2
D.2 g H 完全燃烧生成液态水,放出285.8 kJ热量,氢气燃烧的热化学方程式可表示为
2
2H(g)+O(g)===2H O(l) ΔH=-285.8 kJ/mol
2 2 2
D [燃烧热是以1 mol 物质完全燃烧生成稳定氧化物放出的热量为基准,故1 mol 钠与
2 mol 钠完全燃烧时,燃烧热相同,A项正确;CO(g)的燃烧热ΔH=-283.0 kJ/mol,则2 mol
CO(g)完全燃烧放出热量为2×283.0 kJ,热化学方程式为2CO(g)+O(g)===2CO (g)的ΔH=
2 2
-(2×283.0)kJ/mol,B项正确;含1 mol HNO 的稀溶液与含1 mol Ba(OH) 的稀溶液混合生
3 2
成1 mol H O(l),故放出的热量为57.3 kJ,C项正确;2 g H 为1 mol,完全燃烧生成液态水,放
2 2
出285.8 kJ热量,则氢气燃烧的热化学方程式可表示为 2H(g)+O(g)===2H O(l) ΔH=-
2 2 2
571.6 kJ/mol,D项错误。]
2.(2021·浙江东阳调研)根据能量变化示意图,下列热化学方程式正确的是( )
A.N(g)+3H(g)===2NH(g) ΔH=-(b-a)kJ·mol-1
2 2 3
B.N(g)+3H(g)===2NH(g) ΔH=-(a-b)kJ·mol-1
2 2 3
C.2NH (l)===N (g)+3H(g) ΔH=2(a+b-c)kJ·mol-1
3 2 2
D.2NH (l)===N (g)+3H(g) ΔH=2(b+c-a)kJ·mol-1
3 2 2
D [由图可知,0.5 mol N(g)+1.5mol H (g)→1 mol NH (g)断键吸收a kJ热量,成键释
2 2 3
放b kJ热量,据此可得热化学方程式:N(g)+3H(g)===2NH(g) ΔH=-2(b-a)kJ·mol-1,
2 2 3
A、B项均错误;逆向分析,1 mol NH (l)→1 mol NH (g)吸收c kJ热量,1 mol NH (g)→1
3 3 3
mol N+3 mol H 吸收b kJ热量,1 mol N+3 mol H →0.5 mol N(g)+1.5 mol H(g)放出a kJ
2 2
热量,据此可得1 mol NH (l)→0.5 mol N(g)+1.5 mol H(g)要吸收(b+c-a) kJ热量,据此可
3 2 2
得热化学方程式:2NH (l)===N (g)+3H(g) ΔH=2(b+c-a)kJ·mol-1,D项正确,C项错误。]
3 2 2
3.(2021·广东惠州检测)下图是某同学设计的原电池装置,下列叙述中正确的是( )A.氧化剂和还原剂必须直接接触才能发生反应
B.电极Ⅱ上发生还原反应,作原电池的正极
C.该原电池的总反应式为2Fe3++Cu===Cu2++2Fe2+
D.盐桥中装有含氯化钾的琼脂,K+移向负极区
C [双液原电池中,氧化剂在正极区,还原剂在负极区,并非直接接触,A项错误;Pt电
极是惰性电极,则电极Ⅱ(Cu)是负极,发生氧化反应,B项错误;负极上Cu被氧化生成Cu2+,
正极上Fe3+被还原生成Fe2+,则电池总反应式为:2Fe3++Cu===Cu2++2Fe2+,C项正确;原
电池中,阳离子向正极区移动,则盐桥中K+移向正极区,D项错误。]
4.(2021·江苏南京学情调研)保护海水中钢闸门的一种方法如图所示。下列说法不正确
的是( )
A.锌板作牺牲阳极
B.钢闸门作正极(阴极)
C.锌板发生的电极反应式为Zn-2e-===Zn2+
D.电子由钢闸门向锌板移动
D [钢闸门与锌板相连浸泡在海水中,形成原电池,采取牺牲阳极法,锌板作负极,即牺
牲阳极,钢闸门作正极(阴极),A、B项正确;锌板是负极,被氧化生成Zn2+,C项正确;原电池
中电子由负极流向正极,则电子由锌板向钢闸门移动,D项错误。]
5.(2021·湖北武汉联考)环己酮(O)在生产生活中有重要的用途,可在酸性溶液中用环己
醇间接电解氧化法制备,其原理如图所示。下列说法正确的是( )
A.a 极与电源负极相连
B.a 极电极反应式是 2Cr3+-6e-+14OH-===Cr O+7HO
2 2
C.b 极发生氧化反应
D.理论上生成 1 mol 环己酮时,有 1 mol H 生成
2
D [根据原理图可知,a极为电解池的阳极,Cr3+失电子发生氧化反应,电极反应式是2Cr3++7HO-6e-===Cr O+14H+,b极为阴极,氢离子得电子发生还原反应生成氢气,结合
2 2
转移电子数相等计算。由上述分析可知,A、B、C项错误;理论上由环己醇(C H O)生成1 mol
6 12
环己酮(C H O),转移2 mol电子,根据电子守恒可知,阴极有1 mol氢气放出,D项正确。]
6 10
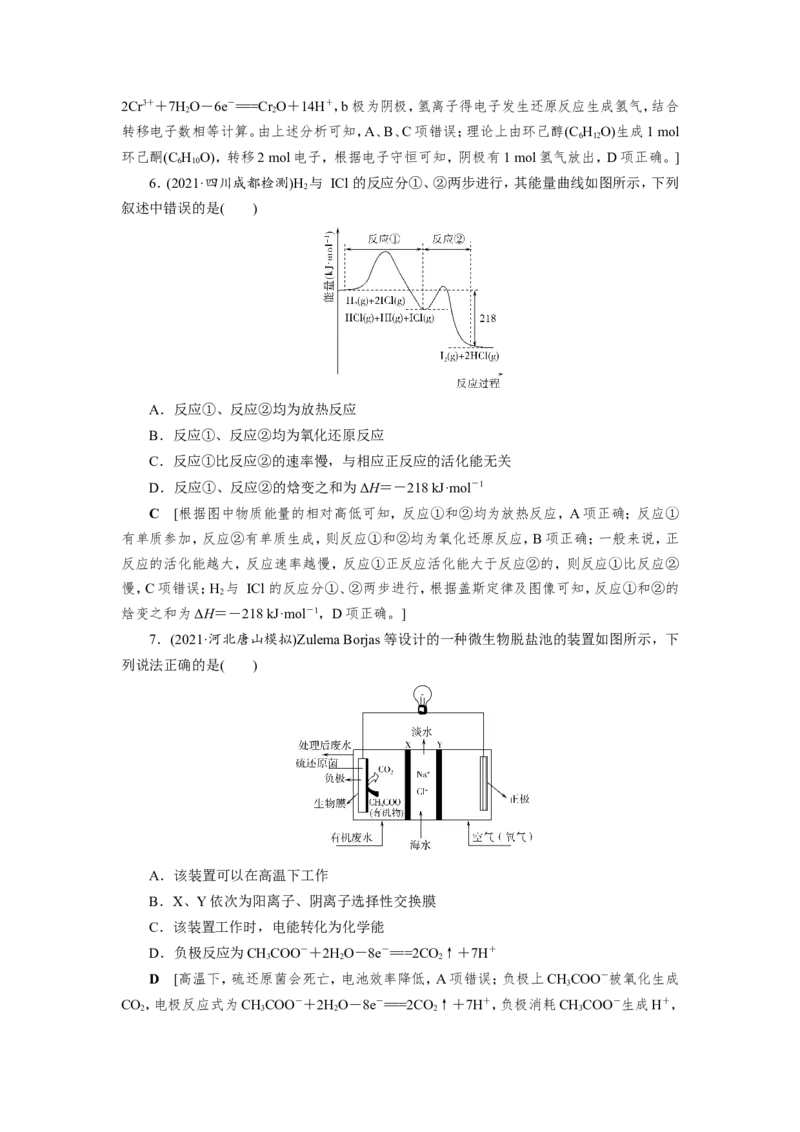
6.(2021·四川成都检测)H 与 ICl 的反应分①、②两步进行,其能量曲线如图所示,下列
2
叙述中错误的是( )
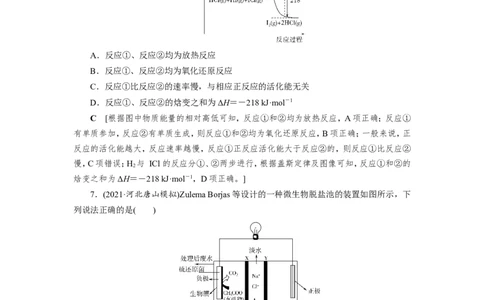
A.反应①、反应②均为放热反应
B.反应①、反应②均为氧化还原反应
C.反应①比反应②的速率慢,与相应正反应的活化能无关
D.反应①、反应②的焓变之和为ΔH=-218 kJ·mol-1
C [根据图中物质能量的相对高低可知,反应①和②均为放热反应,A项正确;反应①
有单质参加,反应②有单质生成,则反应①和②均为氧化还原反应,B项正确;一般来说,正
反应的活化能越大,反应速率越慢,反应①正反应活化能大于反应②的,则反应①比反应②
慢,C项错误;H 与 ICl 的反应分①、②两步进行,根据盖斯定律及图像可知,反应①和②的
2
焓变之和为ΔH=-218 kJ·mol-1,D项正确。]
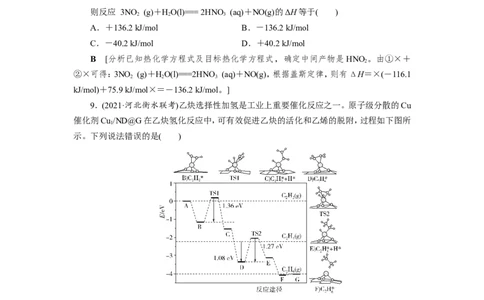
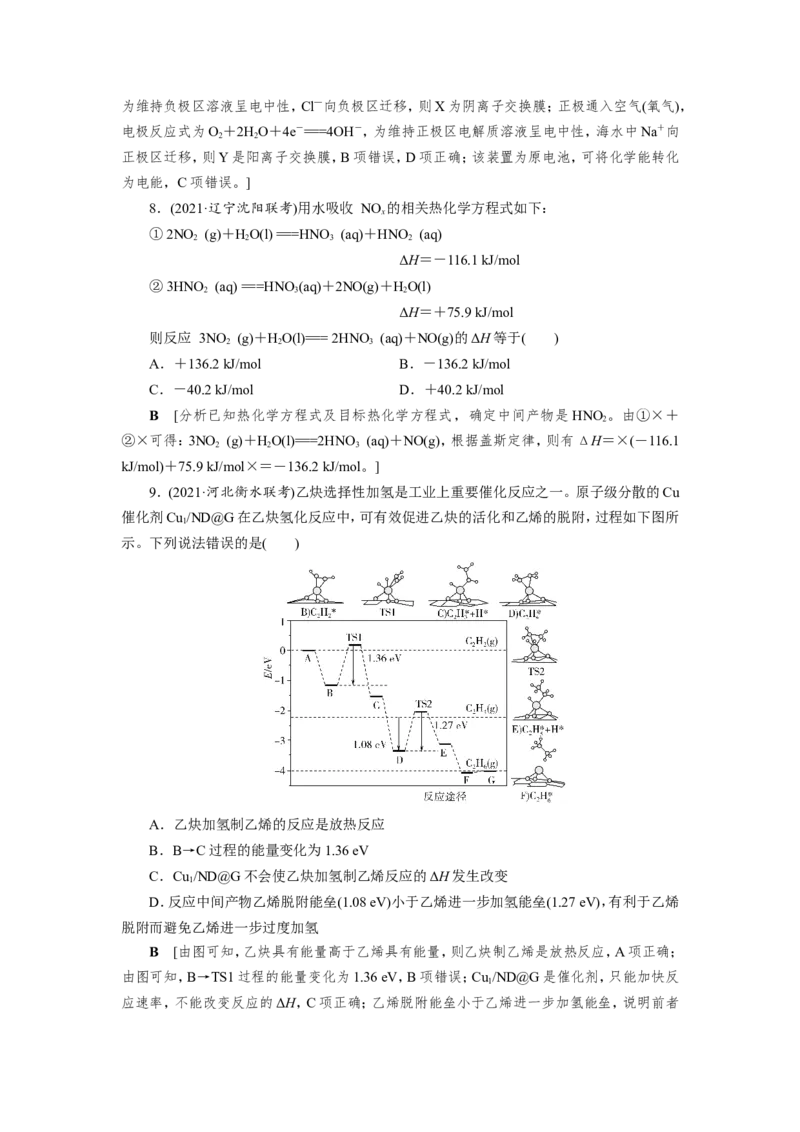
7.(2021·河北唐山模拟)Zulema Borjas等设计的一种微生物脱盐池的装置如图所示,下
列说法正确的是( )
A.该装置可以在高温下工作
B.X、Y依次为阳离子、阴离子选择性交换膜
C.该装置工作时,电能转化为化学能
D.负极反应为CHCOO-+2HO-8e-===2CO ↑+7H+
3 2 2
D [高温下,硫还原菌会死亡,电池效率降低,A项错误;负极上CHCOO-被氧化生成
3
CO,电极反应式为CHCOO-+2HO-8e-===2CO ↑+7H+,负极消耗CHCOO-生成H+,
2 3 2 2 3为维持负极区溶液呈电中性,Cl—向负极区迁移,则X为阴离子交换膜;正极通入空气(氧气),
电极反应式为O+2HO+4e-===4OH-,为维持正极区电解质溶液呈电中性,海水中Na+向
2 2
正极区迁移,则Y是阳离子交换膜,B项错误,D项正确;该装置为原电池,可将化学能转化
为电能,C项错误。]
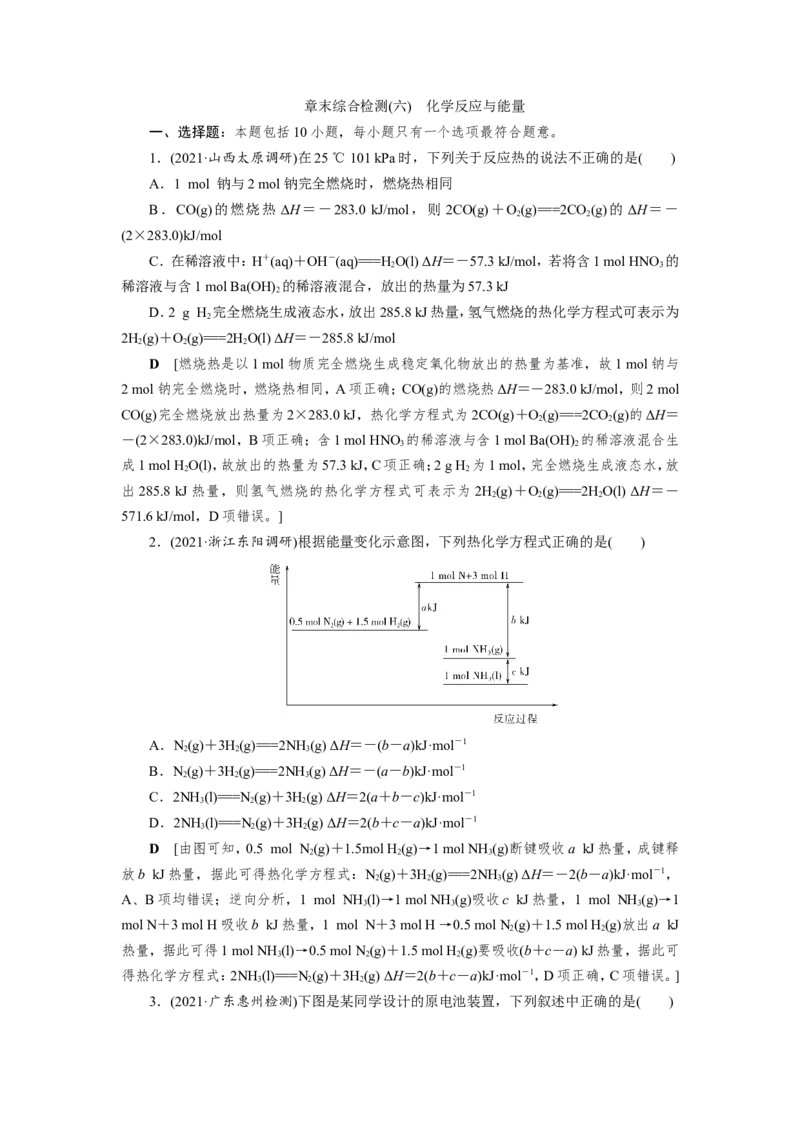
8.(2021·辽宁沈阳联考)用水吸收 NO 的相关热化学方程式如下:
x
①2NO (g)+HO(l) ===HNO (aq)+HNO (aq)
2 2 3 2
ΔH=-116.1 kJ/mol
②3HNO (aq) ===HNO (aq)+2NO(g)+HO(l)
2 3 2
ΔH=+75.9 kJ/mol
则反应 3NO (g)+HO(l)=== 2HNO (aq)+NO(g)的ΔH等于( )
2 2 3
A.+136.2 kJ/mol B.-136.2 kJ/mol
C.-40.2 kJ/mol D.+40.2 kJ/mol
B [分析已知热化学方程式及目标热化学方程式,确定中间产物是HNO 。由①×+
2
②×可得:3NO (g)+HO(l)===2HNO (aq)+NO(g),根据盖斯定律,则有ΔH=×(-116.1
2 2 3
kJ/mol)+75.9 kJ/mol×=-136.2 kJ/mol。]
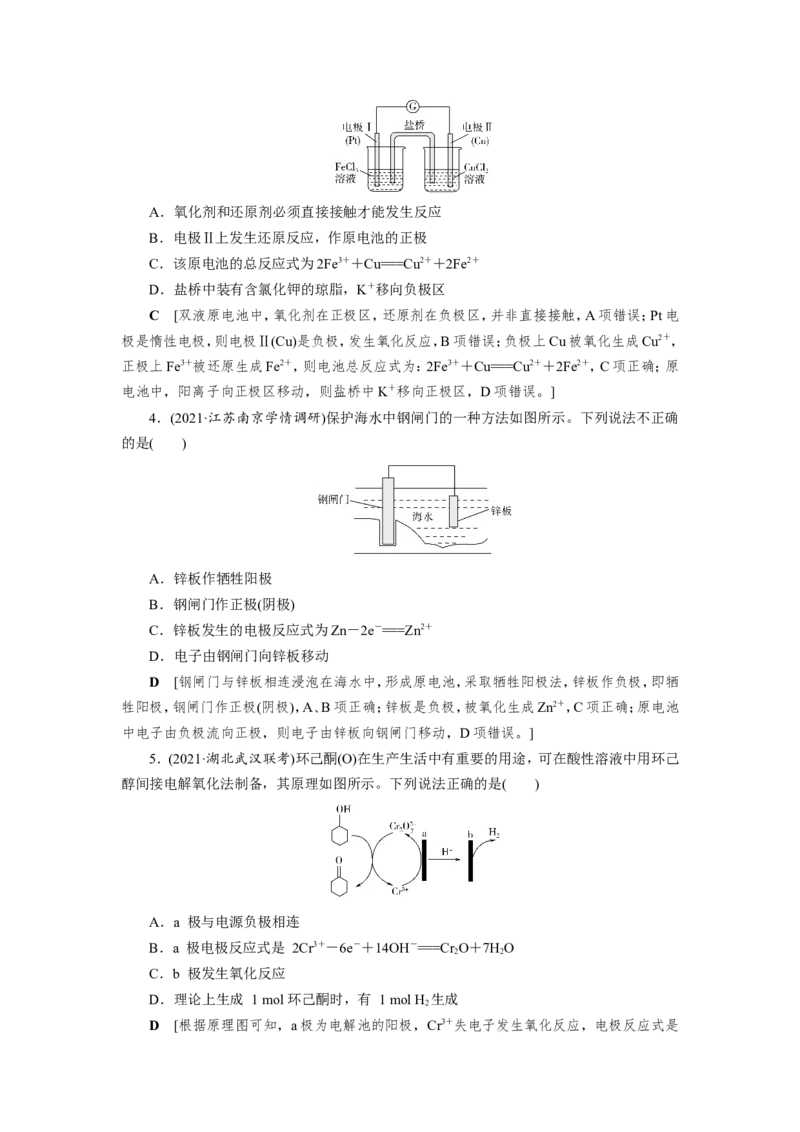
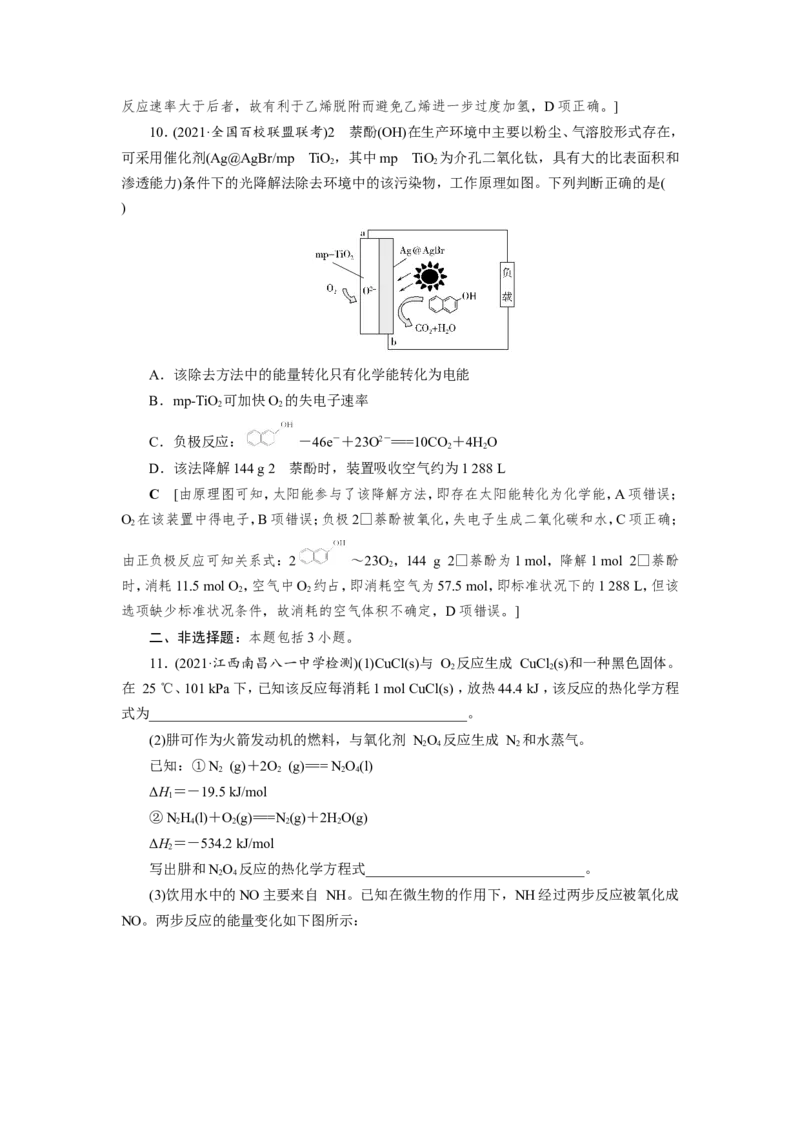
9.(2021·河北衡水联考)乙炔选择性加氢是工业上重要催化反应之一。原子级分散的Cu
催化剂Cu /ND@G在乙炔氢化反应中,可有效促进乙炔的活化和乙烯的脱附,过程如下图所
1
示。下列说法错误的是( )
A.乙炔加氢制乙烯的反应是放热反应
B.B→C过程的能量变化为1.36 eV
C.Cu /ND@G不会使乙炔加氢制乙烯反应的ΔH发生改变
1
D.反应中间产物乙烯脱附能垒(1.08 eV)小于乙烯进一步加氢能垒(1.27 eV),有利于乙烯
脱附而避免乙烯进一步过度加氢
B [由图可知,乙炔具有能量高于乙烯具有能量,则乙炔制乙烯是放热反应,A项正确;
由图可知,B→TS1过程的能量变化为1.36 eV,B项错误;Cu /ND@G是催化剂,只能加快反
1
应速率,不能改变反应的ΔH,C项正确;乙烯脱附能垒小于乙烯进一步加氢能垒,说明前者反应速率大于后者,故有利于乙烯脱附而避免乙烯进一步过度加氢,D项正确。]
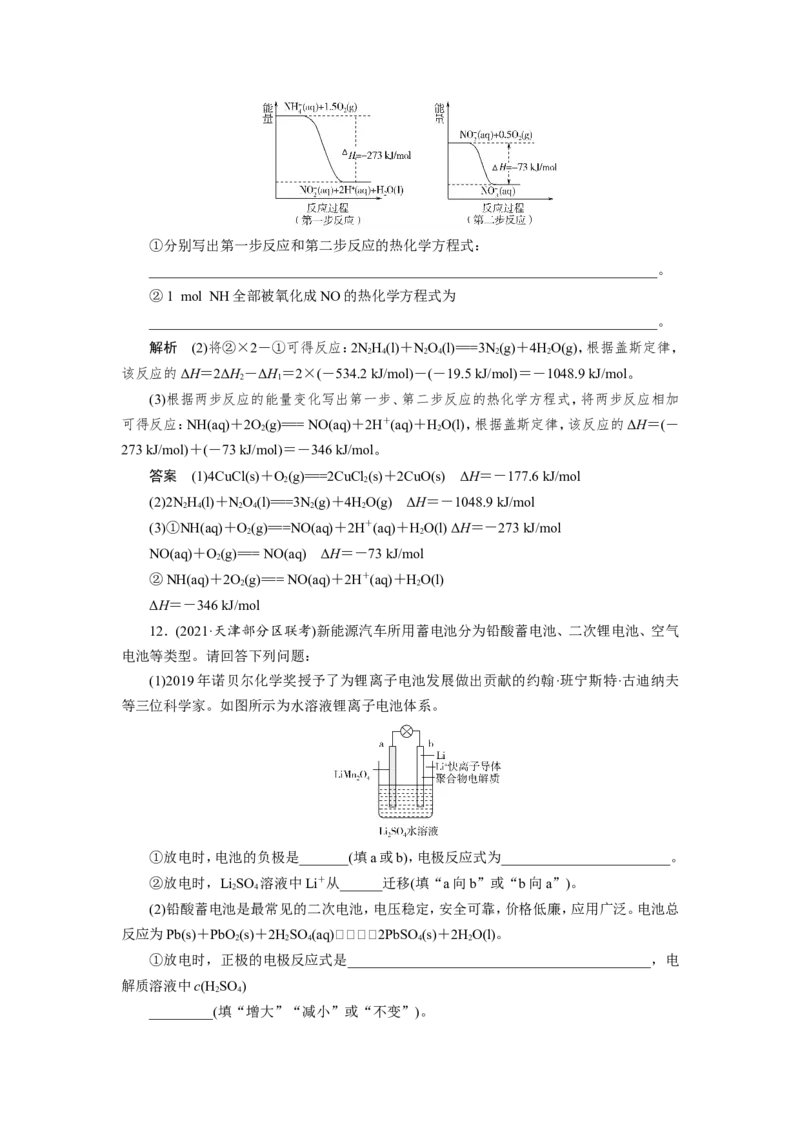
10.(2021·全国百校联盟联考)2萘酚(OH)在生产环境中主要以粉尘、气溶胶形式存在,
可采用催化剂(Ag@AgBr/mpTiO,其中mpTiO 为介孔二氧化钛,具有大的比表面积和
2 2
渗透能力)条件下的光降解法除去环境中的该污染物,工作原理如图。下列判断正确的是(
)
A.该除去方法中的能量转化只有化学能转化为电能
B.mp-TiO 可加快O 的失电子速率
2 2
C.负极反应: -46e-+23O2-===10CO +4HO
2 2
D.该法降解144 g 2萘酚时,装置吸收空气约为1 288 L
C [由原理图可知,太阳能参与了该降解方法,即存在太阳能转化为化学能,A项错误;
O 在该装置中得电子,B项错误;负极2萘酚被氧化,失电子生成二氧化碳和水,C项正确;
2
由正负极反应可知关系式:2 ~23O,144 g 2萘酚为1 mol,降解1 mol 2萘酚
2
时,消耗11.5 mol O ,空气中O 约占,即消耗空气为57.5 mol,即标准状况下的1 288 L,但该
2 2
选项缺少标准状况条件,故消耗的空气体积不确定,D项错误。]
二、非选择题:本题包括3小题。
11.(2021·江西南昌八一中学检测)(1)CuCl(s)与 O 反应生成 CuCl (s)和一种黑色固体。
2 2
在 25 ℃、101 kPa 下,已知该反应每消耗1 mol CuCl(s) ,放热44.4 kJ ,该反应的热化学方程
式为_____________________________________________。
(2)肼可作为火箭发动机的燃料,与氧化剂 NO 反应生成 N 和水蒸气。
2 4 2
已知:①N (g)+2O (g)=== N O(l)
2 2 2 4
ΔH=-19.5 kJ/mol
1
②NH(l)+O(g)===N (g)+2HO(g)
2 4 2 2 2
ΔH=-534.2 kJ/mol
2
写出肼和NO 反应的热化学方程式_______________________________。
2 4
(3)饮用水中的NO主要来自 NH。已知在微生物的作用下,NH经过两步反应被氧化成
NO。两步反应的能量变化如下图所示:①分别写出第一步反应和第二步反应的热化学方程式:
________________________________________________________________________。
②1 mol NH全部被氧化成NO的热化学方程式为
________________________________________________________________________。
解析 (2)将②×2-①可得反应:2NH(l)+NO(l)===3N (g)+4HO(g),根据盖斯定律,
2 4 2 4 2 2
该反应的ΔH=2ΔH-ΔH=2×(-534.2 kJ/mol)-(-19.5 kJ/mol)=-1048.9 kJ/mol。
2 1
(3)根据两步反应的能量变化写出第一步、第二步反应的热化学方程式,将两步反应相加
可得反应:NH(aq)+2O(g)=== NO(aq)+2H+(aq)+HO(l),根据盖斯定律,该反应的ΔH=(-
2 2
273 kJ/mol)+(-73 kJ/mol)=-346 kJ/mol。
答案 (1)4CuCl(s)+O(g)===2CuCl (s)+2CuO(s) ΔH=-177.6 kJ/mol
2 2
(2)2N H(l)+NO(l)===3N (g)+4HO(g) ΔH=-1048.9 kJ/mol
2 4 2 4 2 2
(3)①NH(aq)+O(g)===NO(aq)+2H+(aq)+HO(l) ΔH=-273 kJ/mol
2 2
NO(aq)+O(g)=== NO(aq) ΔH=-73 kJ/mol
2
②NH(aq)+2O(g)=== NO(aq)+2H+(aq)+HO(l)
2 2
ΔH=-346 kJ/mol
12.(2021·天津部分区联考)新能源汽车所用蓄电池分为铅酸蓄电池、二次锂电池、空气
电池等类型。请回答下列问题:
(1)2019年诺贝尔化学奖授予了为锂离子电池发展做出贡献的约翰·班宁斯特·古迪纳夫
等三位科学家。如图所示为水溶液锂离子电池体系。
①放电时,电池的负极是_______(填a或b),电极反应式为________________________。
②放电时,LiSO 溶液中Li+从______迁移(填“a向b”或“b向a”)。
2 4
(2)铅酸蓄电池是最常见的二次电池,电压稳定,安全可靠,价格低廉,应用广泛。电池总
反应为Pb(s)+PbO (s)+2HSO (aq)2PbSO (s)+2HO(l)。
2 2 4 4 2
①放电时,正极的电极反应式是___________________________________________,电
解质溶液中c(H SO )
2 4
_________(填“增大”“减小”或“不变”)。②用该蓄电池作电源,进行粗铜(含Ag、Pt、Au等杂质)的电解精炼。如图所示,电解液c
选用____________溶液,A电极的材料是_______,B电极反应式是___________________。
③用该蓄电池作电源,A、B为石墨电极,c为氯化钠溶液,进行电解。如上图所示,则A
电极产生的气体是________,B电极的电极反应式为____________________________。
解析 (1)Li是活泼金属,放电时,Li作负极被氧化为Li+,电极反应为Li-e-===Li+。
LiSO 溶液中Li+向负极移动。
2 4
(2)① 放电时,PbO 在正极发生还原反应,电极反应式为 PbO +4H++SO+2e-
2 2
===PbSO+2HO,反应中消耗HSO ,溶液中c(H SO )减小。
4 2 2 4 2 4
②根据图中电流的流向判断,A是阳极,B是阴极。电解精炼粗铜时,粗铜作阳极,纯铜
作阴极,电解液是CuSO 或CuCl 等。
4 2
③电解氯化钠溶液,A电极是阳极,Cl-放电产生Cl;B电极是阴极,电极反应式为2HO
2 2
+2e-===2OH-+H↑。
2
答案 (1)①b Li-e-===Li+ ②b向a
(2)①PbO +4H++SO+2e-===PbSO+2HO 减小
2 4 2
②CuSO (或CuCl 等) 粗铜 Cu2++2e-===Cu
4 2
③Cl 2HO+2e-===2OH-+H↑
2 2 2
13.(2021·贵州铜仁一中检测)某化学兴趣小组的同学用如下图所示装置研究有关电化
学的问题。当闭合K时,观察到电流表的指针发生了偏移。
请回答下列问题:
(1)乙装置的名称是________;Zn为________极。
(2)写出电极反应:Cu极:___________________________________;
石墨棒极:______________________。
(3)当甲中产生0.1 mol气体时,乙中产生的气体在标准状况下的体积应为________。
(4)若乙中溶液不变,将其电极都换成铜电极,闭合K一段时间后,乙中溶液的颜色
________(填“变深”“变浅”或“不变”)。
(5)若乙中电极不变,将其溶液换成NaCl溶液,闭合K一段时间后,甲中溶液的pH将________(填“增大”“减小”或“不变”,下同);乙中溶液的pH将________。
(6)若乙中电极不变,将其溶液换成饱和NaSO 溶液,闭合K一段时间,当阴极上有a
2 4
mol气体生成时,同时有ω g Na SO ·10H O析出,假设温度不变,剩余溶液中溶质的质量分
2 4 2
数应为__________________(用含ω、a的表达式表示,不必化简)。
解析 (1)乙中Pt、石墨棒都是惰性电极,甲中Zn和Cu都是活性电极,则甲是原电池,
Zn是负极,Cu是正极;乙是电解池,Pt是阳极,石墨棒是阴极。
(2)甲中电解液是稀硫酸,Cu极的电极反应式为2H++2e-===H ↑;石墨棒阴极上Cu2+
2
发生还原反应,电极反应式为Cu2++2e-===Cu。
(3)甲中Cu电极产生H,产生0.1 mol气体时,电路中通过0.2 mol电子;乙中Pt电极反
2
应式为2Cl--2e-===Cl↑,则转移0.2 mol 电子时生成0.1 mol Cl ,在标准状况下的体积为
2 2
2.24 L。
(4)铜电极是活性电极,乙为电镀池,在石墨棒上电镀铜,电解液中c(Cu2+)不变,则乙中
溶液的颜色不变。
(5)甲中电池总反应为Zn+2H+===Zn2++H↑,溶液的pH增大;乙中电极不变,将其溶
2
液换成NaCl溶液,电池总反应为 2NaCl+2HO=====2NaOH+H↑+Cl↑,反应生成
2 2 2
NaOH,溶液的pH增大。
(6)利用惰性电极电解饱和NaSO 溶液,电池总反应式为2HO=====2H↑+O↑,阴极
2 4 2 2 2
上析出H,则阴极上有a mol气体生成时,消耗a mol HO,同时有ω g NaSO ·10HO析
2 2 2 4 2
出,剩余溶液仍为饱和 NaSO 溶液,故a mol HO和ω g NaSO ·10HO也形成饱和
2 4 2 2 4 2
NaSO 溶液,ω g NaSO ·10HO中含有NaSO 的质量为 g,因此剩余溶液中溶质的质量
2 4 2 4 2 2 4
分数为 =×100%。
答案 (1)电解池 负 (2)2H++2e-===H ↑ Cu2++2e-===Cu
2
(3)2.24 L (4)不变
(5)增大 增大 (6)×100%