文档内容
专题突破(八) 突破酸碱中和图像中的五个关键点
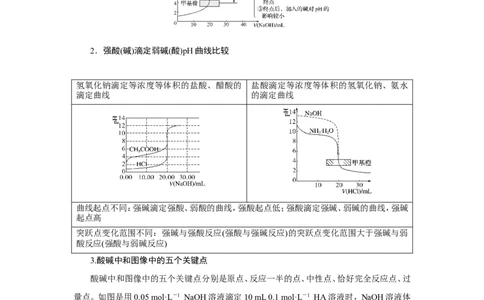
1.图示强酸与强碱滴定过程中pH曲线
(以0.100 0 mol·L-1 NaOH溶液滴定20.00 mL 0.100 0 mol·L-1盐酸为例)
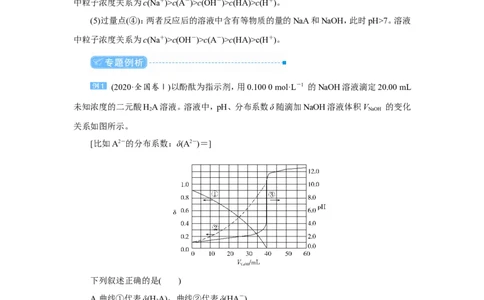
2.强酸(碱)滴定弱碱(酸)pH曲线比较
氢氧化钠滴定等浓度等体积的盐酸、醋酸的 盐酸滴定等浓度等体积的氢氧化钠、氨水
滴定曲线 的滴定曲线
曲线起点不同:强碱滴定强酸、弱酸的曲线,强酸起点低;强酸滴定强碱、弱碱的曲线,强碱
起点高
突跃点变化范围不同:强碱与强酸反应(强酸与强碱反应)的突跃点变化范围大于强碱与弱
酸反应(强酸与弱碱反应)
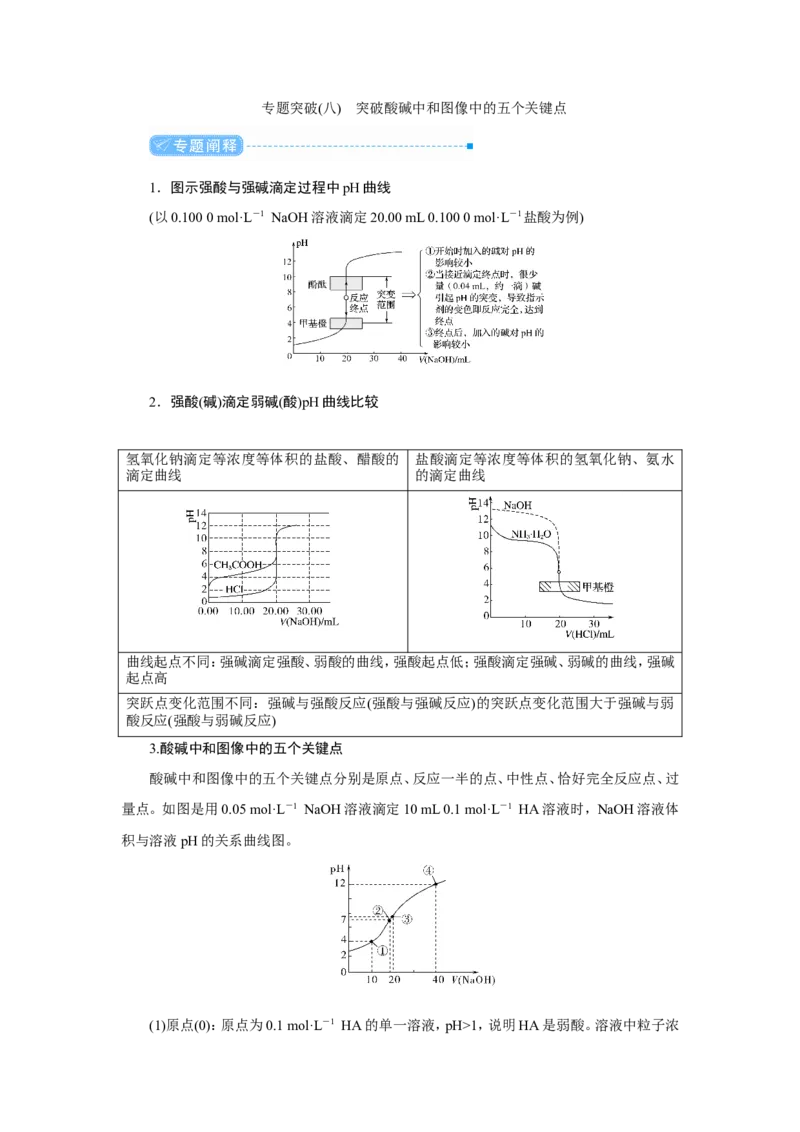
3.酸碱中和图像中的五个关键点
酸碱中和图像中的五个关键点分别是原点、反应一半的点、中性点、恰好完全反应点、过
量点。如图是用0.05 mol·L-1 NaOH溶液滴定10 mL 0.1 mol·L-1 HA溶液时,NaOH溶液体
积与溶液pH的关系曲线图。
(1)原点(0):原点为0.1 mol·L-1 HA的单一溶液,pH>1,说明HA是弱酸。溶液中粒子浓度关系为c(HA)>c(H+)>c(A-)>c(OH-)。
(2)反应一半的点(①):两者反应后的溶液中含有等物质的量的NaA和HA,此时pH<7,
说明 HA 的电离大于 NaA 的水解。溶液中粒子浓度关系为 c(A-)>c(Na+)>c(HA)>c(H
+)>c(OH-)。
(3)中性点(②):两者反应后的溶液中含有NaA溶液和过量的HA溶液,此时pH=7,溶
液中粒子浓度关系为c(A-)=c(Na+)>c(HA)>c(H+)=c(OH-)。
(4)恰好反应点(③):两者恰好完全反应生成NaA,NaA为强碱弱酸盐,水解呈碱性。溶液
中粒子浓度关系为c(Na+)>c(A-)>c(OH-)>c(HA)>c(H+)。
(5)过量点(④):两者反应后的溶液中含有等物质的量的NaA和NaOH,此时pH>7。溶液
中粒子浓度关系为c(Na+)>c(OH-)>c(A-)>c(HA)>c(H+)。
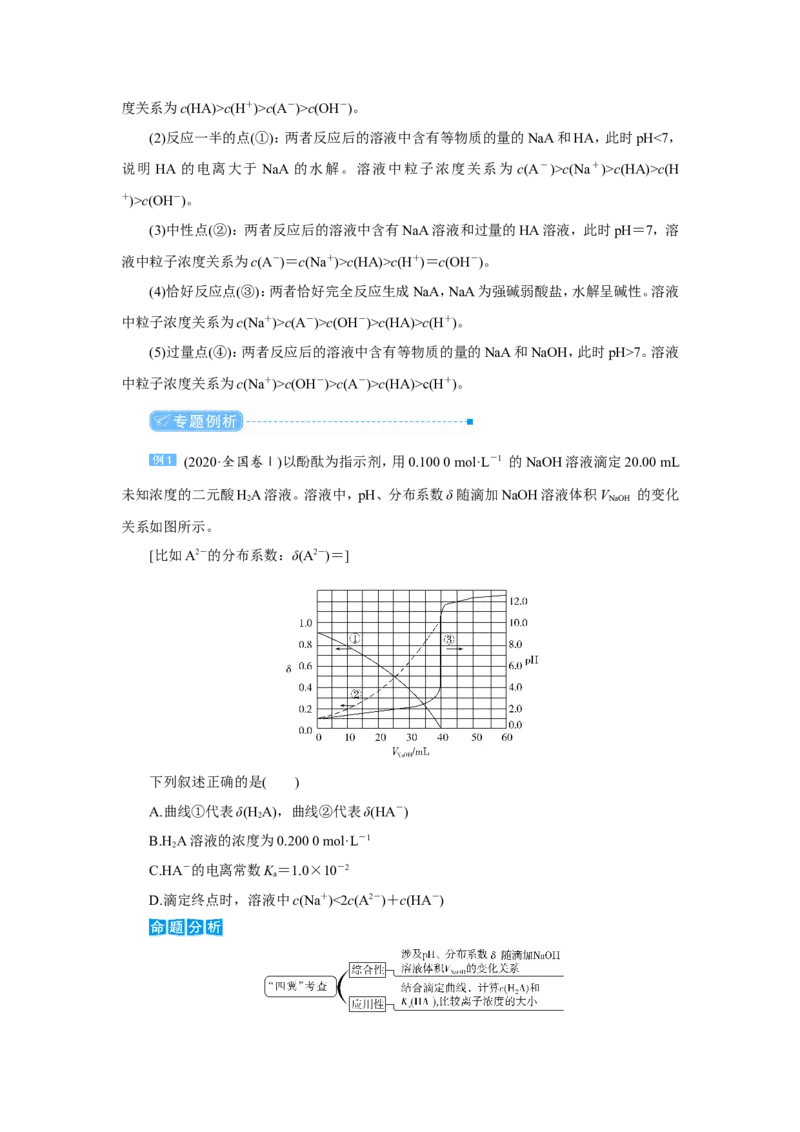
(2020·全国卷Ⅰ)以酚酞为指示剂,用0.100 0 mol·L-1 的NaOH溶液滴定20.00 mL
未知浓度的二元酸HA溶液。溶液中,pH、分布系数δ随滴加NaOH溶液体积V 的变化
2 NaOH
关系如图所示。
[比如A2-的分布系数:δ(A2-)=]
下列叙述正确的是( )
A.曲线①代表δ(H A),曲线②代表δ(HA-)
2
B.H A溶液的浓度为0.200 0 mol·L-1
2
C.HA-的电离常数K=1.0×10-2
a
D.滴定终点时,溶液中c(Na+)<2c(A2-)+c(HA-)C [根据题干信息并结合图中分布系数和pH变化可知,HA为二元酸,且第一步完全
2
电离,又因滴定终点附近pH曲线突跃明显,故HA-的酸性较强。曲线①代表δ(HA-),曲线②
代表δ(A2-),A项错误;根据HA为二元酸,HA和NaOH按物质的量之比为1∶2完全反应,
2 2
故c(H A)=0.100 0 mol·L-1,B项错误;当加入25.00 mL NaOH溶液时,c(HA-)=c(A2-),此
2
时pH=2.0,故K=c(H+),故K=1.0×10-2,C项正确;根据电荷守恒c(H+)+c(Na+)=c(OH
a a
-)+c(HA-)+2c(A2-),又因滴定终点时溶质为NaA,A2-水解使溶液显碱性,则c(H+)c(HA-)+2c(A2-),D项错误。]
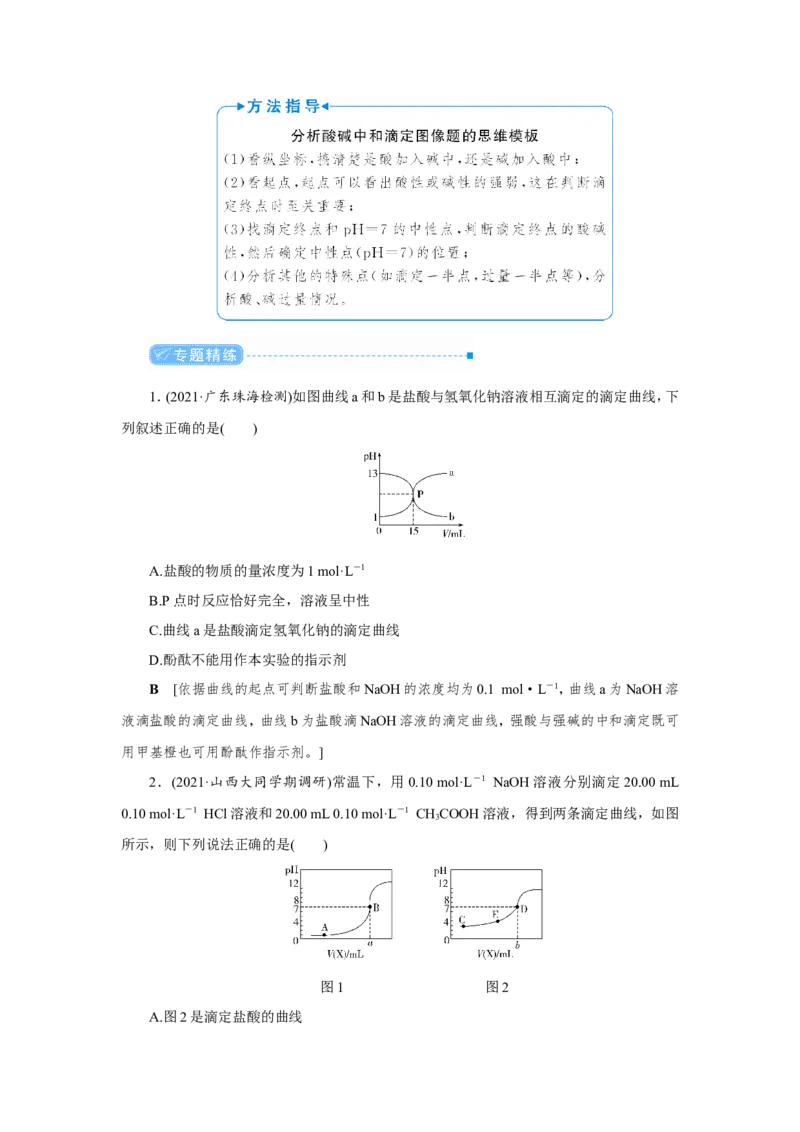
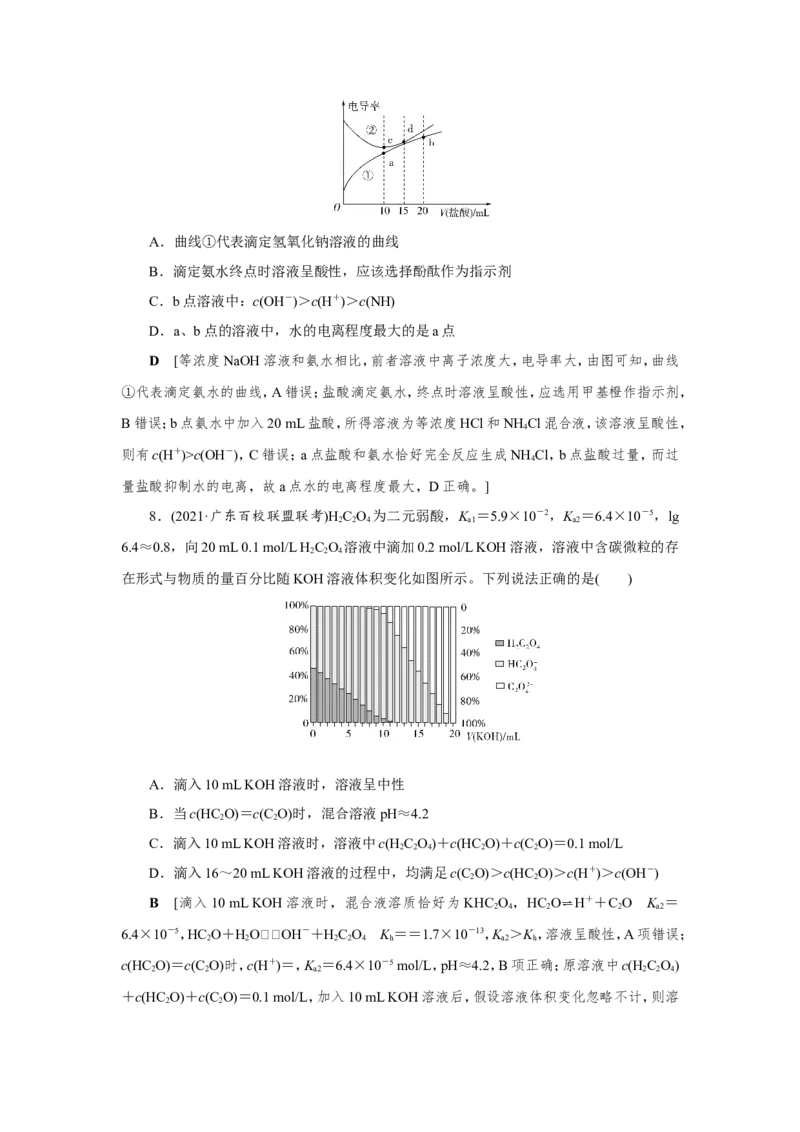
(2021·湖北武汉联考)用0.100 0 mol·L-1的标准盐酸分别滴定20.00 mL的0.100 0
mol·L-1氨水和20.00 mL的0.100 0 mol·L-1氢氧化钠溶液的滴定曲线如图所示,横坐标为滴
定百分数(滴定用量/总滴定用量),纵坐标为滴定过程中溶液pH,甲基红是一种酸碱指示剂,
变色范围为4.4~6.2,下列有关滴定过程说法正确的是( )
A.滴定氨水,当滴定分数为50%时,各离子浓度间存在关系:c(NH)+c(H+)=c(OH-)
B.滴定分数为100%时,即为滴定过程中反应恰好完全的时刻
C.从滴定曲线可以判断,使用甲基橙作为滴定过程中的指示剂准确性更佳
D.滴定氨水,当滴定分数为 150%时,所得溶液中离子浓度有大小关系 c(Cl-)>c(H
+)>c(NH)>c(OH-)
B [溶液中存在的电荷守恒应为c(NH)+c(H+)=c(OH-)+c(Cl-),A错误;滴定分数为
100%时,酸与碱的物质的量相等,即为滴定过程中反应恰好完全的时刻,B正确;从滴定曲线
看甲基红变色范围更接近于滴定终点,使用甲基橙显示偏晚,C错误;滴定分数为150%时,
即加入盐酸30.00 mL,此时溶质是NH Cl和HCl,物质的量之比为2∶1,故c(NH)>c(H+),D
4
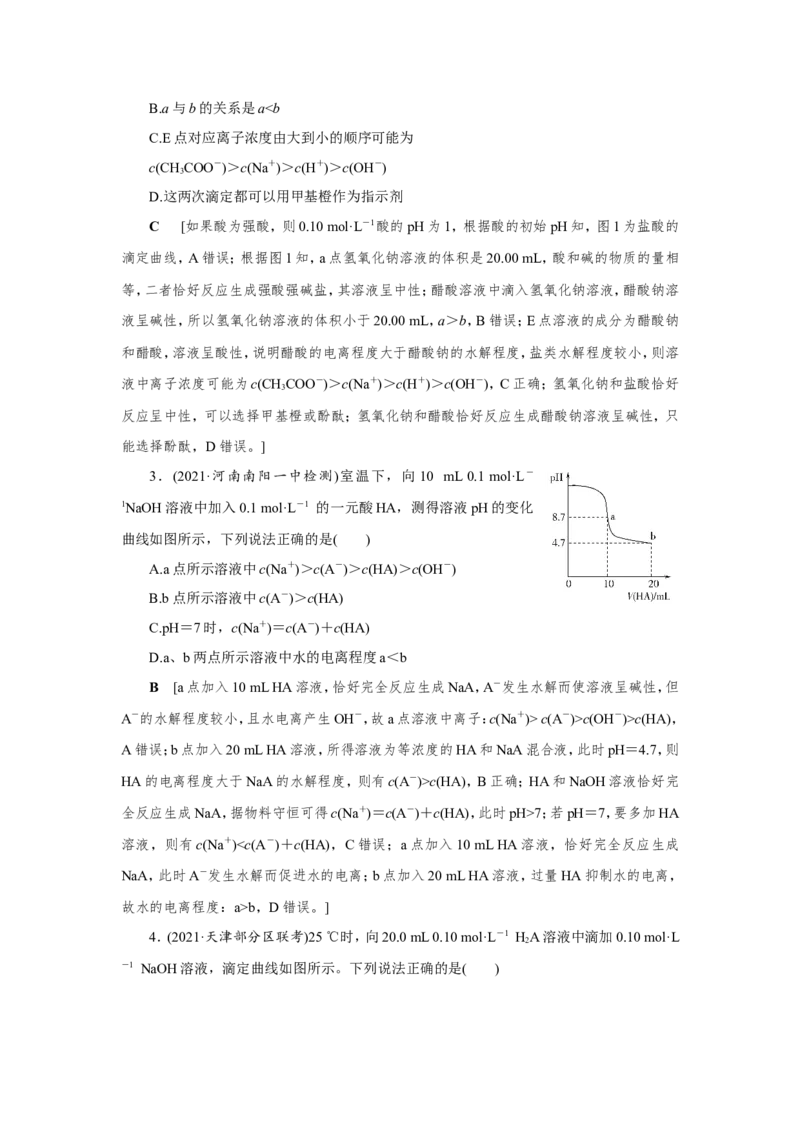
错误。]1.(2021·广东珠海检测)如图曲线a和b是盐酸与氢氧化钠溶液相互滴定的滴定曲线,下
列叙述正确的是( )
A.盐酸的物质的量浓度为1 mol·L-1
B.P点时反应恰好完全,溶液呈中性
C.曲线a是盐酸滴定氢氧化钠的滴定曲线
D.酚酞不能用作本实验的指示剂
B [依据曲线的起点可判断盐酸和NaOH的浓度均为0.1 mol·L-1,曲线a为NaOH溶
液滴盐酸的滴定曲线,曲线b为盐酸滴NaOH溶液的滴定曲线,强酸与强碱的中和滴定既可
用甲基橙也可用酚酞作指示剂。]
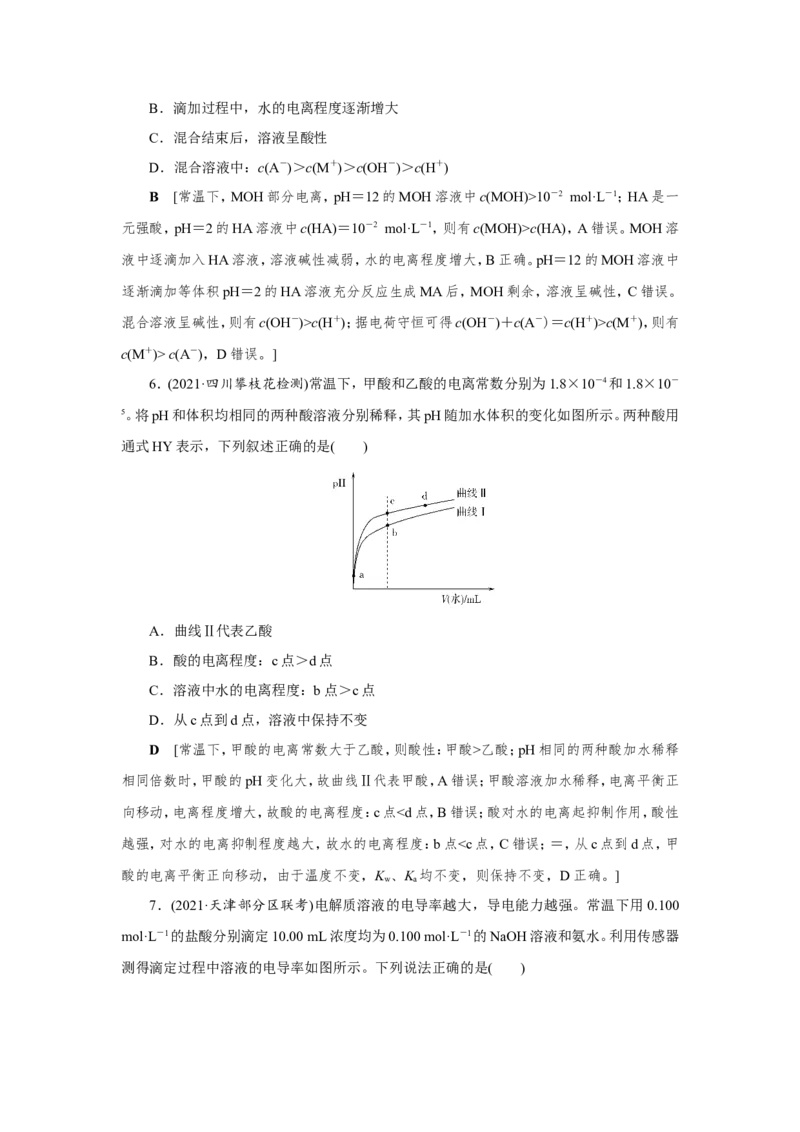
2.(2021·山西大同学期调研)常温下,用0.10 mol·L-1 NaOH溶液分别滴定20.00 mL
0.10 mol·L-1 HCl溶液和20.00 mL 0.10 mol·L-1 CHCOOH溶液,得到两条滴定曲线,如图
3
所示,则下列说法正确的是( )
图1 图2
A.图2是滴定盐酸的曲线B.a与b的关系是a c(A-)>c(OH-)>c(HA),
A错误;b点加入20 mL HA溶液,所得溶液为等浓度的HA和NaA混合液,此时pH=4.7,则
HA的电离程度大于NaA的水解程度,则有c(A-)>c(HA),B正确;HA和NaOH溶液恰好完
全反应生成NaA,据物料守恒可得c(Na+)=c(A-)+c(HA),此时pH>7;若pH=7,要多加HA
溶液,则有c(Na+)b,D错误。]
4.(2021·天津部分区联考)25 ℃时,向20.0 mL 0.10 mol·L-1 HA溶液中滴加0.10 mol·L
2
-1 NaOH溶液,滴定曲线如图所示。下列说法正确的是( )A.该滴定过程应该选择石蕊溶液作指示剂
B.W点到X点发生的主要反应的离子方程式为HA+2OH-===A2-+2HO
2 2
C.Y点对应的溶液中c(Na+)+c(H+)===c(OH-)+2c(A2-)
D.反应HA+A2-2HA-的平衡常数K=1.0×107.4
2
D [石蕊不能用作酸碱中和滴定的指示剂,根据图示滴定终点的pH,可知第二反应终
点应用酚酞作指示剂,A错误;X点对应的溶液中溶质主要是NaHA,W点到X点发生的主
要反应的离子方程式为HA+OH-===HA-+HO,B错误;根据电荷守恒,c(Na+)+c(H+)=
2 2
c(OH-)+c(HA-)+2c(A2-),因为Y点对应的溶液中c(HA-)=c(A2-),则有c(Na+)+c(H+)=
c(OH-)+3c(A2-),C错误;HAHA-+H+,K =,由于W点c(HA-)=c(H A),故K =c(H
2 a1 2 a1
+)=1.0×10-2.3;HA-A2-+H+,K =,由于Y点对应的溶液中c(HA-)=c(A2-),故K =
a2 a2
c(H+)=10×10-9.7;HAHA-+H+与HA-A2-+H+相减即得HA+A2-2HA-,
2 2
此时的平衡常数K===1.0×107.4,D正确。]
章末综合检测(八) 水溶液中的离子平衡
一、选择题:本题包括10小题,每小题只有一个选项最符合题意。
1.(2021·贵州思南中学检测)下列说法正确的是( )
A.25 ℃时,NH Cl溶液的K 大于100 ℃时NH Cl溶液的K
4 w 4 w
B.将浓度为0.1 mol/L HF溶液加水不断稀释,c(H+)/c(HF)保持不变
C.加入铝粉能产生氢气的溶液中,可能存在大量的Na+、Ba2+、AlO、NO
D.100 ℃时,将pH=2的盐酸与pH=12的NaOH溶液等体积混合,溶液显中性
C [温度升高,水的离子积K 增大,故100 ℃时NH Cl溶液的K 大,A错误;HF溶液
w 4 w
加水不断稀释,HF的电离平衡正向移动,n(H+)增大,n(HF)减小,则c(H+)/c(HF)增大,B错误;
加入铝粉能产生氢气的溶液可能呈强酸性或强碱性,若为强碱性,则四种离子可以大量共存,
C正确;100 ℃时,水的电离程度增大,则有K >1×10-14,pH=12的NaOH溶液中c(OH-)大
w
于10-2 mol/L,故pH=2的盐酸与pH=12的NaOH溶液等体积混合,NaOH剩余,所得混合液呈碱性,D错误。]
2.(2021·重庆云阳县检测)常温下,在等体积:①pH=0的硫酸;②0.1 mol·L-1NaOH溶
液;③pH=10的纯碱溶液中,水的电离程度的大小顺序是( )
A.①>②>③ B.②>①>③
C.③>①>② D.③>②>①
D [酸或碱抑制水的电离,且c(H+)或c(OH-)越大,水的电离程度越小,则水的电离程
度:①<②;纯碱(Na CO)是强碱弱酸盐,发生水解而促进水的电离,则水的电离程度最大。]
2 3
3.(2021·福建三明一中检测)根据下列实验不能证明一元酸HR为弱酸的是( )
A.室温下,NaR溶液的pH大于7
B.HR溶液加入少量NaR固体,溶解后溶液的pH变大
C.HR溶液的导电性比盐酸弱
D.室温下,0.01 mol·L-1的HR溶液pH=2.8
C [室温下,NaR溶液的pH大于7,说明R-发生水解反应,则HR是弱酸,A正确;HR
溶液加入少量NaR固体,溶解后溶液的pH变大,说明存在电离平衡:HR⇌H++R-,加入少
量NaR固体,c(R-)增大,平衡逆向移动,溶液的酸性减弱,pH变大,B正确;题目未指明HR
溶液和盐酸的浓度大小,不能通过导电性判断HR是否为弱酸,C错误;室温下,0.01 mol·L-
1的HR溶液pH=2.8,说明HR部分电离,则HR为弱酸,D正确。]
4.(2021·湖北荆州联考)下列实验事实不能用平衡移动原理解释的是( )
A.室温下,pH=11的氨水稀释10倍后溶液pH>10
B.将饱和氯化铁溶液滴入沸水,溶液变成红褐色
C.对于CO(g)+NO
2
(g)⇌CO
2
(g)+NO(g)的平衡体系,增大压强可使颜色变深
D.水垢中含有CaSO,可先用饱和NaCO 溶液浸泡处理,而后用盐酸去除
4 2 3
C [室温下,pH=11的氨水稀释10倍,NH ·HO的电离平衡正向移动,n(OH-)增大,
3 2
溶液pH>10,A正确;饱和FeCl 溶液滴入沸水中,促进了Fe3+的水解,得到红褐色Fe(OH)
3 3
胶体,B正确;增大压强,平衡不移动,由于容器体积缩小,则c(NO )增大,颜色变深,不能用
2
平衡移动原理解释,C错误;水垢中含有CaSO
4
,存在溶解平衡:CaSO
4
(s)⇌Ca2+(aq)+
SO(aq),用饱和NaCO 溶液浸泡处理,Ca2+与CO结合生成CaCO ,平衡正向移动,再用盐酸
2 3 3
除去CaCO ,D正确。]
3
5.(2021·广州荔湾区检测)常温下,向pH=12的一元弱碱(MOH)溶液中逐渐滴加等体积
pH=2的一元强酸(HA)溶液。下列说法正确的是( )
A.弱碱的物质的量浓度小于强酸B.滴加过程中,水的电离程度逐渐增大
C.混合结束后,溶液呈酸性
D.混合溶液中:c(A-)>c(M+)>c(OH-)>c(H+)
B [常温下,MOH部分电离,pH=12的MOH溶液中c(MOH)>10-2 mol·L-1;HA是一
元强酸,pH=2的HA溶液中c(HA)=10-2 mol·L-1,则有c(MOH)>c(HA),A错误。MOH溶
液中逐滴加入HA溶液,溶液碱性减弱,水的电离程度增大,B正确。pH=12的MOH溶液中
逐渐滴加等体积pH=2的HA溶液充分反应生成MA后,MOH剩余,溶液呈碱性,C错误。
混合溶液呈碱性,则有c(OH-)>c(H+);据电荷守恒可得c(OH-)+c(A-)=c(H+)>c(M+),则有
c(M+)> c(A-),D错误。]
6.(2021·四川攀枝花检测)常温下,甲酸和乙酸的电离常数分别为1.8×10-4和1.8×10-
5。将pH和体积均相同的两种酸溶液分别稀释,其pH随加水体积的变化如图所示。两种酸用
通式HY表示,下列叙述正确的是( )
A.曲线Ⅱ代表乙酸
B.酸的电离程度:c点>d点
C.溶液中水的电离程度:b点>c点
D.从c点到d点,溶液中保持不变
D [常温下,甲酸的电离常数大于乙酸,则酸性:甲酸>乙酸;pH相同的两种酸加水稀释
相同倍数时,甲酸的pH变化大,故曲线Ⅱ代表甲酸,A错误;甲酸溶液加水稀释,电离平衡正
向移动,电离程度增大,故酸的电离程度:c点c(OH-),C错误;a点盐酸和氨水恰好完全反应生成NH Cl,b点盐酸过量,而过
4
量盐酸抑制水的电离,故a点水的电离程度最大,D正确。]
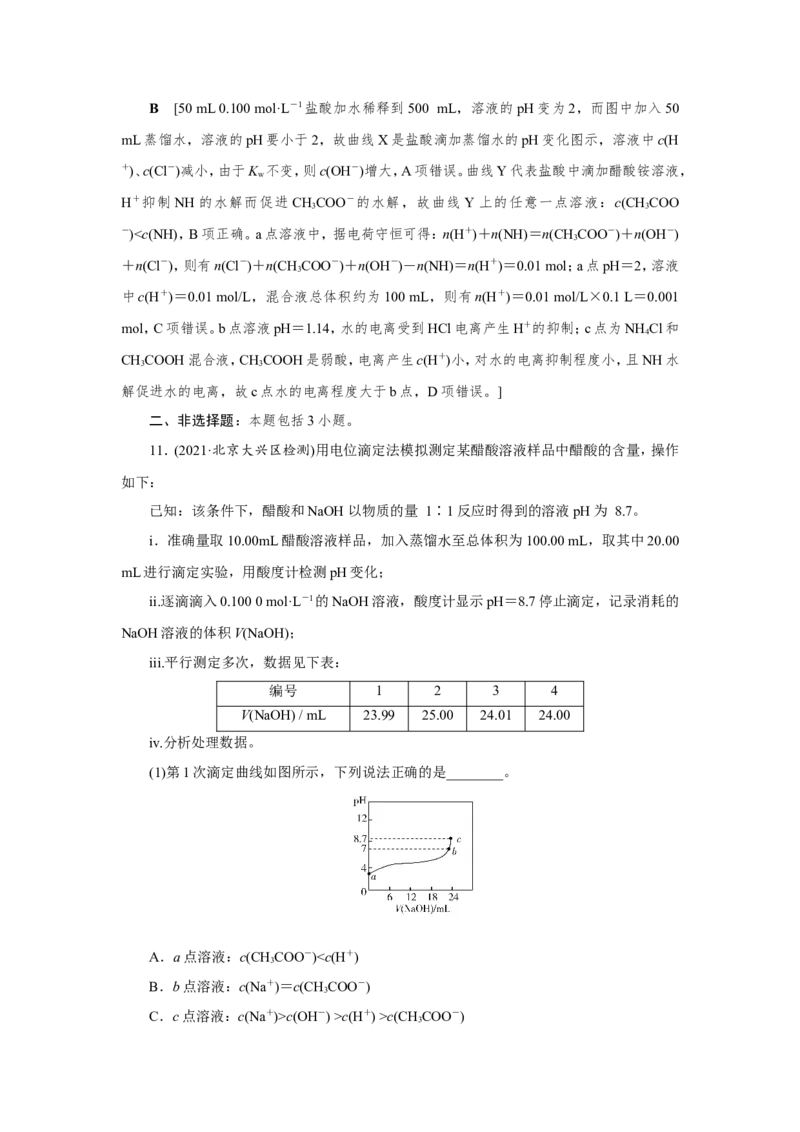
8.(2021·广东百校联盟联考)HC O 为二元弱酸,K =5.9×10-2,K =6.4×10-5,lg
2 2 4 a1 a2
6.4≈0.8,向20 mL 0.1 mol/L H C O 溶液中滴加0.2 mol/L KOH溶液,溶液中含碳微粒的存
2 2 4
在形式与物质的量百分比随KOH溶液体积变化如图所示。下列说法正确的是( )
A.滴入10 mL KOH溶液时,溶液呈中性
B.当c(HC O)=c(C O)时,混合溶液pH≈4.2
2 2
C.滴入10 mL KOH溶液时,溶液中c(H C O)+c(HC O)+c(C O)=0.1 mol/L
2 2 4 2 2
D.滴入16~20 mL KOH溶液的过程中,均满足c(C O)>c(HC O)>c(H+)>c(OH-)
2 2
B [滴入10 mL KOH溶液时,混合液溶质恰好为KHC
2
O
4
,HC
2
O⇌H++C
2
O K
a2
=
6.4×10-5,HC O+HOOH-+HC O K ==1.7×10-13,K >K ,溶液呈酸性,A项错误;
2 2 2 2 4 h a2 h
c(HC O)=c(C O)时,c(H+)=,K =6.4×10-5 mol/L,pH≈4.2,B项正确;原溶液中c(H C O)
2 2 a2 2 2 4
+c(HC O)+c(C O)=0.1 mol/L,加入10 mL KOH溶液后,假设溶液体积变化忽略不计,则溶
2 2液从20 mL变为30 mL,此时c(H C O)+c(HC O)+c(C O)=×0.1 mol/L,C项错误;滴入20
2 2 4 2 2
mL KOH溶液时,混合液溶质为KC O,溶液水解显碱性,c(OH-)>c(H+),此时不满足,D项
2 2 4
错误。]
9.(2021·四川内江检测)绿矾(FeSO ·7H O)是治疗缺铁性贫血药品的重要成分。某化学兴
4 2
趣小组采用以下方法测定某绿矾样品的纯度。a.称取2.850 g绿矾产品,溶解,在250 mL容量
瓶中定容配成待测液;b.量取25.00 mL待测溶液于锥形瓶中;c.用硫酸酸化的0.010 00 mol·L
-1KMnO 溶液滴定至终点,消耗KMnO 溶液体积的平均值为20.00 mL。下列说法不正确的
4 4
是( )
A.a步骤中定容时,仰视会使所测绿矾晶体的纯度偏低
B.滴定时盛放KMnO 溶液的仪器为酸式滴定管
4
C.滴加最后一滴KMnO 溶液时,溶液变成浅红色,即为滴定终点
4
D.上述样品中FeSO ·7H O的质量分数约为97.5%
4 2
C [配制待测液,定容时仰视,液面高于刻度线,则所配溶液的浓度偏低,测得绿矾晶体
的纯度偏低,A正确;KMnO 溶液具有强氧化性,滴定时要盛放在酸式滴定管中,B正确;滴
4
加最后一滴KMnO 溶液,溶液变为浅红色,若半分钟内不褪色,则为滴定终点,C错误;用标
4
准 KMnO 溶液滴定 FeSO 待测液时,存在关系:KMnO ~5FeSO ,则绿矾样品中
4 4 4 4
FeSO ·7HO的质量为5×0.010 00 mol·L-1×20.00×10-3 L××278 g·mol-1=2.78 g,故
4 2
样品中FeSO ·7HO的质量分数为×100%≈97.5%,D正确。]
4 2
10.(2020·福建龙岩一模)常温下,向盛50 mL 0.100 mol·L-1盐酸的两个烧杯中各自匀速
滴加50 mL的蒸馏水、0.100 mol·L-1醋酸铵溶液,测得溶液pH随时间变化如图所示。已知
K(CHCOOH)=1.8×10-5,K (NH ·H O)=1.8×10-5。下列说法正确的是( )
a 3 b 3 2
A.曲线X是盐酸滴加蒸馏水的pH变化图,滴加过程中溶液各种离子浓度逐渐减小
B.曲线Y上的任意一点溶液中均存在c(CHCOO-)c(OH-) >c(H+) >c(CHCOO-)
3(2)滴定过程中,从a点到c点水电离出的c(OH-)逐渐增大,用平衡移动原理解释:
________________________________________________________________________
________________________________________________________________________
________________________________________________________________________。
(3)根据表中的有效数据,计算消耗的 NaOH 溶液的平均体积V(NaOH)=________mL。
该醋酸溶液样品中醋酸的含量是________g/100 mL。[M(CHCOOH)=60 g·mol-1]
3
解析 (1)据电荷守恒可知,a点溶液中:c(CHCOO-)+c(OH-)=c(H+),则有c(CHCOO
3 3
-)c(CHCOO-) >c(OH-)>c(H+) ,C项错误。
3
(3)表中第2组数据存在明显错误,应舍去,取其他三组数据计算平均体积V(NaOH)=
(23.99+24.01+24.00)mL/3=24.00 mL。10.00 mL醋酸溶液样品中:n(CHCOOH)=n(NaOH)
3
=0.100 0 mol/L×24.00×10-3 L×=0.012 mol,则有m(CHCOOH)=0.012 mol×60 g/mol=
3
0.72g,故该醋酸溶液样品中醋酸的含量为0.72 g/10.00 mL=7.2 g/100 mL。
答案 (1)AB
(2)溶液中存在水的电离平衡H
2
O⇌OH-+H+,随着NaOH 加入,CH
3
COOH浓度降低,
醋酸对水电离的抑制程度减弱
(3)24.00 7.2
12.(2021·山西大学附中检测)水溶液中的离子平衡是中学学习的一个重要内容。
(1)下列溶液①0.1 mol/L盐酸 ②0.1 mol/L H SO 溶液 ③0.1 mol/L CH COONa溶液 ④
2 4 3
0.1 mol/L NH Cl溶液 ⑤0.1 mol/L氨水,按pH由小到大顺序为________________(填序号)。
4
(2)等浓度的盐酸、氨水中,由水电离出的H+浓度c(H+) ________c(H+) (填“大于”
盐酸 氨水
“小于”或“等于”) 。在25 ℃下,将a mol/L的氨水与0.01 mol/L的盐酸等体积混合,充分
反 应 后 溶 液 呈 中 性 , 则 反 应 后 溶 液 存 在 的 离 子 浓 度 的 大 小 顺 序 为
________________________________________________________________________,氨水
的浓度a________0.01 mol/L(填“>”“ <”或“=”)。
(3) 某 同 学 查 阅 资 料 发 现 , 人 体 血 液 里 存 在 重 要 的 酸 碱 平 衡 : CO +
2
H
2
O⇌H
2
CO
3
HCO,使人体血液pH保持在7.35~7.45,否则就会发生酸中毒或碱中毒。
①人体血液酸中毒时,可注射________(填选项)缓解;
A.NaOH溶液 B.NaHCO 溶液
3C.NaCl溶液 D.NaSO 溶液
2 4
②已知 25 ℃时,CO 水解反应的一级平衡常数 K =2×10-4 mol/L,当溶液中
h
c(HCO)∶c(CO)=2∶1时,溶液的pH=________。
(4)已知25 ℃时,AgCl的K =1.8×10-10,该温度下向1 L 0.03 mol/L的AgNO 溶液中
sp 3
加入1 L 0.01 mol/L的NaCl溶液之后,溶液中c(Cl-)=________mol/L(忽略混合前后溶液体
积的变化)。平衡后,若向该体系中再加入少量AgCl固体,则c(Cl-)________(填“增大”
“减小”或“不变”)。
解析 (1)①、②、④溶液呈酸性,HSO 是二元酸,等浓度时②的酸性强于①,④是强酸
2 4
弱碱盐溶液,酸性最弱;③、⑤溶液呈碱性,③是强碱弱酸盐溶液,其碱性小于⑤,故溶液的
pH:②<①<④<③<⑤。
(2)HCl是强酸,NH ·HO是弱碱,等浓度时盐酸中c(H+)大于氨水中c(OH-),而c(H+)
3 2
或c(OH-)越大,水的电离程度越小,故由水电离出的H+浓度c(H+) 小于c(H+) 。
盐酸 氨水
氨水与盐酸恰好完全反应生成NH Cl时,所得溶液呈酸性,若充分反应后溶液呈中性,
4
应使氨水稍过量,则有氨水的浓度a>0.01 mol·L-1。所得溶液呈中性,则有c(H+)=c(OH-),
结合电荷守恒推知c(Cl-)=c(NH),故溶液中离子浓度:c(Cl-)=c(NH)>c(H+)=c(OH-)。
(3)②CO 的一级水解反应:CO+H
2
O⇌HCO+OH-,水解常数 K
h1
=[c(HCO)·c(OH
-)]/c(CO)=2×10-4 mol/L,当溶液中c(HCO)∶c(CO)=2∶1时,可得c(OH-)=10-4 mol/L,
故溶液的pH=10。
(4)向1 L 0.03 mol/L的AgNO 溶液中加入1 L 0.01 mol/L的NaCl溶液,充分反应后剩余
3
AgNO ,反应后溶液中c(Ag+)=0.01 mol/L,则该温度下溶液中 c(Cl-)===1.8×10-8
3
mol/L。平衡后,若向该体系中再加入少量AgCl固体,对AgCl的沉淀溶解平衡无影响,故溶
液中c(Cl-)不变。
答案 (1)②<①<④<③<⑤
(2)小于 c(Cl-)=c(NH)>c(H+)=c(OH-) >
(3)①B ②10
(4)1.8×10-8 不变
13.(2021·北京朝阳区检测)乙二酸(H C O)俗称草酸,在实验研究和化学工业中应用广
2 2 4
泛。
(1)室温下,测得0.1 mol·L-1 HC O 溶液pH=1.3,写出草酸的电离方程式
2 2 4
________________________________________________________________________。
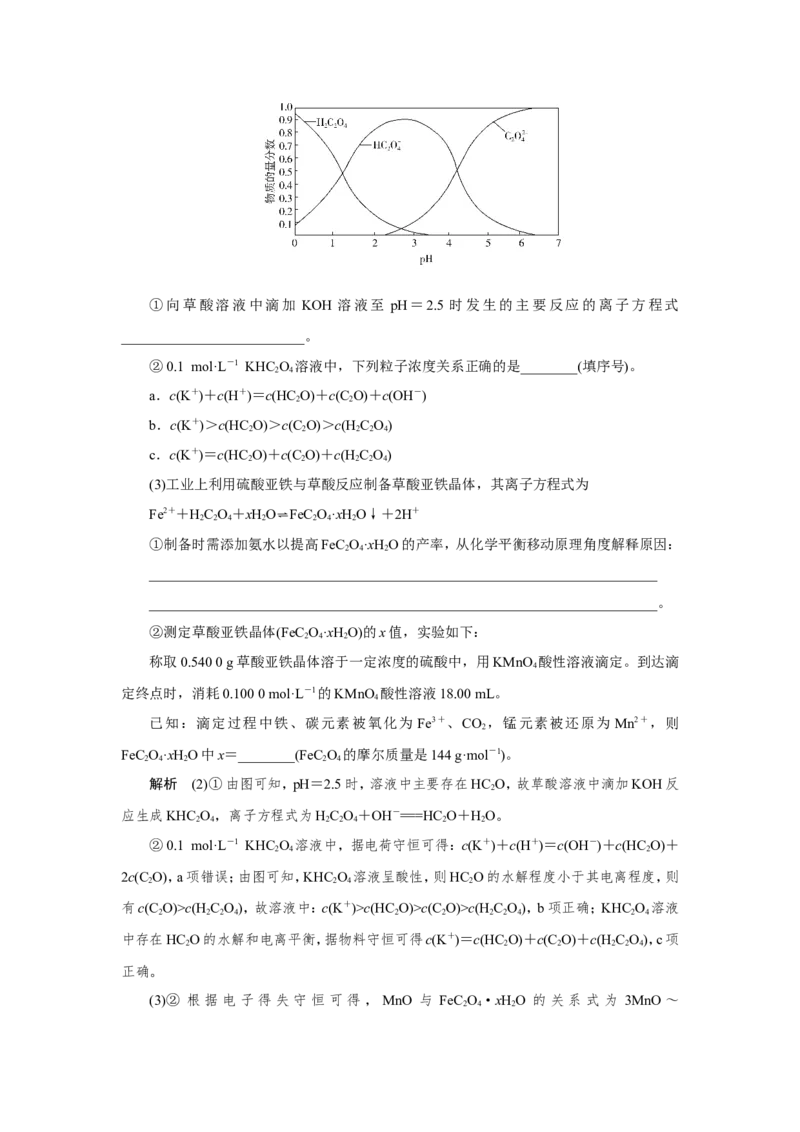
(2)草酸溶液中各粒子的物质的量分数随溶液pH变化关系如下图所示:①向草酸溶液中滴加 KOH 溶液至 pH=2.5 时发生的主要反应的离子方程式
__________________________。
②0.1 mol·L-1 KHC O 溶液中,下列粒子浓度关系正确的是________(填序号)。
2 4
a.c(K+)+c(H+)=c(HC O)+c(C O)+c(OH-)
2 2
b.c(K+)>c(HC O)>c(C O)>c(H C O)
2 2 2 2 4
c.c(K+)=c(HC O)+c(C O)+c(H C O)
2 2 2 2 4
(3)工业上利用硫酸亚铁与草酸反应制备草酸亚铁晶体,其离子方程式为
Fe2++H
2
C
2
O
4
+xH
2
O⇌FeC
2
O
4
·xH
2
O↓+2H+
①制备时需添加氨水以提高FeC O·xHO的产率,从化学平衡移动原理角度解释原因:
2 4 2
________________________________________________________________________
________________________________________________________________________。
②测定草酸亚铁晶体(FeC O·xHO)的x值,实验如下:
2 4 2
称取0.540 0 g草酸亚铁晶体溶于一定浓度的硫酸中,用KMnO 酸性溶液滴定。到达滴
4
定终点时,消耗0.100 0 mol·L-1的KMnO 酸性溶液18.00 mL。
4
已知:滴定过程中铁、碳元素被氧化为 Fe3+、CO ,锰元素被还原为 Mn2+,则
2
FeC O·xHO中x=________(FeC O 的摩尔质量是144 g·mol-1)。
2 4 2 2 4
解析 (2)①由图可知,pH=2.5时,溶液中主要存在HC O,故草酸溶液中滴加KOH反
2
应生成KHC O,离子方程式为HC O+OH-===HC O+HO。
2 4 2 2 4 2 2
②0.1 mol·L-1 KHC O 溶液中,据电荷守恒可得:c(K+)+c(H+)=c(OH-)+c(HC O)+
2 4 2
2c(C O),a项错误;由图可知,KHC O 溶液呈酸性,则HC O的水解程度小于其电离程度,则
2 2 4 2
有c(C O)>c(H C O),故溶液中:c(K+)>c(HC O)>c(C O)>c(H C O),b项正确;KHC O 溶液
2 2 2 4 2 2 2 2 4 2 4
中存在HC O的水解和电离平衡,据物料守恒可得c(K+)=c(HC O)+c(C O)+c(H C O),c项
2 2 2 2 2 4
正确。
(3)② 根据电子得失守恒可得 ,MnO 与 FeC O·xHO 的关系式为 3MnO~
2 4 25FeC O·xHO,达到滴定终点时,消耗 18.00 mL 0.100 0 mol·L-1 KMnO 溶液,则有
2 4 2 4
n(FeC O·xHO)=×0.100 0 mol·L-1×18.00×10-3 L=3×10-3 mol,草酸亚铁晶体的质
2 4 2
量为0.540 0 g,则有M(FeC O·xHO)==180 g·mol-1,又知M(FeC O)=144 g·mol-1,故
2 4 2 2 4
FeC O·xHO中x==2。
2 4 2
答案 (1)H
2
C
2
O 4⇌HC
2
O+H+、HC
2
O⇌C
2
O+H+、HC
2
O⇌C
2
O+H+
(2)①HC O+OH-===HC O+HO ②bc
2 2 4 2 2
(3)①NH ·H O 与 H+反应,使 c(H+)减小,平衡向正反应方向移动,产生更多的
3 2
FeC O·xHO
2 4 2
②2