文档内容
专题讲座(八)有机合成与推断
【化学学科素养】
有机推断题是历年高考的必考点,也是难点之一, 综观近几年化学高考试题,作为高考化学理
综命题不可缺少的有机化学而言,其命题呈现如下趋势:①是以烃及烃的衍生物的转化关系为内容的
传统考查方式仍将继续,②是有机推断中渗透有机实验、有机计算等其它有机综合性问题、开放性的
考查形式。这类试题既能检查学生对基础知识的掌握情况,又能考察学生灵活运用知识的能力,更能
考察学生的分析问题和逻辑推理的能力。
【必备知识解读】
一、有机推断题高考命题方向
近几年有机化学试题保持高考改革特点,注重基础知识,突出能力的考查,主要从以下五方面来考查
1.有机物分子式、结构简式的书写(含有苯环及其它2种官能团以上的物质);
2.有机方程式的书写(重点为加成反应,酯化反应,水解反应,羧酸酚与NaOH溶液的中和反应。而醛
与银氨溶液、新制氢氧化铜浊液的反应一般不会让考生书写);
3.醇、醛、酸、酯的衍生关系;
4.同分异构体种类确定或书写(含有苯环及其它2种官能团以上的物质;从不同角度给一些限定条件);
5.有机反应类型的判断(加成反应、酯化反应、水解反应、氧化反应、还原反应)。
二、有机推断题的解题思路
1.解题思路
原题→审题、综合分析,隐含条件明显条件→找出解题突破口 (结构、反应、性质、现象特征), 顺
推可逆推→ 结论←检验
2. 解题关键:
⑴根据有机物的物理性质,有机物特定的反应条件寻找突破口。
⑵根据有机物之间的相互衍变关系寻找突破口。
⑶根据有机物结构上的变化,及某些特征现象上寻找突破口。
⑷根据某些特定量的变化寻找突破口。
三、有机推断题的突破口
解题的突破口也叫做题眼,题眼可以是一种特殊的现象、反应、性质、用途或反应条件,或在框图推
断试题中,有几条线同时经过一种物质,往往这就是题眼。根据有机化学知识,突破口可从下列几方面寻
找:
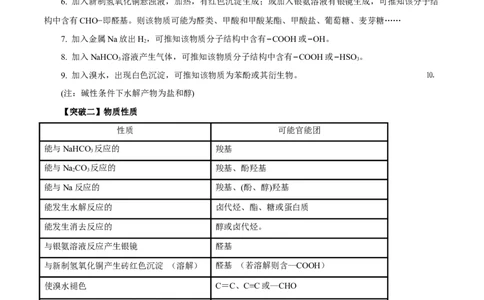
【突破一】反应现象1. 能使溴水褪色的物质有:含碳双键或碳三键的物质因加成而褪色;含醛基的物质因氧化而褪色;酚
类物质因取代而褪色;液态饱和烃、液态饱和酯、苯及其同系物、氯仿、四氯化碳因萃取而褪色。
2. 能使酸性高锰酸钾溶液褪色的物质可能含有:碳碳双键、碳碳三键、含苯环且连苯环的碳上有氢原
子、醇—OH、酚—OH、醛基。
3. 遇三氯化铁溶液显紫色,可推知该物质分子含有酚羟基。
4. 遇浓硝酸变黄,可推知该物质是含有苯环结构的蛋白质。
5. 遇I 水变蓝,可推知该物质为淀粉。
2
6. 加入新制氢氧化铜悬浊液,加热,有红色沉淀生成;或加入银氨溶液有银镜生成,可推知该分子结
构中含有CHO−即醛基。则该物质可能为醛类、甲酸和甲酸某酯、甲酸盐、葡萄糖、麦芽糖……
7. 加入金属Na放出H,可推知该物质分子结构中含有−COOH或−OH。
2
8. 加入NaHCO 溶液产生气体,可推知该物质分子结构中含有−COOH或−HSO 。
3 3
9. 加入溴水,出现白色沉淀,可推知该物质为苯酚或其衍生物。 ⒑
(注:碱性条件下水解产物为盐和醇)
【突破二】物质性质
性质 可能官能团
能与NaHCO 反应的 羧基
3
能与NaCO 反应的 羧基、酚羟基
2 3
能与Na反应的 羧基、(酚、醇)羟基
能发生水解反应的 卤代烃、酯、糖或蛋白质
能发生消去反应的 醇或卤代烃。
与银氨溶液反应产生银镜 醛基
与新制氢氧化铜产生砖红色沉淀 (溶解) 醛基 (若溶解则含—COOH)
使溴水褪色 C=C、C≡C或—CHO
加溴水产生白色沉淀、遇Fe3+显紫色 酚
使酸性KMnO 溶液褪色 C=C、C≡C、酚类或—CHO、苯的同系物等
4
显酸性的 有机物可能含有:羧基、酚羟基
显碱性的 可能含有—NH 或—NH—或—N—。
2
①可能含有羧基(酚羟基) 和—NH 或—
既能与酸又能与碱反应的 2
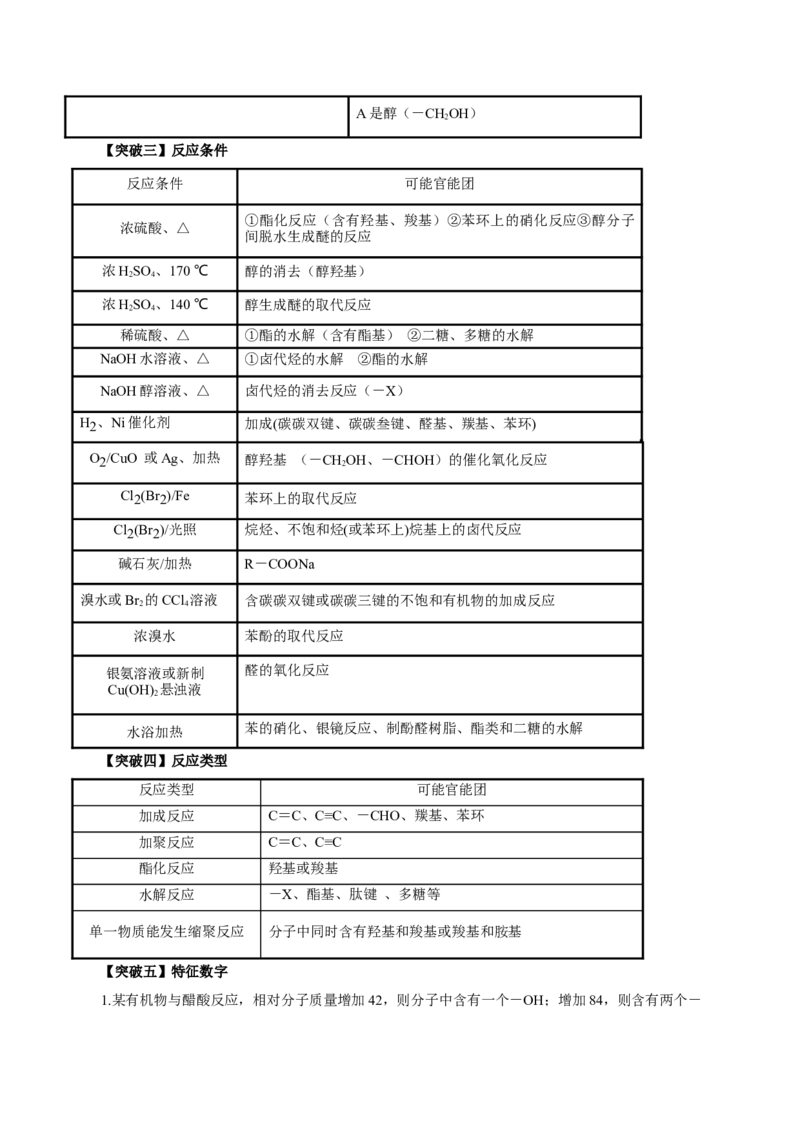
NH—或—N—②羧酸的铵盐A是醇(-CHOH)
2
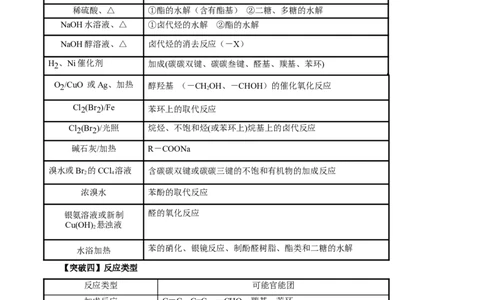
【突破三】反应条件
反应条件 可能官能团
①酯化反应(含有羟基、羧基)②苯环上的硝化反应③醇分子
浓硫酸、△
间脱水生成醚的反应
浓HSO 、170 ℃ 醇的消去(醇羟基)
2 4
浓HSO 、140 ℃ 醇生成醚的取代反应
2 4
稀硫酸、△ ①酯的水解(含有酯基) ②二糖、多糖的水解
NaOH水溶液、△ ①卤代烃的水解 ②酯的水解
NaOH醇溶液、△ 卤代烃的消去反应(-X)
H2 、Ni催化剂 加成(碳碳双键、碳碳叁键、醛基、羰基、苯环)
O2/CuO 或Ag、加热 醇羟基 (-CH
2
OH、-CHOH)的催化氧化反应
Cl2(Br2)/Fe 苯环上的取代反应
Cl2(Br2)/光照 烷烃、不饱和烃(或苯环上)烷基上的卤代反应
碱石灰/加热 R-COONa
溴水或Br 的CCl 溶液 含碳碳双键或碳碳三键的不饱和有机物的加成反应
2 4
浓溴水 苯酚的取代反应
银氨溶液或新制 醛的氧化反应
Cu(OH) 悬浊液
2
水浴加热 苯的硝化、银镜反应、制酚醛树脂、酯类和二糖的水解
【突破四】反应类型
反应类型 可能官能团
加成反应 C=C、C≡C、-CHO、羰基、苯环
加聚反应 C=C、C≡C
酯化反应 羟基或羧基
水解反应 -X、酯基、肽键 、多糖等
单一物质能发生缩聚反应 分子中同时含有羟基和羧基或羧基和胺基
【突破五】特征数字
1.某有机物与醋酸反应,相对分子质量增加42,则分子中含有一个-OH;增加84,则含有两个-OH。
缘由-OH转变为−OOCCH 。
3
2. 某有机物在催化剂作用下被氧气氧化,若相对分子质量增加16,则表明有机物分子内有一个-
CHO
(变为-COOH);若增加32,则表明有机物分子内有两个-CHO(变为-COOH)。
3. 若有机物与Cl 反应,若有机物的相对分子质量增加71,则说明有机物分子内含有一个碳碳双键;
2
若增加142,则说明有机物分子内含有二个碳碳双键或一个碳碳叁键。
【突破六】反应产物推知官能团位置
1. 若由醇氧化得醛或羧酸,可推知-OH一定连接在有2个氢原子的碳原子上,即存在−CHOH;由
2
醇氧化为酮,推知-OH一定连在有1个氢原子的碳原子上,即存在 -CHOH ; 若醇不能在催化剂作用下
被氧化,则-OH所连的碳原子上无氢原子。
2. 由消去反应的产物,可确定-OH或-X的位置
3. 由取代反应产物的种数,可确定碳链结构。如烷烃,已知其分子式和一氯代物的种数时,可推断其
可能的结构。有时甚至可以在不知其分子式的情况下,判断其可能的结构简式。
4. 由加氢后碳链的结构,可确定原物质分子C=C或CC−=的位置。
5.由有机物发生酯化反应生成酯的结构,可以推断反应物中羧基和羟基的位置:由有机物发生成肽反
应
生成肽的结构,可以推断反应物中羧基和氨基的位置。
【突破七】反应产物推知官能团的个数
1. 与银氨溶液反应,若1mol有机物生成2mol银,则该有机物分子中含有一个醛基;若生成4mol
银,则含有二个醛基或该物质为甲醛。
2. 与金属钠反应,若1mol有机物生成0.5mol2H,则其分子中含有一个活泼氢原子,或为一个醇羟
基,或酚羟基,也可能为一个羧基。
【突破八】特殊的现象和物理性质
1.特殊的颜色:酚类物质遇Fe3+呈紫色;淀粉遇碘水呈蓝色;蛋白质遇浓硝酸呈黄色;多羟基的物质
遇新制的Cu(OH) 悬浊液呈绛蓝色溶液;苯酚无色,但在空气中因部分氧化而显粉红色。
2
2.特殊的气味:硝基苯有苦杏仁味;乙醇和低级酯有香味;甲醛、乙醛、甲酸、乙酸有刺激性味;乙
二醇、丙三醇、蔗糖、葡萄糖有甜味;苯及其同系物、苯酚、石油、萘有特殊气味;乙炔(常因混有
HS、PH 等而带有臭味)、甲烷无味。
2 3
3.特殊的水溶性、熔沸点等:苯酚常温时水溶性不大,但高于65℃以任意比互溶;常温下呈气态的物质有:碳原子小于4的烃类、甲烷、甲醛、新戊烷、CHCl、CHCHCl等。
3 3 2
4.特殊的用途:甲苯、苯酚、甘油、纤维素能制备炸药;乙二醇可用做防冻液;甲醛的水溶液可用来
消毒、杀菌、浸制生物标本;葡萄糖或醛类物质可用于制镜业。
四、有机题的答题要规范
高考题的有机推断题中的赋分点多为结构简式、化学方程式的书写,这就要求考生有较强的文字表达
能力和较规范的书写,在复习中,要注意减少随意性、注意规范性,及时纠正错误。要特别注意:
(1)有机物结构简式、分子式书写时不要少H或多H,结构简式书写时应正确写出官能团及连接方
式 (2)方
程式应书写完整,不要漏掉反应条件或小分子
(3)同分异构体不要漏写或错写等等。
注意:烃的衍生物是中学有机化学的核心内容,在各类烃的衍生物中,以含氧衍生物为重点.教材在
介绍每一种代表物时,一般先介绍物质的分子结构,然后联系分子结构讨论其性质、用途和制法等.在学
习这一章时首先掌握同类衍生物的组成、结构特点(官能团)和它们的化学性质,在此基础上要注意各类官
能团之间的衍变关系,熟悉官能团的引入和转化的方法,能选择适宜的反应条件和反应途径合成有机物.
【关键能力拓展】
一、有机推断题的突破方法
1.根据反应条件推断反应物或生成物
(1)“光照”为烷烃的卤代反应。
(2)“NaOH水溶液、加热”为R—X的水解反应,或酯( )的水解反应。
(3)“NaOH醇溶液、加热”为R—X的消去反应。
(4)“浓HNO(浓HSO 、加热)”为苯环上的硝化反应。
3 2 4
(5)“浓HSO 、加热”为R—OH的消去或酯化反应。
2 4
(6)“浓HSO 、170 ℃”是乙醇消去反应的条件。
2 4
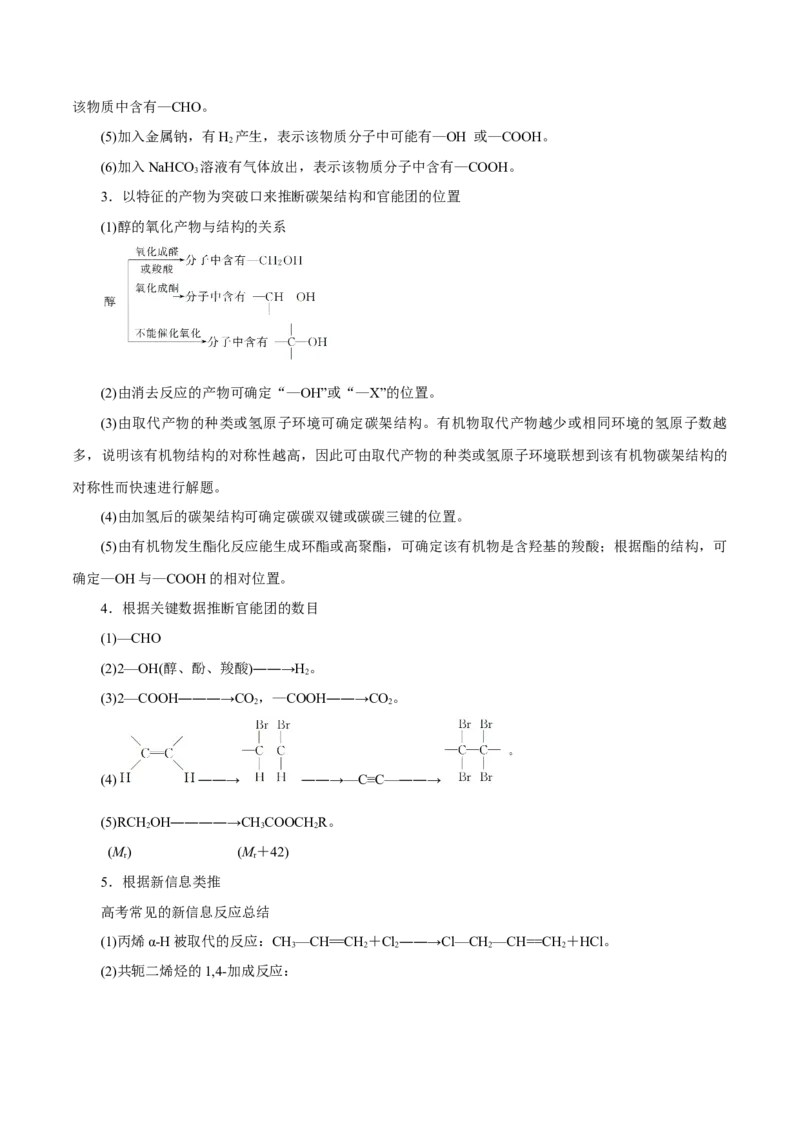
2.根据有机反应的特殊现象推断有机物的官能团
(1)使溴水褪色,则表示有机物分子中可能含有碳碳双键、碳碳三键或醛基。
(2)使酸性KMnO 溶液褪色,则该物质中可能含有碳碳双键、碳碳三键、醛基或苯的同系物(苯环上的
4
氢原子被烷基取代的物质)。
(3)遇FeCl 溶液显紫色或加入浓溴水出现白色沉淀,表示该物质分子中含有酚羟基。
3
(4)加入新制Cu(OH) 悬浊液并加热,有红色沉淀生成(或加入银氨溶液并水浴加热有银镜出现),说明
2该物质中含有—CHO。
(5)加入金属钠,有H 产生,表示该物质分子中可能有—OH 或—COOH。
2
(6)加入NaHCO 溶液有气体放出,表示该物质分子中含有—COOH。
3
3.以特征的产物为突破口来推断碳架结构和官能团的位置
(1)醇的氧化产物与结构的关系
(2)由消去反应的产物可确定“—OH”或“—X”的位置。
(3)由取代产物的种类或氢原子环境可确定碳架结构。有机物取代产物越少或相同环境的氢原子数越
多,说明该有机物结构的对称性越高,因此可由取代产物的种类或氢原子环境联想到该有机物碳架结构的
对称性而快速进行解题。
(4)由加氢后的碳架结构可确定碳碳双键或碳碳三键的位置。
(5)由有机物发生酯化反应能生成环酯或高聚酯,可确定该有机物是含羟基的羧酸;根据酯的结构,可
确定—OH与—COOH的相对位置。
4.根据关键数据推断官能团的数目
(1)—CHO
(2)2—OH(醇、酚、羧酸)――→H。
2
(3)2—COOH―――→CO,—COOH――→CO。
2 2
(4) ――→ ――→—C≡C—――→
(5)RCHOH――――→CHCOOCH R。
2 3 2
(M) (M+42)
r r
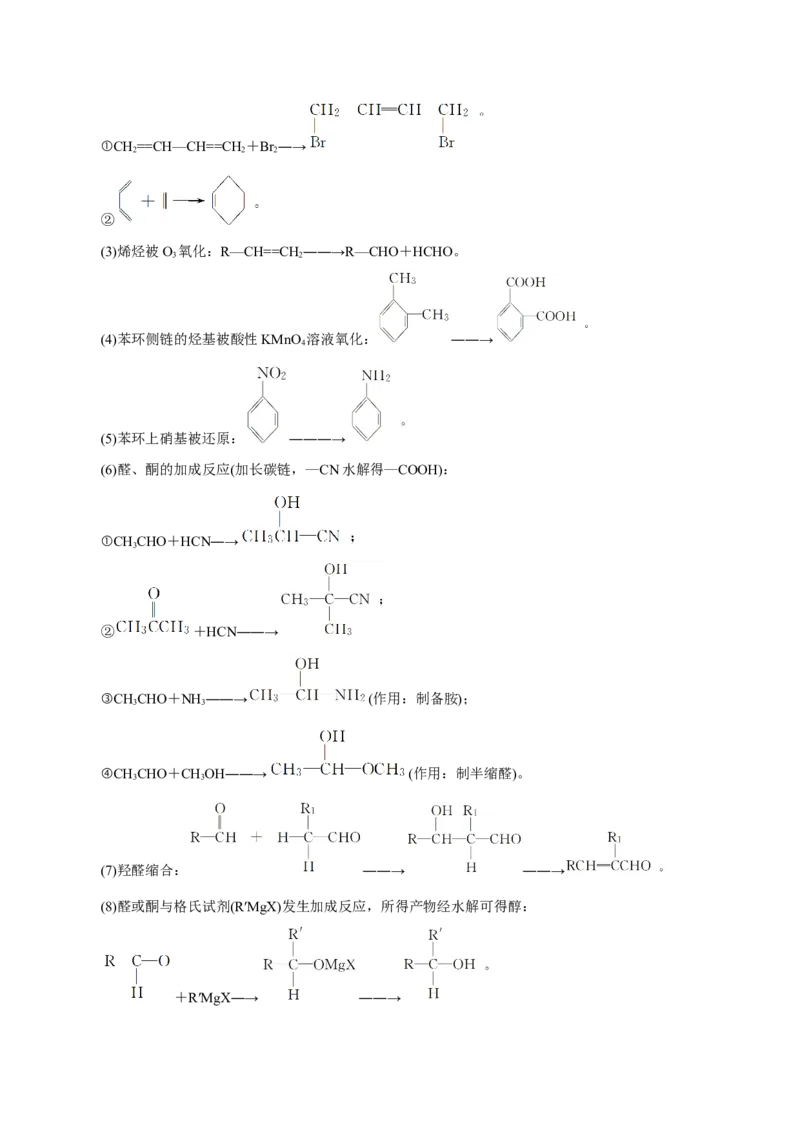
5.根据新信息类推
高考常见的新信息反应总结
(1)丙烯α-H被取代的反应:CH—CH==CH+Cl――→Cl—CH —CH==CH +HCl。
3 2 2 2 2
(2)共轭二烯烃的1,4-加成反应:①CH==CH—CH==CH +Br ―→
2 2 2
②
(3)烯烃被O 氧化:R—CH==CH ――→R—CHO+HCHO。
3 2
(4)苯环侧链的烃基被酸性KMnO 溶液氧化: ――→
4
(5)苯环上硝基被还原: ―――→
(6)醛、酮的加成反应(加长碳链,—CN水解得—COOH):
①CHCHO+HCN―→
3
② +HCN――→
③CH CHO+NH ――→ (作用:制备胺);
3 3
④CH CHO+CHOH――→ (作用:制半缩醛)。
3 3
(7)羟醛缩合: ――→ ――→
(8)醛或酮与格氏试剂(R′MgX)发生加成反应,所得产物经水解可得醇:
+R′MgX―→ ――→(9)羧酸分子中的α-H被取代的反应:
RCHCOOH+Cl――→ +HCl。
2 2
(10)羧酸用LiAlH 还原时,可生成相应的醇:RCOOH――→RCHOH。
4 2
(11)酯交换反应(酯的醇解):R COOR +R OH―→R COOR +R OH。
1 2 3 1 3 2
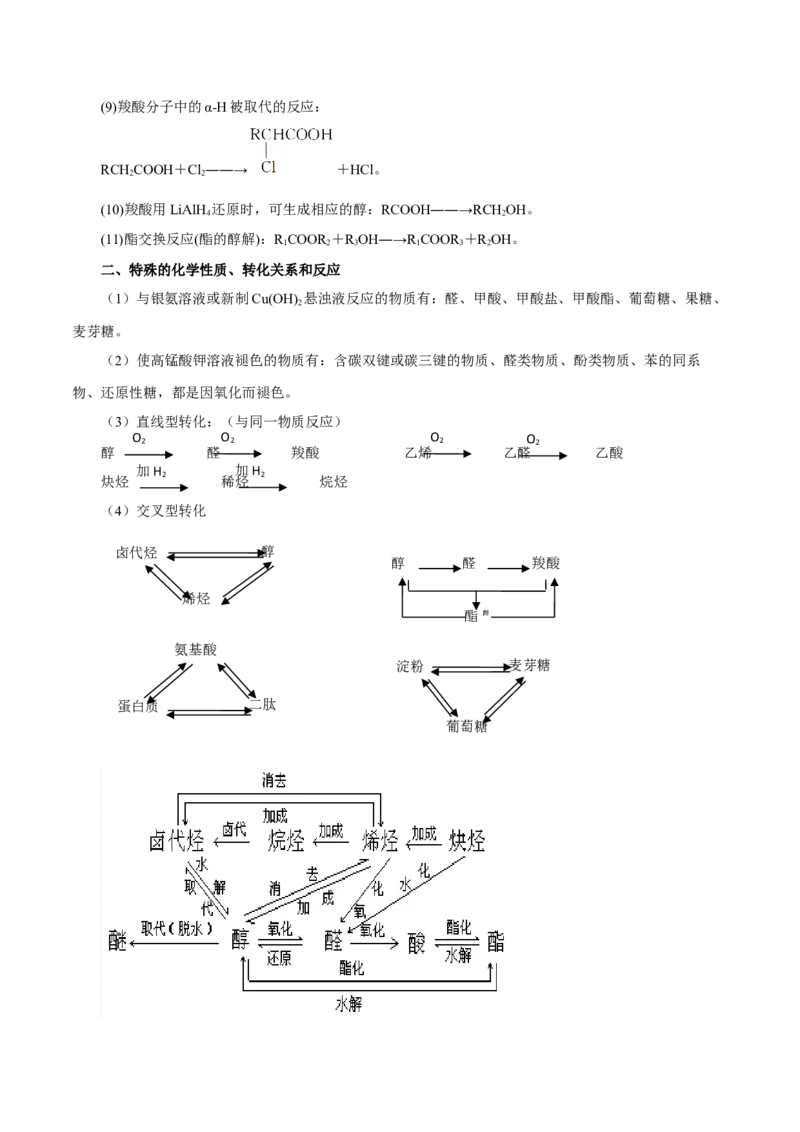
二、特殊的化学性质、转化关系和反应
(1)与银氨溶液或新制Cu(OH) 悬浊液反应的物质有:醛、甲酸、甲酸盐、甲酸酯、葡萄糖、果糖、
2
麦芽糖。
(2)使高锰酸钾溶液褪色的物质有:含碳双键或碳三键的物质、醛类物质、酚类物质、苯的同系
物、还原性糖,都是因氧化而褪色。
(3)直线型转化:(与同一物质反应)
O 2 O 2 O 2 O 2
醇 醛 羧酸 乙烯 乙醛 乙酸
加H 加H
炔烃 2 稀烃 2 烷烃
(4)交叉型转化
卤代烃 醇
醇 醛 羧酸
烯烃
酯 醇
氨基酸
淀粉 麦芽糖
蛋白质 二肽
葡萄糖(5)能形成环状物质的反应有:多元醇(大于或等于二元,以下同)和多元羧酸酯化反应、羟基羧
酸分子间或分子内酯化反应、氨基酸分子间或分子内脱水、多元醇分子内或分子间脱水、多元羧酸分子间
或分子内脱水。
【核心题型例解】
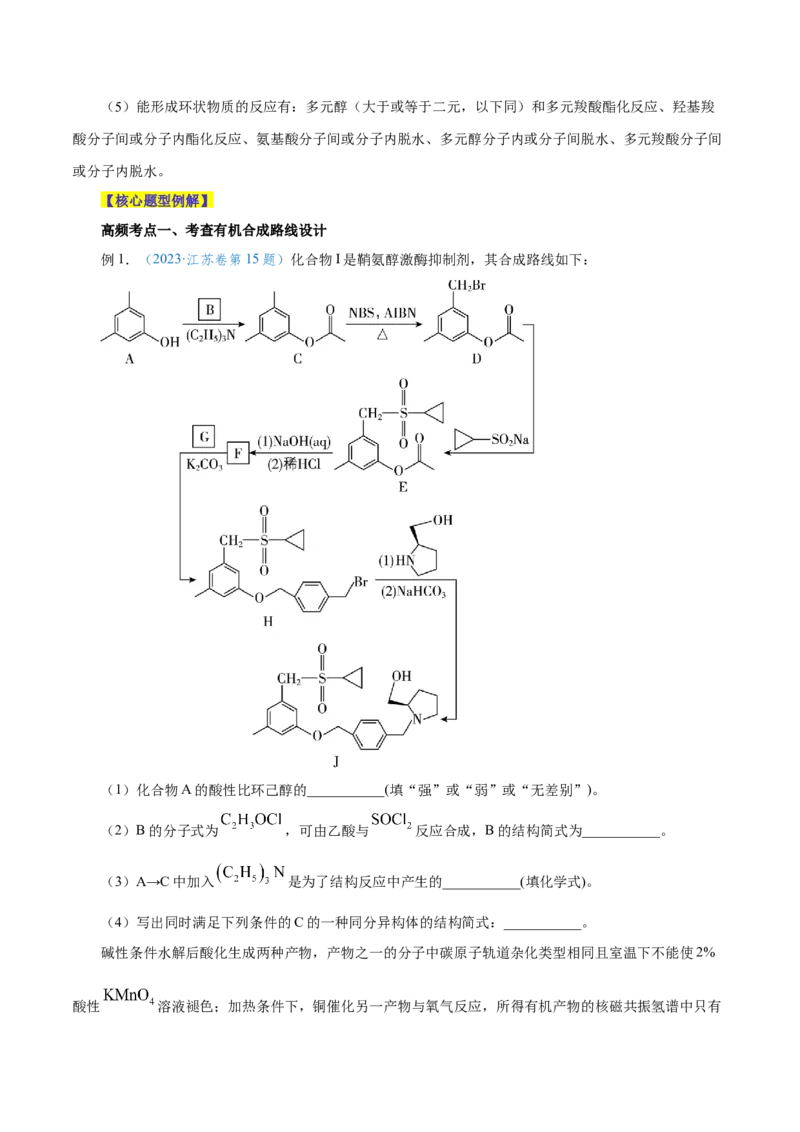
高频考点一、考查有机合成路线设计
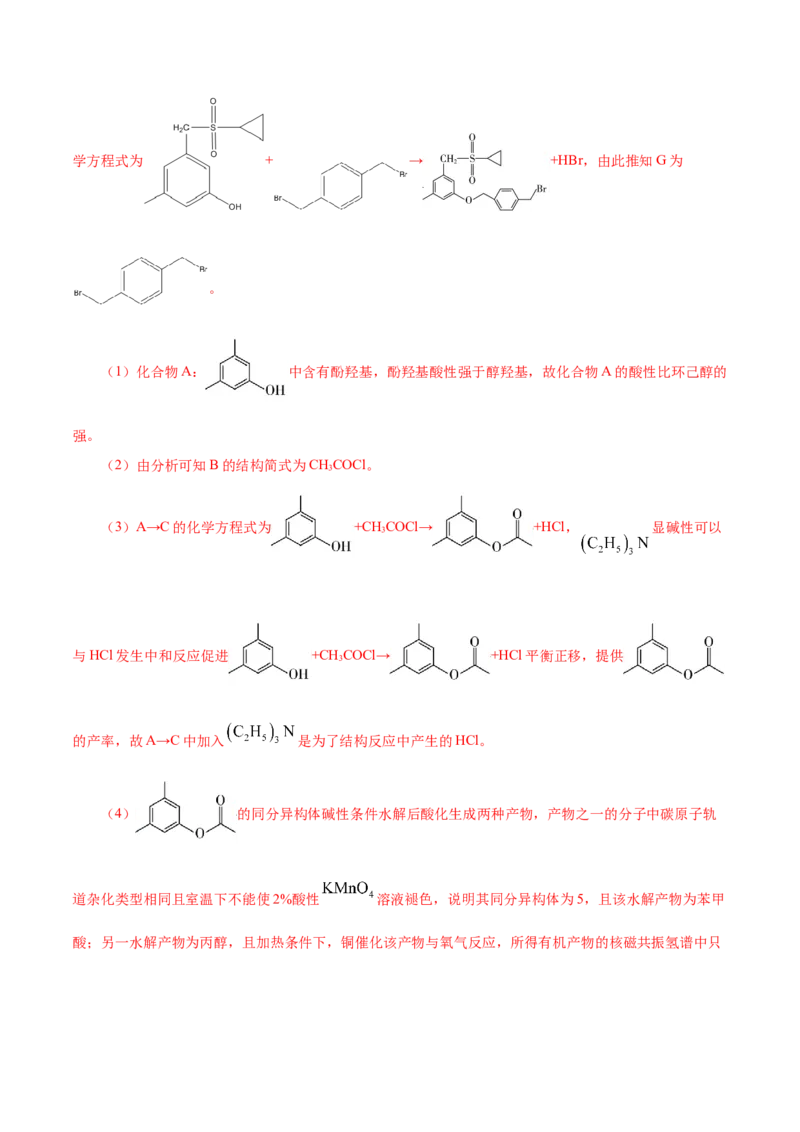
例1.(2023·江苏卷第15题)化合物I是鞘氨醇激酶抑制剂,其合成路线如下:
(1)化合物A的酸性比环己醇的___________(填“强”或“弱”或“无差别”)。
(2)B的分子式为 ,可由乙酸与 反应合成,B的结构简式为___________。
(3)A→C中加入 是为了结构反应中产生的___________(填化学式)。
(4)写出同时满足下列条件的C的一种同分异构体的结构简式:___________。
碱性条件水解后酸化生成两种产物,产物之一的分子中碳原子轨道杂化类型相同且室温下不能使2%
酸性 溶液褪色;加热条件下,铜催化另一产物与氧气反应,所得有机产物的核磁共振氢谱中只有1个峰。
(5)G的分子式为 ,F→H的反应类型为___________。
(6)写出以 、 和 为原料制备 的合成路线流图
___________ (须用NBS和AlBN,无机试剂和有机溶剂任用,合成路线流程图示例见本题题干)。
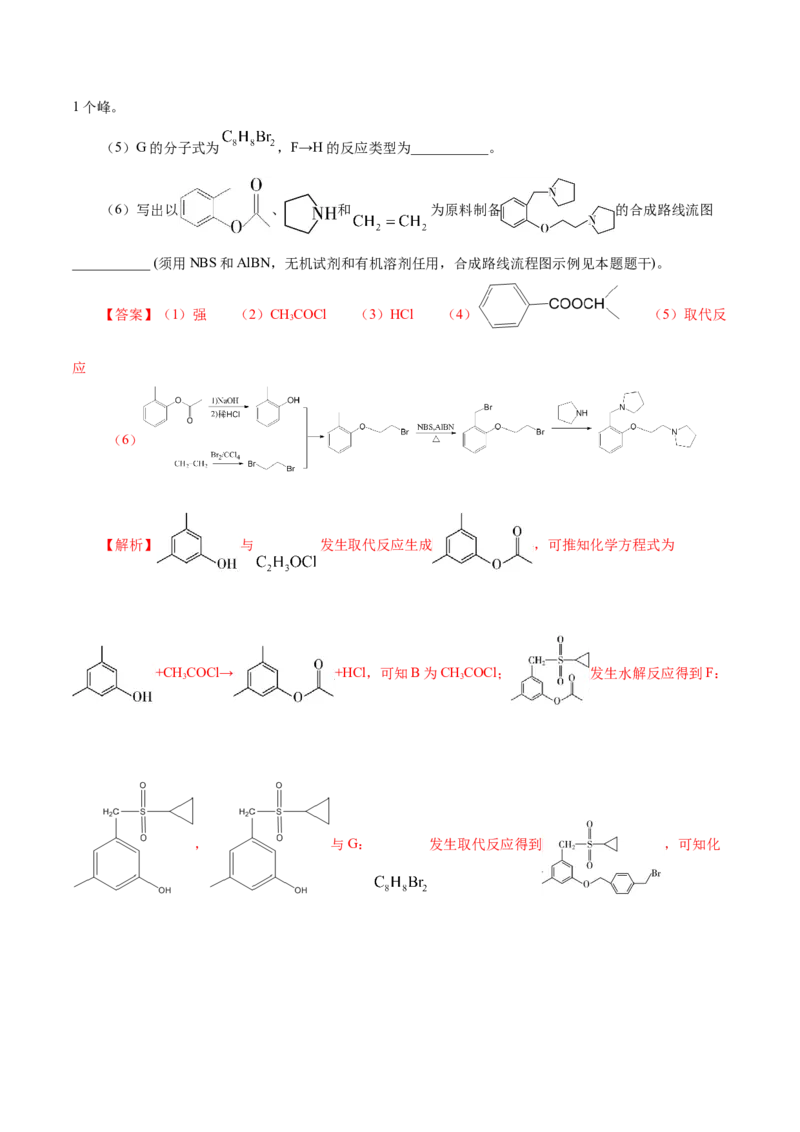
【答案】(1)强 (2)CHCOCl (3)HCl (4) (5)取代反
3
应
(6)
【解析】 与 发生取代反应生成 ,可推知化学方程式为
+CH COCl→ +HCl,可知B为CHCOCl; 发生水解反应得到F:
3 3
, 与G: 发生取代反应得到 ,可知化学方程式为 + → +HBr,由此推知G为
。
(1)化合物A: 中含有酚羟基,酚羟基酸性强于醇羟基,故化合物A的酸性比环己醇的
强。
(2)由分析可知B的结构简式为CHCOCl。
3
(3)A→C的化学方程式为 +CH COCl→ +HCl, 显碱性可以
3
与HCl发生中和反应促进 +CH COCl→ +HCl平衡正移,提供
3
的产率,故A→C中加入 是为了结构反应中产生的HCl。
(4) 的同分异构体碱性条件水解后酸化生成两种产物,产物之一的分子中碳原子轨
道杂化类型相同且室温下不能使2%酸性 溶液褪色,说明其同分异构体为5,且该水解产物为苯甲
酸;另一水解产物为丙醇,且加热条件下,铜催化该产物与氧气反应,所得有机产物的核磁共振氢谱中只有1个峰,由此确定该醇为2-丙醇,由此确定 的同分异构体为 。
(5)由分析可知F→H的反应为 + →
+HBr,该反应为取代反应。
(6)结合F→H可设计以下合成路线:
。
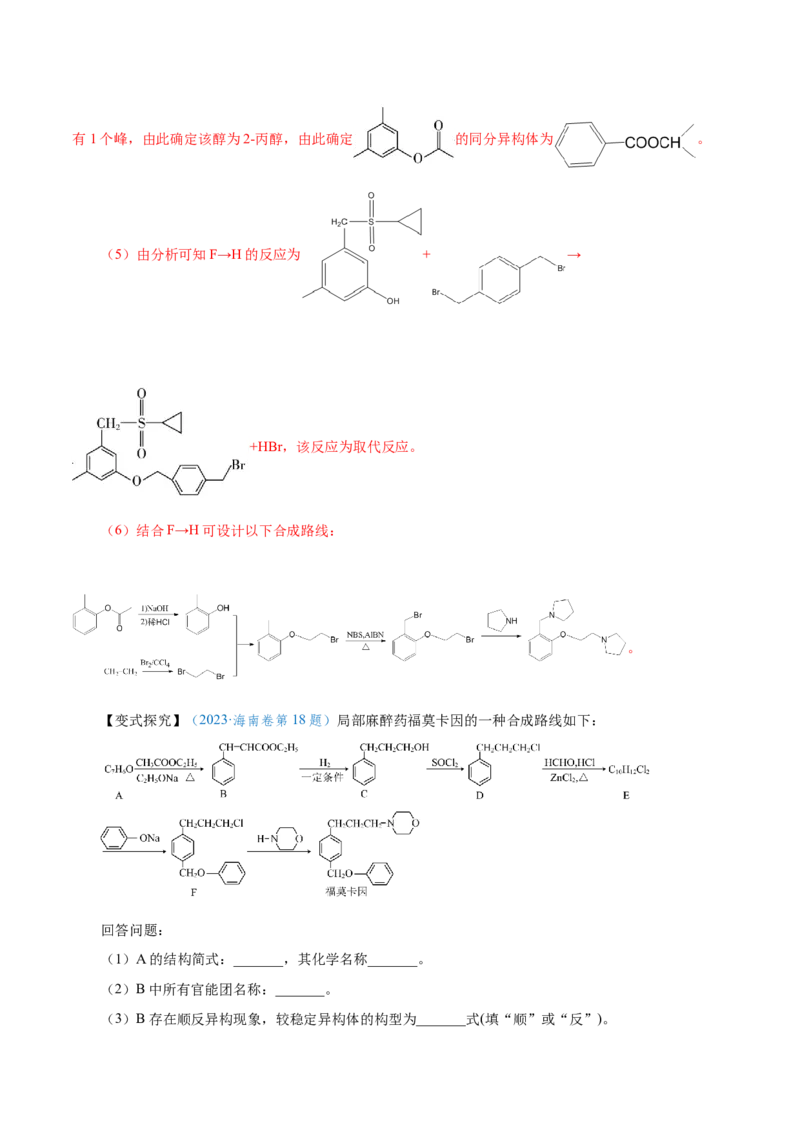
【变式探究】(2023·海南卷第18题)局部麻醉药福莫卡因的一种合成路线如下:
回答问题:
(1)A的结构简式:_______,其化学名称_______。
(2)B中所有官能团名称:_______。
(3)B存在顺反异构现象,较稳定异构体的构型为_______式(填“顺”或“反”)。(4)B→C的反应类型为_______。
(5)与E互为同分异构体之——X,满足条件①含有苯环②核磁共振氢谱只有1组吸收峰,则X的简
式为:_______(任写一种)
(6)E→F的反应方程式为_______。
(7)结合下图合成路线的相关信息。以苯甲醛和一两个碳的有机物为原料,设计路线合成
_______。
【答案】(1) 苯甲醛 (2)碳碳双键、酯基 (3)反 (4)还原反应
(5) (6)
(7)
【解析】结合B的结构式,可逆向推得A的结构为 ,B与氢气一定条件下反应还原
生成C,C在SOCl2条件下发生取代反应生成D,D在HCHO、HCl、ZnCl,发生取代反应生成E(
2
),E与 发生取代生成F,F与 发生取代反应生成
福莫卡因。
(1)结合上述分析可知,A的结构简式: ,其化学名称苯甲醛;
(2)结合题干信息中B的结构式,B中所有官能团名称碳碳双键、酯基;
(3)顺式中的两个取代基处于同一侧,空间比较拥挤,范德华力较大,分子内能较高,不稳定,反
式较顺式稳定;
(4)结合上述分析,B→C的反应类型为还原反应;(5)E的结构为 ,同分异构体满足①含有苯环②核磁共振氢谱只有1组吸收
峰,说明结构高度对称,则X的一种结构简式为 ;
(6)E→F的反应方程式为: ;
(7)乙醇分别催化氧化为乙醛、乙酸,乙酸与乙醇发生酯化反应生成乙酸乙酯,乙醛 乙酸乙酯反应
生成CHCH=CHCOOC H;苯甲醛与CHCH=CHCOOC H 反应生成 ,再水解生成
3 2 5 3 2 5
,合成路线为:
。
【变式探究】(2023·广东卷)室温下可见光催化合成技术,对于人工模仿自然界、发展有机合成新方
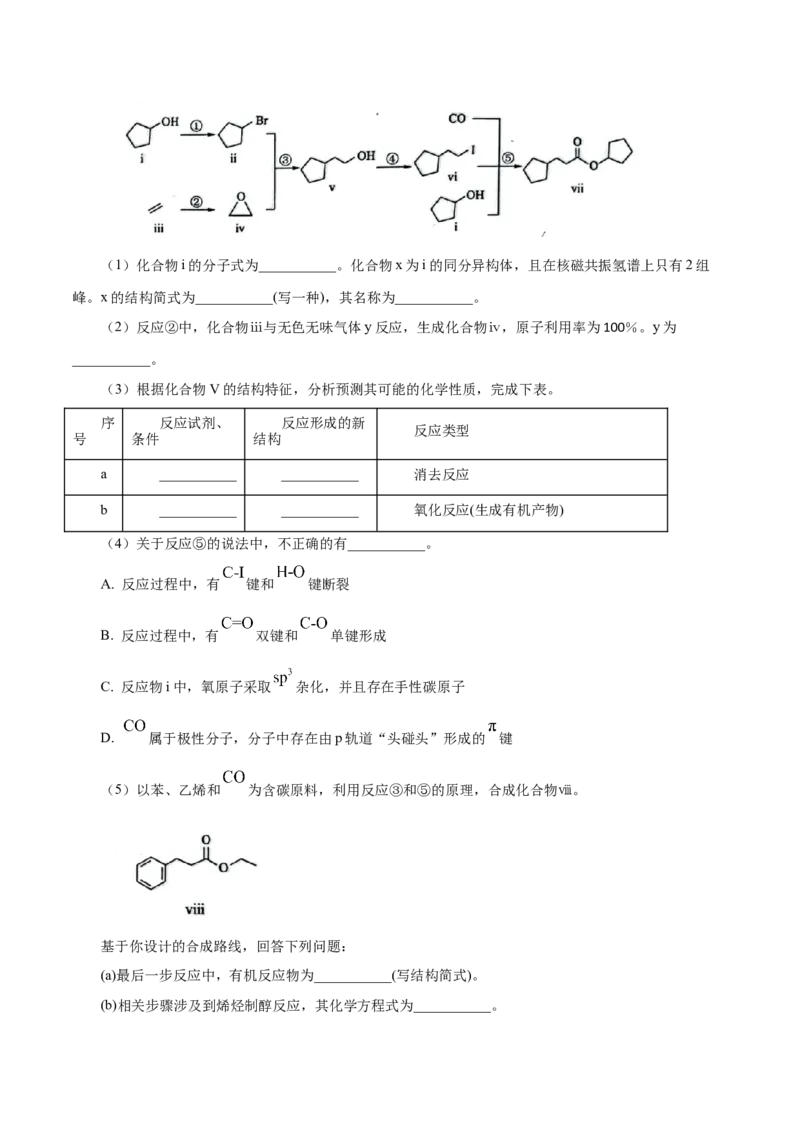
法意义重大。一种基于CO、碘代烃类等,合成化合物ⅶ的路线如下(加料顺序、反应条件略):(1)化合物i的分子式为___________。化合物x为i的同分异构体,且在核磁共振氢谱上只有2组
峰。x的结构简式为___________(写一种),其名称为___________。
(2)反应②中,化合物ⅲ与无色无味气体y反应,生成化合物ⅳ,原子利用率为100%。y为
___________。
(3)根据化合物V的结构特征,分析预测其可能的化学性质,完成下表。
序 反应试剂、 反应形成的新
反应类型
号 条件 结构
a ___________ ___________ 消去反应
b ___________ ___________ 氧化反应(生成有机产物)
(4)关于反应⑤的说法中,不正确的有___________。
A. 反应过程中,有 键和 键断裂
B. 反应过程中,有 双键和 单键形成
C. 反应物i中,氧原子采取 杂化,并且存在手性碳原子
D. 属于极性分子,分子中存在由p轨道“头碰头”形成的 键
(5)以苯、乙烯和 为含碳原料,利用反应③和⑤的原理,合成化合物ⅷ。
基于你设计的合成路线,回答下列问题:
(a)最后一步反应中,有机反应物为___________(写结构简式)。
(b)相关步骤涉及到烯烃制醇反应,其化学方程式为___________。(c)从苯出发,第一步的化学方程式为___________(注明反应条件)。
【答案】(1) C H O (或 或 ) 3-戊酮(或2,2-二甲基丙
5 10
醛或3,3-二甲基氧杂环丁烷) (2)O 或氧气
2
(3) 浓硫酸,加热 O 、Cu,加热(或酸性KMnO 溶液)
2 4
(或 ) (4)CD
(5) 和CH CH OH
3 2
【解析】 与HBr加热发生取代反应生成 ,②乙烯在催化剂作用下氧化生成
,③ 与 发生开环加成生成 ,④ 发生取代反应生成
,⑤ 与 及CO反应生成 。
(1)化合物i 的分子式为C H O。 不饱和度为1,x可形成碳碳双键或碳氧双
5 10
键或一个圆环,化合物x为i的同分异构体,且在核磁共振氢谱上只有2组峰,说明分子中有对称结构,不对称的部分放在对称轴上,x的结构简式含酮羰基时为 (或含醛基时为 或含圆环
是为 ),其名称为3-戊酮(或2,2-二甲基丙醛或3,3-二甲基氧杂环丁烷)。
(2)反应②中,化合物ⅲ与无色无味气体y反应,生成化合物ⅳ,原子利用率为100%,②乙烯在催
化剂作用下氧化生成 ,y为O 或氧气。
2
(3)根据化合物V 的结构特征,分析预测其可能的化学性质:含有羟基,且与羟基
相连的碳的邻碳上有氢,可在浓硫酸、加热条件下发生消去反应生成 ,与羟基相连的碳上有
氢,可在铜或银催化作用下氧化生成 ,或酸性KMnO 溶液中氧化生成
4
,见下表:
序号 反应试剂、条件 反应形成的新结构 反应类型
a 浓硫酸,加热 消去反应
O 、Cu,,
2 氧化反应(生成有机
b 加热(或酸性 (或 )
产物)
KMnO 溶液)
4
(4)从产物中不存在C-I键和H-O键可以看出,反应过程中,有C-I键和H-O键断裂,故A正确;反
应物中不存在CCOO双键,酰碘基中碘原子离去与羟基中氢离去,余下的部分结合形成酯基中C-O单键,所以反应过程中,有C=O双键和C-O单键形成,故B正确;反应物i 中,氧原子采取sp3杂化,
但与羟基相连的碳有对称轴,其它碳上均有2个氢,分子中不存在手性碳原子,故C错误;CO属于极性分
子,分子中存在由p轨道“肩并肩”形成的π键,故D错误;故答案为CD;
(5)以苯、乙烯和CO为含碳原料,利用反应③和⑤的原理,合成化合物ⅷ。乙烯与水在催化剂加热
加压条件下合成乙醇;乙烯在银催化作用下氧化生成环氧乙醚;苯在铁催化作用下与溴生成溴苯,溴苯与
环氧乙醚生成 ,与HI反应合成 ,最后根据反应⑤的原理, 与
乙醇、CO合成化合物ⅷ。(a)最后一步反应中,有机反应物为 和CH CH OH。 (b)相关步骤
3 2
涉及到烯烃制醇反应,其化学方程式为 。 (c)从苯出发,第一
步的化学方程式为 。
高频考点二、考查有机合成与同分异构体
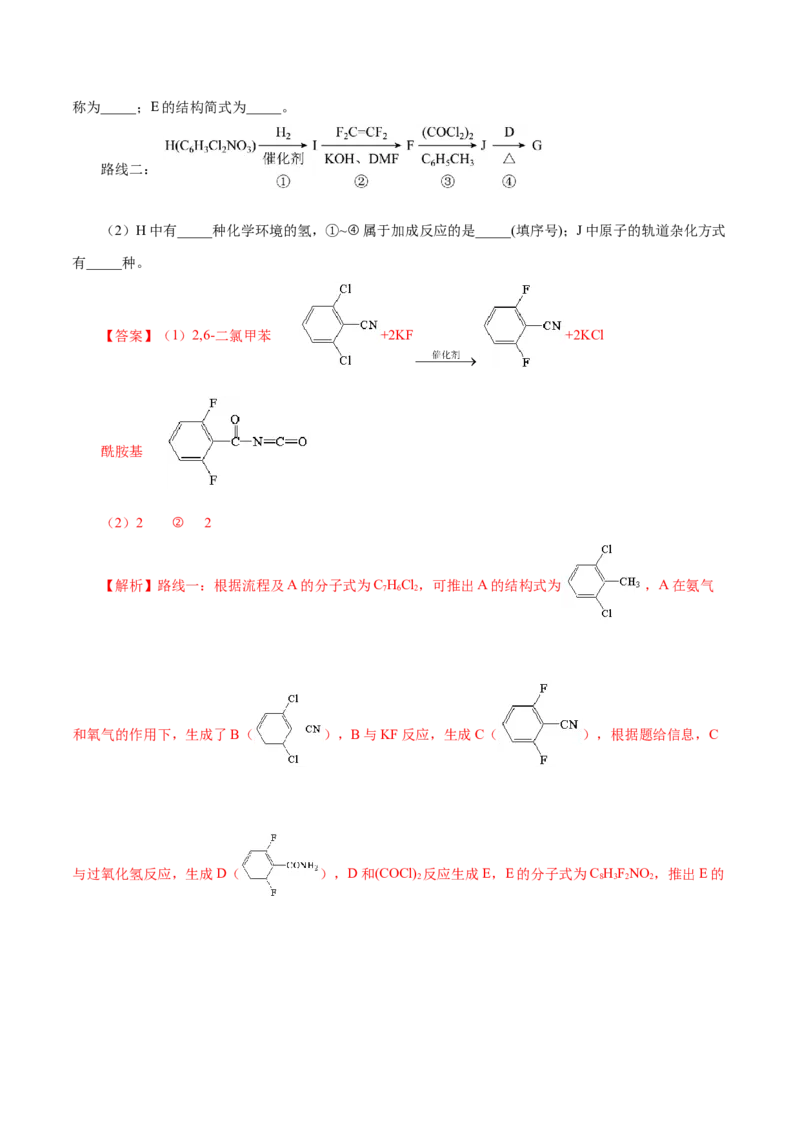
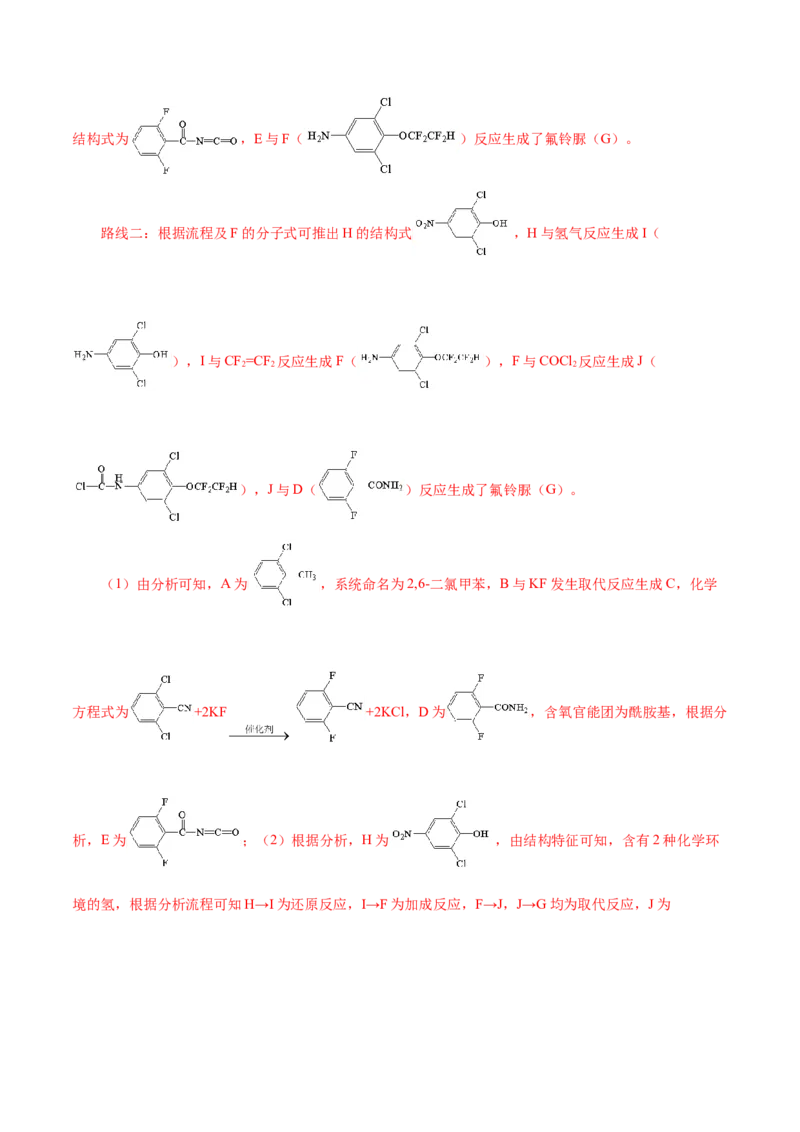
例2.(2023·山东卷第19题)根据杀虫剂氟铃脲(G)的两条合成路线,回答下列问题。
已知:Ⅰ.R NH +OCNR →
1 2 2
Ⅱ.
路线:
(1)A的化学名称为_____(用系统命名法命名); 的化学方程式为_____;D中含氧官能团的名称为_____;E的结构简式为_____。
路线二:
(2)H中有_____种化学环境的氢,①~④属于加成反应的是_____(填序号);J中原子的轨道杂化方式
有_____种。
【答案】(1)2,6-二氯甲苯 +2KF +2KCl
酰胺基
(2)2 ② 2
【解析】路线一:根据流程及A的分子式为C HCl,可推出A的结构式为 ,A在氨气
7 6 2
和氧气的作用下,生成了B( ),B与KF反应,生成C( ),根据题给信息,C
与过氧化氢反应,生成D( ),D和(COCl) 反应生成E,E的分子式为C HFNO ,推出E的
2 8 3 2 2结构式为 ,E与F( )反应生成了氟铃脲(G)。
路线二:根据流程及F的分子式可推出H的结构式 ,H与氢气反应生成I(
),I与CF=CF 反应生成F( ),F与COCl 反应生成J(
2 2 2
),J与D( )反应生成了氟铃脲(G)。
(1)由分析可知,A为 ,系统命名为2,6-二氯甲苯,B与KF发生取代反应生成C,化学
方程式为 +2KF +2KCl,D为 ,含氧官能团为酰胺基,根据分
析,E为 ;(2)根据分析,H为 ,由结构特征可知,含有2种化学环
境的氢,根据分析流程可知H→I为还原反应,I→F为加成反应,F→J,J→G均为取代反应,J为,C原子的杂化方式有sp2,sp3两种,NO原子的杂化方式均为sp3,所以J中
原子的杂化方式有2种。
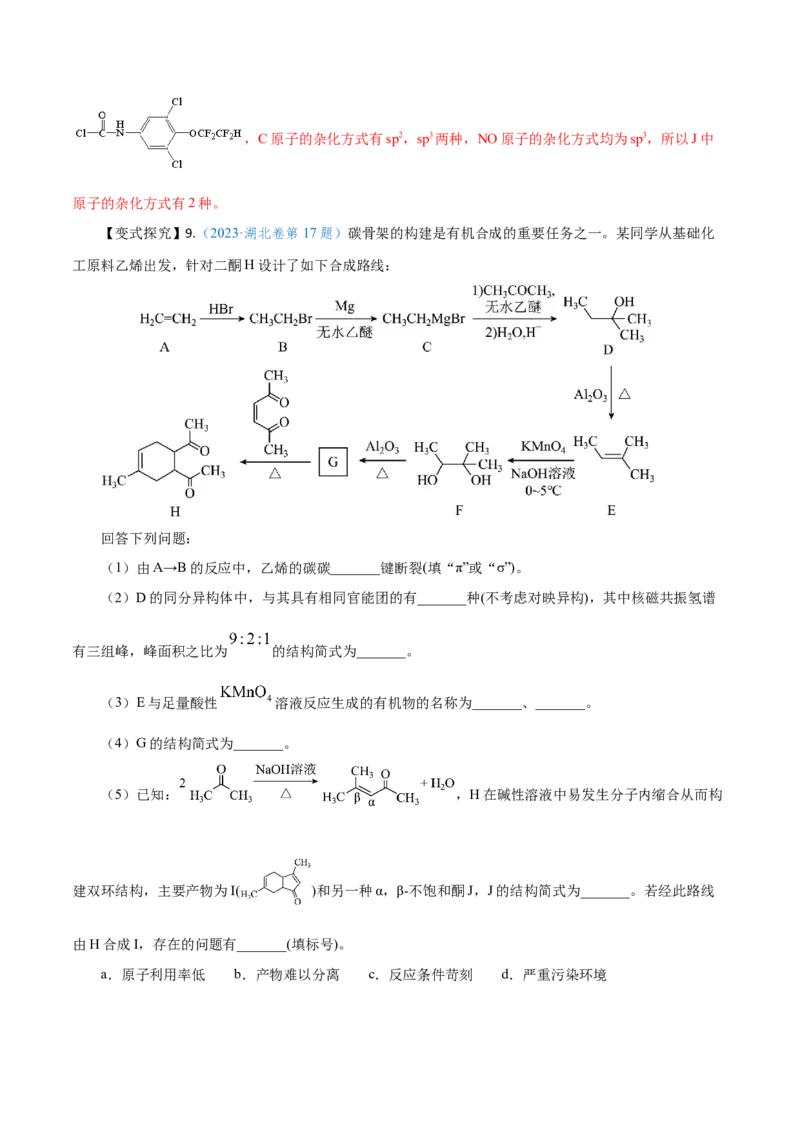
【变式探究】9.(2023·湖北卷第17题)碳骨架的构建是有机合成的重要任务之一。某同学从基础化
工原料乙烯出发,针对二酮H设计了如下合成路线:
回答下列问题:
(1)由A→B的反应中,乙烯的碳碳_______键断裂(填“π”或“σ”)。
(2)D的同分异构体中,与其具有相同官能团的有_______种(不考虑对映异构),其中核磁共振氢谱
有三组峰,峰面积之比为 的结构简式为_______。
(3)E与足量酸性 溶液反应生成的有机物的名称为_______、_______。
(4)G的结构简式为_______。
(5)已知: ,H在碱性溶液中易发生分子内缩合从而构
建双环结构,主要产物为I( )和另一种α,β-不饱和酮J,J的结构简式为_______。若经此路线
由H合成I,存在的问题有_______(填标号)。
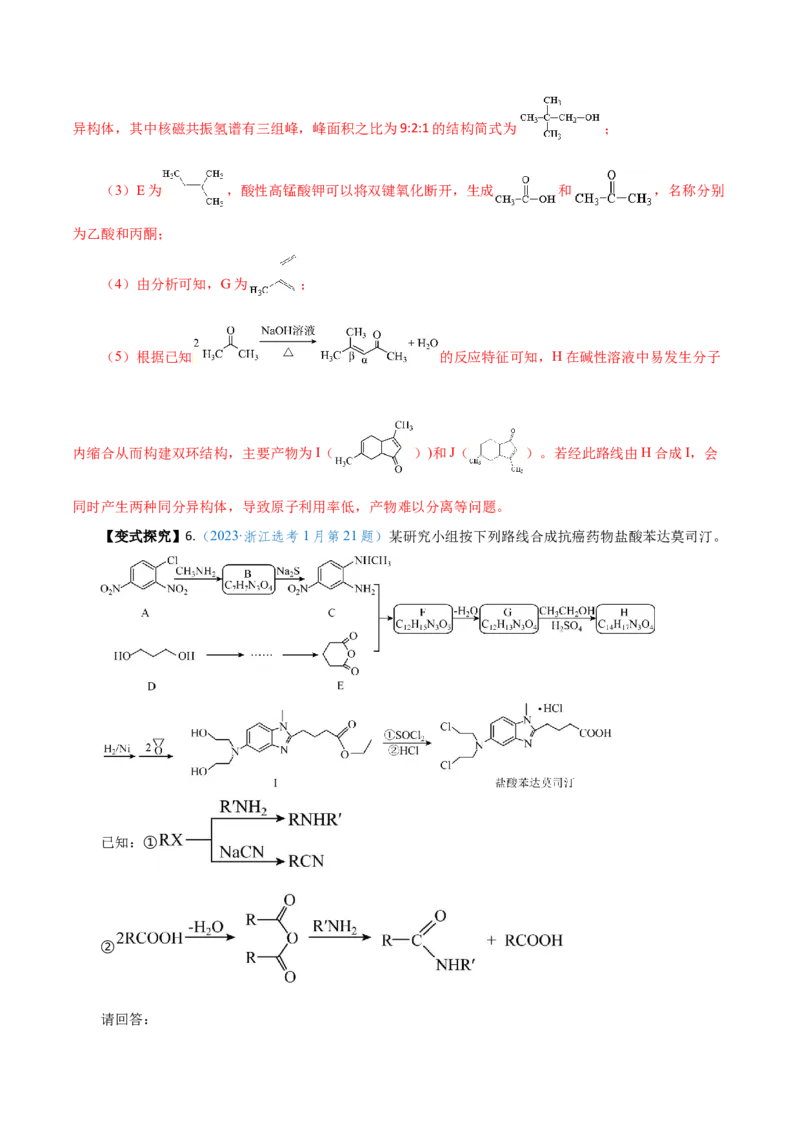
a.原子利用率低 b.产物难以分离 c.反应条件苛刻 d.严重污染环境【答案】(1)π (2)7 (3)乙酸 丙酮
(4) (5) ab
【解析】A为CH=CH ,与HBr发生加成反应生成B(CHCHBr),B与Mg在无水乙醚中发生生成
2 2 3 2
C(CHCHMgBr),C与CHCOCH 反应生成D( ),D在氧化铝催化下发生消去反应生成E
3 2 3 3
( ),E和碱性高锰酸钾反应生成F( ),参考D~E反应,F在氧化铝催化
下发生消去反应生成G( ),G与 反应加成反应生成二酮H,据此分析解答。
(1)A为CH=CH ,与HBr发生加成反应生成B(CHCHBr),乙烯的π键断裂;
2 2 3 2
(2)D为 ,分子式为C H O,含有羟基的同分异构体分别为:
5 12
共8种,除去D自身,还有7种同分异构体,其中核磁共振氢谱有三组峰,峰面积之比为9:2:1的结构简式为 ;
(3)E为 ,酸性高锰酸钾可以将双键氧化断开,生成 和 ,名称分别
为乙酸和丙酮;
(4)由分析可知,G为 ;
(5)根据已知 的反应特征可知,H在碱性溶液中易发生分子
内缩合从而构建双环结构,主要产物为I( ))和J( )。若经此路线由H合成I,会
同时产生两种同分异构体,导致原子利用率低,产物难以分离等问题。
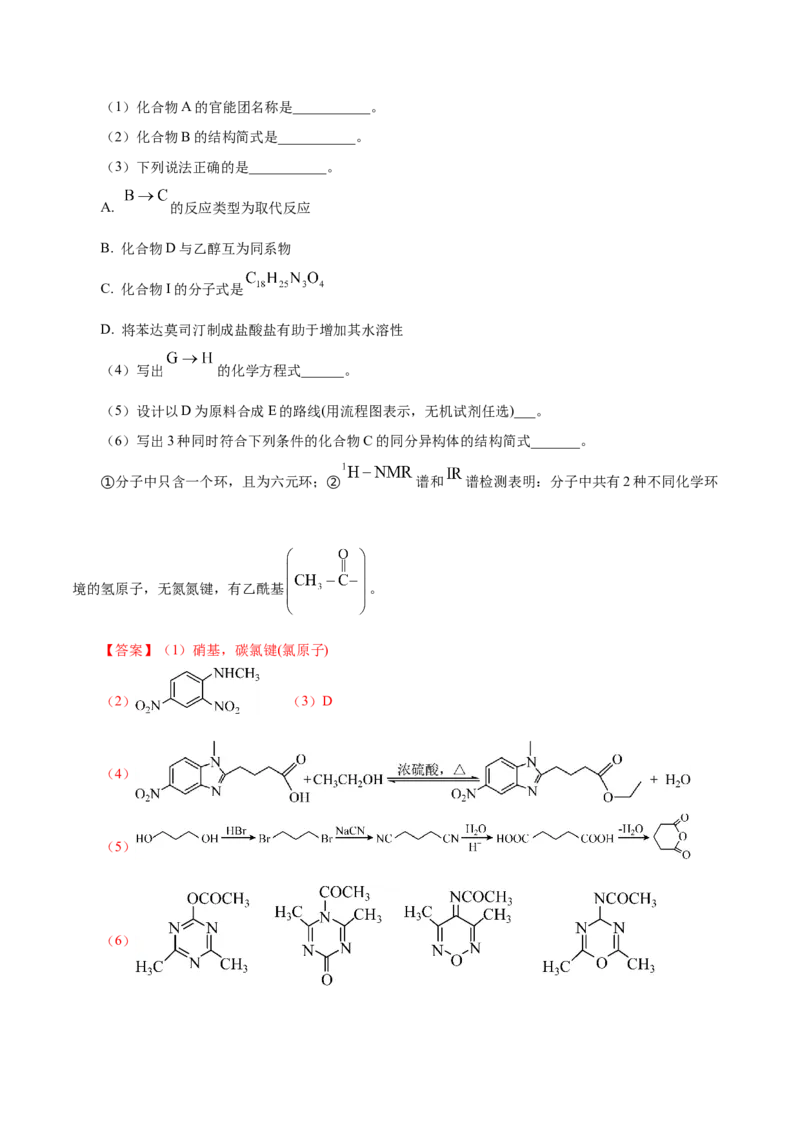
【变式探究】6.(2023·浙江选考1月第21题)某研究小组按下列路线合成抗癌药物盐酸苯达莫司汀。
已知:①
②
请回答:(1)化合物A的官能团名称是___________。
(2)化合物B的结构简式是___________。
(3)下列说法正确的是___________。
A. 的反应类型为取代反应
B. 化合物D与乙醇互为同系物
C. 化合物I的分子式是
D. 将苯达莫司汀制成盐酸盐有助于增加其水溶性
(4)写出 的化学方程式______。
(5)设计以D为原料合成E的路线(用流程图表示,无机试剂任选)___。
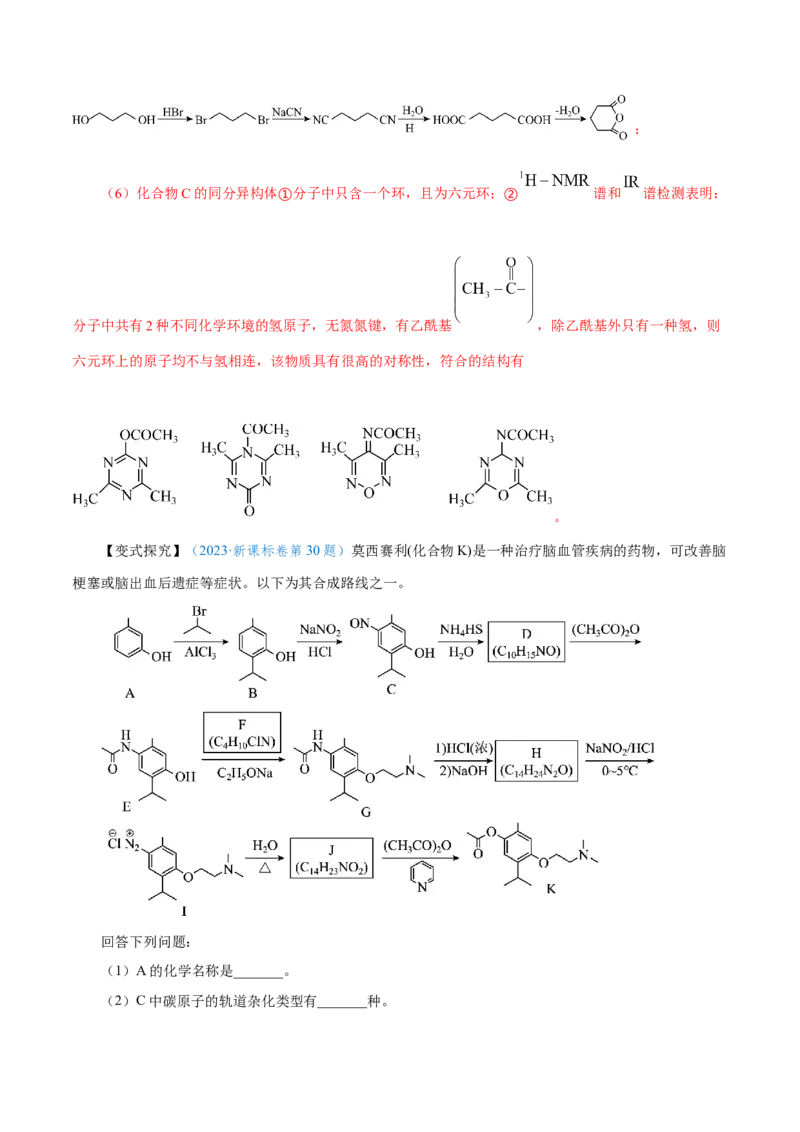
(6)写出3种同时符合下列条件的化合物C的同分异构体的结构简式_______。
①分子中只含一个环,且为六元环;② 谱和 谱检测表明:分子中共有2种不同化学环
境的氢原子,无氮氮键,有乙酰基 。
【答案】(1)硝基,碳氯键(氯原子)
(2) (3)D
(4)
(5)
(6)【解析】 与CHNH 反应生成B,B与硫化钠发生还原反应生成C,结合C的结构可知A
3 2
到B为取代反应,B为 ,C与E发生已知中反应生成F,F为
,F脱水生成G ,G与乙醇发生酯化反应生成H
,H与氢气加成后再与环氧乙烷发生反应生成I,I与SOCl 发生取代反应后
2
再与盐酸反应生成盐酸苯达莫司汀,据此分析解答。
(1)由A的结构可知其所含官能团为硝基和氯原子;
(2)由以上分析可知化合物B的结构简式 ;
(3) 的反应中B中一个硝基转化为氨基,反应类型为还原反应,故A错误;化合物D中含有
两个羟基,与乙醇不是同系物,故B错误;化合物I的分子式是 ,故C错误;将苯达莫司汀
制成盐酸盐,可以增加其水溶性,利于吸收,故D正确;故答案为D;
(4)G与乙醇发生酯化反应生成H ,反应方程式为:
;
(5)1,3-丙二醇与HBr发生取代反应生成1,3-二溴丙烷,1,3-二溴丙烷与NaCN发生取代反应生
成 , 发生水解生成戊二酸,戊二酸分子内脱水生成 ,合成路线为:;
(6)化合物C的同分异构体①分子中只含一个环,且为六元环;② 谱和 谱检测表明:
分子中共有2种不同化学环境的氢原子,无氮氮键,有乙酰基 ,除乙酰基外只有一种氢,则
六元环上的原子均不与氢相连,该物质具有很高的对称性,符合的结构有
。
【变式探究】(2023·新课标卷第30题)莫西赛利(化合物K)是一种治疗脑血管疾病的药物,可改善脑
梗塞或脑出血后遗症等症状。以下为其合成路线之一。
回答下列问题:
(1)A的化学名称是_______。
(2)C中碳原子的轨道杂化类型有_______种。(3)D中官能团的名称为_______、_______。
(4)E与F反应生成G的反应类型为_______。
(5)F的结构简式为_______。
(6)I转变为J的化学方程式为_______。
(7)在B的同分异构体中,同时满足下列条件的共有_______种(不考虑立体异构);
①含有手性碳;②含有三个甲基;③含有苯环。
其中,核磁共振氢谱显示为6组峰,且峰面积比为3:3:3:2:2:1的同分异构体的结构简式为_______。
【答案】(1)3-甲基苯酚(间甲基苯酚) (2)2 (3) 氨基 羟基 (4)取代反应
(5)
(6) +H O +HCl+N ↑ (7) 9
2 2
【解析】根据流程,A与2-溴丙烷发生取代反应生成B,B与NaNO 发生反应生成C,C与NH HS反
2 4
应生成D,D与乙酸酐[(CH CO) O]反应生成E,结合E的结构简式和D的分子式可知,D为 ;E
3 2
与F反应生成G,结合E和G的结构简式和F的分子式可知,F为 ;G发生两步反应生成H,
H再与NaNO /HCl反应生成I,结合I的结构和H的分子式可知,H为 ;I与水反应生成J,J
2
与乙酸酐[(CH CO) O]反应生成K,结合K的结构简式和J的分子式可知,J为 ;据此分析解
3 2
题。
(1)根据有机物A的结构,有机物A的化学名称为3-甲基苯酚(间甲基苯酚)。
(2)有机物C中含有苯环,苯环上的C原子的杂化类型为sp2杂化,还含有甲基和异丙基,甲基和异
丙基上的C原子的杂化类型为sp3杂化,故答案为2种。(3)根据分析,有机物D的结构为 ,其官能团为氨基和羟基。
(4)有机物E与有机物F发生反应生成有机物G,有机物中的羟基与有机物F中的Cl发生取代反应
生成有机物G,故反应类型为取代反应。
(5)根据分析,有机物F的结构简式为 。
(6)有机物I与水反应生成有机物J,该反应的方程式为 +H O
2
+HCl+N ↑。
2
(7)连有4个不同原子或原子团的碳原子称为手性碳原子。在B的同分异构体中,含有手性碳、含
有3个甲基、含有苯环的同分异构体有9种,分别为: 、 、 、 、
、 、 、 、 ;其中,核磁共振氢谱显示为6组峰,且峰面积比为
3:3:3:2:2:1的同分异构体的结构简式为 。
高频考点三、综合考查有机推断
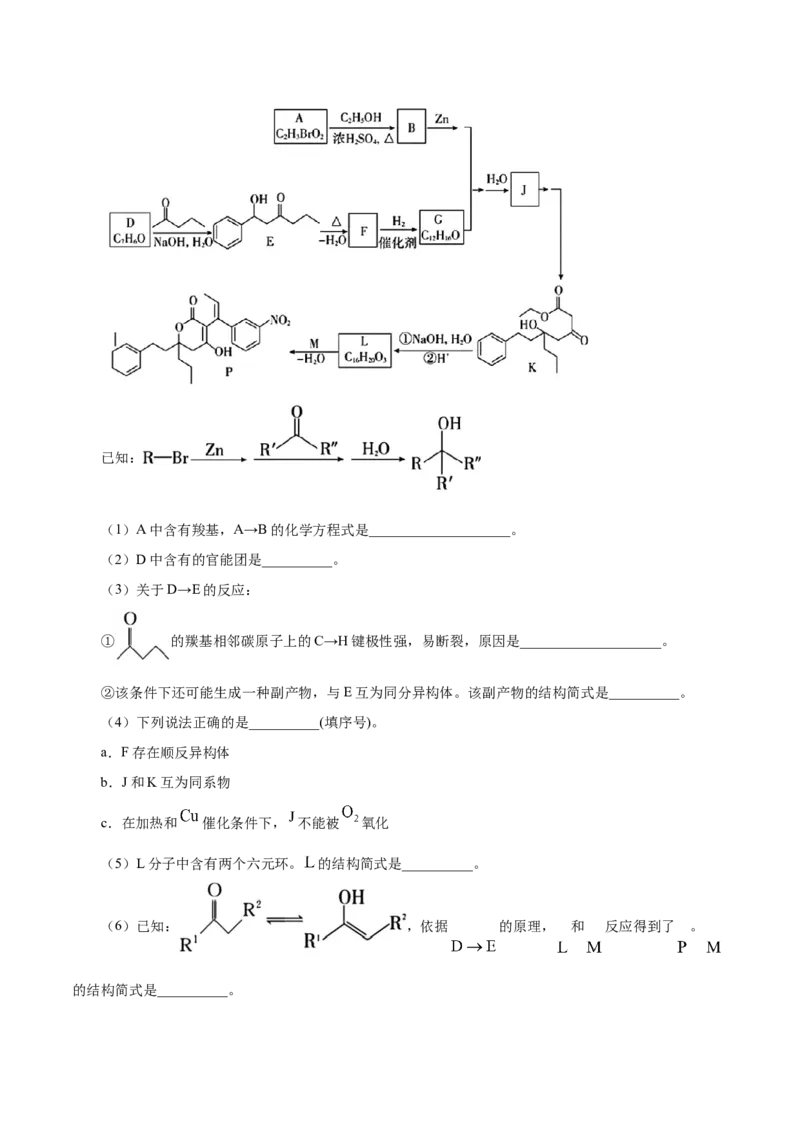
例3.(2023·北京卷第17题)化合物P是合成抗病毒药物普拉那韦的原料,其合成路线如下。已知:
(1)A中含有羧基,A→B的化学方程式是____________________。
(2)D中含有的官能团是__________。
(3)关于D→E的反应:
① 的羰基相邻碳原子上的C→H键极性强,易断裂,原因是____________________。
②该条件下还可能生成一种副产物,与E互为同分异构体。该副产物的结构简式是__________。
(4)下列说法正确的是__________(填序号)。
a.F存在顺反异构体
b.J和K互为同系物
c.在加热和 催化条件下, 不能被 氧化
(5)L分子中含有两个六元环。 的结构简式是__________。
(6)已知: ,依据 的原理, 和 反应得到了 。
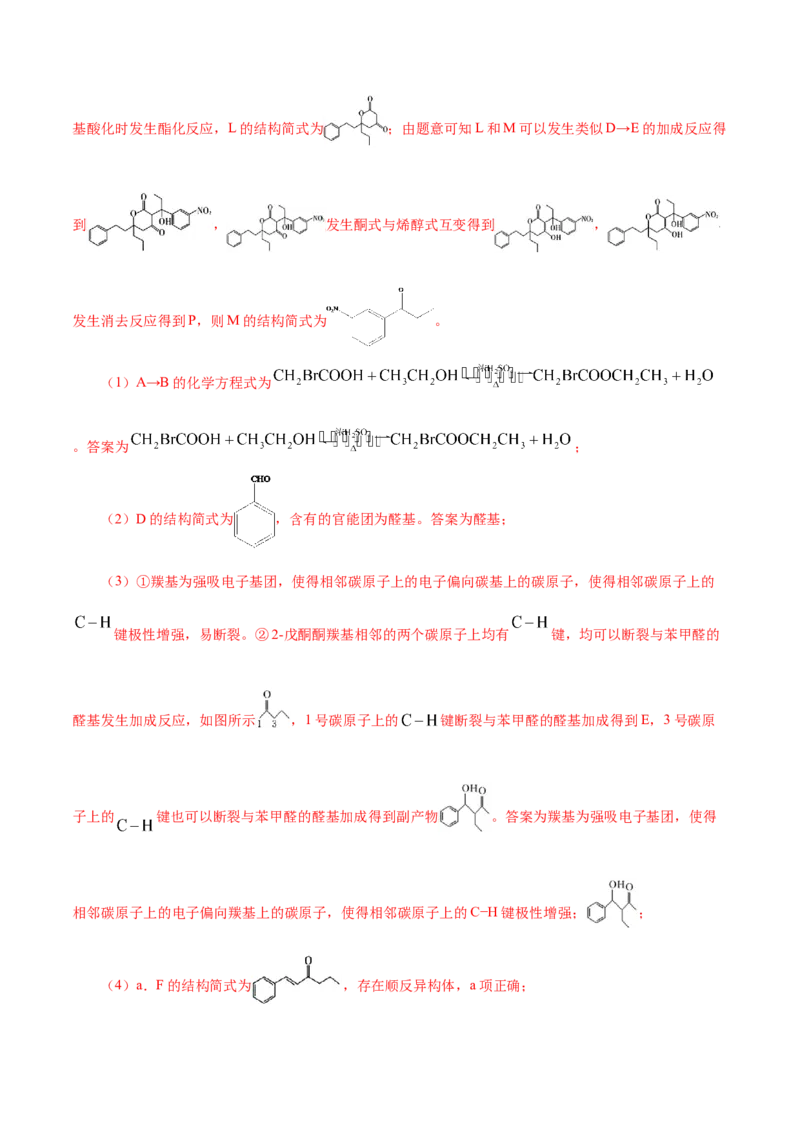
的结构简式是__________。【答案】(1) (2)醛基
(3)羰基为强吸电子基团,使得相邻碳原子上的电子偏向羰基上的碳原子,使得相邻碳原子上的
键极性增强
(4)ac (5) (6)
【解析】A中含有羧基,结合A的分子式可知A为 ;A与乙醇发生酯化反应,B的结
构简式为 ;D与2-戊酮发生加成反应生成E,结合E的结构简式和D的分子式可知
D的结构简式为 ,E发生消去反应脱去1个水分子生成F,F的结构简式为 ,D→F的
整个过程为羟醛缩合反应,结合G的分子式以及G能与B发生已知信息的反应可知G中含有酮羰基,说明
F中的碳碳双键与 发生加成反应生成G,G的结构简式为 ;B与G发生已知信息的反应生成
J,J为 ;K在 溶液中发生水解反应生成 ,酸化得到
;结合题中信息可知L分子中含有两个六元环,由L的分子式可知 中羧基与羟基酸化时发生酯化反应,L的结构简式为 ;由题意可知L和M可以发生类似D→E的加成反应得
到 , 发生酮式与烯醇式互变得到 ,
发生消去反应得到P,则M的结构简式为 。
(1)A→B的化学方程式为
。答案为 ;
(2)D的结构简式为 ,含有的官能团为醛基。答案为醛基;
(3)①羰基为强吸电子基团,使得相邻碳原子上的电子偏向碳基上的碳原子,使得相邻碳原子上的
键极性增强,易断裂。②2-戊酮酮羰基相邻的两个碳原子上均有 键,均可以断裂与苯甲醛的
醛基发生加成反应,如图所示 ,1号碳原子上的 键断裂与苯甲醛的醛基加成得到E,3号碳原
子上的 键也可以断裂与苯甲醛的醛基加成得到副产物 。答案为羰基为强吸电子基团,使得
相邻碳原子上的电子偏向羰基上的碳原子,使得相邻碳原子上的C−H键极性增强; ;
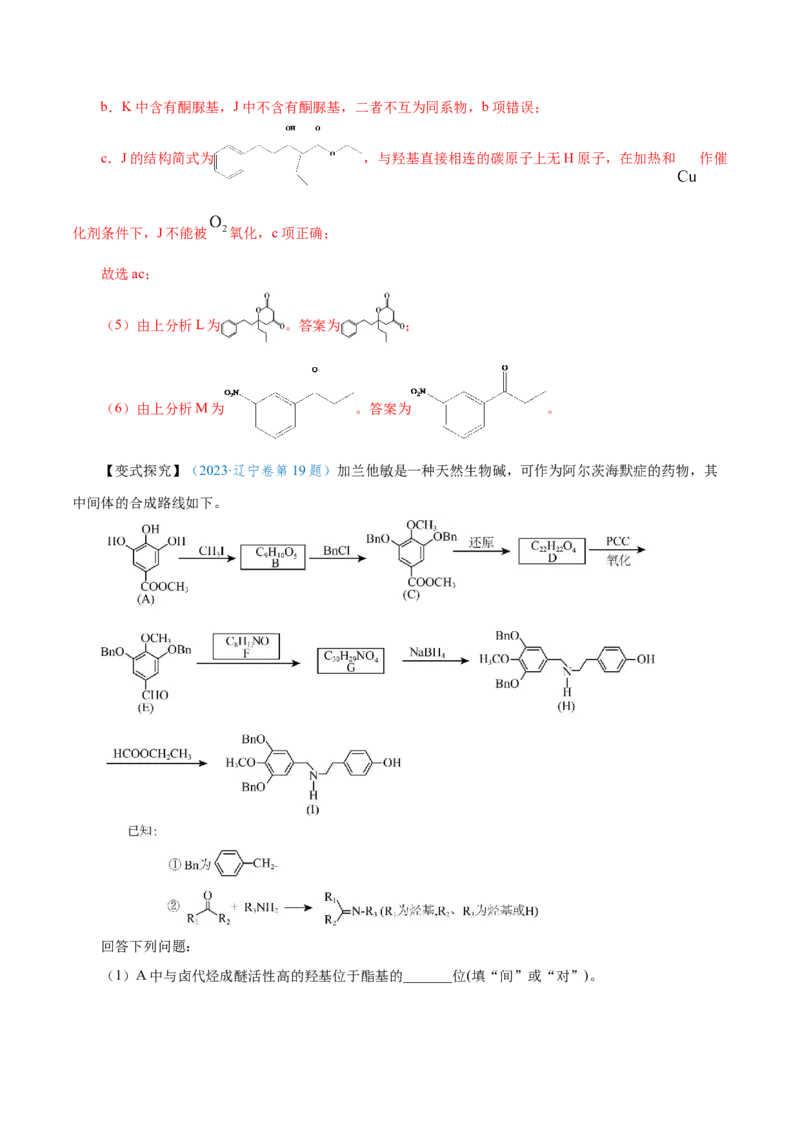
(4)a.F的结构简式为 ,存在顺反异构体,a项正确;b.K中含有酮脲基,J中不含有酮脲基,二者不互为同系物,b项错误;
c.J的结构简式为 ,与羟基直接相连的碳原子上无H原子,在加热和 作催
化剂条件下,J不能被 氧化,c项正确;
故选ac;
(5)由上分析L为 。答案为 ;
(6)由上分析M为 。答案为 。
【变式探究】(2023·辽宁卷第19题)加兰他敏是一种天然生物碱,可作为阿尔茨海默症的药物,其
中间体的合成路线如下。
回答下列问题:
(1)A中与卤代烃成醚活性高的羟基位于酯基的_______位(填“间”或“对”)。的
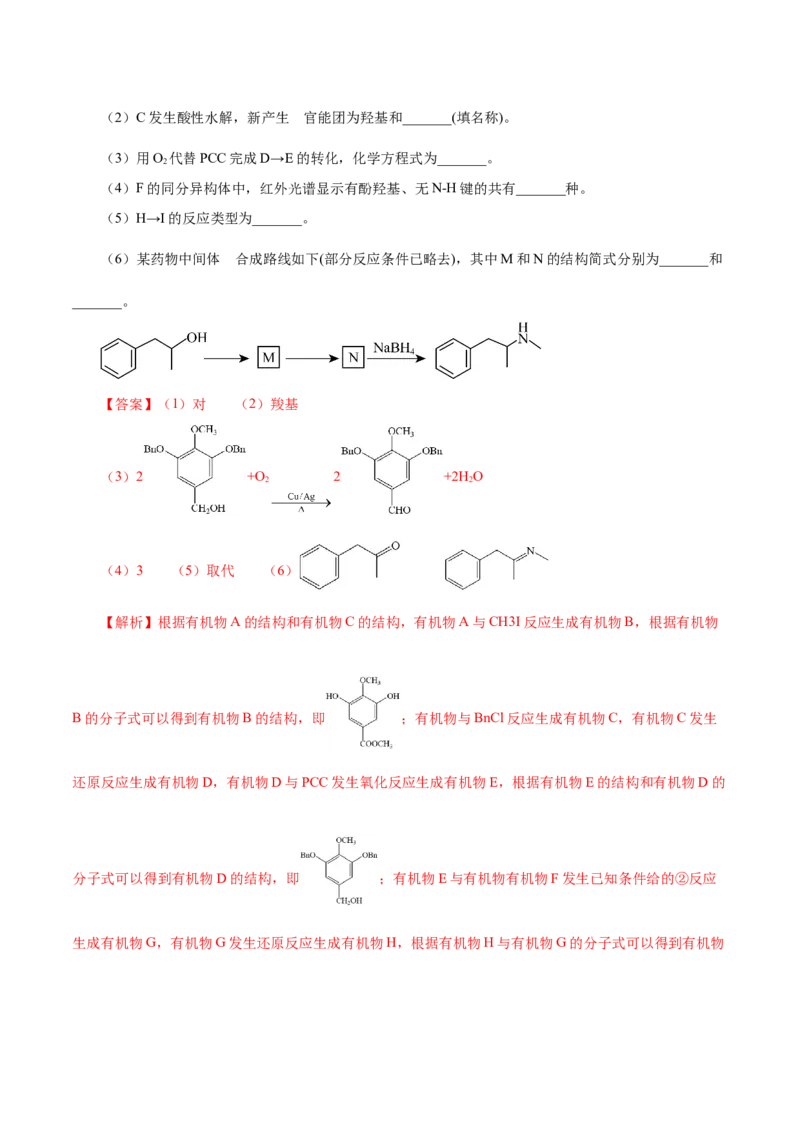
(2)C发生酸性水解,新产生 官能团为羟基和_______(填名称)。
(3)用O 代替PCC完成D→E的转化,化学方程式为_______。
2
(4)F的同分异构体中,红外光谱显示有酚羟基、无N-H键的共有_______种。
(5)H→I的反应类型为_______。
的
(6)某药物中间体 合成路线如下(部分反应条件已略去),其中M和N的结构简式分别为_______和
_______。
【答案】(1)对 (2)羧基
(3)2 +O 2 +2H O
2 2
(4)3 (5)取代 (6)
【解析】根据有机物A的结构和有机物C的结构,有机物A与CH3I反应生成有机物B,根据有机物
B的分子式可以得到有机物B的结构,即 ;有机物与BnCl反应生成有机物C,有机物C发生
还原反应生成有机物D,有机物D与PCC发生氧化反应生成有机物E,根据有机物E的结构和有机物D的
分子式可以得到有机物D的结构,即 ;有机物E与有机物有机物F发生已知条件给的②反应
生成有机物G,有机物G发生还原反应生成有机物H,根据有机物H与有机物G的分子式可以得到有机物G的结构,即 ,同时也可得到有机物F的结构,即 ;随后
有机物H与HCOOCH CH 反应生成有机物I。由此分析解题。
2 3
(1)由有机物A与CHI反应得到有机物B可知,酚与卤代烃反应成醚时,优先与其含有的其他官能
3
团的对位羟基发生反应,即酯基对位的酚羟基活性最高,可以发生成醚反应,故答案为;对位。
(2)有机物C在酸性条件下发生水解,其含有的酯基发生水解生成羧基,其含有的醚键发生水解生
成酚羟基,故答案为羧基。
(3)O 与有机物D发生催化氧化反应生成有机物E,反应的化学方程式为2 +O
2 2
2 +2H O。
2
(4)F的同分异构体中不含有N-H键,说明结构中含有 结构,又因红外中含有酚羟基,说明
结构中含有苯环和羟基,固定羟基的位置, 有邻、间、对三种情况,故有3种同分异构体。
(5)有机物H与HCOOCH CH 反应生成有机物I,反应时,有机物H中的N-H键发生断裂,与
2 3
HCOOCH CH 中断裂的醛基结合,故反应类型为取代反应。
2 3
(6)根据题目中给的反应条件和已知条件,利用逆合成法分析,有机物N可以与NaBH 反应生成最
4
终产物,类似于题中有机物G与NaBH 反应生成有机物H,作用位置为有机物N的N=C上,故有机物N
4
的结构为 ,有机物M可以发生已知条件所给的反应生成有机物N,说明有机物M中含有
C=O,结合反应原料中含有羟基,说明原料发生反应生成有机物M的反应是羟基的催化氧化,有机物M的结构为 。
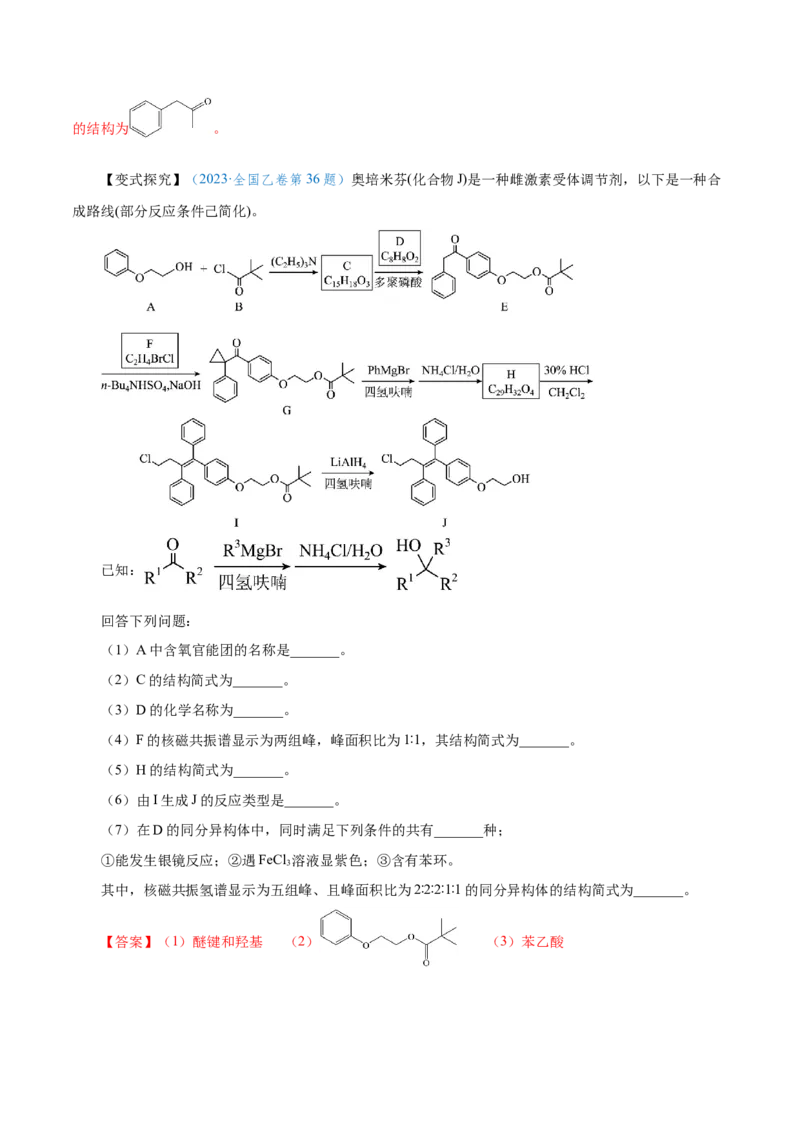
【变式探究】(2023·全国乙卷第36题)奥培米芬(化合物J)是一种雌激素受体调节剂,以下是一种合
成路线(部分反应条件己简化)。
已知:
回答下列问题:
(1)A中含氧官能团的名称是_______。
(2)C的结构简式为_______。
(3)D的化学名称为_______。
(4)F的核磁共振谱显示为两组峰,峰面积比为1∶1,其结构简式为_______。
(5)H的结构简式为_______。
(6)由I生成J的反应类型是_______。
(7)在D的同分异构体中,同时满足下列条件的共有_______种;
①能发生银镜反应;②遇FeCl 溶液显紫色;③含有苯环。
3
其中,核磁共振氢谱显示为五组峰、且峰面积比为2∶2∶2∶1∶1的同分异构体的结构简式为_______。
【答案】(1)醚键和羟基 (2) (3)苯乙酸(4) (5) (6)还原反应 (7)13
【解析】
【分析】有机物A与有机物B发生反应生成有机物C,有机物C与有机物D在多聚磷酸的条件下反应
生成有机物E,根据有机物E的结构可以推测,有机物C的结构为 ,进而推断出有
机物D的结构为 ;有机物E与有机物F反应生成有机物G,有机物G根据已知条件发生反应生成有
机物H,有机物H的结构为 ,有机物H发生两步反应得到目标化合物J(奥培米芬);据
此分析解题。
(1)根据有机物A的结构,有机物A中的含氧官能团是醚键和羟基。
(2)根据分析,有机物C的结构简式为 。
(3)根据分析,有机物D的结构为 ,其化学名称为苯乙酸。
(4)有机物F的核磁共振氢谱显示未两组峰,封面积比为1:1,说明这4个H原子被分为两组,且
物质应该是一种对称的结构,结合有机物F的分子式可以得到,有机物F的结构简式为 。(5)根据分析,有机物H的结构简式为 。
(6)根据流程,有机物I在LiAlH /四氢呋喃的条件下生成有机物J,LiAlH 是一种非常强的还原剂能
4 4
将酯基中的羰基部分还原为醇,该反应作用在有机物I的酯基上得到醇,因此该反应为还原反应。
(7)能发生银镜反应说明该结构中含有醛基,能遇FeCl 溶液显紫色说明该结构中含有酚羟基,则满
3
足这三个条件的同分异构体有13种。此时可能是情况有,固定醛基、酚羟基的位置处在邻位上,变换甲基
的位置,这种情况下有4种可能;固定醛基、酚羟基的位置处在间位上,变换甲基的位置,这种情况下有
4种可能;固定醛基、酚羟基的位置处在对位上,变换甲基的位置,这种情况下有2种可能;将醛基与亚
甲基相连,变换酚羟基的位置,这种情况下有3种可能,因此满足以上条件的同分异构体有4+4+2+3=13
种。其中,核磁共振氢谱显示为五组峰,且峰面积比为2:2:2:1:1,说明这总同分异构体中不能含有
甲基且结构为一种对称结构,因此,这种同分异构体的结构简式为: 。