文档内容
专题 5 氧化还原反应的概念、规律及应用
1.下列叙述不涉及氧化还原反应的是( )
A.食物腐败变质
B.对电力不足的新能源汽车充电
C.用SO 漂白纸浆
2
D.苯酚放置在空气中变为粉红色
2.(2022·辽宁省高三联考)二氧化氯(ClO )是高效、无毒的消毒剂,见光易分解,其中一种
2
制 备 方 法 是 用 氯 酸 钾 (KClO) 和 浓 HSO 一 定 条 件 下 发 生 反 应 : 3KClO +
3 2 4 3
3HSO (浓)===3KHSO+X+2ClO ↑+HO。下列说法错误的是( )
2 4 4 2 2
A.物质X为HClO
4
B.ClO 见光分解的化学方程式为2ClO =====Cl+2O
2 2 2 2
C.相同质量的Cl 和ClO 消毒时,Cl 的消毒效率比ClO 高
2 2 2 2
D.ClO 对CN-进行无毒化处理是利用其强氧化性
2
3.(2022·山西省吕梁市名校金科大联考)反应 Ⅰ:5FeO+3Mn2++16H+===5Fe3++3MnO+
8HO
2
反应Ⅱ:5SO+2Mn2++8HO===10SO+2MnO+16H+
2 2
反应Ⅲ:2MnO+5HO+6H+===2Mn2++5O↑+8HO
2 2 2 2
下列说法错误的是( )
A.氧化性:FeO>MnO>HO
2 2
B.用KI-淀粉试纸可鉴别NaSO 和NaHSO 溶液
2 2 8 4
C.反应 Ⅰ 和反应Ⅲ中的H+可由浓盐酸或浓硫酸提供
D.若将反应 Ⅱ 设计成原电池,正极反应式为SO+2e-===2SO
2
4.(2022·湖南岳阳一模)过二硫酸是一种硫的含氧酸,化学式为HSO 。它的结构可以表示
2 2 8
成HO SOOSO H。它的盐称为过二硫酸盐,在工业上用途广泛,用作强氧化剂等。下列反
3 3
应分别是Cr3+与过二硫酸盐和高锰酸盐反应的离子方程式(未配平)。
Ⅰ.Cr3++SO+HO――――→Cr O+SO+H+
2 2 2
Ⅱ.Cr3++MnO+HO――→Cr O+Mn2++H+
2 2
下列说法错误的是( )
A.过二硫酸根中显-2价的氧原子和显-1价的氧原子的数目比是3∶1
B.反应Ⅰ中氧化剂和还原剂的物质的量之比是3∶2
C.反应Ⅱ中每生成1 mol Cr O,转移电子的物质的量为6 mol
2
D.若反应Ⅰ和反应Ⅱ中消耗的Cr3+的物质的量相同,则反应Ⅰ和Ⅱ中消耗的氧化剂的物质
的量之比为2∶55.(2022·陕西咸阳一模)ClO 是一种绿色的饮用水消毒剂。常用下列两种反应原理制备:
2
反应Ⅰ:4HCl+2KClO===2ClO ↑+Cl↑+2KCl+2HO
3 2 2 2
反应Ⅱ:C H O+24KClO+12HSO ===12KSO +24ClO ↑+6CO↑+18HO
6 12 6 3 2 4 2 4 2 2 2
下列说法正确的是( )
A.两个反应中KClO 都作氧化剂
3
B.反应Ⅰ中氧化剂与还原剂的物质的量之比为1∶2
C.反应Ⅱ中每转移6 mol电子,生成气体的物质的量为15 mol
D.制备等量的ClO ,反应Ⅰ比反应Ⅱ转移的电子总数多
2
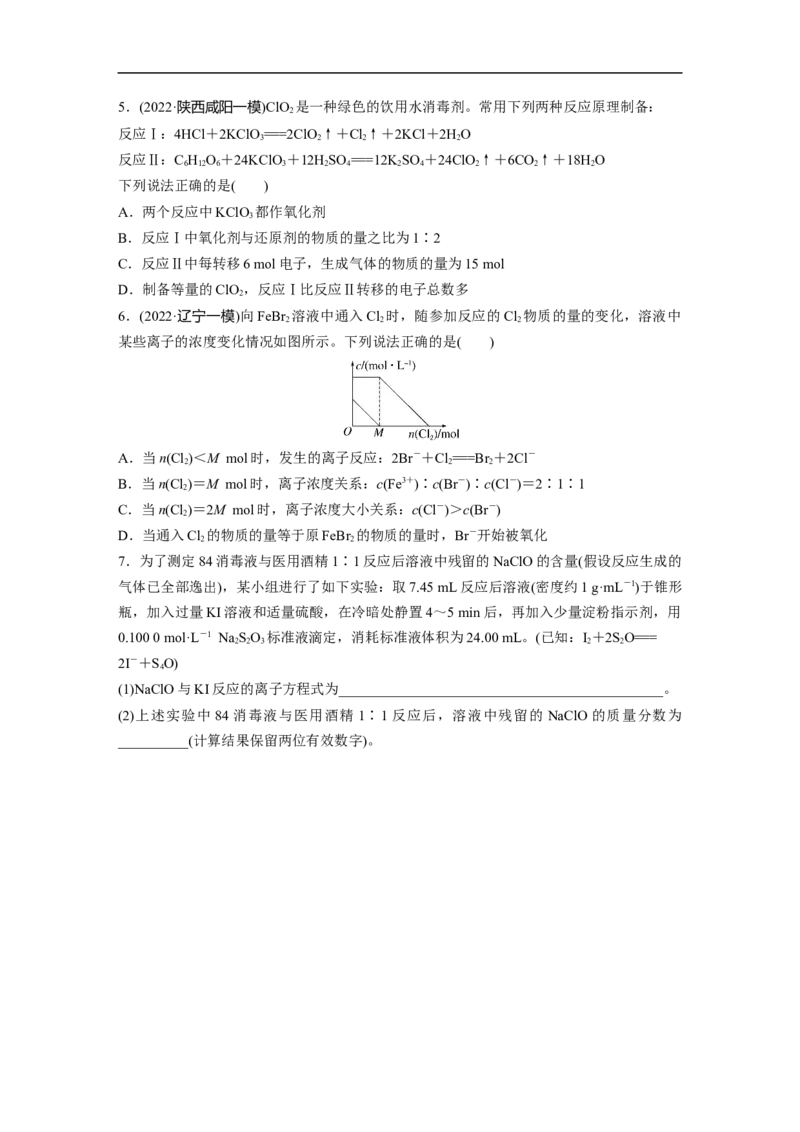
6.(2022·辽宁一模)向FeBr 溶液中通入Cl 时,随参加反应的Cl 物质的量的变化,溶液中
2 2 2
某些离子的浓度变化情况如图所示。下列说法正确的是( )
A.当n(Cl )<M mol时,发生的离子反应:2Br-+Cl===Br +2Cl-
2 2 2
B.当n(Cl )=M mol时,离子浓度关系:c(Fe3+)∶c(Br-)∶c(Cl-)=2∶1∶1
2
C.当n(Cl )=2M mol时,离子浓度大小关系:c(Cl-)>c(Br-)
2
D.当通入Cl 的物质的量等于原FeBr 的物质的量时,Br-开始被氧化
2 2
7.为了测定84消毒液与医用酒精1∶1反应后溶液中残留的NaClO的含量(假设反应生成的
气体已全部逸出),某小组进行了如下实验:取7.45 mL反应后溶液(密度约1 g·mL-1)于锥形
瓶,加入过量KI溶液和适量硫酸,在冷暗处静置4~5 min后,再加入少量淀粉指示剂,用
0.100 0 mol·L-1 Na SO 标准液滴定,消耗标准液体积为24.00 mL。(已知:I+2SO===
2 2 3 2 2
2I-+SO)
4
(1)NaClO与KI反应的离子方程式为______________________________________________。
(2)上述实验中 84消毒液与医用酒精 1∶1反应后,溶液中残留的 NaClO的质量分数为
__________(计算结果保留两位有效数字)。